| 对非 - 酒精 脂肪肝病 (NAFLD) 受试者进行 pemvidutidutidutide 24- 周(12- 延期)试验 纳斯达克:ALT Stephen Harrison,医学博士,首席研究员 2022 年 12 月 20 日 |
| 向前看 - 的陈述 Safe - Harbor 声明 这份 演示文稿 由 Altimmune 编写 , 。 (“我们,” “我们,” “我们的,” “Altimmune” 或 “公司”) 和 包括 “向前 - ” 看 的陈述” 中 表示 1995 年 的 私人 证券 诉讼 改革 法案 , 包括 与 未来 财务 或 业绩、 条件、 计划、 趋势、 或 策略相关的 声明 和 其他 财务 和 业务 事项, 包括没有 限制的 , 的 时机 我们的 临床 资产的里程碑 , 的 数据 读数 NAFLD 试验 , 期 pemvidutidutide 和 有望获得 监管部门批准 , 将 或 销售 任何 产品 或 候选药物 。 另外, 当 或 在 本新闻稿中使用 时 , “可以”、 “可以”、 “应该”、 “预期”、 “相信”、 “估计”、 “期待”, “打算”, “计划”, “预测” 和 相似 和 它们的 变体, 他们 将 与 相关联 } 声明 。 公司 警告 这些 前瞻性 - 的陈述 是 受 多个 假设、 风险、 和 的不确定性, 在 时间内 发生变化 。 重要 因素 可能 导致 实际结果 和 不同 与 存在重大差异 在 中讨论 向前 看 的陈述 或 的历史 经验 包括 br} 风险 和 不确定性, 包括 与 相关的 风险 : 可能的 影响 乌克兰 和 COVID - 大流行, 如 } 延迟 监管 审查 、 制造 和 供应链 中断, 进入 临床 站点、 注册人数、 对 医疗保健 系统的不良影响 和 对 全球 经济 的影响 阶段 1 b NAFLD 研究 有关 未来 试验 的成功 的 的可靠性 的结果 与 人类 安全 br} 和 可能产生的 不利影响 公司的 候选产品 产生 公司 有能力 制造 临床 试验 材料 在 时间轴 预期 ; 和 未来 产品 的进步 的 成功 未来的 临床 试验 。 更多 有关 的 因素 和 的风险 可以 影响 公司 业务、 财务 状况 和 的 的结果 br} 公司 的申报文件 和 U 。 S 。 证券 和 交易所 委员会, 包括 标题 下的 “风险 因素” 中 公司 年度 报告 上的 表 } 年 已于 截止 31、 2021 年 和 我们的 其他 申报 sec , 是 在 www 上线。 秒 。 gov 。 2 |
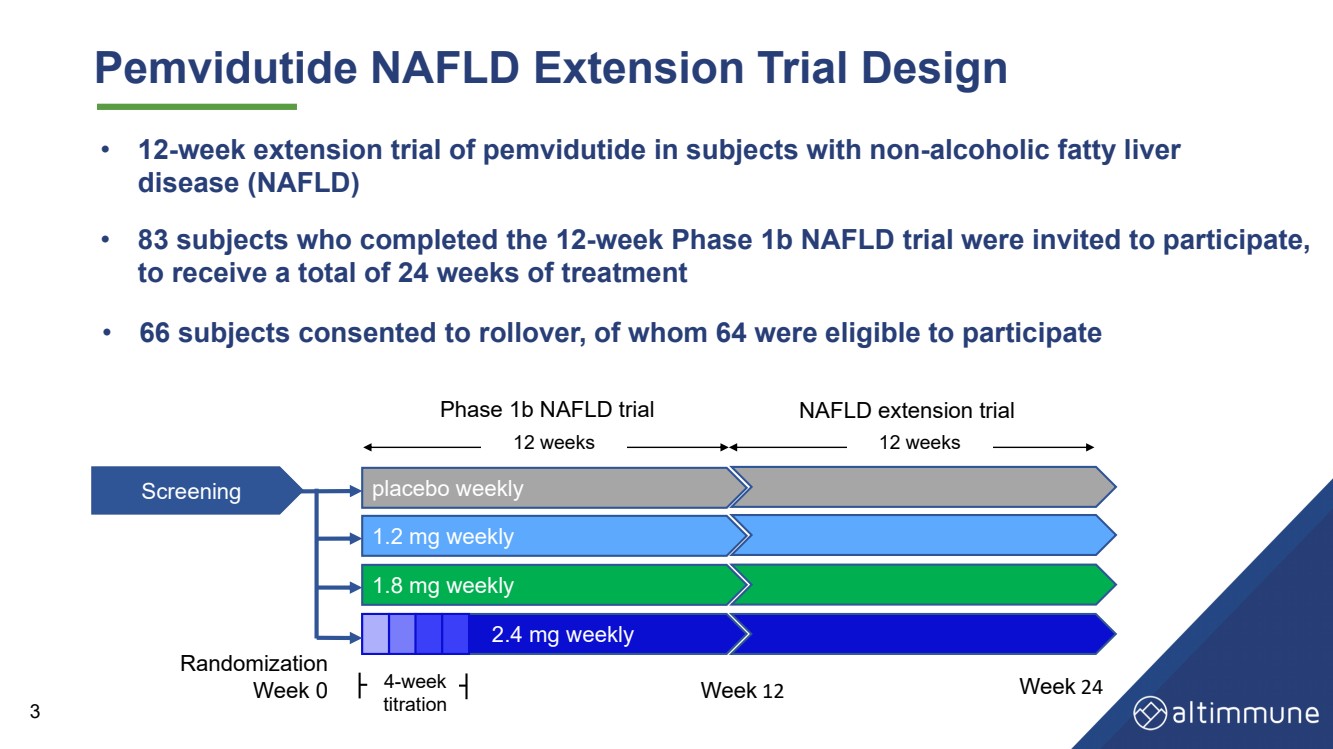
| Pemvidutide NAFLD 延期试验设计 • 83 名完成 12- 周 1b 期 NAFLD 试验的受试者应邀参加, 将接受总计 24 周的治疗 • 对非 - 酒精性脂肪肝 病受试者的培姆维度肽延期试验 br} 3 • 66 名受试者同意展期,其中 64 名有资格参加 每周筛查 安慰剂 每周 1.8 mg 每周 1.2 mg 4- 周 滴定 随机化 NAFLD延期试用 12 周 12 周 周 12 周 24 |
| 研究人群 — 关键资格标准 受试者需要在 12- 周的 1b 期 NAFLD 试验中完成给药并在家长试验进入时符合以下标准: • 65 岁 • BMI ≥ 28 kg/m 2 • NAFLD,定义为肝脏磁共振成像测出的脂肪含量 (LFC) - PDFF ≥ 10% • 无明显纤维化,定义为 FibroScan ® LSM |
| 研究终点 功效 • 主要终点: • 与第 0 周相比,第 24 周肝脏脂肪含量 (LFC) 降低 - PDFF • 关键次要终点: 血清丙氨酸氨基转移酶 (ALT) 水平导致肝脏炎症,并比较第 24 周修正的 T1 (cT1) 成像到第 0 周 • 与第 0 周相比,第 24 周体重减轻百分比 (%) 安全性 • 不良事件 (AE) 导致停药的严重和严重不良事件 • 胃肠道耐受性 • 血糖控制(空腹血糖,Hba1c) 5 |
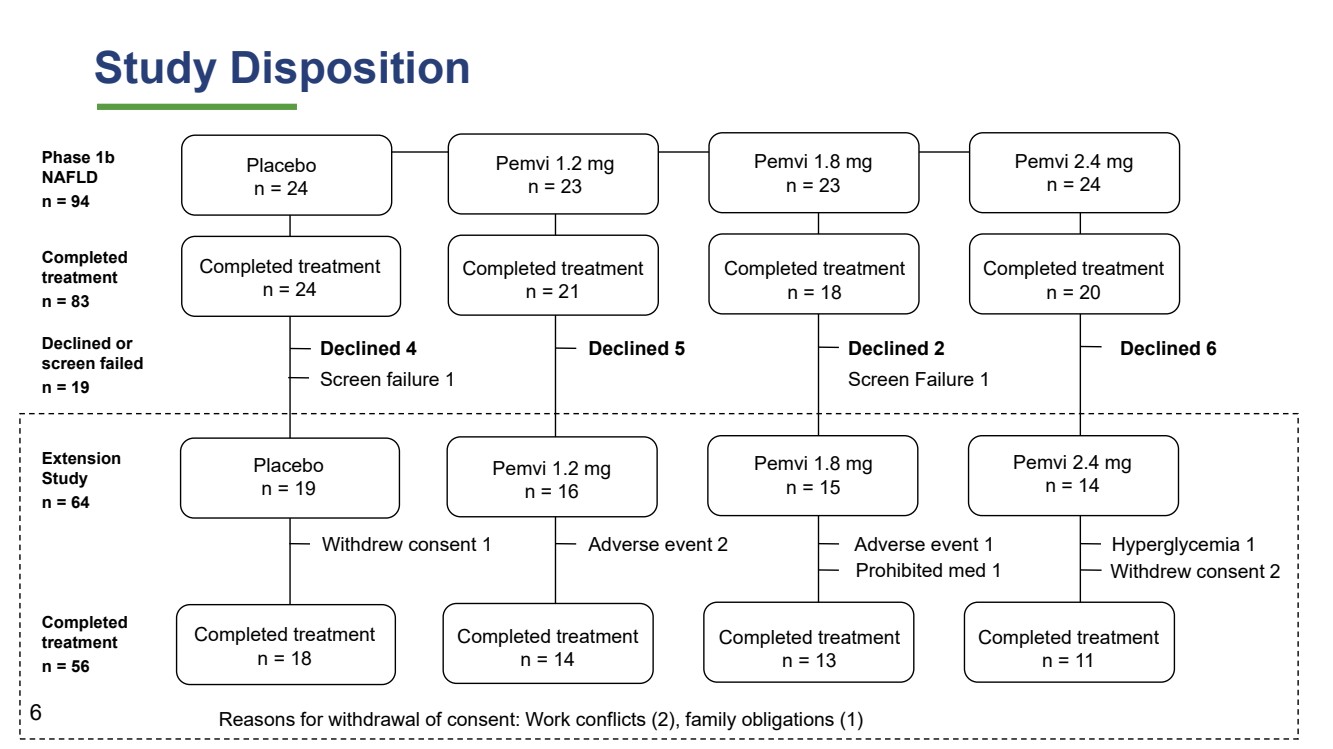
| 研究安排 安慰剂 n = 24 Pemvi 1.2 mg n = 23 Pemvi 1.8 mg n = 23 Pemvi 2.4 mg n = 24 已完成治疗 n = 21 已完成治疗 n = 18 安慰剂 n = 19 Pemvi 1.2 mg n = 16 Pemvi 2.4 mg n = 14 Pemvi 1.8 mg n = 15 被拒绝 5 被拒绝 6 已完成治疗 n = 18 已完成治疗 n = 14 已完成治疗 n = 11 已完成治疗 n = 13 撤回同意 1 不良事件 1 撤回同意 2 阶段 1b n = 94 延期 研究 n = 64 6 违禁药物 1 高血糖 1 已拒绝 4 筛查失败 1 被拒绝 2 筛查失败 1 撤回同意的原因:工作冲突 (2)、家庭义务 (1) 已完成 治疗 n = 83 已完成 n = 56 被拒绝或 n = 19 |
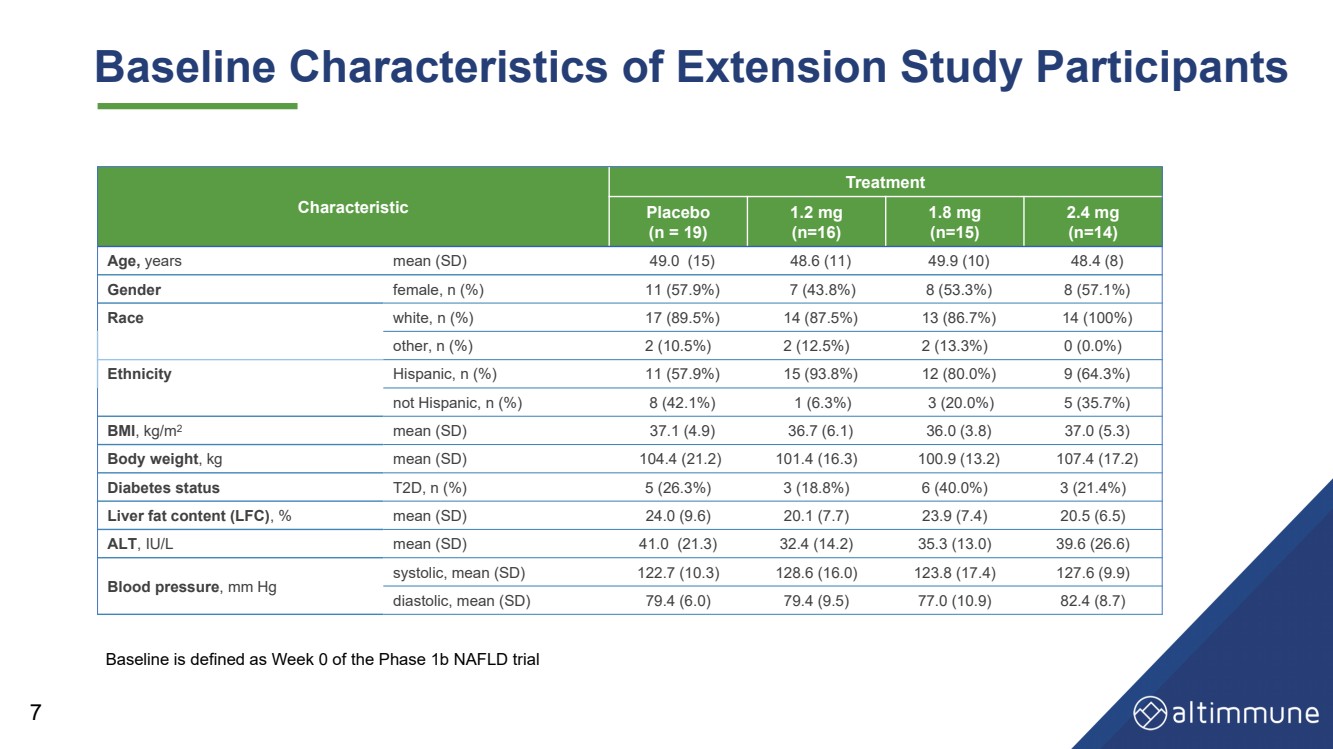
| 扩展研究参与者的基线特征 治疗 安慰剂 (n = 19) 1.2 mg (n=16) 1.8 mg (n=15) (n=15) (n=14) 年龄, 平均值 (SD) 49.0 (15) 8.6 (11) 49.9 (10) 48.4 (8) 性别 女,n (%) 11 (57.9%) 7 (43.8%) 8 (53.3%) 8 (57.1%) br} 14 (87.5%) 13 (86.7%) 14 (100%) 其他,n (%) 2 (10.5%) 2 (12.5%) 2 (13.3%) 0 (0.0%) 0 (0.0%) 0 (0.0%) ) 12 (80.0%) 9 (64.3%) 不是西班牙裔,n (%) 8 (42.1%) 1 (6.3%) 3 (20.0%) 5 (35.7%) br},kg/m 2 mean (SD) 37.1 (4.9) 36.0 (3.8) 37.0 (5.3) 37.0 (5.3) br} 体重 ,kg mean (SD) 104.4 (21.2) 101.4 (16.3) 100.9 (13.2) 107.4 (17.2) 状态 t2D,n (%) 5 (26.3%) 3 (18.8%) 6 (40.0%) 3 (21.4%) ,% mean (SD) 24.0 (9.6) 20.1 (7.7) 23.9 (7.4) 20.5 (6.5) 2.4 (14.2) 35.3 (13.0) 39.6 (26.6) 血压 ,mm Hg 收缩压,平均值 (SD) 122.7 (10.3) 128.6 (16.0) 123.8 (17.4) 127.6 (9.9) 舒张压,平均值 (SD) 79.4 (9.5) 77.0 (10.9) 82.4 (8.7)) 7 基线定义为 1b 期 NAFLD 试验的第 0 周 |
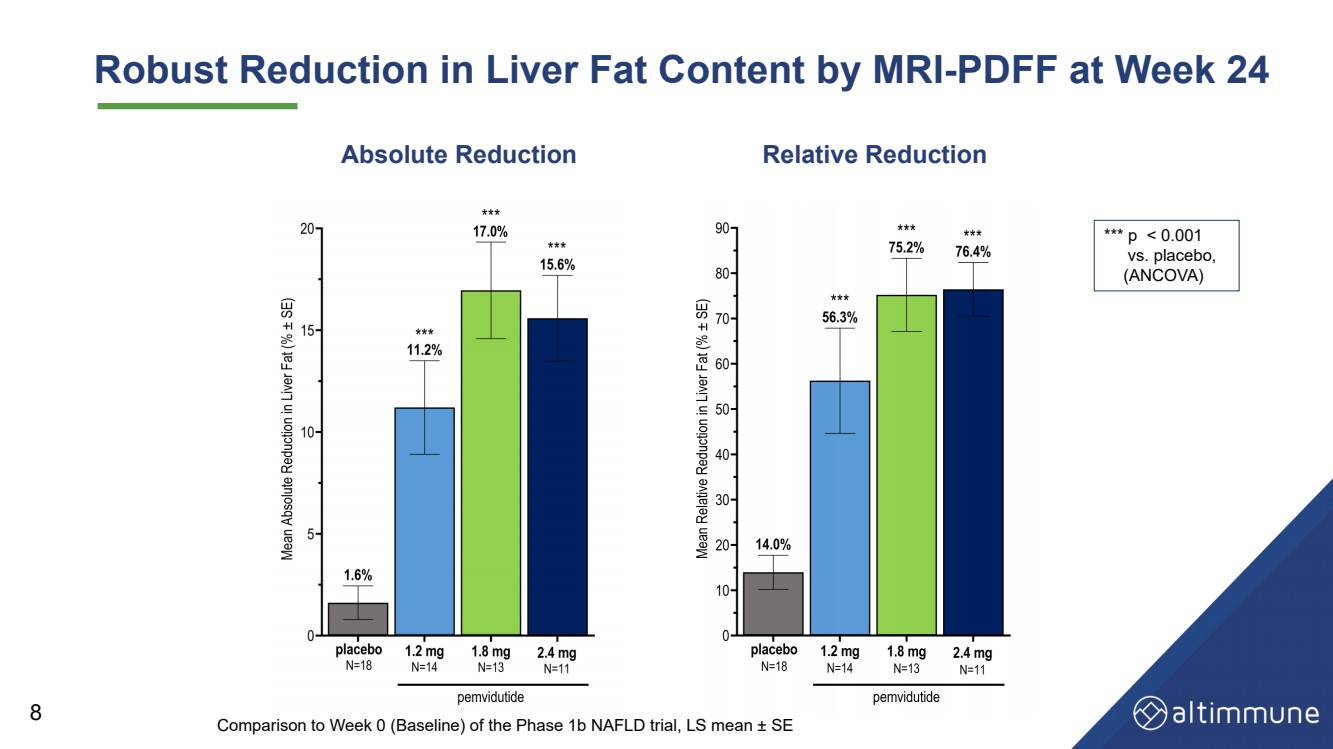
| 磁共振成像在第 24 周大幅降低肝脏脂肪含量 - PDFF 8 绝对降低 相对减少 *** p |
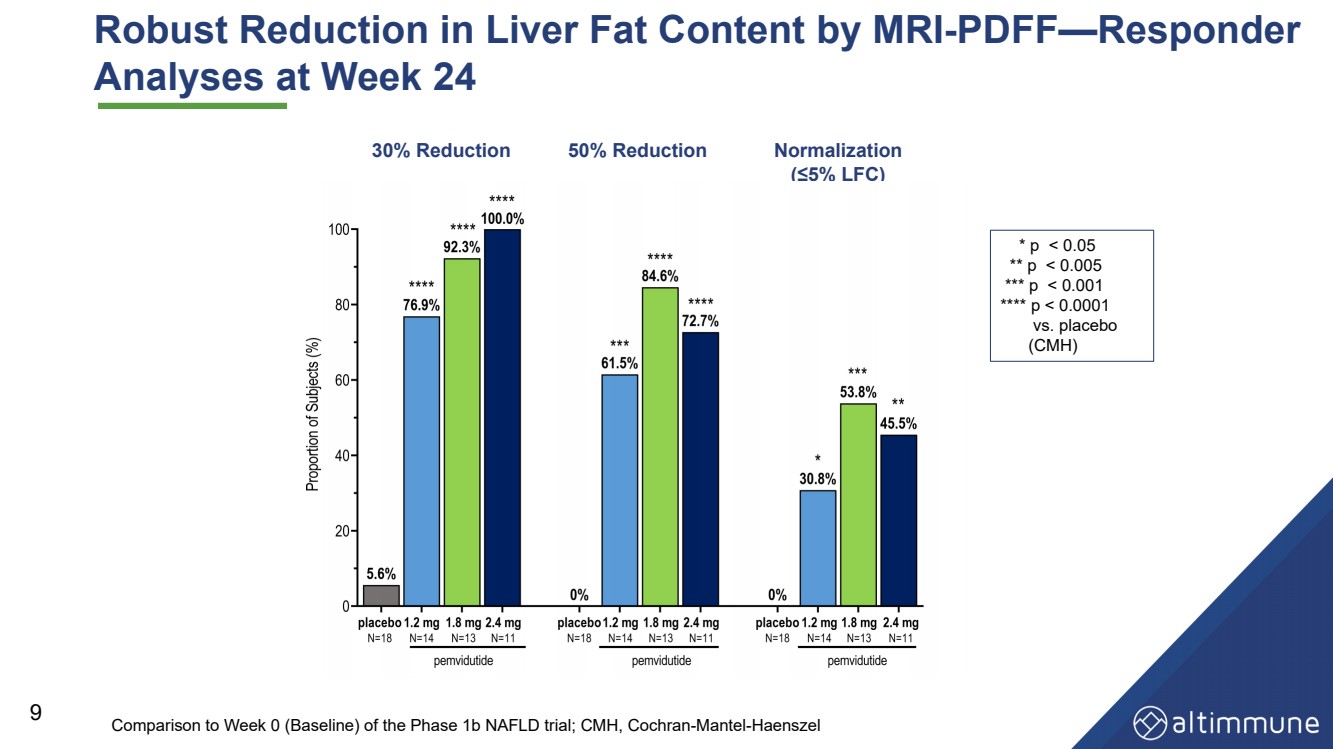
| 9 核磁共振成像 - PDFF — — Responder 第 24 周分析与 1b 期 NAFLD 试验第 0 周(基线)的比较;CMH、Cochran - Haenszel 减少 30% 标准化 } (≤ 5% 液化合物) * p |
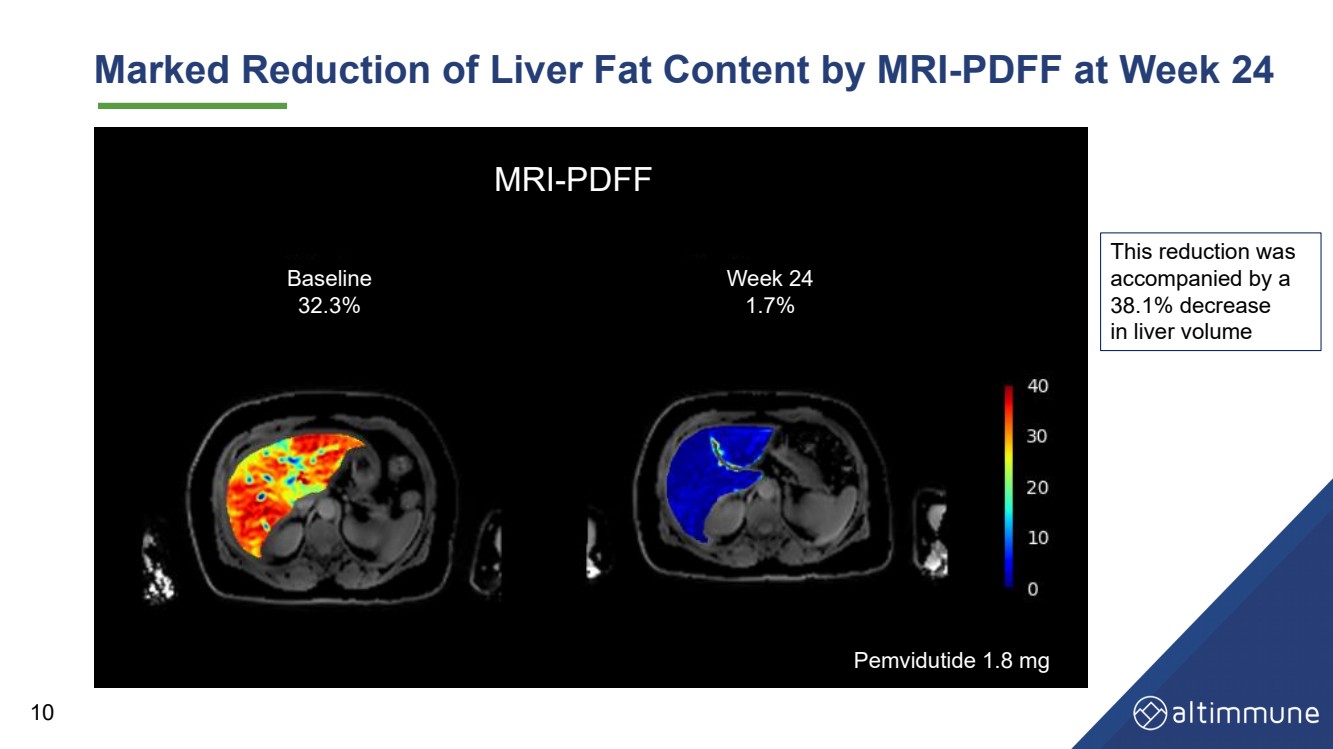
| 10 核磁共振成像在第 24 周显著降低肝脏脂肪含量 - PDFF Pemvidutidutide 1.8 mg - PDFF 基线 32.3% 第 24 周 1.7% 这种降低 同时肝脏 体积 |
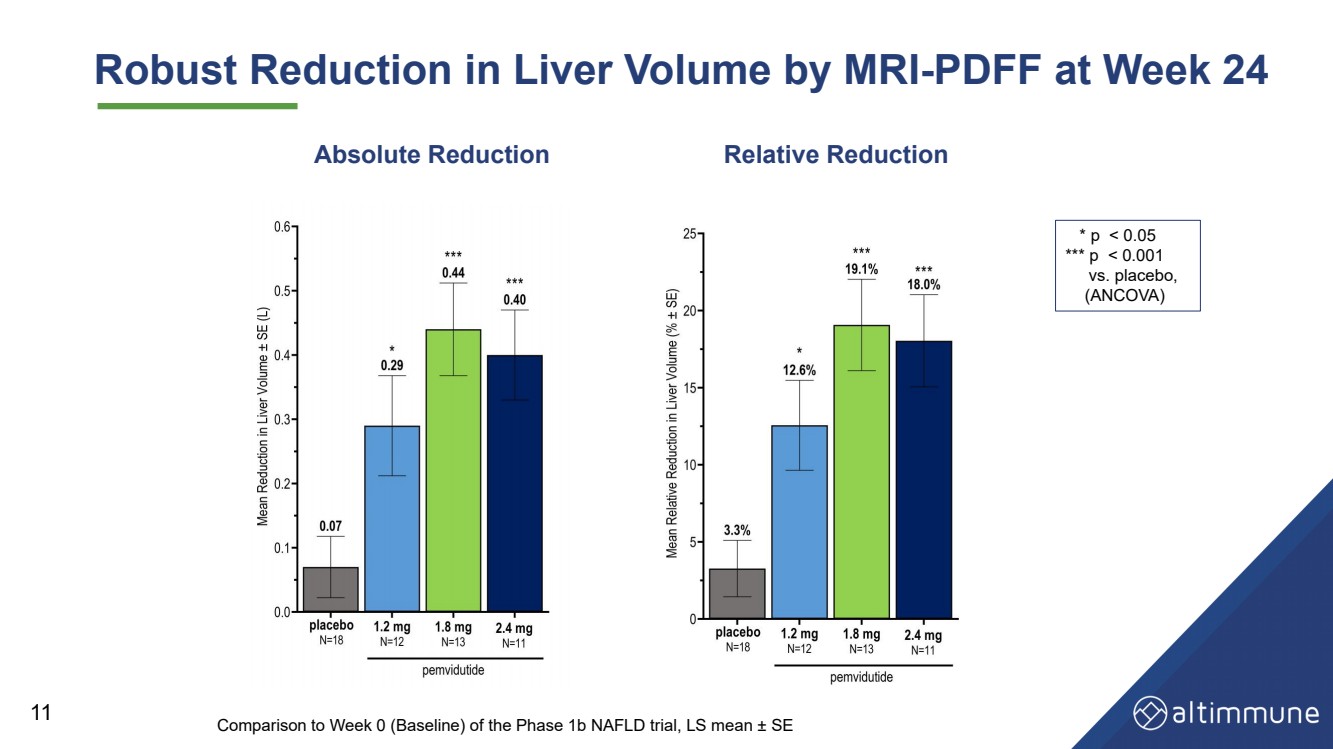
| 第 24 周 MRI 可大幅减少肝脏容量 - PDFF 11 * p |
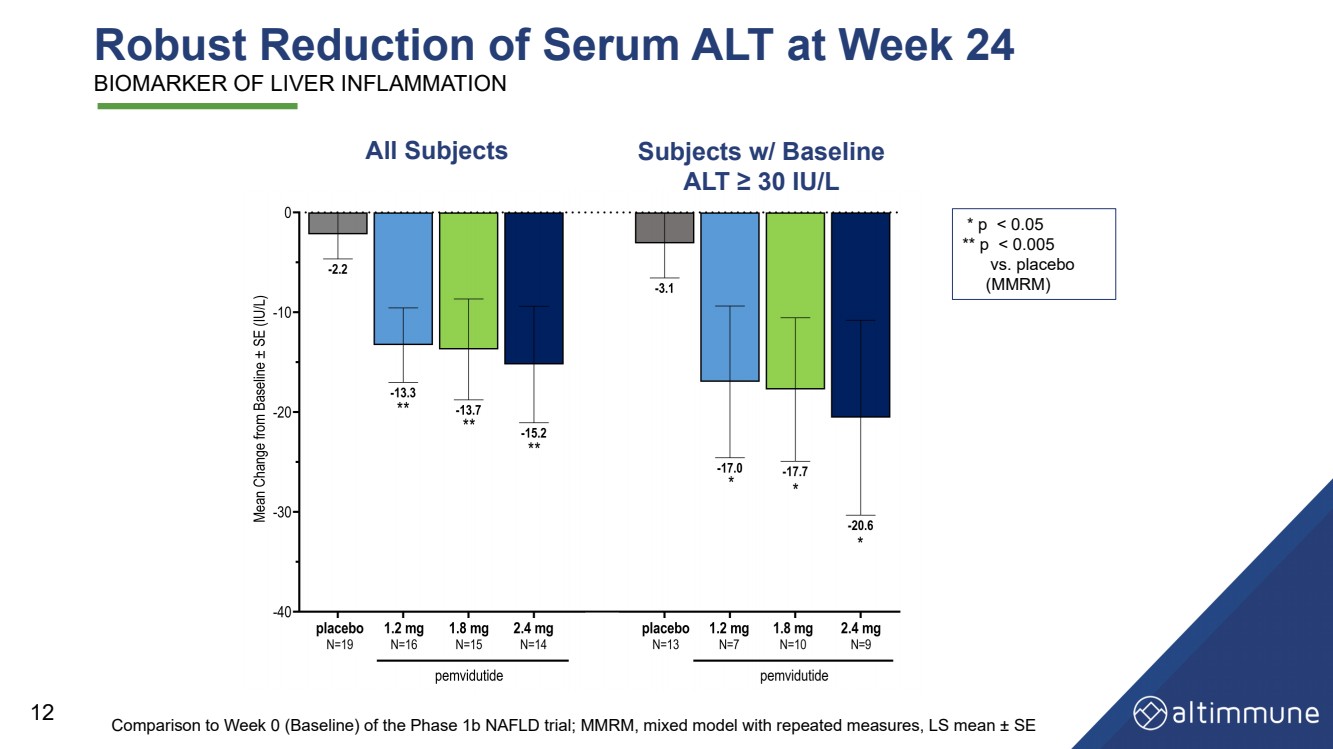
| 第 24 周血清 ALT 肝炎生物标志物 12 与 1b 期 NAFLD 试验第 0 周(基线)的比较;MMRM,重复测量的混合模型,LS 平均值 ± SE 所有受试者 alt ≥ 30 IU/L * p |
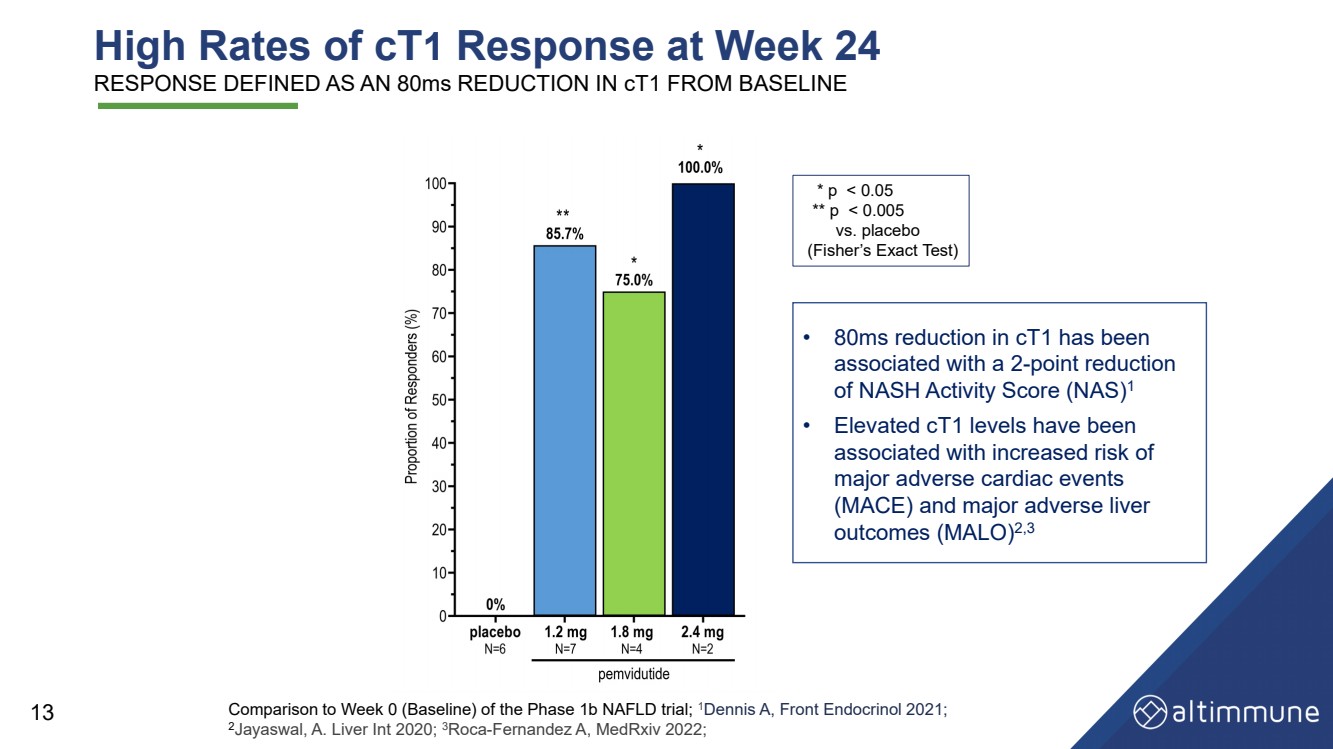
| 第 24 周的 cT 1 反应率高 的反应定义为 c T1 比基线减少 80 毫秒 13 与 1b 期 NAFLD 试验第 0 周(基线)的比较; 1 Dennis A,Front Endermonol 2021; 2 Jayaswal,A. Liver Int 2020; 3 Roca - } 费尔南德斯 A,medrXiv 2022; * p |
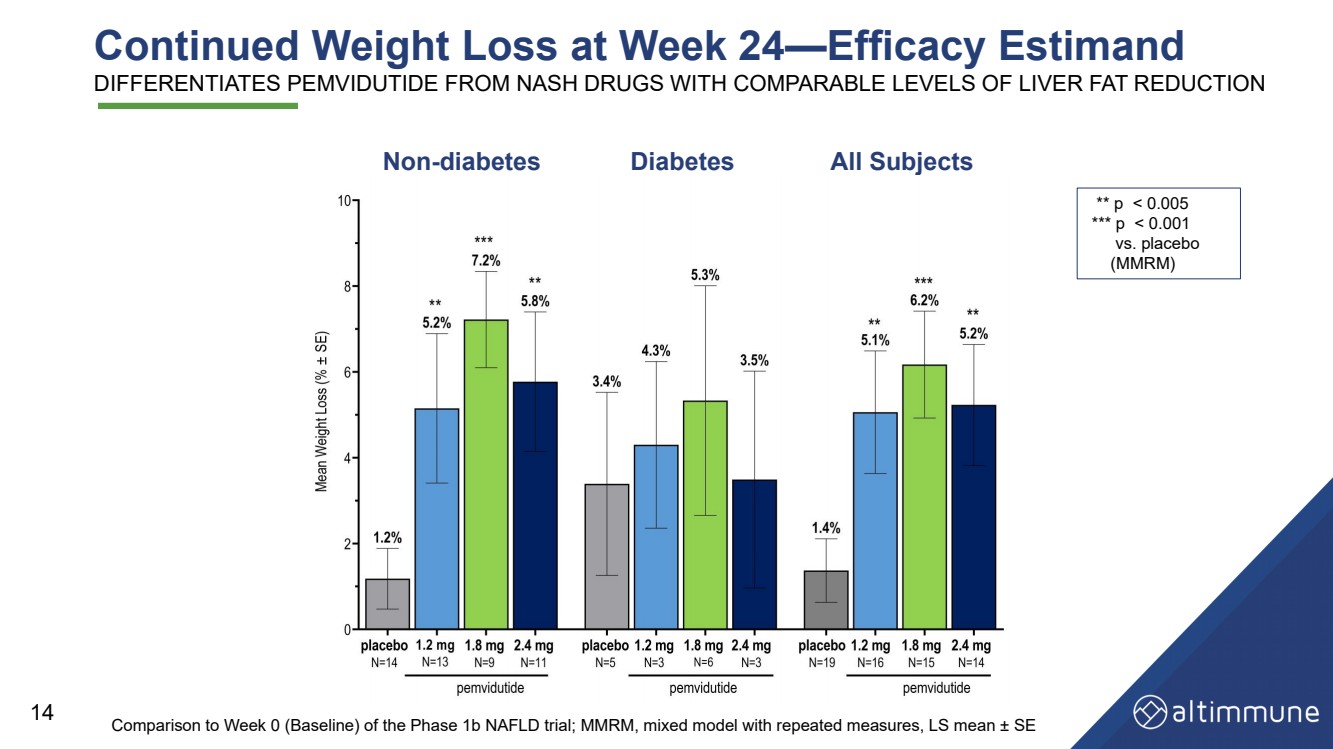
| 14 ** p |
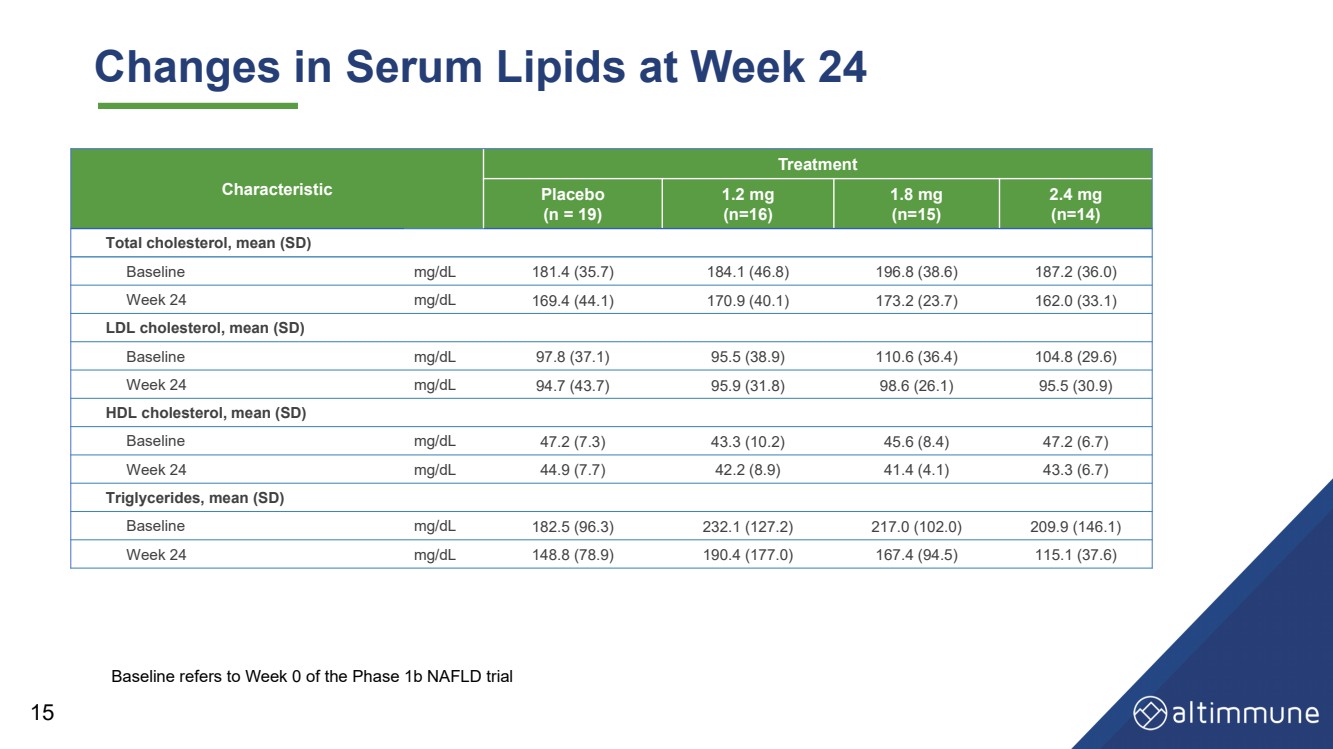
| 第 24 周血清脂质变化 特征 治疗 安慰剂 (n = 19) 1.2 mg (n=16) 1.8 mg (n=15) 181.4 (35.7) 184.1 (46.8) 196.8 (38.6) 187.2 (36.0) 第 24 周 mg/dL 169.4 (44.1) 170.9 (40.1) 173.2 (23.7) 低密度脂蛋白胆固醇,平均值 (SD) {br)} 基线 mg/dL 97.8 (37.1) 95.5 (38.9) 110.6 (36.4) 104.8 (29.6) 第 24 周 mg/dL 94.7 (43.7) 95.9 (31.8) 98.6 (26.1) 95.5 (30.9) L 胆固醇,平均值 (SD) 基线 mg/dL 47.2 (7.3) 43.3 (10.2) 45.6 (8.4) 47.2 (6.7) 44.9 (7.7) 44.9 (8.9) 41.4 (4.1) 43.3 (6.7) 甘油三酯,平均值 (SD) 基线 mg/dL 182.5 (96.3) 232.1 (127.2) 217.0 (102.0) 209.9 (146.1) 148.8 (78.9) 190.4 (177.0) 167.4 (94.5) 115.1 (37.5) 6) 基线指的是 1b 期 NAFLD 试验的第 0 周 |
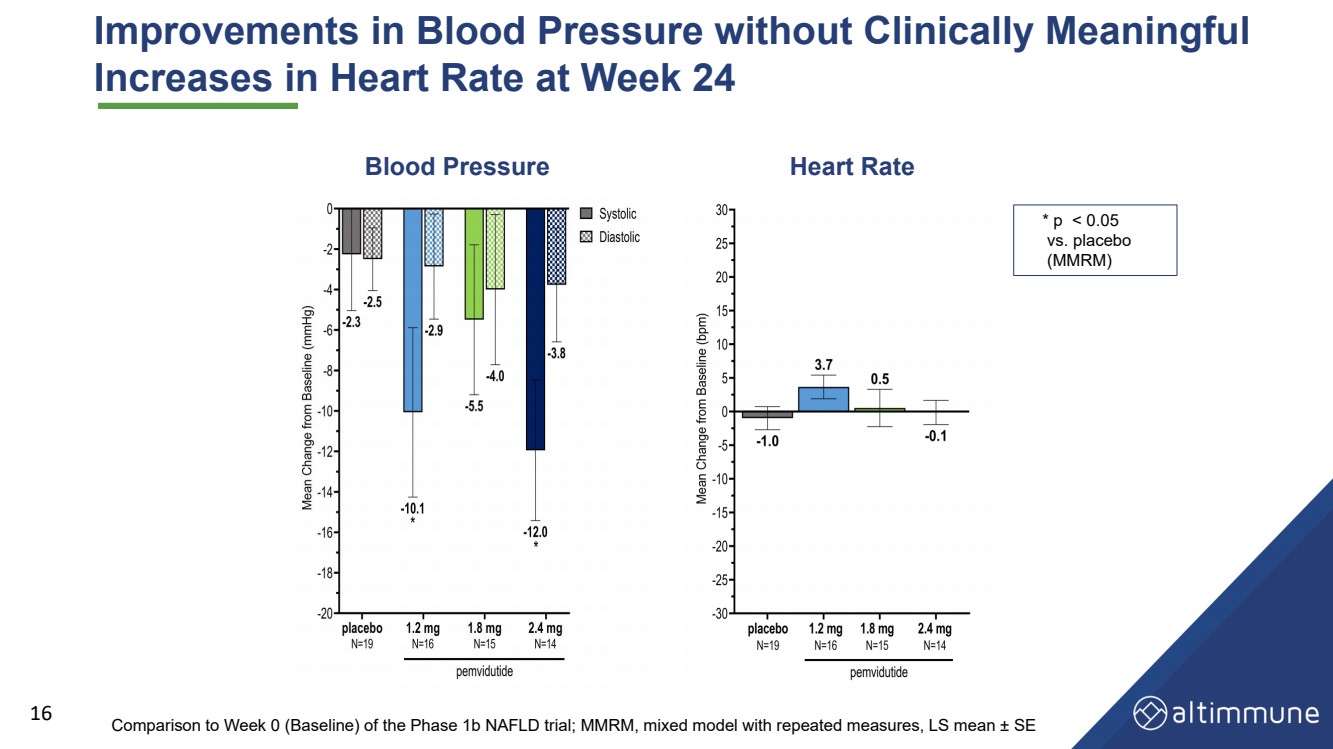
| 血压 在没有临床意义的情况下改善血压 在第 24 周心率 血压 与 1b 期 NAFLD 试验第 0 周(基线)的比较;MMRM,重复测量的混合模型,LS 平均值 ± se * p |
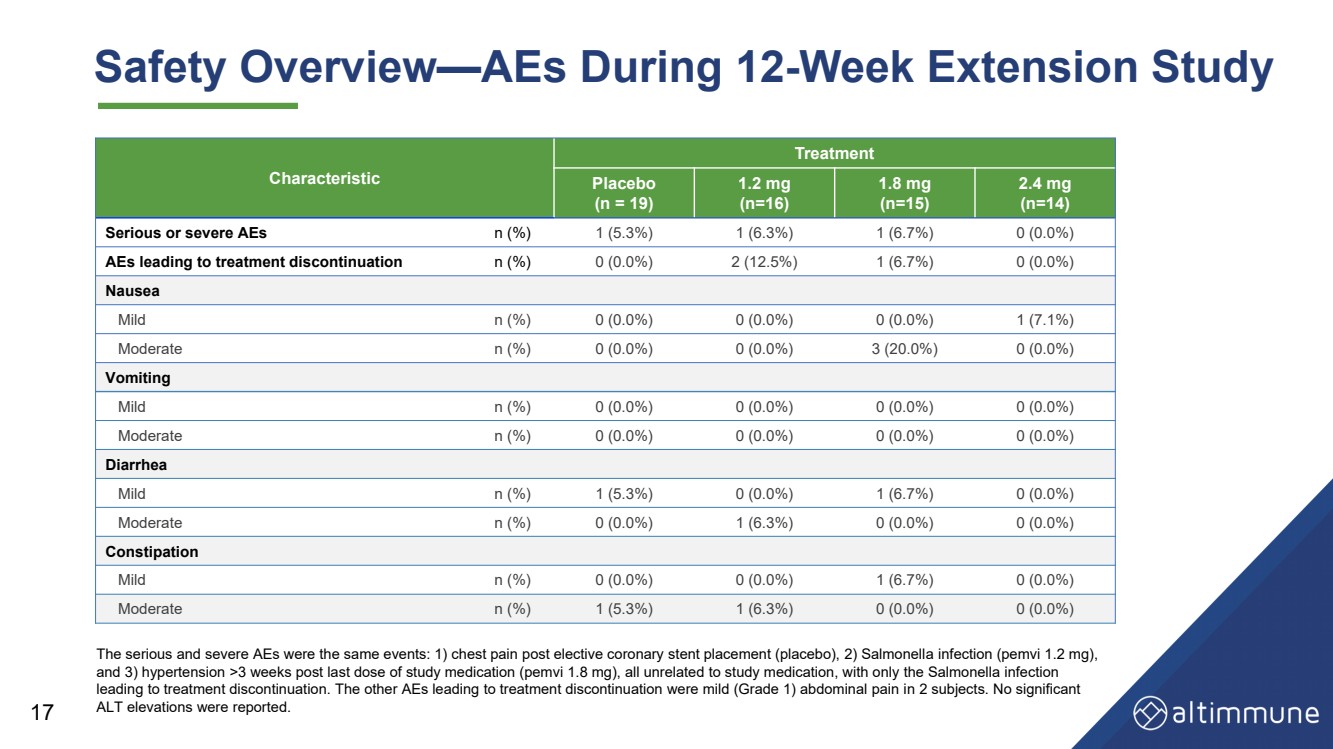
| Characteristic Treatment Placebo (n = 19) 1.2 mg (n=16) 1.8 mg (n=15) 2.4 mg (n=14) Serious or severe AEs n (%) 1 (5.3%) 1 (6.3%) 1 (6.7%) 0 (0.0%) AEs leading to treatment discontinuation n (%) 0 (0.0%) 2 (12.5%) 1 (6.7%) 0 (0.0%) Nausea Mild n (%) 0 (0.0%) 0 (0.0%) 0 (0.0%) 1 (7.1%) Moderate n (%) 0 (0.0%) 0 (0.0%) 3 (20.0%) 0 (0.0%) Vomiting Mild n (%) 0 (0.0%) 0 (0.0%) 0 (0.0%) 0 (0.0%) Moderate n (%) 0 (0.0%) 0 (0.0%) 0 (0.0%) 0 (0.0%) Diarrhea Mild n (%) 1 (5.3%) 0 (0.0%) 1 (6.7%) 0 (0.0%) Moderate n (%) 0 (0.0%) 1 (6.3%) 0 (0.0%) 0 (0.0%) Constipation Mild n (%) 0 (0.0%) 0 (0.0%) 1 (6.7%) 0 (0.0%) Moderate n (%) 1 (5.3%) 1 (6.3%) 0 (0.0%) 0 (0.0%) 17 Safety Overview — AEs During 12 - Week Extension Study The serious and severe AEs were the same events: 1) chest pain post elective coronary stent placement (placebo), 2) Salmonell a i nfection (pemvi 1.2 mg), and 3) hypertension >3 weeks post last dose of study medication (pemvi 1.8 mg), all unrelated to study medication, with only the Salmonella infection leading to treatment discontinuation. The other AEs leading to treatment discontinuation were mild (Grade 1) abdominal pain i n 2 subjects. No significant ALT elevations were reported. |
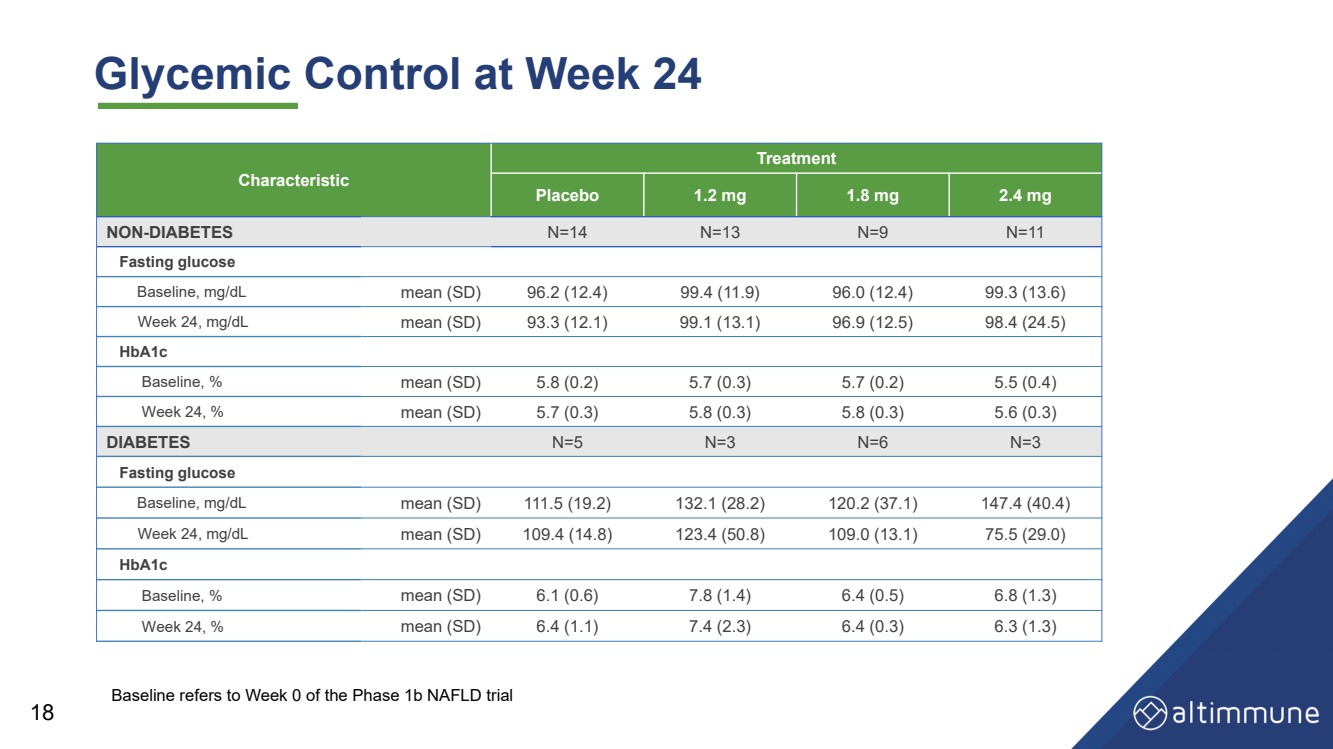
| Glycemic Control at Week 24 18 Characteristic Treatment Placebo 1.2 mg 1.8 mg 2.4 mg NON - DIABETES N=14 N=13 N=9 N=11 Fasting glucose Baseline, mg/dL mean (SD) 96.2 (12.4) 99.4 (11.9) 96.0 (12.4) 99.3 (13.6) Week 24, mg/dL mean (SD) 93.3 (12.1) 99.1 (13.1) 96.9 (12.5) 98.4 (24.5) HbA1c Baseline, % mean (SD) 5.8 (0.2) 5.7 (0.3) 5.7 (0.2) 5.5 (0.4) Week 24, % mean (SD) 5.7 (0.3) 5.8 (0.3) 5.8 (0.3) 5.6 (0.3) DIABETES N=5 N=3 N=6 N=3 Fasting glucose Baseline, mg/dL mean (SD) 111.5 (19.2) 132.1 (28.2) 120.2 (37.1) 147.4 (40.4) Week 24, mg/dL mean (SD) 109.4 (14.8) 123.4 (50.8) 109.0 (13.1) 75.5 (29.0) HbA1c Baseline, % mean (SD) 6.1 (0.6) 7.8 (1.4) 6.4 (0.5) 6.8 (1.3) Week 24, % mean (SD) 6.4 (1.1) 7.4 (2.3) 6.4 (0.3) 6.3 (1.3) Baseline refers to Week 0 of the Phase 1b NAFLD trial |
| Summary and Conclusions • Greater than 75% relative liver fat reduction at 24 weeks, better than or equal to the effects of other leading NASH candidates • Significant reductions and normalization in serum ALT and improvement in cT1 point to potent effects in NASH clinical trials • Non - diabetes — continued weight loss, achieving 7.2% at pemvidutide 1.8 mg at Week 24 • Diabetes — achieved 5.3% weight loss at pemvidutide 1.8 mg at Week 24 Liver fat reduction Weight loss • Low rates of AEs leading to treatment discontinuation, no serious/severe AEs related to pemvidutide • Cardioprotective reductions in blood pressure without increases in heart rate • Glycemic control maintained with trends toward improvements in fasting glucose and HbA1c in subjects with diabetes • No clinically significant ALT elevations Safety and tolerability 19 |
| NASDAQ: ALT Questions pertaining to this presentation: Rich Eisenstadt, CFO reisenstadt@altimmune.com |