

开发解决癌症免疫耐药性的下一代免疫疗法 KA(纳斯达克)2023 年 11 月附录 99.2

免责声明和其他信息关于前瞻性陈述的警示声明本演示文稿包含1995年《私人证券诉讼改革法》所指的 “前瞻性陈述”。使用但不限于 “相信”、“期望”、“估计”、“计划”、“打算”、“未来”、“潜力”、“继续”、“可能”、“可能”、“计划”、“将”、“应该”、“寻求”、“预期” 或 “可能” 等词语以及其他类似的词语或表达方式旨在识别前瞻性陈述。前瞻性陈述既不是历史事实,也不是对未来表现的保证。相反,它们基于Kineta当前对Kineta业务未来、未来计划和战略、临床结果和其他未来状况的信念、预期和假设。新的风险和不确定性可能会不时出现,因此不可能预测所有风险和不确定性。对任何此类前瞻性陈述的准确性不作任何陈述或保证(明示或暗示)。此类前瞻性陈述存在许多重大风险和不确定性,包括但不限于:Kineta的资本是否足以支持其未来运营(包括其完成先前披露的第二批私募配售的能力)及其成功启动和完成临床试验的能力;预测Kineta候选产品开发的时间和成本的困难;Kineta研究、开发和商业化其当前和未来的计划候选产品,包括但不限于 KVA12123;Kineta 计划中的临床前研究和临床试验的时间和预期结果,以及 Kineta 的临床前研究和临床试验结果可能无法预测未来与未来研究或临床试验相关的结果的风险;Kineta 临床试验数据可用的时间;任何计划中的研究性新药申请或新药申请的时间;停止或延迟任何正在进行的研究性新药申请或新药申请的风险或计划对Kineta或其进行临床试验合作者;Kineta候选产品的临床效用、潜在收益和市场接受度;Kineta的商业化、营销和制造能力及战略;与Kineta竞争对手及其行业相关的发展和预测;政府法律法规的影响;Kineta计划与监管机构互动的时间和结果;Kineta保护其知识产权地位的能力;Kineta对未来收入、支出、资本要求和额外需求的估计融资;2023年4月和2023年10月完成的注册直接发行所得收益的预期用途;以及Kineta于2023年3月31日向美国证券交易委员会(“SEC”)提交的最新10-K表年度报告和2023年5月11日和2023年8月11日向美国证券交易委员会提交的10-Q表季度报告以及关于潜在风险、不确定性和其他问题的讨论中以 “风险因素” 为标题列出的风险 Kineta随后向美国证券交易委员会提交文件中的重要因素。任何前瞻性陈述仅代表其发表之日。除非法律要求,否则Kineta没有义务公开更新或修改任何前瞻性陈述,无论是由于新信息、未来事件还是其他原因。

KVA12123:在TME 1/2期临床研究中,VISTA阻断单抗以解决免疫抑制问题,该研究评估了晚期实体瘤中单独使用 KVA12123 以及与pembrolizumab联合治疗的初始单一疗法数据:清除了前 3 个队列,无剂量限制毒性,VISTA 受体占有率> 90% 临床前抗 CD27 激动剂 maB 以解决耗尽的 T 细胞预计现金流将持续到 2025 年初* 1,030 万股流通股(KA:纳斯达克)4QQ 23:初始单一疗法疗效数据 2Q24:其他单一疗法安全性和疗效数据 2Q24:初始联合疗法数据以先天免疫为重点的管道预期 KVA12123 催化剂的财务状况 Kineta 正在开发解决癌症免疫抵抗问题的下一代免疫疗法,潜在的里程碑付款约为 13 亿美元,加上净销售额的特许权使用费 *包括截至第 23 季度的 780 万美元现金、10 月 23 日收到的 300 万美元默沙东里程碑款项以及预计于 4 月 24 日完成的 2250 万美元的 PIPE 融资
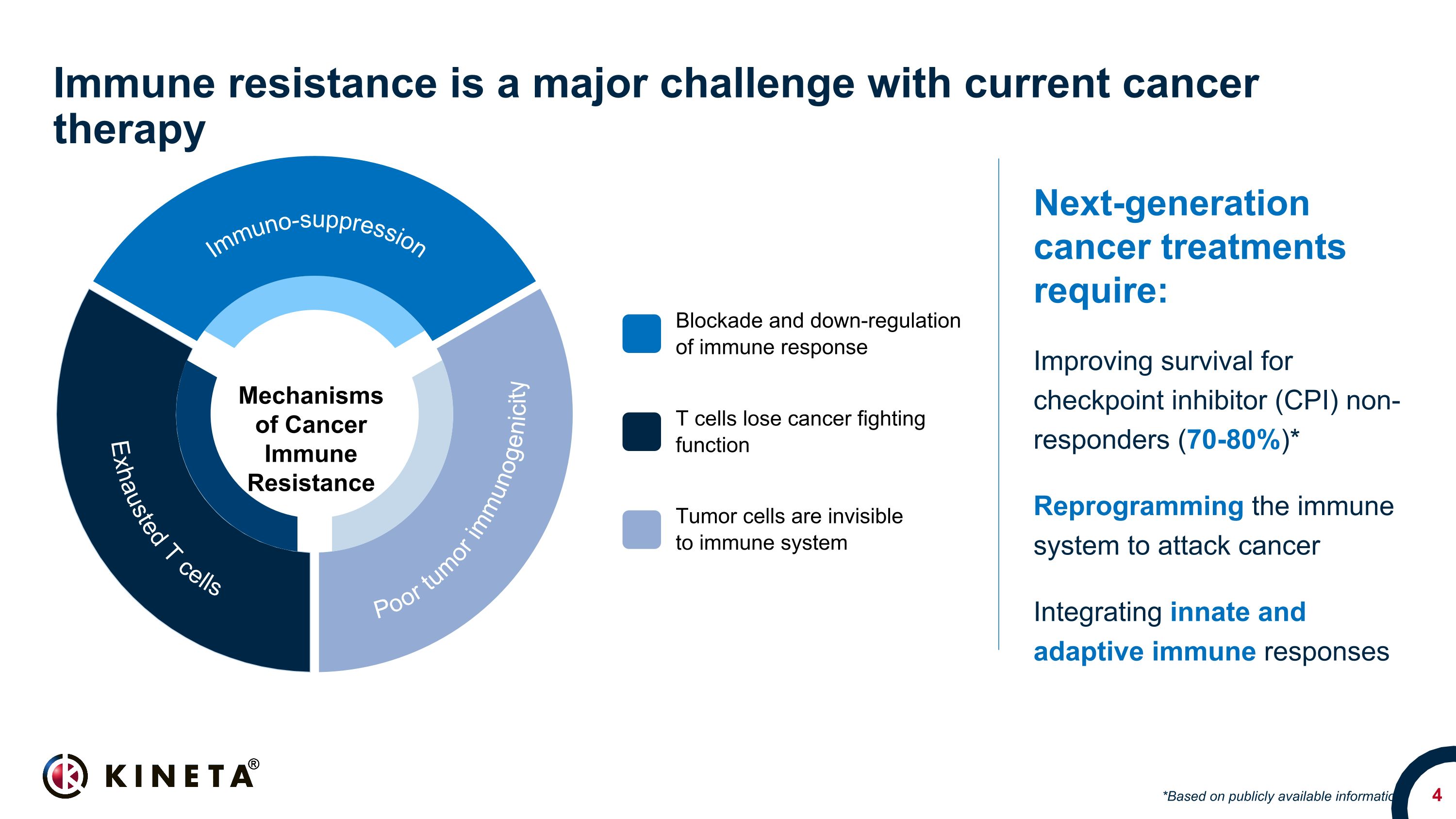
免疫耐药性是当前癌症治疗面临的主要挑战下一代癌症治疗需要:提高检查点抑制剂(CPI)无应答者的存活率(70-80%)* 重新编程免疫系统以攻击癌症整合先天和适应性免疫反应 *基于公开信息 T细胞失去抗癌功能肿瘤免疫抵抗机制肿瘤免疫原性差免疫抑制

Kineta 产品线整合了先天免疫和适应性免疫以解决抗癌机制先天免疫参与癌症早期反应参与适当适应性免疫的必要驱动因素抗癌的重要原因适应性免疫大多数竞争对手的药物开发仅专注于 T 细胞适应性免疫固有免疫适应性免疫树突状细胞巨噬细胞巨噬细胞嗜酸性粒细胞 basphil Natural Killer tcell B 细胞抗体 CD4 T 细胞 CD8 T 细胞 ab T 细胞
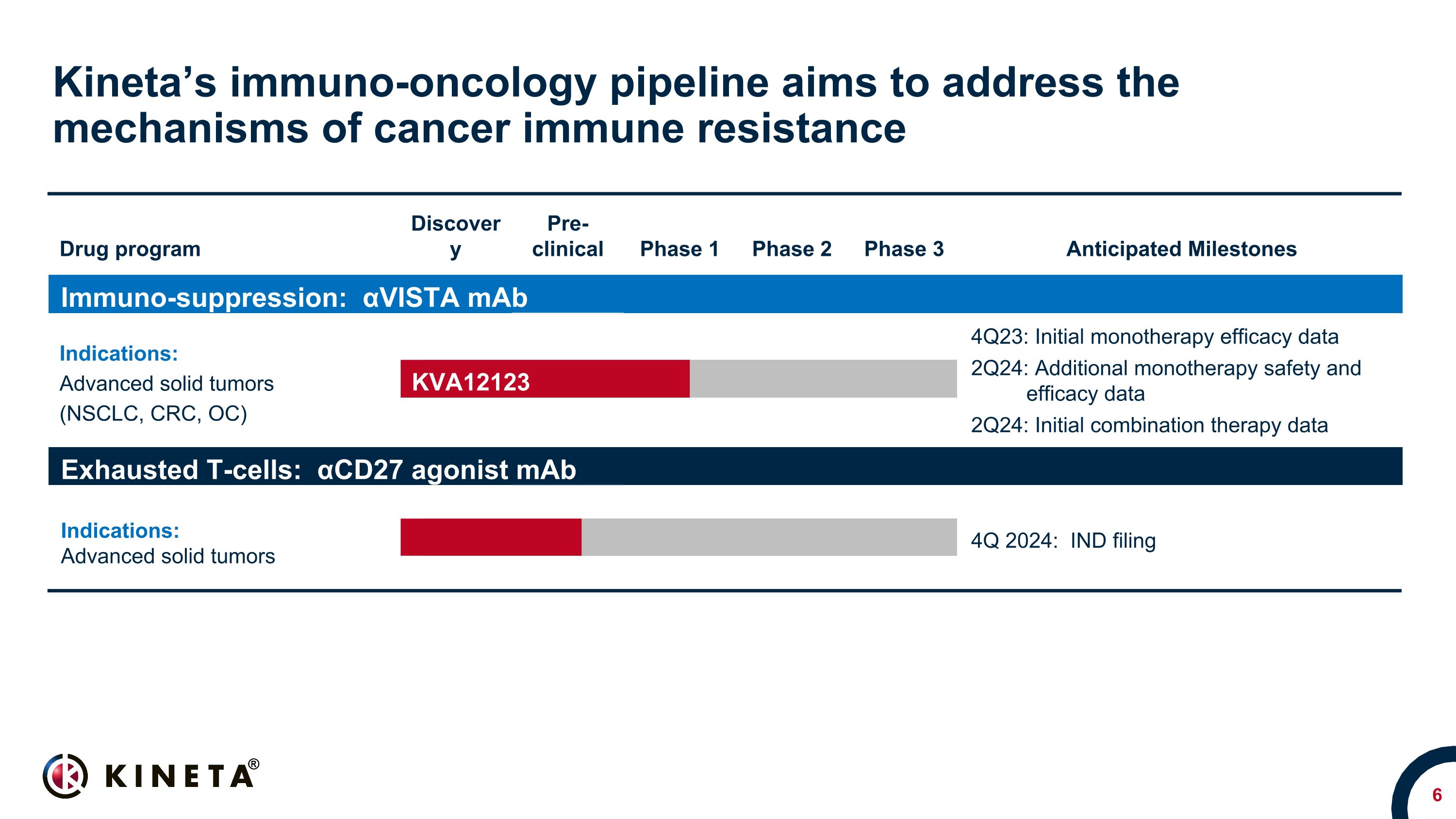
Kineta 的免疫肿瘤学产品线旨在解决癌症免疫耐药药物项目的机制临床前 1 期 2 期 3 期预期里程碑免疫抑制:αVista 单抗适应症:晚期实体瘤(NSCLC、CRC、OC)晚期实体瘤 NSCLC、CRC、OC 和 SCCHN* 4Q23:单一疗法初始疗效数据 2Q24:其他单一疗法安全性和有效性数据 2Q24:初始组合治疗数据耗尽 T 细胞:αCD27 激动剂 maB 适应症:晚期实体瘤晚期实体瘤 2024 年第四季度:IND 申报 KVA12123

kva12123 潜在的差异化 VISTA 阻断免疫疗法

VISTA 是肿瘤微环境中免疫抑制的关键驱动因素骨髓细胞上表达的免疫抑制蛋白在包括肺癌、结肠癌和卵巢癌在内的感冒肿瘤中高度表达 CPI 治疗后预后上调与治疗失败相关人类肿瘤中 VISTA 阴性 Brown 染色表明 VISTA 表达 VISTA 患者存活率在 pembrolizizi 期间黑色素瘤患者 VISTA 表达增加 umab 复发/进展 2 参考文献:1.Kuklinski 等人。2018;2.Kakavand 等人。2017
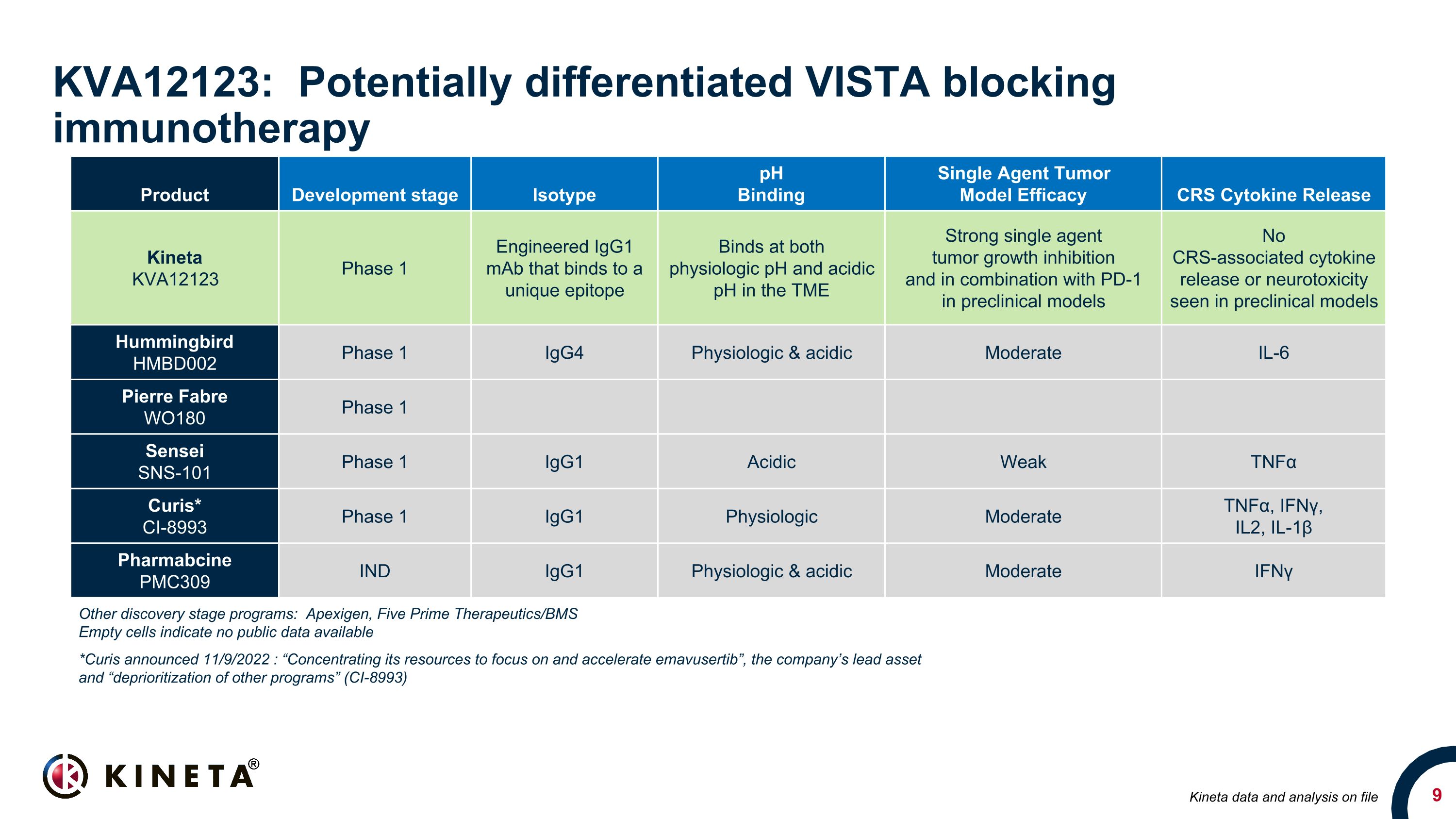
KVA12123:潜在差异化 VISTA 阻断免疫疗法产品开发阶段同型 pH 结合单剂肿瘤模型功效 CRS 细胞因子释放 Kineta KVA12123 1 期工程化的 IgG1 单抗结合独特的表位在 TME 的生理 pH 值和酸性 pH 值下结合强烈的单药肿瘤生长抑制以及在临床前模型中与 PD-1 联合使用临床前模型中未出现与 CRS 相关的细胞因子释放或神经毒性模型 Hummingbird HMBD002 第 1 期 IgG4 生理学和酸性中度 IL-6 Pierre Fabre WO180 第 1 阶段 SenseiSNS-101 第 1 期 Igg1 酸性弱肿瘤坏死因子 α Curis* CI-8993 第 1 期 Igg1 生理中度肿瘤坏死因子 α、IFNγ、IL-1β Pharmaccine PMC309 IND Igg1 生理和酸性中度 IFNγ其他发现阶段项目:Apexigen、Five Prime Therapeutics/BMS 空细胞表示没有可用的公开数据 *Curis 于 2022 年 9 月 11 日宣布:“将其资源集中于关注并加速公司的主要资产 “emavusertib” 和 “降低其他程序的优先级” (CI-8993) Kineta 数据和存档分析
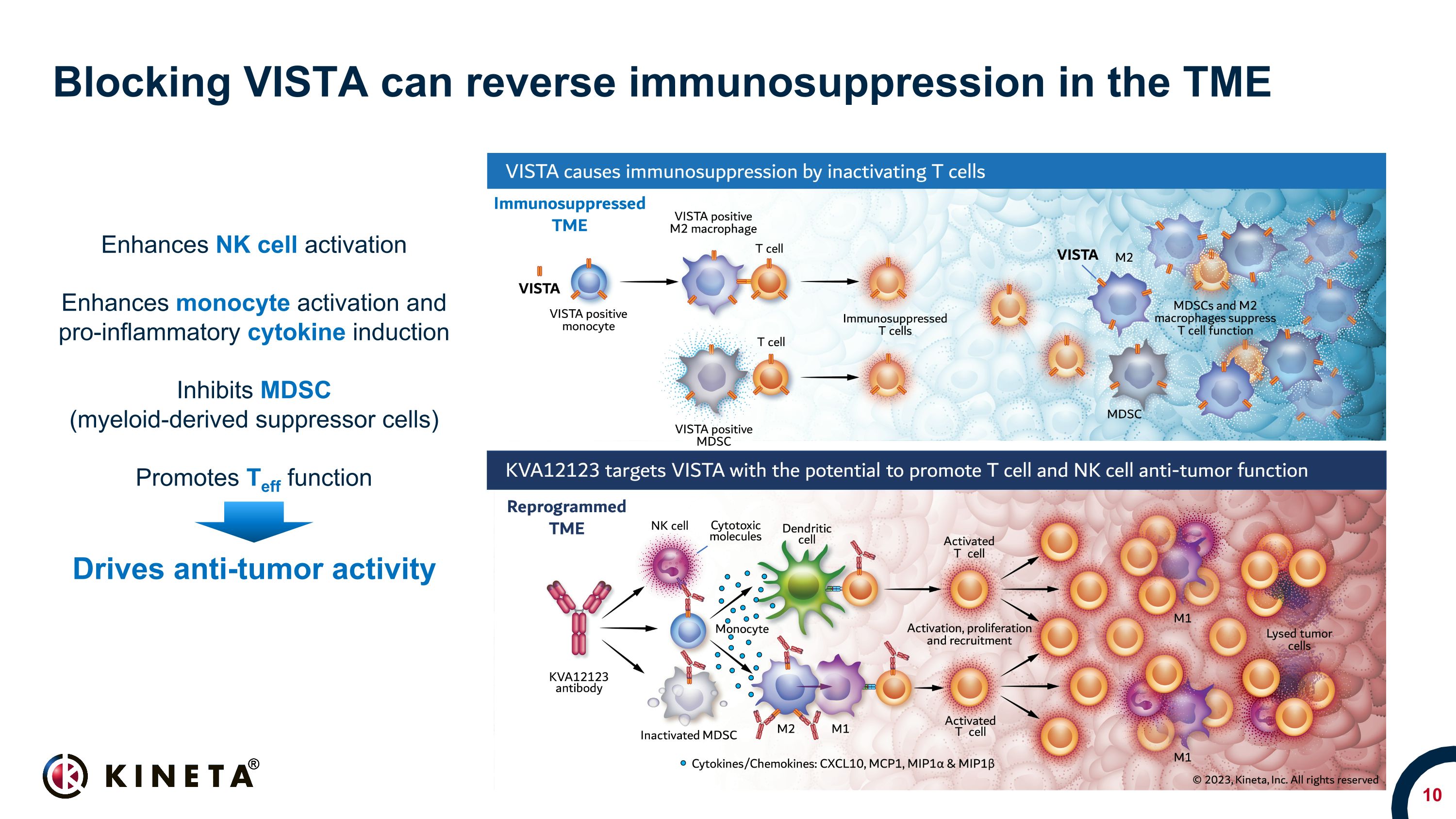
阻断 VISTA 可以逆转 TME 中的免疫抑制增强 NK 细胞活化增强单核细胞激活和促炎细胞因子诱导抑制 MDSC(髓系衍生抑制细胞)促进 Teff 功能推动抗肿瘤活性
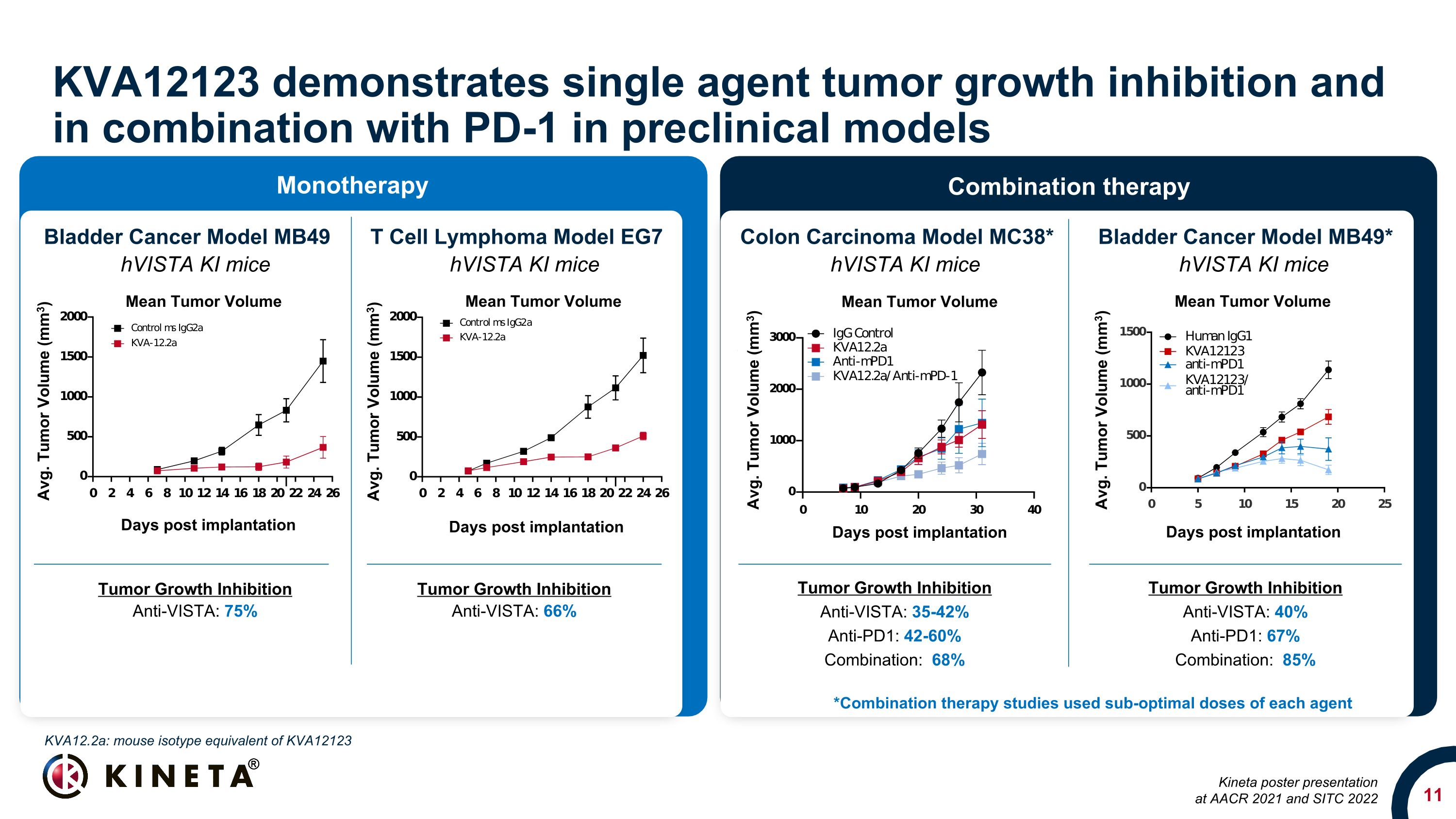
KVA12123 表现出单药肿瘤生长抑制作用,在临床前模型中与 PD-1 联合使用肿瘤生长抑制剂 Anti-Vista:35-42% 抗 PD1:42-60% 组合:68% 结肠癌模型 MC38* 膀胱癌模型 MB49 T 细胞淋巴瘤模型 MB49* HVista KI 小鼠肿瘤生长抑制抗Vista:40% Anti-PD1:67% 组合:85% 肿瘤生长抑制剂 AntiVista:75% 肿瘤生长抑制剂 AntiVista:66% *联合疗法研究使用了每种药物的次优剂量kva12.2a:小鼠同型相当于 KVA12123 Kineta 海报在 AACR 2021 和 SITC 2022 单一疗法联合疗法植入后平均肿瘤体积天数平均值。肿瘤体积 (mm3) 植入后平均肿瘤体积天数肿瘤体积 (mm3) 平均值肿瘤体积 (mm3) 植入后天数平均值肿瘤体积 (mm3) 植入后平均肿瘤体积天数肿瘤体积 (mm3) 平均肿瘤体积
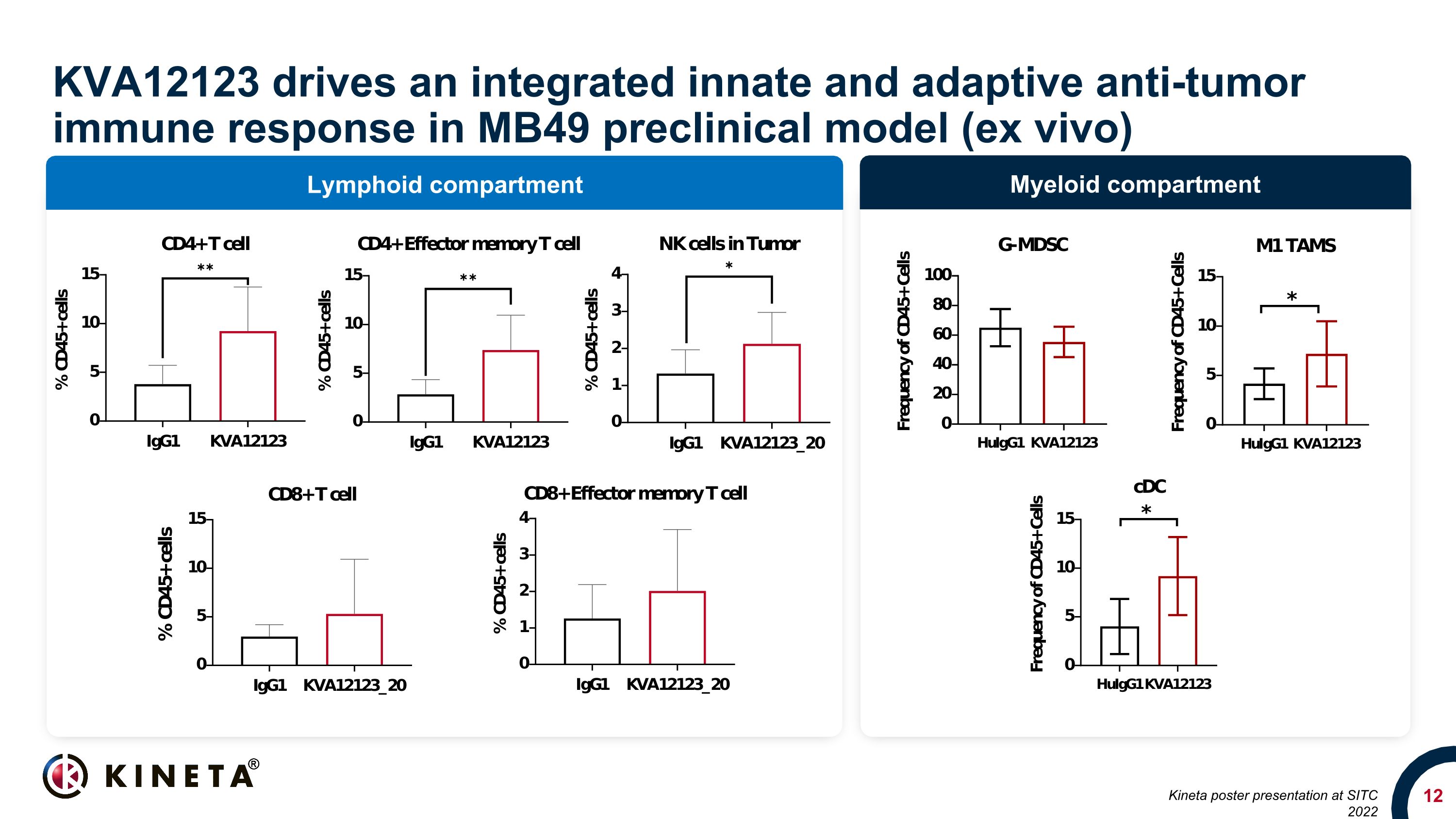
骨髓隔室 Lymphoid 隔间 KVA12123 在 MB49 临床前模型(体外)中推动 Kineta 海报在 SITC 2022 上发布的综合先天和适应性抗肿瘤免疫反应
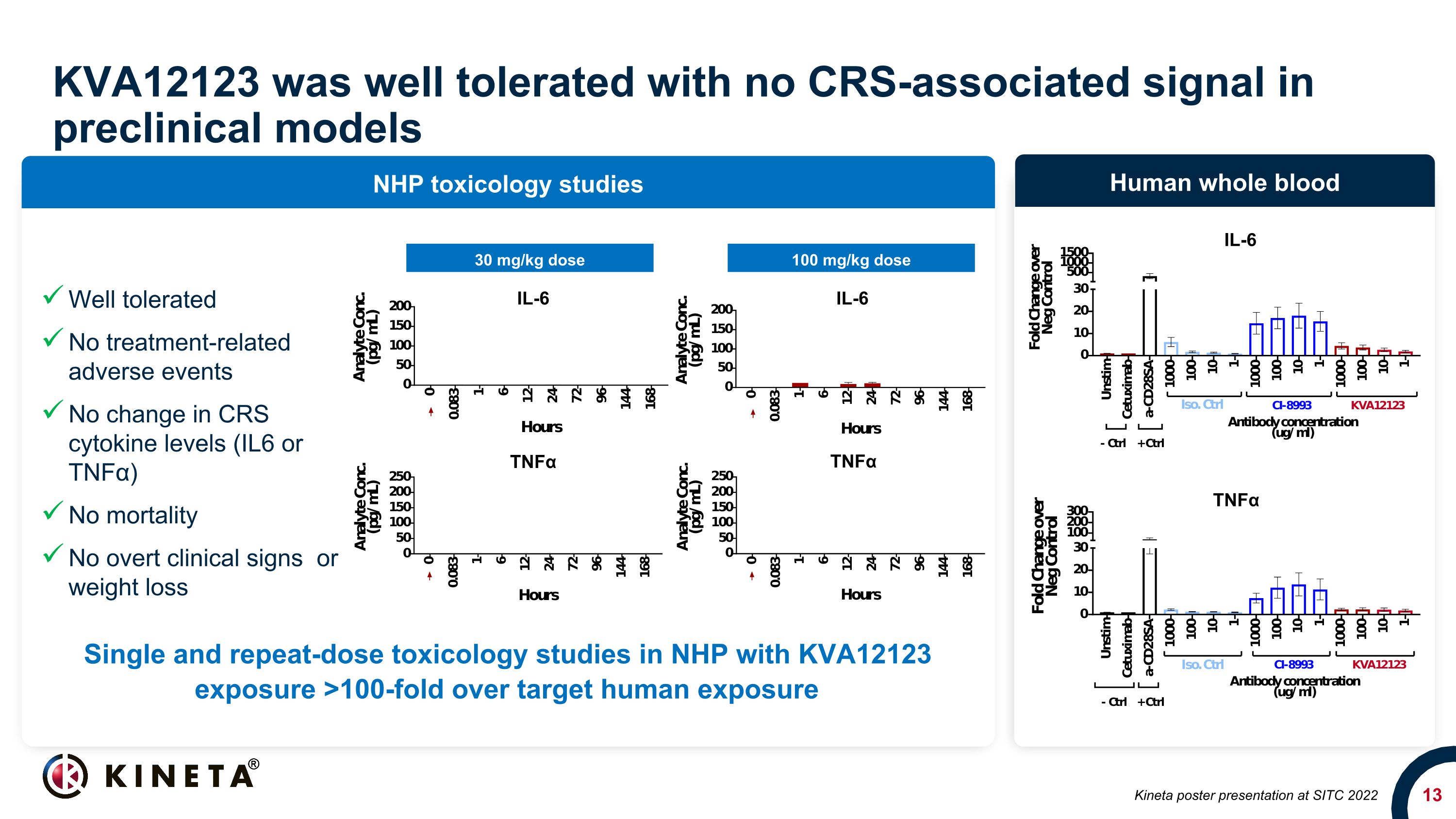
KVA12123 耐受性良好,临床前模型中没有 CRS 相关信号 NHP 毒理学研究人类全血 30 mg/kg 剂量 100 mg/kg 剂量 TNFα IL-6 Kineta 海报在 SITC 2022 上进行单剂量和重复剂量毒理学研究中 KVA12123 暴露量比目标人体暴露量高出 100 倍耐受性良好无治疗相关不良事件 CRS 细胞因子水平(IL6 或 TNFα)无死亡率没有明显的临床症状或减肥 IL-6 IL-6 TNFα 肿瘤坏死因子α
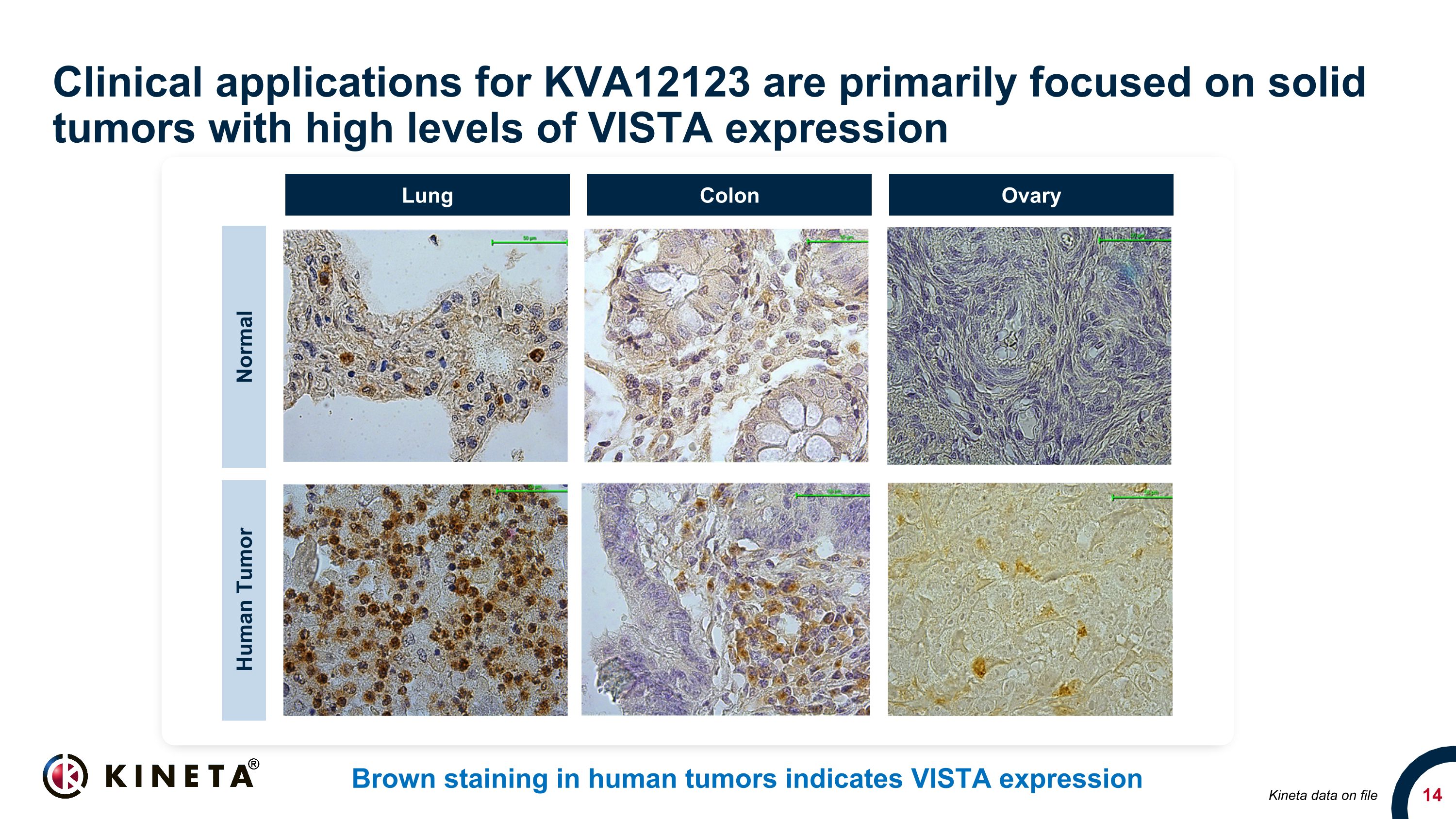
KVA12123 的临床应用主要集中在 VISTA 表达水平高的实体瘤上。人类肿瘤中的棕色染色表明 VISTA 表达 20x 20x 正常人类肿瘤肺结肠子房 Kineta 数据存档

VISTA-101:在晚期实体瘤患者中单独使用 KVA12123 以及与派姆博利珠单抗联合使用的 1/2 期开放标签临床试验患者群体:针对晚期实体瘤患者(最多 60 名患者)的 1 期篮子试验 NSCLC、HNSCC、OC、CRC、RCC 和 TBD 其他患者 2 期研究目标:主要:安全性和耐受性、推荐的 2 期剂量(RP2D)或最大耐受剂量(MTD)) of KVA12123 次要:ireCist (ORR) 中晚期实体瘤受试者的药代动力学、免疫原性、肿瘤反应探索性:生物标志物和受体占用默沙东研究合作临床试验合作和 KEYTRUDA® 供应协议
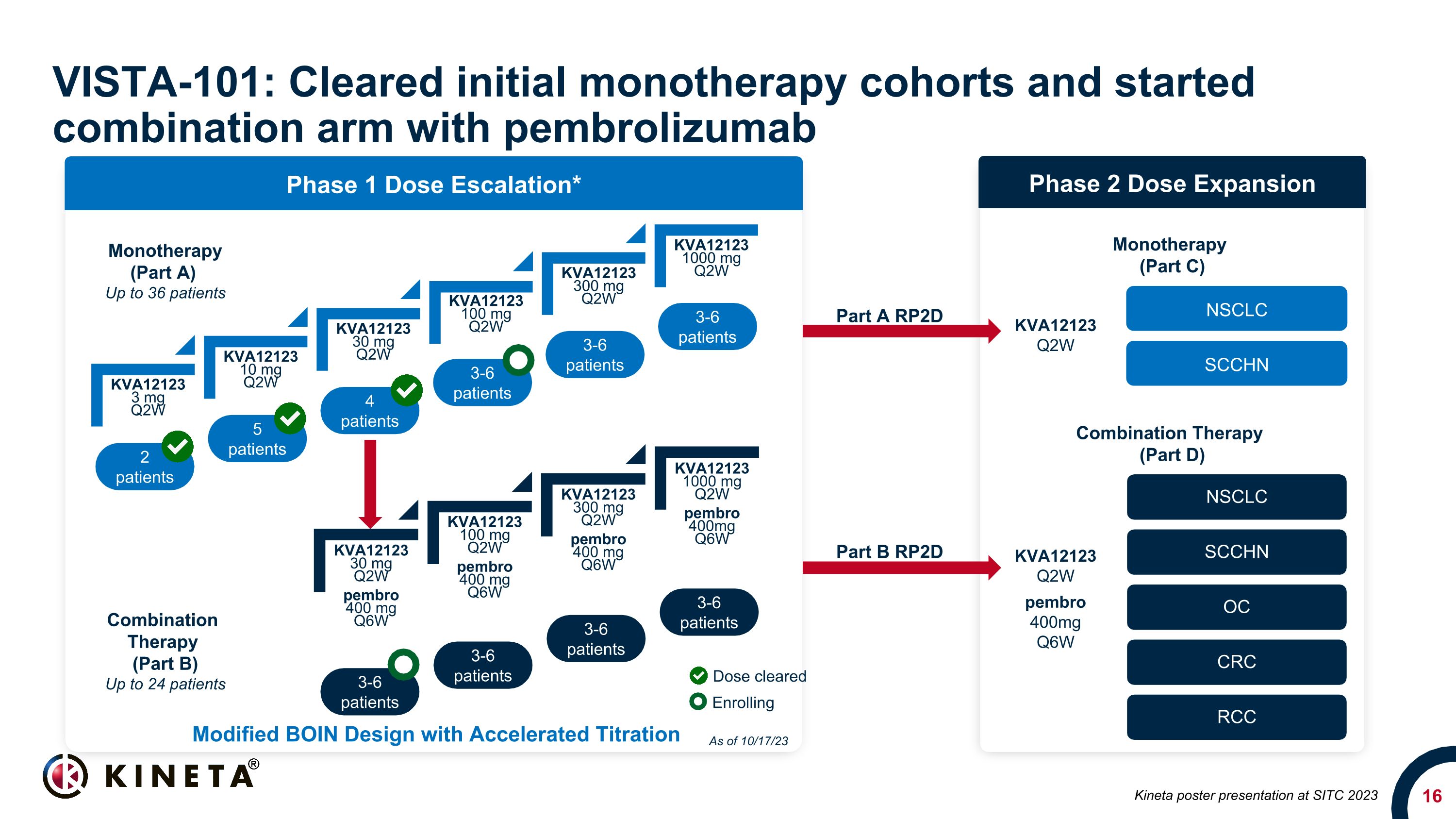
KVA12123 3 mg Q2W KVA12123 10 mg Q2W KVA12123 30 mg Q2W KVA12123 100 mg Q2W KVA12123 300 mg Q2W KVA12123 1000 mg Q2W VISTA-101:清理了最初的单一疗法队列并开始联合使用 pembrolizumab 2 名患者 5 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名患者 3-6 名CLC SCCHN OC CRC RCC NSCLC SCCHN 单一疗法(A 部分)最多 36 名患者联合疗法(B 部分)最多 24 名患者单一疗法(C 部分)组合疗法(D 部分)A 部分 RP2D 部分B RP2D KVA12123 Q2W pembro 400mg Q6W KVA12123 Q2W 经过修改的 BOIN 设计已批准加速滴定剂量正在注册 KVA12123 30 mg Q2W pembro 400 mg q6W KVA12123 100 mg Q2W pembro 400 mg Q6W KVA12123 300 mg Q2W pembro 400 mg q6W 截至 10 月 17 日 Kineta 海报在 2023 年国际贸易标准大会上的演讲 KVA12123
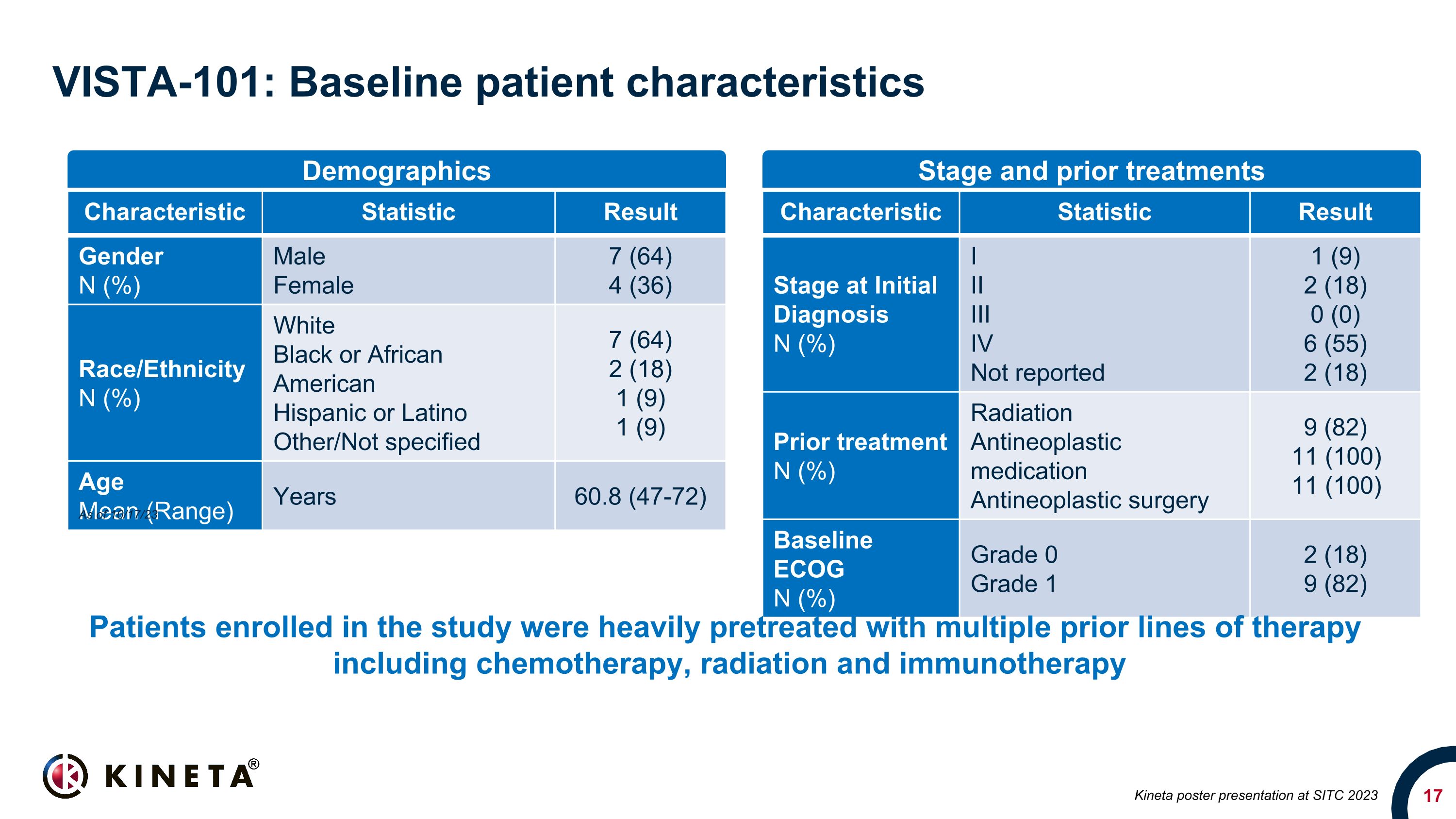
VISTA-101:基线患者特征特征统计结果性别 N (%) 男女 7 (64) 4 (36) 种族/民族 N (%) 白人黑人或非裔美国人西班牙裔或拉丁裔其他/未指定 7 (64) 2 (18) 1 (9) 1 (9) 年龄平均值(范围)年龄 60.8 (47-72) 初始诊断时的特征统计结果阶段 N (%) I III IV 未报告 1 (9) 2 (18) 0 (0) 6 (55) 2 (18) 之前的治疗 N (%) 放射抗肿瘤药物抗肿瘤手术 9 (82) 11 (100) 11 (100) 基线 ECOG N (%) 0 级 1 2 (18) 9 (82) 人口统计阶段和之前的治疗 Kineta 在 SITC 2023 上的海报展示截至 23 年 10 月 17 日,参加该研究的患者接受了包括化疗、放射治疗和免疫疗法在内的多种先前疗法的大量预治疗
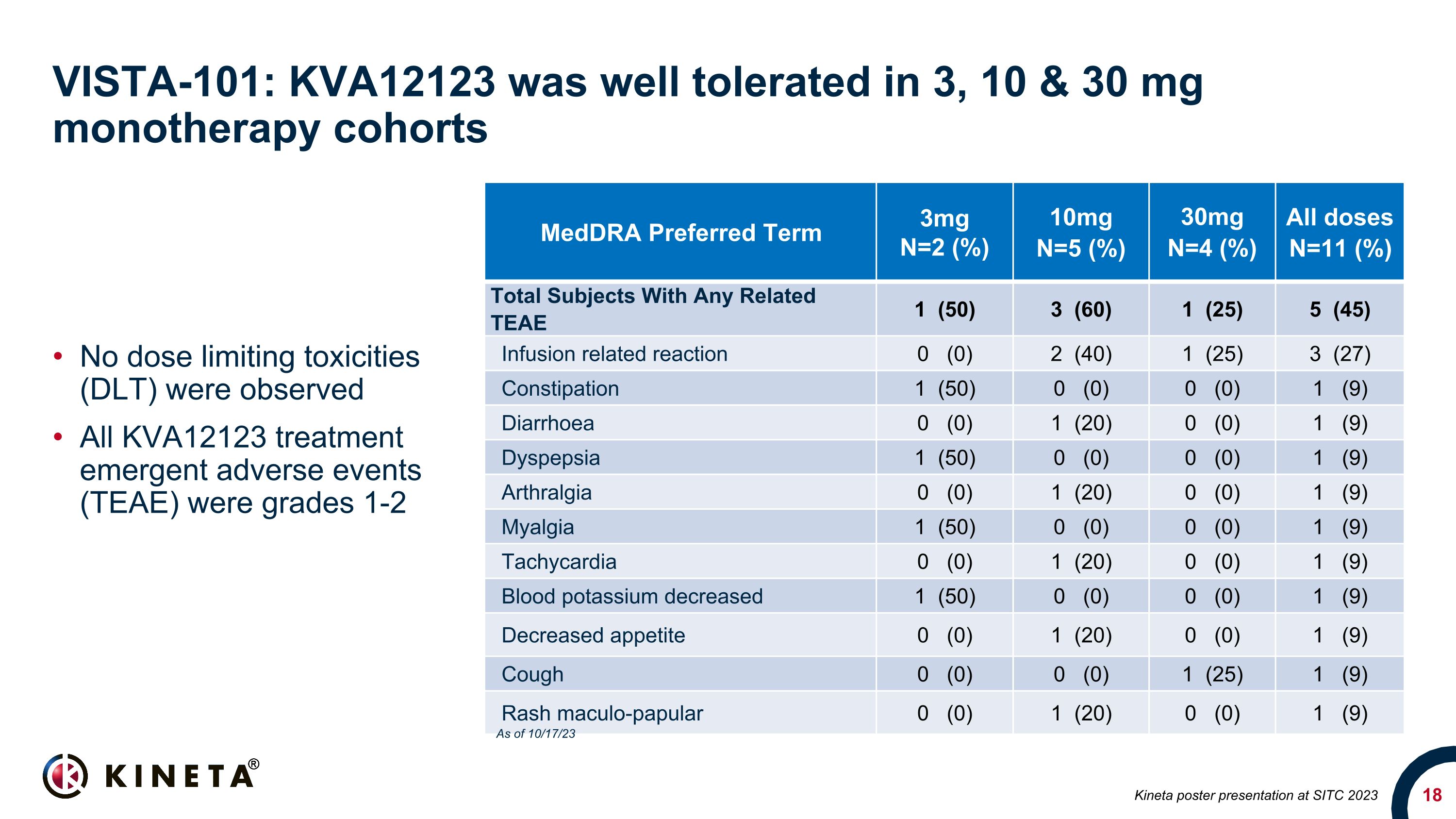
VISTA-101:KVA12123 在 3、10 和 30 mg 的单一疗法队列中耐受性良好。未观察到剂量限制毒性 (DLT) 所有 KVA12123 治疗紧急不良事件 (TEAE) 均为 1-2 级 medDra 优先周期 3mg N=2 (%) 10mg N=4 (%) 所有剂量n=11 (%) 任何相关的 Teae 的受试者总数 1 (50) 3 (60) 1 (25) 5 (45) 输液相关反应 0 (0) 2 (40) 1 (25) 3 (27) 便秘 1 (50) 0 (0) 0 (0) 1 (9) 腹泻 0 (0) 1 (0) 0 (0) 0 (0) 0 (0) 1 (9) 消化不良 1 (50) 0 (0) 0 (0) 1 (9) 关节痛 0 (0) 1 (0) 1 (20) 0 (0) 1 (9) Myalgia 1 (50) 0 (0) 0 (0) 1 (9)心动过速 0 (0) 1 (20) 0 (0) 1 (9) 血钾降低 1 (50) 0 (0) 0 (0) 0 (0) 1 (9) 食欲下降 0 (0) 1 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (9) 0 (0) 0 (0) 1 (0) 1 (0) 1 (0) 1 (0) (9) 截至 23 年 10 月 17 日,在 SITC 2023 上发布 Kineta 海报
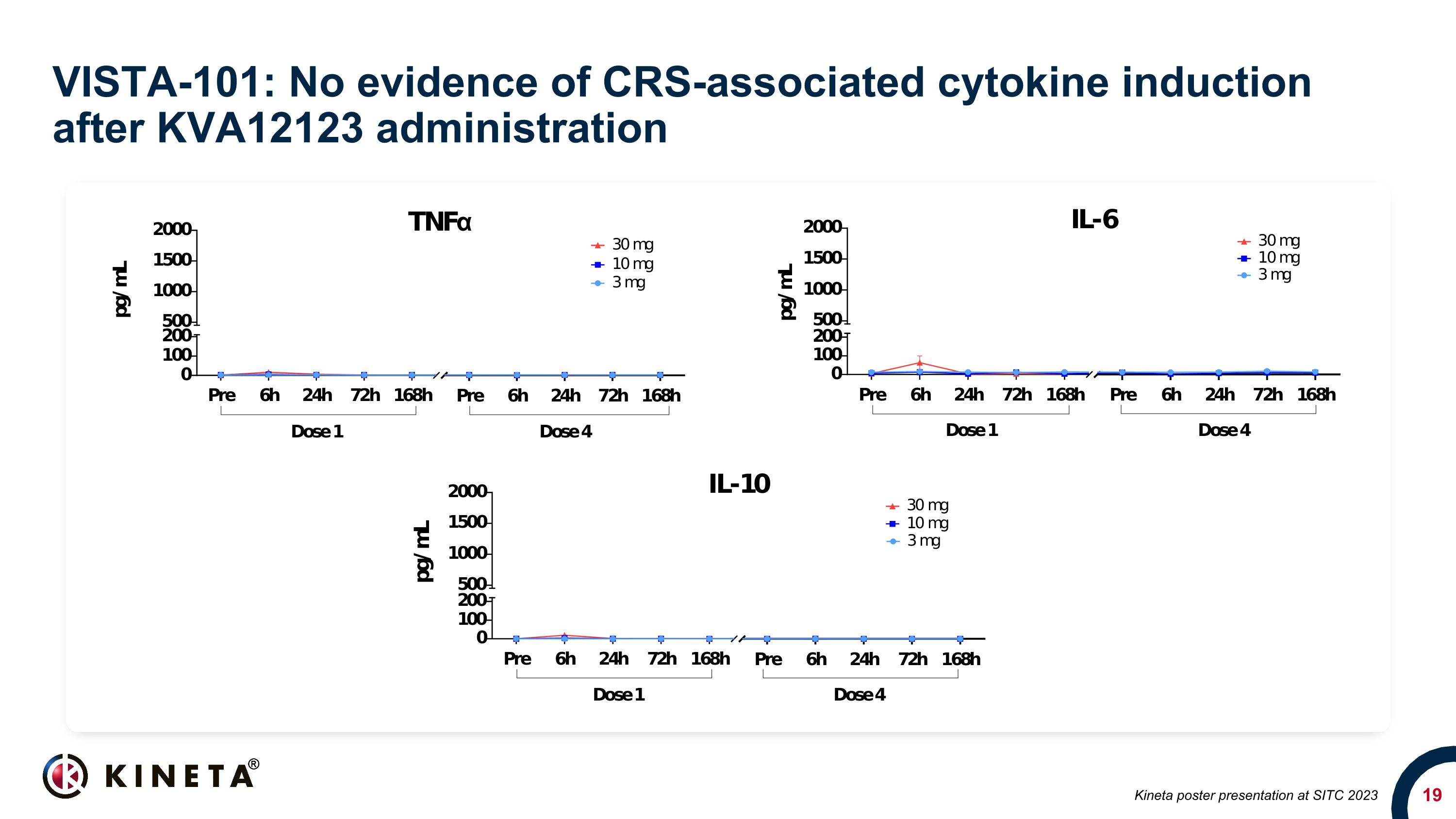
VISTA-101:使用 KVA12123 后没有证据显示 CRS 相关的细胞因子诱导 Kineta 在 SITC 2023 上发布海报

VISTA-101:KVA12123 表现出大于剂量比例的 PK 曲线,在 30 mg 队列中,VISTA 受体占有率 (RO) 的患者的 VISTA RO 超过 90% * 药代动力学 *单次给药 KVA12123 后 11 名患者循环单核细胞的 Vista 受体占有率。Kineta 利用专有方法评估 VISTA 受体占用率。*** p
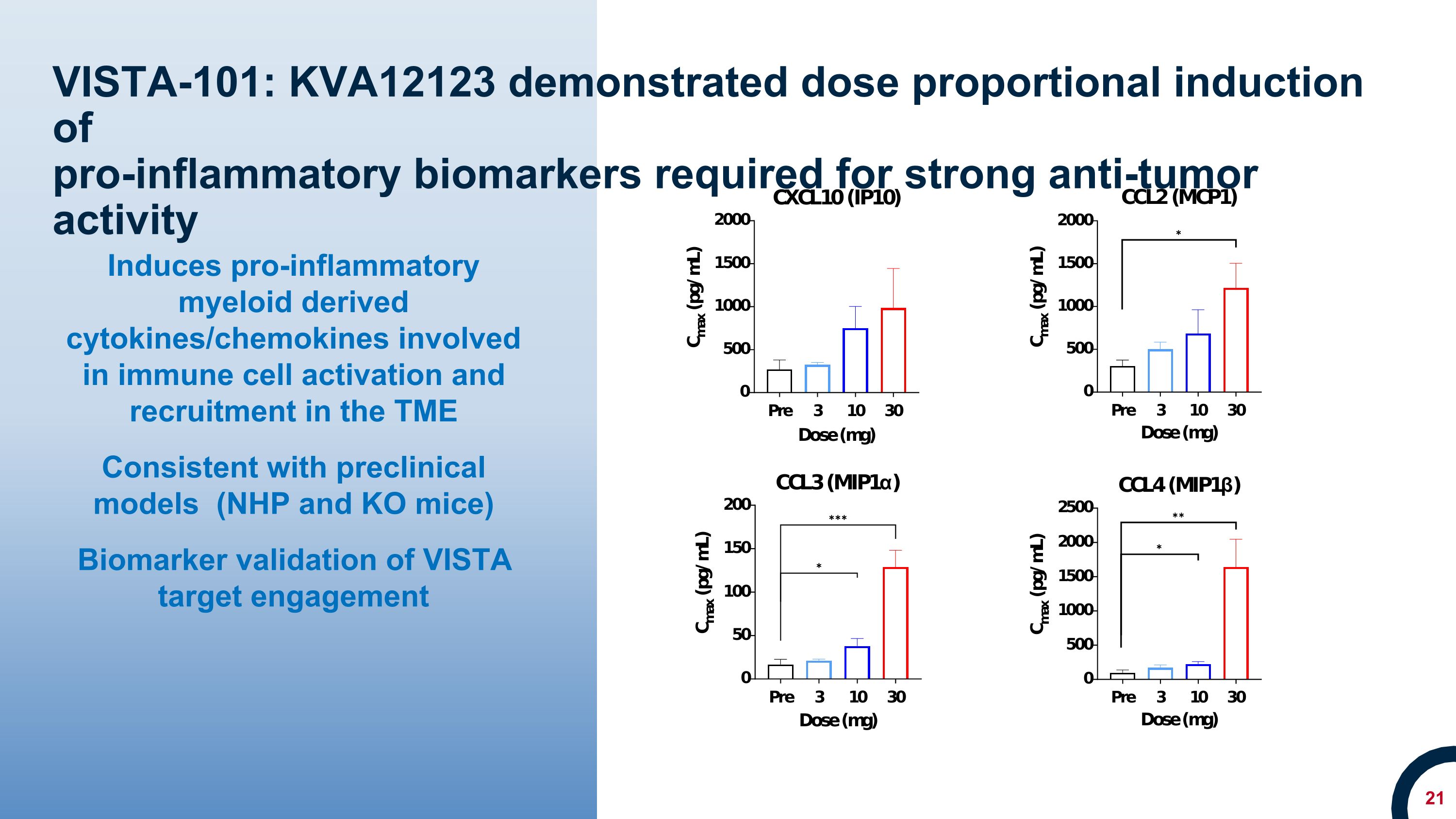
VISTA-101:KVA12123 证明了强抗肿瘤活性所需的促炎生物标志物的剂量成比例诱导促炎髓系衍生的细胞因子/趋化因子参与免疫细胞在 TME 中的激活和招募与临床前模型(NHP 和 KO 小鼠)一致 VISTA 靶标参与度的生物标志物验证
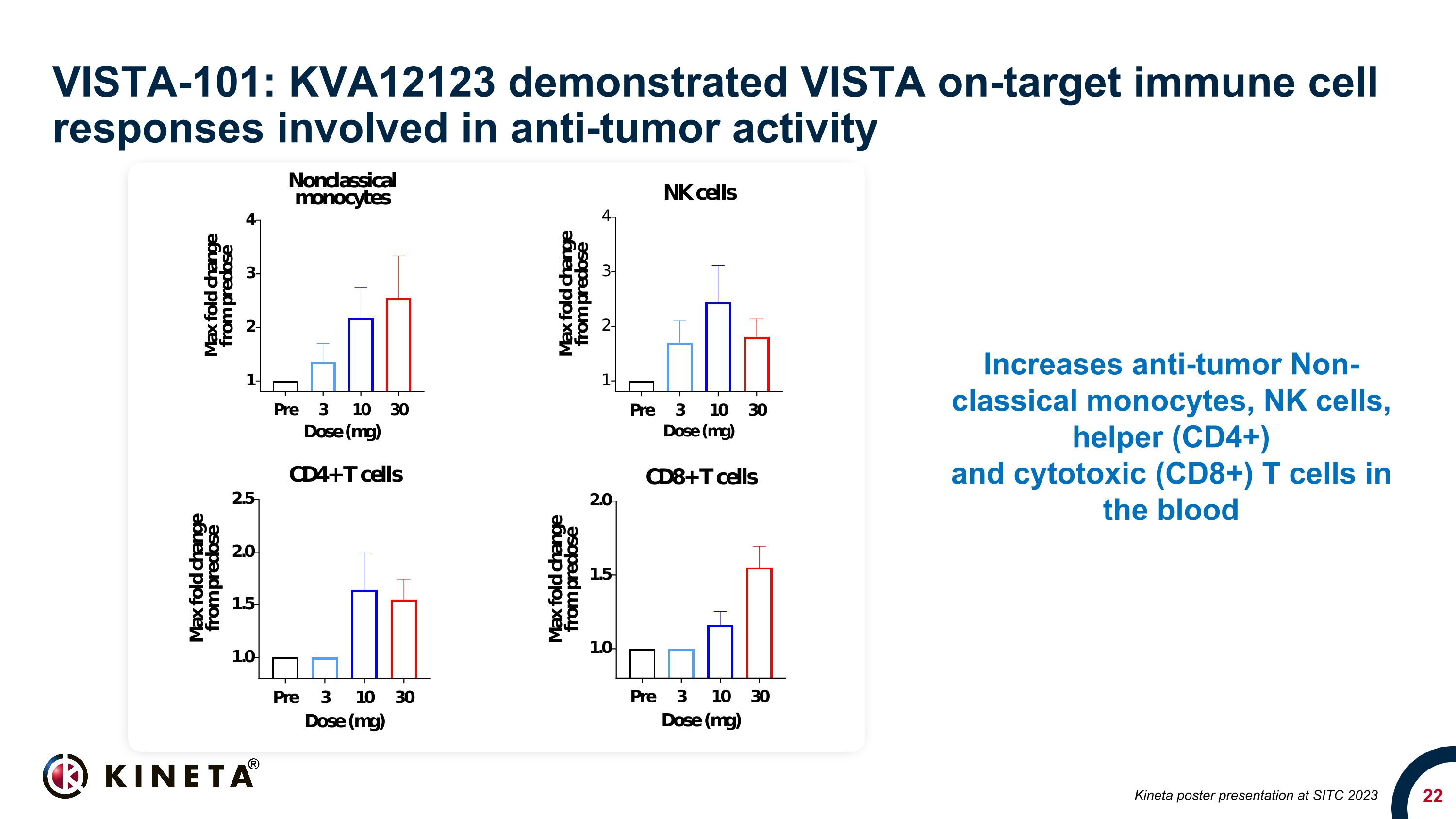
VISTA-101:KVA12123 在 SITC 2023 上展示了参与抗肿瘤活性的 VISTA 靶向免疫细胞反应增加血液中的抗肿瘤非经典单核细胞、NK 细胞、辅助细胞 (CD4+) 和细胞毒性 (CD8+) T 细胞

VISTA-101:KVA12123 临床概况摘要安全性通过前三组 KVA12123 单一疗法队列(3、10、30 mg),其中 11 名患者给药耐受性良好,无剂量限制毒性(DLT)未检测到与 CRS 相关的细胞因子(IL-6、TNFα 和 IL-10)的证据。药代动力学分析显示,药代动力学和受体占用 (RO) KVA12123 的剂量达到 90% 以上 VISTA RO在所有评估剂量中,药物暴露量的增加均大于剂量成比例,这与靶向介导的药物处置一致低剂量生物标志物显示 CXCL10、MCP1、MIP1α 和 MIP1β 与疗效相关的细胞因子分泌,治疗后观察到抗肿瘤免疫细胞亚群发生了显著变化
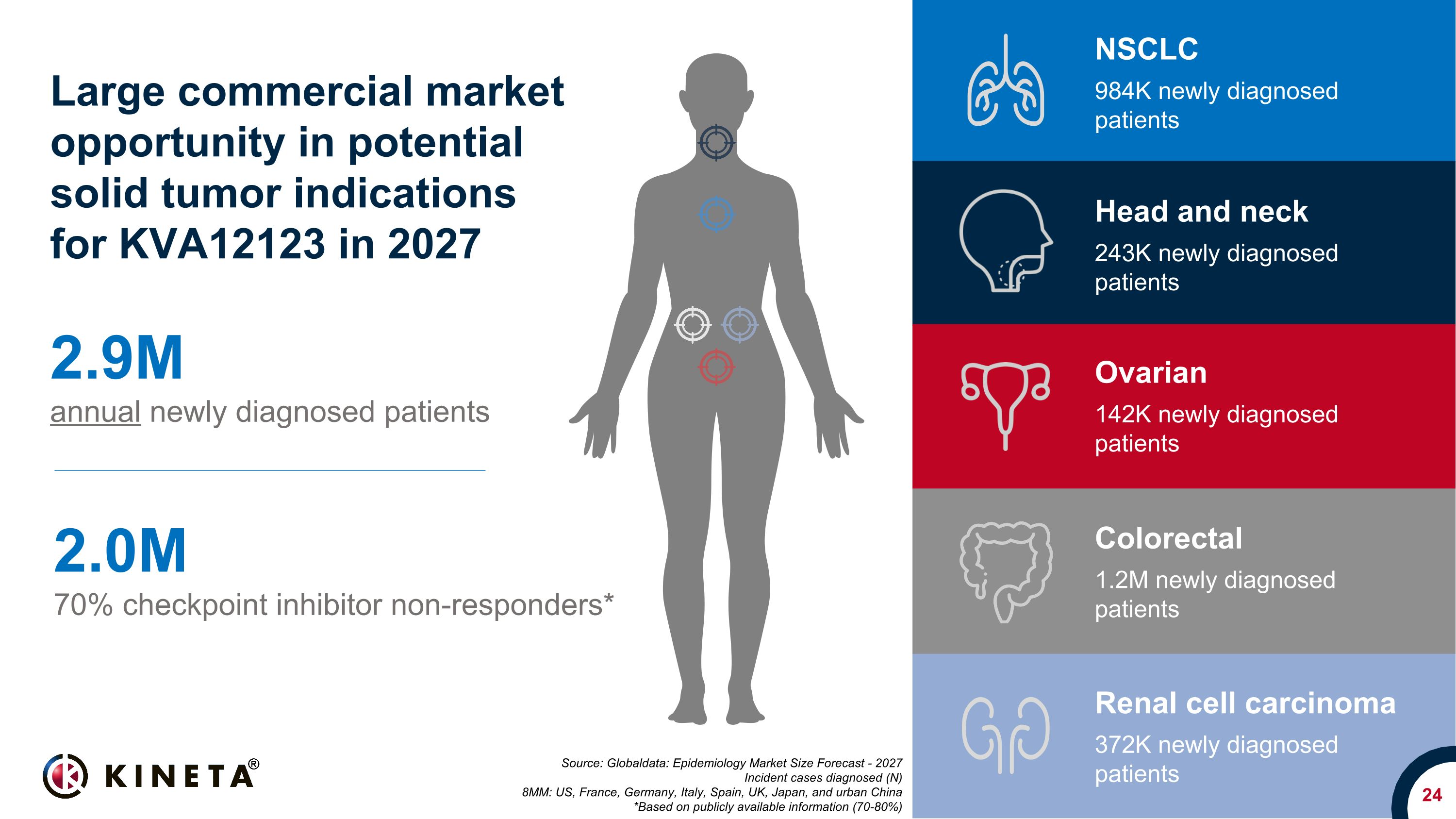
24 来源:全球数据:流行病学市场规模预测——2027 年确诊的事故病例(N)8MM:美国、法国、德国、意大利、西班牙、英国、日本和中国城市 *基于公开信息(70-80%)每年新增确诊患者 290万人 70% 检查点抑制剂无反应者* 2027 年 KVA12123 潜在实体瘤适应症的巨大商业市场机会 NSCLC 984K 新诊断患者结直肠癌 120万新诊断的患者卵巢 142K 新诊断的患者头部和颈部 243K 新诊断的患者肾细胞癌 372K新诊断的患者
抗CD27激动剂单抗免疫疗法
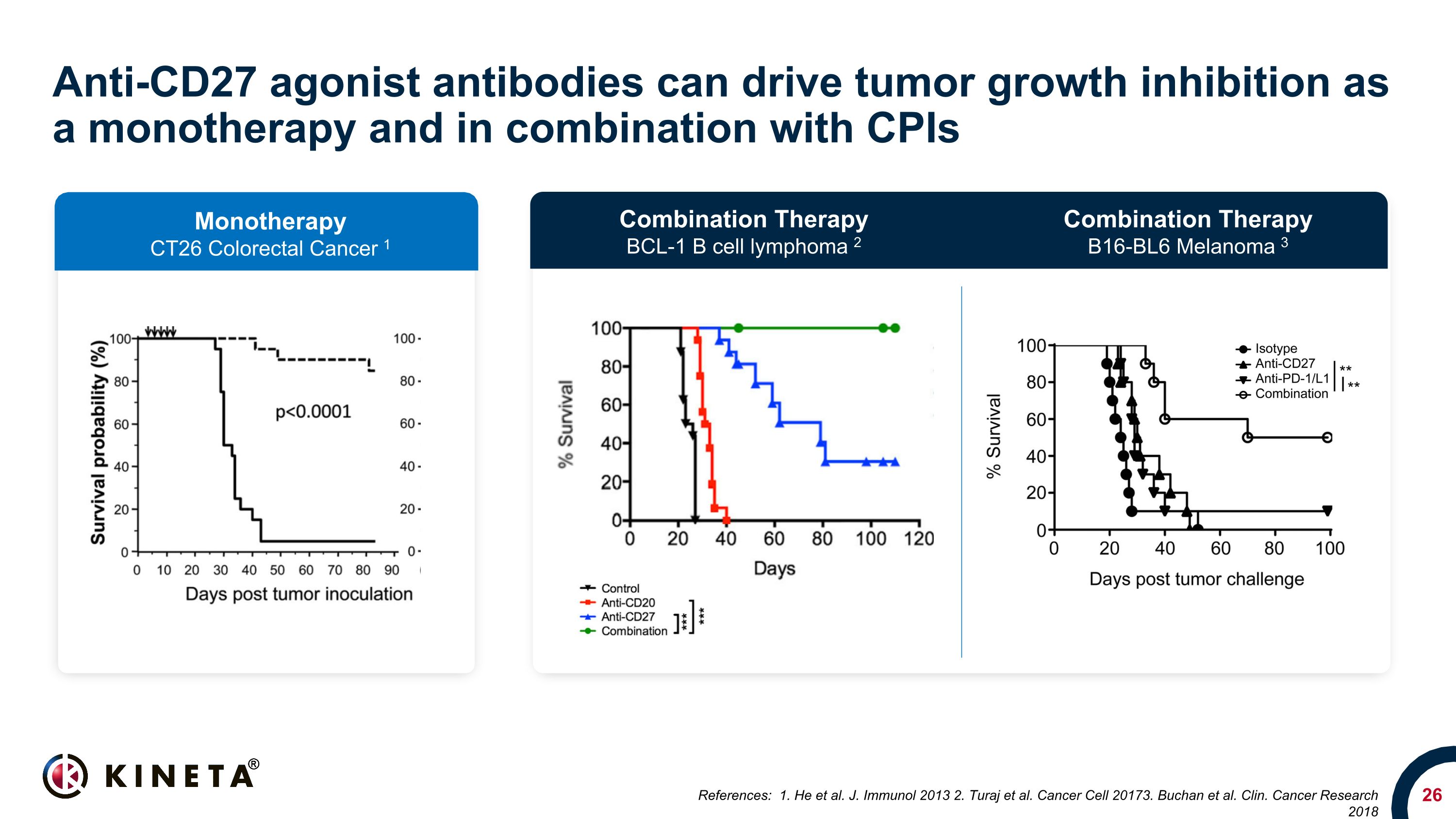
抗CD27激动剂抗体可作为单一疗法驱动肿瘤生长抑制,并与CPIs联合使用参考文献:1.他等。J. Immunol 2013 2.Turaj 等人Cancer Cell 20173。Buchan 等。克林。Cancer Research 2018 单一疗法 CT26 结直肠癌 1 联合疗法 BCL-1 B 细胞淋巴瘤 2 联合疗法 B16-BL6 黑色素瘤 3
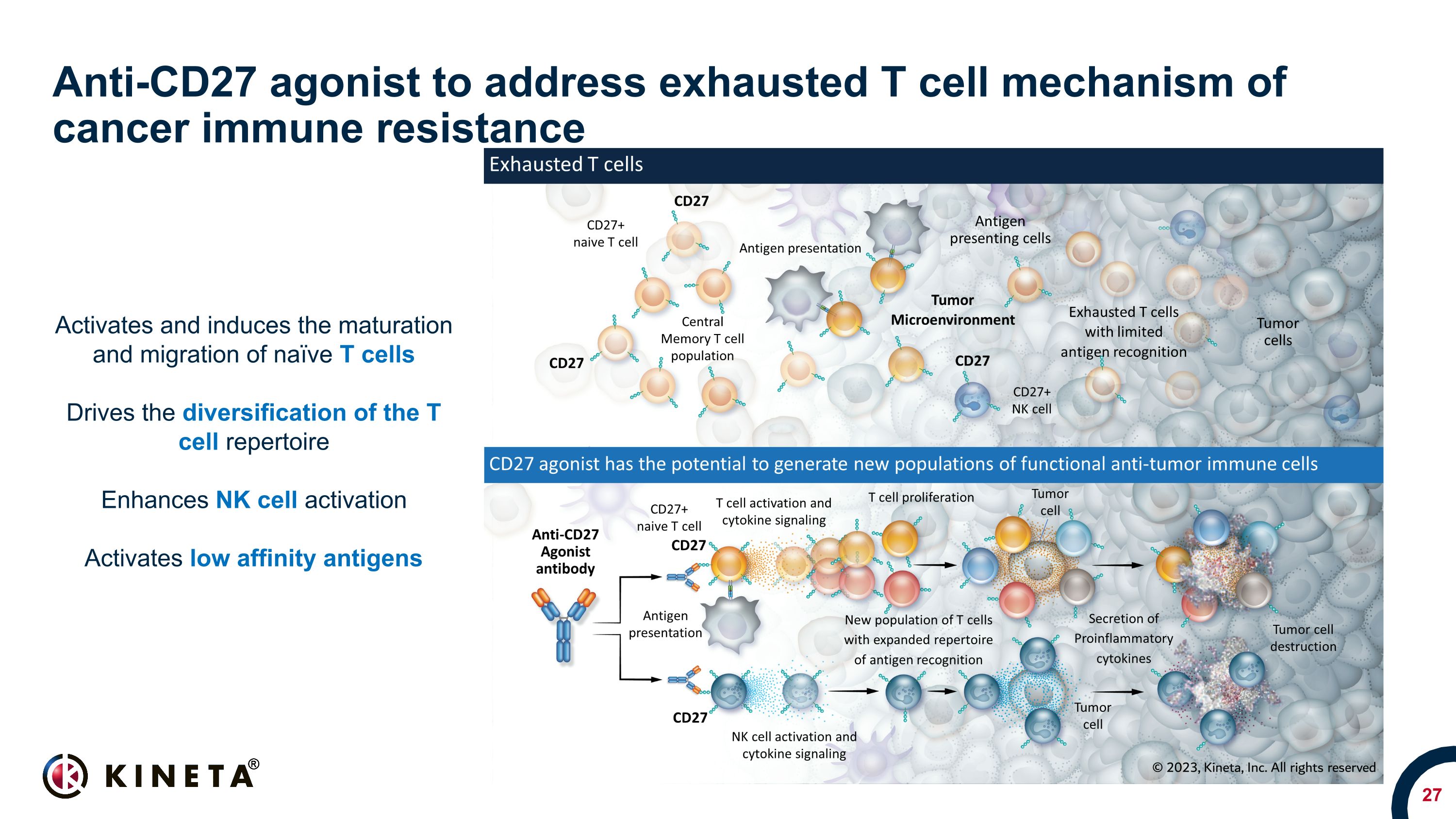
抗CD27激动剂可解决耗尽的T细胞癌症免疫抵抗机制激活和诱导幼稚T细胞的成熟和迁移推动 T 细胞库的多样化增强 NK 细胞激活激活低亲和力抗原
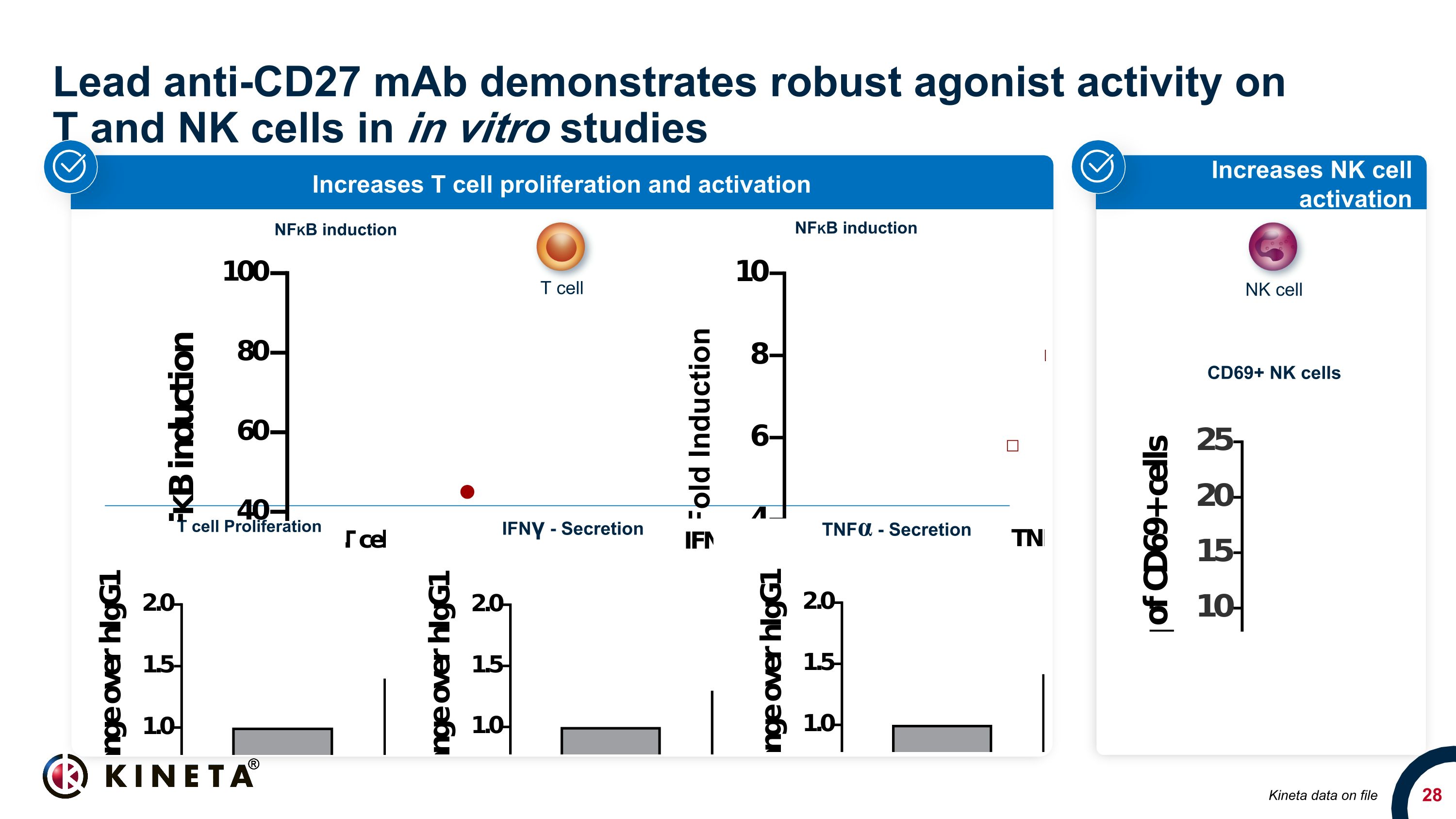
Lead Anti-CD27 单抗体在体外研究中显示出对 T 和 NK 细胞的强大激动剂活性提高 NK 细胞活化增加 T 细胞增殖和激活 T 细胞增殖 IFNγ-分泌物 TNFα-分泌 Kineta 数据存档 CD69+ NK 细胞 T 细胞 NFKB 诱导 NFKB 诱导
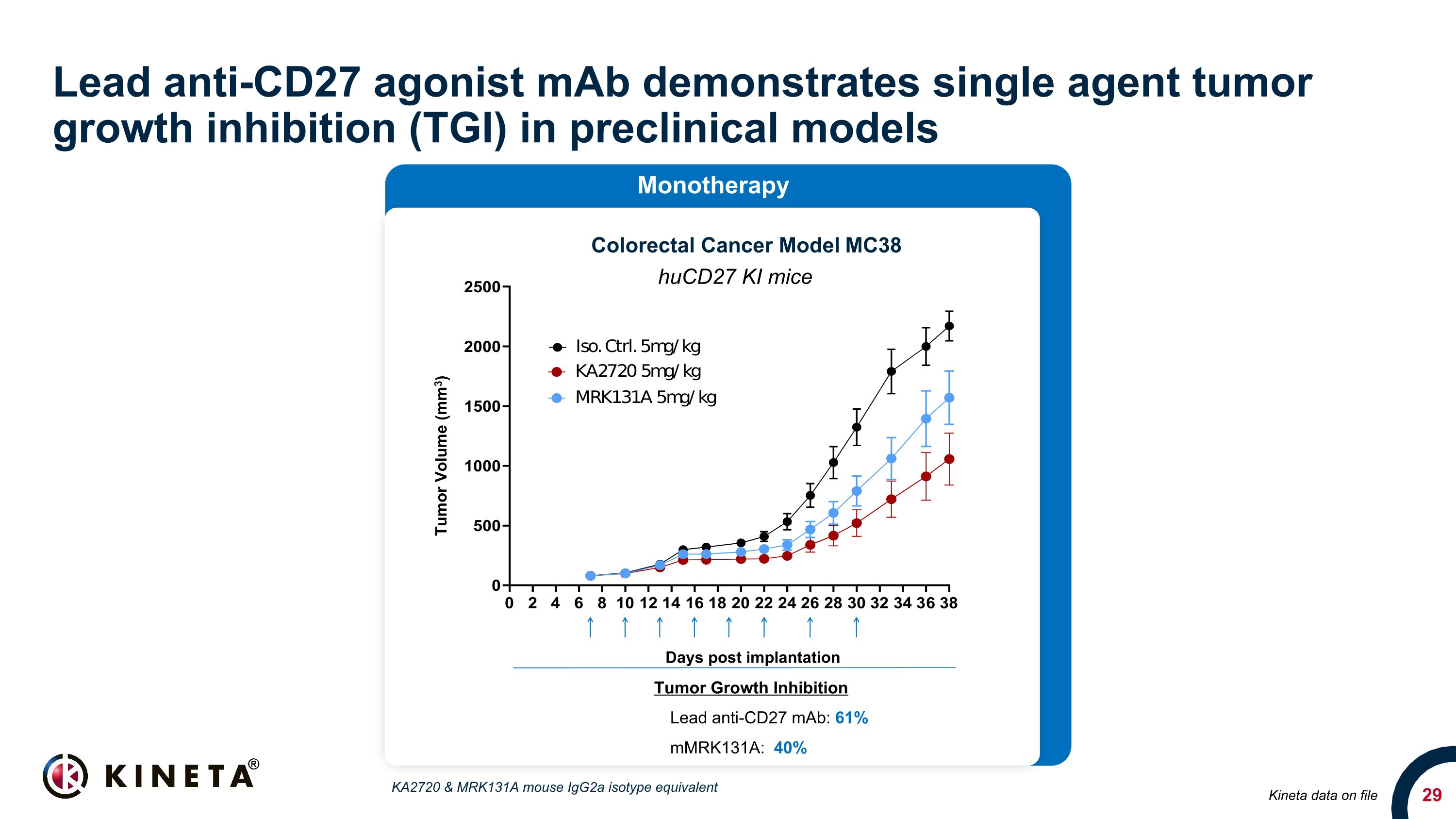
主要抗 CD27 激动剂 maB 在临床前模型中表现出单药肿瘤生长抑制 (TGI) Kineta 数据存档结直肠癌模型 MC38 Hucd27 KI 小鼠肿瘤生长抑制铅抗:61% mmrk131a:40% 植入后单药天数肿瘤体积 (mm3) KA2720 和 MRK131A 小鼠 Igg2a 同种型
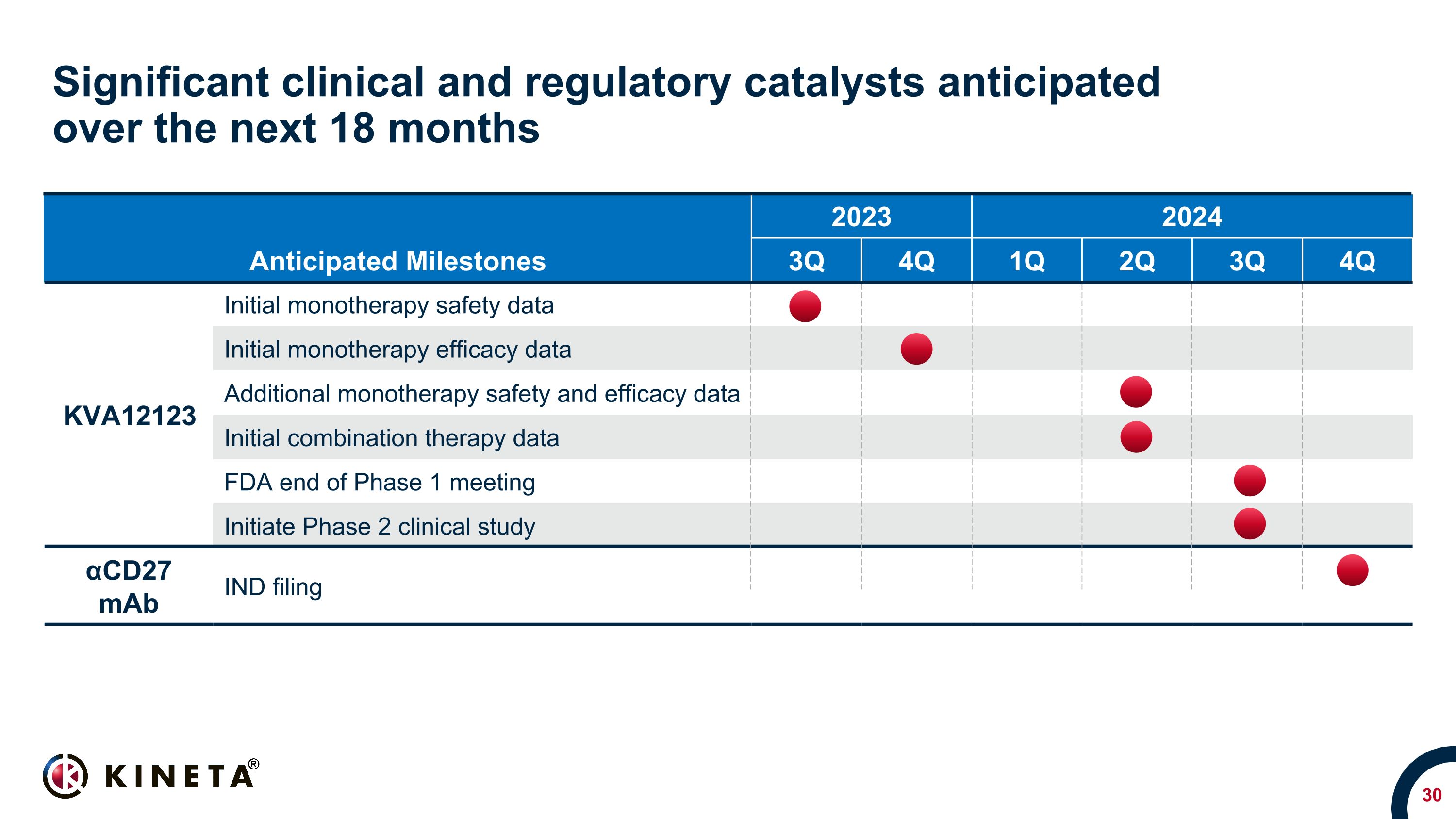
预计在未来 18 个月内将出现重要的临床和监管催化剂预期里程碑 2024 年 2024 年 2024 年 3 季度 4Q 第 1 季度第 2 季度 4Q KVA12123 单一疗法初始安全性数据单一疗法初始疗效数据其他单一疗法安全性和疗效数据初始联合疗法数据 FDA 第 1 阶段结束会议启动 2 期临床研究 αCD27 maB IND 备案

项目神经肌肉疾病-ALS 肿瘤学囊性纤维化合作伙伴关键交易条款2023年7月收到500万美元里程碑付款高达2.55亿美元里程碑净销售特许权使用费高达9600万美元里程碑净销售特许权使用费仅限商业里程碑净销售特许权使用费次级许可付款的收入份额约13亿美元加上净销售许可协议的特许权使用费

肖恩·艾多纳托,博士首席执行官 Vinny Hayreh,医学博士临床研究副总裁 Thierry Guillaudeux,博士首席科学官 Jacques Bouchy 投资者关系与业务发展执行副总裁经验丰富的领导团队克雷格·飞利浦总裁基思·贝克首席财务官 Pauline Kenny 法律顾问

KVA12123:在TME 1/2期临床研究中,VISTA阻断单抗以解决免疫抑制问题,该研究评估了晚期实体瘤中单独使用 KVA12123 以及与pembrolizumab联合治疗的初始单一疗法数据:清除了前 3 个队列,无剂量限制毒性,VISTA 受体占有率> 90% 临床前抗 CD27 激动剂 maB 以解决耗尽的 T 细胞预计现金流将持续到 2025 年初* 1,030 万股流通股(KA:纳斯达克)4QQ 23:初始单一疗法疗效数据 2Q24:其他单一疗法安全性和疗效数据 2Q24:初始联合疗法数据以先天免疫为重点的管道预期 KVA12123 催化剂的财务状况 Kineta 正在开发解决癌症免疫抵抗问题的下一代免疫疗法,潜在的里程碑付款约为 13 亿美元,加上净销售额的特许权使用费 *包括截至第 23 季度的 780 万美元现金、10 月 23 日收到的 300 万美元默沙东里程碑款项以及预计于 4 月 24 日完成的 2250 万美元的 PIPE 融资

为癌症患者开发下一代免疫疗法 www.kinetabio.com

附录
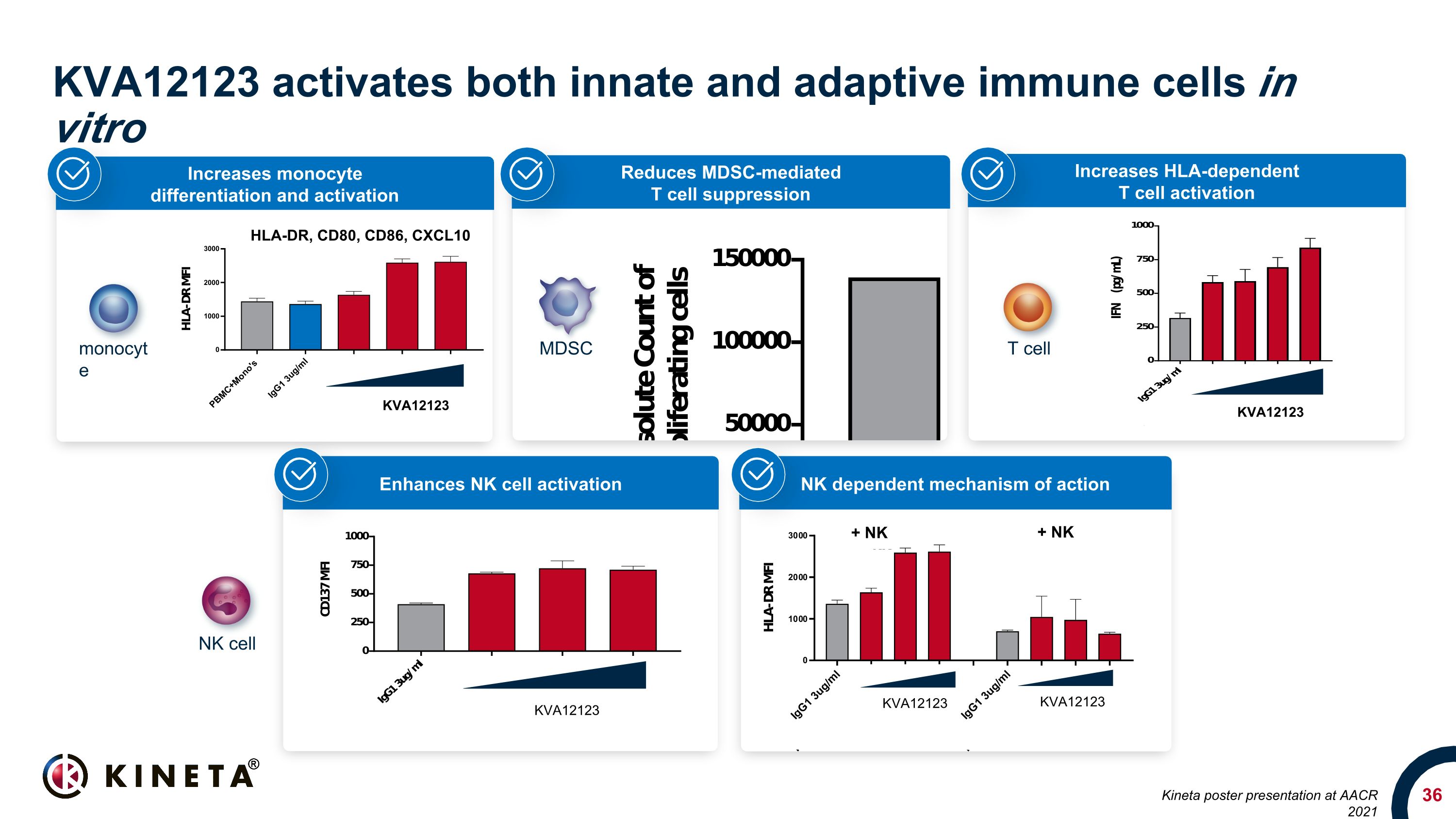
增加 HLA 依赖性 T 细胞活化降低 mdsc 介导的 T 细胞抑制 KVA12123 在体外激活先天和适应性免疫细胞 HLA-DR、CD80、CD86、CXCL10 KVA12123 增加单核细胞分化和激活 KVA12123 KVA12123 NK 依赖作用机制增强 NK 细胞激活 MDSC T 细胞 NK 细胞单核细胞 KVA12123 KVA12123 + NK + NK Kineta 在 AACR 上发布海报

KVA12123 在生理学和酸性 pH 上结合 ELISA 和 Octet 的结合研究表明,从 pH 7.4 到 pH 6.0 ELISA Octet Kineta 数据在文件 0.5 0.4 0.1 0.2 0 nm 0 50 100 150 250 300 Time 350 450 500 600 KVA12123 pH 6.0 KVA12123 pH 6.0 pH 6.0 pH 7.0 各种 pH 关联和解离 pH 7.0 pH 6.0 6.5 pH 7.4 KVA12123 绑定 KVA 浓度 (ng/mL) OD 450 KVA12123 KVA12123