

第 2b 阶段 AHFIRM 标题业绩 2023 年 11 月附录 99.2

免责声明本演示文稿以及我们在本演讲中发表的各种言论包含了DURECT Corporation(“DURECT”、“公司”、“我们” 或 “我们”)及其合作伙伴在适用证券法律和法规的含义范围内的前瞻性陈述,这些陈述受1995年《私人证券诉讼改革法》的安全港条款约束,包括与larsucosterol有可能证明死亡率降低或肝移植相关的陈述酒精相关性肝炎(“AH”)患者和为了挽救生命,DURECT计划与美国食品药品管理局和其他监管机构会面,审查AHFIRM试验的结果,larsucosterol的3期试验可能显示AH的治疗与标准护理相比有统计学上的显著改善,用于治疗AH的larsucosterol可能获得FDA或其他监管机构的批准,larsucosterol的预期产品收益和其他潜在用途,预期的产品市场和潜在销售,以及临床试验结果和计划。实际结果可能与本演示文稿中包含的前瞻性陈述中包含的结果存在重大差异,因此报告的结果不应被视为未来表现的指标。这些前瞻性陈述涉及风险和不确定性,可能导致实际结果与此类前瞻性陈述中的结果存在重大差异。潜在的风险和不确定性包括但不限于larsucosterol的未来临床试验无法证实AHFIRM试验(包括地理或其他细分)或早期临床或临床前试验的子集分析结果,或无法以具有统计学意义的方式证明larsucosterol的安全性或有效性的风险,FDA或其他政府机构可能要求对larsucosterol进行额外的临床试验的风险在批准用于治疗 AH 之前,以及与之相关的风险我们的现金资源充足、预期的资本需求和资本支出、我们对额外融资的需求或愿望、我们获得资本为运营和支出提供资金的能力以及我们继续作为持续经营企业经营的能力。有关这些风险和其他风险的更多信息包含在DURECT最新的美国证券交易委员会(“SEC”)文件中,包括分别向美国证券交易委员会提交的10-K表或10-Q表年度和季度报告,标题为 “风险因素”。除非法律要求,否则DIRECT没有义务在本陈述发布之日之后更新任何这些前瞻性陈述,以使这些陈述符合实际业绩或修订后的预期。提醒现有和潜在投资者不要过分依赖这些前瞻性陈述,这些陈述仅代表截至本文发布之日。随后的事件和发展可能会导致DURECT的期望和信念发生变化。本陈述不构成出售要约或招揽购买公司任何证券的要约。任何证券要约只能根据向美国证券交易委员会提交的注册声明(包括基本招股说明书)和招股说明书补充文件进行,其副本可在我们的网站www.durect.com的 “投资者” 选项卡下免费获得,也可以访问美国证券交易委员会网站www.sec.gov上的EDGAR免费获得。本演示文稿中提供的所有信息均基于截至2023年11月7日DURECT可用的信息,除非法律要求,否则DURECT没有义务根据未来事件或事态发展更新这些信息。

进入以 90 天死亡率为主要终点的注册性 3 期试验的充分理由 AHFIRM 试验的关键要点 90 天死亡率降低 90 mg 剂量减少 41% 剂量 90 mg 剂量减少 35% 的数字改善未达到统计学意义美国人群 90 天死亡率明显降低 57% 剂量减少 30 mg 剂量降低 58% 90 mg 剂量两剂量劳索固醇耐受性良好
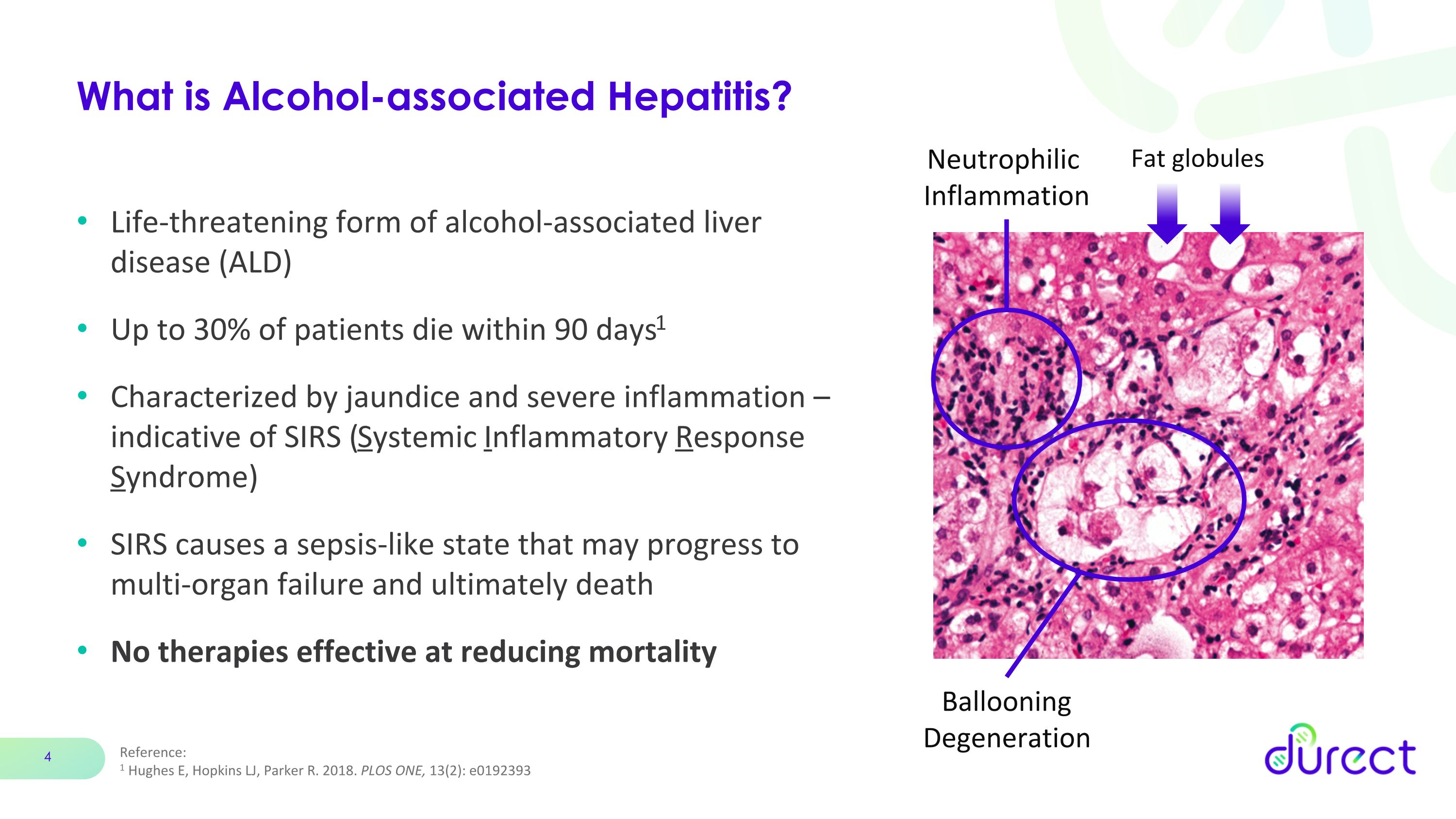
参考:1 Hughes E、Hopkins LJ、Parker R. 2018。PLOS ONE,13 (2):e0192393 什么是酒精相关性肝炎?危及生命的酒精相关性肝病 (ALD) 多达 30% 的患者在 90 天内死亡1 以黄疸和严重炎症为特征——提示着 SIRS(全身性炎症反应综合征)SIRS 会导致败血症样状态,可能发展为多器官衰竭并最终死亡。没有有效降低死亡率的疗法脂球气球变性中性粒细胞炎症
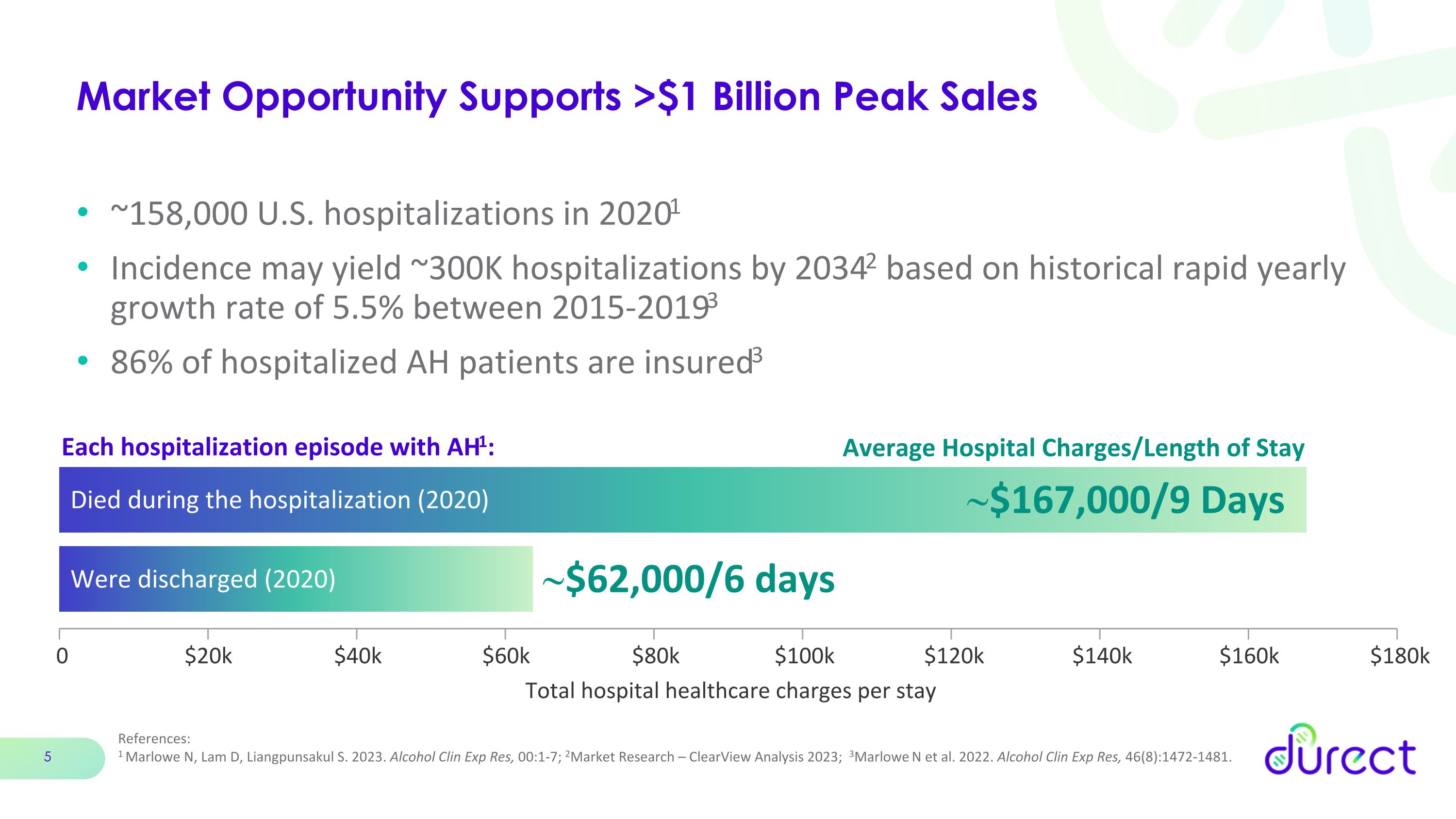
市场机会支持超过10亿美元的峰值销售额,2020年美国住院人数约为15.8万人1 根据2015-2019年间5.5%的历史快速年增长率,到20342年,发病率可能导致约30万人住院。86%的住院AH患者获得了保险3 AH1的每次住院发作:在住院期间死亡(2020年)每次住院的总住院费用约为16.7万美元/9天约为62,000美元 4 万美元 6 万美元 8 万美元 10 万美元 12 万美元 14 万美元 16 万美元 18 万美元参考文献:1 Marlowe N、Lam D、Lam D、Liangpunsakul S. 2023。Alcohol Clin Exp Res,00:1-7;2市场研究 — ClearView Analysis 2023;3Marlowe N 等人,2022 年。Alcohol Clin Exp Res,46 (8): 1472-1481。平均住院费用/出院时长(2020)

2b 期 AHFIRM 试验设计研究设计筛选期 30 mg larsucosterol 90 mg larsucosterol 标准护理标准 (SOC) 2 MDF1 分数 ≥ 32,MELD1 分数为 21-30 的重度 AH 患者 307 名受试者按照 1:1:1 的比例随机分为三组。在美国、欧盟、澳大利亚和英国进行的全球试验剂量 1 试验概述随访期第 90 天死亡率或肝移植 1 Maddrey's Discentistent 功能(MDF);终末期肝病模型(MELD)2所有患者均接受支持性护理,标准护理(SOC)患者可能包括甲基泼尼松龙胶囊由调查人员自行决定。为了维持失明,如果研究者开出类固醇处方,则两个组的患者将获得相应的安慰剂胶囊。72 小时剂量 2(如果仍在住院)
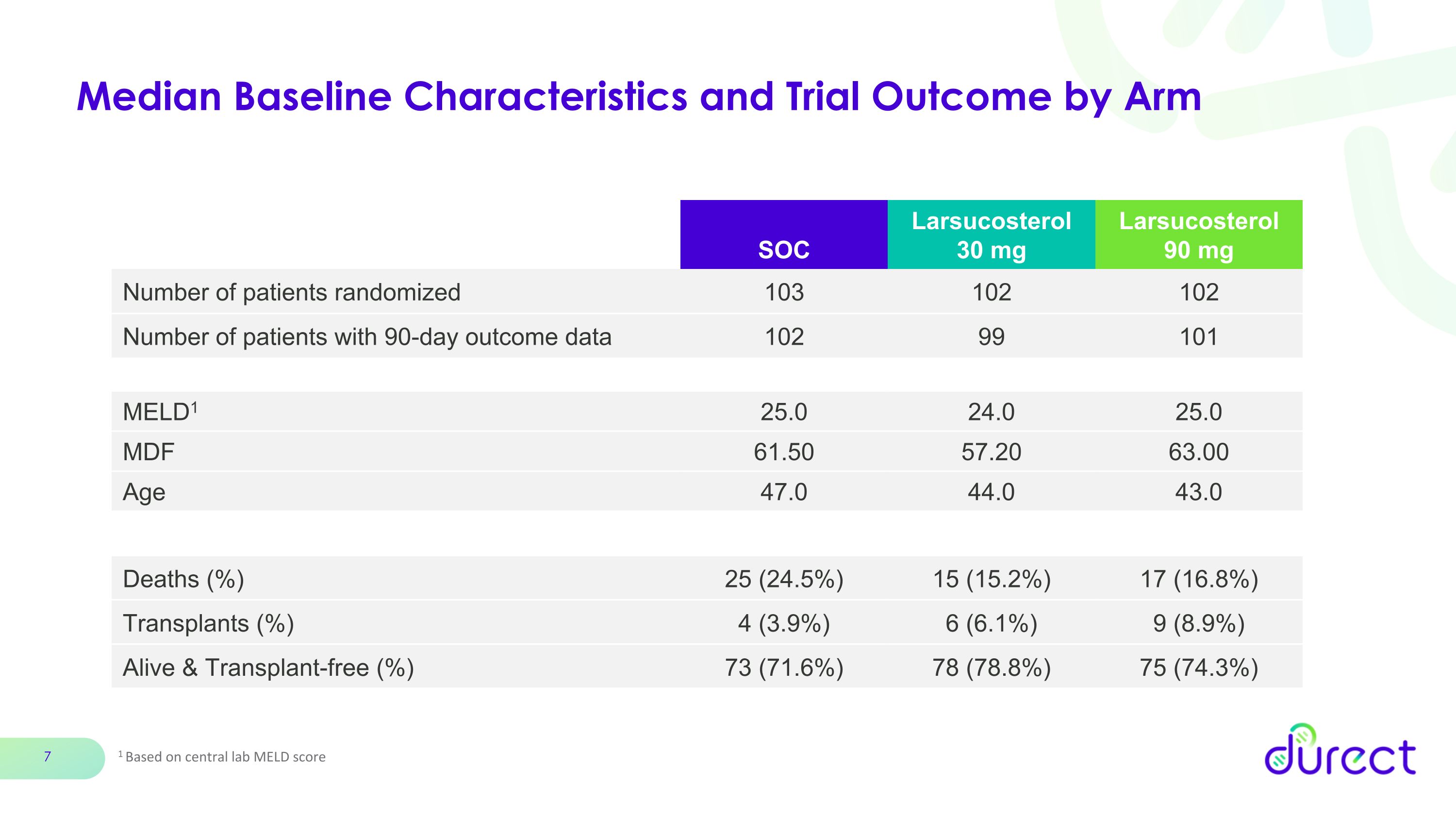
基线特征和试验结果中位数 1 基于中央实验室 MELD 评分 SOC Larsucosterol 30 mg larsucosterol 90 mg 患者人数 103 102 有 90 天预后数据的患者人数 102 99 101 MELD1 25.0 25.0 25.0 57.20 63.0 年龄 47.0 44.0 死亡 (%) 25 (24.2%) 17 (16.8%)) 移植 (%) 4 (3.9%) 6 (6.1%) 9 (8.9%) 活着且无需移植 (%) 73 (71.6%) 78 (78.8%) 75 (74.3%)
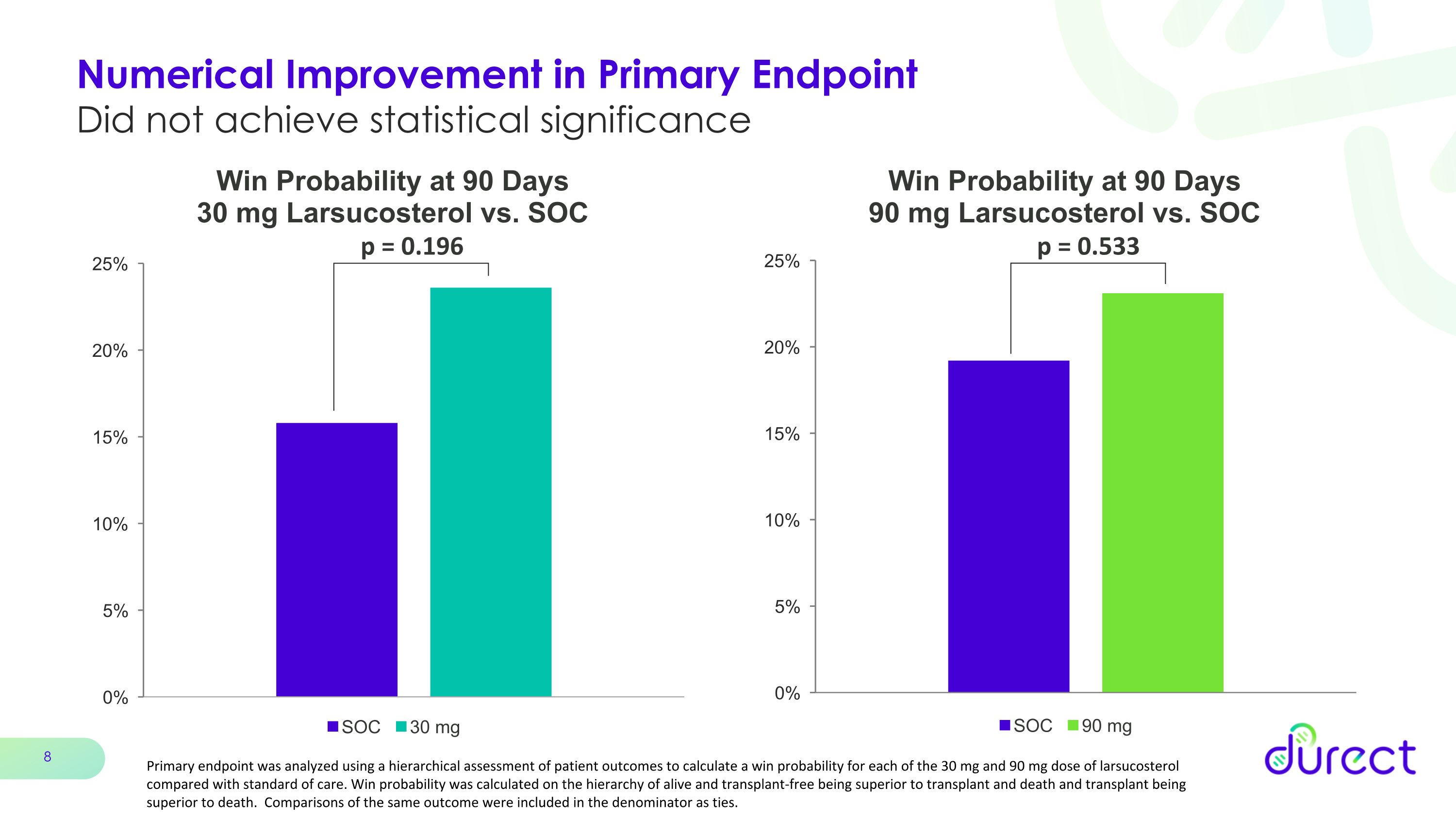
主要终点的数值改善未达到统计学意义 p = 0.533 p = 0.196 使用对患者预后的分层评估来分析主要终点,计算出 30 mg 和 90 mg 剂量larsucosterol中每种剂量与标准治疗相比的获胜概率。获胜概率是根据存活和免移植优于移植和死亡以及移植优于死亡的等级计算得出的。将相同结果的比较作为平局包含在分母中。
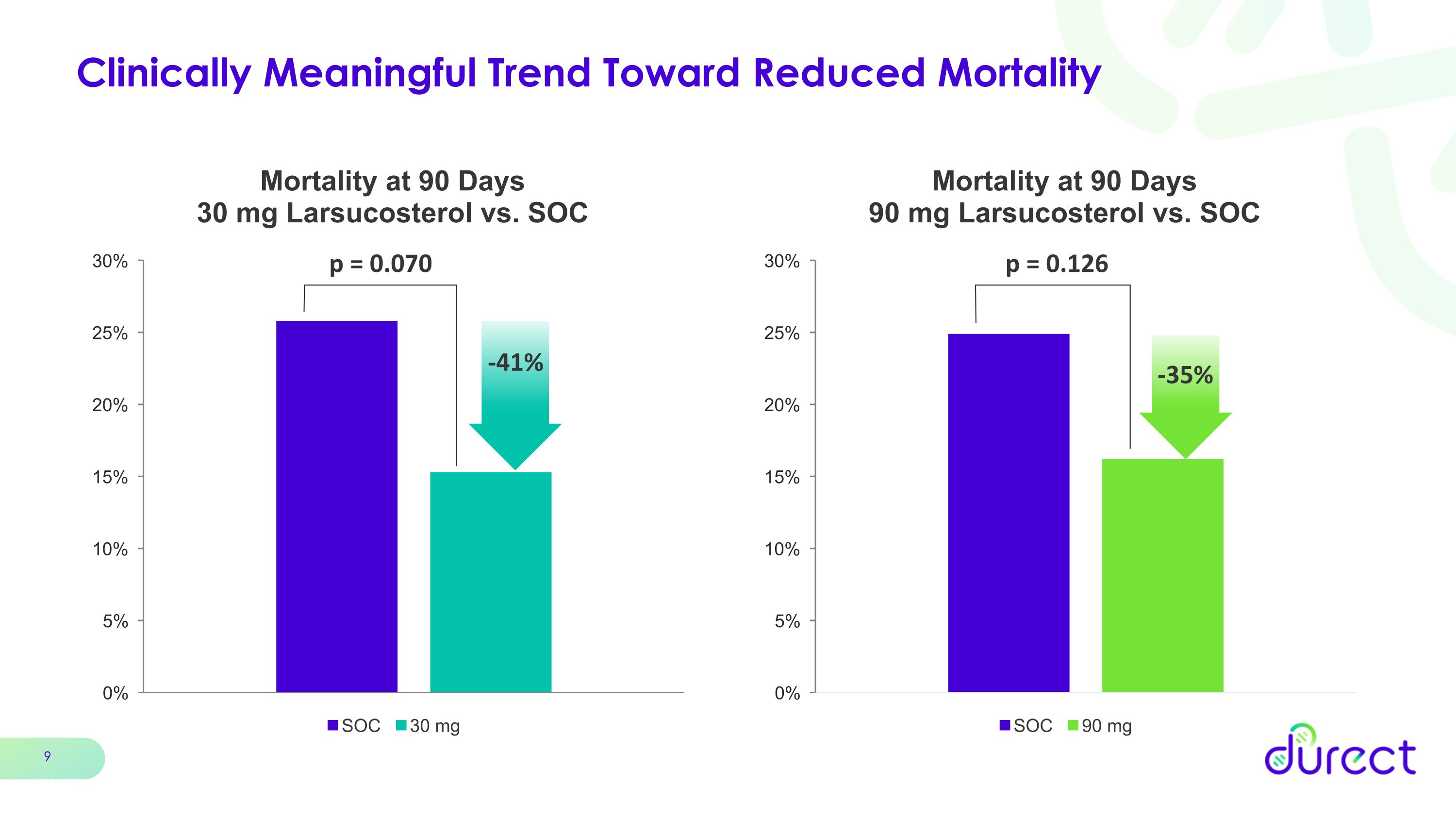
具有临床意义的降低死亡率的趋势 p = 0.126 p = 0.070 -41% -35%
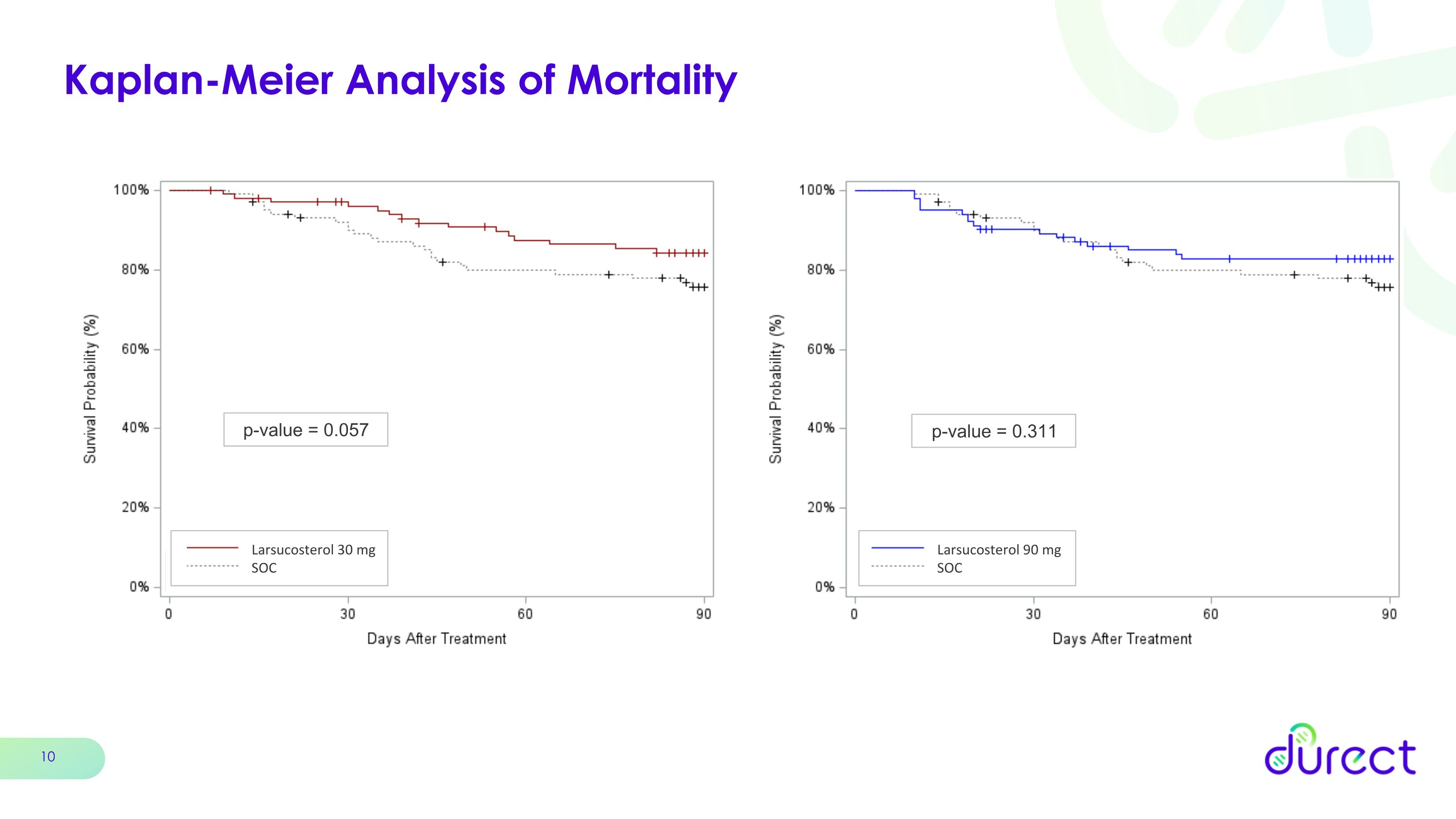
Kaplan-Meier 死亡率分析 p 值 = 0.057 Larsucosterol 30 mg SOC p 值 = 0.311 Larsucosterol 90 mg SOC
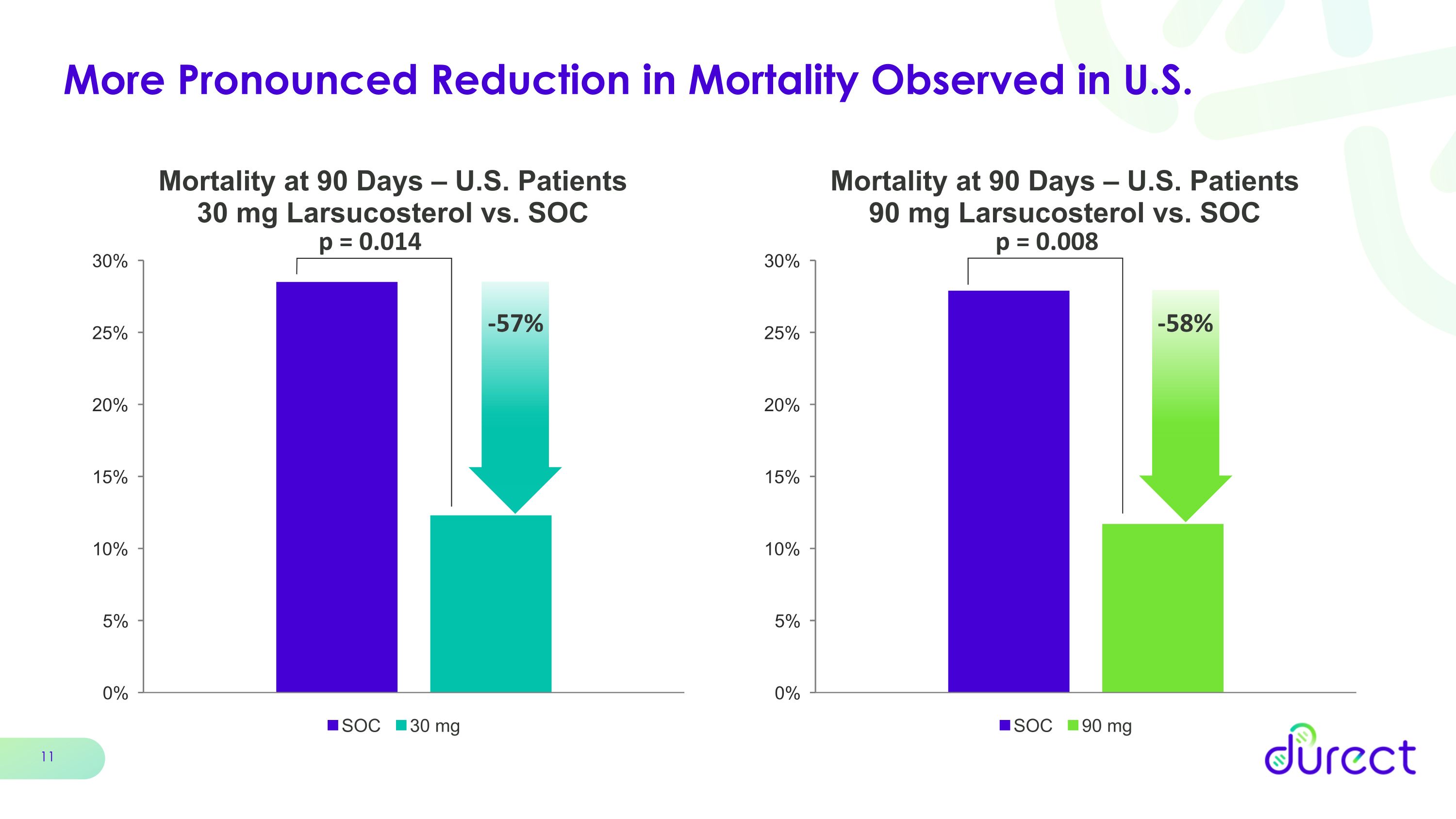
在美国观察到的死亡率下降幅度更大 p = 0.008 p = 0.014 -57% -58%
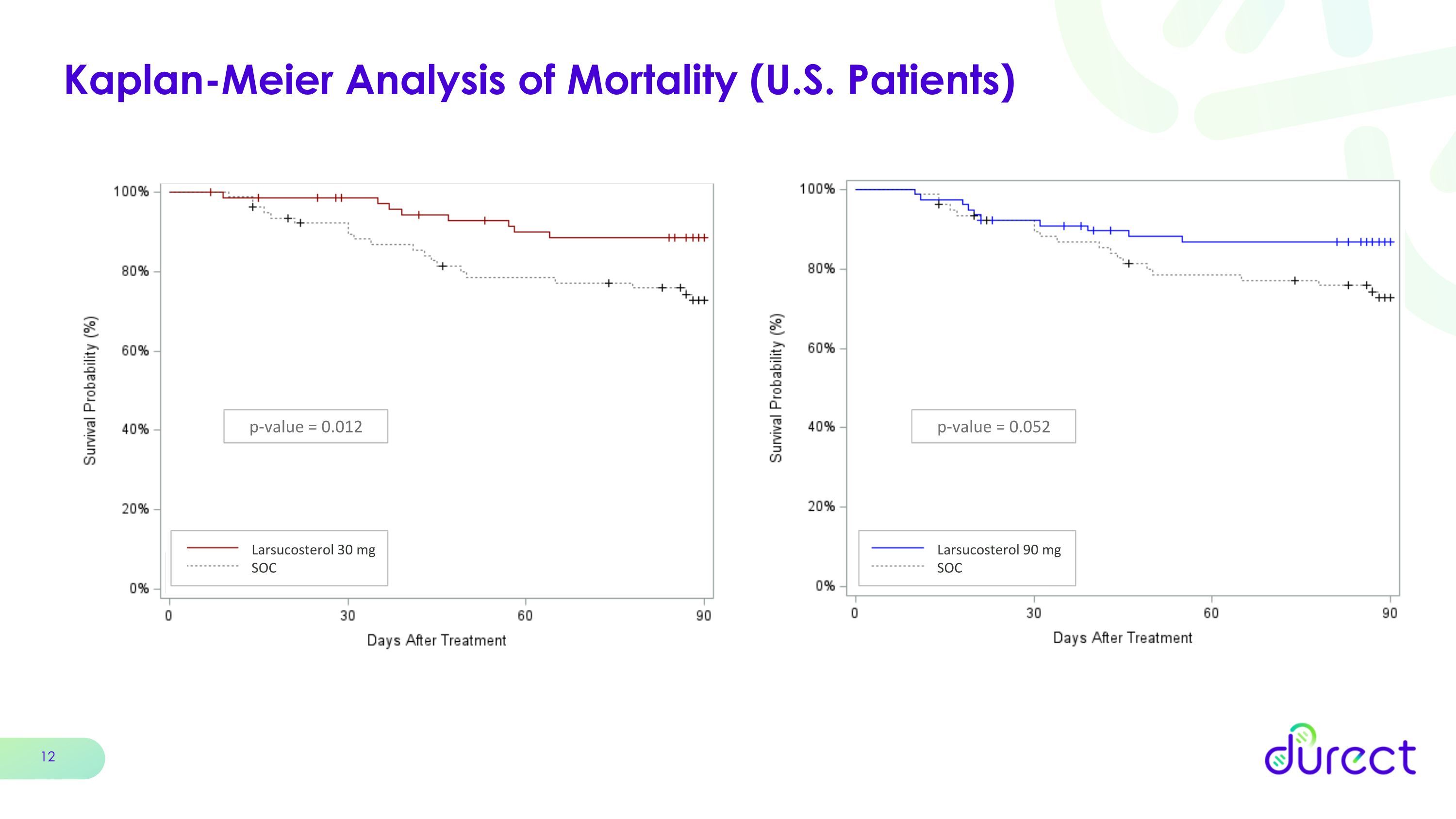
Kaplan-Meier 死亡率分析(美国患者)p 值 = 0.012 Larsucosterol 30 mg SOC p 值 = 0.052 Larsucosterol 90 mg SOC
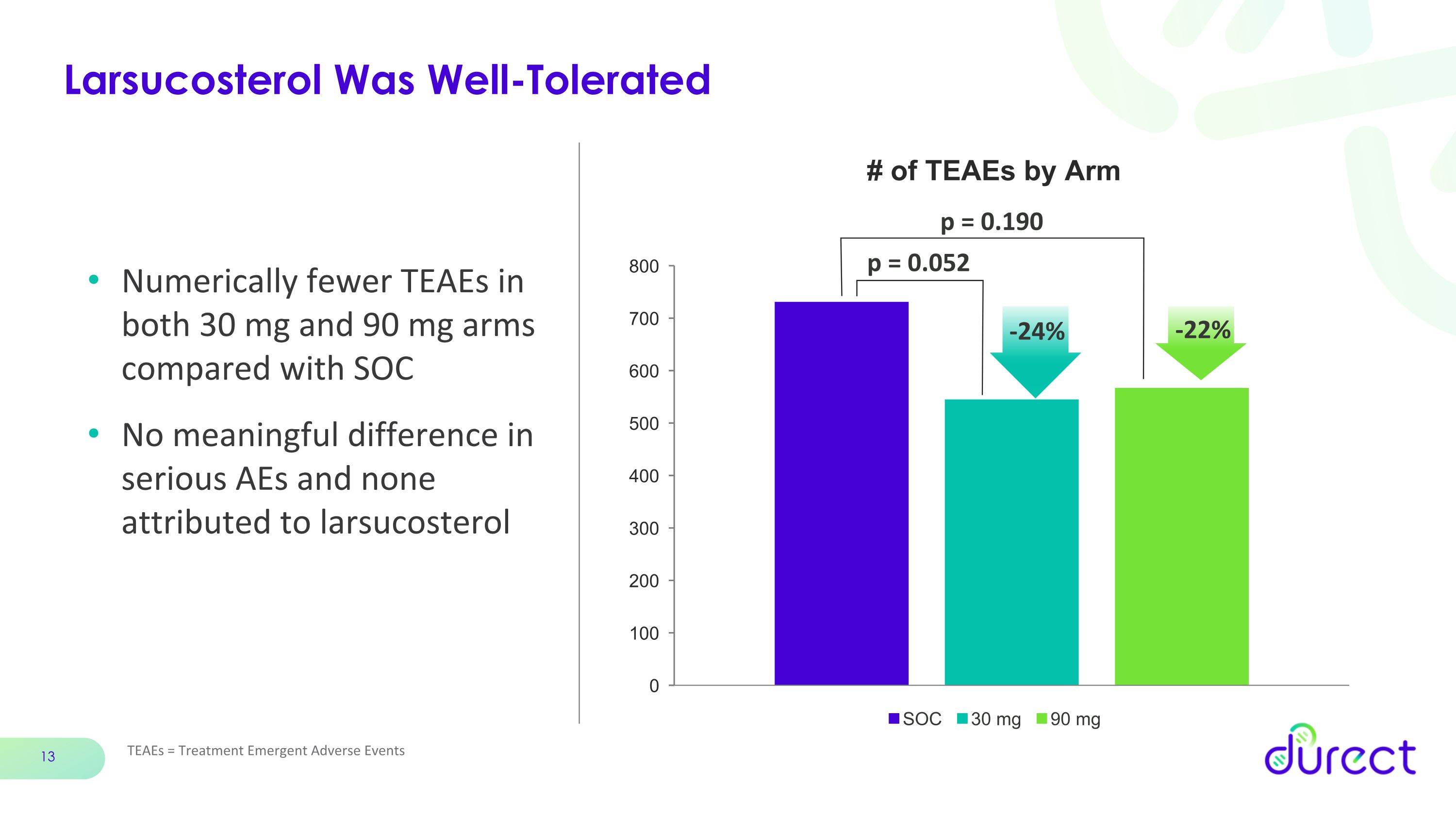
Larsucosterol 耐受性良好 TeaEs = 治疗紧急不良事件与 SOC 相比,30 mg 和 90 mg 组中 TEAE 的数值较少,严重的不良反应没有明显差异 p = 0.052 p = 0.190 -22% -24%

结论 AH中Larsucosterol的后续措施令人信服的疗效信号表明,在降低90天死亡率这一关键次要终点中使用larsucosterol;与SOC相比,30mg剂量为41%,90mg剂量为35%。在美国患者,larsucosterol治疗可将30mg剂量的死亡率降低57%(p=0.014),90 mg剂量的死亡率降低58%(p=0.008)与 SOC 相比,Larsucosterol 的耐受性良好;两个剂量组的不良事件都少于标准治疗下一步:在 2024 年第一季度与 FDA 讨论 AHFIRM 数据有充分的理由将larsucosterol推进到以90天死亡率为主要终点的注册性3期试验 AHFIRM数据将在即将举行的科学会议上公布

问与答