
已根据规则424(B)(8)提交
注册号码333-270511
Nemaura Medical,Inc.

4,796,206股普通股
__________________
本招股说明书涵盖本招股说明书中确定的两名出售 股东(与持有人的任何受让人、质权人、受让人或继承人,即 “出售股东”)合计出售4,796,206股本公司普通股(“普通股”),每股面值0.001美元。根据日期为2023年1月27日的证券购买协议(“购买 协议”),出售股票的股东在根据修订后的1933年证券法(“证券法”)第4(A)(2)条豁免注册的私募交易中购买的认股权证(“认股权证”)可于行使后发行。每份认股权证将使持有者有权以每股2.00美元的行使价购买我们的普通股。我们正在根据购买协议的要求登记 本招股说明书所涵盖普通股股份的转售。
本公司将不会从出售股份的股东 出售股份中获得任何收益,但如果认股权证是以现金形式行使的,我们将从行使认股权证中获得任何收益。我们打算将这些收益(如果有的话)用于一般企业用途。我们正在支付注册本招股说明书涵盖的 股票的费用以及各种相关费用,包括与遵守国家证券或“蓝天”法律有关的费用。出售股份的股东负责所有出售佣金、转让税及其他与要约及出售股份有关的费用。
出售股票的股东可以按固定价格、出售时的市价、与当时的市价相关的价格或协商的价格 出售股份。出售股票的股东可以向或通过承销商、经纪自营商或代理人出售股票,承销商、经纪交易商或代理人可以 以折扣、优惠或佣金的形式从出售股票的股东或股票购买者那里获得补偿,或者同时以折扣、优惠或佣金的形式获得补偿。如果需要,将出售的股票数量、股票的公开发行价、任何承销商、经纪交易商或代理人的名称以及任何适用的佣金或折扣将包括在本招股说明书的附录中,称为招股说明书附录。由于本招股说明书提供的所有股票均由出售股东提供,因此我们目前无法确定根据本招股说明书可能出售的股票的价格。
我们的普通股目前在纳斯达克 资本市场上报价,代码为“NMRD”。2023年8月1日,我们普通股在纳斯达克资本市场的最后一次公布售价为每股0.9美元。敬请索取我们普通股的最新市场报价。
我们的主要执行办公室位于纽约西57街57号,NY 10019。
投资我们的证券涉及风险。 在投资我们的证券之前,您应该仔细考虑从本招股说明书第21页开始的所有风险因素。
美国证券交易委员会和任何州证券委员会都没有批准或不批准这些证券,也没有确定本招股说明书是否真实或完整。 任何相反的陈述都是刑事犯罪。
本招股说明书的日期为2023年8月7日。
目录
| 第7页: | |||
| 关于前瞻性陈述的警告性声明 | 第二部分: | ||
| 市场和行业数据及预测 | 第二部分: | ||
| 商标和著作权 | 第二部分: | ||
| 招股说明书摘要 | 1 | ||
| 风险因素 | 21 | ||
| 收益的使用 | 38 | ||
| 股利政策 | 38 | ||
| 大写 | 38 | ||
| 普通股市场及相关股东事宜 | 39 | ||
| 配送计划 | 41 | ||
| 出售股东 | 43 | ||
| 管理层对财务状况和经营成果的讨论与分析 | 44 | ||
| 业务描述 | 47 | ||
| 管理 | 63 | ||
| 高管薪酬 | 66 | ||
| 某些实益所有人和管理层的担保所有权 | 68 | ||
| 某些关系和关联方交易 | 69 | ||
| 普通股说明 | 69 | ||
| 有资格在未来出售的股份 | 71 | ||
| 法律事务 | 71 | ||
| 专家 | 71 | ||
| 披露证监会对证券法责任弥偿的立场 | 72 | ||
| 在那里您可以找到更多信息 | 72 | ||
| 财务报表索引 | F-1 |
除本招股说明书中所包含的与本招股说明书提出的要约有关的信息或陈述外,任何交易商、销售人员或其他个人均未获授权 提供与本招股说明书提出的要约有关的任何信息或陈述,如果提供或作出该等信息或陈述,则不得将其视为我们或销售股东已授权 。本招股说明书不构成在任何司法管辖区内出售或邀请购买任何证券的要约 ,在任何司法管辖区内,如果此类要约或要约未获授权,或提出要约或要约的人没有资格这样做,或向任何人提出要约或要约是违法的,则本招股说明书不构成要约或要约购买。在任何情况下,本招股说明书的交付或根据本招股说明书进行的任何销售都不能暗示我们的事务没有变化,或在本招股说明书日期之后的任何时间,本招股说明书中包含的信息都是正确的。
对于美国以外的投资者:我们没有,销售股东也没有做任何事情,允许在除美国以外的任何司法管辖区发行或拥有或分发本招股说明书 。获得本招股说明书的美国境外人士必须告知自己,并遵守与发行本招股说明书股票和将本招股说明书分发到美国境外有关的任何限制。
| i |
有关前瞻性陈述的警告性声明
本招股说明书和通过引用纳入本招股说明书的文件中的陈述包含符合修订后的1933年证券法第27A节或证券法和修订后的1934年证券交易法第21E节 或交易法含义的前瞻性陈述。除有关历史事实的陈述外,本文中包含的任何陈述,包括有关我们产品开发计划的进度和时间;我们未来的机会;我们的业务战略、未来运营、预期的财务状况、未来收入和预计成本;我们管理层的前景、计划和目标;以及关于我们管理层未来的预期、信念、目标、计划或前景的任何其他陈述,均为前瞻性陈述。这样的陈述的例子是那些包括诸如“可能”、“假设”、“预测”、“立场”、“预测”、“战略”、“将会”、“预期”、“估计”、“预期”、“相信”、“项目”、“打算”、“计划”等词语的语句。“预算”、“潜在”、 “继续”及其变体。然而,上一句中引用的例句并不是详尽的 ,本招股说明书中包含的关于非历史事实的任何陈述也可能构成前瞻性陈述。
由于这些陈述涉及风险和不确定性以及某些假设,实际结果可能与此类前瞻性陈述所表达或暗示的结果大不相同。可能导致实际结果大相径庭的因素包括但不限于本招股说明书中“风险因素”项下确定的风险。本招股说明书中的信息仅说明该文件的日期,此处通过引用并入的信息仅说明通过引用并入的文件的日期。除法律另有规定外,我们不承担更新任何前瞻性陈述的义务,无论是由于新信息、 未来事件或其他原因。前瞻性陈述包括我们对未来运营的计划和目标,包括与我们的产品和服务以及我们未来的经济表现有关的计划和目标。与上述相关的假设涉及与 对未来经济、竞争和市场状况以及未来业务决策的判断,包括我们未来可能进行的任何 收购、合并、处置、合资企业、投资和任何其他业务发展交易。成功完成我们产品和服务的开发和商业化,以及我们业务计划的任何演变或转变,或执行任何未来战略选择所需的时间和资金数量 很难或不可能准确预测,可能涉及我们无法控制的因素。尽管我们认为本文中包含的前瞻性陈述所依据的假设是合理的,但这些假设中的任何一个都可能被证明是不准确的,因此,我们不能向您保证 本文中包含的任何前瞻性陈述中预期的结果将会实现。
基于本文所述前瞻性陈述中固有的重大不确定性,包含任何此类陈述不应被我们或任何其他人视为我们的目标或计划将会实现的陈述。因此,您不应过度依赖这些前瞻性陈述。
市场和行业数据 和预测
本招股说明书中包含的某些 市场和行业数据源自我们认为可靠的第三方市场研究公司或第三方金融或分析公司提供的信息。市场预估是通过使用独立的行业出版物、政府出版物和第三方预测以及我们对市场的假设来计算的。我们尚未独立核实 此类第三方信息。本招股说明书中使用的市场数据涉及许多假设和限制,敬请您不要过度重视此类估计。虽然我们不知道本招股说明书中关于任何市场、行业或类似数据的任何错误陈述 ,但此类数据包含风险和不确定因素,可能会根据各种因素发生变化,包括本招股说明书中“关于前瞻性陈述的警示声明”和“风险因素”标题下讨论的那些因素。 这些因素和其他因素可能会导致结果与独立各方和我们在估计中表达的结果大不相同。
某些 数据还基于我们的善意估计,这些估计源自管理层对行业和独立来源的了解。 行业出版物、调查和预测一般声明,其中包含的信息是从认为 可靠的来源获得的,但不能保证其中包含的信息的准确性或完整性。我们没有独立核实来自第三方来源的任何数据,也没有确定其中所依赖的基本经济假设。对我们市场状况的陈述是基于我们目前可获得的市场数据。虽然我们不知道关于本文所述行业数据的任何错误陈述 ,但我们的估计涉及风险和不确定因素,并可能根据各种因素而发生变化,包括本招股说明书中“风险因素”标题下讨论的那些 。同样,我们相信我们的内部研究是可靠的,尽管此类研究尚未得到任何独立消息来源的证实。
商标和著作权
我们拥有或有权使用与我们的业务运营相关的商标或商品名称,包括我们的公司名称、徽标和网站名称。此外,我们拥有或拥有版权、商业秘密和其他专有权利,以保护我们产品的内容和此类产品的配方。本招股说明书还可能包含其他公司的商标、服务标志和商品名称,这些都是它们各自所有者的财产。我们在本招股说明书中使用或展示第三方的商标、服务标志、商品名称或产品,不是也不应被解读为暗示与我们的关系或对我们的背书或赞助。仅为方便起见,本招股说明书中提及的某些版权、商号和商标在列表中不带©、®和™符号,但我们将根据适用法律在最大程度上维护我们对我们的版权、商号和商标的权利。所有其他商标都是其各自所有者的财产。
| 第二章 |
招股说明书摘要
本摘要重点介绍了有关我们、本次产品以及本招股说明书中包含的精选信息的某些信息。此摘要不完整,不包含您在决定是否投资我们的普通股之前应考虑的所有信息。为了更全面地了解本公司和此次发行,我们建议您阅读并考虑本招股说明书中更详细的信息,包括“风险 因素”以及财务报表和相关说明。除文意另有所指外,凡提及“公司”、“本公司”、“本公司”或“本公司”,均指Nemaura Medical,Inc.、内华达州的一家公司及其子公司。
业务 概述
我们 是一家医疗技术公司,开发了SugarBEAT®,这是一种非侵入性、灵活的连续血糖监测系统,供糖尿病患者和任何希望确定影响其血糖曲线的因素的人使用。SugarBEat® 由一个带有传感器的一次性粘性皮肤贴片组成,该传感器连接到一个可充电的无线发射器。传感器 每隔5分钟测量一次血糖读数,并通过低能量蓝牙将数据发送到智能设备,如手机 (包括Android和iOS)。智能设备上的一个应用程序使用专有算法来显示真实的血糖值,在数据经过 校准后,至少使用一个手指棒校准。SugarBEat®的工作原理是将皮肤中的葡萄糖提取到与电极传感器直接接触的贴片中的一个腔中。数据记录在应用程序上,可以实时查看,还可以存储所有历史数据以供以后根据需要进行评估。我们相信,任何1型或2型糖尿病患者都可以使用SugarBEAT® ,任何希望确定影响其血糖曲线的因素的人也可以使用该产品。 因此,就胰岛素抵抗而言,他们的代谢健康状况。
2019年5月29日,我们宣布已获得行政长官批准,允许SugarBEat®在欧盟合法销售。CE认证 通过使用CE标志来披露,这是制造商对产品符合适用的欧洲法律要求的声明。欧洲的SugarBEat®临床试验计划评估了75名1型和2型糖尿病患者的525个病人日 ,并于2017年12月完成。CE批准是为SugarBEAT®设备 实现强制性符合性标志以允许其在欧盟合法销售的过程。这是制造商的声明,产品符合适用的欧洲法律的要求。这一批准需要对基础的国际标准化组织13485认证的质量管理体系进行年度审查。 认证于2021年11月成功续签。
我们 还向美国食品和药物管理局(FDA)提交了PMA(上市前批准)申请,其标签 与CE批准的标签相同,CE批准是一种用于糖尿病患者的血糖趋势辅助设备。PMA目前正在接受审查。
在2020年7月,我们向美国食品和药物管理局提交了一份PMA申请,要求使用SugarBEAT®作为血糖趋势指纹检测的辅助工具。 我们和其他申请者随后被美国食品和药物管理局告知,由于美国食品和药物管理局的器械和放射健康中心(CDRH)积极参与应对新冠肺炎疫情,审批过程可能会受到延误,这导致 工作人员被重新分配到其他与新冠肺炎相关的批准请求。2021年4月,FDA确认将重新审查PMA申请,2021年12月,FDA的生物监测研究部门对为支持PMA申请而提交的临床计划进行了审计。仅提出了483条意见,该公司于2022年1月提交了完整的答复。FDA随后计划在2022年第二个日历季度进行上市前检查,旨在涵盖FDA的 质量体系/当前的医疗器械良好制造规范(21 CFR Part 820)。
除此之外,Nemaura还建立了ProBEATTM,基于SugarBEAT®平台,根据FDA健康指南说明使用时,可被归类为 健康指南,以提供提示并教育用户影响其血糖曲线的因素。
我们 相信SugarBEAT®和基本的BEAT技术平台还有其他应用,其中可能包括:
| · | 医生和糖尿病专业人员可访问的网络服务器,以远程跟踪病情,从而降低医疗成本并更有效地管理病情; |
| · | 一个完整的虚拟医生,监测一个人的生命体征,并通过网络传输结果; |
| · | 其他使用BEAT技术平台来测量替代分析物的贴片,包括乳酸。这将是监测条件的一个步骤,特别是在医院环境中。目前,乳酸监测是用来确定职业运动员的相对健康状况的,我们已经完成了初步研究,证明BEAT技术应用于连续乳酸监测;以及 |
| · | 一种可广泛应用的连续温度监测系统。 | ||
| 1 |
在此产品开发期间,公司 经历了经常性亏损和运营现金流为负。在截至2023年3月31日和2022年3月31日的财年中,我们的产品销售收入分别为77,044美元和503,906美元,净亏损分别为14,143,735美元和13,886,805美元,来自运营活动的负现金流分别为8,451,781美元和6,504,041美元。如我们的财务报表所示,截至2023年3月31日,我们的现金余额为10,105,135美元,营运资本赤字为8,730,734美元,累计赤字为51,875,211美元,股东权益总额为11,814,198美元。由于我们历史上的经常性亏损、运营现金流为负以及巨额累积赤字,我们作为一家持续经营的企业继续经营的能力受到了极大的怀疑。见“风险因素-我们 有运营亏损的历史,我们的管理层得出结论,这些因素对我们作为持续经营的企业 继续经营的能力提出了实质性的怀疑。此外,我们的独立注册会计师事务所在其截至2023年3月31日的财政年度的审计报告中加入了一段说明,说明我们是否有能力继续作为一家持续经营的企业。“
虽然公司预计近期运营将继续出现亏损,但由于产品开发、监管活动、临床试验以及其他商业和产品开发相关费用的产生,这些亏损可能会很大,但在截至2021年12月31日的三个月期间,公司达到了一个重要的里程碑,公司开始向其英国被许可人交付其SugarBEAT®设备,使他们能够继续研究基于用户的反馈和证据,这些反馈和证据可能支持在英国的报销。
我们的 业务战略
我们 打算引领创新和有针对性的诊断医疗设备以及数据驱动的数字平台的发现、开发和商业化,以改善消费者福祉空间和医疗部门的疾病监测、管理和整体患者护理 。具体地说,我们打算利用我们的 技术平台,专注于监测可以无创地通过皮肤抽出的分子。除了葡萄糖,这些分子还可能包括乳酸监测和处方药监测,以及有助于诊断、预防或管理糖尿病等疾病的血液生物标志物。我们计划采取以下 步骤来实施我们广泛的业务战略。我们审批后的关键商业战略将首先在欧洲实施,然后 在中东和亚洲的部分地区,然后是美国,如下所示:
| - | 在英国和爱尔兰共和国将SugarBEAT®商业化。我们打算通过MySugarWatch®(以前称为达拉斯Burston ethitronix Limited)(“MSW”)在英国和爱尔兰共和国将糖商业化,我们与MySugarWatch Limited(“MSW”)签订了这两个国家的独家营销权协议。我们还于2018年5月与MySugarWatch(Europe)Limited(前身为Dallas Burston ethitronix(Europe)Limited)就所有其他欧洲地区签署了全面商业协议,作为平等合资协议的一部分。合资企业打算向糖尿病监测领域的一家或多家领先公司寻求转授许可权和机会,以利用它们的网络、基础设施和资源。 |
| - | 与其他方建立许可或合资协议以销售糖类BEAT® 在其他地区我们正在与世界各地的其他几个方面就销售SugarBEAT®设备的许可或合资协议进行详细的讨论和谈判,并已与TP MENA签署了海湾合作委员会的商业协议。TP MENA已向沙特阿拉伯监管机构提交了在KSA(沙特阿拉伯王国)注册SugarBEAT的申请。 |
| - | 寻求FDA PMA批准SugarBEat®.PMA的申请目前正在接受FDA的审查。 |
| - | 扩大这些疾病的适应症SugarBEat®:可以使用设备。我们认为,与在非急性环境中发现的用于监测其他疾病的设备相比,糖类BEAT®设备可能提供显著的好处。这包括用于竞技表演的乳酸监测,以及药物监测。我们已经完成了乳酸监测的初步概念验证,现在计划探索将健康应用于运动表现训练的商业化路线,并计划开展进一步的临床计划,以支持乳酸监测设备的临床使用。 |
| - | 通过我们的专有平台技术、收购和战略许可安排扩大我们的产品线。我们打算利用我们的专有平台技术来扩大我们用于诊断糖尿病和其他疾病的候选产品组合。这包括由我们的传感器在医疗和福利市场收集的数据驱动的数字平台,例如用于新陈代谢健康监测。此外,我们打算授权我们的产品,并获得与我们的研发以及业务重点和战略一致的产品和技术。这可能包括由传感器数据支持的用于管理慢性病的数字解决方案、用于改进糖尿病管理的药物输送产品,例如改进的胰岛素注射器系统,和/或用于糖尿病相关药物的组合药物产品。 |
| 2 |
产品 开发
管理层在诊断医疗设备的监管和临床开发方面拥有丰富的经验。我们打算利用诊断医疗器械领域的这一经验,尝试增加产品在多个地区获得批准的可能性。目前,糖尿病诊断医疗器械的整体监管流程与管理其他诊断设备的监管流程类似。 时间线比新药或完全侵入性诊断设备在临床试验时要短。我们已经成功地测试和评估了该设备的临床输出,在这种情况下,它可以根据通知的机构BSI批准CE批准的血糖水平的准确性和安全性。PMA(上市前批准)申请也已提交给FDA,目前正在审查中。我们将继续寻求与未来授权厂商和营销合作伙伴的合作,以实现我们的 商业增长里程碑。
产品开发和商业化 时间表
| 里程碑 | 目标开始日期 | 现状 |
| 完成1型和2型糖尿病受试者的临床研究,以确定最终的设备声明,并提交CE标志批准最终设备声明。 | 2017年7月 | 已完成 |
| 人体穿戴式发射器CE标志 | 2018年8月 | 已完成 |
| 美国FDA PMA提交 | 2020年6月 | 提交完成,FDA进行BIMO和GMP审核 |
| 在英国推出商业产品,随后在欧洲主要地区推出 | 2020年7月至9月 | 交错发射正在进行中 |
| ProBEAT的初步研究 | 2020年10月至12月 | 初步研究已完成。计划进行进一步的研究。 |
|
扩大商用传感器/贴片制造的规模。 扩大规模意味着我们已经开始着眼于在英国推出产品所需的更大规模 ,这与传感器的制造工艺有关。 |
2020年12月 | 正在进行中 |
| 扩大设备(发射机)制造规模 | 2020年12月 | 正在进行中 |
| 开始向英国被许可方交付产品 | 2021年12月 | 正在进行中 |
公司产品的市场机会
根据国际糖尿病联合会图集10TH:根据2021年版(“IDF”),约有5.37亿成年人患有糖尿病,占世界这一年龄段人口的10.5%。预计到2030年,这一数字将增至6.43亿(11.3%),到2045年将增至7.83亿(12.2%)。此外,据估计,全球有2.4亿人患有未确诊的糖尿病,这意味着几乎每两个患有糖尿病的成年人中就有一个不知道自己患有这种疾病。IDF确认,几乎90%的未确诊糖尿病患者生活在低收入和中等收入国家。
IDF公布的统计数据 证明,糖尿病是一个巨大的、日益严重的问题,尽管社会成本已经很高,但它们仍在继续上升。此外,以色列国防军还指出,欧洲的儿童和青少年1型糖尿病患病率最高,每年的发病率也是最高的。据报道,欧洲的糖尿病患者人均成本位居第二(3086美元),仅次于北美和加勒比海地区(8208美元)。
全球糖尿病统计数据
| 2021 | 2030 | 2045 | |
| 世界总人口 | 79亿 | 86亿 | 95亿 |
| 成年人口(20-79岁) | 51亿 | 57亿 | 64亿 |
| 糖尿病(20-79岁) | |||
| 流行率(%) | 10.5% | 11.3% | 12.2% |
| 糖尿病患者人数 | 5.366亿 | 6.427亿 | 7.832亿 |
| 糖尿病引起的医疗总支出(2021美元) | 9660亿美元 | 10,280亿美元 | 10.54亿美元 |
| 糖耐量受损“IGT”(20-79岁) | |||
| 流行率(%) | 10.6% | 11.0% | 11.4% |
| 糖耐量低减患者人数 | 5.41亿 | 6.227亿 | 7.303亿 |
| 1型糖尿病(0-19岁) | |||
| 患有1型糖尿病的儿童/青少年人数 | 120万 | - | - |
| 每年新诊断病例的数量 | 184,100 | - | - |
| 3 |
1型糖尿病,曾经被称为青少年糖尿病或胰岛素依赖型糖尿病,是一种慢性疾病,胰腺产生很少或没有胰岛素,胰岛素是一种允许糖(葡萄糖)进入细胞产生能量所需的激素。更常见的2型糖尿病发生在身体对胰岛素产生抵抗力或不能产生足够的胰岛素时。
多种因素可能导致1型糖尿病,包括遗传和接触某些病毒。虽然1型糖尿病通常出现在儿童或青春期,但它也可以在成年人中发展。
尽管积极的研究,1型糖尿病是无法治愈的,尽管它是可以控制的。通过适当的治疗,1型糖尿病患者有望比过去活得更长、更健康。1型糖尿病包括自身免疫性1型糖尿病(1a型),其特征是自身抗体阳性,以及特发性1型糖尿病(1b型),其自身抗体阴性,C肽含量 低。1型糖尿病(胰岛素依赖型)患者需要长期使用外源性胰岛素治疗,这些患者对血糖(SMBG)进行自我监测,以计算合适的胰岛素剂量。SMBG是通过使用手指棒采集的血液样本进行的,但频繁的SMBG并不能检测到血糖的所有显著偏差,尤其是在血糖水平迅速波动的患者中。
2型糖尿病,曾经被称为成人起病或非胰岛素依赖型糖尿病,是一种慢性疾病,会影响你身体代谢糖(葡萄糖)的方式,糖是你身体的主要燃料来源。对于2型糖尿病,你的身体要么抵抗胰岛素的影响,要么不能产生足够的胰岛素来维持正常的血糖水平。胰岛素是一种调节糖分进入细胞的激素。如果不治疗,2型糖尿病可能会危及生命。
2型糖尿病在成人中更为常见,随着儿童肥胖症的增加,2型糖尿病对儿童的影响越来越大。虽然目前还没有公认的治疗2型糖尿病的方法,但越来越多的证据表明,通过良好的饮食、锻炼和保持健康的体重可以有效地控制2型糖尿病。如果饮食和锻炼不能控制血糖,可能需要糖尿病药物或胰岛素治疗。
在欧盟和美国,每年都有数以百万计的患者接受糖尿病检测。进行检测的主要原因是检测和评估有糖尿病症状的患者的糖尿病。这些研究在对疑似但未经证实的糖尿病患者以及已确诊糖尿病并需要预后或风险信息的患者的初步评估中提供临床益处。
我们 相信,我们的市场机会与检测、诊断和治疗2型糖尿病的人数直接相关。IDF表明,连续血糖监测设备的总世界市场机会以数十亿美元计,并且随着糖尿病发病率的持续增长,预计每年都会增长。
我们 不相信有可能估计接受手指刺痛或其他类型的侵入性血糖监测的糖尿病患者的数量 。然而,我们不知道目前市场上有任何产品可以实现非侵入性连续血糖监测。 我们相信SugarBEAT®设备很容易被医学界采用,用于对患者进行持续评估。
我们 相信我们的非侵入性糖类®设备具有许多优点,可能是检测个体血糖水平不一致的理想设备 。我们相信CE批准的SugarBEAT®设备可能是一个强有力的解决方案,作为一种非侵入性的持续血糖监测设备,可以帮助糖尿病患者跟踪他们的血糖状况。虽然我们无法 估计我们的SugarBEAT®设备可能占据的市场份额,但我们相信SugarBEAT®设备有潜力夺取 血糖监测和跟踪市场的相当大份额。
商业化 计划
在截至2023年3月31日的财年中,我们与我们的英国被许可方MSW合作,为他们的上市战略提供支持,该战略将我们的SugarBEAT®设备的使用融入到他们自己的品牌产品中。虽然新冠肺炎确实导致了城市生活垃圾用户评估计划的一些短暂延迟,但总体反馈是积极的,尽管城市生活垃圾购买 订单的预期时间表被延长,第一批订单是2021年4月下的5,000台SugarBEAT®发射器和200,000台SugarBEAT®传感器 。在截至2023年3月的财年中,我们的重点一直是支持我们的被许可方收集用户反馈,以支持传感器报销申请,我们将继续支持这些努力。在截至2023年3月31日的财年中,我们还采取了以下行动:
| · | 增加生产操作员人数,以促进产品制造 |
| · | 开始从以前为原材料下的远期订单中接收零部件/材料,以支持扩大规模并确保目前全球供应短缺的项目的库存,即微处理器等电子零部件。 |
| 4 |
| · | 继续与Benchmark Electronics Inc.合作,作为我们的CMO合作伙伴,通过承担电子PCBA(印刷电路板组装)批量认证运行,通过其在泰国的FDA批准的设施,促进未来发射机的批量生产 |
| · | 根据2021年12月从MSW收到的采购订单完成发射器的分阶段交付 |
我们还提前了 在美国发展市场能力的计划,包括:
| · | 2020年7月,我们向美国食品和药物管理局提交了一份PMA申请,申请将SugarBEAT®设备作为手指棒测量的辅助工具,用于血糖谱分析。我们和其他申请者随后被食品和药物管理局通知,由于疾控中心积极参与应对新冠肺炎引发的大流行,导致工作人员被重新分配到其他与新冠肺炎相关的批准请求,因此审批过程受到延误。2021年4月,FDA确认将重新审查PMA申请。 |
| · | 2021年12月,FDA的生物监测研究部门对为支持PMA申请而提交的临床计划进行了审计。只提出了一项483点意见,该公司于2022年1月提交了全面答复。 |
| · | FDA随后在2022年第二个日历季度进行了上市前检查,检查范围包括FDA的质量体系/当前的医疗器械良好制造规范(21 CFR Part 820)。再次提出了一项483点意见,并在规定的时间范围内对此作出了答复。该公司计划在适当时候提供进一步的材料更新。 |
此外,我们还将继续探索其他关键地理市场的商业化机会,并打算在出现问题时提供材料 更新。
竞争格局
据我们所知,目前市场上还没有其他竞争对手的设备,可以提供连续的血糖监测和分析, 非侵入性,传感器只需佩戴一天。我们相信,这使我们在一个可以瞄准糖尿病患者和糖尿病前期患者的市场上独树一帜。此外,我们认为这也可以用来改善体重管理和福祉市场的结果。有一些公司,如德克斯康和雅培,目前提供连续血糖监测(CGM)传感器,分别为连续佩戴10天和14天。如果这些公司符合以下条件,它们可以被视为未来的竞争对手:
| – | 开发和销售比我们当前和/或未来的产品更便宜或更有效的产品; |
| – | 运营更大规模的研发项目,或者拥有比我们多得多的财政资源; |
| – | 比我们更成功地发起或经受住实质性的价格竞争; |
| – | 从有限的现有人才库中更成功地招聘熟练的技术和科学工作者; |
| – | 更有效地协商第三方许可证和战略关系;以及 |
| – | 比我们更容易利用收购或其他机会。 |
我们 可能会在这一一般领域与这些公司和潜在的新来者争夺市场份额。这些潜在竞争对手可能单独或与其合作伙伴一起开发将与我们竞争的新产品,这些竞争对手可能会(在某些情况下确实会)运营更大的研发项目,或者拥有比我们更多的财务资源。
正如 指出的那样,虽然很难分析我们的主要竞争对手,因为目前还没有非侵入性的诊断医疗设备来持续监测血糖水平,但我们预计未来可能会有特定的公司与我们竞争。
监管要求
我们的设备已通过适用的电气安全测试,并已根据相关的欧洲指令、法规和标准进行了生物兼容性验证。如果引入新材料,它们将接受生物兼容性风险评估,并在必要时进行进一步测试。该设备和贴片的批次是为2014年11月至2015年12月期间进行的人体临床研究制造的。这是一个功能齐全的手表设备,通过电线连接到一个贴皮的传感器和电极上。在印度进行的后续研究 该设备于2016年2月获得CE认证。此后,该设备进行了升级,缩小了尺寸,包括增强的传感器系统,并允许通过穿戴在身上的发射器进行无线通信。这款小型化无线设备 于2019年5月获得CE认证,PMA已于2020年7月提交给美国FDA,目前正在审查中。申请CE认证需要公司拥有ISO13485质量管理体系,涵盖医疗器械的设计、开发和制造。Nemaura Medical没有此认证,而是根据与Nemaura Pharma Limited(“Pharma”)于2018年4月4日签订的服务合同条款,Nemaura Medical已将CE审批注册流程外包给Pharma。 Pharma是一家关联公司,由我们的首席执行官、董事会主席兼大股东DF.H.Chowdhury博士控制。根据服务合同的条款,Pharma已根据服务安排费用承担了注册产品以供CE批准的所有必要活动,而Nemaura Medical将保留CE标志的完整所有权和实益所有权,以及 所有相关知识产权,而除服务费外,无需支付任何进一步的费用或版税。
| 5 |
知识产权
我们 认为,与我们的技术相关的清晰和广泛的知识产权是长期成功的核心,我们打算进行相应的投资 。这适用于国内和国际专利覆盖范围、商业秘密和商标。
SugarBEAT®技术受我们的知识产权组合的保护,该组合包括已发布和正在申请的专利和商业秘密 ,涵盖一系列主张,包括以非侵入性方式测量从人体皮肤提取的葡萄糖的方法和设备、从皮肤提取葡萄糖的设备是稳定的方式、用于减少背景噪声信号的设备、将 原始数据转换为血糖值以校准设备的算法,以及 传感器中使用的酶溶液的配方和制备过程。
2014年5月8日,一家关联公司NDM技术有限公司以象征性代价将题为“分析物的累积测量”的英国专利申请1208950.4和国际专利申请PCT/GB2013/051322转让给皮肤病诊断有限公司(“DDL”) 。
未来还将申请更多与该设备和传感器相关的专利,提供新的知识产权保护。最近提交的一些专利和未来的一些专利可能会取代以前的知识产权。
此外, 我们保留与传感器制造工艺和传感器配方相关的大量商业秘密,这是我们花了几年时间开发的,事实证明,逆向工程具有挑战性,因为除了配方成分外,它还包括最终功能传感器特有的复杂组合中的 加工方法。将不会就该技术的这一方面申请专利,以避免技术诀窍的任何公开传播。
这些专利和专有技术涵盖了技术平台的各个方面。此外,BEAT®和SugarBEAT®商标已在全球多个主要地区注册。因此,对SugarBEAT®产品至关重要的所有知识产权均归我们所有,不需要支付版税。我们打算根据需要带头保护和/或起诉这些专利和专利申请 。我们打算随着开发的进展申请更多的专利,这些专利被认为对保护技术平台以及未来的修改和改进有价值。如果无法获得专利,或者现有专利被无法申请专利的新专有技术或技术开发所取代,则知识产权将仅限于专有技术和商业秘密, 这些将受到严格保护。
交易已提交、已授予和正在申请的秘密、商标和专利
| 知识产权:专利(核心权利要求)、专有技术、商标 | 到期日 | 授予/签发的司法管辖区 | 在哪些司法管辖区待决 | 正在进行的版税或里程碑付款 | ||||
| 专利:分析物的累积测量(1) | 2033年5月20日 | 澳大利亚、法国、德国、意大利、波兰、西班牙、荷兰、英国、中国、日本、美国、加拿大、阿联酋、巴西 | 卡塔尔 | 没有。内部发展 | ||||
| 皮肤准备贴片(2) | 2039年12月2日 | 英国 | 欧洲、美国 | 没有。内部发展 | ||||
| 技术诀窍:传感器配方和制造工艺 | 不适用 | 商业秘密 | 不适用 | 没有。内部发展 | ||||
|
商标: 节拍 |
续期将于2026年到期 | 英国、加拿大、中国、欧盟、印度、日本、挪威、俄罗斯、新加坡 | 马来西亚、巴西、墨西哥、瑞士、土耳其 | 没有。内部发展 | ||||
| 商标:SugarBEat | 续期将于2025年到期 | 英国、加拿大、澳大利亚、瑞士、中国、埃及、欧盟、以色列、印度、伊朗、日本、朝鲜、摩洛哥、墨西哥、挪威、新西兰、俄罗斯、新加坡、突尼斯、土耳其、美国 | 不适用 | 没有。内部发展 | ||||
|
代谢健康传感器(3)
|
2041年12月7日 | 不适用 | 英国 | 没有。内部发展 |
(1)本专利提供了一个公式,用于通过减去两个读数之间的差值来计算在定义的时间段内提取的葡萄糖量,从而实现快速检测,而无需耗尽被测量的分析物。
(2)本专利描述了一种用于为提取葡萄糖准备皮肤的设备和方法。
| 6 |
临床试验
我们的 临床测试由全球多个中心的合同临床研究机构进行,覆盖范围广泛 --包括亚洲和欧洲--并由我们的内部管理团队管理。
我们 在2016年6月与FDA举行了2次提交前会议,以确定临床路线图。因此,制定了详细的临床计划并在内部获得批准,并选择并审核了欧洲的一个临床地点,以开始使用 SugarBEAT®的身体穿戴发射器设备版本的临床研究。该研究已完成,并于2020年7月向FDA提交了PMA申请。
这些研究的数据也作为欧洲CE批准的一部分于2019年5月提交。
研发
在截至2023年3月31日和2022年3月31日的财年中,我们在研发方面的支出分别为1,538,615美元和1,556,988美元;管理层目前预计,下一财年在这方面的支出将保持合理一致。
制造业
经CE认证的医疗器械的制造和销售受国际标准化组织规定的指南控制和管理,更具体地说是ISO13485;糖业BEAT®将按照ISO13485质量标准制造和销售。
为了支持SugarBEat®在英国和欧盟的商业销售,我们与我们的制造合作伙伴Nemaura Pharma合作,扩大了各种SugarBEAT®组件的生产规模,并建立了最终组装和包装设施。作为这一过程的一部分,我们在英国拉夫堡大学科学与企业园(LUSEP)的现有总部场地内占用了更多空间,从而扩大了我们的制造和组装能力。
我们 已与各种制造合作伙伴签订了以下类型的协议:
| – | 传感器制造的制造协议 |
| – | 贴片制造的制造协议 |
| – | CGM发射装置制造协议和充电站制造协议 |
销售 和市场营销
2014年3月31日,与Dallas Burston Pharma签署了英国和爱尔兰共和国的独家营销权协议,Dallas Burston Pharma是一家总部位于泽西岛(海峡岛)的公司(DB Pharma)(随后于2018年更新,并于2021年再次更新,将公司名称更改为MySugarWatch Limited“MSW”),该公司在英国拥有药品营销业务,并展示了直接向全科医生营销处方药产品的非常成功的模式。我们收到了不可退还的预付款1百万英磅(按当时汇率计算为167万美元),作为回报,我们向MSW提供了在英国和爱尔兰共和国直接向消费者销售SugarBEAT®设备的独家权利,并通过全科医生的处方销售。 独家营销权协议的关键条款是在2015年8月签署的一份商业协议中签订的。本协议 已于2019年10月更新并重新发布,涵盖了新的知识产权/技术改进。
此外,我们于2018年5月与MySugar Watch(欧洲)有限公司(前身为达拉斯Burston ethitronix (欧洲)有限公司)订立了一项合资协议,根据协议,我们将平均分摊我们的SugarBEAT®系统在欧洲所有地区(英国除外)的销售成本和净利润,这是与MSW达成的一项单独协议的主题。本协议 已于2019年10月更新并重新发布,涵盖了新的知识产权/技术改进。2018年分别与TPMENA和Al-Danah Medical签署了海湾地区(GCC)和卡塔尔的商业协议。
| 7 |
监管事项
政府 法规
我们的业务受到广泛的联邦、州、地方和外国法律法规的约束,包括与环境保护、健康和安全有关的法规。一些相关法律尚未得到监管部门或法院的明确解释,其条款存在多种主观解释。此外,这些法律及其解释可能会更改,或可能颁布新的法律。
联邦和州政府机构继续对医疗保健行业进行严格的监管审查,包括加强民事和刑事执法工作。我们相信,我们的业务运营结构符合所有适用的法律 要求。但是,政府实体或其他第三方可能会以不同的方式解释这些法律,并断言 不同。我们在下面讨论与我们的业务最相关的法规和法规。
联合王国、威尔士和欧盟的规定
英国、威尔士、欧盟和其他国家的政府当局对医疗器械的研究、开发、测试、制造、标签、推广、广告、分销、抽样、营销和进口以及出口进行广泛的监管,包括贴片和其他药品。我们在英国和威尔士的身体佩戴的发射器设备将受到严格的监管,并在商业分销之前需要监管部门的批准。获得政府批准并遵守持续的法规要求的过程需要花费大量的时间和财力。 此外,法规、规则、法规和政策可能会发生变化,可能会发布新的法律或法规来推迟此类 审批。如果我们在产品开发过程、审批过程或审批之后的任何时候未能遵守适用的法规要求,我们可能会受到行政或司法制裁。这些制裁可能包括当局拒绝批准悬而未决的申请、撤回批准、临床搁置、警告信、产品召回、产品扣押、完全或部分暂停我们的业务、禁令、罚款、民事处罚或刑事起诉。任何机构的执法行动都可能对我们产生实质性的不利影响。
欧洲公共卫生委员会(“ECPH”)规定了新的医疗诊断设备的开发和商业化。投放到欧洲市场的任何医疗器械都必须符合相关法律,特别是医疗器械指令93/42/EEC、有源植入性器械指令(90/385/EEC)或体外培养使用设备 指令(98/79/EC)。从26这是到2021年5月,所有新批准的医疗器械必须符合医疗器械法规 (2017/745)。在制造/进口之前,必须确定相关设备是否符合上述任何指令。所有医疗器械必须满足上述指令中规定的基本要求。如果可用,可使用相关标准 来证明符合设备指令中定义的基本要求。
制造商还需要确定适当的符合性评估路线。对于符合指令93/42/EEC/法规2017/745的设备,除定制设备和用于临床研究的设备外,合格评估路线取决于设备的类别,将根据指令/法规中规定的某些规则确定。一旦确定了适用的类别或清单,制造商需要遵循适当的合格评定程序。根据设备类型的不同, 这可能要求制造商在将其产品投放市场之前,由通知机构对其质量体系和技术文档进行审查。通知机构是可以执行欧洲联盟认可的合格评定的第三方机构。被通知的机构在签发相关证书之前,需要确保已满足相关要求。制造商 然后可以在其产品上放置CE标志,以证明符合要求。
CE批准是为SugarBEAT®设备实现强制性符合性标志的过程,以允许其在欧盟合法销售。这是制造商的声明,产品符合适用的欧洲法律的要求。SugarBEAT®Device CE提交和审批流程 涉及以下内容:
1.根据欧洲指令描述的某些类别,该设备被归类为 ,I类产品风险较低(例如创可贴),而III类设备风险最高。这些类别为I类、IIa类、IIb类和III类。风险基于产品或其使用出现问题时对患者的潜在伤害。SugarBEat®设备被归类为IIb设备。
2.将准备一份‘技术文件’ ,其中包含证明该产品符合欧洲指令的基本要求所需的所有信息。这包括与设备的性能和安全相关的信息,如产品规格、标签、使用说明、风险分析以及与支持产品声明的产品相关的特定测试信息/临床证据。
3.技术文件中包含的临床证据预计将证明该设备是安全的,并满足规定的性能要求。此临床证据可以是文献数据的形式,其中存在大量使用相同的葡萄糖提取和测量技术的已发表数据(尽管采用不同的设备格式),或者来自使用SugarBEAT®设备进行的实际临床研究的数据。 第一次CE标记提交基于文献评估3研发该方公布了可在 公共领域获得的临床数据。最终提交的CE标志基于设备的临床性能,基于本文早些时候描述的临床研究。临床数据显示,SugarBEAT®设备可以通过每5分钟测量一次血糖来预测受试者的血糖水平。临床试验数据表明,SugarBEAT®设备的血糖趋势可用于补充正常手指的点刺测量 。
| 8 |
4.技术档案 已由独立检查员(通知机构)进行评估,由主管当局(联合王国的药品和保健产品管理署)进行监管。被通知的机构(已被成员国认可以确定医疗器械是否符合欧洲医疗器械指令的欧盟组织),然后将批准通知欧洲公共卫生委员会(ECPH),被通知的机构将向公司颁发证书 ,然后我们将能够将CE标志应用于该设备。并合法地提供该产品在欧洲经济区(EEA)销售。 CE标志已于2019年5月颁发,该公司现在可以在欧盟提供该设备的商业销售。
5.技术文件 于2018年8月开始审查,2019年5月收到最终审查和签字。自CE认证获得批准以来,我们已经对我们的ISO 13485质量管理体系进行了例行检查,以保持我们的CE认证。还向通知机构提交了附录,并获得批准,以便将发射器连接到的智能设备应用程序的iOS版本包括在经批准的CE标志设备中。
美国食品和药物管理局对医疗器械的监管
美国食品、药物和化妆品法案(“FDCA”)和FDA的法规为人类使用的医疗器械建立了一个全面的监管体系。SugarBEAT®是一种医疗设备,受这些以及其他联邦、州、地方和外国法律和法规的约束。FDA负责执行管理美国医疗器械的法律和法规。
FDA根据医疗设备的风险级别以及确保设备安全和有效性所需的控制类型,将医疗设备分为三类(I类、II类或III类)之一。课程分配是确定在美国上市前所需的 上市前提交或申请类型(如果有)的一个因素。SugarBEat®属于 第三类。
| – | I类设备风险较低,不能维持生命或维持生命。大多数第I类设备仅受“一般控制”(例如,禁止掺假和贴错品牌、注册和上市、良好制造规范、标签和不良事件报告)的约束。一般控制是适用于所有类别的医疗器械的基线要求。) |
| – | 第二类装置风险适中,仅靠一般控制不足以提供安全和有效性的合理保证。第II类设备同时受到一般控制和“特别控制”(如特殊标签、符合性能标准和上市后监督)的约束。除非获得豁免,否则II类设备在上市前通常需要FDA批准,通过上市前通知(510(K))流程。) |
| – | 第三类设备的风险最高。这些设备通常是维持生命的、维持生命的,或者用于对防止损害人类健康或存在潜在的不合理的疾病或伤害风险具有重要意义的用途。第III类装置是指仅有一般控制本身是不够的,而且没有足够的信息来确定采用特别控制将提供安全和有效性的合理保证的装置。III类设备受到一般控制,通常需要FDA批准PMA申请才能上市。 | |
除非 免除上市前审查要求,否则医疗设备在美国进行商业营销、分销或销售之前必须获得FDA的营销授权。获得营销授权的最常见途径是510(K)许可 和PMA。在2016年6月作为提交前会议的一部分与美国食品和药物管理局进行了初步讨论后,确定了糖类BEAT®的途径将是PMA批准。
售前审批途径
PMA审批流程需要对设备的安全性和有效性进行独立演示。PMA是FDA要求的最严格的设备营销申请类型。PMA的批准是基于FDA的确定,即PMA包含足够的 有效科学证据,以确保该设备对于其预期用途是安全有效的。PMA应用程序通常包括有关该设备的大量信息,包括在该设备上进行的临床测试结果和制造工艺的详细说明。
在PMA申请被接受审查后,FDA开始对提交的信息进行深入审查。FDA的规定规定了180天的时间来审查PMA并做出决定;但实际上,审查时间通常更长(例如1-3年)。在此 审查期内,FDA可要求提供更多信息或对已提供的信息进行澄清。此外,在审查期内,可能会召集FDA以外的专家组成顾问小组,审查和评估支持该应用的数据,并就该数据是否合理地保证该设备对于其预期用途而言是安全有效的,向FDA提供建议。此外,FDA通常将对制造设施进行审批前检查,以确保符合质量体系法规,该法规对医疗器械的设计和制造 提出了全面的开发、测试、控制、文档和其他质量保证要求。
| 9 |
根据审查情况,FDA可以(I)发布批准PMA的命令,(Ii)发布声明PMA为“可批准”的信函(例如,需要提供较小的补充信息),(Iii)发布声明PMA为“不可批准”的信函,或(Iv)发布拒绝PMA的命令。在FDA发布批准PMA的命令之前,公司不得销售接受PMA审查的设备。作为PMA批准的一部分,FDA可以施加批准后的条件,以确保该设备的持续安全性和有效性,其中包括限制标签、促销、销售和分销,并要求收集额外的临床数据。如果不遵守批准条件,可能会导致严重不利的执法行动,包括撤回批准。
对PMA批准的设备进行的大多数 修改,包括设计、标签或制造流程的更改,在实施之前都需要事先获得批准。事先通过提交PMA附录获得批准。支持PMA补充剂所需的信息类型和FDA审查PMA补充剂的时间因修改的性质而异。
2020年2月,Nemaura宣布,在与FDA讨论后,确定Nemaura可以在未经FDA批准的情况下在美国销售其CGM产品和数字服务产品,作为非医疗福利应用程序。Nemaura进一步宣布,它 打算于2020年10月至12月在美国以proBEAT‘品牌推出这款产品。该产品使用户能够佩戴CGM设备,数据将从该设备发送到Nemaura在云中的 服务器,从那里数据将被处理,为用户提供教育材料和洞察可能影响他们的血糖水平的因素和健康生活方式和饮食的提示,以期帮助糖尿病前期患者和糖尿病患者过上更健康的 生活。2020年12月开始在美国推出限量产品,使潜在客户能够使用 ProBEAT™与针对糖尿病患者的数字减肥计划一起注册他们的兴趣,品牌为BEATdiabets.life。
临床试验
在美国,医疗器械的临床试验受FDA的调查器械豁免(“IDE”)法规管辖。该规定 赋予临床研究发起人重大责任,包括但不限于:选择合格的研究人员、监督试验、提交所需报告、维护所需记录、确保研究人员获得知情同意、遵守研究方案、控制研究设备的处置、提交所需报告等。
重大风险设备(例如,植入物、用于支持或维持人类生命的设备、在诊断、治愈、减轻或治疗疾病或以其他方式防止损害人类健康方面具有重要意义的设备)的临床试验在开始试验之前需要FDA和机构审查委员会(IRB)的批准。FDA通过提交IDE申请获得批准。 非重大风险(“NSR”)设备(即不符合法规对重大风险设备的定义的设备)的临床试验在启动前只需获得IRB批准。临床试验赞助商负责对临床研究是否存在重大风险或NSR进行初步确定;但是,评审IRB和/或FDA可能会审查该决定并不同意该确定。
IDE应用程序必须有适当的数据支持,如性能数据、动物和实验室测试结果,表明在人体上评估该设备是安全的,并且临床研究方案是科学合理的。不能保证提交IDE将导致能够开始临床试验。此外,在试验开始后,如果FDA得出结论认为临床受试者面临不可接受的健康风险,则可暂停试验或终止试验。
如上所述,FDA可能会要求一家公司在上市后环境中收集设备的临床数据。
收集此类数据可能是PMA批准的条件之一。FDA还有权在某些设备获得批准或批准后的任何时间通过信函下令对这些设备进行上市后 监控研究。
无处不在的 和FDA持续的监管
设备投放市场后,无论其分类或上市前途径如何,通常都适用许多FDA额外要求 。这些措施包括但不限于:
| – | 设施登记和设备清单要求; |
| – | 质量体系规定(“QSR”),规定成品设备的设计、制造、包装、标签、储存、安装和维修所使用的方法、设施和控制; |
| – | 标签要求,要求在器械标签和标签中包括某些内容,一般要求医疗器械的标签和包装包括唯一的器械识别符(“UDI”),还禁止宣传产品用于未经批准或未经批准的用途,即“标签外”用途; |
| – | 医疗器械报告(MDR)法规,要求制造商和进口商在其设备可能导致或促成死亡或严重伤害,或发生故障而很可能导致或促成死亡或严重伤害时,向FDA报告;以及 |
| – | 更正和移除报告条例,该法规要求制造商和进口商在采取行动以减少设备对健康构成的风险或补救可能对健康构成风险的联邦食品、药物和化妆品法案的情况下,向FDA报告召回(即更正或移除);制造商和进口商必须保留他们认为不应报告的召回记录。 |
| 10 |
FDA通过检查和市场监督来执行这些要求。不遵守适用的法规要求可能导致FDA采取执法行动,其中可能包括但不限于以下制裁:
| – | 无标题信件或警告信; |
| – | 罚款、禁令和民事处罚; |
| – | 召回或扣押我们的产品; |
| – | 限产、部分停产或者全面停产的; |
| – | 拒绝510(K)审批或新产品上市前审批的请求; |
| – | 撤回已经批准的510(K)许可或上市前批准;以及 |
| – | 刑事起诉。 |
我们 将接受FDA以及其他监管机构的突击检查,以监督适用的州公共卫生法规的执行和 遵守。这些检查可能包括我们供应商的设施。
英国、威尔士和欧盟的其他法规
医疗保健 报销
在我们开展业务的许多国家/地区(包括英国和威尔士),政府和私营部门限制医疗成本增长的举措(包括价格监管、竞争性定价、覆盖范围和 支付政策以及管理式医疗安排)仍在继续。这些变化导致市场更加重视提供更具成本效益的医疗产品。政府 计划、私人医疗保险和管理式医疗计划试图通过限制他们为特定程序或治疗支付的报销金额来控制成本 。这导致客户对产品的价格敏感度越来越高。 一些第三方付款人还必须批准新的或创新的设备或疗法的承保范围,然后才能向使用医疗设备或疗法的医疗保健提供者报销 。即使新的医疗产品可能已获准用于商业分销,但在获得政府和私人第三方付款人的报销批准之前,我们可能会 发现对该产品的需求有限。
环境法规
我们 还受到英国和威尔士国内外的各种环境法律和法规的约束。与许多其他医疗设备公司一样,我们的业务涉及使用受环境法监管的物质,包括危险废物,主要是制造和灭菌过程。我们预计,遵守环境保护法不会对我们的综合运营结果、财务状况或现金流产生重大影响。然而,这些法律和法规都可能发生变化,我们无法预测此类变化可能对我们的业务、财务状况或运营结果产生什么影响(如果有的话)。
外国监管
无论我们是否获得产品的监管批准,我们都必须获得外国可比监管机构的批准 才能开始在这些国家进行临床试验或销售该产品。审批流程因国家/地区而异, 时间可能比EC审批所需的时间长或短。管理临床试验、产品许可、定价和报销的要求也因国家而异。
此外,除美国以外的大多数国家/地区都需要对价格进行监管审批。我们面临的风险是,监管审批流程产生的价格不足以为我们或我们的合作者带来可接受的回报。
| 11 |
欧盟通用数据保护条例
欧盟一般数据保护条例(GDPR)自2018年5月25日起在所有欧盟成员国生效,取代了 之前的欧盟数据隐私法。虽然现有的一些基本原则将保持不变,但《全球数据保护框架》对数据控制者和数据主体的权利引入了新的义务,其中包括:
| – | 问责制和透明度要求,这将要求数据管制员证明和记录遵守GDPR的情况,并向数据主体提供更详细的处理信息; |
| – | 增强的数据同意要求,其中包括与处理敏感数据有关的“明确”同意; |
| – | 在开发任何新产品或服务时考虑数据隐私的义务,并限制收集、处理、存储的信息量及其可获得性; |
| – | 对使用数据分析数据对象的限制; |
| – | 应要求向资料当事人提供可使用格式的个人资料,并在某些情况下删除个人资料;以及 |
| – | 报告违规行为,不会有不适当的延误(可行时为72小时)。 |
GDPR还对违反要求的行为引入了新的罚款和处罚,包括对严重违规行为的罚款,最高可达全球年收入的4%或2000万欧元,以及对其他指定违规行为的罚款,最高可达全球年收入的2%或1000万欧元(以最高者为准)。GDPR确定了在施加罚款时要考虑的要点清单(包括侵权的性质、严重性和持续时间)。
公司已评估GDPR对其持有的所有个人数据的影响,并已实施措施以确保个人数据 应:
| - | 以合法、公平和透明的方式处理与数据主体有关的信息。 |
| - | 为特定、明确和合法的目的而收集的,并且不以与这些目的不相容的方式进一步处理。 |
| - | 充分、相关且仅限于与处理它们的目的相关的必要内容。 |
| - | 以一种允许识别资料当事人的形式保存,时间不超过处理个人资料所需的时间。 |
| - | 以确保个人数据适当安全的方式处理,包括防止未经授权或非法处理以及使用适当的技术或组织措施防止意外丢失、销毁或损坏。 |
| - | 保持准确和最新,并采取一切合理步骤,确保在考虑到处理个人数据的目的后,不准确的个人数据立即被删除或更正。 |
在本公司目前的发展阶段以及现阶段的收入前,所持有的数据范围以及GDPR的影响都是有限的。GDPR的更多应用将在公司进一步发展之前进行评估和实施,以保证 需要额外的GDPR措施。随着公司产品商业化进程的推进,GDPR对公司的影响程度将增加 ,这将需要对公司的程序和政策进行额外的更改,这可能会对运营和合规成本产生不利影响 。此外,还存在措施不能正确实施或企业内部人员不能完全遵守新程序的风险。如果违反这些措施,公司可能面临重大的行政和金钱制裁以及声誉损害,这可能对其运营、财务状况、 和前景产生重大不利影响。
人力资本管理
我们 相信多样化的员工队伍对我们的成功非常重要。我们将继续专注于女性和代表性不足人群的招聘、留住和晋升,并培养包容和多样化的企业文化。在未来,我们打算继续 评估我们在管理业务中使用的人力资本措施或目标,例如我们在发展、吸引和留住员工以及保持员工队伍多样性方面雇用或寻求雇用的因素。
我们业务的成功从根本上与我们员工的福祉息息相关。因此,我们致力于保障员工的健康、安全和健康。我们为我们的员工提供各种灵活、方便的健康和健康计划,包括提供保护和安全的福利,以便他们可以安心应对可能需要离开工作时间或影响其财务状况的事件;通过提供工具和资源来帮助他们改善或保持健康状况并鼓励他们参与健康行为来支持他们的身心健康;并且在可能的情况下提供选择,以便他们 可以定制他们的福利以满足他们的需求和家庭的需要。
我们 还提供强大的薪酬和福利计划来帮助满足员工的需求。我们相信,我们与员工保持着令人满意的工作关系,没有发生过任何劳资纠纷。截至2023年3月31日,我们的工资单上有38名员工 ,相当于大约36名全职员工。
| 12 |
组织结构
我们是一家控股公司,拥有一家诊断医疗器械公司100%的股份,该公司专门从事发现、开发和商业化专业医疗器械 。我们是根据内华达州的法律于2013年12月24日组织的。我们拥有成立于2013年12月11日的英格兰和威尔士公司Dermal Diagnotics(Holdings) Limited的100%股权。皮肤诊断(控股)有限公司拥有成立于2009年1月20日的英格兰和威尔士公司Demal Diagnostics Limited(“DDL”)以及2011年1月12日成立的英格兰和威尔士公司 Trial Clinic Limited(“TCL”)的100%股份。
下图显示了Nemaura截至2023年8月3日的公司结构:
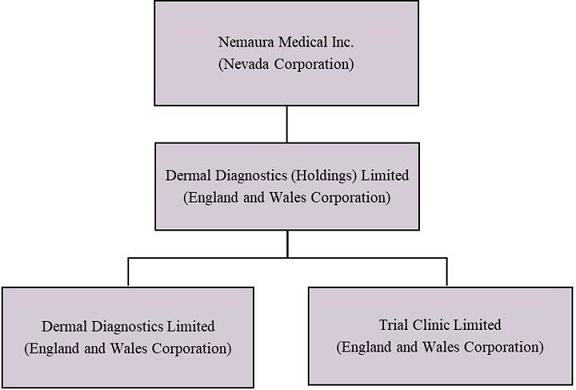
在截至2021年3月31日的财政年度内,董事会评估了集团组织结构的充分性,并得出结论: 不再需要中介控股公司Region Green Limited,因为该实体自成立以来实际上一直处于休眠状态 ,不再需要维持。因此,决定应解除Region Green Limited的清盘,将Region Green Limited持有的资产转移至Nemaura Medical Inc.,随后Region Green Limited将被解散。
资产转移于2021年3月5日进行,Region Green Limited于2021年4月23日正式解散。
2013年12月,我们对公司进行了重组,并将其重新注册为美国国内公司。完成公司重组是为了维护英格兰和威尔士税法下的税收优惠,以造福于Dermal Diagnostics Limited和Trial Clinic Limited的股东。
DDL是一家诊断医疗设备公司,总部位于英国莱斯特郡拉夫堡。DDL成立于2009年1月20日,致力于诊断医疗设备的发现、开发和商业化。该公司最初的重点一直是开发一种新型的CGM设备。
最近的公司历史
解雇首席财务官
自2022年7月1日起,公司解雇了公司首席财务官,并已开始寻找美国的接班人。在选定接班人之前,公司的总裁和首席执行官将担任公司的首席财务和会计 官,公司的财务团队将继续支持公司的会计和财务 报告合规要求。
| 13 |
商业交付
2021年12月,随着SugarBEAT®非侵入性血糖监测仪(“CGM”) 首批交付给英国授权厂商MySugarWatch Limited(“MSW”),标志着公司发展历程中的一个重要里程碑。MSW开发了基于订阅的糖尿病指导和管理服务,该服务将与CGM一起提供,主要针对2型糖尿病患者,并继续进行 研究,以支持英国传感器和糖尿病管理计划的全额报销。
交付反映了与MSW达成的与MSW在2021年早些时候下的初始订单相关的分阶段交付时间表,因此公司开始 确认收入。
此外,2021年9月24日,本公司与MSW的姊妹公司MySugarWatch DuoPack Limited(“MSW-DP”)签订了一份许可、供应和分销协议,根据该协议,MSW-DP将免费向CGM传感器提供广泛用于2型糖尿病患者的某些药物。这些药物于2022年第四季度在欧洲和英国到期,并将于2023年在美国到期。 根据协议条款,向MSW-DP出售传感器的协议价格为美国市场每盒五个传感器20美元,在欧洲和英国,自产品推出起前12个月为12.50欧元,此后每盒四个传感器10欧元。Nemaura在大规模生产中预计每个传感器的商品成本为1美元。截至2022年1月,在欧盟和英国的联合主要领土上,每月有超过200万张处方 用于这些药物。
管理层现在专注于完成剩余的英国授权商的初始订单,并支持MSW在英国的推出,同时还开发公司的能力,通过使用我们的BEAT平台在其他地理市场开发和服务新的业务渠道。这包括将2021年底推出的消费者代谢健康服务Miboko扩展到美国各地的雇主和保险公司。
自动柜员机服务
于2021年7月,本公司与H.C.Wainwright&Co.,LLC(“代理”)订立市场发售协议(“自动柜员机协议”),根据该协议,本公司可不时向或透过代理股份发售本公司普通股。于2022年4月1日,本公司与代理商订立自动柜员机协议修订案(“修订案”),据此,订约方 同意将自动柜员机协议中“登记声明”一词的定义涵义扩大至自2022年4月1日起及其后的时间,包括于2022年3月16日向美国证券交易委员会提交并于2022年3月28日由美国证券交易委员会宣布生效的S-3表格新货架登记声明(档号333-263618)。修正案未对自动取款机协议进行其他更改 。
透过代理人 发售普通股将根据新注册声明及根据 提交予美国证券交易委员会的相关招股说明书补编作出,根据该补充说明书,本公司发售其普通股,总发行价最高可达3,000,000美元。尽管如此,鉴于我们未能及时提交截至2022年12月31日的Form 10-Q季度报告,我们在2024年3月31日之前不再有资格 使用新的注册声明从自动取款机中减持股票。
与EVERSANA达成初步协议
2022年9月27日,公司与EVERSANA签订了一项初步协议,就公司在美国推出BEAT糖尿病计划的战略进行合作。
修正住宅区资本担保本票 附注
于2021年2月8日,本公司、本公司全资附属公司Dermal Diagnostics Limited(“Dermal Diagnostics”)及本公司全资附属公司Trial Clinic Limited(“Trial Clinic”及本公司与本公司及Demal Diagnostics共同发行) 向Uptown Capital,LLC(“Uptown”)(“Uptown Note”)发行本金为24,015,000元的有担保承付票(“Uptown Note”)。Uptown Note的原始发行折扣为400万美元。此外,本公司同意向Uptown支付15,000美元,以支付Uptown的法律费用、会计成本、尽职调查、监测和与买卖Uptown Note有关的其他交易成本,所有金额均包括在Uptown Note的初始本金余额中。因此,Uptown Note的收购价为20,000,000美元。住宅区票据的原始到期日是在住宅区票据的购买价交付日期 后24个月。
2022年10月21日,本公司与本公司、皮肤诊断公司、试验诊所和住宅区签订了日期为2022年10月21日的担保本票修正案 。根据修订条款,本公司与住宅区同意将住宅区票据的到期日延长至2024年7月1日。作为代价 ,本公司同意向Uptown支付5%的延期费用,金额为Uptown票据未偿还余额的5%, 导致应对Uptown的负债增加813,834美元。
本公司及住宅区此前已同意于2022年6月至2023年2月期间,将每月最高赎回金额由2,000,000美元减至500,000美元,减幅仍然有效。根据修订条款,本公司与住宅区同意自2023年3月起至全额支付住宅区票据为止的期间内,将每月最高赎回金额由2,000,000美元减至1,000,000美元;但前提是在发生违约事件时,每月最高赎回金额将自动增加至2,000,000美元。
| 14 |
获得注册直接发行和私募发行及相关附表14C(信息声明)多数已发行和未发行证券的股东批准
2023年1月27日,合计13,596,205股公司普通股(约占公司总投票权的56.4%)的 持有人批准了(I)以每股1.75美元的价格向登记直接发行的投资者发行和出售至多4,796,206股公司普通股(“股份”),交易总额最高可达8,393,360.50美元,以及(Ii) 认股权证(“认股权证”),以购买最多4,796,206股普通股。以每股2.00美元的行使价,以同时私募的方式,以高达9,592,412美元的总收购价 。除其他事项外,该等股东亦批准(I)证券购买协议、配售代理协议(“配售代理协议”) 及认股权证的格式及签立;(Ii)提交招股说明书补充上市说明书以供登记直接发售股份(“招股说明书副刊”);(Iii)提交登记说明书(“转售登记说明书”)以登记认股权证相关股份的转售;及(Iv)向纳斯达克资本市场(“联交所”)提交申请或其他有关文件(S),以使根据招股章程补充及转售注册说明书将分别发售的认股权证相关股份及 股份在联交所上市(“上市申请”)。
2023年4月7日,本公司 向美国证券交易委员会提交了初步附表14C(信息声明),随后向本公司 股东邮寄最终附表14C,通知他们(而不是征求或请求股东批准)持有本公司已发行和已发行有投票权证券 多数的股东批准发行和出售4,797,206股普通股和认股权证,以在同时进行的定向增发中购买同等数量的普通股。
完成840万美元的认股权证登记直接发售和同时私募
于2023年1月31日,本公司根据与两名认可机构投资者订立的证券购买协议完成结算,以S-3表格以登记直接发售方式购买其普通股4,796,206股,并同时私募认购其普通股4,796,206股,行使价为每股2美元。一股普通股和一份认股权证的合并收购价为1.75美元,总收益为8,393,360美元。本公司同意于发售日期起计45天内提交回售登记声明以登记认股权证相关股份的回售,以使该等回售登记声明在发售结束后90天内生效。
未能及时提交表格10-Q的通知
2023年2月23日,纳斯达克证券市场有限责任公司(“纳斯达克”)上市资格部通知本公司,由于未能及时提交截至2022年12月31日的10-Q表格季度报告(“10-Q表格”),纳斯达克未能遵守纳斯达克根据“纳斯达克上市规则”第5250(C)(1)条(“该规则”)继续上市的要求。随后, 2023年2月24日,公司提交了10-Q表格,并重新遵守了规则。
2023年2月27日, 公司收到纳斯达克的通知,根据2023年2月24日的Form 10-Q备案文件,纳斯达克确定公司 遵守规则,此事已结案。
独立注册会计师事务所辞职
2023年2月23日,迈耶·霍夫曼·麦肯会计师事务所(“MHM”)辞去本公司独立注册会计师事务所的职务,自本公司提交截至2022年12月31日的Form 10-Q季度报告后生效。该公司于2023年2月24日提交了截至2022年12月31日的季度报告10-Q。他说:
MHM关于截至2022年和2021年3月31日的财政年度及截至2021年3月31日的财务报表的报告不包含不利意见或免责声明,也没有对不确定性、审计范围或会计原则进行保留或修改,但此类报告对公司作为持续经营企业的能力表示了极大的怀疑。在截至2022年和2021年3月31日的财政年度以及截至2023年2月23日的财政年度内,与MHM在会计原则或惯例、财务报表披露或审计范围或程序方面没有任何分歧,如果这些分歧没有得到解决而令MHM满意,将导致MHM参考与其在该等期间的 公司财务报表报告相关的分歧主题。
在截至2022年和2021年3月31日的财政年度和截至2023年2月23日的财政年度内,不存在S-K法规第304(A)(1)(V)项中所述的“应报告事项” ,但本公司每份(I)截至2022年12月31日的10-Q表格季度报告、(Ii)截至2022年9月30日的10-Q表格季度报告(第1号修正案)中披露的重大弱点除外。和(Iii)截至2022年6月30日的季度报告Form 10-Q/A(修正案1)。
本公司向MHM提供了上述披露的副本,并要求MHM向本公司提供致美国证券交易委员会的信函,声明是否同意MHM向本公司提供并于2023年3月1日提交给美国证券交易委员会的声明。
| 15 |
任命独立注册会计师事务所
2023年5月25日,公司董事会审计委员会任命温伯格公司(“温伯格”)为公司新的独立注册会计师事务所 。在截至2023年3月31日和2022年3月31日的财政年度内以及截至2023年5月25日,本公司或代表本公司行事的任何人均未就S-K法规第304(A)(2)(I)和(Ii)项中规定的任何事项或应报告的事件咨询温伯格。
未能满足纳斯达克上市证券最低市值和最低投标价格要求的通知
2023年04月3日,本公司 收到纳斯达克上市资格部(“纳斯达克员工”)的书面通知(“纳斯达克上市公告”) ,指出本公司不符合“纳斯达克上市规则”第5550(B)(2)条关于继续在纳斯达克资本市场上市的最低上市证券市值3,500万美元的规定。违规通知不会对公司普通股在纳斯达克资本市场的上市或交易产生立竿见影的影响,交易代码为“NMRD”, 公司目前正在监测其上市证券的市值,并在适当时评估其替代方案,以 解决不足并重新遵守此规则。
纳斯达克上市规则“(以下简称”规则“)要求上市证券持有的上市证券的最低市值为3,500万美元,根据纳斯达克员工在过去30个工作日对本公司上市证券的最低市值进行的审查,本公司 不再符合这一要求。但是,规则还为公司提供了180个日历日的合规期,即到2023年10月2日,在此期间重新获得合规性。如果在此合规期内的任何时间,公司的最高合规额在至少连续10个工作日内以3,500万美元或更高的价格收盘,纳斯达克员工将向公司提供书面合规确认, 此事将被了结。不能保证本公司将能够重新遵守MVLS规定,即使 其继续遵守其他上市要求。
2023年4月7日,本公司 收到纳斯达克员工的书面通知(《投标价格通知》),指出本公司未遵守《纳斯达克上市规则》第5550(A)(2)条规定的1.00美元的最低投标价格要求,以便继续在纳斯达克资本市场上市。 不符合规定的通知不会立即影响本公司普通股在纳斯达克资本市场的上市或交易(代码为NMRD),本公司目前正在监测其普通股的收盘投标价格,并在适当时评估其替代方案,以解决不足,并重新遵守这一规则。
纳斯达克上市规则 要求上市证券维持每股1.00美元的最低买入价,而根据最近30个工作日的收盘价 ,公司不再满足这一要求。投标价格通知指出,将向公司提供180个日历 天,或直到2023年10月3日,在此期间重新获得合规。如果在此期间的任何时间,纳斯达克普通股的投标价格连续至少10个工作日收于每股1.00美元或以上,纳斯达克工作人员将向本公司 提供书面确认符合要求,此事将结束。
或者,如果本公司 未能在180个历日期限届满前重新遵守规则5550(A)(2),但满足公开持有股票市值要求和纳斯达克市场首次上市的所有其他适用标准(最低投标价格除外),并提供书面通知,表明其打算在第二个合规期内通过进行反向股票拆分来弥补不足之处,则如有必要,本公司可获得额外180个日历日,以便 恢复遵守规则5550(A)(2)。
不能保证 即使公司继续遵守其他上市要求 ,公司也能够重新遵守投标价格要求。本公司正考虑为回应投标价格通知而可能采取的行动,以重新遵守持续上市规定,但目前尚未就回应作出任何决定。
新冠肺炎的影响
包括新冠肺炎在内的地区或全球卫生大流行可能会严重影响我们的业务、运营业绩和财务状况。 区域或全球卫生大流行可能会对我们的业务产生实质性的不利影响,具体取决于其持续时间和严重程度。 例如,新冠肺炎大流行对全球经济造成了许多影响,世界各地的政府当局已经实施了 措施来减少新冠肺炎的传播。这些措施,包括政府当局建议或要求的停工和“就地避难”命令,或由公司以其他方式选择作为预防措施,对劳动力、客户、消费者情绪、经济和金融市场造成了不利影响,加上消费者支出的减少,导致了我们许多市场的经济低迷。
由于 新冠肺炎疫情的影响,我们评估并执行了可用的步骤,以确保能够为我们的员工提供保护,并在可能的情况下鼓励远程工作,并在工作场所内任何无法远程完成的工作中遵循所有政府建议和指导 。到目前为止,这一过渡对我们的员工工作效率影响很小 ,对我们的业务造成的中断也很有限。虽然与新冠肺炎相关的限制已基本取消,但我们将继续 评估情况,包括遵守任何政府施加的限制,视情况而定。
目前,新冠肺炎对我们业务的潜在影响仍存在一些不确定性。由于感染可能会继续 变得更加普遍,我们可能会对我们的业务、财务状况和运营结果产生严重的负面影响。 就新冠肺炎疫情对我们的业务和财务业绩产生不利影响的程度而言,它还可能增加本招股说明书中“风险因素”一节中描述的许多其他风险。
| 16 |
风险因素
我们的业务受到许多风险和不确定性的影响,包括紧随本招股说明书摘要之后的“风险因素”中描述的风险和不确定性。这些风险对成功实施我们的战略、对我们业务的增长和未来的盈利能力构成了挑战。这些风险包括但不限于以下风险:
| · | 我们有运营亏损的历史。 | |
| · | 我们将需要筹集更多的资金,以便通过负债、合作和许可安排或发行可能导致现有股东稀释或要求我们放弃技术和产品权利的证券,为我们预期的产品商业化提供资金。 |
| · | 产品销售产生的收入在截至2021年3月31日的上一财年才开始,可能永远不会盈利。 |
| · | 我们的巨额债务可能会对我们的现金流和我们经营业务、遵守债务契约和偿还债务的能力产生不利影响。 |
| · | 我们在很大程度上依赖于我们唯一的候选产品--SugarBEAT®设备的成功,而我们可能无法成功地将这一潜在产品商业化。 |
| · | 如果我们未能获得监管部门对SugarBEAT®设备或我们未来任何其他产品的批准,我们将无法将这些潜在产品商业化。 |
| · | 未能将患者纳入我们的临床试验可能会导致SugarBEAT®设备或我们未来的任何产品的开发延迟。 |
| · | 临床测试的延迟可能会导致我们的成本增加,并推迟我们创造收入的能力。 |
| · | 我们当前或将来的任何产品的临床试验可能会产生否定或不确定的结果,我们可能决定或监管机构可能要求我们对这些产品进行额外的临床和/或临床前测试,或停止我们的试验。 |
| · | 如果获得批准,我们的产品SugarBEAT®设备的商业化可能无利可图,因为需要发展销售、营销和分销能力,或与第三方安排执行这些功能。 |
| · | 我们的专有权利可能无法充分保护我们的知识产权和产品,如果我们不能对我们的知识产权和产品获得足够的保护,我们可能无法成功地销售我们的产品。 |
| · | 我们将产品商业化的能力将取决于我们在不侵犯第三方专利或专有权利的情况下销售此类产品的能力。如果我们被起诉侵犯第三方的知识产权,这样的诉讼将耗资巨大且耗时,不利的结果将对我们的业务产生重大不利影响。 |
| · | 如果我们的产品SugarBEAT®设备不能获得医生、患者和医学界的市场接受,我们将无法产生可观的收入(如果有的话)。 |
| · | 我们已经将BEAT®糖的各种组件的大部分商业制造业务外包出去,传感器化学除外,它是在内部进行的。未能找到制造合作伙伴或扩大我们的内部制造设施可能会对我们的业务增长能力产生不利影响。 |
| · | 如果我们不能吸引和留住高级管理人员、顾问、顾问和科学技术人员,我们的产品开发和商业化努力可能会受到损害。 |
| · | 我们希望扩大我们的营销能力,因此我们可能会在管理我们的增长方面遇到困难,这可能会扰乱我们的运营。 |
| · | 外汇汇率的波动可能会对我们的财务状况和经营业绩产生不利影响。 |
| · | 我们的业务、财务状况和运营结果可能会受到包括新冠肺炎在内的全球卫生流行病的实质性不利影响。 |
| 17 |
| · | 我们的竞争对手可能会开发更便宜、更安全或更有效的产品,这可能会减少或消除我们可能商业化的任何潜在产品的商业成功。 |
| · | 在我们的业务中使用危险材料可能会使我们承担环境索赔或责任。 |
| · | 如果我们不遵守监管机构对诊断医疗器械产品执行的广泛法规,我们产品的商业化可能会被阻止、推迟或停止。 |
| · | 未来,我们希望在英国和欧盟以外的地区分销和销售我们的产品,这将使我们面临进一步的监管风险。 |
| · | 如果用户无法从第三方付款人那里获得足够的报销,市场对我们产品的接受度将受到限制。 |
| · | 产品责任索赔可能会损害我们的声誉,如果保险证明不充分,产品责任索赔可能会损害我们的业务。 |
| · | 我们可能会受到欺诈和滥用法律的应用或执行的负面影响,包括反回扣法律和其他反转介法律。 |
| · | 重述我们的某些财务报表可能会使我们面临风险和不确定因素,包括法律诉讼的可能性增加。 |
| · | 我们发现我们对财务报告的内部控制存在重大缺陷,如果不加以补救,可能会对我们财务报表的可靠性产生不利影响,导致我们财务报表中的重大错报,并导致现有和潜在股东对我们的财务报告失去信心,这反过来可能对我们普通股的交易价格产生不利影响。 |
| · | 如果我们不能继续遵守纳斯达克的持续上市要求,我们的普通股可能会从纳斯达克资本市场退市。 |
| · | 我们的普通股可能会受到交易量有限的影响,可能会出现大幅波动。 |
| · | 我们的股票价格可能会波动。 |
我们的管理层得出的结论是,我们历史上的经常性亏损、运营现金流为负以及严重的累积赤字令人对我们继续经营的能力产生了极大的怀疑。此外,我们的独立注册会计师事务所在截至2023年3月31日的财年审计报告中包含了一段说明,说明我们 作为一家持续经营的企业继续经营的能力。
作为一家较小的报告公司的影响
我们是一家“较小的报告公司”, 根据修订后的1934年证券交易法(“交易法”)第12b-2条规则定义。作为一家较小的报告公司 ,我们可能会利用某些降低的报告要求,并免除其他一些重要要求,否则 通常适用于上市公司。例如,规模较小的报告公司不需要获得审计师 关于管理层对财务报告的内部控制评估的认证和报告;不需要提供薪酬讨论和分析;不需要提供绩效薪酬图表或首席执行官薪酬比率披露; 并且只能提交两年经审计的财务报表和相关的MD&A披露。在本财年的最后一天,如果我们的非关联公司持有至少2.5亿美元的未偿还有投票权和无投票权普通股,我们的收入至少为1亿美元,以及我们的非附属公司持有的未偿还有投票权和无投票权普通股至少有7亿美元(在每一种情况下,相对于普通股价值,都是根据该财年第二季度最后一个营业日的衡量),我们将一直是一家“较小的报告公司”。
企业信息
我们的主要执行办公室位于纽约西57街57号,NY 10019。我们的网站是www.nemauramedical.com,我们的电话号码是+1 646-416-8000。在我们网站上找到的或通过我们网站访问的信息 不是本招股说明书的一部分,也不会合并到本招股说明书中,您不应将其视为招股说明书的一部分。
| 18 |
此次发行。
现将所述4,796,206股股票登记转售,具体如下:
| 在行使认股权证时须发行的普通股 | 4,796,206股我们的普通股,可通过行使出售股东在2023年1月27日的私募交易中获得的认股权证而发行。 |
| 认股权证行使前已发行的普通股。 | 28,899,402股普通股(1) |
| 假设行使所有认股权证,普通股将发行。 | 普通股33,695,608股。 |
| 认股权证的条款 | 每股认股权证可行使一股普通股,行权价为每股2.00美元。该等认股权证可于股东批准生效日期或发行日期起计六个月内行使,并于发行日期起计五年半届满。如果没有登记认股权证相关股份的有效登记声明,则可按持有人的选择以“无现金行使”的方式行使认股权证,令持有人可使用认股权证的增值价值(普通股相关股份的市价与认股权证的行使价之间的差额)行使认股权证,而无须支付任何现金。 |
| 收益的使用 | 我们将不会收到出售股东出售在此登记的4,796,206股普通股的任何收益。然而,假设出售股东现金行使所有认股权证,以每股普通股2.00美元的行使价购买在此登记的4,796,206股普通股,我们预计将获得约9,592,412美元的总收益。然而,认股权证可在无现金基础上行使,在此情况下,我们预计不会从行使认股权证的现金中获得任何总收益。我们打算将行使认股权证现金所得款项净额用作营运资金及一般公司用途。 |
| 风险因素 | 投资我们的证券涉及高度风险。见“”标题下所载或以引用方式并入的信息风险因素在本招股说明书和通过引用并入本招股说明书的文件中,以及我们授权使用的任何自由写作招股说明书中。 |
| 市场符号和交易 | 我们的普通股在纳斯达克资本市场上市,代码为NMRD。 |
| (1) | 本次发行后预计发行的普通股数量基于截至2023年8月1日的28,899,402股已发行普通股,不包括: |
| • | 2023年8月1日行使已发行认股权证时可发行的573,092股普通股,加权平均行权价为每股8.69美元;以及 | |
| • | 截至2023年8月1日,在行使已发行期权时可发行40,000股普通股,加权平均行权价为每股3.98美元。 |
| 19 |
选定的历史合并财务数据
下表显示了我们选定的历史 指定期间的合并财务数据。选定的截至2023年3月31日和2022年3月31日的年度的历史综合财务数据和截至2023年3月31日和2022年3月31日的资产负债表数据来自经审计的财务报表。
历史业绩仅供参考,不一定代表我们对未来期间的预期业绩,中期业绩 不一定代表全年业绩。以下提供的数据应结合《管理层对财务状况和经营结果的讨论和分析》以及本招股说明书中其他部分的综合财务报表及其附注阅读。
| 截至的年度 | ||||||||
| 2023年3月31日 | 2022年3月31日 | |||||||
| 运营报表数据 | ||||||||
| 销售额 | $ | 77,044 | $ | 503,906 | ||||
| 销售成本 | (75,328 | ) | (344,300 | ) | ||||
| 销售成本--库存减记 | (1,478,108 | ) | — | |||||
| 毛利(亏损) | (1,476,392 | ) | 159,606 | |||||
| 总运营费用 | 8,118,842 | 7,730,037 | ||||||
| 运营亏损 | (9,595,234 | ) | (7,570,431 | ) | ||||
| 利息支出 | (6,412,501 | ) | (6,666,630 | ) | ||||
| 所得税优惠前亏损 | $ | (14,143,735 | ) | $ | (14,237,061 | ) | ||
| 所得税优惠拨备 | — | 350,256 | ||||||
| 净亏损 | (14,143,735 | ) | (13,886,805 | ) | ||||
| 外币折算调整 | (836,946 | ) | (257,885 | ) | ||||
| 综合损失 | (14,980,681 | ) | (14,144,690 | ) | ||||
| 每股基本和摊薄净亏损 | $ | (0.57 | ) | $ | (0.59 | ) | ||
| 资产负债表数据(期末) | ||||||||
| 现金 | $ | 10,105,135 | $ | 17,749,233 | ||||
| 营运资金(赤字)(1) | (8,730,734 | ) | (494,444 | ) | ||||
| 总资产 | 14,563,233 | 22,101,956 | ||||||
| 总负债 | 26,377,431 | 21,635,872 | ||||||
| 股东(亏损)权益 | (11,814,198 | ) | 466,084 | |||||
(1)营运资本(赤字)等于流动资产总额减去流动负债总额。
| 20 |
风险因素
投资我们的证券会带来很大程度的风险。在您决定购买我们的证券之前,您应仔细考虑以下风险以及 本招股说明书中包含的其他信息,包括本招股说明书中其他地方包含的我们的历史财务报表和相关说明。这些风险和不确定性中的任何一个都有可能对我们的业务、前景、财务状况和经营结果造成重大不利影响,可能导致实际结果与我们所表达的任何前瞻性陈述大不相同 ,并导致我们的普通股价值大幅下降。请参阅“关于前瞻性 声明的警告声明”。
我们可能无法成功地 防止下列任何风险和不确定性可能导致的重大不利影响。这些潜在的风险和不确定性 可能不是我们面临的风险和不确定性的完整清单。可能存在我们目前未意识到或目前认为无关紧要的额外风险和不确定性,这些风险和不确定性在未来可能成为重大风险和不确定性,并对我们产生重大不利影响。由于上述任何风险和不确定性,您可能会 损失全部或相当大一部分投资。
以下是可能对公司及其运营产生重大影响的重大风险、不确定性和其他因素的摘要:
| · | 我们有经营亏损的历史,我们的管理层得出结论,这些因素对我们作为一家持续经营的企业继续存在的能力提出了很大的怀疑。此外,我们的独立注册会计师事务所在其截至2023年3月31日的财政年度的审计报告中包含了一段说明,说明我们是否有能力继续作为一家持续经营的企业。 |
| · | 我们将需要筹集额外的资金,以便通过负债、合作和许可安排或发行可能导致现有股东稀释或要求我们放弃技术和产品权利的证券,为我们预期的产品商业化提供资金。 |
| · | 产品销售产生的收入在截至2021年3月31日的上一财年才开始,可能永远不会盈利。 |
| · | 我们的巨额债务可能会对我们的现金流和我们经营业务、遵守债务契约和偿还债务的能力产生不利影响。 |
| · | 我们在很大程度上依赖于我们唯一的候选产品--SugarBEAT®设备的成功,而我们可能无法成功地将这一潜在产品商业化。 |
| · | 如果我们未能获得监管部门对SugarBEAT®设备或我们未来任何其他产品的批准,我们将无法将这些潜在产品商业化。 |
| · | 未能将患者纳入我们的临床试验可能会导致SugarBEAT®设备或我们未来的任何产品的开发延迟。 |
| · | 临床测试的延迟可能会导致我们的成本增加,并推迟我们创造收入的能力。 |
| · | 我们当前或将来的任何产品的临床试验可能会产生否定或不确定的结果,我们可能决定或监管机构可能要求我们对这些产品进行额外的临床和/或临床前测试,或停止我们的试验。 |
| · | 如果获得批准,我们的产品SugarBEAT®设备的商业化可能无利可图,因为需要发展销售、营销和分销能力,或与第三方安排执行这些功能。 |
| · | 我们的专有权利可能无法充分保护我们的知识产权和产品,如果我们不能对我们的知识产权和产品获得足够的保护,我们可能无法成功地销售我们的产品。 |
| · | 我们将产品商业化的能力将取决于我们在不侵犯第三方专利或专有权利的情况下销售此类产品的能力。如果我们被起诉侵犯第三方的知识产权,这样的诉讼将耗资巨大且耗时,不利的结果将对我们的业务产生重大不利影响。 |
| · | 如果我们的产品SugarBEAT®设备不能获得医生、患者和医学界的市场接受,我们将无法产生可观的收入(如果有的话)。 |
| 21 |
| · | 我们已经将BEAT®糖的各种组件的大部分商业制造业务外包出去,传感器化学除外,它是在内部进行的。未能找到制造合作伙伴或扩大我们的内部制造设施可能会对我们的业务增长能力产生不利影响。 |
| · | 如果我们不能吸引和留住高级管理人员、顾问、顾问和科学技术人员,我们的产品开发和商业化努力可能会受到损害。 |
| · | 我们希望扩大我们的营销能力,因此我们可能会在管理我们的增长方面遇到困难,这可能会扰乱我们的运营。 |
| · | 外汇汇率的波动可能会对我们的财务状况和经营业绩产生不利影响。 |
| · | 我们的业务、财务状况和运营结果可能会受到包括新冠肺炎在内的全球卫生流行病的实质性不利影响。 |
| · | 我们的竞争对手可能会开发更便宜、更安全或更有效的产品,这可能会减少或消除我们可能商业化的任何潜在产品的商业成功。 |
| · | 在我们的业务中使用危险材料可能会使我们承担环境索赔或责任。 |
| · | 如果我们不遵守监管机构对诊断医疗器械产品执行的广泛法规,我们产品的商业化可能会被阻止、推迟或停止。 |
| · | 未来,我们希望在英国和欧盟以外的地区分销和销售我们的产品,这将使我们面临进一步的监管风险。 |
| · | 如果用户无法从第三方付款人那里获得足够的报销,市场对我们产品的接受度将受到限制。 |
| · | 产品责任索赔可能会损害我们的声誉,如果保险证明不充分,产品责任索赔可能会损害我们的业务。 |
| · | 我们可能会受到欺诈和滥用法律的应用或执行的负面影响,包括反回扣法律和其他反转介法律。 |
| · | 重述我们的某些财务报表可能会使我们面临风险和不确定因素,包括法律诉讼的可能性增加。 |
| · | 我们发现我们对财务报告的内部控制存在重大缺陷,如果不加以补救,可能会对我们财务报表的可靠性产生不利影响,导致我们财务报表中的重大错报,并导致现有和潜在股东对我们的财务报告失去信心,这反过来可能对我们普通股的交易价格产生不利影响。 |
| · | 如果我们不能继续遵守纳斯达克的持续上市要求,我们的普通股可能会从纳斯达克资本市场退市。 |
| · | 我们的普通股可能会受到交易量有限的影响,可能会出现大幅波动。 |
| · | 我们的股票价格可能会波动。 |
| 22 |
与我们的业务相关的风险
我们有运营亏损的历史, 我们的管理层得出结论,各种因素对我们作为一家持续经营的企业继续存在的能力提出了极大的怀疑。此外,我们的独立注册会计师事务所在其截至2023年3月31日的财政年度的 审计报告中包含了一段说明,说明我们是否有能力继续作为一家持续经营的企业。
自2009年成立以来,我们每年都出现净亏损。在截至2023年3月31日和2022年3月31日的财政年度,我们报告的净亏损分别为14,143,735美元和13,886,805美元 ,来自运营活动的负现金流分别为8,451,781美元和6,504,041美元。如我们的合并财务报表所示, 截至2023年3月31日,我们的累计赤字为51,875,211美元。我们预计在我们的产品成功发布之前会出现亏损 并且不能确定我们是否会实现盈利。因此,我们的业务受制于 开发新企业所固有的所有风险,例如我们可能无法获得所需的大量额外资本,以支持开发我们的技术和将我们的潜在产品商业化;为我们的潜在产品开发市场;成功地 从一家专注于研究的公司转型为能够制造和销售潜在产品或将我们的潜在产品授权给其他公司的公司;和/或吸引和留住合格的管理、技术和科学人员。我们的管理层 得出的结论是,我们历史上的经常性亏损、运营现金流为负以及巨额累积亏损使人对我们作为一家持续经营的企业继续经营的能力产生了严重的 怀疑。此外,我们的独立注册会计师事务所在其截至2023年3月31日的财年审计报告中包含了一个 说明段落,说明我们作为一家持续经营企业继续经营的能力。
我们的财务报表不包括这种不确定性可能导致的任何调整 。这些调整可能包括我们资产的账面金额的大幅减值,以及如果我们无法履行各种运营承诺可能产生的潜在或有负债。 此外,我们证券的价值将大幅减值。我们作为持续经营企业的持续经营能力取决于从运营中产生足够的现金流以及获得额外的资本和融资。如果我们从运营中产生现金流的能力被推迟或降低,并且我们无法从其他来源筹集额外资金,则即使此次发行成功,我们也可能无法继续经营。有关我们继续作为持续经营企业的能力和我们对未来流动性的计划的进一步讨论, 参见“管理层对财务状况和经营结果的讨论和分析-作为持续经营企业继续经营的能力 ”。
我们将需要 筹集更多资金,以便通过产生债务、通过 协作和许可安排、或通过发行可能导致现有股东股权稀释的证券、或要求我们 放弃对我们技术和产品的权利,来为我们预期的产品商业化提供资金。
开发我们的产品、进行临床试验、建立制造设施以及开发营销和分销能力是昂贵的。 我们将需要通过额外的公共或私募股权发行、债务融资或公司合作以及许可安排来为未来的现金需求融资。我们不能确定是否会以可接受的条件向我们提供额外资金,或者根本不能。如果没有足够的 资金,我们可能会被要求推迟、缩小或取消我们的一个或多个研发计划或商业化努力。如果我们通过发行股权证券筹集额外资金,我们的股东可能会受到稀释。如果我们通过协作和许可安排筹集额外资金,则可能需要 放弃对我们的技术或产品的某些权利,或者以对我们不利的条款授予许可。
产品销售产生的收入 在截至2021年3月31日的上一财年才开始,可能永远不会盈利。
到目前为止,我们在截至2021年3月31日的上一财年首次为产品销售创造了收入。我们创造和增长收入的能力取决于几个因素,包括我们支持我们的英国被许可人进入市场的能力,在所有已确定的将我们的产品线商业化的关键市场上成功获得监管 批准的能力。即使到那时,我们也需要建立和维护销售、市场营销和分销,并在不外包制造的情况下,建立和保持制造能力。我们计划依靠一个或多个 战略合作伙伴来帮助在英国以外的市场创造收入,但是,我们不能确定我们的合作伙伴(如果有的话)是否会成功。我们的创收能力还将受到在新兴市场和不断发展的行业建立新技术和产品时经常遇到的某些挑战、风险和不确定性的影响。这些挑战包括 我们能够:
| – | 执行我们的商业模式; |
| – | 创造品牌认知度; |
| – | 管理我们业务的增长; |
| – | 以符合成本效益的方式建立客户基础; |
| 23 |
| – | 留住客户; |
| – | 在需要时获得额外资本;以及 |
| – | 吸引和留住关键人才。 |
我们不能 确定我们的业务模式是否会成功,或者它是否会成功应对这些和其他挑战、风险和不确定性。 如果我们无法产生可观的收入,我们可能无法盈利,我们可能无法继续运营。即使 如果我们能够将SugarBEAT®设备商业化,我们可能至少在几年内不会实现盈利,如果有的话,在 产生材料收入之后。
我们的巨额债务可能会对我们的现金流和我们的业务运营能力产生不利影响,使我们继续遵守债务契约,并偿还我们的债务。
我们庞大的债务水平增加了我们可能无法产生足够的现金来在到期时支付利息本金或与我们的债务相关的其他到期金额的可能性。作为股东,我们的债务可能会对您产生其他重要后果。例如,它可以:
| – | 使我们更难履行与我们的债务有关的义务,任何未能履行我们的任何债务工具的义务,包括金融和其他限制性契诺,都可能导致高级担保信贷安排和优先次级票据下的违约事件; |
| – | Make更容易受到一般经济、行业和竞争条件的不利变化以及政府监管的不利变化的影响; |
| – | 要求我们将运营现金流的很大一部分用于偿还债务,从而减少了我们现金流用于营运资本、资本支出、收购和其他一般公司用途的可获得性; |
| – | 限制我们在规划或应对业务和我们所在行业的变化方面的灵活性; |
| – | 与负债较少的竞争对手相比,我们处于竞争劣势;以及 |
| – | 限制我们为营运资本、资本支出、收购、偿债要求、执行我们的业务战略或其他目的而借款的能力。 |
与我们的候选产品和运营相关的风险
我们在很大程度上依赖于我们唯一的候选产品--SugarBEAT的成功®是一款设备,我们可能无法 成功地将这一潜在产品商业化。
我们已经产生了 ,并将继续产生与我们唯一的候选产品SugarBEat® 设备的开发和营销相关的巨额成本。我们已获得在欧盟销售此产品的批准,但不能保证我们将在任何司法管辖区 实现这一点,我们可能永远无法获得批准,或者如果获得批准,我们可能无法在其他地区成功地将此产品商业化。
如果我们的产品(S)在多个地区未能成功商业化,我们可能无法产生足够的收入来维持和发展我们的业务,我们的业务、财务状况和经营业绩将受到不利影响。
如果我们未能获得监管机构对SugarBEAT的批准®设备或我们未来的任何其他产品,我们将无法将这些潜在产品 商业化。
我们产品的开发、测试、制造和营销都受到英国和欧盟政府当局的广泛监管。特别是,由通知机构(可以进行欧盟认可的符合性评估的第三方)获得CE批准的过程既昂贵又耗时,而且这种批准所需的时间是不确定的。我们的产品 必须经过严格的临床前和临床测试,以及要求首席执行官进行的广泛的监管审批过程。此类监管审查包括确定制造能力和产品性能。欧洲通知机构BSI于2019年5月批准CE,允许该产品用于商业销售。这一批准需要对基础的国际标准化组织13485认证的质量管理体系进行年度审查。认证于2021年11月成功续签。
不能保证未来的产品将获得所有必要的批准,也不能保证CE审查或行动不会因要求提供更多信息或测试而导致延误,而这可能会对我们产品的上市和销售时间产生不利影响。此外,如果不遵守适用的监管要求,除其他事项外,还可能导致监管审批被暂停 ,并可能受到民事和刑事制裁。
| 24 |
未能将患者纳入我们的临床试验可能会导致开发SugarBEAT的延迟®设备或我们未来的任何产品 。
如果我们无法招募足够的患者来完成临床试验,我们可能会在SugarBEAT®设备或任何其他未来产品的开发和商业化方面遇到 延迟,或无法获得市场批准。我们能否在临床试验中招募足够数量的患者取决于许多因素,包括人群的疾病严重程度、患者群体的大小、临床方案的性质、患者与临床站点的距离以及试验和竞争临床试验的资格标准。根据当地监管机构在其辖区内进行研究的请求,推迟未来任何可能的患者登记,可能会导致成本增加,并损害我们完成临床试验和获得监管批准的能力。
临床测试延迟 可能会导致我们的成本增加,并推迟我们的创收能力。
临床测试的重大延误 可能会对我们的产品开发成本产生重大不利影响。我们不知道计划中的临床试验是否会按时开始、是否需要重组或是否会如期完成(如果有的话)。临床试验可能会因各种原因而被推迟,包括延迟获得监管部门批准以开始和继续研究、延迟与预期地点就可接受的临床研究条款达成协议、延迟获得机构审查委员会批准以在预期地点进行研究,以及延迟招募患者参与研究。
对我们当前或未来的任何产品(包括SugarBEAT®设备)的测试或监管审批出现重大延误 可能会阻止或导致此类候选产品商业化的延迟,减少此类候选产品销售的潜在收入,并导致 我们的成本增加。
我们当前或将来的任何产品的临床试验可能会产生否定或不确定的结果,我们可能决定或监管机构可能要求我们对这些产品进行额外的临床和/或临床前测试,或停止我们的试验。
如果我们能够向适用的监管机构 证明产品是安全有效的,我们才会获得监管部门的批准,才能将候选产品商业化。我们不知道我们未来的临床试验是否会证明安全性和有效性 足以产生适销对路的产品。由于我们对SugarBEAT®设备的临床试验可能产生阴性或不确定的结果 ,我们可能决定或监管机构可能要求我们对该产品进行额外的临床和/或临床前试验,或停止我们的临床试验。如果发生这种情况,我们可能无法获得此产品的批准,或者此 产品的预期上市时间可能会大幅推迟,我们还可能面临巨大的额外开发成本。如果我们更改或扩大产品的适应症,我们还可能被要求进行 额外的临床测试。
如果获得批准, 我们的产品SugarBEat将商业化由于需要开发销售、市场营销和分销能力,或者需要与第三方安排来执行这些功能,®设备可能无法盈利。
为了使我们潜在产品的商业化有利可图,我们的产品必须具有成本效益,并且在商业规模上进行生产是经济的。根据监管部门的批准,我们预计将产生大量的销售、营销和分销,并且在我们 不外包制造的情况下,与SugarBEAT®设备和我们的其他 潜在产品的商业化相关的制造费用。我们目前没有专门的销售队伍,目前的制造能力有限,我们 在医疗诊断设备产品的销售、营销和分销方面的经验也有限。为了将SugarBEAT®设备或我们可能开发的任何其他潜在产品商业化,我们必须发展销售、营销和分销 能力,或与第三方安排执行这些功能。培养一支销售队伍既昂贵又耗时, 我们可能无法开发这一能力。如果我们不能独立或与他人建立足够的销售、营销和分销能力,我们可能无法产生可观的收入,也可能无法盈利。我们未来的盈利能力将取决于许多因素,包括但不限于:
| – | 开发商业规模制造设施的成本和时机,或外包制造SugarBEat®设备的成本; |
| – | 收到监管部门对SugarBEAT®设备的批准; |
| – | 作为监管部门批准的条件而施加的任何营销限制或上市后承诺的条款; |
| – | 提起、起诉、辩护和执行任何专利权利要求和其他知识产权的费用; |
| – | 建立销售、营销和分销能力的成本; |
| – | 竞争的技术和市场发展的影响;以及 |
| – | 我们可能建立的任何合作、许可和其他安排的条款和时间。 |
即使我们获得监管部门对SugarBEAT®设备或任何其他候选产品的批准,我们也可能永远不会从其中的任何 产品中获得可观的收入。如果我们不能成功地将我们潜在的产品商业化,我们将招致重大的额外损失。
| 25 |
我们的专有 权利可能无法充分保护我们的知识产权和产品,如果我们不能获得对我们的知识产权和产品的充分保护,我们可能无法成功地销售我们的产品。
我们的商业成功将在一定程度上取决于获得和维护我们的技术和产品的知识产权保护。我们只能在有效且可强制执行的专利 涵盖我们的技术和产品,或适用其他市场排他性权利的范围内,保护我们的技术和产品不被第三方未经授权使用。虽然我们已经发布了涵盖SugarBEAT®设备的可强制执行专利,但像我们这样的公司的专利地位可能非常不确定,涉及重要的法律和事实问题, 重要的法律原则仍未解决。到目前为止,英国和欧盟还没有就此类公司专利中允许的权利要求的广度制定一致的政策。美国以外的一般专利环境涉及重大不确定性 。因此,我们无法预测可能允许的索赔范围,也无法预测这些专利权的范围是否会提供足够程度的未来保护,从而使我们能够获得或保持我们在该产品和技术方面的竞争优势。此外,像我们这样的公司依赖于创造一系列产品。我们可能无法开发额外的 专有技术或产品,以生产商业上可行的产品或本身可申请专利的产品。
我们颁发的专利 可能会受到挑战,并可能被第三方作废。英国、欧盟或其他国家/地区专利法或专利法解释的变化可能会削弱我们知识产权的市场排他性。
此外, 其他人可能会独立开发类似或替代技术,这些技术可能不在我们的知识产权范围内。如果 第三方获得类似技术的专利权,可能会对我们的业务产生不利影响。同样,未来的发展和改进可能会导致我们现有的专利过时,使知识产权主要以专有技术的形式得到保护。
如果顾问或关键员工将他们或其他人独立开发的技术信息应用于我们的产品,则可能会出现有关信息所有权的纠纷 ,这些纠纷可能不会以有利于我们的方式解决。使用我们的保密和专有技术的顾问和关键员工需要将其发现中的所有知识产权转让给我们。但是,这些顾问或关键员工可能会终止与我们的关系,我们不能无限期地阻止他们与我们的竞争对手打交道。如果我们的商业秘密为拥有更多经验和财力的竞争对手所知,竞争对手 可能会在其产品、方法或技术的进步中复制或使用我们的商业秘密和其他专有信息。如果我们起诉第三方非法获取并使用我们的商业机密,这将是昂贵和耗时的 ,结果将不可预测。此外,英国和欧盟的法院有时比美国法院更不愿意保护商业机密。此外,如果我们的竞争对手独立开发同等的知识,我们 将缺乏对这些信息的任何合同主张,我们的业务可能会受到损害。
我们将产品商业化的能力将取决于我们在不侵犯第三方专利或专有权利的情况下销售此类产品的能力。如果我们被起诉侵犯第三方的知识产权,这类诉讼将耗资巨大且耗时 ,不利的结果将对我们的业务产生重大不利影响。
我们能否将产品商业化将取决于我们能否在不侵犯第三方专利或其他专有权利的情况下销售此类产品 。诊断医疗器械领域的第三方知识产权是复杂的,该领域的第三方知识产权 正在不断演变。我们没有搜索 可能引发操作自由问题的第三方知识产权,也没有获得关于产品商业化的法律意见,而不是在提交专利申请之前进行的专利 研究,以及各自专利审查局的搜索和审查报告。
此外, 由于专利申请在提交后几个月才公布,而且申请可能需要几年时间才能发布,因此目前可能有我们不知道的正在审理的第三方专利申请,这可能会导致以后获得专利。如果第三方 声称我们侵犯了其专利或其他专有权利,我们可能会面临许多问题,这些问题可能会严重损害我们的竞争地位 ,包括:
| – | 侵权指控,无论有没有正当理由,提起诉讼都可能代价高昂,耗时长,可能会推迟监管审批过程,并可能转移管理层对我们核心业务战略的注意力; |
| – | 如果法院判定我们的产品或技术侵犯了竞争对手的专利或其他专有权,我们可能需要为过去的侵权行为支付大量损害赔偿金; |
| – | 如果持有者提供许可,我们可能不得不支付巨额使用费或授予我们的专利或其他专有权的交叉许可;以及 |
| – | 重新设计我们的流程,使其不会侵犯第三方知识产权,这可能是不可能的,或者可能需要大量的时间和费用,包括推迟将我们自己的产品推向市场。 |
此类行为 可能损害我们的竞争地位和创收能力,并可能导致成本增加。
| 26 |
如果我们的 产品,甜品®是一种设备,如果不能获得医生、患者和医学界的市场接受,我们将无法产生可观的收入(如果有的话)。
我们开发的SugarBEAT®设备可能无法获得医生、患者、第三方付款人和医学界其他人的市场接受。 如果我们获得商业化所需的监管批准,市场接受程度将取决于许多因素,包括:
| – | 监管批准的迹象有限; |
| – | 在医学界建立和展示我们产品的临床有效性和安全性,以及它相对于现有诊断医疗设备的潜在优势; |
| – | 任何副作用的流行率和严重程度; |
| – | 我们能够以可接受的价格提供我们的产品; |
| – | 我们的产品相对方便易用; |
| – | 营销和分销支持的实力;以及 |
| – | 足够的第三方承保或报销。 |
基于以上任何因素,市场可能 不会接受SugarBEAT®设备。如果SugarBEAT®设备获得批准,可能会有 其他疗法直接竞争相同的目标市场。市场可能出于各种原因选择继续使用现有的 产品,包括熟悉这些现有产品或对其定价。如果我们的任何产品 未能获得市场认可,可能会削弱我们的创收能力,这可能会对我们未来的业务产生重大不利影响。
我们已将SugarBEAT的各种组件的大部分商业制造操作外包出去®,但传感器化学除外,传感器化学正在内部进行。未能找到制造合作伙伴或扩展我们的内部制造设施 可能会对我们发展业务的能力产生不利影响。
我们在很大程度上依赖第三方根据我们的规格、充足的数量、按时、符合适当的法规标准并以具有竞争力的价格供应我们的产品。我们不能确定我们是否能够以可接受的条款获得足够的候选产品供应,或者根本不能。
提供诊断性医疗器械的制造商必须遵守法规,其中要求遵守ISO13485规定的医疗器械指令中不断变化的法规。任何工厂的产品制造都将受到严格的质量控制、测试和记录保存要求,以及提交安全报告和其他上市后信息的持续义务 。SugarBEAT®设备的传感器和贴片制造设施目前都通过了ISO13485认证。我们不能 保证设施继续通过监管检查,也不能保证未来对ISO13485标准的更改不会 影响传感器和贴片的制造。
如果我们不能吸引和留住高级管理人员、顾问、顾问和科技人员,我们的产品开发和商业化工作可能会受到影响。
我们的业绩在很大程度上取决于我们的高级管理层和关键科技人员的业绩,特别是董事长兼首席执行官迪万·霍克·乔杜里博士和总裁博士。失去我们任何高级管理层成员或我们的科学或技术人员的服务可能会显著延迟或阻碍我们的产品和其他业务目标的开发,因为 会将管理层的注意力转移到过渡事宜和确定合适的替代者(如果有),并可能对我们的业务、运营结果和财务状况产生重大 不利影响。
我们还依赖顾问和顾问来帮助我们制定研发战略。我们的所有顾问和顾问都是 个体户或受雇于其他组织,他们可能存在利益冲突或其他承诺,例如与其他组织的咨询 或咨询合同,这可能会影响他们为我们做出贡献的能力。
| 27 |
此外, 我们认为我们将需要招聘更多的执行管理和科学技术人员。目前对具有相关科学技术专业知识的技术管理人员和员工的竞争非常激烈,这种竞争可能会持续下去。 无法吸引和留住足够的科学、技术和管理人员可能会限制或推迟我们的产品开发工作 ,这将对我们的产品开发和潜在产品的商业化以及我们业务的增长产生不利影响。
我们希望 扩展我们的营销能力,因此在管理我们的增长时可能会遇到困难,这可能会扰乱我们的运营 。
我们预计支出、员工数量和业务范围都会有增长,尤其是那些我们选择独立或与其他公司一起商业化的潜在产品。为了管理我们预期的未来增长,我们必须继续 实施和改进我们的管理、运营和财务系统,扩大我们的设施并继续培训合格的人员。 由于我们的资源有限,我们可能无法有效地管理我们业务的扩展或培训更多的合格人员。 我们业务的实际扩展可能会导致重大成本,并可能转移我们的管理和业务开发资源。 任何无法管理增长的情况都可能推迟我们业务计划的执行或中断我们的运营。
外汇汇率波动 可能会对我们的财务状况和经营业绩产生不利影响。
我们的功能货币是英国英镑(“GBP”)。报告货币为美元(美元)。收入和支出按报告所述期间的适当加权平均汇率换算。资产和负债 按截至资产负债表日的汇率换算。股东权益按历史汇率从英镑折算成美元。汇率波动和对货币兑换的限制可能会对我们的业务产生不利影响,包括 限制我们将英镑兑换成外币的能力,以及如果英镑贬值,我们以美元计算的收入将减少 。只要美元兑外币走强,这些以外币计价的交易的折算将导致我们国际业务的收入、运营费用和净收入减少。同样,如果美元兑外币走弱,这些以外币计价的交易的折算会增加我们国际业务的收入、运营费用和净收入。当我们将海外子公司的财务报表合并为美元时,我们也会受到汇率波动的影响。如果外币汇率发生变化,将境外子公司的财务报表折算为美元将导致折算损益 ,计入其他全面收益(亏损)的组成部分。我们没有达成协议或购买工具来对冲我们的汇率风险。任何套期保值交易的可用性和有效性都可能是有限的,我们可能无法 成功对冲汇率风险。
此外, 近年来发生了许多事件,包括英国脱欧公投、新冠肺炎的影响以及俄罗斯入侵乌克兰,这些事件对全球经济前景以及英镑兑许多货币的走弱都产生了重大的、潜在的持久影响。我们预计将不得不向我们的一些服务提供商和供应商支付美元,考虑到汇率影响和通胀压力,与之前的 年相比,这将意味着业务成本的显著增加。货币汇率继续非常不稳定,因此目前还不清楚英镑未来的影响或进一步走弱 。
我们的业务、财务状况和运营结果可能会受到包括新冠肺炎在内的全球卫生流行病的实质性不利影响。
包括新冠肺炎在内的地区或全球卫生大流行可能会严重影响我们的业务、运营业绩和财务状况。 区域或全球卫生大流行可能会对我们的业务产生实质性的不利影响,具体取决于其持续时间和严重程度。 例如,新冠肺炎大流行对全球经济造成了许多影响,世界各地的政府当局已经实施了 措施来减少新冠肺炎的传播。这些措施,包括政府当局建议或要求的停工和“就地避难”命令,或由公司以其他方式选择作为预防措施,对劳动力、客户、消费者情绪、经济和金融市场造成了不利影响,加上消费者支出的减少,导致了我们许多市场的经济低迷。
由于 新冠肺炎疫情的影响,我们评估并执行了可用的步骤,以确保能够为我们的员工提供保护,并在可能的情况下鼓励远程工作,并在工作场所内任何无法远程完成的工作中遵循所有政府建议和指导 。到目前为止,这一过渡对我们的员工工作效率影响很小 ,对我们的业务造成的中断也很有限。虽然与新冠肺炎相关的限制已基本取消,但我们将继续 评估情况,包括遵守任何政府施加的限制,视情况而定。
目前,新冠肺炎对我们业务的潜在影响仍存在一些不确定性。由于感染可能会继续 变得更广泛,我们可能会对我们的业务、财务状况和运营结果产生严重的负面影响。 就新冠肺炎疫情对我们的业务和财务业绩产生不利影响的程度而言,它还可能增加本“风险因素”部分描述的许多其他风险。
| 28 |
与我们行业相关的风险
我们的竞争对手 可能会开发更便宜、更安全或更有效的产品,这可能会削弱或消除我们可能商业化的任何潜在产品的商业成功。
如果我们的竞争对手 销售比我们从候选产品开发的未来产品更便宜、更安全或更有效的产品,或者 在我们的产品之前上市,我们可能无法取得商业成功。例如,如果获得批准,SugarBEAT®设备在血糖监测设备设置方面的主要竞争对手将是生产血糖监测设备的德克斯康、雅培和Senseonics 等公司。市场可能出于各种原因选择继续使用现有产品,包括对这些现有产品的熟悉程度或定价。如果我们的产品无法与竞争对手销售的产品竞争,将削弱我们的创收能力,这将对我们未来的业务、财务状况和运营结果产生重大不利影响 。
我们预计将与包括Dexcom、雅培和Senseonics在内的几家公司竞争,我们的竞争对手可能:
| – | 开发和销售比我们未来的产品更便宜或更有效的产品; |
| – | 在我们可以推出从我们的候选产品开发的任何产品之前,将竞争产品商业化; |
| – | 运营更大规模的研发项目,或者拥有比我们多得多的财政资源; |
| – | 比我们更成功地发起或经受住实质性的价格竞争; |
| – | 从有限的现有人才库中更成功地招聘熟练的技术和科学工作者; |
| – | 更有效地协商第三方许可证和战略关系;以及 |
| – | 比我们更容易利用收购或其他机会。 |
我们希望 与大型医疗诊断设备制造公司、与较大公司合作的较小公司、新公司以及其他公共和私人研究组织争夺市场份额。
此外,我们的行业以快速的技术变革为特征。由于我们的研究方法集成了许多技术,因此我们可能很难跟上每项技术的快速变化。如果我们不能保持在技术变革的前沿,我们可能就无法有效地竞争。我们的竞争对手可能会因为现有技术方法的进步或开发新的或不同的方法而使我们的技术过时,这可能会消除我们认为 我们从研究方法和专有技术中获得的产品发现过程中的优势。
在我们的运营中使用危险材料可能会使我们承担环境索赔或责任。
我们的研究和开发活动涉及使用危险化学材料。这些材料可能会造成伤害或污染, 我们可能要对超出我们可用财务资源的任何损害负责。此负债可能会对我们的业务、财务状况和运营结果产生重大不利影响。
我们受管理危险材料和废物的使用、制造、储存、搬运和处置的法律法规的约束。我们可能需要 在未来承担遵守环境法律法规的巨额成本,这可能会对我们的业务、财务状况和运营结果产生重大不利影响。
| 29 |
如果我们未能 遵守监管机构针对诊断医疗设备产品执行的广泛法规,我们产品的商业化 可能会被阻止、推迟或停止。
我们产品的研究、临床前开发、临床试验、制造和营销都受到多个政府机构的广泛监管。 我们尚未获得SugarBEAT®设备在我们所有目标市场的营销批准。获得所需的监管批准的过程既漫长又昂贵,而且此类批准所需的时间也不确定。审批流程受以下因素影响 :
| – | 诊断装置的适应症和权利要求; |
| – | 与产品有关的提交质量; |
| – | 该产品的临床疗效和安全性; |
| – | 制造设施合规性; |
| – | 替代设备的可用性; |
| – | 在临床试验中显示的风险和益处;以及 |
| – | 某些创新产品的专利地位和市场独占权。 |
我们或我们的合作伙伴为我们的产品获得的任何监管批准也可能受到产品可能用于市场的指定用途的限制,或者包含可能代价高昂的上市后后续研究的要求。随后发现产品存在以前未知的问题,包括预料不到的严重程度或频率的不良事件,可能会导致限制产品的营销和将产品从市场上召回。
制造、标签、储存和分销活动也受到政府当局的严格监管和许可。我们产品的制造设施将接受监管机构的定期检查,这些机构可能会不时发出缺陷通知。我们或我们的制造设施未能继续 达到监管标准或补救任何缺陷,可能会导致当局采取纠正措施,包括中断 或阻止营销、关闭我们的制造设施,以及罚款或处罚。
监管机构 还将要求进行上市后监督,以监测和报告我们产品的潜在不良影响。如果获得批准,我们的任何产品如果随后未能遵守适用的监管要求,除其他外,可能会导致警告信、 罚款、暂停或撤销监管批准、产品召回或扣押、运营限制、禁令和刑事 起诉。
政府政策 可能会发生变化,可能会颁布额外的政府法规,以阻止或推迟对我们产品的监管审批。我们无法 预测未来立法或行政行动可能产生的不利政府监管的可能性、性质或程度。 如果我们不能保持监管合规性,我们可能无法销售我们的产品,我们的业务可能会受到影响。
未来,我们希望在英国和欧盟以外的地区分销和销售我们的产品,这将使我们面临进一步的监管风险。
除了保持英国和欧盟对SugarBEAT®设备的批准外,我们还可能寻求 沙特阿拉伯和阿拉伯联合酋长国、香港、澳大利亚和美国的监管批准,以销售SugarBEAT®设备,但 不能保证我们会这样做。我们未来还可能寻求批准更多的国家。监管审查过程因国家而异,外国政府当局的批准是不可预测的、不确定的,而且通常代价高昂。由于延迟收到或未能获得必要的批准或许可,销售我们产品的能力可能会受到很大限制。 在每个国家/地区获得所需批准或 豁免之前,不允许在这些国家/地区和大多数其他国家/地区销售我们的产品。如果不能获得必要的监管批准,可能会削弱我们从国际来源获得收入的能力。
| 30 |
市场 如果用户无法从第三方付款人那里获得足够的报销,我们产品的接受度将受到限制。
政府健康管理机构、私人健康保险公司和其他组织通常为我们的产品提供报销 ,我们的商业成功在一定程度上将取决于这些第三方付款人同意向患者报销我们产品的成本。 即使我们成功地将我们的产品推向市场,我们也不能向您保证,第三方付款人会认为我们的产品具有成本效益 ,或者为其使用提供全部或部分补偿。
新批准的保健产品的报销状态存在重大不确定性 。我们的产品旨在替换或更改现有疗法或程序。这些第三方付款人可能会得出结论,我们的产品不如现有疗法或程序安全、有效或成本效益高。因此,第三方付款人可能不会批准我们的产品进行报销。
如果第三方付款人不批准我们的产品进行报销或未能充分报销,销售将受到影响,因为一些医生或他们的患者将选择已批准报销或得到充分报销的竞争产品。即使第三方付款人 提供报销,这些付款人的报销政策可能会对我们的能力以及我们的潜在合作伙伴在盈利的基础上销售我们的产品的能力产生不利影响。
管理医疗保健的趋势、健康维护组织等组织的增长以及改革医疗保健和政府保险计划的立法建议可能会显著影响医疗保健服务和产品的购买,从而导致价格下降 并减少对我们产品的需求,这可能会对我们的业务、财务状况和运营结果产生不利影响。
此外,在监管机构批准我们的产品上市之前或之后,影响我们产品定价的法律和法规可能会以对我们不利的方式发生变化。虽然我们无法预测任何这些立法或监管建议的可能性,但如果任何政府或监管机构采用这些建议,它们可能会对我们的业务、财务状况和 运营结果产生重大不利影响。
产品 责任索赔可能会损害我们的声誉,如果保险证明不充分,产品责任索赔可能会损害我们的业务。
与我们行业的其他公司一样,我们可能面临诊断医疗设备行业固有的产品责任索赔风险。 产品责任索赔可能会引起对我们产品安全性和有效性的质疑,从而损害我们的声誉,并可能通过阻止或干扰我们产品的商业化来限制我们销售产品的能力。
此外,我们行业的产品责任保险通常都很昂贵,只要它是可用的。无法保证 我们将能够以可接受的条款维持此类保险,或我们将能够确保随着产品商业化进程而增加承保范围 ,或我们的产品责任保险将涵盖未来对我们的索赔。此外, 不能保证任何保险单中的任何产品责任保险和/或我们目前拥有的任何赔偿和缴费权利将抵消任何/所有未来的索赔。就未投保的责任和不受任何赔偿或贡献的 向我们提出成功索赔,可能会对我们的业务、财务状况和运营结果产生重大不利影响 。
我们可能会 受到欺诈和滥用法律的应用或执行的负面影响,包括反回扣法律和其他反推荐法律 。
我们不知道 当前有任何商业行为违反了任何欺诈和滥用法律。但是,继续保持警惕以确保遵守所有可能适用的法律将是与产品开发相关的必要费用。例如,必须严格审查所有产品营销活动 ,以确保它们不会违反任何 反回扣法规,与向推荐来源支付不当报酬有关。报酬可能包括我们产品未来的潜在活动,包括折扣、返点和捆绑销售,这些活动必须得到适当的结构,以利用法律和法规的“安全港”。我们可能会不时邀请医生参与咨询活动。此外,我们可能会决定为医生或其他医务人员举办继续医学教育活动。我们也可能不定期授予或赞助医生学习助学金。与医生的所有关系,包括咨询安排、继续医学教育和学习资助,都必须进行类似的审查,以确保遵守任何反回扣法规,以确保不会为转介提供报酬。患者引诱也可能是非法的。根据各种理论,不准确的产品定价报告,或未能以合适的价格向各种政府实体提供产品,也可能成为执法行动的依据。
如果确定了违规的其他要素 ,则因回扣或违反自我推荐规则而被“玷污”的索赔可被指控为虚假索赔。由于我们的潜在客户可能会要求医疗保健计划为我们的产品付款,即使是在临床试验阶段,我们也必须确保我们不会采取任何可能导致提交虚假索赔的操作。例如,明知或不顾后果地向医疗保健计划收费的免费 产品样本可能构成虚假索赔。如果实践 是由我们促成或培育的,我们可能会承担责任。此外,不充分核算或滥用用于产品研究和开发的赠款资金可被指控违反相关法律。
我们的 被发现违反这些法律的风险增加了,因为其中许多法律没有得到监管机构或法院的充分解释,而且他们的条款可能会有各种解释,以及额外的法律或监管变更。
| 31 |
重述我们的某些财务报表可能会使我们面临风险和不确定因素,包括法律诉讼的可能性增加。
2023年2月17日,公司董事会管理层和审计委员会得出结论,以下财务报表应重述,不应再依赖:
(I)披露公司截至2022年6月30日止三个月的未经审计简明综合财务报表,包括在公司于2022年8月12日提交给美国证券交易委员会(“美国证券交易委员会”)的 表格10-Q季度报告(“2022年第一季度10-Q表格”);以及
(Ii)披露公司截至2022年9月30日止三个月及六个月的未经审计简明综合财务报表,包括在公司于2022年11月14日提交予美国证券交易委员会的10-Q表格季度报告(“2022年第二季度10-Q表格”及与2022年第一季度10-Q表格一起,简称“文件”)。
以下 错误影响了申请:(I)没有正确换算按市值计价合同的外币余额;以及(Ii)在计算借款票据的实际利率时,没有将某些债务发行成本计入。
本公司确定 上述错误的报告影响对本公司截至2022年6月30日的三个月(如2022年第一季度10-Q报告)以及截至2022年9月30日的三个月和六个月(如2022年第二季度10-Q报告)的未经审计简明综合财务报表 产生重大影响。因此,本公司决定应重报截至2022年6月30日止三个月的未经审计简明综合财务报表及截至2022年9月30日止三个月及六个月的未经审计简明综合财务报表,并应向美国证券交易委员会提交对2022年第一季度10-Q及2022 10-Q第二季度的修正案。
由于 重述,我们可能会受到其他风险和不确定性的影响,其中包括通过法律程序或美国证券交易委员会和其他监管机构进行审查的可能性增加。针对此类法律诉讼或行政诉讼进行辩护的成本可能会很高。此外,我们可能面临可能对我们的业务、财务状况和经营业绩产生实质性不利影响的金钱判决、处罚或其他制裁。此外,重述如下:
| • | 可能会侵蚀投资者对我们以及我们的财务报告和会计做法和程序的信心; |
| • | 可能对我们普通股的交易价格产生负面影响; |
| • | 转移并可能继续转移管理层对我们业务运营的注意力; |
| • | 要求我们招致额外费用,并可能要求我们招致与任何诉讼或监管检查、调查、诉讼或命令有关的重大额外费用; |
| • | 可能会使我们在必要时以可接受的条件筹集资金(如果有的话)更加困难、昂贵和耗时;以及 |
| • | 可能会使我们更难进行交易或实施可能对我们的业务有利的业务战略。 |
发生或继续发生上述任何情况都可能对我们的业务、经营业绩和财务状况产生重大不利影响。
| 32 |
我们已发现我们在财务报告的内部控制方面存在重大弱点,如果不加以补救,可能会对我们财务报表的可靠性产生不利影响 ,导致我们财务报表中的重大错报,并导致现有和潜在股东 对我们的财务报告失去信心,进而可能对我们普通股的交易价格产生不利影响。
我们发现,截至2023年3月31日,财务报告内部控制存在以下重大缺陷:
在提交截至2022年9月30日的第二季度的Form 10-Q之后,由于在准备截至2022年12月31日的第三季度的Form 10-Q时进行了额外的分析,管理层意识到公司没有对以下事项的准备和审查保持有效的 控制:(I)按市值计价合同的外币余额会计;以及(Ii)在计算借款票据的实际利率时,主要由于缺乏足够的技术专长,以及随后对截至2022年6月30日和2022年9月30日的季度期间的影响,将某些债务发行成本计入。这导致了我们在截至2022年3月31日和2022年6月30日的 季度报告中以Form 10-Q格式最初报告的中期综合季度财务报表中出现错误,进而需要重报这些期间的中期综合财务数据 。管理层认定,截至2022年6月30日和2022年9月30日,这一控制缺陷构成了财务报告内部控制的重大缺陷。重大缺陷是财务报告内部控制的缺陷或缺陷的组合,因此,年度或中期财务报表的重大错报很有可能无法得到及时预防或发现。
控制不足导致在使用有效利率计算和将标记换算为负债的情况下摊销债务发行成本时出现重大错误 。我们评估了是否存在由于上述控制缺陷而无法及时防止或发现重大错报的合理可能性。
基于上述因素, 我们得出结论,上述缺陷上升到了实质性缺陷的程度。根据上市公司会计监督委员会的标准,重大缺陷是财务报告内部控制的缺陷或缺陷的组合,因此我们的合并年度或中期财务报表的错误陈述有合理的可能性将无法防止或及时发现。这个问题的存在可能会对我们、我们的声誉或投资者对我们的看法产生不利影响。
我们正在实施改进和补救措施,以应对实质性的薄弱环节。我们目前正在招聘 一名具有美国上市公司经验和技术专长的继任者CFO。此外,我们正在与具有美国报告专业知识的其他顾问 接洽。这一弱点尚未得到弥补。随着我们继续评估和努力补救重大缺陷, 我们可能决定采取其他措施来解决控制缺陷。
尽管我们计划尽快完成此补救过程,但我们不能保证补救过程将于 完成,我们的措施可能无法成功补救重大缺陷。如果我们的补救措施不足以解决重大弱点,或者如果我们在财务报告的内部控制中发现或未来出现更多重大弱点或重大缺陷,我们的合并财务报表可能包含错误陈述,我们可能被要求 重述我们的财务业绩。此外,如果我们无法成功弥补重大弱点,或者如果我们无法在未来编制准确的合并财务报表,我们的股价、流动性和进入资本市场的机会可能会受到不利影响,我们可能无法保持遵守适用的证券交易所上市要求和债务契约要求。 此外,由于其固有的局限性,即使我们经过补救和有效的财务报告内部控制也可能无法阻止或检测所有错误陈述。此外,对未来期间的任何有效性评估的预测可能会受到以下风险的影响:由于我们条件的变化,控制 可能会变得不充分,或者我们政策或程序的遵守程度可能会恶化。
| 33 |
与我们的普通股、发行和缺乏流动性有关的风险
如果我们不能继续遵守纳斯达克的持续上市要求,我们的普通股可能会从纳斯达克资本市场退市。
我们的普通股在纳斯达克资本市场上市。为了保持我们在纳斯达克资本市场的上市,我们必须满足多项持续上市要求。
2023年2月23日,纳斯达克证券市场有限责任公司(“纳斯达克”)上市资格部通知本公司,由于未能及时提交截至2022年12月31日的10-Q表格季度报告(“10-Q表格”),纳斯达克未能遵守纳斯达克根据“纳斯达克上市规则”第5250(C)(1)条(“该规则”)继续上市的要求。随后, 2023年2月24日,公司提交了10-Q表格,并重新遵守了规则。
2023年2月27日, 公司收到纳斯达克的通知,根据2023年2月24日的Form 10-Q备案文件,纳斯达克确定公司 遵守规则,此事已结案。
2023年04月3日,本公司 收到纳斯达克上市资格部(“纳斯达克员工”)的书面通知(“纳斯达克上市公告”) ,指出本公司不符合“纳斯达克上市规则”第5550(B)(2)条关于继续在纳斯达克资本市场上市的最低上市证券市值3,500万美元的规定。违规通知不会对公司普通股在纳斯达克资本市场的上市或交易产生立竿见影的影响,交易代码为“NMRD”, 公司目前正在监测其上市证券的市值,并在适当时评估其替代方案,以 解决不足并重新遵守此规则。
纳斯达克上市规则“(以下简称”规则“)要求上市证券持有的上市证券的最低市值为3,500万美元,根据纳斯达克员工在过去30个工作日对本公司上市证券的最低市值进行的审查,本公司 不再符合这一要求。但是,规则还为公司提供了180个日历日的合规期,即到2023年10月2日,在此期间重新获得合规性。如果在此合规期内的任何时间,公司的最高合规额在至少连续10个工作日内以3,500万美元或更高的价格收盘,纳斯达克员工将向公司提供书面合规确认, 此事将被了结。不能保证本公司将能够重新遵守MVLS规定,即使 其继续遵守其他上市要求。
2023年4月7日,本公司 收到纳斯达克员工的书面通知(《投标价格通知》),指出本公司未遵守《纳斯达克上市规则》第5550(A)(2)条规定的1.00美元的最低投标价格要求,以便继续在纳斯达克资本市场上市。 不符合规定的通知不会立即影响本公司普通股在纳斯达克资本市场的上市或交易(代码为NMRD),本公司目前正在监测其普通股的收盘投标价格,并在适当时评估其替代方案,以解决不足,并重新遵守这一规则。
纳斯达克上市规则 要求上市证券维持每股1.00美元的最低买入价,而根据最近30个工作日的收盘价 ,公司不再满足这一要求。投标价格通知指出,将向公司提供180个日历 天,或直到2023年10月3日,在此期间重新获得合规。如果在此期间的任何时间,纳斯达克普通股的投标价格连续至少10个工作日收于每股1.00美元或以上,纳斯达克工作人员将向本公司 提供书面确认符合要求,此事将结束。
或者,如果本公司 未能在180个历日期限届满前重新遵守规则5550(A)(2),但满足公开持有股票市值要求和纳斯达克市场首次上市的所有其他适用标准(最低投标价格除外),并提供书面通知,表明其打算在第二个合规期内通过进行反向股票拆分来弥补不足之处,则如有必要,本公司可获得额外180个日历日,以便 恢复遵守规则5550(A)(2)。
不能保证 即使公司继续遵守其他上市要求 ,公司也能够重新遵守投标价格要求。本公司正考虑为回应投标价格通知而可能采取的行动,以重新遵守持续上市规定,但目前尚未就回应作出任何决定。
此外,我们不能向您保证我们的证券将 满足未来将在纳斯达克上市的持续上市要求。如果纳斯达克将我们的普通股从其交易所退市, 我们可能面临重大不利后果,包括:
| • | 我们证券的市场报价有限; |
| • | 确定我们的普通股是“细价股”,这将要求交易我们普通股的经纪商遵守更严格的规则,并可能导致我们普通股在二级交易市场的交易活动减少; |
| 34 |
| • | 对我们公司的新闻和分析师报道的数量有限;以及 |
| • | 未来发行更多证券或获得更多融资的能力下降。 |
如果我们未能保持遵守所有适用的纳斯达克资本市场持续上市要求,而纳斯达克决定将我们的普通股退市,退市可能会对我们普通股的市场流动性、我们获得融资偿还债务和为我们的运营提供资金的能力产生不利的 影响。
我们的普通股可能会受到交易量有限的影响,可能会大幅波动。
我们的普通股在纳斯达克资本市场交易。 虽然我们的普通股已经形成了活跃的交易市场,但不能保证我们的普通股的活跃交易市场将持续下去。 如果我们的普通股未能保持活跃的交易市场,可能会对我们的股东在短时间内出售我们的普通股的能力产生不利影响,或者根本不影响。我们的普通股已经并可能在未来经历重大的价格和成交量波动,这可能会对我们普通股的市场价格产生不利影响。
我们的股票 价格可能会波动。
股票市场,尤其是最近几年,在制药、生物技术和其他诊断性医疗设备公司的股票方面经历了显著的波动。制药、生物技术和其他诊断医疗设备公司股票的波动性通常与股票代表的公司的经营业绩无关。可能导致我们普通股市场价格波动的因素包括:
| – | 我们临床试验的结果和任何延迟; |
| – | 我们的产品未能或延迟进入临床试验; |
| – | 我们的任何研究项目失败或中断; |
| – | 迟迟未能建立新的战略关系; |
| – | 延迟我们产品的开发或商业化; |
| 35 |
| – | 诊断医疗器械行业的市场状况以及发布新的或变更的证券分析师报告或建议; |
| – | 财务和经营业绩的实际和预期波动; |
| – | 关于我们的知识产权或其他专有权利的发展或争议; |
| – | 我们或我们的竞争对手引进技术创新或新的商业产品; |
| – | 在制造我们的产品时出现的问题; |
| – | 我们的产品被市场接受; |
| – | 第三方医疗报销政策; |
| – | 影响我们或我们行业的监管行动; |
| – | 诉讼或公众对我们产品安全的担忧;以及 |
| – | 关键人员的增减。 |
这些和其他外部因素可能会导致我们普通股的市场价格和需求大幅波动,这可能会限制或阻止投资者 随时出售他们持有的普通股,否则可能会对我们普通股的流动性产生负面影响。过去,当一只股票的市场价格波动时,该股票的持有者会对发行该股票的 公司提起证券集体诉讼。如果我们的任何股东对我们提起诉讼,我们可能会产生为诉讼辩护的巨额费用。这样的诉讼也可能转移我们管理层的时间和注意力。
我们已 未支付,并且可能不会支付普通股的任何股息。
到目前为止,我们没有为我们的普通股支付任何股息,并且在可预见的未来可能不会向我们普通股的持有者支付股息。虽然我们未来的股息政策将基于业务的经营业绩和资本需求,但目前预计将保留任何 收益,为我们未来的扩张和业务计划的实施提供资金。作为投资者,您应该 注意,缺少股息会进一步影响我们股票的市值,并可能显著影响对我们公司的任何投资的价值 。
我们 遵守联邦证券法的报告要求。这可能代价高昂,并可能从其他项目中分流资源, 从而削弱我们的增长能力。
我们必须遵守经修订的1934年《证券交易法》(以下简称《交易法》)和其他联邦证券法的信息和报告要求,包括遵守2002年的《萨班斯-奥克斯利法案》(《萨班斯-奥克斯利法案》)。准备和向美国证券交易委员会提交年度和季度报告、委托书和其他信息(包括报告未来可能发生的任何合并)以及向股东提供经审计的报告的成本 将导致我们的费用比我们保持私人持股的情况下的费用更高。
如果我们未能 建立和维护有效的内部控制系统,我们可能无法准确报告财务结果或 防止欺诈。任何不能准确、及时地报告和提交我们的财务业绩的行为都可能损害我们的声誉,并对我们普通股的交易价格造成不利影响。
根据美国证券法,我们 有报告义务。美国证券交易委员会根据萨班斯-奥克斯利法案(“萨班斯-奥克斯利法案”)第404条的要求, 要求每家上市公司在其年报中包括一份关于该公司财务报告内部控制的管理报告 ,其中包含管理层对公司财务报告内部控制有效性的评估 。
公开的公司合规可能会使吸引和留住高管和董事变得更加困难。
随后由美国证券交易委员会实施的萨班斯-奥克斯利法案和规则要求改变上市公司的公司治理做法。作为一家上市公司,我们预计这些规章制度将在2021年及以后增加我们的合规成本,并使某些活动更加耗时且成本更高。作为一家上市公司,我们还预计这些规章制度可能会使我们在未来获得董事和高级管理人员责任保险变得更加困难和昂贵 我们可能被要求接受降低的保单限额和承保范围 或者产生更高的成本才能获得相同或类似的承保范围。因此,我们可能更难吸引和留住合格的人员加入我们的董事会或担任高管。
| 36 |
如果我们的普通股从纳斯达克资本市场退市,并且我们的普通股价格保持在每股5美元以下,我们的普通股将符合“便士股”的定义”.
我们的普通股 将受根据《交易法》第15(G)节通过的“细价股”规则的约束。根据《交易法》第15(G)节通过的细价股规则 一般适用于普通股未在纳斯达克或其他国家证券交易所上市且每股交易价格低于5美元的公司,但过去三年平均收入至少为6,000,000美元或有形净资产至少为5,000,000美元(如果公司经营了三年或更长时间,则为2,000,000美元)的公司除外。这些规则除其他事项外,还要求向“已确定客户”以外的人交易细价股的经纪商填写某些文件,向投资者进行适当性查询,并向投资者提供有关证券交易的某些信息,包括在某些情况下的风险披露文件和报价信息。由于细价股规则的要求,许多经纪商已决定不交易细价股,因此,愿意在此类证券中充当做市商的经纪自营商数量有限。如果我们的普通股从纳斯达克资本市场退市,并且我们的普通股价格保持在每股5美元以下,我们的有形净资产仍然低于2,000,000美元,那么我们的普通股将符合 “细价股”的定义。如果我们在任何重要时期内继续遵守细价股规则,可能会对市场产生不利影响,如果有的话,对我们的证券。如果我们的证券受到细价股规则的约束,投资者将发现更难处置我们的证券。
要约或出售我们普通股的大量股份可能会导致我们普通股的价格下跌。
如果我们的股东 根据第144条规则 在任何法定持有期到期时在公开市场上出售大量我们的普通股,或者在行使未偿还期权或认股权证时发行,这可能会造成通常被称为“悬而未决”的情况 ,预计我们普通股的市场价格可能会下跌。存在悬而未决的情况,无论销售是否已经发生或正在发生,也可能使我们在未来以我们认为合理或适当的时间和价格通过出售股权或与股权相关的证券来筹集额外融资的能力变得更加困难。
D.F.H.Chowdhury博士或其他大股东的利益可能并不总是与我们和我们其他股东的利益一致,这些大股东可能对我们施加重大控制或重大影响,并可能采取不符合或可能与公众股东的最大利益相冲突的行动。
重要股东,包括D.F.H.Chowdhury、我们的首席执行官Bashir Timol、董事和Sufyman Ismail,控制着总计约47%有资格在我们的任何年度或特别会议上投票的股份的投票权的行使。因此,这些重要股东将能够对需要我们获得股东批准的所有事项施加重大影响,包括选举董事会董事和批准我们可能考虑的重大公司交易,例如合并 或以其他方式出售我们的公司或其资产。大股东可能导致我们采取不符合或可能与我们或公众股东的利益相冲突的行动。在大股东的利益与我们其他股东的利益发生冲突的情况下,或者如果大股东选择让我们追求与我们其他股东的利益相冲突的目标,该等其他股东可能会因大股东的此类行动而处于不利地位,我们的普通股价格可能会受到不利影响。
我们 受内华达州修订的管理企业合并和控制股份收购的法规中的反收购条款约束。
内华达州企业合并法规的适用性 如果不能获得我们董事会的批准,将阻碍有意控制我们公司的各方。这些条款可能禁止或推迟合并或其他收购或控制权变更尝试 ,并因此可能阻止收购我们公司的尝试,即使此类交易可能为我们的股东提供机会 以高于当前市场价格的价格出售他们的股票。
内华达州控制权股份法规的效力是,收购人以及与收购人相关行动的人将仅获得股东在股东年度会议或特别会议上的决议授予的控制权股份的投票权。内华达州的控股股份法,如果适用,可能会产生阻止基于我们的组织结构对我们公司的收购的效果。
我们需要遵守多个税务管辖区的规定。
当我们在英国和美国以外进行交易时,我们必须遵守这两个司法管辖区的报税要求。
| 37 |
收益的使用
我们正在登记4,796,206股普通股 供出售股东转售。我们将不会从出售本招股说明书提供的股份中获得任何收益。
然而,假设所有认股权证现金行使以购买现登记的4,796,206股普通股,我们预计将获得约9,592,412美元的总收益 ,行使价为每股普通股2.00美元。然而,认股权证可在无现金基础上行使,在此情况下,我们预计不会因行使认股权证现金而获得任何总收益。我们打算将行使认股权证所得款项净额用作营运资金及一般公司用途。
股利政策
我们从未宣布或支付过我们的股本的任何现金股利,我们目前也不打算在可预见的未来对我们的普通股支付任何现金股利。我们希望 保留未来的收益(如果有的话),为我们业务的发展和增长提供资金。未来是否决定为我们的普通股支付股息将由我们的董事会酌情决定,并将取决于我们的运营结果、 财务状况、资本要求和任何合同限制等因素。
大写
下表列出了我们截至2023年3月31日的实际资本额。
阅读本表时应结合本招股说明书中包含的信息,包括“管理层对财务状况和经营结果的讨论和分析”,以及我们的财务报表及其相关附注,这些信息通过引用并入本招股说明书中。
自.起 2023年3月31日 | ||||
| 实际 | ||||
| (经审计) | ||||
| 现金 | $ | 10,105,135 | ||
| 应付票据 | 20,030,151 | |||
| 股东权益: | ||||
| 普通股,面值0.001美元,核准股42,000,000股,实际发行和发行在外28,899,402股 | 28,899 | |||
| 额外实收资本 | 40,991,377 | |||
| 累计赤字 | (51,875,211 | ) | ||
| 累计其他综合(亏损)收入 | (959,263 | ) | ||
| 股东权益合计(亏损) | (11,814,198 | ) | ||
| 总市值 | $ | 8,215,953 | ||
| 38 |
普通股及相关股东的市场价格 事项
市场信息
我们的普通股于2014年11月4日在场外交易平台 开始报价,代码为“NMRD”。2017年6月30日,我们的普通股在OTCQB开始报价。
2018年1月25日,公司普通股 开始在纳斯达克资本市场交易,现有交易代码为NMRD。以下 表列出了普通股每股的最高和最低买入价。以下报价反映了基于交易商间价格的对我们 普通股的高报价和低报价,没有零售加价、降价或佣金,可能不代表实际交易。
| 投标价格 | |||||||||
| 低 | 高 | ||||||||
| 2020财年 | |||||||||
| 第一季度(2019年4月1日至2019年6月30日) | $ | 8.00 | $ | 14.800 | |||||
| 第二季度(2019年7月1日至2019年9月30日) | $ | 7.06 | $ | 11.000 | |||||
| 第三季度(2019年10月1日至2019年12月31日) | $ | 3.22 | $ | 8.600 | |||||
| 第四季度(2020年1月1日至2020年3月31日) | $ | 2.50 | $ | 10.400 | |||||
| 2021财年 | |||||||||
| 第一季度(2020年4月1日至2020年6月30日) | $ | 4.620 | $ | 16.500 | |||||
| 第二季度(2020年7月1日至2020年9月30日) | $ | 3.117 | $ | 10.660 | |||||
| 第三季度(2020年10月1日至2020年12月31日) | $ | 3.301 | $ | 4.75 | |||||
| 第四季度(2021年1月1日至2021年3月31日) | $ | 3.71 | $ | 12.59 | |||||
| 2022财年 | |||||||||
| 第一季度(2021年4月1日至2021年6月30日) | $ | 4.58 | $ | 17.40 | |||||
| 第二季度(2021年7月1日至2021年9月30日) | $ | 5.72 | $ | 10.726 | |||||
| 第三季度(2021年10月1日至2021年12月31日) | $ | 4.03 | $ | 6.55 | |||||
| 第四季度(2022年1月1日至2022年3月31日) | $ | 3.51 | $ | 4.85 | |||||
| 2023财年 | |||||||||
| 第一季度(2022年4月1日至2022年6月30日) | $ | 2.15 | $ | 4.500 | |||||
| 第二季度(2022年7月1日至2022年9月30日) | $ | 1.500 | $ | 2.605 | |||||
| 第三季度(2022年10月1日至2022年12月31日) | $ | 1.690 | $ | 3.399 | |||||
| 第四季度(2023年1月1日至2023年3月31日) | $ | 0.700 | $ | 3.430 | |||||
| 2024财年 | |||||||||
| 第一季度(2023年4月1日至2023年6月30日) | $ | 0.480 | $ | 0.950 | |||||
| 第二季度(2023年7月1日至2023年9月30日*) | $ | 0.812 | $ | 1.235 | |||||
*至2023年8月1日
2023年8月1日,据纳斯达克资本市场报道,我们普通股的收盘价为每股0.9美元。
截至2023年8月1日,已发行和流通的普通股约为28,899,402股,我们普通股的活跃记录持有者为81人。记录持有者的数量不包括普通股的实益所有人,其股票以银行、经纪商、被提名人或其他受托人的名义持有。
分红
我们从未宣布或支付过我们的股本的任何现金股利,我们目前也不打算在可预见的未来对我们的普通股支付任何现金股利。我们希望 保留未来的收益(如果有的话),为我们业务的发展和增长提供资金。未来是否决定为我们的普通股支付股息将由我们的董事会酌情决定,并将取决于我们的运营结果、 财务状况、资本要求和任何合同限制等因素。
| 39 |
根据股权补偿计划授权发行的证券
我们还没有采用股权补偿计划。
未登记的证券销售
于2023年1月31日,本公司根据与两名认可机构投资者订立的证券购买协议完成认购完成 ,以S-3表格以登记直接发售方式购买4,796,206股其普通股 ,并同时以每股2.00美元的行使价购买4,796,206股普通股的认股权证。一股普通股和一份认股权证的合并收购价为1.75美元,总收益为8,393,360美元。
注册人及关联购买人购买股权证券
我们没有回购任何普通股。
| 40 |
配送计划
出售股票的股东及其任何质权人、受让人或其他利益继承人可以随时在股票交易所在的任何证券交易所、市场或交易设施上或在私下交易中出售、转让或以其他方式处置其持有的任何或全部普通股或普通股权益。该等处置可按固定价格、按出售时的现行市价、按与当时的市价有关的价格、按出售时厘定的不同价格或按协定价格出售。这些销售 可能会在交易中受到影响,可能涉及交叉交易或阻止交易。出售股份的股东可以采用下列一种或者多种方式处置股份或者股份权益:
| ● | 普通经纪交易和经纪自营商招揽买受人的交易; | |
| ● | 大宗交易中,经纪交易商将试图作为代理人出售股票,但可能会以委托人的身份定位和转售部分大宗股票,以促进交易; | |
| ● | 通过可以单独代理的经纪人、交易商或承销商; | |
| ● | 经纪自营商作为本金买入,并由经纪自营商代为转售; | |
| ● | 根据适用交易所的规则进行的交易所分配; | |
| ● | 私下协商的交易; | |
| ● | 通过撰写或结算在登记说明书生效日期后达成的期权或其他套期保值交易,无论是通过期权交易所还是其他方式; | |
| ● | 在本招股说明书所属的登记说明书生效之日后达成的卖空结算; | |
| ● | 经纪自营商可以与出售股票的股东约定,以约定的每股价格出售一定数量的此类股票; | |
| ● | 任何该等处置方法的组合;及 | |
| ● | 依照适用法律允许的任何其他方法。 |
出售股票的股东还可以根据证券法下的规则144(如果有)或证券法下的第4(A)(1)节出售股票,而不是根据本招股说明书出售股票,前提是这些股票符合标准并符合这些条款的要求。
如果出售股票的股东将普通股出售给承销商或者通过承销商、经纪公司或者代理人、承销商、经纪公司或者由出售股东聘请的代理人进行此类交易,可以安排其他经纪公司参与销售。经纪-交易商可以从出售股票的股东那里获得佣金或折扣 (或者,如果任何经纪-交易商充当股票购买者的代理,则从购买者那里获得佣金或折扣),金额将 协商。出售股票的股东不希望这些佣金和折扣超过所涉及交易类型的惯例 。
出售股东可不时将其拥有的部分或全部普通股股份质押或授予担保权益,如果他们未能履行其担保债务,质权人或有担保的当事人可根据本招股说明书或根据第424(B)(3)条或证券法其他适用条款修订出售股东名单, 如有必要,可不时根据本招股说明书、 或根据本招股说明书的补充或修正案将质权人包括在内,受让人或其他利益继承人作为本招股说明书下的出售股东。
每名出售股票的股东已通知本公司,其并非注册经纪交易商,亦未直接或间接与 任何人士订立任何书面或口头协议或谅解以分销普通股。如果出售股票的股东书面通知本公司已与经纪交易商就通过大宗交易、特别发售、交换分销或二级分销或经纪或交易商购买普通股达成任何重大安排,我们将根据证券法规则424(B)在必要时提交本招股说明书的补充文件,披露(I)每个出售股票股东和参与的经纪交易商的名称, (Ii)涉及的股份数量,(Iii)该等普通股的出售价格;(Iv)向该经纪交易商支付的佣金或折扣或准许的优惠(如适用);(V)该经纪交易商并无进行任何调查以核实本招股说明书所载或以引用方式并入的资料;及(Vi)对交易有重大影响的其他事实。此外,在销售股东以书面形式通知受赠人或质押拟出售超过500股普通股后,公司将根据适用的证券法提交本招股说明书的补充文件。
| 41 |
在其他情况下,出售股东也可以转让普通股股份,在这种情况下,受让人、质权人或其他利益继承人将是本招股说明书中的出售受益者。
出售普通股或普通股权益的,出售股东可以在本招股说明书生效日期后与经纪自营商或其他金融机构进行套期保值交易,经纪自营商或其他金融机构可以在对其持有的头寸进行套期保值的过程中进行卖空普通股交易。出售股票的股东也可以在本招股说明书生效日期后卖空 普通股,并交付这些证券以平仓,或将普通股出借或质押给经纪自营商,经纪自营商可能会出售这些证券。出售 股东也可以在登记说明书生效日期后与经纪自营商或其他金融机构达成期权或其他交易,或设立一种或多种衍生证券,要求向该经纪自营商或其他金融机构交付 本招股说明书提供的股份,该经纪自营商或其他金融机构可根据本招股说明书转售股份(经补充或修订以反映此类交易)。
出售股票的股东和参与出售股票的任何经纪自营商或代理人将被视为与此类出售相关的证券法 所指的“承销商”。经纪-交易商可以从卖方股东(或如果任何经纪-交易商 充当证券买方的代理人,则从买方)收取佣金或折扣,金额有待协商,但除本招股说明书附录 中所述外,在代理交易不超过惯例经纪佣金的情况下,遵守金融 行业监管局(“FINRA”)第2121条;在主要交易的情况下,根据FINRA规则2121进行加价或降价。在这种情况下,此类经纪自营商或代理人收取的任何佣金以及转售其购买的股票的任何利润可被视为证券法项下的承销佣金或折扣。
本公司已通知出售股份的股东, 他们须遵守根据1934年证券交易法(经修订)颁布的规则M,在他们 可能从事股份分派的时间内。上述情况可能会影响普通股的可售性。
出售股东出售普通股所得的总收益 将是普通股的购买价格减去折扣或佣金(如果有的话)。 每个出售股票的股东均有权接受并与其代理人一起,不时拒绝直接或通过代理人购买普通股的任何建议。公司将不会从此次发行中获得任何收益 。
本公司须支付与股份登记有关的所有费用及开支。本公司已同意赔偿出售股东的某些损失、索赔、损害赔偿和责任,包括证券法或其他规定下的责任。
本公司已与出售股东 同意保留构成本招股说明书一部分的登记说明书的效力,直至(A)本招股说明书所涵盖的所有股份已根据及按照该登记说明书出售,或(B)本招股说明书所涵盖的普通股股份可由非联属公司出售或转让而不受任何数量限制或根据证券法第144条规定的日期(以较早者为准)为止。
| 42 |
出售股东:
我们准备这份招股说明书是为了允许Armistics Capital Master Fund Ltd.和Alyeska Master Fund,L.P.作为出售股东,不时向出售股东提供最多4,796,206股普通股,在行使各自出售股东目前持有的某些认股权证时发行给出售股东 。
于2023年1月27日,本公司与销售股东(即机构认可投资者)订立证券购买协议(“购买协议”),据此(其中包括)本公司发行及出售可行使合共4,796,206股普通股(“股份”)的认股权证(“认股权证”),行使价为每股2.00美元。认股权证将于股东批准生效日期后的 或发行日期后六个月行使,并于发行日期起计五年零六个月届满。
其下的认股权证和可发行普通股的股份根据1933年证券法未经注册而出售和发行,依据证券法第(Br)4(A)(2)节作为不涉及公开发行的交易和根据证券法颁布的规则506作为向认可投资者销售的豁免而规定的豁免。
下表所列的出售股东可根据本招股说明书不时发售及出售以下所列本公司普通股的任何或全部股份。当我们在本招股说明书中提到 “出售股东”时,我们是指下表中所列的人,以及质权人、受让人、允许受让人、受让人、继承人以及后来通过公开出售以外的方式持有出售股东在我们 普通股股份中的任何权益的其他人。
下表列出了截至本招股说明书之日,我们正在为其登记股票以向公众转售的出售股东的姓名,以及根据本招股说明书,每个该等出售股东可提供的此类 股票数量。适用的百分比基于2023年8月1日发行的28,899,402股普通股 。
我们不能建议出售股票的股东 是否真的会出售部分或全部股份。此外,出售股票的股东可能已出售、转让或以其他方式处置, 或可能在他们提供下表所列信息的日期后,随时、不时地出售、转让或以其他方式处置豁免证券法登记要求的交易中的股份。
|
股票 在此之后实益拥有 产品(2) |
||||||||||||||||
| 出售股东(1) | 透过以下途径实益拥有的股份数目 2023年4月17日 |
本次发行中可能出售的认股权证相关股份数量 | 数量 个共享 |
未偿债务总额的百分比 普通股 |
||||||||||||
| 停战资本总基金有限公司。(3) | 2,398,103 | 2,398,103 | 0 | 0 | % | |||||||||||
| Alyeska Master Fund,L.P.(4) | 2,398,103 | 2,398,103 | 0 | 0 | % | |||||||||||
| (1) | 如有需要,除上表所列出售股东的任何未来受让人、质权人、受让人或继任人外,其他出售股东的信息将在招股说明书补充或修订中列出,本招股说明书是招股说明书的一部分。此外,注册说明书的生效后修正案将被提交,以披露最终招股说明书中包含的描述对分配计划的任何重大变化。 |
| (2) | 假设出售股东在此提供的所有股份均已售出,且出售股东在本次发售完成前不再购买或出售任何额外的普通股。 |
| (3) | 包括2,398,103股可在行使停战资本总基金有限公司(“总基金”)所持有的认股权证时发行的普通股,该认股权证须受若干实益拥有权限制(视乎适用而定)所规限,该等认股权证持有人将无权行使其任何部分,而该等认股权证持有人连同其联属公司在行使该等权利后将实益拥有超过已发行普通股股数的4.99%,但须在至少61天前通知吾等,持股人可以增加或减少最多9.99%的已发行普通股数量的限制。停战资本有限责任公司(“停战”)的首席信息官史蒂文·博伊德对主基金持有的证券拥有投票权和投资自由裁量权。停战和史蒂文·博伊德否认对报告的证券的实益所有权,但他们各自拥有的金钱利益除外。因此,尽管上文所列由总基金、停战及博伊德先生实益拥有的普通股股份数目,总基金、停战及博伊德先生各自进一步否认实益拥有于行使所有认股权证时可发行的普通股股份,惟总基金、停战及博伊德先生及任何其他人士或实体各自实益拥有的普通股股份数目将超过已发行普通股股份总数的9.99%。*停战资本主基金有限公司的地址是麦迪逊大道510号,7号这是Floor,New York,NY 10022。 |
| 43 |
| (4) | 包括(A)2,483,271股由Alyeska Master Fund,L.P.直接持有的普通股及(B)2,398,103股可在行使Alyeska Master Fund,L.P.持有的认股权证后发行的本公司普通股,该等认股权证的持有人须受若干实益拥有权限制(视何者适用而定)所规限,而该等认股权证持有人将无权行使其任何部分,而该等认股权证持有人连同其联属公司,在紧接行使该等权利后实益拥有的已发行普通股股数超过4.99%(或9.99%,视何者适用而定),但在给予吾等至少61天的事先通知后,该持有人可增加或减少最多不超过已发行普通股数量的9.99%的限额。Alyeska Master Fund,L.P.的投资经理Alyeska Investment Group,L.P.对Alyeska Master Fund,L.P.持有的股份拥有投票权和投资控制权。Anand Parekh是Alyeska Investment Group,L.P.的首席执行官,可能被视为该等股份的实益拥有人。然而,Parekh先生否认对Alyeska Master Fund,L.P.持有的股份拥有任何实益所有权。Alyeska Master Fund,L.P.的注册地址为开曼群岛KY1-1104,开曼群岛南教堂街乔治镇Ugland House,P.O.Box 309,c/o Maples Corporate Services Limited。Alyeska Investment Group,L.P.位于芝加哥伊利诺伊州伊利诺伊州60601号,W.W.77,Suite700。 |
管理层对财务状况的探讨与分析
以及行动的结果
以下讨论及分析总结了影响本公司截至及于以下期间的经营业绩、财务状况、流动资金及现金流的重要因素。以下讨论和分析应与本招股说明书中其他部分包含的综合财务报表及其相关附注一并阅读。讨论包含基于管理层信念的前瞻性陈述,以及管理层所做的假设和目前可获得的信息。由于各种因素,实际结果可能与前瞻性陈述中讨论或暗示的结果大不相同,包括下文和本招股说明书其他部分讨论的结果,特别是在有关前瞻性陈述的“风险因素”和“告诫陈述”部分。本文中使用的术语“公司”、“我们”、“我们”和“我们”是指Nemaura Medical,Inc.及其合并的子公司。
公司概况
我们 是一家医疗技术公司,开发了SugarBEAT®,这是一种非侵入性、灵活的连续血糖监测系统,供糖尿病患者和任何希望确定影响其血糖曲线的因素的人使用。SugarBEat® 由一个带有传感器的一次性粘性皮肤贴片组成,该传感器连接到一个可充电的无线发射器。传感器 每隔5分钟测量一次血糖读数,并通过低能量蓝牙将数据发送到智能设备,如手机 (包括Android和iOS)。智能设备上的一个应用程序使用专有算法来显示真实的血糖值,在数据经过 校准后,至少使用一个手指棒校准。SugarBEat®的工作原理是将皮肤中的葡萄糖提取到与电极传感器直接接触的贴片中的一个腔中。数据记录在应用程序上,可以实时查看,还可以存储所有历史数据以供以后根据需要进行评估。我们相信,任何1型或2型糖尿病患者都可以使用SugarBEAT® ,任何希望确定影响其血糖曲线的因素的人也可以使用该产品。 因此,就胰岛素抵抗而言,他们的代谢健康状况。
2019年5月29日,我们宣布已获得行政长官批准,允许SugarBEat®在欧盟合法销售。CE认证 通过使用CE标志来披露,这是制造商对产品符合适用的欧洲法律要求的声明。欧洲的SugarBEat®临床试验计划评估了75名1型和2型糖尿病患者的525个病人日 ,并于2017年12月完成。CE批准是为SugarBEAT®设备 实现强制性符合性标志以允许其在欧盟合法销售的过程。这是制造商的声明,产品符合适用的欧洲法律的要求。这一批准需要对基础的国际标准化组织13485认证的质量管理体系进行年度审查。 认证于2021年11月成功续签。
我们 还向美国食品和药物管理局(FDA)提交了PMA(上市前批准)申请,其标签 与CE批准的标签相同,CE批准是一种用于糖尿病患者的血糖趋势辅助设备。PMA目前正在接受审查。
在2020年7月,我们向美国食品和药物管理局提交了一份PMA申请,要求使用SugarBEAT®作为血糖趋势指纹检测的辅助工具。 我们和其他申请者随后被美国食品和药物管理局告知,由于美国食品和药物管理局的器械和放射健康中心(CDRH)积极参与应对新冠肺炎疫情,审批过程可能会受到延误,这导致 工作人员被重新分配到其他与新冠肺炎相关的批准请求。2021年4月,FDA确认将重新审查PMA申请,2021年12月,FDA的生物监测研究部门对为支持PMA申请而提交的临床计划进行了审计。仅提出了483条意见,该公司于2022年1月提交了完整的答复。FDA随后计划在2022年第二个日历季度进行上市前检查,旨在涵盖FDA的 质量体系/当前的医疗器械良好制造规范(21 CFR Part 820)。
除此之外,Nemaura还建立了基于SugarBEat™平台的ProBEAT®,当根据FDA健康指南使用时,可以根据健康指南进行分类,以提供提示并教育用户影响他们 血糖曲线的因素。
| 44 |
我们 相信SugarBEAT®和基本的BEAT技术平台还有其他应用,其中可能包括:
| · | 医生和糖尿病专业人员可访问的网络服务器,以远程跟踪病情,从而降低医疗成本并更有效地管理病情; |
| · | 一个完整的虚拟医生,监测一个人的生命体征,并通过网络传输结果; |
| · | 其他使用BEAT技术平台来测量替代分析物的贴片,包括乳酸。这将是监测条件的一个步骤,特别是在医院环境中。目前,乳酸监测是用来确定职业运动员的相对健康状况的,我们已经完成了初步研究,证明BEAT技术应用于连续乳酸监测;以及 |
| · | 一种可广泛应用的连续温度监测系统。 | ||
在此产品开发期间,公司 经历了经常性亏损和运营现金流为负。在截至2023年3月31日和2022年3月31日的财年中,我们的产品销售收入分别为77,044美元和503,906美元,净亏损分别为14,143,735美元和13,886,805美元,来自运营活动的负现金流分别为8,451,781美元和6,504,041美元。如我们的财务报表所示,截至2023年3月31日,我们的现金余额为10,105,135美元,营运资本赤字为8,730,734美元,累计赤字为51,875,211美元,股东权益总额为11,814,198美元。由于我们历史上的经常性亏损、运营现金流为负以及巨额累积赤字,我们作为一家持续经营的企业继续经营的能力受到了极大的怀疑。见“风险因素-我们 有运营亏损的历史,我们的管理层得出结论,这些因素对我们作为持续经营的企业 继续经营的能力提出了实质性的怀疑。此外,我们的独立注册会计师事务所在其截至2023年3月31日的财政年度的审计报告中加入了一段说明,说明我们是否有能力继续作为一家持续经营的企业。“
虽然公司预计近期运营将继续出现亏损,但由于产品开发、监管活动、临床试验以及其他商业和产品开发相关费用的产生,这些亏损可能会很大,但在截至2021年12月31日的三个月期间,公司达到了一个重要的里程碑,公司开始向其英国被许可人交付其SugarBEAT®设备,使他们能够继续研究基于用户的反馈和证据,这些反馈和证据可能支持在英国的报销。
行动的结果
管理层的 计划和演示基础
该公司经历了经常性亏损和运营现金流为负。截至2023年3月31日,公司现金余额为10,105,135美元,股东权益总额为11,814,198美元,累计亏损51,875,211美元。到目前为止,本公司主要依靠股权融资为其运营提供资金。最初的额外资金也来自关联方捐款。公司预计近期将继续出现运营亏损,随着公司实施和扩大其产品商业化战略,这些亏损可能会非常严重。
管理层的战略评估包括 以下潜在选项:
| – | 支持英国和欧盟推出SugarBEat®; |
| – | 在美国等其他国家获得对SugarBEAT®设备的进一步监管批准; |
| – | 在其他地区探索许可和合作机会; |
| – | 为其他应用开发商业化的SugarBEAT®设备;以及 |
| – | 考虑未来额外的资本募集是否可以进一步加强和加速实现公司的战略增长目标。 |
经营成果
截至2023年3月31日的财政年度与截至2022年3月31日的财政年度相比
收入
2023财年确认的销售额为77,044美元,而2022财年为503,906美元。
2021年12月标志着公司的一个重要里程碑,公司根据2021年4月下的第一个订单 开始向都市垃圾交付糖BEAT®。在本财政年度的剩余时间里,这些交付继续按照与MSW商定的时间表进行。
虽然2022年确认的大部分收入与货物交付有关,但2022年确认的收入还包括确认 之前收到并在递延收入中持有的100万英镑(约132万美元)的部分,与与MSW签署的独家营销权协议有关。我们预计将在从开始向MSW销售之日起的大约 10年内记录剩余收入。
| 45 |
毛利(亏损)
总亏损为1,476,392美元,而截至2023年3月31日和2022年3月31日的财年毛利润分别为159,606美元。2023财年的销售成本 受到1,478,107美元旧库存减值的影响。
研究和开发费用
截至2023年3月31日和2022年3月31日的财年,研发费用分别为1,538,615美元和1,556,988美元。这里的成本稳定是由于公司与临床试验相关的历史上更大的研发支出和对SugarBEAT®设备的改进在过去一年中开始趋于平稳。我们预计未来随着该产品的推出,SugarBEAT®的相关研究和开发费用将减少,但公司预计将继续产生研究和开发成本,以增强、完善和扩展平台的替代应用能力。
一般费用 和管理费用
截至2023年3月31日和2022年3月31日的财年,一般和行政费用分别为6,580,227美元和6,173,049美元。这包括法律、专业、咨询、审计服务、投资者关系、保险、广告、一般和运营工资以及无形资产减值的费用。费用的增加主要是由工资增加推动的,因为增加了额外的员工人数, 支持我们英国和美国团队的运营扩展流程。保险、租金和折旧以及摊销也出现增长,被认为与本报告所述期间采取的商业化步骤直接相关。此外,还计入了291,534美元的非现金项目费用,这是由于财政期间结束时实施的远期外币合同重估按市值计价的影响,以及980,039美元的无形长期持有资产的一次性减值。
随着公司继续扩大规模以服务于其现有订单,预计一般和管理费用将继续 继续呈现类似的更高成本状况,因为业务继续过渡到以运营为重点的基础,预计 将导致与生产、销售、营销、客户服务相关的功能费用增加,以及对其他现有功能的增强 。
其他 综合收益
在截至2023年3月31日和2022年3月31日的财政年度,其他全面收益的费用为836,946美元(2022年费用为257,885美元),源于外币换算调整 。
流动性 与资本资源
持续经营和流动资金
截至2023年3月31日的年度,公司录得净亏损14,143,735美元,运营中使用现金8,451,781美元。这些因素使人对公司在财务报表发布之日起一年内作为持续经营企业继续经营的能力产生了极大的怀疑。 财务报表不包括如果公司无法作为持续经营企业继续经营可能需要进行的任何调整。 此外,公司的独立注册会计师事务所在其关于公司2023年3月31日经审计财务报表的报告中对公司作为持续经营企业继续经营的能力提出了重大怀疑。
在评估公司的持续经营状况时,管理层考虑了潜在的资金提供者,并相信未来运营的资金可以通过股权和/或债务融资来提供。即使公司能够获得额外的融资,它也可能对我们的运营施加不适当的限制,在债务融资的情况下,或者在股权融资的情况下,对我们的股东造成严重的稀释。
我们历来通过债务和股权融资相结合的方式为我们的运营提供资金。在截至2023年3月31日的财政年度内,发行了4,796,536股普通股,总收益为8,394,056美元,扣除与融资相关的成本 737,658美元后,净收益为7,656,398美元。
截至2023年3月31日,公司有净营运资金短缺(8,730,734美元),其中包括现金余额10,105,135美元和当前应付票据16,942,500美元。
现金流
截至2023年3月31日的财政年度,我们经营活动使用的现金净额为8,451,781美元,反映了以下主要现金流量变动:净亏损14,143,735美元,其中包括与债务贴现增加相关的非现金项目1,871,593美元,外汇合同衍生负债公允价值变动291,534美元,认股权证负债公允价值变动1,864,000美元折旧 和摊销444,177美元,库存减记1,478,108美元,以及无形资产减值980,039美元。
| 46 |
现金流也受到与采购原材料相关的1,745,189美元库存和1,022,077美元应收/应付关联方增加的影响 ,以支持生产和向我们的英国被许可方交付产品。
营运资金现金流也受到应付账款增加190,330美元的影响,这是由于购买的时机以及其他负债的减少和应计费用427,748美元。
截至2022年3月31日的财年,我们的经营活动使用的现金净额为6,504,041美元,反映了以下主要现金流变动:净亏损13,886,805美元,其中包括作为债务折扣增加相关费用入账的非现金项目(6,666,630美元),财政年度末持有的外币远期合同按市值计价(440,196美元),支付给 员工的股票薪酬(220,917美元),以及折旧和摊销(229,810美元)。
|
截至2023年3月31日的财政年度,用于投资活动的现金净额为539,217美元,这反映了用于支持在本年度开始生产待售产品的财产和设备支出 376,170美元,以及用于软件开发的持续支出(27,879美元)和专利 成本(135,168美元),以加强业务数字产品供应和保护开发的知识产权。
|
截至2022年3月31日的财政年度,用于投资活动的现金净额为956,482美元,反映了用于支持在本年度开始生产待售产品的财产和设备支出 481,718美元,以及用于软件开发的持续支出 (391,073美元)和专利成本(83,691美元),以加强业务数字产品供应和保护开发的知识产权。
截至2023年3月31日的财年,通过为活动提供资金而提供的现金净额为2,082,117美元。这包括与债务融资有关的偿还10,274,281美元, 由发行普通股与股权融资有关的收益8,393,361美元和相关现金成本 737,658美元抵消,以及从新贷款安排获得资金4,700,000美元。
截至2022年3月31日的财年,融资活动中使用的现金净额为6,368,315美元。这包括与债务融资相关的还款12,400,000美元,但与股权融资相关的普通股发行所得款项 为3,118,792美元,相关现金成本为50,765美元,再加上出售认股权证提供了另外2,963,658美元的现金 资金。
表外安排 表内安排
我们 没有表外安排对我们的财务状况、财务状况、收入或支出、经营结果、流动性、资本支出或资本资源的当前或未来产生重大影响。
合同义务
没有。
关键的会计政策以及重要的判断和估计
我们的管理层对我们的财务状况和经营结果的讨论和分析是基于我们根据美国公认会计原则(“美国公认会计原则”)编制的经审计的综合财务报表 。 这些综合财务报表的编制要求我们作出估计和假设,这些估计和假设会影响在合并财务报表之日报告的资产和负债金额、或有资产和负债的披露,以及报告期内报告的经营结果。我们的估计是基于我们的历史经验和我们认为在当时情况下合理的各种其他因素,这些因素的结果构成了对资产和负债的账面价值作出判断的基础,而这些资产和负债的账面价值从其他来源看起来并不明显。在不同的假设或条件下,实际结果可能与这些估计值不同。我们的重要会计政策在本招股说明书其他部分包括的综合财务报表的附注 中有更详细的说明。
业务描述
业务 概述
我们 是一家医疗技术公司,开发了SugarBEAT®,这是一种非侵入性、灵活的连续血糖监测系统,供糖尿病患者和任何希望确定影响其血糖曲线的因素的人使用。SugarBEat® 由一个带有传感器的一次性粘性皮肤贴片组成,该传感器连接到一个可充电的无线发射器。传感器 每隔5分钟测量一次血糖读数,并通过低能量蓝牙将数据发送到智能设备,如手机 (包括Android和iOS)。智能设备上的一个应用程序使用专有算法来显示真实的血糖值,在数据经过 校准后,至少使用一个手指棒校准。SugarBEat®的工作原理是将皮肤中的葡萄糖提取到与电极传感器直接接触的贴片中的一个腔中。数据记录在应用程序上,可以实时查看,还可以存储所有历史数据以供以后根据需要进行评估。我们相信,任何1型或2型糖尿病患者都可以使用SugarBEAT® ,任何希望确定影响其血糖曲线的因素的人也可以使用该产品。 因此,就胰岛素抵抗而言,他们的代谢健康状况。
| 47 |
2019年5月29日,我们宣布已获得行政长官批准,允许SugarBEat®在欧盟合法销售。CE认证 通过使用CE标志来披露,这是制造商对产品符合适用的欧洲法律要求的声明。欧洲的SugarBEat®临床试验计划评估了75名1型和2型糖尿病患者的525个病人日 ,并于2017年12月完成。CE批准是为SugarBEAT®设备 实现强制性符合性标志以允许其在欧盟合法销售的过程。这是制造商的声明,产品符合适用的欧洲法律的要求。这一批准需要对基础的国际标准化组织13485认证的质量管理体系进行年度审查。 认证于2021年11月成功续签。
我们 还向美国食品和药物管理局(FDA)提交了PMA(上市前批准)申请,其标签 与CE批准的标签相同,CE批准是一种用于糖尿病患者的血糖趋势辅助设备。PMA目前正在接受审查。
在2020年7月,我们向美国食品和药物管理局提交了一份PMA申请,要求使用SugarBEAT®作为血糖趋势指纹检测的辅助工具。 我们和其他申请者随后被美国食品和药物管理局告知,由于美国食品和药物管理局的器械和放射健康中心(CDRH)积极参与应对新冠肺炎疫情,审批过程可能会受到延误,这导致 工作人员被重新分配到其他与新冠肺炎相关的批准请求。2021年4月,FDA确认将重新审查PMA申请,2021年12月,FDA的生物监测研究部门对为支持PMA申请而提交的临床计划进行了审计。仅提出了483条意见,该公司于2022年1月提交了完整的答复。FDA随后计划在2022年第二个日历季度进行上市前检查,旨在涵盖FDA的 质量体系/当前的医疗器械良好制造规范(21 CFR Part 820)。
除此之外,Nemaura还建立了ProBEATTM,基于SugarBEAT®平台,根据FDA健康指南说明使用时,可被归类为 健康指南,以提供提示并教育用户影响其血糖曲线的因素。
我们 相信SugarBEAT®和基本的BEAT技术平台还有其他应用,其中可能包括:
| · | 医生和糖尿病专业人员可访问的网络服务器,以远程跟踪病情,从而降低医疗成本并更有效地管理病情; |
| · | 一个完整的虚拟医生,监测一个人的生命体征,并通过网络传输结果; |
| · | 其他使用BEAT技术平台来测量替代分析物的贴片,包括乳酸。这将是监测条件的一个步骤,特别是在医院环境中。目前,乳酸监测是用来确定职业运动员的相对健康状况的,我们已经完成了初步研究,证明BEAT技术应用于连续乳酸监测;以及 |
| · | 一种可广泛应用的连续温度监测系统。 | ||
在此产品开发期间,公司 经历了经常性亏损和运营现金流为负。在截至2023年3月31日和2022年3月31日的财年中,我们的产品销售收入分别为77,044美元和503,906美元,净亏损分别为14,143,735美元和13,886,805美元,来自运营活动的负现金流分别为8,451,781美元和6,504,041美元。如我们的财务报表所示,截至2023年3月31日,我们的现金余额为10,105,135美元,营运资本赤字为8,730,734美元,累计赤字为51,875,211美元,股东权益总额为11,814,198美元。由于我们历史上的经常性亏损、运营现金流为负以及巨额累积赤字,我们作为一家持续经营的企业继续经营的能力受到了极大的怀疑。见“风险因素-我们 有运营亏损的历史,我们的管理层得出结论,这些因素对我们作为持续经营的企业 继续经营的能力提出了实质性的怀疑。此外,我们的独立注册会计师事务所在其截至2023年3月31日的财政年度的审计报告中加入了一段说明,说明我们是否有能力继续作为一家持续经营的企业。“
虽然公司预计近期运营将继续出现亏损,但由于产品开发、监管活动、临床试验以及其他商业和产品开发相关费用的产生,这些亏损可能会很大,但在截至2021年12月31日的三个月期间,公司达到了一个重要的里程碑,公司开始向其英国被许可人交付其SugarBEAT®设备,使他们能够继续研究基于用户的反馈和证据,这些反馈和证据可能支持在英国的报销。
我们的 业务战略
我们 打算引领创新和有针对性的诊断医疗设备以及数据驱动的数字平台的发现、开发和商业化,以改善消费者福祉空间和医疗部门的疾病监测、管理和整体患者护理 。具体地说,我们打算利用我们的 技术平台,专注于监测可以无创地通过皮肤抽出的分子。除了葡萄糖,这些分子还可能包括乳酸监测和处方药监测,以及有助于诊断、预防或管理糖尿病等疾病的血液生物标志物。我们计划采取以下 步骤来实施我们广泛的业务战略。我们审批后的关键商业战略将首先在欧洲实施,然后 在中东和亚洲的部分地区,然后是美国,如下所示:
| 48 |
| - | 在英国和爱尔兰共和国将SugarBEAT®商业化。我们打算通过MySugarWatch®(以前称为达拉斯Burston ethitronix Limited)(“MSW”)在英国和爱尔兰共和国将糖商业化,我们与MySugarWatch Limited(“MSW”)签订了这两个国家的独家营销权协议。我们还于2018年5月与MySugarWatch(Europe)Limited(前身为Dallas Burston ethitronix(Europe)Limited)就所有其他欧洲地区签署了全面商业协议,作为平等合资协议的一部分。合资企业打算向糖尿病监测领域的一家或多家领先公司寻求转授许可权和机会,以利用它们的网络、基础设施和资源。 |
| - | 与其他方建立许可或合资协议以销售糖类BEAT® 在其他地区我们正在与世界各地的其他几个方面就销售SugarBEAT®设备的许可或合资协议进行详细的讨论和谈判,并已与TP MENA签署了海湾合作委员会的商业协议。TP MENA已向沙特阿拉伯监管机构提交了在KSA(沙特阿拉伯王国)注册SugarBEAT的申请。 |
| - | 寻求FDA PMA批准SugarBEat®.PMA的申请目前正在接受FDA的审查。 |
| - | 扩大这些疾病的适应症SugarBEat®:可以使用设备。我们认为,与在非急性环境中发现的用于监测其他疾病的设备相比,糖类BEAT®设备可能提供显著的好处。这包括用于竞技表演的乳酸监测,以及药物监测。我们已经完成了乳酸监测的初步概念验证,现在计划探索将健康应用于运动表现训练的商业化路线,并计划开展进一步的临床计划,以支持乳酸监测设备的临床使用。 |
| - | 通过我们的专有平台技术、收购和战略许可安排扩大我们的产品线。我们打算利用我们的专有平台技术来扩大我们用于诊断糖尿病和其他疾病的候选产品组合。这包括由我们的传感器在医疗和福利市场收集的数据驱动的数字平台,例如用于新陈代谢健康监测。此外,我们打算授权我们的产品,并获得与我们的研发以及业务重点和战略一致的产品和技术。这可能包括由传感器数据支持的用于管理慢性病的数字解决方案、用于改进糖尿病管理的药物输送产品,例如改进的胰岛素注射器系统,和/或用于糖尿病相关药物的组合药物产品。 |
产品 开发
管理层在诊断医疗设备的监管和临床开发方面拥有丰富的经验。我们打算利用诊断医疗器械领域的这一经验,尝试增加产品在多个地区获得批准的可能性。目前,糖尿病诊断医疗器械的整体监管流程与管理其他诊断设备的监管流程类似。 时间线比新药或完全侵入性诊断设备在临床试验时要短。我们已经成功地测试和评估了该设备的临床输出,在这种情况下,它可以根据通知的机构BSI批准CE批准的血糖水平的准确性和安全性。PMA(上市前批准)申请也已提交给FDA,目前正在审查中。我们将继续寻求与未来授权厂商和营销合作伙伴的合作,以实现我们的 商业增长里程碑。
| 49 |
产品开发和商业化 时间表
| 里程碑 | 目标开始日期 | 现状 |
| 完成1型和2型糖尿病受试者的临床研究,以确定最终的设备声明,并提交CE标志批准最终设备声明。 | 2017年7月 | 已完成 |
| 人体穿戴式发射器CE标志 | 2018年8月 | 已完成 |
| 美国FDA PMA提交 | 2020年6月 | 提交完成,FDA进行BIMO和GMP审核 |
| 在英国推出商业产品,随后在欧洲主要地区推出 | 2020年7月至9月 | 交错发射正在进行中 |
| ProBEAT的初步研究 | 2020年10月至12月 | 初步研究已完成。计划进行进一步的研究。 |
|
扩大商用传感器/贴片制造的规模。 扩大规模意味着我们已经开始着眼于在英国推出产品所需的更大规模 ,这与传感器的制造工艺有关。 |
2020年12月 | 正在进行中 |
| 扩大设备(发射机)制造规模 | 2020年12月 | 正在进行中 |
| 开始向英国被许可方交付产品 | 2021年12月 | 正在进行中 |
公司产品的市场机会
根据国际糖尿病联合会图集10TH:根据2021年版(“IDF”),约有5.37亿成年人患有糖尿病,占世界这一年龄段人口的10.5%。预计到2030年,这一数字将增至6.43亿(11.3%),到2045年将增至7.83亿(12.2%)。此外,据估计,全球有2.4亿人患有未确诊的糖尿病,这意味着几乎每两个患有糖尿病的成年人中就有一个不知道自己患有这种疾病。IDF确认,几乎90%的未确诊糖尿病患者生活在低收入和中等收入国家。
IDF公布的统计数据 证明,糖尿病是一个巨大的、日益严重的问题,尽管社会成本已经很高,但它们仍在继续上升。此外,以色列国防军还指出,欧洲的儿童和青少年1型糖尿病患病率最高,每年的发病率也是最高的。据报道,欧洲的糖尿病患者人均成本位居第二(3086美元),仅次于北美和加勒比海地区(8208美元)。
全球糖尿病统计数据
| 2021 | 2030 | 2045 | |
| 世界总人口 | 79亿 | 86亿 | 95亿 |
| 成年人口(20-79岁) | 51亿 | 57亿 | 64亿 |
| 糖尿病(20-79岁) | |||
| 流行率(%) | 10.5% | 11.3% | 12.2% |
| 糖尿病患者人数 | 5.366亿 | 6.427亿 | 7.832亿 |
| 糖尿病引起的医疗总支出(2021美元) | 9660亿美元 | 10,280亿美元 | 10.54亿美元 |
| 糖耐量受损“IGT”(20-79岁) | |||
| 流行率(%) | 10.6% | 11.0% | 11.4% |
| 糖耐量低减患者人数 | 5.41亿 | 6.227亿 | 7.303亿 |
| 1型糖尿病(0-19岁) | |||
| 患有1型糖尿病的儿童/青少年人数 | 120万 | - | - |
| 每年新诊断病例的数量 | 184,100 | - | - |
1型糖尿病,曾经被称为青少年糖尿病或胰岛素依赖型糖尿病,是一种慢性疾病,胰腺产生很少或没有胰岛素,胰岛素是一种允许糖(葡萄糖)进入细胞产生能量所需的激素。更常见的2型糖尿病发生在身体对胰岛素产生抵抗力或不能产生足够的胰岛素时。
多种因素可能导致1型糖尿病,包括遗传和接触某些病毒。虽然1型糖尿病通常出现在儿童或青春期,但它也可以在成年人中发展。
| 50 |
尽管积极的研究,1型糖尿病是无法治愈的,尽管它是可以控制的。通过适当的治疗,1型糖尿病患者有望比过去活得更长、更健康。1型糖尿病包括自身免疫性1型糖尿病(1a型),其特征是自身抗体阳性,以及特发性1型糖尿病(1b型),其自身抗体阴性,C肽含量 低。1型糖尿病(胰岛素依赖型)患者需要长期使用外源性胰岛素治疗,这些患者对血糖(SMBG)进行自我监测,以计算合适的胰岛素剂量。SMBG是通过使用手指棒采集的血液样本进行的,但频繁的SMBG并不能检测到血糖的所有显著偏差,尤其是在血糖水平迅速波动的患者中。
2型糖尿病,曾经被称为成人起病或非胰岛素依赖型糖尿病,是一种慢性疾病,会影响你身体代谢糖(葡萄糖)的方式,糖是你身体的主要燃料来源。对于2型糖尿病,你的身体要么抵抗胰岛素的影响,要么不能产生足够的胰岛素来维持正常的血糖水平。胰岛素是一种调节糖分进入细胞的激素。如果不治疗,2型糖尿病可能会危及生命。
2型糖尿病在成人中更为常见,随着儿童肥胖症的增加,2型糖尿病对儿童的影响越来越大。虽然目前还没有公认的治疗2型糖尿病的方法,但越来越多的证据表明,通过良好的饮食、锻炼和保持健康的体重可以有效地控制2型糖尿病。如果饮食和锻炼不能控制血糖,可能需要糖尿病药物或胰岛素治疗。
在欧盟和美国,每年都有数以百万计的患者接受糖尿病检测。进行检测的主要原因是检测和评估有糖尿病症状的患者的糖尿病。这些研究在对疑似但未经证实的糖尿病患者以及已确诊糖尿病并需要预后或风险信息的患者的初步评估中提供临床益处。
我们 相信,我们的市场机会与检测、诊断和治疗2型糖尿病的人数直接相关。IDF表明,连续血糖监测设备的总世界市场机会以数十亿美元计,并且随着糖尿病发病率的持续增长,预计每年都会增长。
我们 不相信有可能估计接受手指刺痛或其他类型的侵入性血糖监测的糖尿病患者的数量 。然而,我们不知道目前市场上有任何产品可以实现非侵入性连续血糖监测。 我们相信SugarBEAT®设备很容易被医学界采用,用于对患者进行持续评估。
我们 相信我们的非侵入性糖类®设备具有许多优点,可能是检测个体血糖水平不一致的理想设备 。我们相信CE批准的SugarBEAT®设备可能是一个强有力的解决方案,作为一种非侵入性的持续血糖监测设备,可以帮助糖尿病患者跟踪他们的血糖状况。虽然我们无法 估计我们的SugarBEat®设备可能占据的市场份额,但我们相信SugarBEat®设备有潜力夺取 血糖曲线和跟踪市场的相当大份额。
商业化 计划
在截至2023年3月31日的财年中,我们与我们的英国被许可方MSW合作,为他们的上市战略提供支持,该战略将我们的SugarBEAT®设备的使用融入到他们自己的品牌产品中。虽然新冠肺炎确实导致了城市生活垃圾用户评估计划的一些短暂延迟,但总体反馈是积极的,尽管城市生活垃圾购买 订单的预期时间表被延长,第一批订单是2021年4月下的5,000台SugarBEAT®发射器和200,000台SugarBEAT®传感器 。在截至2023年3月的财年中,我们的重点一直是支持我们的被许可方收集用户反馈,以支持传感器报销申请,我们将继续支持这些努力。在截至2023年3月31日的财年中,我们还采取了以下行动:
| · | 增加生产操作员人数,以促进产品制造 |
| · | 开始从以前为原材料下的远期订单中接收零部件/材料,以支持扩大规模并确保目前全球供应短缺的项目的库存,即微处理器等电子零部件。 |
| · | 继续与Benchmark Electronics Inc.合作,作为我们的CMO合作伙伴,通过承担电子PCBA(印刷电路板组装)批量认证运行,通过其在泰国的FDA批准的设施,促进未来发射机的批量生产 |
| · | 根据2021年12月从MSW收到的采购订单完成发射器的分阶段交付 |
| 51 |
我们还提前了 在美国发展市场能力的计划,包括:
| · | 2020年7月,我们向美国食品和药物管理局提交了一份PMA申请,申请将SugarBEAT®设备作为手指棒测量的辅助工具,用于血糖谱分析。我们和其他申请者随后被食品和药物管理局通知,由于疾控中心积极参与应对新冠肺炎引发的大流行,导致工作人员被重新分配到其他与新冠肺炎相关的批准请求,因此审批过程受到延误。2021年4月,FDA确认将重新审查PMA申请。 |
| · | 2021年12月,FDA的生物监测研究部门对为支持PMA申请而提交的临床计划进行了审计。只提出了一项483点意见,该公司于2022年1月提交了全面答复。 |
| · | FDA随后在2022年第二个日历季度进行了上市前检查,检查范围包括FDA的质量体系/当前的医疗器械良好制造规范(21 CFR Part 820)。再次提出了一项483点意见,并在规定的时间范围内对此作出了答复。该公司计划在适当时候提供进一步的材料更新。 |
此外,我们还将继续探索其他关键地理市场的商业化机会,并打算在出现问题时提供材料 更新。
竞争格局
据我们所知,目前市场上还没有其他竞争对手的设备,可以提供连续的血糖监测和分析, 非侵入性,传感器只需佩戴一天。我们相信,这使我们在一个可以瞄准糖尿病患者和糖尿病前期患者的市场上独树一帜。此外,我们认为这也可以用来改善体重管理和福祉市场的结果。有一些公司,如德克斯康和雅培,目前提供连续血糖监测(CGM)传感器,分别为连续佩戴10天和14天。如果这些公司符合以下条件,它们可以被视为未来的竞争对手:
| – | 开发和销售比我们当前和/或未来的产品更便宜或更有效的产品; |
| – | 运营更大规模的研发项目,或者拥有比我们多得多的财政资源; |
| – | 比我们更成功地发起或经受住实质性的价格竞争; |
| – | 从有限的现有人才库中更成功地招聘熟练的技术和科学工作者; |
| – | 更有效地协商第三方许可证和战略关系;以及 |
| – | 比我们更容易利用收购或其他机会。 |
我们 可能会在这一一般领域与这些公司和潜在的新来者争夺市场份额。这些潜在竞争对手可能单独或与其合作伙伴一起开发将与我们竞争的新产品,这些竞争对手可能会(在某些情况下确实会)运营更大的研发项目,或者拥有比我们更多的财务资源。
正如 指出的那样,虽然很难分析我们的主要竞争对手,因为目前还没有非侵入性的诊断医疗设备来持续监测血糖水平,但我们预计未来可能会有特定的公司与我们竞争。
监管要求
我们的设备已通过适用的电气安全测试,并已根据相关的欧洲指令、法规和标准进行了生物兼容性验证。如果引入新材料,它们将接受生物兼容性风险评估,并在必要时进行进一步测试。该设备和贴片的批次是为2014年11月至2015年12月期间进行的人体临床研究制造的。这是一个功能齐全的手表设备,通过电线连接到一个贴皮的传感器和电极上。在印度进行的后续研究 该设备于2016年2月获得CE认证。此后,该设备进行了升级,缩小了尺寸,包括增强的传感器系统,并允许通过穿戴在身上的发射器进行无线通信。这款小型化无线设备 于2019年5月获得CE认证,PMA已于2020年7月提交给美国FDA,目前正在审查中。申请CE认证需要公司拥有ISO13485质量管理体系,涵盖医疗器械的设计、开发和制造。Nemaura Medical没有此认证,而是根据与Nemaura Pharma Limited(“Pharma”)于2018年4月4日签订的服务合同条款,Nemaura Medical已将CE审批注册流程外包给Pharma。 Pharma是一家关联公司,由我们的首席执行官、董事会主席兼大股东DF.H.Chowdhury博士控制。根据服务合同的条款,Pharma已根据服务安排费用承担了注册产品以供CE批准的所有必要活动,而Nemaura Medical将保留CE标志的完整所有权和实益所有权,以及 所有相关知识产权,而除服务费外,无需支付任何进一步的费用或版税。
| 52 |
知识产权
我们 认为,与我们的技术相关的清晰和广泛的知识产权是长期成功的核心,我们打算进行相应的投资 。这适用于国内和国际专利覆盖范围、商业秘密和商标。
SugarBEAT®技术受我们的知识产权组合的保护,该组合包括已发布和正在申请的专利和商业秘密 ,涵盖一系列主张,包括以非侵入性方式测量从人体皮肤提取的葡萄糖的方法和设备、从皮肤提取葡萄糖的设备是稳定的方式、用于减少背景噪声信号的设备、将 原始数据转换为血糖值以校准设备的算法,以及 传感器中使用的酶溶液的配方和制备过程。
2014年5月8日,一家关联公司NDM技术有限公司以象征性代价将题为“分析物的累积测量”的英国专利申请1208950.4和国际专利申请PCT/GB2013/051322转让给皮肤病诊断有限公司(“DDL”) 。
未来还将申请更多与该设备和传感器相关的专利,提供新的知识产权保护。最近提交的一些专利和未来的一些专利可能会取代以前的知识产权。
此外, 我们保留与传感器制造工艺和传感器配方相关的大量商业秘密,这是我们花了几年时间开发的,事实证明,逆向工程具有挑战性,因为除了配方成分外,它还包括最终功能传感器特有的复杂组合中的 加工方法。将不会就该技术的这一方面申请专利,以避免技术诀窍的任何公开传播。
这些专利和专有技术涵盖了技术平台的各个方面。此外,BEAT®和SugarBEAT®商标已在全球多个主要地区注册。因此,对SugarBEAT®产品至关重要的所有知识产权均归我们所有,不需要支付版税。我们打算根据需要带头保护和/或起诉这些专利和专利申请 。我们打算随着开发的进展申请更多的专利,这些专利被认为对保护技术平台以及未来的修改和改进有价值。如果无法获得专利,或者现有专利被无法申请专利的新专有技术或技术开发所取代,则知识产权将仅限于专有技术和商业秘密, 这些将受到严格保护。
交易已提交、已授予和正在申请的秘密、商标和专利
| 知识产权:专利(核心权利要求)、专有技术、商标 | 到期日 | 授予/签发的司法管辖区 | 在哪些司法管辖区待决 | 正在进行的版税或里程碑付款 | ||||
| 专利:分析物的累积测量(1) | 2033年5月20日 | 澳大利亚、法国、德国、意大利、波兰、西班牙、荷兰、英国、中国、日本、美国、加拿大、阿联酋、巴西 | 卡塔尔 | 没有。内部发展 | ||||
| 皮肤准备贴片(2) | 2039年12月2日 | 英国 | 欧洲、美国 | 没有。内部发展 | ||||
| 技术诀窍:传感器配方和制造工艺 | 不适用 | 商业秘密 | 不适用 | 没有。内部发展 | ||||
|
商标: 节拍 |
续期将于2026年到期 | 英国、加拿大、中国、欧盟、印度、日本、挪威、俄罗斯、新加坡 | 马来西亚、巴西、墨西哥、瑞士、土耳其 | 没有。内部发展 | ||||
| 商标:SugarBEat | 续期将于2025年到期 | 英国、加拿大、澳大利亚、瑞士、中国、埃及、欧盟、以色列、印度、伊朗、日本、朝鲜、摩洛哥、墨西哥、挪威、新西兰、俄罗斯、新加坡、突尼斯、土耳其、美国 | 不适用 | 没有。内部发展 | ||||
|
代谢健康传感器(3)
|
2041年12月7日 | 不适用 | 英国 | 没有。内部发展 |
(1)本专利提供了一个公式,用于通过减去两个读数之间的差值来计算在定义的时间段内提取的葡萄糖量,从而实现快速检测,而无需耗尽被测量的分析物。
(2)本专利描述了一种用于为提取葡萄糖准备皮肤的设备和方法。
| 53 |
临床试验
我们的 临床测试由全球多个中心的合同临床研究机构进行,覆盖范围广泛 --包括亚洲和欧洲--并由我们的内部管理团队管理。
我们 在2016年6月与FDA举行了2次提交前会议,以确定临床路线图。因此,制定了详细的临床计划并在内部获得批准,并选择并审核了欧洲的一个临床地点,以开始使用 SugarBEAT®的身体穿戴发射器设备版本的临床研究。该研究已完成,并于2020年7月向FDA提交了PMA申请。
这些研究的数据也作为欧洲CE批准的一部分于2019年5月提交。
研发
在截至2023年3月31日和2022年3月31日的财年中,我们在研发方面的支出分别为1,538,615美元和1,556,988美元;管理层目前预计,下一财年在这方面的支出将保持合理一致。
制造业
经CE认证的医疗器械的制造和销售受国际标准化组织规定的指南控制和管理,更具体地说是ISO13485;糖业BEAT®将按照ISO13485质量标准制造和销售。
为了支持SugarBEat®在英国和欧盟的商业销售,我们与我们的制造合作伙伴Nemaura Pharma合作,扩大了各种SugarBEAT®组件的生产规模,并建立了最终组装和包装设施。作为这一过程的一部分,我们在英国拉夫堡大学科学与企业园(LUSEP)的现有总部场地内占用了更多空间,从而扩大了我们的制造和组装能力。
我们 已与各种制造合作伙伴签订了以下类型的协议:
| – | 传感器制造的制造协议 |
| – | 贴片制造的制造协议 |
| – | CGM发射装置制造协议和充电站制造协议 |
销售 和市场营销
2014年3月31日,与Dallas Burston Pharma签署了英国和爱尔兰共和国的独家营销权协议,Dallas Burston Pharma是一家总部位于泽西岛(海峡岛)的公司(DB Pharma)(随后于2018年更新,并于2021年再次更新,将公司名称更改为MySugarWatch Limited“MSW”),该公司在英国拥有药品营销业务,并展示了直接向全科医生营销处方药产品的非常成功的模式。我们收到了不可退还的预付款1百万英磅(按当时汇率计算为167万美元),作为回报,我们向MSW提供了在英国和爱尔兰共和国直接向消费者销售SugarBEAT®设备的独家权利,并通过全科医生的处方销售。 独家营销权协议的关键条款是在2015年8月签署的一份商业协议中签订的。本协议 已于2019年10月更新并重新发布,涵盖了新的知识产权/技术改进。
此外,我们于2018年5月与MySugar Watch(欧洲)有限公司(前身为达拉斯Burston ethitronix (欧洲)有限公司)订立了一项合资协议,根据协议,我们将平均分摊我们的SugarBEAT®系统在欧洲所有地区(英国除外)的销售成本和净利润,这是与MSW达成的一项单独协议的主题。本协议 已于2019年10月更新并重新发布,涵盖了新的知识产权/技术改进。2018年分别与TPMENA和Al-Danah Medical签署了海湾地区(GCC)和卡塔尔的商业协议。
| 54 |
监管事项
政府 法规
我们的业务受到广泛的联邦、州、地方和外国法律法规的约束,包括与环境保护、健康和安全有关的法规。一些相关法律尚未得到监管部门或法院的明确解释,其条款存在多种主观解释。此外,这些法律及其解释可能会更改,或可能颁布新的法律。
联邦和州政府机构继续对医疗保健行业进行严格的监管审查,包括加强民事和刑事执法工作。我们相信,我们的业务运营结构符合所有适用的法律 要求。但是,政府实体或其他第三方可能会以不同的方式解释这些法律,并断言 不同。我们在下面讨论与我们的业务最相关的法规和法规。
联合王国、威尔士和欧盟的规定
英国、威尔士、欧盟和其他国家的政府当局对医疗器械的研究、开发、测试、制造、标签、推广、广告、分销、抽样、营销和进口以及出口进行广泛的监管,包括贴片和其他药品。我们在英国和威尔士的身体佩戴的发射器设备将受到严格的监管,并在商业分销之前需要监管部门的批准。获得政府批准并遵守持续的法规要求的过程需要花费大量的时间和财力。 此外,法规、规则、法规和政策可能会发生变化,可能会发布新的法律或法规来推迟此类 审批。如果我们在产品开发过程、审批过程或审批之后的任何时候未能遵守适用的法规要求,我们可能会受到行政或司法制裁。这些制裁可能包括当局拒绝批准悬而未决的申请、撤回批准、临床搁置、警告信、产品召回、产品扣押、完全或部分暂停我们的业务、禁令、罚款、民事处罚或刑事起诉。任何机构的执法行动都可能对我们产生实质性的不利影响。
欧洲公共卫生委员会(“ECPH”)规定了新的医疗诊断设备的开发和商业化。投放到欧洲市场的任何医疗器械都必须符合相关法律,特别是医疗器械指令93/42/EEC、有源植入性器械指令(90/385/EEC)或体外培养使用设备 指令(98/79/EC)。从26这是到2021年5月,所有新批准的医疗器械必须符合医疗器械法规 (2017/745)。在制造/进口之前,必须确定相关设备是否符合上述任何指令。所有医疗器械必须满足上述指令中规定的基本要求。如果可用,可使用相关标准 来证明符合设备指令中定义的基本要求。
制造商还需要确定适当的符合性评估路线。对于符合指令93/42/EEC/法规2017/745的设备,除定制设备和用于临床研究的设备外,合格评估路线取决于设备的类别,将根据指令/法规中规定的某些规则确定。一旦确定了适用的类别或清单,制造商需要遵循适当的合格评定程序。根据设备类型的不同, 这可能要求制造商在将其产品投放市场之前,由通知机构对其质量体系和技术文档进行审查。通知机构是可以执行欧洲联盟认可的合格评定的第三方机构。被通知的机构在签发相关证书之前,需要确保已满足相关要求。制造商 然后可以在其产品上放置CE标志,以证明符合要求。
CE批准是为SugarBEAT®设备实现强制性符合性标志的过程,以允许其在欧盟合法销售。这是制造商的声明,产品符合适用的欧洲法律的要求。SugarBEAT®Device CE提交和审批流程 涉及以下内容:
1.根据欧洲指令描述的某些类别,该设备被归类为 ,I类产品风险较低(例如创可贴),而III类设备风险最高。这些类别为I类、IIa类、IIb类和III类。风险基于产品或其使用出现问题时对患者的潜在伤害。SugarBEat®设备被归类为IIb设备。
2.将准备一份‘技术文件’ ,其中包含证明该产品符合欧洲指令的基本要求所需的所有信息。这包括与设备的性能和安全相关的信息,如产品规格、标签、使用说明、风险分析以及与支持产品声明的产品相关的特定测试信息/临床证据。
3.技术文件中包含的临床证据预计将证明该设备是安全的,并满足规定的性能要求。此临床证据可以是文献数据的形式,其中存在大量使用相同的葡萄糖提取和测量技术的已发表数据(尽管采用不同的设备格式),或者来自使用SugarBEAT®设备进行的实际临床研究的数据。 第一次CE标记提交基于文献评估3研发该方公布了可在 公共领域获得的临床数据。最终提交的CE标志基于设备的临床性能,基于本文早些时候描述的临床研究。临床数据显示,SugarBEAT®设备可以通过每5分钟测量一次血糖来预测受试者的血糖水平。临床试验数据表明,SugarBEAT®设备的血糖趋势可用于补充正常手指的点刺测量 。
4.技术档案 已由独立检查员(通知机构)进行评估,由主管当局(联合王国的药品和保健产品管理署)进行监管。被通知的机构(已被成员国认可以确定医疗器械是否符合欧洲医疗器械指令的欧盟组织),然后将批准通知欧洲公共卫生委员会(ECPH),被通知的机构将向公司颁发证书 ,然后我们将能够将CE标志应用于该设备。并合法地提供该产品在欧洲经济区(EEA)销售。 CE标志已于2019年5月颁发,该公司现在可以在欧盟提供该设备的商业销售。
| 55 |
5.技术文件 于2018年8月开始审查,2019年5月收到最终审查和签字。自CE认证获得批准以来,我们已经对我们的ISO 13485质量管理体系进行了例行检查,以保持我们的CE认证。还向通知机构提交了附录,并获得批准,以便将发射器连接到的智能设备应用程序的iOS版本包括在经批准的CE标志设备中。
美国食品和药物管理局对医疗器械的监管
美国食品、药物和化妆品法案(“FDCA”)和FDA的法规为人类使用的医疗器械建立了一个全面的监管体系。SugarBEAT®是一种医疗设备,受这些以及其他联邦、州、地方和外国法律和法规的约束。FDA负责执行管理美国医疗器械的法律和法规。
FDA根据医疗设备的风险级别以及确保设备安全和有效性所需的控制类型,将医疗设备分为三类(I类、II类或III类)之一。课程分配是确定在美国上市前所需的 上市前提交或申请类型(如果有)的一个因素。SugarBEat®属于 第三类。
| – | I类设备风险较低,不能维持生命或维持生命。大多数第I类设备仅受“一般控制”(例如,禁止掺假和贴错品牌、注册和上市、良好制造规范、标签和不良事件报告)的约束。一般控制是适用于所有类别的医疗器械的基线要求。) |
| – | 第二类装置风险适中,仅靠一般控制不足以提供安全和有效性的合理保证。第II类设备同时受到一般控制和“特别控制”(如特殊标签、符合性能标准和上市后监督)的约束。除非获得豁免,否则II类设备在上市前通常需要FDA批准,通过上市前通知(510(K))流程。) |
| – | 第三类设备的风险最高。这些设备通常是维持生命的、维持生命的,或者用于对防止损害人类健康或存在潜在的不合理的疾病或伤害风险具有重要意义的用途。第III类装置是指仅有一般控制本身是不够的,而且没有足够的信息来确定采用特别控制将提供安全和有效性的合理保证的装置。III类设备受到一般控制,通常需要FDA批准PMA申请才能上市。 | |
除非 免除上市前审查要求,否则医疗设备在美国进行商业营销、分销或销售之前必须获得FDA的营销授权。获得营销授权的最常见途径是510(K)许可 和PMA。在2016年6月作为提交前会议的一部分与美国食品和药物管理局进行了初步讨论后,确定了糖类BEAT®的途径将是PMA批准。
售前审批途径
PMA审批流程需要对设备的安全性和有效性进行独立演示。PMA是FDA要求的最严格的设备营销申请类型。PMA的批准是基于FDA的确定,即PMA包含足够的 有效科学证据,以确保该设备对于其预期用途是安全有效的。PMA应用程序通常包括有关该设备的大量信息,包括在该设备上进行的临床测试结果和制造工艺的详细说明。
在PMA申请被接受审查后,FDA开始对提交的信息进行深入审查。FDA的规定规定了180天的时间来审查PMA并做出决定;但实际上,审查时间通常更长(例如1-3年)。在此 审查期内,FDA可要求提供更多信息或对已提供的信息进行澄清。此外,在审查期内,可能会召集FDA以外的专家组成顾问小组,审查和评估支持该应用的数据,并就该数据是否合理地保证该设备对于其预期用途而言是安全有效的,向FDA提供建议。此外,FDA通常将对制造设施进行审批前检查,以确保符合质量体系法规,该法规对医疗器械的设计和制造 提出了全面的开发、测试、控制、文档和其他质量保证要求。
根据审查情况,FDA可以(I)发布批准PMA的命令,(Ii)发布声明PMA为“可批准”的信函(例如,需要提供较小的补充信息),(Iii)发布声明PMA为“不可批准”的信函,或(Iv)发布拒绝PMA的命令。在FDA发布批准PMA的命令之前,公司不得销售接受PMA审查的设备。作为PMA批准的一部分,FDA可以施加批准后的条件,以确保该设备的持续安全性和有效性,其中包括限制标签、促销、销售和分销,并要求收集额外的临床数据。如果不遵守批准条件,可能会导致严重不利的执法行动,包括撤回批准。
| 56 |
对PMA批准的设备进行的大多数 修改,包括设计、标签或制造流程的更改,在实施之前都需要事先获得批准。事先通过提交PMA附录获得批准。支持PMA补充剂所需的信息类型和FDA审查PMA补充剂的时间因修改的性质而异。
2020年2月,Nemaura宣布,在与FDA讨论后,确定Nemaura可以在未经FDA批准的情况下在美国销售其CGM产品和数字服务产品,作为非医疗福利应用程序。Nemaura进一步宣布,它 打算于2020年10月至12月在美国以proBEAT‘品牌推出这款产品。该产品使用户能够佩戴CGM设备,数据将从该设备发送到Nemaura在云中的 服务器,从那里数据将被处理,为用户提供教育材料和洞察可能影响他们的血糖水平的因素和健康生活方式和饮食的提示,以期帮助糖尿病前期患者和糖尿病患者过上更健康的 生活。2020年12月开始在美国推出限量产品,使潜在客户能够使用 ProBEAT™与针对糖尿病患者的数字减肥计划一起注册他们的兴趣,品牌为BEATdiabets.life。
临床试验
在美国,医疗器械的临床试验受FDA的调查器械豁免(“IDE”)法规管辖。该规定 赋予临床研究发起人重大责任,包括但不限于:选择合格的研究人员、监督试验、提交所需报告、维护所需记录、确保研究人员获得知情同意、遵守研究方案、控制研究设备的处置、提交所需报告等。
重大风险设备(例如,植入物、用于支持或维持人类生命的设备、在诊断、治愈、减轻或治疗疾病或以其他方式防止损害人类健康方面具有重要意义的设备)的临床试验在开始试验之前需要FDA和机构审查委员会(IRB)的批准。FDA通过提交IDE申请获得批准。 非重大风险(“NSR”)设备(即不符合法规对重大风险设备的定义的设备)的临床试验在启动前只需获得IRB批准。临床试验赞助商负责对临床研究是否存在重大风险或NSR进行初步确定;但是,评审IRB和/或FDA可能会审查该决定并不同意该确定。
IDE应用程序必须有适当的数据支持,如性能数据、动物和实验室测试结果,表明在人体上评估该设备是安全的,并且临床研究方案是科学合理的。不能保证提交IDE将导致能够开始临床试验。此外,在试验开始后,如果FDA得出结论认为临床受试者面临不可接受的健康风险,则可暂停试验或终止试验。
如上所述,FDA可能会要求一家公司在上市后环境中收集设备的临床数据。
收集此类数据可能是PMA批准的条件之一。FDA还有权在某些设备获得批准或批准后的任何时间通过信函下令对这些设备进行上市后 监控研究。
无处不在的 和FDA持续的监管
设备投放市场后,无论其分类或上市前途径如何,通常都适用许多FDA额外要求 。这些措施包括但不限于:
| – | 设施登记和设备清单要求; |
| – | 质量体系规定(“QSR”),规定成品设备的设计、制造、包装、标签、储存、安装和维修所使用的方法、设施和控制; |
| – | 标签要求,要求在器械标签和标签中包括某些内容,一般要求医疗器械的标签和包装包括唯一的器械识别符(“UDI”),还禁止宣传产品用于未经批准或未经批准的用途,即“标签外”用途; |
| – | 医疗器械报告(MDR)法规,要求制造商和进口商在其设备可能导致或促成死亡或严重伤害,或发生故障而很可能导致或促成死亡或严重伤害时,向FDA报告;以及 |
| – | 更正和移除报告条例,该法规要求制造商和进口商在采取行动以减少设备对健康构成的风险或补救可能对健康构成风险的联邦食品、药物和化妆品法案的情况下,向FDA报告召回(即更正或移除);制造商和进口商必须保留他们认为不应报告的召回记录。 |
| 57 |
FDA通过检查和市场监督来执行这些要求。不遵守适用的法规要求可能导致FDA采取执法行动,其中可能包括但不限于以下制裁:
| – | 无标题信件或警告信; |
| – | 罚款、禁令和民事处罚; |
| – | 召回或扣押我们的产品; |
| – | 限产、部分停产或者全面停产的; |
| – | 拒绝510(K)审批或新产品上市前审批的请求; |
| – | 撤回已经批准的510(K)许可或上市前批准;以及 |
| – | 刑事起诉。 |
我们 将接受FDA以及其他监管机构的突击检查,以监督适用的州公共卫生法规的执行和 遵守。这些检查可能包括我们供应商的设施。
英国、威尔士和欧盟的其他法规
医疗保健 报销
在我们开展业务的许多国家/地区(包括英国和威尔士),政府和私营部门限制医疗成本增长的举措(包括价格监管、竞争性定价、覆盖范围和 支付政策以及管理式医疗安排)仍在继续。这些变化导致市场更加重视提供更具成本效益的医疗产品。政府 计划、私人医疗保险和管理式医疗计划试图通过限制他们为特定程序或治疗支付的报销金额来控制成本 。这导致客户对产品的价格敏感度越来越高。 一些第三方付款人还必须批准新的或创新的设备或疗法的承保范围,然后才能向使用医疗设备或疗法的医疗保健提供者报销 。即使新的医疗产品可能已获准用于商业分销,但在获得政府和私人第三方付款人的报销批准之前,我们可能会 发现对该产品的需求有限。
环境法规
我们 还受到英国和威尔士国内外的各种环境法律和法规的约束。与许多其他医疗设备公司一样,我们的业务涉及使用受环境法监管的物质,包括危险废物,主要是制造和灭菌过程。我们预计,遵守环境保护法不会对我们的综合运营结果、财务状况或现金流产生重大影响。然而,这些法律和法规都可能发生变化,我们无法预测此类变化可能对我们的业务、财务状况或运营结果产生什么影响(如果有的话)。
外国监管
无论我们是否获得产品的监管批准,我们都必须获得外国可比监管机构的批准 才能开始在这些国家进行临床试验或销售该产品。审批流程因国家/地区而异, 时间可能比EC审批所需的时间长或短。管理临床试验、产品许可、定价和报销的要求也因国家而异。
此外,除美国以外的大多数国家/地区都需要对价格进行监管审批。我们面临的风险是,监管审批流程产生的价格不足以为我们或我们的合作者带来可接受的回报。
欧盟通用数据保护条例
欧盟一般数据保护条例(GDPR)自2018年5月25日起在所有欧盟成员国生效,取代了 之前的欧盟数据隐私法。虽然现有的一些基本原则将保持不变,但《全球数据保护框架》对数据控制者和数据主体的权利引入了新的义务,其中包括:
| – | 问责制和透明度要求,这将要求数据管制员证明和记录遵守GDPR的情况,并向数据主体提供更详细的处理信息; |
| – | 增强的数据同意要求,其中包括与处理敏感数据有关的“明确”同意; |
| – | 在开发任何新产品或服务时考虑数据隐私的义务,并限制收集、处理、存储的信息量及其可获得性; |
| – | 对使用数据分析数据对象的限制; |
| – | 应要求向资料当事人提供可使用格式的个人资料,并在某些情况下删除个人资料;以及 |
| – | 报告违规行为,不会有不适当的延误(可行时为72小时)。 |
| 58 |
GDPR还对违反要求的行为引入了新的罚款和处罚,包括对严重违规行为的罚款,最高可达全球年收入的4%或2000万欧元,以及对其他指定违规行为的罚款,最高可达全球年收入的2%或1000万欧元(以最高者为准)。GDPR确定了在施加罚款时要考虑的要点清单(包括侵权的性质、严重性和持续时间)。
公司已评估GDPR对其持有的所有个人数据的影响,并已实施措施以确保个人数据 应:
| - | 以合法、公平和透明的方式处理与数据主体有关的信息。 |
| - | 为特定、明确和合法的目的而收集的,并且不以与这些目的不相容的方式进一步处理。 |
| - | 充分、相关且仅限于与处理它们的目的相关的必要内容。 |
| - | 以一种允许识别资料当事人的形式保存,时间不超过处理个人资料所需的时间。 |
| - | 以确保个人数据适当安全的方式处理,包括防止未经授权或非法处理以及使用适当的技术或组织措施防止意外丢失、销毁或损坏。 |
| - | 保持准确和最新,并采取一切合理步骤,确保在考虑到处理个人数据的目的后,不准确的个人数据立即被删除或更正。 |
在本公司目前的发展阶段以及现阶段的收入前,所持有的数据范围以及GDPR的影响都是有限的。GDPR的更多应用将在公司进一步发展之前进行评估和实施,以保证 需要额外的GDPR措施。随着公司产品商业化进程的推进,GDPR对公司的影响程度将增加 ,这将需要对公司的程序和政策进行额外的更改,这可能会对运营和合规成本产生不利影响 。此外,还存在措施不能正确实施或企业内部人员不能完全遵守新程序的风险。如果违反这些措施,公司可能面临重大的行政和金钱制裁以及声誉损害,这可能对其运营、财务状况、 和前景产生重大不利影响。
人力资本管理
我们 相信多样化的员工队伍对我们的成功非常重要。我们将继续专注于女性和代表性不足人群的招聘、留住和晋升,并培养包容和多样化的企业文化。在未来,我们打算继续 评估我们在管理业务中使用的人力资本措施或目标,例如我们在发展、吸引和留住员工以及保持员工队伍多样性方面雇用或寻求雇用的因素。
我们业务的成功从根本上与我们员工的福祉息息相关。因此,我们致力于保障员工的健康、安全和健康。我们为我们的员工提供各种灵活、方便的健康和健康计划,包括提供保护和安全的福利,以便他们可以安心应对可能需要离开工作时间或影响其财务状况的事件;通过提供工具和资源来帮助他们改善或保持健康状况并鼓励他们参与健康行为来支持他们的身心健康;并且在可能的情况下提供选择,以便他们 可以定制他们的福利以满足他们的需求和家庭的需要。
我们 还提供强大的薪酬和福利计划来帮助满足员工的需求。我们相信,我们与员工保持着令人满意的工作关系,没有发生过任何劳资纠纷。截至2023年3月31日,我们的工资单上有38名员工 ,相当于大约36名全职员工。
| 59 |
组织结构
我们是一家控股公司,拥有一家诊断医疗器械公司100%的股份,该公司专门从事发现、开发和商业化专业医疗器械 。我们是根据内华达州的法律于2013年12月24日组织的。我们拥有成立于2013年12月11日的英格兰和威尔士公司Dermal Diagnotics(Holdings) Limited的100%股权。皮肤诊断(控股)有限公司拥有成立于2009年1月20日的英格兰和威尔士公司Demal Diagnostics Limited(“DDL”)以及2011年1月12日成立的英格兰和威尔士公司 Trial Clinic Limited(“TCL”)的100%股份。
下图显示了Nemaura截至2023年8月3日的公司结构:

在截至2021年3月31日的财政年度内,董事会评估了集团组织结构的充分性,并得出结论: 不再需要中介控股公司Region Green Limited,因为该实体自成立以来实际上一直处于休眠状态 ,不再需要维持。因此,决定应解除Region Green Limited的清盘,将Region Green Limited持有的资产转移至Nemaura Medical Inc.,随后Region Green Limited将被解散。
资产转移于2021年3月5日进行,Region Green Limited于2021年4月23日正式解散。
2013年12月,我们对公司进行了重组,并将其重新注册为美国国内公司。完成公司重组是为了维护英格兰和威尔士税法下的税收优惠,以造福于Dermal Diagnostics Limited和Trial Clinic Limited的股东。
DDL是一家诊断医疗设备公司,总部位于英国莱斯特郡拉夫堡。DDL成立于2009年1月20日,致力于诊断医疗设备的发现、开发和商业化。该公司最初的重点一直是开发一种新型的CGM设备。
最近的公司历史
解雇首席财务官
自2022年7月1日起,公司解雇了公司的首席财务官,并已开始寻找美国的继任者。在选定继任者之前,公司的总裁和首席执行官将担任公司的首席财务和会计 官,公司的财务团队将继续支持公司的会计和财务 报告合规要求。
商业交付
2021年12月,随着SugarBEAT®非侵入性血糖监测仪(“CGM”) 首批交付给英国授权厂商MySugarWatch Limited(“MSW”),标志着公司发展历程中的一个重要里程碑。MSW开发了基于订阅的糖尿病指导和管理服务,该服务将与CGM一起提供,主要针对2型糖尿病患者,并继续进行 研究,以支持英国传感器和糖尿病管理计划的全额报销。
交付反映了与MSW达成的与MSW在2021年早些时候下的初始订单相关的分阶段交付时间表,因此公司开始 确认收入。
此外,2021年9月24日,本公司与MSW的姊妹公司MySugarWatch DuoPack Limited(“MSW-DP”)签订了一份许可、供应和分销协议,根据该协议,MSW-DP将免费向CGM传感器提供广泛用于2型糖尿病患者的某些药物。这些药物于2022年第四季度在欧洲和英国到期,并将于2023年在美国到期。 根据协议条款,向MSW-DP出售传感器的协议价格为美国市场每盒五个传感器20美元,在欧洲和英国,自产品推出起前12个月为12.50欧元,此后每盒四个传感器10欧元。Nemaura在大规模生产中预计每个传感器的商品成本为1美元。截至2022年1月,在欧盟和英国的联合主要领土上,每月有超过200万张处方 用于这些药物。
管理层现在专注于完成剩余的英国授权商的初始订单,并支持MSW在英国的推出,同时还开发公司的能力,通过使用我们的BEAT平台在其他地理市场开发和服务新的业务渠道。这包括将2021年底推出的消费者代谢健康服务Miboko扩展到美国各地的雇主和保险公司。
自动柜员机服务
于2021年7月,本公司与H.C.Wainwright&Co.,LLC(“代理”)订立市场发售协议(“自动柜员机协议”),根据该协议,本公司可不时向或透过代理股份发售本公司普通股。于2022年4月1日,本公司与代理商订立自动柜员机协议修订案(“修订案”),据此,订约方 同意将自动柜员机协议中“登记声明”一词的定义涵义扩大至自2022年4月1日起及其后的时间,包括于2022年3月16日向美国证券交易委员会提交并于2022年3月28日由美国证券交易委员会宣布生效的S-3表格新货架登记声明(档号333-263618)。修正案未对自动取款机协议进行其他更改 。
透过代理人 发售普通股将根据新注册声明及根据 提交予美国证券交易委员会的相关招股说明书补编作出,根据该补充说明书,本公司发售其普通股,总发行价最高可达3,000,000美元。尽管如此,鉴于我们未能及时提交截至2022年12月31日的Form 10-Q季度报告,我们在2024年3月31日之前不再有资格 使用新的注册声明从自动取款机中减持股票。
与EVERSANA达成初步协议
2022年9月27日,公司与EVERSANA签订了一项初步协议,就公司在美国推出BEAT糖尿病计划的战略进行合作。
修正住宅区资本担保本票 附注
于2021年2月8日,本公司、本公司全资附属公司Dermal Diagnostics Limited(“Dermal Diagnostics”)及本公司全资附属公司Trial Clinic Limited(“Trial Clinic”及本公司与本公司及Demal Diagnostics共同发行) 向Uptown Capital,LLC(“Uptown”)(“Uptown Note”)发行本金为24,015,000元的有担保承付票(“Uptown Note”)。Uptown Note的原始发行折扣为400万美元。此外,本公司同意向Uptown支付15,000美元,以支付Uptown的法律费用、会计成本、尽职调查、监测和与买卖Uptown Note有关的其他交易成本,所有金额均包括在Uptown Note的初始本金余额中。因此,Uptown Note的收购价为20,000,000美元。住宅区票据的原始到期日是在住宅区票据的购买价交付日期 后24个月。
2022年10月21日,本公司与本公司、皮肤诊断公司、试验诊所和住宅区签订了日期为2022年10月21日的担保本票修正案 。根据修订条款,本公司与住宅区同意将住宅区票据的到期日延长至2024年7月1日。作为代价 ,本公司同意向Uptown支付5%的延期费用,金额为Uptown票据未偿还余额的5%, 导致应对Uptown的负债增加813,834美元。
本公司及住宅区此前已同意于2022年6月至2023年2月期间,将每月最高赎回金额由2,000,000美元减至500,000美元,减幅仍然有效。根据修订条款,本公司与住宅区同意自2023年3月起至全额支付住宅区票据为止的期间内,将每月最高赎回金额由2,000,000美元减至1,000,000美元;但前提是在发生违约事件时,每月最高赎回金额将自动增加至2,000,000美元。
| 60 |
获得注册直接发行和私募发行及相关附表14C(信息声明)多数已发行和未发行证券的股东批准
2023年1月27日,合计13,596,205股公司普通股(约占公司总投票权的56.4%)的 持有人批准了(I)以每股1.75美元的价格向登记直接发行的投资者发行和出售至多4,796,206股公司普通股(“股份”),交易总额最高可达8,393,360.50美元,以及(Ii) 认股权证(“认股权证”),以购买最多4,796,206股普通股。以每股2.00美元的行使价,以同时私募的方式,以高达9,592,412美元的总收购价 。除其他事项外,该等股东亦批准(I)证券购买协议、配售代理协议(“配售代理协议”) 及认股权证的格式及签立;(Ii)提交招股说明书补充上市说明书以供登记直接发售股份(“招股说明书副刊”);(Iii)提交登记说明书(“转售登记说明书”)以登记认股权证相关股份的转售;及(Iv)向纳斯达克资本市场(“联交所”)提交申请或其他有关文件(S),以使根据招股章程补充及转售注册说明书将分别发售的认股权证相关股份及 股份在联交所上市(“上市申请”)。
2023年4月7日,本公司 向美国证券交易委员会提交了初步附表14C(信息声明),随后向本公司 股东邮寄最终附表14C,通知他们(而不是征求或请求股东批准)持有本公司已发行和已发行有投票权证券 多数的股东批准发行和出售4,797,206股普通股和认股权证,以在同时进行的定向增发中购买同等数量的普通股。
完成840万美元的认股权证登记直接发售和同时私募
于2023年1月31日,本公司根据与两名认可机构投资者订立的证券购买协议完成结算,以S-3表格以登记直接发售方式购买其普通股4,796,206股,并同时私募认购其普通股4,796,206股,行使价为每股2美元。一股普通股和一份认股权证的合并收购价为1.75美元,总收益为8,393,360美元。本公司同意于发售日期起计45天内提交回售登记声明以登记认股权证相关股份的回售,以使该等回售登记声明在发售结束后90天内生效。
未能及时提交表格10-Q的通知
2023年2月23日,纳斯达克证券市场有限责任公司(“纳斯达克”)上市资格部通知本公司,由于未能及时提交截至2022年12月31日的10-Q表格季度报告(“10-Q表格”),纳斯达克未能遵守纳斯达克根据“纳斯达克上市规则”第5250(C)(1)条(“该规则”)继续上市的要求。随后, 2023年2月24日,公司提交了10-Q表格,并重新遵守了规则。
2023年2月27日, 公司收到纳斯达克的通知,根据2023年2月24日的Form 10-Q备案文件,纳斯达克确定公司 遵守规则,此事已结案。
独立注册会计师事务所辞职
2023年2月23日,迈耶·霍夫曼·麦肯会计师事务所(“MHM”)辞去本公司独立注册会计师事务所的职务,自本公司提交截至2022年12月31日的Form 10-Q季度报告后生效。该公司于2023年2月24日提交了截至2022年12月31日的季度报告10-Q。他说:
MHM关于截至2022年和2021年3月31日的财政年度及截至2021年3月31日的财务报表的报告不包含不利意见或免责声明,也没有对不确定性、审计范围或会计原则进行保留或修改,但此类报告对公司作为持续经营企业的能力表示了极大的怀疑。在截至2022年和2021年3月31日的财政年度以及截至2023年2月23日的财政年度内,与MHM在会计原则或惯例、财务报表披露或审计范围或程序方面没有任何分歧,如果这些分歧没有得到解决而令MHM满意,将导致MHM参考与其在该等期间的 公司财务报表报告相关的分歧主题。
在截至2022年和2021年3月31日的财政年度和截至2023年2月23日的财政年度内,不存在S-K法规第304(A)(1)(V)项中所述的“应报告事项” ,但本公司每份(I)截至2022年12月31日的10-Q表格季度报告、(Ii)截至2022年9月30日的10-Q表格季度报告(第1号修正案)中披露的重大弱点除外。和(Iii)截至2022年6月30日的季度报告Form 10-Q/A(修正案1)。
本公司向MHM提供了上述披露的副本,并要求MHM向本公司提供致美国证券交易委员会的信函,声明是否同意MHM向本公司提供并于2023年3月1日提交给美国证券交易委员会的声明。
任命独立注册会计师事务所
2023年5月25日,公司董事会审计委员会任命温伯格公司(“温伯格”)为公司新的独立注册会计师事务所 。于截至2023年及2022年3月31日止财政年度及截至2023年5月25日止财政年度内,本公司或代表本公司行事的任何人士概未就S-K规例第304(A)(2)(I)及(Ii)项所载任何事项或须予报告的事件征询温伯格的意见。
| 61 |
未能满足纳斯达克上市证券最低市值和最低投标价格要求的通知
2023年04月3日,本公司 收到纳斯达克上市资格部(“纳斯达克员工”)的书面通知(“纳斯达克上市公告”) ,指出本公司不符合“纳斯达克上市规则”第5550(B)(2)条关于继续在纳斯达克资本市场上市的最低上市证券市值3,500万美元的规定。违规通知不会对公司普通股在纳斯达克资本市场的上市或交易产生立竿见影的影响,交易代码为“NMRD”, 公司目前正在监测其上市证券的市值,并在适当时评估其替代方案,以 解决不足并重新遵守此规则。
纳斯达克上市规则“(以下简称”规则“)要求上市证券持有的上市证券的最低市值为3,500万美元,根据纳斯达克员工在过去30个工作日对本公司上市证券的最低市值进行的审查,本公司 不再符合这一要求。但是,规则还为公司提供了180个日历日的合规期,即到2023年10月2日,在此期间重新获得合规性。如果在此合规期内的任何时间,公司的最高合规额在至少连续10个工作日内以3,500万美元或更高的价格收盘,纳斯达克员工将向公司提供书面合规确认, 此事将被了结。不能保证本公司将能够重新遵守MVLS规定,即使 其继续遵守其他上市要求。
2023年4月7日,本公司 收到纳斯达克员工的书面通知(《投标价格通知》),指出本公司未遵守《纳斯达克上市规则》第5550(A)(2)条规定的1.00美元的最低投标价格要求,以便继续在纳斯达克资本市场上市。 不符合规定的通知不会立即影响本公司普通股在纳斯达克资本市场的上市或交易(代码为NMRD),本公司目前正在监测其普通股的收盘投标价格,并在适当时评估其替代方案,以解决不足,并重新遵守这一规则。
纳斯达克上市规则 要求上市证券维持每股1.00美元的最低买入价,而根据最近30个工作日的收盘价 ,公司不再满足这一要求。投标价格通知指出,将向公司提供180个日历 天,或直到2023年10月3日,在此期间重新获得合规。如果在此期间的任何时间,纳斯达克普通股的投标价格连续至少10个工作日收于每股1.00美元或以上,纳斯达克工作人员将向本公司 提供书面确认符合要求,此事将结束。
或者,如果本公司 未能在180个历日期限届满前重新遵守规则5550(A)(2),但满足公开持有股票市值要求和纳斯达克市场首次上市的所有其他适用标准(最低投标价格除外),并提供书面通知,表明其打算在第二个合规期内通过进行反向股票拆分来弥补不足之处,则如有必要,本公司可获得额外180个日历日,以便 恢复遵守规则5550(A)(2)。
不能保证 即使公司继续遵守其他上市要求 ,公司也能够重新遵守投标价格要求。本公司正考虑为回应投标价格通知而可能采取的行动,以重新遵守持续上市规定,但目前尚未就回应作出任何决定。
新冠肺炎的影响
包括新冠肺炎在内的地区或全球卫生大流行可能会严重影响我们的业务、运营业绩和财务状况。 区域或全球卫生大流行可能会对我们的业务产生实质性的不利影响,具体取决于其持续时间和严重程度。 例如,新冠肺炎大流行对全球经济造成了许多影响,世界各地的政府当局已经实施了 措施来减少新冠肺炎的传播。这些措施,包括政府当局建议或要求的停工和“就地避难”命令,或由公司以其他方式选择作为预防措施,对劳动力、客户、消费者情绪、经济和金融市场造成了不利影响,加上消费者支出的减少,导致了我们许多市场的经济低迷。
由于 新冠肺炎疫情的影响,我们评估并执行了可用的步骤,以确保能够为我们的员工提供保护,并在可能的情况下鼓励远程工作,并在工作场所内任何无法远程完成的工作中遵循所有政府建议和指导 。到目前为止,这一过渡对我们的员工工作效率影响很小 ,对我们的业务造成的中断也很有限。虽然与新冠肺炎相关的限制已基本取消,但我们将继续 评估情况,包括遵守任何政府施加的限制,视情况而定。
目前,新冠肺炎对我们业务的潜在影响仍存在一些不确定性。由于感染可能会继续 变得更加普遍,我们可能会对我们的业务、财务状况和运营结果产生严重的负面影响。 就新冠肺炎疫情对我们的业务和财务业绩产生不利影响的程度而言,它还可能增加本招股说明书中“风险因素”一节中描述的许多其他风险。
属性
我们已在美国注册了公司办事处,地址为57 West 57这是纽约曼哈顿大街,邮编:10019。我们在英国莱斯特郡拉夫堡大学科学与企业园(LUSEP)的两个地点设有办公室和实验室。每月租金总额约为51,000美元。目前,所有租约均按12个月滚动租期运营。不同租约的条款提供了中断选项,允许业主和租户在提供不少于一个月的事先书面通知的情况下终止 。
法律诉讼
我们不知道 针对我们或我们的子公司的任何重大的、正在进行的、未决的或威胁的诉讼,我们或任何子公司也没有作为 原告或被告参与任何重大诉讼或未决诉讼。
| 62 |
管理
以下 人员为本公司的执行主管和董事,于本合同生效之日起担任与其姓名相对的职位。
| 名字 | 年龄 | 职位 | 委任日期 | ||||||
| Dewan Fazlul Hoque Chowdhury | 50 | 首席执行官总裁、临时首席财务官兼董事 | 2013年12月24日 | ||||||
| 阿拉什·加达尔 | 46 | 首席运营官 | 2022年1月5日 | ||||||
| 巴希尔·蒂莫尔 | 48 |
董事 首席商务官 |
2013年12月24日2018年4月9日 | ||||||
| 托马斯·摩尔 | 59 | 独立董事 | 2017年8月3日 | ||||||
| 萨利姆·纳塔博士 | 56 | 独立董事 | 2017年7月26日 | ||||||
| 蒂莫西·约翰逊 | 39 | 独立董事 | 2017年7月17日 | ||||||
我们的董事 任职到他们去世、辞职或被免职的较早者,或他们的继任者获得资格为止。
自2009年1月20日DDL成立以来,D.F.H.Chowdhury博士一直担任我们的首席执行官兼董事会成员 ,并自2022年7月1日起担任我们的临时首席财务官。他负责我们核心技术的研发、产品开发、创新和商业化。他还协调并监督法律合规;公司使命的发展;政策和规划。在成立公司之前,乔杜里博士是Microneedle Technologies和Nemaura Pharma Limited的创始人兼首席执行官。D.F.H.乔杜里博士一直负责谈判一种治疗阿尔茨海默病的透皮贴片的许可协议。此外,他还参与了商业谈判和全球战略制定。
D.F.H.Chowdhury博士拥有克兰菲尔德大学微系统和纳米技术硕士学位,以及牛津大学纳米药物输送博士学位。他在制药行业的经验包括产品开发、制造以及技术和企业管理。
Arash Ghadar。 Ghadar博士于2022年1月5日加入公司担任首席运营官,在加入Nemaura之前,Ghadar博士在英国拉夫堡的Datalink电子公司(Datalink)担任了十年的技术董事 ,作为Datalink内部的一个独立实体管理设计团队。他负责管理设计团队的日常运营、业务规划、法律事务、财务、销售、 和业务开发。在这一职位上,他还监督了医疗保健和工业客户的众多技术项目,包括产品开发生命周期、可行性研究、设计、开发、原型制作、验证、认证、质量管理和批量生产。
Ghadar博士 目前也是英格兰中部地区生命科学行业协会Medilink Midland的非执行董事成员,其愿景 旨在刺激中部地区生命科学部门的增长。他拥有电子和控制系统工程理学学士学位和硕士学位,分别获得了一等学位和优异成绩,他还拥有英国华威大学生物传感器博士学位 。
Bashir Timol。-Timol先生自2013年12月成立以来一直担任Nemaura Medical的董事会成员。他共同创立、管理和资助了多家生物技术和生命科学公司,并领导了为Nemaura Medical最初两轮融资提供资金的投资财团。蒂莫尔先生在英国中央兰开夏大学获得经济学学士学位。
蒂莫西·约翰逊。 约翰逊先生于2017年7月当选董事会员。他目前在英国的几家税务咨询和会计公司担任高管职位。他是一名执业的特许税务顾问,并拥有英国曼彻斯特大学数学和物理专业的一流理科硕士学位。Johnson先生的工作包括每天深入审查和分析财务报表,他在财务账户、税务、财务管理、金融监管要求和反洗钱要求方面拥有丰富的经验。
托马斯·摩尔。-摩尔先生于2017年8月当选为董事的一员。他目前担任董事、税务顾问和一家税务咨询公司(西桥)的共同所有者,在均富会计师事务所、毕马威和普华永道等领先会计师事务所积累了三十年的会计和咨询领域的经验。在过去五年中,摩尔先生自2017年5月以来一直在西桥担任 目前的职务,在此之前是董事在均富英国有限公司的职务。他是一名执业的特许税务顾问,并在英国诺森比亚大学获得了法语和俄语的一等文学士学位。穆尔先生担任该职位的资格包括在与会计、财务管理和金融监管要求相关的事务方面拥有丰富的经验,包括他目前在两家公司担任MLRO的经验。
| 63 |
Salim{br]Natha博士。Natha博士于2017年7月当选为董事。他目前是英国国家医疗服务体系(NHS)的眼科医生,是阿什顿、维根和利地区20,000多名糖尿病患者视网膜病变筛查项目的临床负责人。 他在医学文献中发表了多篇文章,同时也是英国国家糖尿病视网膜病变筛查项目的同行评审员。娜莎博士以优异的成绩毕业于利物浦大学医学院。
家庭关系
我们的任何董事或高管之间都没有 家族关系。
参与某些法律诉讼。
没有。
董事会
所有董事均任职至下一届年度股东大会,并直至其继任者正式选出并符合资格为止。董事由年会选举产生,任期一年。管理人员由董事会选举,并由董事会酌情决定。 我们的董事会至少每季度举行一次会议。
董事会在公司治理方面遵守纳斯达克上市规则。根据纳斯达克规则,我们 必须维持一个由至少50%的独立董事组成的董事会,以及一个至少由两名成员组成的审计委员会,该委员会 仅由也符合1934年证券交易法规则10A-3要求的独立董事组成。
董事独立自主
董事会应用纳斯达克独立性标准对我们董事的独立性进行了审查。基于此次审查,董事会 决定Thomas Moore、Salim Natha博士和Timothy Johnson在纳斯达克规则的含义内都是独立的 。在作出这一决定时,我们的董事会考虑了这些非雇员董事与我们的关系,以及董事会认为与确定他们的独立性相关的所有其他事实和情况。根据纳斯达克适用规则的要求,我们预计我们的独立董事将尽可能频繁地定期开会,以履行其职责,包括至少每年在没有非独立董事和管理层出席的执行会议上开会。
董事会委员会
我们的董事会已经建立了履行职责的常设委员会。这些委员会包括审计委员会、薪酬委员会和提名和公司治理委员会。我们的董事会已经通过了每个委员会的书面章程 。章程的副本可以在我们的网站上找到。我们的董事会可以在其认为必要或适当的情况下不时设立其他委员会 。
审计委员会
我们的审计委员会 由独立董事Thomas Moore、Salim Natha博士和Timothy Johnson组成。约翰逊先生有资格担任根据证券法颁布的S-K法规第407(D)(5)项所界定的审计委员会财务专家。
根据其章程,审核委员会至少由三名成员组成,每名成员均须为董事会已决定符合董事及美国证券交易委员会的独立性要求的非雇员纳斯达克,并受规则10A-3(B)(1)及规则10A-3(B)(1)的规限,但须受规则10A-3(C)所载豁免的规限。《审计委员会章程》阐述了审计委员会的主要职能,包括:
| – | 监督公司的会计和财务报告流程; |
| – | 监督公司合并财务报表的审计; |
| – | 讨论与风险评估和风险管理有关的政策,讨论公司的主要财务风险敞口以及管理层为监测和控制此类敞口而采取的步骤; | |
|
|
– | 与管理层审查和讨论本公司经审计的综合财务报表,并在向美国证券交易委员会提交任何包含此类合并财务报表的报告之前,与管理层和本公司的独立注册会计师事务所审查本公司的综合财务报表。 |
| 64 |
| – | 建议董事会将本公司经审计的综合财务报表列入上一财政年度的Form 10-K年度报告; |
| – | 分别、定期、与管理层、公司内部审计师(或其他负责内部审计职能的人员)和公司的独立注册会计师事务所举行会议; |
| – | 直接负责为本公司编制或发布审计报告的任何独立注册会计师事务所的任命、薪酬、保留和监督工作; |
| – | 采取或建议董事会采取适当行动,以监督和确保本公司独立注册会计师事务所的独立性;以及 |
| – | 根据公司独立注册会计师事务所、内部审计师或管理层的建议,对公司的审计和会计原则和做法进行重大变更审查。 |
薪酬委员会
除其他事项外,薪酬委员会负责:
| – | 审查和批准或建议董事会批准我们首席执行官和其他高管和董事的薪酬,审查关键的员工薪酬目标、政策、计划和计划; |
| – | 管理激励性薪酬和股权薪酬; |
| – | 审查和批准我们与行政人员之间的雇佣协议和其他类似安排;以及 |
| – | 任命和监督任何薪酬顾问或顾问。 |
我们的薪酬委员会由Thomas Moore、Salim Natha博士和Timothy Johnson组成。萨利姆·纳塔博士担任赔偿委员会主席。
公司治理和提名委员会
公司治理和提名委员会负责除其他事项外:
| – | 遴选或者推荐董事职务的遴选人选; |
| – | 对董事和董事提名人的独立性进行评估; |
| – | 对董事会和董事会委员会的结构和组成进行审查并提出建议; |
| – | 制定并向董事会推荐公司治理的原则和做法; |
| – | 审查和监督公司的道德准则;以及 |
| – | 监督对公司管理层的评估。 |
我们的公司治理和提名委员会由Thomas Moore、Salim Natha博士和Timothy Johnson组成。约翰逊先生是公司治理和提名委员会的主席。
对证券持有人推荐董事会候选人的程序进行重大修改
我们目前没有证券持有人向董事会推荐被提名者的程序。在我们的普通股在纳斯达克上市之前,作为一家股东基础有限的私人公司,我们认为提供这样的程序并不重要。但是,作为一家纳斯达克上市公司,要求每年召开股东大会,我们将考虑在未来 实施这一政策。
董事会没有关于董事会候选人资格的正式政策。董事会在评估董事提名人选时,可能会考虑董事会或股东认为合适的因素,包括判断力、技能、性格力量、在规模或范围上与公司相当的企业和组织的经验、相对于其他董事会成员的经验和技能,以及专业知识或经验。 根据董事会当前的需求,某些因素可能会得到或多或少的重视。在考虑 董事会的候选人时,董事对每个候选人的资历进行全面评估,并且不具备任何必须满足的特定最低资格要求。董事将从任何合理来源考虑候选人,包括现任董事会成员、股东、专业猎头公司或其他人士。董事们不会根据谁提出了推荐而对候选人进行不同的评估。
| 65 |
董事会领导层在风险监督中的结构和作用
乔杜里博士担任本公司首席执行官和董事会主席。董事会认为,乔杜里博士作为首席执行官和董事会主席的服务符合公司及其股东的最佳利益。Chowdhury博士对公司在业务中面临的问题、机遇和挑战拥有详细和深入的知识,因此能够制定议程,确保董事会的时间和注意力集中在与公司业务有关的最关键事项上。他的联合作用使公司能够发挥决定性的领导作用,确保明确的责任,并增强公司 向公司股东、员工和客户清晰一致地传达其信息和战略的能力。
董事会尚未将 指定为主要董事。鉴于组成董事会的董事人数有限,独立董事召集和计划他们的 执行会议,并在董事会会议之间直接与管理层和其他人沟通。在这种 情况下,董事们认为,指定一名首席董事来负责他们目前都参与的职能 可能会减损而不是加强他们作为董事的职责。
管理层负责评估和管理风险,接受董事会的监督。董事会监督我们的风险管理政策和风险偏好,包括运营风险和与我们的业务战略和交易相关的风险。董事会的各个委员会在各自的专业领域协助董事会履行监督职责。
| – | 审计委员会协助董事会监督我们的财务报告、独立审计师和内部控制。它负责发现企业管理中的任何缺陷,并建议补救措施,检测欺诈风险,并实施反欺诈措施。审计委员会进一步讨论了Nemaura在财务报告方面的风险评估和管理政策。 |
| – | 薪酬委员会负责监督薪酬、留用、继承和其他与人力资源有关的问题和风险。 |
| – | 公司治理和提名委员会负责审查与我们的治理政策和倡议相关的风险。 |
道德规范:
我们已通过了适用于我们的首席执行官、首席财务官和其他执行类似职能的人员的道德准则。 我们的道德准则副本可在我们的网站上找到。我们打算在我们的网站上发布适用于我们的首席执行官、首席财务官或执行类似职能的人员的道德守则的修正案或豁免条款。
高管薪酬
2023摘要 薪酬表
此表披露了2023财年和2022财年向我们指定的高管支付的薪酬。
| 被任命为首席执行官 和主体地位 |
年 | 薪金 | 奖金 | 股票大奖 | 期权大奖 | 所有其他补偿 | 总计 | |||||||||||||||||||||
| $ | $ | $ | $ | $ | $ | |||||||||||||||||||||||
| D.F.H.乔杜里医生, | 2023 | 98,913 | — | — | — | 239,665 | (4) | 337,577 | ||||||||||||||||||||
| 首席执行官兼总裁 | 2022 | 109,416 | — | — | 26,706 | (1) | 3,849 | 139,971 | ||||||||||||||||||||
| 贾斯汀·麦克拉尼 | 2023 | 28,245 | — | — | 50,728 | 78,973 | ||||||||||||||||||||||
| 首席财务官(2) | 2022 | 256,444 | (3) | — | — | — | 2,498 | 258,942 | ||||||||||||||||||||
| (1) | 2022年1月28日,作为对乔杜里博士作为董事服务的补偿,公司董事会授予乔杜里博士以每股3.98美元的行使价购买8,000股普通股的选择权,这是授予日公司普通股的收盘价。该购股权于授出时已完全归属,并可于授出日期起计五年内行使。归因于期权的公允价值是使用布莱克-斯科尔斯期权定价模型计算的。 |
| (2) | 麦克拉尼于2022年7月辞去公司首席财务官一职。此后,乔杜里博士担任临时首席财务官。 |
| (3) | 其中169,055美元以现金支付,87,389美元以股票支付。麦克拉尼当选时,他的部分基本工资是以股票形式支付的。因此,在2022年1月31日,麦克拉尼以3.92美元的市价获得了22,293股。 |
| (4) | 2022年4月,薪酬委员会同意改变乔杜里博士的薪酬,自2013年以来一直没有变化。现已确定,他的年薪应为40万美元,外加一笔酌情奖金(业绩要求将在以后确定)。*董事会于2022年7月批准了这一点。这也包括对养老金计划的支付。 |
| 66 |
D.F.H.乔杜里博士
我们于2013年11月2日与D.F.H.Chowdhury博士签订了雇佣协议。D.F.H.乔杜里博士的合同期限不详。他可以在通知后离开公司,或者公司可以通知终止他的合同。解约可以是有理由的,也可以是没有原因的。D.F.H.乔杜里博士的年薪为80,000英镑(约合109,000美元)。我们与D.F.H.Chowdhury博士的合同不包括任何有关股票期权或股权激励的条款。
根据高管聘用协议,D.F.H.Chowdhury博士的年薪按比例进行调整,以仅反映Nemaura Medical Inc.所做的工作。表中的披露分别反映了他在截至2022年3月31日和2021年3月31日期间的按比例薪酬 。
J.麦克拉尼先生
我们于2020年9月15日与我们的首席财务官贾斯汀·麦克拉尼先生签订了雇佣协议。麦克拉尼的合同期限不详。他 可以在通知后离开公司,或者公司可以通知终止他的合同。解约可以是有理由的,也可以是没有原因的。麦克拉尼先生的年基本工资为90,000英镑(约合123,000美元)。我们与麦克拉尼先生的合同安排允许在满足某些条件的情况下提供股票期权、股权或现金激励。雇佣关系于2022年7月经双方同意终止。
截至2023年3月31日的财政年度未偿还股权奖励 。
下表列出了截至2023年3月31日被任命的高管的未偿还期权奖励;截至该日期,没有新的未偿还股票奖励:
|
数量 证券 潜在的 未锻炼身体 选项 (#) 可操练 |
数量 证券 潜在的 未锻炼身体 选项 (#) 不能行使 |
选择权 锻炼 价格: ($) |
选择权 期满 日期 | |||||||||||
| D.F.H.乔杜里博士 | 8,000 | — | 3.98 | 2027年1月28日 | ||||||||||
终止或 控制权变更时的潜在付款。
没有。
董事薪酬
我们的每位独立董事在截至2023年3月31日的年度获得5,000英镑(约合6,031美元)的年费,以表彰他们在我们董事会和委员会中的服务。
| 名字 |
以现金支付或赚取的费用 ($) |
|||
| 蒂莫西·约翰逊 | 6,182 | |||
| 萨利姆·纳塔博士 | 6,182 | |||
| 托马斯·摩尔 | 6,182 | |||
| 67 |
某些受益所有者和管理层的安全所有权
下表列出了截至2023年8月1日我们普通股的实益所有权的某些信息,包括:(I)据我们所知拥有我们普通股5%以上的每个个人或实体;(Ii)我们被点名的高管;(Iii)每个董事;以及(Iv)我们作为一个整体的所有高管和董事 。
除非下表的脚注中另有说明,否则表中列出的每个人都拥有唯一投票权和投资权,且此人的地址是c/o Nemaura医疗公司,高级技术创新中心,5 Oakwood Drive,Loughborough,Leicester shire,UK LE11 3QF。
| 实益拥有人姓名或名称 | 实益所有权的数额和性质 | 百分比(1) |
| D.F.H.乔杜里博士 | 8,761,700 (2) | 30.3% |
| 巴希尔·蒂莫尔 | 2,798,310 (3) | 9.7% |
| 蒂莫西·约翰逊 | 8,000 (4) | * |
| 萨利姆·纳塔博士 | 408,640 (2) | 1.4% |
| 托马斯·摩尔 | 8,000 (4) | * |
| 全体行政人员和董事(6人) | 12,025,693 (5) | 41.5% |
| 持有我们5%或以上的普通股 | ||
| 苏夫扬伊斯梅尔(6) | 2,134,295 | 7.4% |
*低于1%。
(1)基于2023年8月1日已发行的28,899,402股普通股
(2)包括报告人在行使购买8,000股普通股的既得选择权后,有权在2023年8月1日起60天内收购的8,000股。
(3)代表(I)由举报人直接持有的2,708,210股,(Ii)由举报人的配偶持有的82,100股,以及(Iii)举报人有权在2023年8月1日起60天内购买8,000股普通股的既得选择权 。
(4)代表报告人在行使购买8,000股普通股的既得选择权后,有权在2023年8月1日起60天内收购的8,000股普通股。
(5)包括40,000股公司高管和董事有权在2023年8月1日起60天内行使既得期权购买40,000股普通股 。
(6)伊斯梅尔先生的地址是英国兰开夏郡BL6 HDT博尔顿,Lostock,Hollybank High Bank Lane。
| 68 |
某些关系 和关联方交易
Pharma和NDM是由我们的首席执行官、董事会主席兼大股东D.F.H.Chowdhury博士控制的实体。
Pharma已向我们的子公司DDL和TCL开具研发服务发票。此外,DDL和TCL的某些运营费用 已由Pharma和NDM支付,并已向我们开具发票。Pharma和NDM产生的某些成本直接归因于DDL和 TCL,这些成本已向我们开出账单。
截至2023年3月31日的年度,Pharma和NDM向我们收取的总成本为4,767,586美元。
DDL与Nemaura Pharma Limited(“Pharma”)签订了一项服务协议,Nemaura Pharma Limited(“Pharma”)是一家由公司总裁和首席执行官控制的实体,根据Pharma的ISO13485认证提供开发、制造和监管审批流程。Pharma在成本加成的基础上为这些服务开具DDL发票。
以下是本公司与Pharma和NDM在截至2023年3月31日和2022年3月31日的年度内的活动摘要。
| 3月31日, | ||||||||
| 2023 | 2022 | |||||||
| ($) | ($) | |||||||
| 年初欠(来自)关联方的 | (101,297 | ) | 148,795 | |||||
| Pharma向DDL、NM和TCL开具发票的金额 | 4,767,586 | 3,245,985 | ||||||
| DDL向Pharma开出的发票金额 | (3,245 | ) | (2,495 | ) | ||||
| DDL向Pharma支付的金额 | (3,773,217 | ) | (3,492,962 | ) | ||||
| 外汇差额 | 30,953 | (620 | ) | |||||
| 应于年底付给关联方的款项 | 920,780 | (101,297 | ) | |||||
普通股说明
一般信息
以下是对我们普通股的说明,仅为摘要,并不完整。本招股说明书是作为注册说明书的证物而存档的,并受经修订的公司章程(“公司章程”)及经修订及重新修订的附例(“附例”)作为证物而提交的本公司章程(“公司章程”)及本章程所载证物的整体约束及保留。我们鼓励您阅读我们的公司章程、我们的章程和内华达州修订法令(“NRS”)的适用条款,以获取更多信息。
截至2023年8月1日,我们的法定股本包括42,000,000股普通股,每股面值0.001美元,其中28,899,402股已发行和流通股, 和200,000股优先股,面值0.001美元,其中没有发行和流通股。普通股和优先股的授权股票和未发行股票 无需公司股东采取进一步行动即可发行,除非适用法律、纳斯达克资本市场或我们证券可能在其上市的任何其他证券交易所的规则要求采取此类 行动。除非需要得到公司股东的批准,否则公司董事会不会为发行和出售我们的普通股或优先股寻求股东的批准。
普通股
本公司普通股持有人有权就提交股东表决的所有事项,就每股股份投一票。普通股持有人没有累计投票权。 因此,普通股过半数股东可以投票选举所有董事。持有本公司已发行股本、已发行股本及有权投票的普通股的股东 必须亲自或委派代表出席,方可构成任何股东大会的法定人数。
| 69 |
公司普通股的持有者有权 分享董事会自行决定从合法可用资金中宣布的所有股息。在发生清算、解散或清盘的情况下,每股流通股持有人有权按比例参与偿付债务和按优先于普通股计提每类股票(如有)后剩余的所有资产。本公司普通股 没有优先购买权,没有换股权利,也没有适用于本公司普通股的赎回条款。
内华达州法律和我国公司章程各项条款的反收购效果
NRS和我们的公司章程和章程的规定可能会使通过要约收购、代理竞争或其他方式收购我们变得更加困难, 或罢免现任高级管理人员和董事。这些条款总结如下,预计将阻止我们董事会认为不充分的某些类型的强制性收购做法和收购要约,并鼓励寻求获得对我们的控制权的人首先与我们谈判。我们相信,加强保护我们与收购或重组我们的不友好或主动提议的提倡者谈判的能力的好处将超过阻止收购或收购提议的坏处 因为谈判这些提议可能会导致其条款的改善。
已授权但未发行的普通股和空白支票优先股的效果. 存在授权但未发行的普通股和未指定优先股的影响之一可能是使我们的董事会更难或阻止 通过合并、要约收购、代理竞争或其他方式获得对我们公司的控制权的企图,从而保护管理层的连续性 。如果董事会在适当行使其受托责任时确定收购提议不符合我们的最佳利益,董事会可以在一项或多项交易中发行此类股票,而无需股东批准。 这些交易可能会通过稀释拟议收购人或反叛股东集团的投票权或其他权利而阻止或增加完成收购交易的难度或成本 将大量投票权置于机构或其他可能承诺支持现任董事会地位的手中,通过实施可能使收购复杂化或排除收购的收购,或者是其他原因。
此外,我们的公司章程 授予我们的董事会广泛的权力,以确立优先股的授权和未发行股份的权利和优先权。 优先股的发行可能会减少可用于分配给普通股持有者的收益和资产的金额 。此次发行还可能对这些持有人的权利和权力(包括投票权)产生不利影响,并可能具有推迟、威慑或阻止我们公司控制权变更的效果。
《股东利益相关法》。我们 受内华达州与利益相关股东法规(内华达州修订法规(NRS)78.411至78.444节)的约束,该法规禁止“利益股东”与我们达成“合并”,除非满足 某些条件。“有利害关系的股东”是指与关联公司和联营公司一起实益拥有(或在之前两年内确实实益拥有)我们有权投票的10%或更多股本的人。然而,我们已在修订和重新修订的公司章程中选择 不受NRS第78.411至78.444条的规定管辖。
《控制权股份条例》。 我们受内华达州《控制股份条例》(NRS第78.378至78.3793条)的约束,该法规限制个人和 团体收购内华达州公司五分之一或更多有投票权的股份的能力,该公司拥有200名或更多登记在册的股东,其中至少有 100人在内华达州有地址,在没有股东批准股份收购交易或公司选择退出的情况下,行使所收购股份的投票权。被收购股份的投票权限制在收购后三年内。为避免投票限制,收购控股权必须获得以下两方面的批准:(A)公司多数投票权的持有人,以及(B)如果收购将不利地改变或改变给予任何其他类别或系列流通股的任何优惠或任何相对或其他权利,则受影响的每个类别或系列的多数股权的持有人,不包括任何利益股东行使投票权的股份,并且批准必须明确包括授予此类投票权。尽管我们没有选择退出本法规,但公司也可以选择明确地选择不受其公司章程或章程中的规定管辖。此外,面对潜在的控制权股份交易,公司如果没有选择退出法定条款,可以在收购人收购控股权后10天前通过修改公司章程或章程来退出控制权股份法规 。
责任限制 以及对高级职员和董事的赔偿。NRS限制或消除了董事因违反董事作为董事的受托责任而对公司及其股东造成的金钱损害的个人责任。我们修改和重新修订的公司条款 包括要求我们在《国税法》允许的最大程度上赔偿我们的董事或高管因作为董事或本公司高管所采取的行为,或应我们的请求作为董事或高管或其他公司或企业的其他职位(视情况而定)而遭受的金钱损害的条款。我们修订和重新修订的公司章程还 规定,我们必须向我们的董事和高级管理人员赔偿并垫付合理的费用,前提是我们收到了NRS可能要求的受赔偿方的承诺 。我们还被明确授权购买董事和高级管理人员保险,以保护我们的公司、我们的董事、高级管理人员和某些员工承担一些责任。
| 70 |
《国税法》以及我们修订和重新修订的公司章程和章程中规定的责任限制和赔偿条款可能会阻止股东 因董事违反受托责任而对其提起诉讼。这些规定还可能降低针对董事和高级管理人员提起衍生品诉讼的可能性,即使此类诉讼如果成功,可能会使我们和我们的股东受益。但是,这些规定并不限制或消除我们或任何股东在董事违反受托责任时寻求非金钱救济(如禁令或撤销)的权利。此外,这些条款不会改变联邦证券法规定的董事责任。
传输代理
内华达代理和转让公司 (“转让代理”)是我们的转让代理和注册商。转移代理的地址是50 West Liberty Street,Suite 880,Reno内华达89501,其电话号码是(775)3220626。
有资格在未来出售的股份
我们无法预测市场 出售我们普通股的股票或可供出售的我们普通股的股票将对我们不时流行的普通股的市场价格产生的影响。未来我们普通股在公开市场上的销售,或该等股票在公开市场上的销售 ,可能会不时对当时的市场价格产生不利影响。通过行使已发行认股权证获得的相当数量的普通股可供出售,可能会对我们普通股的市场价格产生重大不利影响。此外,在下述限制失效后,我们的普通股在公开市场上的销售,或认为可能发生的销售,可能会导致当前市场价格下降或低于在没有这些销售或看法的情况下的价格 。
限售股份的出售
截至2023年8月1日,已发行普通股为28,899,402股 。本招股说明书提供的4,796,206股普通股将可自由交易,不受证券法第144(A)条规定的规则144(A)所界定的自由交易,不受证券法的限制或登记。
规则第144条
一般而言,根据现行的第144条规则, 任何人(或其股份需要汇总的人),包括可能被视为一家公司的“关联公司”的人,如果实益拥有受限证券至少六个月,可在任何三个月内出售数量不超过以下较大者的 股票:(1)当时已发行的普通股的1%,或(2)普通股 在国家证券交易所上市,普通股在根据规则第144条提交出售通知之日之前的四个日历周内的平均每周交易量。根据规则144进行的销售还受有关销售方式、通知和当前有关我们公司的公开信息的可用性等方面的特定要求的约束。任何人士如在出售前90天内任何时间未被视为吾等的联属公司,且实益拥有受限股份至少 一年,则有权根据第144条出售该等股份,而不受上述任何限制。
我们无法估计现有股东根据第144条将选择出售的普通股 股票数量。
法律事务
本招股说明书提供的证券的有效性将由Anthony L.G.,PLLC为我们传递,地址为佛罗里达州33401,西棕榈滩,Flagler Drive北625号Suite600。
专家
Nemaura Medical,Inc.截至2023年3月31日及截至2023年3月31日年度的综合财务报表,包括本招股说明书的一部分,已由独立注册会计师事务所Weinberg and Company,P.A.进行审计,如其报告中所述(其中包括 关于本公司作为持续经营企业继续经营的能力存在重大怀疑的说明性段落) ,并依据审计和会计专家事务所在提供该报告时提供的权威报告而包括在内。
Nemaura Medical,Inc.截至2022年3月31日及截至2022年3月31日的综合财务报表包括在本注册说明书中,该综合财务报表 已由独立注册会计师事务所Mayer Hoffman McCann P.C.审计,如其报告中所述(其中包括 关于公司持续经营能力存在重大疑虑的说明性段落) ,并依据该公司作为审计和会计专家在提供该报告时的权威而包括在内。
| 71 |
披露证监会对证券法责任赔偿的立场
我们的董事和高级管理人员受到内华达州法律、经修订的公司章程和公司章程的保障。我们已同意赔偿每位董事和某些 高级管理人员的某些责任,包括《证券法》规定的责任。鉴于根据证券法 可能允许我们的董事、高级管理人员和控制人根据上述条款 或其他规定对责任进行赔偿,我们已被告知,美国证券交易委员会认为,此类赔偿违反证券法 所表达的公共政策,因此不可执行。如果董事、高级职员或控股人士就正在登记的证券提出赔偿要求(我们的董事、高级职员或控股人士为成功抗辩任何诉讼、诉讼或法律程序而支付的 费用除外) ,我们将向具有适当管辖权的法院提交问题 该赔偿是否违反证券法中所表达的公共政策,并将受该问题的最终裁决 管辖。
在那里您可以找到更多信息
我们已根据证券法向美国证券交易委员会提交了S-1表格登记说明书中本招股说明书所提供证券的登记说明。本招股说明书是注册说明书的一部分,并不包含注册说明书和随附的证物中的所有信息,其中一些信息在美国证券交易委员会规则和法规允许的情况下被遗漏了 。有关我们和本招股说明书提供的证券的更多信息, 我们参考注册声明和随附的证物。本招股说明书中有关 任何合同或其他文件内容的陈述不一定完整。在每一种情况下,我们都请您参考作为注册声明证物存档的合同和/或其他文件的副本。
S-1表格注册说明书包括展品在内,是招股说明书的一部分,可在美国证券交易委员会网站上查阅。Http://www.sec.gov。您也可以在美国证券交易委员会的公共参考设施中阅读和复制我们向其提交或提供给该网站的任何文件:
| 公共资料室办公室 | |
| 地址:东北F街100号 | |
| 1580房间 | |
| 华盛顿特区,20549 |
您也可以写信至美国证券交易委员会的公众参考科,以规定的 费率获取这些文件的副本,地址为华盛顿特区20549,N.E.100F Street,1580室。美国的来电者也可以拨打(202)551-8090,以获得有关公共参考设施运作的进一步信息。
| 72 |
Nemaura Medical,Inc.
财务报表索引
| 页面 | |
| 截至2023年3月31日和2022年3月31日的年度经审计的综合财务报表 | |
| 独立注册会计师事务所报告(PCAOB ID:572) | F-2 |
| 独立注册会计师事务所报告(PCAOB ID:0199) | F-4 |
| 截至2023年3月31日和2022年3月31日的合并资产负债表 | F-5 |
| 截至2023年3月31日和2022年3月31日的综合经营报表和全面亏损报表 | F-6 |
| 截至2023年3月31日和2022年3月31日止年度股东权益(亏损)综合变动表 | F-7 |
| 截至2023年3月31日和2022年3月31日的合并现金流量表 | F-8 |
| 合并财务报表附注 | F-9 - 21 |
| F-1 |
独立注册会计师事务所报告
致Nemaura Medical Inc.的股东和董事会。
对财务报表的几点看法
本公司已审核所附Nemaura Medical Inc.(“本公司”)于2023年3月31日的综合资产负债表、截至该日止年度的相关综合经营报表及全面亏损、股东权益(亏损)变动及现金流量,以及相关附注(统称为“财务报表”)。我们认为,该等财务报表在各重大方面均公平地反映了本公司于2023年3月31日的财务状况,以及截至该年度的经营业绩及现金流量,符合美国公认的会计原则。
持续经营的企业
所附财务报表已编制 假设本公司将继续作为持续经营的企业。如财务报表附注1所述,于截至2023年3月31日止年度内,本公司于营运中出现净亏损及运用现金流量,并自成立以来出现经常性亏损。这些 条件使人对公司作为持续经营企业的持续经营能力产生了极大的怀疑。管理层关于这些事项的计划也在附注1中说明。财务报表不包括可能因这种不确定性的结果而产生的任何调整。
意见基础
这些财务报表由公司管理层负责。我们的责任是根据我们的审计对公司的财务报表发表意见。我们是一家在美国上市公司会计监督委员会(“PCAOB”)(“PCAOB”)注册的公共会计师事务所,根据美国联邦证券法以及美国证券交易委员会和PCAOB适用的规则和法规,我们必须对公司保持独立。
我们按照PCAOB的标准 进行审核。这些标准要求我们计划和执行审计,以获得关于财务报表是否没有重大错报的合理保证,无论是由于错误还是舞弊。本公司不需要,也不需要我们对其财务报告的内部控制进行审计。作为我们审计的一部分,我们需要了解财务报告的内部控制,但不是为了对公司财务报告内部控制的有效性发表意见。因此,我们不表达这样的意见。
我们的审计包括执行程序以评估财务报表重大错报的风险(无论是由于错误还是欺诈),以及执行应对这些风险的程序。这些程序包括在测试的基础上审查与财务报表中的金额和披露有关的证据。 我们的审计还包括评估管理层使用的会计原则和作出的重大估计,以及评估财务报表的整体列报。我们相信,我们的审计为我们的观点提供了合理的基础。
关键审计事项
以下所述的关键审计事项为:(1)涉及对财务报表具有重大意义的账目或披露;(2)涉及我们特别具有挑战性、主观性或复杂性的判断。关键审计事项的沟通不会以任何方式改变我们对整个财务报表的意见,我们也不会通过沟通下面的关键审计事项,就关键审计事项或与之相关的账目或披露提供单独的意见 。
存货计价
如财务报表附注3及附注5所述,本公司的存货按成本或可变现净值中较低者列账,按先进先出(“FIFO”)原则厘定。截至2023年3月31日,该公司的库存为180万美元。公司定期评估存货的账面价值, 这要求管理层作出假设并估计为减值而调整存货所需的金额。他说:
由于管理层需要做出重大判断和估计,我们将库存估值确定为一项关键的审计事项。确定价值是否已经下降 需要在估计未来需求和市场状况时做出重大判断。这需要审计师高度的判断力,并增加审计师在审计此类假设方面的努力。
我们为解决这一关键审计问题而执行的主要程序包括:
| ● | 我们通过制定对降价调整库存的估计,并将我们的估计与管理层的估计进行比较,来评估管理层调整降价库存的合理性。 | |
| ● | 我们测试了库存余额的准确性和完整性,以及库存的整体老化情况。 | |
| ● | 我们通过识别移动缓慢的库存并与管理层的分析进行比较,检验了库存估值调整的完整性。 | |
| ● | 我们测试了该公司计算降价调整库存的数学准确性。 |
| F-2 |
认股权证法律责任
如财务报表附注8所述,在截至2023年3月31日的年度内,本公司发出认股权证,要求管理层评估认股权证是否需要进行责任分类 。管理层决定,权证须于发行时按公允价值入账及按公允价值入账,其后于结算时或于每个报告期结束时按公允价值重新计量。截至2023年3月31日,公司的权证负债余额为310万美元。管理层使用Black-Scholes定价模型估计认股权证负债的公允价值。
由于管理层在确定权证是否需要进行负债分类时使用重大判断,以及在确定权证负债的公允价值时使用重大判断,因此我们将权证负债的会计和估值确定为一项关键审计事项。这需要审计师高度的判断力,并增加审计师在审计认股权证负债的会计和估值方面的努力。
我们为解决这一关键审计问题而执行的主要程序包括:
| ● | 我们获得并阅读了权证协议,以评估管理层确定权证符合作为负债分类的标准。 | |
| ● | 我们检验了布莱克-斯科尔斯模型中管理层使用的假设的合理性,这些假设包括行权价格、预期期限、预期波动率和无风险利率。 | |
| ● | 我们使用Black-Scholes模型建立了对权证负债的独立预期,并将我们的独立预期与管理层的估计进行了比较。 |
外汇合约衍生负债
如财务报表附注8所述,本公司拥有一份外汇合约,该合约符合ASC 815指引下衍生工具的定义,并按公允价值确认,并于每个报告期末的收益中确认公允价值变动。截至2023年3月31日,公司的外汇合约衍生品负债为731,730美元。
由于管理层在确定外汇合约衍生负债的公允价值时所使用的重大判断,我们将外汇合约衍生负债的估值审计确定为一项重要的审计事项。这需要核数师高度的判断力,并增加核数师在审核外汇合约衍生工具负债估值方面的努力。
我们为解决这一关键审计问题而执行的主要程序包括:
| ● | 我们获得并阅读了外汇合同,并就2023年3月31日的名义金额和杠杆金额与合同条款达成一致。 | |
| ● | 得到了管理层对外汇合约衍生负债公允价值的计算。 | |
| ● | 我们对外汇合约衍生负债的公允价值制定了独立预期,并将我们的独立预期与公司的估计进行了比较。 |
我们自2023年以来一直担任本公司的审计师。
/S/温伯格公司,P.A.
加利福尼亚州洛杉矶
2023年7月13日
| F-3 |
独立注册会计师事务所报告
致Nemaura Medical Inc.董事会和股东
对财务报表的几点看法
我们审计了Nemaura Medical Inc.(本公司)截至2022年3月31日和2021年3月31日的合并资产负债表,以及截至2022年3月31日的两年期间各年度的相关综合经营表和全面亏损、股东权益和现金流量,以及相关附注(统称财务报表)。我们认为,财务报表按照美国公认的会计原则,公平地反映了公司截至2022年3月31日、2022年3月31日和2021年3月31日的财务状况,以及截至2022年3月31日的两年期间各年度的经营结果和现金流量。
对持续经营的严重怀疑
所附财务报表 是在假设本公司将继续经营的情况下编制的。正如财务报表附注1所述,公司 因经营而遭受经常性亏损,到期的当前债务超过当前现金余额,并累计亏损,这令人对其作为持续经营企业的能力产生了严重的怀疑。附注1也说明了管理层在这些事项上的计划。财务报表不包括可能因这种不确定性的结果而产生的任何调整。
意见基础
这些财务报表由公司管理层负责。我们的责任是根据我们的审计对公司的财务报表发表意见。我们是一家在美国上市公司会计监督委员会(PCAOB)注册的公共会计师事务所,根据美国联邦证券法以及美国证券交易委员会和PCAOB的适用规则和法规,我们必须与公司保持独立。
我们按照PCAOB的标准进行审核。这些标准要求我们计划和执行审计,以获得关于财务报表是否没有重大错报的合理保证,无论是由于错误还是舞弊。本公司不需要,也不受委托对其财务报告的内部控制进行审计。作为我们审计的一部分,我们需要了解财务报告的内部控制,但不是为了对公司财务报告内部控制的有效性发表意见。因此,我们不表达这样的意见。
我们的审计包括执行程序 以评估财务报表重大错报的风险,无论是由于错误还是欺诈,以及执行程序以应对这些风险。这些程序包括在测试的基础上审查有关财务报表中的金额和披露的证据。我们的审计还包括评估管理层使用的会计原则和作出的重大估计,以及评估财务报表的整体列报。我们相信,我们的审计为我们的观点提供了合理的基础。
关键审计事项
关键审计事项是指在本期审计财务报表时产生的、已传达或要求传达给审计委员会的事项,(1)涉及对财务报表具有重大意义的账目或披露,以及(2)涉及我们特别具有挑战性的、 主观或复杂的判断。我们确定没有关键的审计事项。
迈耶·霍夫曼·麦肯P.C.
自2018年以来,我们一直担任本公司的审计师。
科罗拉多州丹佛市
2022年6月29日
| F-4 |
Nemaura医疗公司。
合并资产负债表:
| 截至3月31日, | 截至3月31日, | |||||||
| 2023 | 2022 | |||||||
| 资产 | ||||||||
| 流动资产: | ||||||||
| 现金 | $ | 10,105,135 | $ | 17,749,233 | ||||
| 库存,净额 | 1,754,852 | 1,487,771 | ||||||
| 预付费用和其他流动资产 | 357,934 | 495,055 | ||||||
| 增值税应收账款 | 409,648 | 255,112 | ||||||
| 外汇合同保证金 | 909,666 | — | ||||||
| 关联方应收账款 | — | 101,297 | ||||||
| 流动资产总额 | 13,537,235 | 20,088,468 | ||||||
| 财产和设备,累计折旧后的净额 | 641,906 | 532,508 | ||||||
| 无形资产,累计摊销净额 | 384,092 | 1,480,980 | ||||||
| 总资产 | $ | 14,563,233 | $ | 22,101,956 | ||||
| 负债和股东权益(赤字) | ||||||||
| 流动负债: | ||||||||
| 应付帐款 | $ | 326,641 | $ | 136,310 | ||||
| 应计费用和其他负债 | 130,678 | 558,426 | ||||||
| 应付票据,本期部分 | 16,942,500 | 19,188,724 | ||||||
| 应付关联方 | 920,780 | — | ||||||
| 递延收入,本期部分 | 123,640 | 259,256 | ||||||
| 外汇合约衍生负债 | 731,730 | 440,196 | ||||||
| 认股权证法律责任 | 3,092,000 | — | ||||||
| 流动负债总额 | 22,267,969 | 20,582,912 | ||||||
| 应付票据,非流动部分 | 3,087,651 | — | ||||||
| 递延收入,非当期部分 | 1,021,811 | 1,052,960 | ||||||
| 总负债 | 26,377,431 | 21,635,872 | ||||||
| 承付款和或有事项 | — | — | ||||||
| 股东权益(赤字): | ||||||||
| 普通股,面值$0.001 -授权:42,000,000 股票;已发行和已发行股票:28,899,402 和24,102,866 分别截至2023年3月31日和2022年3月31日 | 28,899 | 24,103 | ||||||
| 额外实收资本 | 40,991,377 | 38,295,775 | ||||||
| 累计赤字 | (51,875,211 | ) | (37,731,476 | ) | ||||
| 累计其他综合(亏损)收入 | (959,263 | ) | (122,318 | ) | ||||
| 股东权益合计(亏损) | (11,814,198 | ) | 466,084 | |||||
| 总负债和股东权益(赤字) | $ | 14,563,233 | $ | 22,101,956 | ||||
请参阅合并财务报表附注 。
| F-5 |
Nemaura医疗公司。
合并经营报表和全面亏损
| 截至3月31日止年度, | ||||||||
| 2023 | 2022 | |||||||
| 销售额 | $ | 77,044 | $ | 503,906 | ||||
| 销售成本 | (75,328 | ) | (344,300 | ) | ||||
| 销售成本--库存减记 | (1,478,108 | ) | — | |||||
| 毛利(亏损) | (1,476,392 | ) | 159,606 | |||||
| 运营费用: | ||||||||
| 研发 | 1,538,615 | 1,556,988 | ||||||
| 一般和行政 | 5,600,188 | 6,173,049 | ||||||
| 无形资产减值准备 | 980,039 | — | ||||||
| 总运营费用 | 8,118,842 | 7,730,037 | ||||||
| 运营亏损 | (9,595,234 | ) | (7,570,431 | ) | ||||
| 利息支出 | (6,412,501 | ) | (6,666,630 | ) | ||||
| 认股权证负债的公允价值变动 | 1,864,000 | |||||||
| 所得税优惠前亏损 | (14,143,735 | ) | (14,237,061 | ) | ||||
| 所得税优惠拨备 | — | 350,256 | ||||||
| 净亏损 | (14,143,735 | ) | (13,886,805 | ) | ||||
| 其他全面收入: | ||||||||
| 外币折算调整 | (836,946 | ) | (257,885 | ) | ||||
| 综合损失 | $ | (14,980,681 | ) | $ | (14,144,690 | ) | ||
| 每股基本和稀释后净亏损 | $ | (0.57 | ) | $ | (0.59 | ) | ||
| 加权平均流通股数 | 24,878,196 | 23,383,758 | ||||||
请参阅合并财务报表附注 。
| F-6 |
Nemaura医疗公司。
合并股东权益变动表(亏损)
| 普通股 | ||||||||||||||||||||||||
| 股票 | 金额 | 额外实收资本 | 累计赤字 | 累计其他综合损失 | 股东权益合计(亏损) | |||||||||||||||||||
| 2021年3月31日的余额 | 22,941,157 | $ | 22,941 | $ | 32,044,335 | $ | (23,844,671 | ) | $ | 135,567 | $ | 8,358,172 | ||||||||||||
| 发行普通股,扣除成本净额$50,765 | 772,524 | 773 | 3,067,254 | — | — | 3,068,027 | ||||||||||||||||||
| 认股权证的行使 | 366,892 | 367 | 2,963,291 | — | — | 2,963,658 | ||||||||||||||||||
| 作为股票补偿发行的限制性股票 | 22,293 | 22 | 87,366 | — | — | 87,388 | ||||||||||||||||||
| 向董事发行的期权 | — | — | 133,529 | — | — | 133,529 | ||||||||||||||||||
| 外币折算调整 | — | — | — | — | (257,885 | ) | (257,885 | ) | ||||||||||||||||
| 净亏损 | — | — | — | (13,886,805 | ) | — | (13,886,805 | ) | ||||||||||||||||
| 2022年3月31日的余额 | 24,102,866 | 24,103 | 38,295,775 | (37,731,476 | ) | (122,318 | ) | 466,084 | ||||||||||||||||
| 发行普通股,扣除成本 | 4,796,536 | 4,796 | 7,651,602 | — | — | 7,656,398 | ||||||||||||||||||
| 与发行普通股相关的认股权证负债的公允价值 | — | — | (4,956,000) | — | — | (4,956,000 | ) | |||||||||||||||||
| 外币折算调整 | — | (836,946 | ) | (836,946 | ) | |||||||||||||||||||
| 净亏损 | — | (14,143,735 | ) | (14,143,735 | ) | |||||||||||||||||||
| 2023年3月31日的余额 | 28,899,402 | $ | 28,899 | $ | 40,991,377 | $ | (51,875,211 | ) | $ | (959,263 | ) | $ | (11,814,198 | ) | ||||||||||
请参阅合并财务报表附注。
| F-7 |
Nemaura医疗公司。
合并现金流量表
| 截至三月三十一日止年度, | ||||||||
2023 | 2022 | |||||||
| 经营活动的现金流: | ||||||||
| 净亏损 | $ | (14,143,735 | ) | $ | (13,886,805 | ) | ||
| 对净亏损与经营活动中使用的现金净额进行的调整: | ||||||||
| 折旧及摊销 | 444,177 | 229,810 | ||||||
| 债务贴现的增加 | 1,871,593 | 6,666,630 | ||||||
| 监控费利息支出计入应付票据 | 2,240,339 | — | ||||||
| 票据修改费用加到应付票据上的费用 | 2,304,539 | — | ||||||
| 库存减记 | 1,478,108 | — | ||||||
| 无形资产减值准备 | 980,039 | — | ||||||
外汇合约衍生负债公允价值变动 | 291,534 | 440,196 | ||||||
| 认股权证负债的公允价值变动 | (1,864,000 | ) | — | |||||
| 基于股票的薪酬 | — | 220,917 | ||||||
| 经营性资产和负债变动情况: | ||||||||
| 库存 | (1,745,189 | ) | (637,149 | ) | ||||
| 预付费用和应收增值税 | (17,415 | ) | 519,346 | |||||
| 外汇合同保证金 | (909,666 | ) | — | |||||
| 应付帐款 | 190,331 | (117,384 | ) | |||||
| 应计费用和其他负债 | (427,748 | ) | 310,490 | |||||
| 应收/应付关联方 | 1,022,077 | (250,092 | ) | |||||
| 递延收入 | (166,765 | ) | — | |||||
| 用于经营活动的现金净额 | (8,451,781 | ) | (6,504,041 | ) | ||||
| 投资活动产生的现金流: | ||||||||
| 购置财产和设备 | (376,170 | ) | (481,718 | ) | ||||
| 资本化专利成本 | (135,168 | ) | (83,691 | ) | ||||
| 资本化的软件开发成本 | (27,879 | ) | (391,073 | ) | ||||
| 用于投资活动的现金净额 | (539,217 | ) | (956,482 | ) | ||||
| 融资活动的现金流: | ||||||||
| 发行普通股所得款项 | 8,394,056 | 3,118,792 | ||||||
| 与股权融资有关的成本 | (737,658 | ) | (50,765 | ) | ||||
| 行使认股权证所得收益 | — | 2,963,658 | ||||||
| 发行长期债券的收益,扣除贴现后的净额 | 4,700,000 | — | ||||||
| 应付票据的偿还 | (10,274,281 | ) | (12,400,000 | ) | ||||
| 融资活动提供的现金净额(用于) | 2,082,117 | (6,368,315 | ) | |||||
| 现金净减少 | (6,908,881 | ) | (13,828,838 | ) | ||||
| 汇率变动对现金的影响 | (735,217 | ) | (287,300 | ) | ||||
| 年初现金 | 17,749,233 | 31,865,371 | ||||||
| 年终现金 | $ | 10,105,135 | $ | 17,749,233 | ||||
| 补充现金流信息: | ||||||||
| 支付的利息 | — | — | ||||||
| 已缴纳的税款 | — | — | ||||||
| 补充披露非现金融资活动: | ||||||||
| 与发行普通股相关的认股权证负债的公允价值 | $ | 4,956,000 | $ | — | ||||
| 应付票据中增加的监控费 | $ | 2,240,339 | $ | 2,764,775 | ||||
请参阅合并财务报表附注 。
| F-8 |
Nemaura医疗公司。
合并财务报表附注
截至2023年3月31日和2022年3月31日的年度
注1-组织、主要活动和管理部门的计划
Nemaura Medical Inc.(“Nemaura”或“公司”)通过其运营子公司进行医疗器械研究和生产名为SugarBEAT®的连续血糖监测系统(“CGM”)。SugarBEAT®设备是一种非侵入性无线设备,供I型和II型糖尿病患者使用,也可用于筛查糖尿病前期患者。SugarBEAT®设备以非侵入性方式将葡萄糖等分析物提取到皮肤表面,使用独特的传感器进行测量,并使用独特的算法进行解释。
Nemaura是内华达州的一家控股公司,成立于2013年。Nemaura拥有德马尔诊断(控股)有限公司100%(100%)的股份,德马尔诊断(控股)有限公司是一家成立于2013年12月11日的英格兰和威尔士公司(“DDHL”) ,而德马尔诊断有限公司又拥有德马尔诊断有限公司(一家成立于2009年1月20日的英格兰和威尔士公司(“DDL”))和试验诊所有限公司(一家成立于2011年1月12日的英格兰和威尔士公司(“TCL”))的100%(100%)股份。
DDL是一家诊断医疗设备公司,总部位于英国莱斯特郡拉夫堡,致力于诊断医疗设备的发现、开发和商业化。该公司最初的重点是开发SugarBEAT®设备,它由一个包含传感器的一次性贴片和一个非一次性微型发射器设备组成,该设备带有可充电电源,旨在实现血糖水平的 趋势或跟踪。该公司的所有业务和资产都位于英国。
该公司成立于2013年,到目前为止, 报告了运营的经常性亏损。这些操作 已成功完成临床项目,以支持CE标志(欧盟对该产品的批准)批准、 以及向美国食品和药物管理局(FDA)提交的De Novo 510(K)医疗器械申请。公司 预计在通过许可费或产品销售产生收入之前,将继续在运营中蒙受亏损。然而,考虑到必要的临床计划的完成,这些损失预计将随着时间的推移而减少。管理层已与与英国(“UK”)、欧洲、卡塔尔和海湾合作委员会所有国家/地区有关的无关第三方签订了许可、供应或合作协议。
持续经营的企业
随附的财务报表 是以持续经营为基础编制的,其中考虑了在正常业务过程中的资产变现、负债结算和 承诺。如所附财务报表所示,截至2023年3月31日的年度,本公司录得净亏损14,143,735美元,运营中使用现金8,451,781美元。 这些因素令人对本公司在财务报表发布之日起一年内继续经营下去的能力产生重大怀疑。如果公司无法继续经营下去,财务报表不包括任何可能需要的调整。
在评估公司的持续经营状况时,管理层考虑了潜在的融资提供者,并相信未来运营的融资可以通过股权和/或债务融资来提供。即使公司能够获得额外的融资,它也可能对我们的运营施加不适当的限制,在债务融资的情况下,或者在股权融资的情况下,对我们的股东造成严重的稀释。
| F-9 |
附注2--陈述的依据
随附的合并财务报表 包括本公司及其子公司DDL、TCL和DDHL的账目。合并财务报表是根据美国公认会计原则(“美国公认会计原则”)编制的,所有公司间结余和交易均已在合并中冲销。
本公司大部分业务的本位币为英镑,报告货币为美元(“美元”)。
附注 3--重要会计政策摘要
预算的使用
根据美国公认会计原则编制合并财务报表要求管理层作出估计和假设,这些估计和假设会影响合并财务报表日期报告的资产和负债额以及或有资产和负债的披露,以及列报期间报告的收入和费用。重大估计包括潜在负债的应计项目、存货的可变现净值、债务和权益工具的估值、衍生负债的公允价值、为服务发行的股票期权的估值以及递延税项估值 免税额中使用的 假设。实际结果可能与这些估计不同。
收入确认
本公司根据财务会计准则委员会(“FASB”)会计准则编纂(“ASC”)606“与客户的合同收入”(“ASC 606”)确认收入。ASC 606的基本原则是确认收入,以描述将商品或服务转移给客户的预期收入额。ASC606创建了一个五步模型,要求实体在考虑合同条款时进行判断(S),其中包括(1)确定与客户的合同或协议,(2)确定合同或协议中的履约义务,(3)确定交易价格,(4)将交易价格分配给单独的履约义务,以及(5)在履行每项履约义务时确认收入。
公司仅在以下情况下才将五步模式应用于合同: 实体很可能会收取其有权收取的对价,以换取其转让给客户的商品或服务 。在合同开始时,一旦合同被确定在ASC 606的范围内,公司将评估每份合同中承诺的货物或服务,确定属于履约义务的货物或服务,并评估每项承诺的货物或服务是否不同。然后,公司将在履行履约义务时分配给相应履约义务的交易价格金额确认为收入。
公司可与合作伙伴签订产品开发 和其他协议。协议条款可能包括不可退还的签约费和许可费、里程碑 付款以及从协作中获得的任何产品销售的版税。
特许权使用费收入将在 销售相关产品时确认,前提是公司在协议项下没有剩余的履约义务。
递延收入
公司已签订许可协议 ,只有在许可对客户具有独立价值的情况下,才会在许可交付时将预付许可付款确认为收入。 但是,如果必须满足进一步的绩效标准,收入将递延并在被认为适合与许可相关的条件的基础上确认,并在公司预期完成这些履行义务的期间内确认。
研发费用
公司将研发费用计入已发生的运营 。研发费用主要包括人员和外部承包商的工资和相关费用 和咨询服务。其他研发费用包括用于研发、原型制造、临床研究、相关信息技术和设施成本分配的材料和用品的成本。
| F-10 |
现金和现金等价物
现金及现金等价物主要由英国境内的现金存款构成。
我们维持美元、英镑和欧元的现金余额。下表按美元报告,按货币面值分列我们的现金余额 :
| 按货币面值分列的现金余额明细表 | ||||||||
| 3月
31, 2023 | 3月31日
2022 | |||||||
| 现金以下列单位计价: | ||||||||
| 美元 | $ | 5,606,972 | $ | 14,769,720 | ||||
| 英镑 | 4,446,720 | 2,911,117 | ||||||
| 欧元 | 51,443 | 68,396 | ||||||
| 总计 | $ | 10,105,135 | $ | 17,749,233 | ||||
库存成本
存货按成本或可变现净值中较低者列报,成本以先进先出(“FIFO”)为基础确定。公司根据对库存需求的估计预测记录对其库存的调整,其中考虑了库存周转率、库存现有量、未完成的客户订货量和预测需求等。如果估计的可变现净值被确定为小于存货的记录成本,差额在发生差额时确认为损失。一旦库存被减记,它就会为库存创建一个新的成本基础,随后可能不会被计入。
财产和设备
财产和设备按成本列报,并按资产估计使用年限进行折旧 ,一般为四至五年。折旧计入 运营费用。
无形资产
无形资产包括主要与SugarBEAT®设备相关的许可证和专利 ,并以直线方式摊销,一般按估计使用年限或法定年限中较短的时间摊销。资本化的成本涉及从第三方收到的发票,而不是任何内部成本。当事件或情况显示 无形资产(所有资产的寿命均有限)及其他长期资产可能无法收回,或至少每年一次,本公司便会评估其无形资产及其他长期资产的减值。有限年限无形资产及其他长期资产的回收能力是通过将资产组的账面价值与该资产组预期产生的未来未贴现净现金流量进行比较来衡量的。 为进行此类审核,本公司按资产组的可识别现金流在很大程度上独立于其他资产组和负债组的现金流的最低水平对资产进行了分组。有限年限内应确认的减值金额 无形资产和其他长期资产按资产组的账面价值和公允价值之间的差额计算, 一般通过对估计的未来现金流量进行贴现来计量。
软件开发成本
公司将实施供其内部使用的软件所产生的成本资本化,包括支持公司计划服务的托管应用程序成本。在截至2023年3月31日的年度内,公司确定软件开发成本已减值,并计入减值655,641美元。
所得税。
所得税按 资产负债法核算。递延所得税资产和负债确认为可归因于 现有资产和负债的账面金额与其各自计税基础之间的差额和营业亏损结转的未来税项后果。递延所得税资产和负债采用颁布税率计量,预计适用于预计收回或结算这些临时差额的年度的应纳税所得额。税率变动对递延所得税资产和负债的影响在包括颁布日期在内的期间的收入中确认。若部分或全部递延所得税资产被认为更有可能无法变现,则提供估值拨备以减少递延所得税资产的账面金额。
本公司只有在收入 纳税头寸更有可能持续的情况下才会确认这些头寸的影响。已确认所得税头寸以实现可能性大于50%的最大金额计量。确认或计量的变化反映在判断发生变化的期间。本公司已选择在综合全面损失表中将与未确认的税收优惠相关的利息和罚款归类为所得税费用的 部分。该公司做到了不是在截至2023年3月31日及2022年3月31日止年度内,本集团并无任何应计利息或罚款 与任何未确认税项优惠相关,亦无任何与未确认税项优惠相关的利息支出。
| F-11 |
每股基本亏损 的计算方法为:普通股股东可获得的亏损除以 期间已发行普通股的加权平均数。每股摊薄亏损的计算方法与每股基本亏损类似,不同之处在于分母增加以包括潜在普通股已发行及额外普通股为摊薄股份时将会发行的额外普通股数目 。每股普通股摊薄亏损反映了如果可转换债券、期权和认股权证被行使或转换或以其他方式导致发行普通股时可能发生的摊薄,这些普通股随后在实体的收益 中分享。
由于截至2023年3月31日、2023年3月31日及2022年3月31日止年度的未偿还期权及认股权证的影响为反摊薄,因此这些工具相关的普通股股份不计入每股普通股亏损。
以下列出了截至2023年3月31日和2022年3月31日的普通股已发行期权和认股权证的股份数量:
| 普通股相关未偿期权一览表 | ||||||||
| 3月31日, | ||||||||
| 2023 | 2022 | |||||||
| 认股权证 | 6,369,304 | 1,573,098 | ||||||
| 股票期权 | 40,000 | 40,000 | ||||||
| 6,409,304 | 1,613,098 | |||||||
外币折算
公司的本位币为英镑, 报告币种为美元。资产和负债按资产负债表日的汇率换算为美元,收入和支出金额按期间的平均汇率换算。股东权益按历史汇率折算。将财务报表金额换算成美元产生的收益和损失在股东亏损中作为累计其他综合损失的单独组成部分入账。
我们使用下表中的汇率来换算截至和所述期间内以非美元货币计价的金额:
| 汇率折算金额明细表 | ||||||||
| 截至2013年3月31日, | ||||||||
| 2023 | 2022 | |||||||
| 3月31日汇率: | ||||||||
| 英镑:美元 | 1.236 | 1.316 | ||||||
| 欧元:美元 | 1.138 | 1.184 | ||||||
| 在截至以下年度的 3月31日, | ||||||||
| 2023 | 2022 | |||||||
| 截至3月31日止年度的平均汇率: | ||||||||
| 英镑:美元 | 1.215 | 1.342 | ||||||
衍生金融工具
本公司根据ASC主题815“衍生工具和对冲”(“ASC 815”)对其金融工具进行评估,以确定该等工具是否为衍生工具或包含符合嵌入衍生工具资格的特征。对于作为负债入账的衍生金融工具,该衍生工具最初按其公允价值入账,然后于每个报告日期重新估值,并在经营报表中报告公允价值的变动。本公司使用衍生金融工具一般仅限于管理汇率风险。此外,本公司发行的不符合股权处理标准的权证将被记录为负债 。我们不使用金融工具或衍生品进行任何交易。
金融工具的公允价值
根据ASC 820《公允价值计量和披露》,该公司使用可观察到的投入来确定金融工具的公允价值,并在计量公允价值时尽量减少使用不可观察到的投入。ASC 820根据围绕用于计量公允价值的投入的独立、客观证据的水平建立公允价值层次结构。金融工具在 公允价值层次中的分类基于对公允价值计量重要的最低投入水平。ASC 820将输入划分为可用于衡量公允价值的三个级别:
1级:适用于具有相同资产或负债的活跃市场报价的 资产或负债。
2级适用于资产或负债中存在可观察到的报价以外的其他信息的资产或负债,如活跃市场中类似资产或负债的报价;成交量不足或交易不频繁(市场不太活跃)的市场中相同资产或负债的报价;或重大投入可观察到或主要可从可观测市场数据中得出或可由可观测市场数据证实的模型衍生估值。
3级:适用于资产或负债 在估值方法中存在对计量资产或负债的公允价值具有重大意义的不可观察的输入。
本公司根据 对整体公允价值计量具有重大意义的最低水平投入,确定公允价值体系中每个公允价值计量整体所属的水平。在确定适当水平时,公司在每个报告期结束时对资产和负债进行分析 。
| F-12 |
下表在公允价值层次结构中按级别列出了公司截至2023年3月31日和2022年3月31日的资产和负债:
| 按公允价值计算的资产和负债表 | ||||||||||||||||
| 2023年3月31日 | ||||||||||||||||
| 级别 1 | 级别 2 | 第 3级 | 总计 | |||||||||||||
| 资产 | $ | — | $ | — | $ | — | $ | — | ||||||||
| 总资产 | $ | — | $ | — | $ | — | $ | — | ||||||||
| 负债 | ||||||||||||||||
| 外汇合约衍生品负债 | $ | — | $ | 731,730 | $ | — | $ | 731,730 | ||||||||
| 认股权证衍生法律责任 | — | — | 3,092,000 | 3,092,000 | ||||||||||||
| 总负债 | $ | — | $ | 731,730 | $ | 3,092,000 | $ | 3,823,730 | ||||||||
| 2022年3月31日 | ||||||||||||||||
| 级别 1 | 级别 2 | 第 3级 | 总计 | |||||||||||||
| 资产 | $ | — | $ | — | $ | — | $ | — | ||||||||
| 总资产 | $ | — | $ | — | $ | — | $ | — | ||||||||
| 负债 | ||||||||||||||||
| 外汇合约衍生品负债 | $ | — | $ | 440,196 | $ | — | $ | 440,196 | ||||||||
| 总负债 | $ | — | $ | 440,196 | $ | — | $ | 440,196 | ||||||||
截至2022年3月31日,不存在任何权证衍生品负债。下表提供了在截至2023年3月31日的年度内,使用不可观察的第三级投入,按公允价值 经常性计量的权证衍生负债的前滚,如下:
| 按公允价值经常性计量的权证衍生负债表 | ||||
3月 31, 2023 | ||||
| 认股权证法律责任 | ||||
| 期初余额--2022年3月31日 | $ | — | ||
| 于2023年1月发行认股权证时确认的认股权证负债公允价值 | 4,956,000 | |||
| 认股权证衍生负债的公允价值变动 | (1,864,000 | ) | ||
| 截至期末的余额-2023年3月31日 | $ | 3,092,000 | ||
本公司相信其金融工具(包括现金、应收账款、应付账款及应计负债)的账面金额因该等工具的短期性质而接近公允价值。
| F-13 |
退休福利计划
该公司运营着一项退休计划,该计划 覆盖了我们在英国的大多数正式员工,并允许他们做出贡献。公司还为部分员工缴费提供相应的缴费 。在截至2023年3月31日和2022年3月31日的财年中,根据该计划产生的总支出分别为37,645美元和24,300美元。
基于股票的薪酬
公司 定期向非融资交易中的员工和非员工发放股票期权和限制性股票奖励,以换取服务 和融资成本。本公司根据ASC 718对发放和归属的此类赠与进行核算,薪酬-股票薪酬 因此,奖励的价值在授予之日计量,并在归属期间以直线 为基础确认为雇员的补偿费用。确认非雇员薪酬支出的时间和方式与公司为服务支付现金的时间和方式相同。公司在其运营报表中确认股票薪酬的公允价值 ,并根据所提供服务的性质进行分类。
公司股票期权的公允价值 是使用Black-Scholes期权定价模型估计的,该模型使用了与无风险利率、预期波动率、股票期权或限制性股票的预期寿命以及未来股息相关的某些假设。 薪酬支出是根据Black-Scholes期权定价模型得出的价值和实际经验来记录的。 Black-Scholes期权定价模型中使用的假设可能会对未来 期间记录的薪酬支出产生重大影响。
股权发行产生的直接成本
本公司包括与成功发行股票有关的所有直接成本,作为额外实收资本的一部分。不成功的股票发行所产生的直接成本将计入费用。
重新分类
上一年度的某些余额已重新分类,以符合本年度的列报方式。在列报公司于2022年3月31日的综合资产负债表时,公司列报了应收增值税255,112美元,作为预付费用和其他应收账款750,167美元的一部分。在提交公司于2023年3月31日的综合资产负债表时,公司已将255,112美元的余额重新归类为单独的增值税应收项目,而495,055美元的余额在2022年3月31日的财务报表中作为预付费用列报。
最近的会计声明
本公司持续评估任何新的会计声明,以确定其适用性。当确定新的会计声明影响本公司的财务报告时,本公司将进行研究,以确定变更对其综合财务报表的影响 ,并确保有适当的控制措施,以确保本公司的综合财务报表正确反映了变更。
| F-14 |
注4- 许可协议
于2014年3月,本公司与一名无关第三方订立独家 营销权协议,授予该第三方独家权利在英国、爱尔兰共和国、海峡群岛及马恩岛以其自有品牌销售及推广SugarBEAT®设备及相关补丁。签署协议后,该公司收到了100万英镑的全额不可退还现金(截至2023年3月31日和2022年3月31日分别约为123万美元和132万美元)。
由于本协议规定本公司有持续履行义务 ,因此从本协议收到的预付费用已递延,并将在公司完成其履行义务时,在商业许可协议期限内记作收入。截至2023年3月31日,许可协议的递延总收入为1,081,676美元。
注5--库存
存货按成本(先进先出) 或可变现净值中较低者计价,其构成如下:
| 库存计划表 | ||||||||
| 2023年3月31日 | 2022年3月31日 | |||||||
| 原料 | $ | 1,586,777 | $ | 1,481,946 | ||||
| 成品 | 168,075 | 5,825 | ||||||
| 总计 | $ | 1,754,852 | $ | 1,487,771 | ||||
于2023年3月31日,管理层确定本公司存货的可变现净值已低于其历史账面成本。 因此,本公司于截至2023年3月31日的年度录得存货减记1,478,108美元,计入售出货品成本。截至2023年3月31日,上图所示的库存余额反映了减记后的新成本基础。截至2022年3月31日止年度,并无记录存货减记。
附注 6--财产和设备
截至2023年3月31日和2022年3月31日,财产和设备摘要如下:
| 财产和设备明细表 | ||||||||
| 3月31日, | ||||||||
| 2023 | 2022 | |||||||
| 财产和设备 | ||||||||
| 厂房和机械 | $ | 998,635 | $ | 727,250 | ||||
| 家具和固定装置 | 114,863 | 78,867 | ||||||
| 财产和设备毛额 | 1,113,498 | 806,117 | ||||||
| 减去累计折旧 | (471,592 | ) | (273,609 | ) | ||||
| 账面净值 | $ | 641,906 | $ | 532,508 | ||||
截至2023年3月31日和2022年3月31日止年度,与物业和设备有关的折旧支出分别约为156,000美元和138,000美元。
附注7--无形资产
下表汇总了我们在2023年3月31日的无形资产和资本化软件开发成本:
| 无形资产明细表 | ||||||||
| 3月31日, | ||||||||
2023 | 2022 | |||||||
| 专利和许可证 | $ | 1,175,580 | $ | 1,084,081 | ||||
| 累计摊销较少 | (467,091 | ) | (186,927 | ) | ||||
| 减损较少 | (324,397 | ) | — | |||||
| 384,092 | 897,154 | |||||||
| *软件开发成本 | 655,641 | 583,826 | ||||||
| 减值较少 | (655,641 | ) | — | |||||
| — | 583,826 | |||||||
| $ | 384,092 | $ | 1,480,980 | |||||
截至2023年3月31日及2022年3月31日止年度的综合经营报表内摊销支出及与无形资产有关的全面亏损分别约为193,000美元及92,000美元。截至2023年3月31日,无形资产和资本化软件成本已分别减值324,397美元和655,641美元。截至2022年3月31日,未记录任何减值
| F-15 |
附注 8--衍生负债
认股权证法律责任
本公司于2023年1月完成股权发行(见附注11),其中包括发行4,796,206份认股权证。在发生某些交易(“基本交易”,定义为“基本面交易”)时,认股权证提供一个采用布莱克·斯科尔斯模型确定的价值,其投入按照认股权证协议中所述计算,其中包括要利用的波动性投入的100% 下限。本公司已确定,此条款为认股权证持有人引入杠杆,可能导致 价值大于本公司本身股本股份的固定换固定期权的结算金额。 因此,根据ASC 815,本公司已将认股权证的公允价值归类为负债,将于每个报告期结束时根据营运报表中所报告的价值变动重新计量。
权证负债在以下 个日期使用Black-Scholes模型进行估值,该模型具有以下假设:
| 认股权证法律责任附表 | ||||||||
3月 31, 2023 | 2023年1月31日 (发布日期 ) | |||||||
| 认股权证责任: | ||||||||
| 库存 价格 | $ | 0.90 | $ | 1.33 | ||||
| 无风险利率 | 3.60 | % | 3.63 | % | ||||
| 预期波动率 | 108 | % | 109 | % | ||||
| 预期寿命(年) | 5.34 | 5.50 | ||||||
| 预期股息收益率 | — | — | ||||||
| 权证责任的公允价值 | $ | 3,092,000 | $ | 4,956,000 | ||||
无风险利率以授予时生效的美国国债收益率曲线为基础。预期波动率是根据本公司的历史波动率数据厘定,而授权证的预期期限则根据认股权证预期未清偿的时间长短而厘定。由于本公司历史上从未派发过股息,因此本公司认股权证的股息 收益率假设为零。
外汇合同责任
公司面临外汇汇率波动的影响,因为很大一部分费用是以英镑计价的,而公司的现金是以美元和英镑计价的。2021年2月,该公司签订了一份远期合同,卖出美元,买入英镑。该合同符合ASC 815指导下的衍生产品的 定义,不符合对冲会计,因此按公允价值确认 ,公允价值变动在收益中确认。
合同期限为25个月,自2022年7月至2024年8月止。合同最初的最高名义金额为6,250,000美元(最高杠杆金额等于名义金额的两倍,即12,500,000美元)。 合同名义金额中的250,000美元每月结算(到期)至2024年8月。在每个月结算日,如果美元兑英镑现货汇率高于1.359美元,公司有权以1.359美元的固定汇率将250,000美元兑换成英镑 。如果结算日的即期汇率在1.359美元至1.319美元之间,公司没有义务,但 可以按即期汇率将250,000美元兑换成英镑。最后,如果即期汇率在结算日低于1.319美元,公司有义务按1.359美元的固定汇率将500,000美元(结算日杠杆金额)转换为英镑。或者,公司可以将现汇汇率和1.359美元汇率的差额支付给交易对手500,000美元(净结算),而不是出售500,000美元。在截至2023年3月31日的年度内,杠杆金额中有4,000,000美元(以及名义金额中的2,000,000美元)到期。
在2023年3月31日和2022年3月31日,外币合同负债的公允价值如下:
| 外币合同负债公允价值表 | ||||||||
3月 31, 2023 | 3月 31, 2022 | |||||||
| 名义金额 | $ | 4,250,000 | $ | 6,250,000 | ||||
| 杠杆量(用于确定合同负债在2023年3月31日和2022年3月31日的公允价值) | $ | 8,500,000 | $ | 12,500,000 | ||||
| 预期剩余期限(月) | 17 | 25 | ||||||
| 公允价值: | ||||||||
| 外币合同责任 | $ | 731,730 | $ | 440,196 | ||||
本公司的外币远期合约按公允价值按公允价值经常性计量,并归类为第2级公允价值计量。截至2023年3月31日,本公司已向与外币远期合同相关的交易对手交存了909,666美元作为抵押品。
| F-16 |
附注9-应付票据
| 应付票据明细表 | ||||||||
| 3月31日, | ||||||||
| 2023 | 2022 | |||||||
| 票据购买协议1(已于2022年4月支付) | $ | — | $ | 270,979 | ||||
| 附注购买协议2 | 14,772,293 | 20,241,421 | ||||||
| 附注购买协议3 | 6,024,941 | — | ||||||
| *应付票据总额 | 20,797,234 | 20,512,400 | ||||||
| 未摊销债务贴现 | (767,083 | ) | (1,323,676 | ) | ||||
应付票据,扣除票据折扣后的净额 | 20,030,151 | 19,188,724 | ||||||
| 当前部分 | (16,942,500 | ) | (19,188,724 | ) | ||||
| 非流动部分 | $ | 3,087,651 | $ | — | ||||
备注采购协议1(已支付 2022年4月)
2020年4月15日,本公司向第三方投资者发行了一份 应付票据(《票据购买协议1》)。票据面额为6,015,000美元,于2022年4月15日到期 ,并以本公司所有资产作抵押。公司收到现金收益4,675,000美元,折价1,340,000美元,其中包括1,000,000美元的原始发行折扣(“OID”),从收益中支付的325,000美元的佣金,以及用于支付交易费用的15,000美元。此外,本公司记录了每月0.833%的费用,这是实质利息,年利率约为10%,每月添加到票据本金中(作为实物支付,或“实物”利息)。债务 减去贴现及交易费用乃按实际利率法于票据期限内累加。票据购买 协议1已于2022年4月偿还,并由2022年5月发行的票据购买协议3取代(见下文)。
附注采购协议2
2021年2月8日,本公司向第三方投资者发行了一份应付票据(《票据购买协议2》,《票据2》)。该票据面额为24,015,000美元,最初于2023年2月9日到期,并以本公司所有资产为抵押。本公司收到现金收益18,800,000美元,折扣额为5,215,000美元,其中包括4,000,000美元的原始发行折扣(“OID”)、从收益中支付的1,200,000美元佣金和15,000美元的交易费用。本公司同意从2021年8月开始支付本金,每月400,000美元,2022年2月增加到每月2,000,000美元。此外,本公司须按月收取相当于未偿还余额的0.833%的PIK费用,即实质利息,年利率约为10%,而票据本金则按月计算。债务减去贴现和交易费用将使用实际利率法在票据期限内增加 。
附注2于2022年5月修订, 将本金付款从每月2,000,000美元降至每月500,000美元。附注2于2022年10月再次修订,将到期日从2023年2月9日延长至2024年7月1日,并从2023年3月开始将本金支付增加到每月1,000,000美元。作为对价,本公司同意向投资者支付合共2,304,539美元的费用,并已加入附注2的本金余额。本公司根据债务清偿模型进行的修订入账,是因为修订后的附注2(“新”附注)的现值与附注2(“旧”附注)原有条款下剩余现金流的现值相差 逾10%。新票据的公允价值被确定为17,090,513美元,减去旧票据16,609,176美元的账面价值, 加上2,304,539美元的费用,导致清偿亏损2,785,876美元,这笔亏损已计入截至2023年3月31日的年度的利息支出。
| F-17 |
附注采购协议3
2022年5月20日,本公司与第三方投资者签发了应付票据(“票据 购买协议3”)。票据面额为6,015,000美元, 将于2024年5月20日到期,并以本公司的所有资产为抵押。本公司收到现金收益4,700,000美元, 折扣1,315,000美元,其中包括1,000,000美元的原始发行折扣(“OID”), 从收益中支付的300,000美元佣金,以及15,000美元用于支付交易费用。此外,本公司须按月收取相当于未偿还余额的0.833%的PIK费用,该余额为实质利息,年利率约为10%, 每月加入票据本金。债务减去贴现和交易费用将使用有效利率法在票据期限内增加。截至2023年3月31日,有待摊销的剩余债务贴现为767,083美元。
附注10--关联方交易
Nemaura Pharma Limited(“Pharma”)、 黑白医疗保健有限公司(“B&W”)和NDM Technologies Limited(“NDM”)是由公司首席执行官和大股东控制的实体。
Pharma与DDL签订了一项服务协议,根据Pharma的ISO13485认证进行开发、制造和监管审批。Pharma定期为上述服务开具DDL发票。服务按成本价外加不到总成本10%的服务附加费提供。
以下是截至2023年3月31日至2022年3月31日本公司与Pharma、B&W和NDM之间的活动摘要:
| 关联方交易明细表 | ||||||||
| 3月 31, | ||||||||
2023 | 2022 | |||||||
年初欠关联方[来自]关联方 | $ | (101,297 | ) | $ | 148,795 | |||
Pharma向DDL、NM和TCL开具的发票金额主要涉及 研发费用 | 4,767,586 | 3,245,985 | ||||||
| DDL向Pharma开出的发票金额 | — | (2,495 | ) | |||||
| DDL向Pharma偿还的金额 | (3,773,217 | ) | (3,492,962 | ) | ||||
| 外汇差额 | 27,708 | (620 | ) | |||||
应于年底付给关联方/来自关联方 | $ | 920,780 | $ | (101,297 | ) | |||
附注11--所得税
本公司及其子公司分别提交 所得税申报表。
美利坚合众国
本公司在美国注册成立,截至2023年3月31日的年度需缴纳21%的美国联邦企业所得税税率,截至2022年3月31日的年度需缴纳21%的美国联邦企业所得税税率。
英属维尔京群岛
RGL在英属维尔京群岛(“BVI”)注册成立。 根据英属维尔京群岛的现行法律,RGL无需缴纳所得税或资本利得税。此外,在RGL支付股息时,不征收英属维尔京群岛预扣税。在截至2022年3月31日和2021年3月31日的年度内,英属维尔京群岛没有收入或支出;截至2021年4月23日,RGL正式解散。
| F-18 |
英国
DDL、TCL和DDHL均在英国注册成立,这些公司适用的英国法定所得税税率为19%。
在截至2023年3月31日和2022年3月31日的财政年度,英国和美国出现所得税优惠前的亏损情况如下:
| 所得税前损益表 | ||||||||
| 3月 31, | ||||||||
2023 | 2022 | |||||||
| 在英国发生的所得税前亏损 | $ | (13,314,440 | ) | $ | (11,716,916 | ) | ||
| 在美国发生的所得税前亏损 | (829,295 | ) | (2,520,145 | ) | ||||
| 所得税优惠前总亏损 | $ | (14,143,735 | ) | $ | (14,237,061 | ) | ||
我们的有效税率与按法定美国联邦税率计算的亏损的对账如下:
| 有效税率对账 | ||||||||||||||||
| 3月31日, | ||||||||||||||||
| 2023 | 2022 | |||||||||||||||
| 所得税前亏损 | $ | (14,143,735 | ) | $ | (14,237,061 | ) | ||||||||||
| 预期税收优惠 | (3,145,943 | ) | (22 | %) | (2,989,783 | ) | (21 | %) | ||||||||
| 外国税差 | 235,938 | 2 | % | 234,338 | 2 | % | ||||||||||
| 加强研究和开发 | (369,946 | ) | (3 | %) | (463,591 | ) | (3 | %) | ||||||||
| 前一年北环线的实况 | (46,393 | ) | 0 | % | 2,401,930 | 17 | % | |||||||||
| 其他 | 338,278 | 2 | % | 74,579 | 1 | % | ||||||||||
| 更改估值免税额 | 2,988,066 | 21 | % | 742,527 | 5 | % | ||||||||||
| 获得R&D积分 | — | — | 350,256 | 2 | % | |||||||||||
| 实际所得税优惠 | $ | — | — | $ | 350,256 | 2 | % | |||||||||
导致较大部分递延所得税资产的暂时性差异的税收影响如下:
| 递延所得税资产表 | ||||||||
| 3月 31, | ||||||||
| 2023 | 2022 | |||||||
| 营业税金净亏损 结转 | $ | 9,259,000 | $ | 6,671,000 | ||||
| 研究和开发增强 | 361,000 | 335,000 | ||||||
| 其他项目 | 38,000 | (335,000 | ) | |||||
| 估值免税额 | (9,658,000 | ) | (6,671,000 | ) | ||||
| 递延净额 纳税资产 | $ | — | $ | — | ||||
在截至2023年3月31日的财政年度内,本公司未收到英国税务及海关总署(HMRC)就截至2022年3月31日的财政年度内发生的研发开支所作的税项抵免报销 。在截至2022年3月31日的财年中,公司从英国税务及海关总署获得了350,256美元的税收抵免,用于偿还截至2021年3月31日的财年发生的研发费用。
对于截至2023年3月31日和2022年3月31日的每个财政年度,本公司没有未确认的税收优惠,因此不会产生与未确认的税收优惠相关的利息或罚款 。管理层预计未确认税项优惠金额在未来12个月内不会有重大变化。
该公司主要在美国和英国提交所得税申报单。从2019年开始的纳税年度,该公司须接受美国税务机关的联邦所得税审查。在英国 从2018年4月1日开始的纳税年度,公司英国子公司的纳税申报单可供英国税务机关审查。
截至2023年3月31日,该公司在美国和英国的净营业亏损分别约为11,300,000美元和36,230,000美元。NOL可以无限期结转 。此外,该公司还为英国所得税申报结转了大约1,899,000美元的研究和开发增强扣减。
| F-19 |
附注12--股东权益
本公司以S-3表格向美国证券交易委员会备案,于2022年03月24日被美国证券交易委员会宣布生效(《2022年货架登记书》)。根据可用股份的不同,《2022年货架注册声明》使公司能够不时发行注册声明中所述的普通股和其他证券,总金额最高可达2.246亿美元。
2023年1月,停战资本有限责任公司和Alyeska Master基金有限责任公司同意以每股1.75美元的价格购买总计4796,206股普通股,外加认股权证,以每股2.00美元的行使价购买4796,206股普通股。扣除737,385美元的成本前,总收益为8,393,361美元。
2021年7月23日,本公司与H.C.Wainwright&Co.,LLC订立了一项在市场上 发售协议(“2021年自动柜员机”),根据该协议,本公司可不时按其选择发售及出售合共1亿美元的普通股(于2022年4月1日修订为300万美元)。
在截至2022年3月31日的年度内,本公司按2021年自动柜员机按每股4.07美元的平均价发行及出售了397,524股普通股(包括向Tiger Trading Partners L.L.C.出售的375,000股,见下文),扣除佣金及公司应付的发售费用后,净收益合计为160万美元 。
在截至2022年3月31日的年度内,本公司同意以每股4美元的价格向Tiger Trading Partners L.L.C.(Tiger Management L.L.C.(Julian H.Robertson家族办公室的工具)的关联公司)出售750,000股股票;其中375,000股在上述2021年自动取款机设施内出售,其中375,000股在2022年2月10日完成的直接发行中出售。
股票期权
截至2023年3月31日和2022年3月31日的年度期权活动摘要如下:
| 选项奖励活动时间表 | ||||||||||||
| 选项数量 | 加权 平均行权价格: | 权重 平均剩余合同期限(年) | ||||||||||
| 2021年4月1日的余额 | — | — | ||||||||||
| 授与 | 40,000 | $ | 3.98 | |||||||||
| 已锻炼 | — | — | ||||||||||
| 被没收 | — | — | ||||||||||
| 过期 | — | — | ||||||||||
| 2022年3月31日的余额 | 40,000 | 3.98 | 4.83 | |||||||||
| 授与 | — | — | ||||||||||
| 已锻炼 | — | — | ||||||||||
| 被没收 | — | — | ||||||||||
| 过期 | — | — | ||||||||||
| 2023年3月31日的余额 | 40,000 | $ | 3.98 | 2.7 | ||||||||
| 于2023年3月31日归属并可行使 | 40,000 | $ | 3.98 | 2.7 | ||||||||
在截至2023年3月31日的财政年度内,未授予任何股票期权。他说:
2022年1月28日,董事会授予其董事购买40,000股普通股的期权,行权价为每股3.98美元,这是授予日公司普通股的收盘价。该等购股权于授出时获悉数授予,并可于授出日期起计五年内行使。股票期权的公允价值通过布莱克-斯科尔斯期权定价模型确定为133,529美元,其假设如下:
| 主要假设明细表 | |
| 股价 | $3.98 |
| 行权价格 | $3.98 |
| 术语 | 5年 |
| 波动率 | 122.52% |
| 预期股息率(%) | — |
| 贴现率(债券等值收益率) | 2.28% |
| F-20 |
认股权证
以下是截至2023年3月31日和2022年3月31日的认股权证活动摘要:
| 认股权证活动时间表 | ||||||||||||
| 认股权证数量 | 加权 平均行权价 | 权重 平均剩余合同期限(年) | ||||||||||
| 2021年4月1日的余额 | 1,939,990 | $ | 6.30 | 4.62 | ||||||||
| 授与 | — | — | ||||||||||
| 已锻炼 | (366,892 | ) | 8.08 | 4.08 | ||||||||
| 被没收 | — | — | ||||||||||
| 过期 | — | — | ||||||||||
| 2022年3月31日的余额 | 1,573,098 | 6.64 | 4.07 | |||||||||
| 授与 | 4,796,206 | 2.00 | 5.00 | |||||||||
| 已锻炼 | — | — | ||||||||||
| 被没收 | — | — | ||||||||||
| 过期 | — | 5.00 | — | |||||||||
| 2023年3月31日的余额 | 6,369,304 | $ | 2.7 | 4.87 | ||||||||
| 于2023年3月31日归属并可行使 | 6,369,304 | $ | 2.7 | 4.87 | ||||||||
注13--或有事项
新冠肺炎
新型冠状病毒 (新冠肺炎)的全球暴发已导致全球一般经济活动严重中断,因为企业和政府已采取广泛行动 来缓解这一公共卫生危机。鉴于新冠肺炎传播的不确定性和不断变化的形势,此次疫情可能会对公司构成风险。冠状病毒对公司业务运营的影响程度 将取决于未来的发展,这些发展具有高度的不确定性,目前无法预测。该公司打算继续 监测新冠肺炎的全球疫情,并正在与我们的员工、供应商和其他利益相关者合作,以降低其传播带来的风险 。新冠肺炎预计不会对公司的成功产生任何长期不利影响。虽然在我们的运营地点与新冠肺炎相关的限制已基本取消,但我们将继续评估情况,包括遵守任何 政府施加的限制,视情况而定。
通货膨胀率
通货膨胀、利率上升、政府应对措施以及由此可能导致的经济衰退等宏观经济因素也给我们的业务增加了重大不确定性,并可能 影响公司未来可获得的融资金额和类型。
附注14--后续活动
本公司对截至美国证券交易委员会提交该等合并财务报表之日为止的后续事件进行评估,并确定并无任何重大后续事件影响或可能影响合并财务报表中的金额或披露。
| F-21 |

Nemaura Medical,Inc.
最高可达4796,206
普通股股份
招股说明书
2023年8月7日
至2023年9月16日(含该日)( 40这是),所有交易这些证券的交易商,无论是否参与此次发行,都可能被要求提交招股说明书。这是交易商在作为承销商并就未售出的配售或认购提交招股说明书的义务之外的义务。