(1) 截至2022年6月30日和2021年12月31日,该公司的限制性现金分别为0美元和1,146,186美元。
经营活动
截至2023年6月30日的六个月中,用于经营活动的净现金为1,290万美元,而去年同期为1,300万美元。
在截至2023年6月30日的六个月中,用于经营活动的净现金为1,290万美元。在截至2023年6月30日的六个月中,经营活动产生的现金流变化是由于持续经营的净亏损为830万美元,运营资产和负债的变化增加了70万美元,已终止业务中使用的现金为580万美元。除此之外,持续经营业务还获得了50万美元的股票薪酬。
在截至2022年6月30日的六个月中,用于经营活动的净现金为1,300万美元。在截至2022年6月30日的六个月中,经营活动产生的现金流变化是由于持续经营净亏损1,100万美元,运营资产和负债的变化减少了310万美元,终止业务中使用的现金减少了90万美元。此外还有200万美元的股票薪酬。
投资活动
投资活动提供的净现金为1,870万美元,主要来自出售折扣业务中的资产。
在截至2022年6月30日的六个月中,用于投资活动的净现金为470万美元,用于购买不动产和设备以及与我们的制造工厂相关的在建工程。
融资活动
在截至2023年6月30日的六个月中,融资活动提供的净现金为60万美元,这要归因于根据自动柜员机协议和林肯公园购买协议(定义见下文)出售普通股。
未来资本要求
迄今为止,我们尚未从经批准的药品的商业销售中获得任何收入,而且我们预计至少在未来几年内不会产生可观的收入。如果我们未能及时完成候选产品的开发或未能获得监管部门的批准,我们未来创造收入的能力将受到损害。我们不知道何时或是否会从候选产品中获得任何收入,除非候选产品获得监管部门的批准并将其商业化,否则我们预计不会产生可观的收入。我们预计,由于我们正在进行的活动,我们的支出将增加,尤其是在我们继续研究和开发、继续或启动候选产品的临床试验以及寻求上市批准的情况下。此外,如果我们的任何候选产品获得批准,我们预计将产生与销售、营销、制造和分销相关的巨额商业化费用。我们预计,在持续运营方面,我们将需要大量额外资金。如果我们无法在需要时或以有吸引力的条件筹集资金,我们可能被迫推迟、减少或取消我们的研发计划或未来的商业化工作。
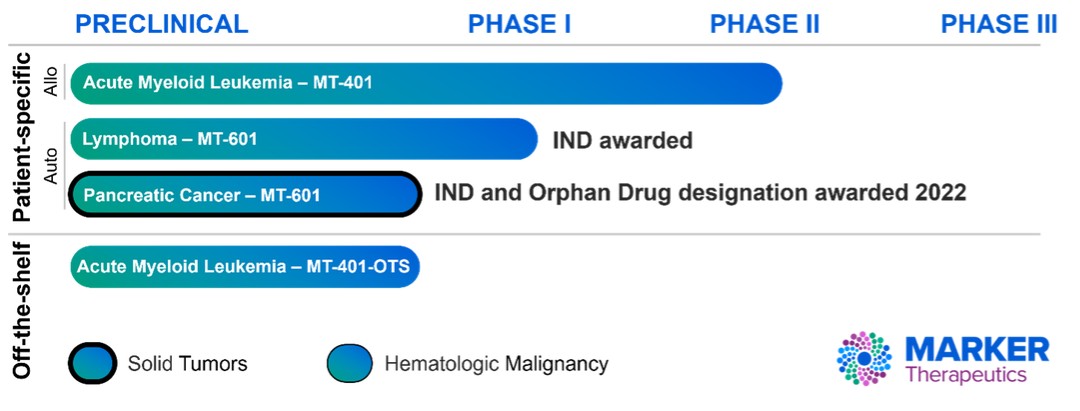
2021 年 8 月,我们收到 CPRIT 提供的总额约为 1,310 万美元的产品开发研究奖励通知,用于支持我们的 MT-401 二期临床试验。CPRIT 奖项旨在支持该公司 2 期临床试验的辅助部门,该试验评估 MT-401 在造血干细胞移植后作为辅助疗法给予急性髓系白血病患者。与随机对照组相比,该试验辅助部分的主要目标是评估 MT-401 治疗后的无复发存活率。迄今为止,我们已经从CPRIT的拨款中获得了690万美元的资金。
2022 年 9 月,我们收到了美国食品药品监督管理局(FDA)的通知,称美国食品药品监督管理局(FDA)孤儿产品补助计划向我们发放了 200 万美元的补助金,用于支持我们用于治疗移植后急性髓细胞白血病的 MT-401 第 2 期临床试验。迄今为止,我们已经从林业发展局的拨款中收到了20万美元的资金。
2023年6月26日,我们完成了先前宣布的与Cell Ready的交易。根据自截止日期起生效的Cell Ready购买协议,我们将购买的资产(如适用)分配并出售给了Cell Ready。截止日期之后,