
2023 年 8 月公司简报 1

前瞻性陈述 2 本演示文稿包含1995年《私人证券诉讼改革法》所指的前瞻性陈述。任何描述Acumen的目标、预期、财务或其他预测、意图或信念的陈述均为前瞻性陈述,应被视为风险陈述。诸如 “相信”、“期望”、“预期”、“可以”、“将”、“寻求”、“目标”、“计划”、“潜力”、“意志” 等词语旨在识别前瞻性陈述,尽管并非所有前瞻性陈述都包含这些识别词。前瞻性陈述包括关于 Acumen 业务、Acumen 实现其战略和财务目标的能力(包括其现金、现金等价物和有价证券的预计使用情况及其现金资源的充足性)以及 Acumen 候选产品 ACU193 的治疗潜力的陈述,包括与正在开发的其他单克隆抗体相比,其安全性和有效性得到提高的可能性,以及对 INCTERPT-AD 试验和 Acumen 计划中的第 2 阶段试验的预期 3 项临床试验,包括预计启动试验的时间。这些陈述基于Acumen管理层当前的信念和期望,受某些因素、风险和不确定性的影响,尤其是发现、开发和商业化安全有效的人类疗法过程中固有的因素、风险和不确定性。COVID-19 疫情的影响可能会加剧此类风险。Acumen向美国证券交易委员会(“SEC”)提交的文件中更详细地描述了与Acumen计划有关的这些风险和其他风险,包括Acumen最新的10-K年度报告表以及Acumen未来的文件和报告。这些文件和其他文档的副本可从 Acumen 获得。Acumen不时向美国证券交易委员会提交的其他文件中将提供更多信息。这些前瞻性陈述仅代表截至本文发布之日,Acumen明确声明不承担任何更新或修改任何前瞻性陈述的义务,除非法律另有要求,无论是由于新信息、未来事件还是其他原因。在本列报中,提及的现金还包括现金等价物。

3 推进针对早期阿尔茨海默氏病 (AD) 的潜在同类最佳抗体产品 • 市场庞大 • 需求未得到满足 • 最近的科学和监管势头 • β淀粉样蛋白低聚物 (aβOS) 被视为毒性最强的 Aβ • 潜在有效的 AD 治疗的新靶标 ACU193:第一种选择性靶向 AβOS 的临床阶段单克隆抗体 (mAb) • 经验丰富的领导团队 • AD 临床、药物开发和监管礼来公司的领导者 • 7 月份公布的针对早期 AD 患者 1 期临床试验的积极结果2023 • 强劲的资产负债表:截至 6 月 23 日,现金约为 1.72 亿美元 • 2023 年 7 月 FPO 净收益约为 1.22 亿美元我们相信 Acumen 拥有将 ACU193 推进 2026 年下半年的组织专业知识和财政资源

Acumen Business Strategy:2023-2026 4 → 通过对早期 AD 患者的临床开发快速推进 ACU193;→ 评估组合方法以补充我们的核心 ACU193 单一疗法战略;→ 通过许可和/或开发更多候选药物和/或替代配方或衍生物 ACU193 来扩大我们的产品组合;→ 优化 ACU193 和未来候选药物在主要市场的价值。

AD、淀粉样蛋白和 Abeta 低聚物

6 阿尔茨海默病病理学中的β淀粉样蛋白低聚物 (AβOS)

毒性 aβO 代表理想的阿尔茨海默病药物靶标 7 AβOS 在 AD 1Cleary 等人,2005 年;Townsend 等人,2006 年;Poling 等人,2008 年;Reed 等人,2011 年;Batista 等人,2018 年。2Shankar 等人,2007 年。3Ferreira,S. T. 和 Klein,W. L.,2011 年。4Lambert 等人,2011 年。4Lambert 等人,2011 年。al.,1998;Walsh 等人,2002 年;Wang 等人,2002 年;Klyubin 等人,2005 年;Townsend 等人,2006 年;Shankar 等人,2007 年、2008 年。5De Felice 等人,2008 年;Zempel 等人,2010 年;Ochalek 等人,2017 年。突触功能受损1 大鼠器官型切片中的金字塔神经元在暴露于 picomolar 水平的可溶性低聚物后,树突刺的密度和电生理活性突触的数量明显下降2 1 导致记忆和认知受损3 已发现可溶性 AβO(但不是单体)会阻断海马长期增强(LTP),a 记忆与学习的突触相关性4 2 诱导 tau 过度磷酸化5 2008 年证明 aβOS 能够诱导 tau 过度磷酸化没有纤维的神经元5 3

• 为靶向毒性 Aβ 低聚物而开发的人源化、亲和力成熟的单克隆抗体 • AβOS 的选择性比 Aβ 单体高 >500 倍 • ABO 的选择性大于 Ab 原纤维 85 倍 • 效应器功能降低的 IgG2 亚类 mAB • 与 Aβ 斑块定向的 maB 相比,AβOS 的选择性更高,ARIA-E 可能更具选择性 • ACU193 是 Acumen 研究合作的一部分还有 Merck & Co. • 目前由礼来公司全球阿尔茨海默氏症开发团队的几位前高级成员开发 • ACU193 已获得 Fast Track美国食品药品管理局指定用于治疗早期阿尔茨海默氏病 ACU193:一种选择性结合毒性 AβOS 的单克隆抗体 ACU193 对毒性 AβOS 的高选择性,可以提供有意义的认知功效,提高安全性和耐受性 8

9 ABO 可能由 2 到 >200 个 Ab 肽组成 Ab 肽什么是 Aβ 低聚物?____________________ 资料来源:Kelley 等人《化学物理学杂志》2008。图 1。由 3 (a) 和 18 (b) Ab 肽组成的 ABO 如下所示。____________________ 来源:Relini 等人Biomolecules 2014。图 2。淀粉样蛋白聚集代表性步骤的原子力显微镜图像:(A)低聚物;(B)原原纤维;(C)成熟原纤维。扫描尺寸 1.0 微米。Z 范围 (A) 8.0 nm;(B) 15 nm;(C) 20 nm。Aβ 低聚物、原纤维和原纤维的四元结构 (a) (b)

10 * 结合淀粉样蛋白斑块的 IgG1 单克隆抗体与 ARIA-E 的高发率有关。例如,参见 Plotkin,《疾病神经生物学》,2020 年。• 上面列出的任何候选产品之间都没有进行过正面交锋的临床试验。每种候选产品的研究设计和方案都不同,候选产品的结果可能无法比较。1 AAP:加速批准 solanezumab igG1、ph3 stop、A4、DIAN 阴性 lecanemab igG1 Ph3 阳性 3Q22 已获批准 (AAP1) 2023 年 7 月 aducanumab* iGG1 批准 (AAP1),CMS CED 商业停止 ACU193 iGG2 Ph1 阳性 3Q23 bapineuzumab* Igg1,ph3 stop gantenerumab* igG1 Ph3 阴性 4Q22 crenezumab igG4,ph3 停止,API 阴性 Aβ 低聚物 donanemab* Igg1 Ph2 阳性 CRL 1Q23 (AAP1) Ph3 阳性 2Q23 Aβprotofibrils ACU193 相对于后期阶段和经批准的 Anti-Ab/Place mAbs 的定位 ACU193 对 AβOS 的高选择性,加上后续研究中预期的 ARIA 发生率较低,预计与抗斑块单克隆抗体相比,将提供更好的安全性和有效性

药物:ACU193 是一种人源化、亲和力成熟的单克隆抗体,对毒性 aβOS 与 Aβ 单体(>500x)具有很高的选择性,ABO 的选择性大于 Ab fibrils 的 85 倍 ACU193 是一种 IgG2 亚类 mAb,效应器功能降低。人群:早期 AD — AD 引起的轻度认知障碍和轻度痴呆剂量:每 4 周静脉输注一次,计划持续时间:AD 早期 AD 期间的慢性治疗价值主张:与非选择性抗 aβ/斑块单克相比,毒性 aβO 的选择性可能提供有意义的认知功效以及更高的安全性和耐受性,包括:• 减缓 AD 早期记忆力和认知能力下降 • 减少 AβO 诱导的记忆力和耐受性突触和神经元网络毒性 • 减缓疾病进展和对下游的影响tau、神经变性和神经炎症 • 在随后的研究中,ARIA 的发病率预计较低 • 作为独立疗法或与其他有症状、抗炎和/或 tau 定向的疗法联合使用可能有效 ACU193 目标产品简介:同类最佳、一线、抗 AβO、疾病改良免疫疗法,适用于 AD 11 早期

(1) 上面列出的任何候选产品之间都没有进行过正面交锋的试验。每种候选产品的研究设计和方案都不同,候选产品的结果可能无法比较。(2)Goure等人(2014)。靶向适当的β淀粉样蛋白神经元毒素:阿尔茨海默病免疫治疗的前进道路。阿尔茨海默氏症的研究与治疗。6:42。DOI:http://alzres.com/content/6/4/42。(3) 第 3 阶段因主要 AD 适应症而停止。(4) van Dyck,C. (2017)。阿尔茨海默病的抗淀粉样蛋白B单克隆抗体:陷阱与希望。生物精神病学。83:4,311-319。DOI:https://doi.org/10.1016/j.biopsych.2017.08.010。mAb 表位/isotype (4) Ab 靶点选择性 (1) (2) 安全概况公司资产单体斑块纤维低聚物 ARIA-E (4) 功效概况 ACU193 N 期,确诊性 IgG2-+ ++++ 预计第二阶段处于低位 Eisai /Biogen leqembitM N 期,确认 IgG1-+++ + protofibrils +++ 低阳性 ph2 和 ph3 CLARITY-AD Lilly donanemab n3pg igg1-++++ ++-高阳性 ph2 和 ph.3 开拓者 Biogen AduhelmtM n-term Igg1-++++ phig ph3 呈阳性,与负面罗氏交战gantenerumab (3) n-term + Mid domain Igg1-++++ ++ ++ High ph3 负值礼来索拉尼珠单抗 (3) Mid domain /igG1 +++----无 ph3 负值,没有趋势辉瑞/Janssen bapineuzumab (3) n-term IgG1 ++ ++ ++ ++ ++ ++ 最近和目前正在开发的抗 Ab 抗体的高 pH3 阴性比较特征 12

ACU193:价值主张 13 阿尔茨海默氏病市场正处于关键转折点,最近和预期的批准为 AD 的治疗铺平了新的道路... 而 ACU193 完全有能力成为潜在的首选治疗方法。在未来几年中,随着Abo疗法成为主要治疗选择,市场可能会保持整合,利益相关者对AD治疗领域的进步感到鼓舞,他们正在共同努力实现更广泛的患者获得机会。由于aBo选择性具有潜在的临床和安全益处,ACU193 有机会成为更广泛的早期 AD 人群的首选治疗方法

ACU193 的 INCTERCT-AD 第 1 阶段结果呈阳性

INCERT-AD:AD 早期患者的随机安慰剂对照 1 期 15 Q2W:每两周给药一次;Q4W:每四周给药一次。A 部分:单次递增剂量 n = 每队列 8(总共 32 个)B 部分:多重递增剂量 n = 每队列 10 剂(总共 30 次)3 次药物或安慰剂;每队列 8:2 1:2 mg/kg ACU193 或安慰剂 2mg 队列 2:10 mg/kg ACU193 或安慰剂 10mg 队列 3:25 mg/kg ACU193 或安慰剂 25mg 队列 4:60 mg/kg ACU193 或安慰剂 60mg 队列 5:10 mg/kg ACU193 或安慰剂 (Q4W) 10mg 队列 6:60 mg/kg ACU193 或者安慰剂 (Q4W) 60mg 队列 7:25 mg/kg ACU193 或安慰剂 (Q2W) * ≥ 1wk ≥ 1wk ≥ 1wk ≥ 1wk ≥ 1wk ≥ 1wk ≥ 1wk ≥ 1wk

16 在研究的更高剂量(60 mg/kg Q4W 和 25 mg/kg Q2W 队列)下观察到的快速、剂量相关、具有统计学意义的淀粉样蛋白斑块减少* • 与目前批准的临床开发相似时间点的 Aβ 单克隆抗体可与剂量相关的第一种以剂量相关方式展示靶向参与的抗体 • 血清和脑脊液暴露剂量成正比;抗体浓度明显超过脑脊液中内源性低聚物的水平 • 研究的最高剂量(25 mg/kg Q2W 和 60mg/kg Q4W)接近最大目标参与度(23.2 au/mL Emax)令人信服的总体安全性,ARIA-E 的比率很低 • 没有已知的药物相关的 SAE;治疗新发的 ADAS 滴度一直很低 • 在 10 mg/kg Q4W 剂量时没有出现症状 ARIA-E • 在 Apoe4 纯合子 (n=6) 广泛治疗指数中没有观察到 ARIA-E;通往更方便的每月给药方案的明确途径 1 2 3 4 *群组内从基线到终点的统计学显著降低 (p = 0.01) INCTERCT-AD 结果证实 ACU193 的机制证明以及证明在研究的更高剂量下淀粉样蛋白斑块会减少

机制证明表明 ARIA-E 水平低,与剂量相关的靶标参与度,CSF ACU193 水平超过 abO 水平,支持 Q4W 给药 17 种潜在的治疗剂量终点关键成功因子 10mg/kg 25mg/kg 60mg/kg 安全性和耐受性 • 死亡、与研究药物相关的 SAE 无任何• 任何 ARIA-E 1/14 (7.1%) 3/14 (21.4%) • 有症状 ARIA-E 0/14 (21.4%) (21.4%) (21.4%) (0.0%) 0/14 (0.0%) 1/14 (7.1%) PK • 剂量相关 PK • 脑脊液暴露量达到内源性脑脊液低聚物水平以上(明显高于报告的 Aβ 低聚物水平)已实现(比报告的 Aβ 低聚物水平高几个数量级)已实现(比报告的 Aβ 低聚物水平高几个数量级)目标参与度 • 脑脊液测量中对 acu193-Ab 寡聚物复合物的测量实现剂量相关;接近最大目标参与度剂量相关;接近最大目标参与度淀粉样蛋白 PET • MAD 队列中淀粉样蛋白 PET 减少未观察到减少(p = 0.01) MAD 同类群组内的减少 (p = 0.01)
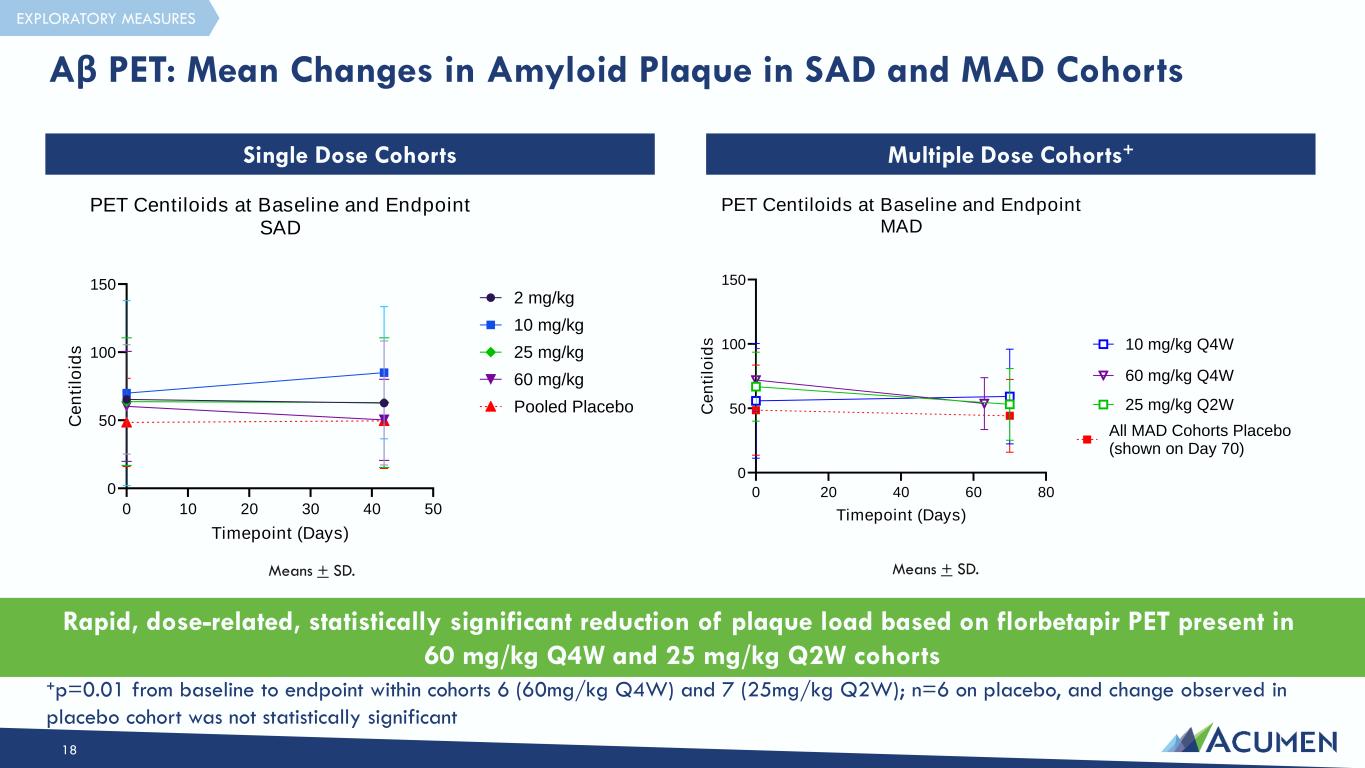
根据存在于 60 mg/kg Q4W 和 25 mg/kg Q2W 群组 Means + SD 中的 florbetapir PET,可以快速、剂量相关且具有统计学意义的斑块负荷降低。意思是 + SD。+p=0.01 在群组 6(60mg/kg Q4W)和 7(25mg/kg Q2W)中从基线到终点;使用安慰剂 n=6,在安慰剂队列中观察到的变化在统计学上并不显著 Aβ PET:SAD 和 MAD 队列中淀粉样蛋白斑块的平均变化 18 单剂量队列多剂量队列+ 探索性措施 0 20 40 60 80 0 50 100 150 PET centiloids 在基线和终点 MAD 时间点(天)C e n ti lo id s 所有 MAD 队列安慰剂(显示在第 70 天)25 mg/kg Q2W 60 mg/kg Q4W 10 20 30 40 50 50 100 150 PET centiloids 在基线和终点 SADTimepoint (Days) C e n ti lo id s 2 mg/kg 10 mg/kg 25 mg/kg 60 mg/kg 汇集安慰剂

Aβ PET:个体患者在 60 mg/kg Q4W 时的 60 mg/kg Q4W 和 7 队列在 25 mg/kg Q2W 时淀粉样蛋白斑块的变化 19 在 60 mg/kg Q4W 和 25 mg/kg Q2W 队列中,大多数患者在 63 或 70 天后斑块负荷有所减少。探索性措施

30 40 50 60 70 80 90 天 0 天 63 天 70 天 90 最高剂量的 ACU193 表明淀粉样蛋白斑块减少速度快可与 Lecanemab(处于第 3 阶段)相当 20 淀粉样斑块(centiloids)的平均减少 ACU193 60 mg/kg Q4W (n=8) * ACU193 25 mg/kg Q2W (n=8) * Lecanemab 10 mg/kg Q2W (n=344) 索引值绝对值(p=0.01 表示淀粉样蛋白斑块在 ACU193 队列中从基线到终点的变化)-30 -25 -20 -15 -5 0 第 0 天 63 天 70 天 (25.3%) (20.6%) (25.7%) (18.1) (13.7) (20.0) p=0.01P=0.01 *统计学队列内从基线到终点的显著减少(p = 0.01)。资料来源:Acumen Pharmicals,存档数据;van Dyck(2023),NEJM(根据图表估算淀粉样蛋白 PET 减少量);累计给药药物:ACU193 60mg/kg = 180 mg/kg(给药三剂);ACU193 25mg/kg = 75mg/kg(给药三剂)注意:上面列出的候选产品之间没有正面交锋的临床试验。每种候选产品的研究设计和方案都不同,因此,候选产品的结果可能无法比较。探索性措施

SAD MAD 10 mg/kg Cohorts 2、5 25 mg/kg 同组 3、7 60 mg/kg 同组 4、6 NO ARIA-E 无症状 ARIA-E 有症状 ARIA-E 已停产 ApoE D21 3,4 3,4 PBO 3,4 3,4 PBO 3,4 d126 3,4 3,4 PBO D126 3,4 3,4 PBO PBO 3,3 3,4 3,4 3,4 PBO PBO 3,3 Apoe D28 D70 D196 2,3 3,3 3,3 3,3 3,3 PBO PBO 3,4 3,3 3,4 3,4 PBO PBO 3,3 3,3 PBO 3,3 3,3 Apoe D70 98 3,3 3,4 3,4 3,4 3,4 PBO PBO 3,3 3,4 PBO PBO 4,4 4,4 Apoe D21 D140 4,4 PBO 3,4 3,4 PBO 3,3 3,4 2,4 2mg/kg Cohort 1 ApoE D21 D140 3,4 3,3 PBO 3,4 2,3 3,4 PBO 3,3 3,3 ARIA-E INCTERCT-AD 21 没有 ε4 纯合子尽管在研究中占 13% 但仍会出现 ARIA-E;4/5 ARIA-E 病例是 ε4 杂合子,占我们研究人群的 47% PBO:服用安慰剂安全的患者

ACU193 Serum PK 22 单剂量队列多剂量队列血清暴露量与剂量成正比,没有积累 PHARMAKINETICS 估计血清末端 T1/2 为 5-7 天

与剂量相关的脑脊液 ACU193 暴露量:高于内源性脑脊液 aβO 水平 23 个单剂量队列多剂量队列* 脑脊液暴露量与剂量方案成正比 *排除了来自队列 5(10 mg/kg Q4W)的一名患者,因为只服用了一次药物(空隙性梗塞后研究药物停用)。药代动力学

ACU193 药物特异性捕获(抗 acu193 idiotype maB)24 通过测量 CSF 中的 acu193-Abo 复合物来评估目标参与度 abO 选择性检测(抗 ABO maB)只有药物/ABO 复合物是可测量的新型测定配置,专为选择性检测脑脊液中的 acu193-Abo 复合物作为靶点参与度的直接衡量标准 acu193-Abo 复合物 MSD S-Plex (Turbo) 免疫分析靶点参与度而量身定制的新型测定配置

ACU193 与 aβOS 的目标参与是剂量比例 25 个单剂量队列多剂量队列* 2 mg/kg 10 mg/kg 25 mg/kg 60 mg/kg 0 10 20 30 ACU193 IV 输液剂量 C S F A C U 1 9 3-a β O li g o m e r c o m le x (A U /m L) a t V 是 8 (D a y 2 1) 剂量相关目标参与度 *一名患者从第5组群(10 mg/kg Q4W)中排除在外,因为只服用了一次药物(研究药物在空隙性梗塞后停用)。目标参与度 p = 0.001 p = 0.03 p = 0.0007没有显著差异

剂量为 25 mg/kg Q2W 和 60 mg/kg Q4W 26 单剂和多剂量队列——暴露反应关系(Emax 模型)Emax:23.2 au/mL acu193-aβO 复合物 EC50:1.43 x 105 pg/mL ACU193 目标参与度 *排除了来自队列 5(10 mg/kg Q4W)的一名患者,因为只服用了一次药物(研究药物在 lack 后停药)月球梗塞)。再加上令人信服的安全特征和快速减少斑块,接近最大TE的剂量应指导下一个研究阶段的剂量选择

第 1 阶段数据支持进入第 2/3 期在较高剂量队列中观察到的快速、剂量相关、具有统计学意义的淀粉样蛋白斑块减少 Topline 结果表明 ACU193 的机制证明,第一临床阶段 aβO 靶向抗体 ACU193 在早期 AD 患者中耐受性良好;没有与药物相关的 SAE;ARIA-E ACU193 的低比率接近毒性 aβO 的最大中心靶点参与度,确立了广泛的中心靶点参与度治疗指数和每月方便给药的途径探索性措施:— 正如预期的那样,在这项持续时间短的小型研究中,临床认知测量没有观察到任何效果——正如预期的那样,在这项持续时间短的小型研究中,使用核磁共振ASL脉冲序列没有观察到任何效果——预计2023年第四季度流体生物标志物数据 27 令人信服的机制证明了下一步行动:预计2023年第四季度美国食品药品管理局互动;预计在2024年上半年启动第二阶段

ACU193:临床前数据

ACU193:支持开发的大量数据包 ACU193 是一种很有前途的早期 AD 免疫疗法,有望提供有意义的认知和功能益处,减缓疾病进展,并提供有吸引力的安全性。AβOS 的纳米摩尔亲和力,AβOS 的选择性比 Aβ 单体高出 500 倍以上,与血管淀粉样蛋白或密集的核心淀粉样蛋白斑块的结合有限或根本没有可辨别的内源性 Aβ,从二聚体到高分子量 aβOS 大脑渗透和生物分布,在多个物种中都得到了证实表现与其他外周给药的中枢神经单克隆抗体在多种体外神经保护测定中的剂量依赖性效应 AD IgG2 亚类的多个体内转基因小鼠模型的积极记忆和行为效应缺乏炎症效应器功能信号(fcγR 结合)非临床微出血研究显示微出血风险没有增加 GLP 研究显示出可接受的安全性支持临床给药计划,包括 Ph 2/3 SELECTIVITY PHARMACTIOLOGY PK/PD SAFETY 29

与 Aβ 单体相比,Aβ 低聚物具有很高的选择性即使存在大量过量的 Aβ 单体,ACU193 与 AβOS 的结合也不会改变 ACU193 与 AβOS 的结合 >500 倍与 Aβ 单体的结合 Log [竞争抗原]μM ACU193 Selectivity ACU193 在 5μM 单体存在下的选择性 Aβ ACU193 Log μM SELECTIVITY ACU193 是第一款为选择性靶向 aβOS 而开发的单克隆抗体 ACU193 即使在存在大量过量的 Aβ 单体(例如大脑中存在的单体)的情况下也能保留,从而限制 “靶向分散注意力” 30

比较 SEC 分数中的 Aβ 物种-MAB 复合物信号 SELECTIVITY ACU193 与 Ab 的低聚物种结合,这些物种与 hu266(solaneuzumab)或 Hu3D6(bapineuzumab)ACU193 结合的低聚物种 Ab 31 有区别

AD Hippocampus thios/Amyloid 斑块 AD Hippocampus acu193/ABOS 物种 ____________________ 来源:E. Cline 等人CTAD 2019。ACU193 对人类 AB 脑切片中的 aβOS versues Aβ 斑块 32 ACU193 染色具有很高的选择性 ACU193(红色)结合非硫黄素 S 阳性 Ab(绿色)选择性 ACU193 与人类 AD 脑组织中的硫黄素 S 阳性原纤维 Aβ 斑块的结合很少或根本没有

药理学选择性与神经元结合后,ABO 会破坏长期增强 (LTP),导致细胞内钙的病理性增加,从而对细胞造成破坏。aβOS 与神经元结合并有毒;ACU193 的小鼠类似物可防止毒性 33 ACU3B3 可防止 AβO 抑制海马 LTP 体外控制 Aβ42 (50 nM) Aβ42 (50 nM) + ACU3B3 (100 pM) ACU3B3 可防止 AβO 介导的细胞培养物升高注意:(1) 是小鼠单克隆抗体前体和等效于人源化 ACU193 ACU3B3 的变化异常的神经元活动被认为是 AD 记忆力减退的基础,可以防止 aBo 介导的神经元培养中钙稳态的中断 ACU3B3

ACU193 (ACU3B3) 的小鼠亲本版本用于治疗有沉积斑块的年轻小鼠或斑块丰富的年龄较大的小鼠治疗 AD 的转基因小鼠模型可改善行为 34 治疗可显著减少年轻(5-7 个月)的转基因小鼠的缺陷药理学选择性缺陷 MWM 游泳速度异常(**p
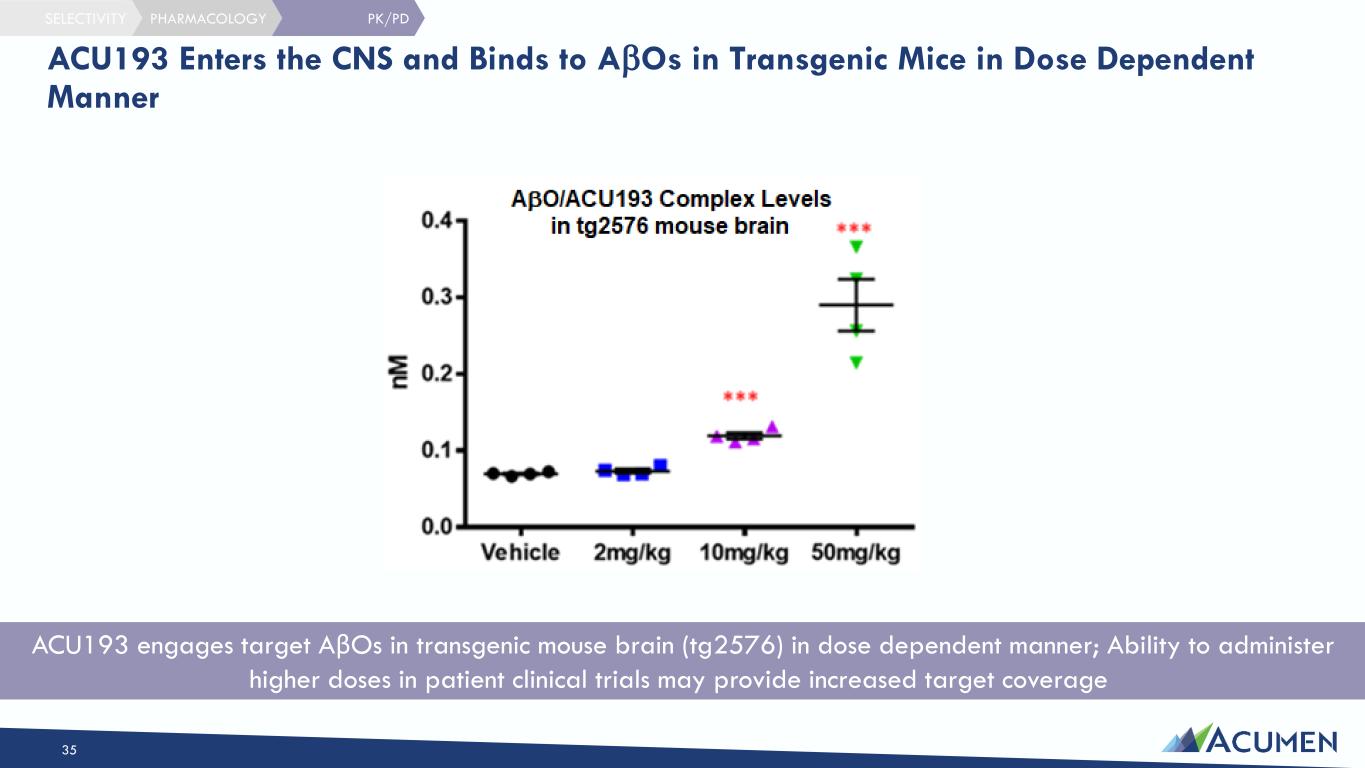
ACU193 以剂量依赖性的方式利用转基因小鼠大脑 (tg2576) 中的靶点 AβO;能够在患者临床试验中施用更高剂量可以增加靶标覆盖率 PK/PD ACU193 进入中枢神经系统并以剂量依赖方式与 ABO 结合 35 药理学选择性

临床开发计划和战略考虑

Acumen 领导团队在 AD/Neuro 药物开发方面经验丰富 Acumen 团队在阿尔茨海默氏症药物发现和开发方面拥有数十年的经验 JANICE HITCHCOCK,博士,监管事务副总裁 ROBERT DEAN,医学博士,生物标志物和分析方法高级开发顾问 JASNA JERECIC,博士分析方法负责人,研究科学家 ERIC SIEMERS,医学博士,首席医学官 MATT ZUGA 首席财务官兼首席商务官罗素·巴顿首席运营官 DANIEL O'CONNN ELL 总裁兼首席执行官 LIEAN SCHENK 副总裁、CMC 负责人 SIEW TIN GAN 临床主管运营 37 DEREK MEISNER,JD 首席法务官 JULIE BOCKENSTETTE 执行副总裁、人力资源主管

ACU193 开发摘要 38 差异化特征:非临床和 1 期数据与 Ab 低聚物的毒性以及 ACU193 与 Ab 低聚物的选择性结合一致评估安全性、PK 和靶点参与度的 Phase1 研究的积极顶线结果预计在 2023 年第四季度美国食品药品管理局互动之后,从 2 期研究开始,根据中期分析,有可能扩展到 3 期注册研究

ACU193 知识产权和市场排他性 • 默克对其淀粉样蛋白衍生的扩散配体 (ADDL) IP 的独家、永久、不可撤销、全球免版税许可,包括已颁发的 ACU193 专利 • ACU193 全球知识产权:✓ 在 19 个国家颁发的专利 ✓ 物质专利组成和使用方法有效期可能延长 3-5 年,具体取决于司法管辖区 • 生物制剂市场预计将独家经营权 ACU193 作为一种新型生物药物 ✓ 美国为新型生物制剂提供 12 年的市场独家经营权 ✓ 欧洲提供 10 年的市场独家经营权 ✓新型生物制剂的市场独家经营权 39

Acumen 资本充足,预计将在 2026 年下半年出现现金和有价证券。我们相信 Acumen 手头有足够的现金和有价证券将 ACU193 推进 2026 年下半年,截至 2023 年 6 月 30 日约1.27亿美元现金、现金等价物和有价证券 2023 年 7 月扩大公开后续发行的额外净收益 40 个里程碑状态/预期时间机制证明业绩 ✓ 生物标志物第一阶段研究的结果 2023 年第四季度预计与 FDA 的互动 2023 年第四季度预计将于 2024 年上半年启动 2 期试验

ABOS:关键要点经验丰富的AD药物开发团队AD 的大量未得到满足的需求、最近的有利趋势和累积的学习领域 2023 年即将到来的行业催化剂针对有毒的 ABO 蓝筹股投资者的差异化候选产品、非常强劲的资产负债表和 2026 年下半年的现金跑道 2023 年 7 月公布的 1 期临床正面数据 41

附录 www.acumenparm.com 42

Lecanemab 第 2 阶段表明,仅减少淀粉样蛋白斑块不足以优化阿尔茨海默氏病减速 * 43 *治疗后 ban2401 介导的淀粉样蛋白减少的持续性:对早期阿尔茨海默氏病受试者 BAN2401-G000-201 核心阶段和开放标签延期基线之间的淀粉样蛋白状态的初步比较(1330);Chad J. Swanson 等神经病学 2020 年 4 月,94(15 份补编)1330;*在 2020 年 4 月的美国神经病学会(AAN)会议上发表。• Lecanemab(BAN2401)研究 201 — 开放标签扩展(OLE)研究开始前的 “间隔” 期证实,尽管淀粉样斑块(Ab PET suvR)持续减少,但停用 Lecanemab 后认知结果(CDR-SB)恶化。Ab PET 可测量大脑中的淀粉样蛋白斑块,但不能测量可溶性 Ab 物种,例如低聚物或原原纤维在 CDR-SB 中的变化:研究 201 核心与 OLE 基线变化淀粉样蛋白 PET suvR:研究 201 核心与 OLE 基线表明可溶性 Ab 聚集物种(例如原原原纤维、低聚物)在临床下降中起作用 Core Baseline 18m OLE 基线基线 18m OLE 基线安慰剂每月 10 mg/kg 10 mg/kg biWeeklyTreation On 治疗关闭治疗关闭治疗 W o rs e n in g im p ro v in g

实测结果** solanezumab EXPERTIONAB 3(第 3 阶段)aducanumab EMERGE(第 3 期)aducanumab ENGAG(第 3 期)lecanemab Clarity-ad(第 3 阶段)+ donanemab TRAILBLAZER-2(中级 Tau)adas-CoG -11% -27% -26% -20% -32% S-ADL -15% -40% -18% -37% -28% -40% CDR-SB -15% -23% -29% -36% MMSE -13% -15% N.A. N.A. iadrs -11% N.A. N.A. N.A. N.A. N.A.-A.-A. -11% N.A. N.A. N.A. N.A. N.A. A.A.-A.-A. -22-35% 来自最近 3 期抗淀粉样蛋白单抗体ADRs研究的阳性信号和概念验证认知/功能减缓百分比 TRAILBLAZER-2Decline* 注意:ENGAGE 协议后版本 4 — 至少 14 剂量 10 mg/kg,与安慰剂相比,高剂量队列的 CDR-SB 改善了 27% * 减缓百分比 = P[1- [(终点分数-基线分数)active/(终点分数-基线分数)安慰剂]]* 100% * (-1) ** ADAS-COG:阿尔茨海默氏病评估量表 — 认知子量表 ADCS-ADL:阿尔茨海默氏病合作研究 — 日常生活活动 CDR-SB:临床痴呆评级 — 盒子总和 MMSE:迷你精神状态检查 iADR:阿尔茨海默氏病综合评级量表 “我们正在寻找可以再接再厉的对抗阿尔茨海默氏症的生物学立足点。所以,这些影响很小,但我认为它们很有意义,我希望它们是我们可以增加的过程的开始。”-Stephen Salloway,布朗大学医学博士 ++ __________________ + 来源:卫材/Biogen 新闻稿,2022 年 9 月 28 日。++ 来源:礼来公司 2023 年 5 月 3 日新闻稿。++来源:《华尔街日报》,Biogen详细介绍有争议的阿尔茨海默氏症药物案例,2019年12月5日出版。例如,参见 Plotkin,《疾病神经生物学》,2020年。上面列出的任何候选产品之间都没有进行过正面交锋的临床试验。每种候选产品的研究设计和方案都不同,候选产品的结果可能无法比较。44

靶向 AB 单体 solanezumab EXPEDITION 3(第 3 阶段)aducanumab EMERGE(第 3 期)aducanumab(第 3 阶段)donanemab(第 3 期)++ pc 处理 pc 低高 PC 处理 ARIA-E 0.2% 0.1% 2.2% 26.1% 34.4% 3.0% 25.6% 35.7% 0.8% 24% 0.8% 9.9% 1.7% 12.6% 有症状 6% 3% ApoE ε4 携带者 1.9% 29.8% 42.5% 41.8% 44.0% 14.6% 2.8% ApoE ε4 非载体 2.9% 18.1% 17.7% 0.0% 5.4% 任何一个ARIA E 或 H 10.3% 32.8% 41.2% 9.8% 30.7% 40.3% 8.0% 38.9% 31% 9.5% 21.5% 抗斑块单克抗体显示剂量相关的 ARIA 可能会限制其使用 45 * PC = 安慰剂,低 = 低剂量;高 = 高剂量表明使用靶向 Aβ 单体(solanezumab)的抗体(solanezumab)治疗后不存在 ARIA,而在增加剂量时,ARIA 的存在率会增加靶向淀粉样蛋白斑块(aducanumab、BAN2401 和 donanemab)的抗体的水平表明 ARIA 是由去除血管周围淀粉样蛋白斑块引起的,而且可能确实如此不是使用靶向其他物种 Aβ(即 Aβ 单体和 AβOS)的抗体治疗所致。抗Aβ/斑块mabs的ARIA事件百分比* ARIA-E代表了与淀粉样斑块结合的单抗的剂量限制不良反应;我们认为,表现出较低ARIA-E的抗体应该更安全、更可行,可能在更高的剂量下给药。上面列出的任何候选产品之间都没有正面交锋的临床试验。每种候选产品的研究设计和方案都不同,候选产品的结果可能无法比较。+ 来源:卫材/Biogen 新闻稿,2022 年 9 月 28 日。++ 来源:礼来公司新闻稿 2023 年 5 月 3 日。45 靶向原纤维靶向淀粉样蛋白斑块