
附录 99.1

2023 年 5 月公司发布会

2 关于本演示的免责声明本投资者介绍会(“演示文稿”)不构成 (i) 就任何证券或拟议的业务合并征求委托书、同意或授权,或 (ii) 出售要约、征求购买要约或建议购买Priveterra、公司或其任何关联公司的任何证券。除非通过符合经修订的1933年《证券法》第10条要求的招股说明书,否则不得进行此类证券发行。前瞻性陈述本演示文稿中的某些陈述、估计、目标和预测可能被视为前瞻性陈述。前瞻性陈述通常与Priveterra Acquisition Corp.(“Priveterra”)或AEON Biopharma, Inc.(“公司”)的未来事件或涉及其未来业绩或未来业绩有关。例如,对未来EBI TDA的预测、关于公司运营所在行业预期增长和公司产品需求预期增长的陈述、对公司未来财务业绩和其他指标的预测、Priveterra与公司之间即将达成的业务合并(“业务合并”)的完成条件的满意度以及业务合并完成的时机都是前瞻性的陈述。在某些情况下,您可以通过术语来识别前瞻性陈述,例如 “预期”、“可能”、“可能”、“计划”、“可能”、“项目”、“努力”、“预算”、“预期”、“预期”、“将”、“估计”、“预期”、“相信”、“预测”、“潜在” 或 “继续”,或者这些术语的否定词或它们的变体或类似术语。此类前瞻性陈述受风险、不确定性和其他因素的影响,这些因素可能导致实际结果与此类前瞻性陈述所表达或暗示的结果存在重大差异。这些前瞻性陈述基于估计和假设,尽管Priveterra及其管理层以及公司及其管理层(视情况而定)认为这些估计和假设是合理的,但本质上是不确定的。可能导致实际业绩与当前预期存在重大差异的因素 i ncl ude,但不限于:(i) 发生任何可能导致与业务合并有关的谈判和后续最终协议终止的事件、变更或其他情况;(ii) 在宣布业务合并后可能对Priveterra、公司、合并后的公司或其他公司提起的任何法律诉讼的结果以及任何与 resp 等达成的最终协议;(iii)由于未能获得Priveterra或公司股东的批准或未能满足其他关闭条件而无法完成业务合并;(iv) 由于适用的法律或法规或作为获得监管部门批准业务合并的条件,业务合并的提案结构可能被要求或适当;(v) 业务合并完成后能够满足 s toc k 交易所上市标准; (vi) 业务合并的风险由于业务合并的宣布和完成,扰乱了公司当前的计划和运营;(vii) 识别业务合并预期收益的能力,这可能受到识别、开发和商业化候选产品的能力、当前或计划中的临床前研究和临床试验的启动、成本、时机、进展或结果、产品接受和/或获得监管批准等因素的影响对于候选产品,包括相关的里程碑,未来运营的管理计划、战略和目标、管理层对未来事件、潜在市场或市场规模或技术发展的信念和假设、生物制药行业研发活动的竞争和进展、合并后的公司以盈利方式增长和管理增长、维持与供应商关系并留住管理层和关键员工的能力、与业务合并相关的成本、适用法律或法规的变化、可能性公司或合并后的公司可能受到其他经济、业务、监管和/或竞争因素的不利影响;公司对支出和盈利能力的估计;公司竞争市场的演变;公司实施战略举措和继续创新现有候选产品的能力;公司捍卫其知识产权和满足监管要求的能力;COVID-19疫情对公司业务的影响;以及 (v iii) 其他风险和Priveterra 于 2021 年 2 月 11 日的最终招股说明书中标题为 “风险因素” 和 “关于前瞻性陈述的警示性说明” 部分中提出的不确定性,涉及其首次公开发行许可证以及将提交给Priveterra股东的最终委托书和相关注册声明(包括其中 “风险因素” 下规定的风险和不确定性)以及其他将提交的文件中不时指出的风险和不确定性 Priveterra 与美国证券交易委员会合作。本演示文稿包括截至20-23年3月31日的三个月的初步财务信息(或 “快讯” 信息),这些信息有待进一步的财务审查完成,与S-4表格上向Priveterra股东和相关注册州提交的最终委托书中的财务信息不同。由于公司完成审查调整以及从现在到该期间此类财务信息最终确定之时可能出现的其他事态发展,实际业绩可能会有所不同。因此,这些估计是初步的,可能会发生变化并构成前瞻性信息,因此受到风险和不确定性的影响。公司的独立注册会计师事务所和任何其他独立注册会计师事务所均未审计、审查或遵守任何与初步业绩有关的程序,也没有就初步财务信息发表任何意见或任何其他或形式的保证。本演示文稿中的任何内容均不应被视为任何人表示此处提出的前瞻性陈述将得以实现,或者此类前瞻性陈述的任何预期结果都将实现。你不应过分依赖前瞻性陈述,这些陈述仅代表其发表之日。Priveterra和公司均不承担任何责任更新这些前瞻性声明。

3 免责声明(续)目标本演示文稿包含公司的某些长期财务目标。Priveterra和公司的独立审计师均未审计、研究、审查、汇编或执行任何与目标有关的程序,以便将其纳入本演示文稿,因此,他们没有就此发表任何意见或提供任何其他形式的保证。这些目标是前瞻性陈述,不应将其视为未来业绩的必然指标。这些目标所依据的假设动向和估计本质上是不确定的,并且受到各种重大的商业、经济和竞争风险和不确定性的影响,这些风险和不确定性可能导致实际业绩与目标存在重大差异。因此,无法保证这些目标代表着公司的未来业绩,也无法保证实际业绩与提出的业绩不会有重大差异。在本演示文稿中纳入税收规定不应被视为任何人表示目标将得到实现。行业和市场数据在本演示文稿中,公司依赖并提到了从第三方来源获得的某些信息和统计数据,我们认为这些信息和统计数据是可靠的。Priveterra和公司均未独立验证任何此类第三方信息的准确性或完整性。商标本演示文稿可能包含其他公司的商标、服务标志、商品名称和版权,这些是其各自所有者的财产。仅为方便起见,本演示文稿中提及的某些商标、服务标志、商品名称和版权可能不带TM、SM、© 或® 符号,但 Pri vet erra 和公司将在适用法律的最大范围内维护适用所有者(如果有)对这些商标、服务标志、商品名称和版权(如果有)的权利。其他信息 Priveterra已向美国证券交易委员会(“SEC”)提交了S-4表的注册声明,其中包括一份委托书/招股说明书,这既是向Priveterra的A类普通股持有人分发的委托书,涉及Priveterra的股票kho lders就商业合并和其他事项征求代理人进行表决注册声明,以及与即将发行和出售证券有关的招股说明书在业务合并中发行。注册声明宣布生效后,Priveterra将向其股东邮寄最终委托书/招股说明书和其他相关文件。本演示文稿不包含有关拟议业务合并应考虑的所有信息,也无意构成与业务合并有关的任何投资决策或任何其他决定的基础。建议Priveterra的股东和其他利益相关人士阅读注册声明及其修正案中包含的初步委托书/招股说明书以及与拟议业务合并有关的最终委托书/招股说明书和其他文件,因为这些材料将包含有关公司、Priveterra和业务合并的重要信息。如果有,拟议业务合并的最终委托书/招股说明书和其他相关材料将自创纪录的日期邮寄给Priveterra的股东,以便对拟议的业务合并进行表决。斯托克霍尔还可以在美国证券交易委员会的网站www.sec.gov上免费获得向美国证券交易委员会提交的初步委托书、最终委托书和其他文件的副本,一旦公布,或直接向位于佛罗里达州劳德代尔堡东南二街300号600套房的Priveterra秘书提出申请 33301,754-220-9229。招标的参与者Priveterra及其董事和执行官可能被视为参与了就拟议的业务合并向Priveterra的股东征求代理人的活动。这些董事和执行官的姓名名单以及他们在Priveterra中的权益描述载于Priveterra于2021年2月11日发布的与首次公开募股有关的招股说明书,该招股说明书已提交给美国证券交易委员会,可在美国证券交易委员会的网站www.sec.gov上免费查阅。如果自那时以来Priveterra证券的持有量可能发生了变化,则此类变化已经或将反映在向美国证券交易委员会提交的表格4的所有权变更声明中。有关此类参与者利益的更多信息包含在拟议业务合并的代理统计数据eme nt/招股说明书中。公司及其董事和执行官也可能被视为参与了就拟议的业务合并向Priveterra的股东征求代理人的活动。拟议业务合并的委托书/招股说明书中包含此类董事和执行官的姓名名单以及有关他们在拟议的商业公司合并中的权益的信息。
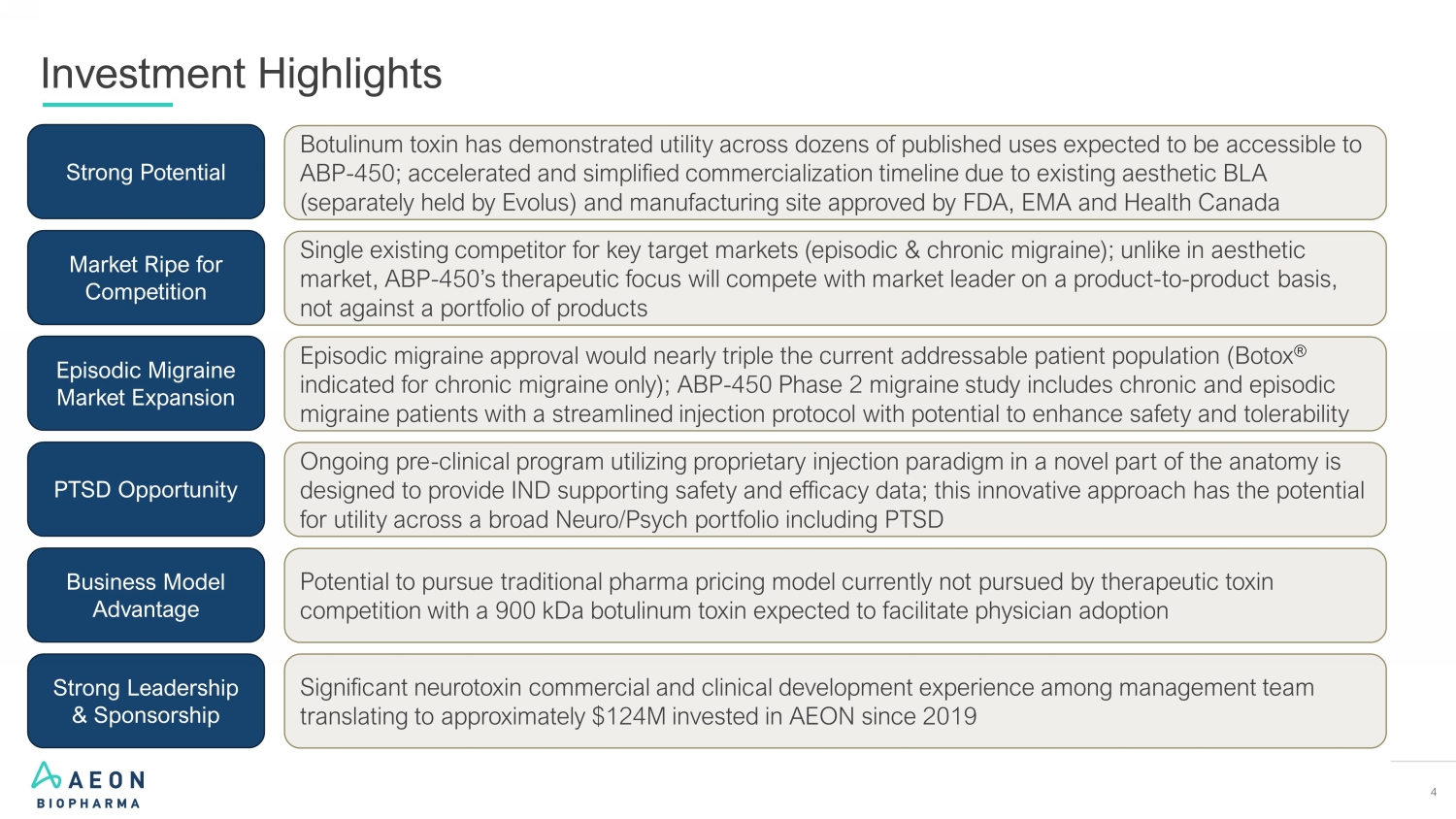
4 投资亮点肉毒杆菌毒素已在数十种已公布用途中显示出效用,预计ABP-450;由于现有的美学BLA(由Evolus单独持有)和生产基地获得美国食品药品管理局、欧洲药品管理局和加拿大卫生部批准的发作性偏头痛将使目前可治疗的患者群体增加近三倍(Botox® 仅适用于慢性偏头痛);ABP-450 2 期偏头痛研究包括慢性偏头痛和发作性偏头痛注射方案简化的患者有可能提高安全性和耐受性有可能推行治疗毒素竞争对手目前所不追求的传统药物定价模式,预计将促进医生采用管理团队拥有丰富的神经毒素商业和临床开发经验,这意味着自2019年以来向AEON投资了1.24亿美元强大潜力发作性偏头痛市场扩张商业模式优势强大的领导力和赞助市场竞争时机已成熟关键目标市场的单一现有竞争对手(发作和慢性偏头痛);与美学市场不同,ABP-450的治疗重点将在产品到产品的基础上与市场领导者竞争 Neuro/Psych Opportunity 正在进行的临床前项目在解剖学的新部分中利用专有注射范式旨在提供IND支持的安全性和有效性数据;这种创新方法有可能在广泛的神经/心理产品组合(例如创伤后应激障碍、焦虑症、等等)

5 个具有高度相关行业经验和成功记录的领导团队经验丰富的管理团队 Marc Forth Chad Oh,医学博士首席执行官首席医学官 • 生物制药工作超过 25 年 • BOTOX® 治疗的美国业务负责人 • 在 Allergan 工作了 16 年,负责整个 BOTOX® 特许经营权 • 在 TAP Pharmacels 工作了 7 年,负责 Lupron Depot(泌尿外科、肿瘤学和妇科)• 在学术界和医学界拥有 30 多年的综合经验制药行业 • 负责提交多份 IND、NDA 和 BLA •加州大学洛杉矶分校医学中心海港过敏和免疫学系主任 • 加州大学洛杉矶分校医学院儿科系副教授 • 发表了多篇科学论文、书籍、书籍章节和摘要,包括 38 篇经过同行评审的原创科学论文 • 在公司治理、并购和资本市场方面拥有 10 多年的法律经验 • Glaukos Corporation的副总法律顾问,负责业务发展活动、资本市场、公司治理和美国证券交易委员会的报告 • 法律顾问 • 法律顾问在 O'Melveny & Myers• 杨百翰大学商业管理学士学位和加州大学洛杉矶分校法学院法学博士总法律顾问兼公司秘书亚历克斯·威尔逊彼得·雷诺兹代理首席财务官 • 在医疗保健、医疗器械和美容毒素领域拥有 25 年以上的财务经验 • 曾在上市公司和私人控股公司担任高级财务职务 • 在合并、收购和公开募股方面拥有丰富经验

6 肉毒杆菌毒素:终极平台产品

7 全球治疗毒素景观 AbbVie Inc. Merz Pharma Ipsen Group 分子大小 900 kDa 900 kDa 150 kDa ~400 kDa 150 kDa 批准的适应症 1.眼睑痉挛 2.斜视 3.宫颈肌张力障碍 4.多汗症 5.痉挛 6.慢性偏头痛 7.膀胱过度活跃 8.神经源性逼尿器过度活跃(成人和儿童)无 1.眼睑痉挛 2.宫颈肌张力障碍 3.成人痉挛(上肢)4.慢性腹泻 1.宫颈肌张力障碍 2.Spasticity None 在开发中 1.心房颤动 2.发作性偏头痛 3.特发性震颤 4.IC/BPS 1.偏头痛(发作性和慢性)2.宫颈肌张力障碍 3.胃轻瘫 4.创伤后应激障碍 (PTSD) 未公开 1.神经源性逼尿器过度活跃 1.宫颈肌张力障碍 2.成人痉挛(上肢)美国食品药品管理局批准的美国股票 95% 2% 2% 资料来源:决策资源集团2021年全球肉毒杆菌毒素治疗性市场分析
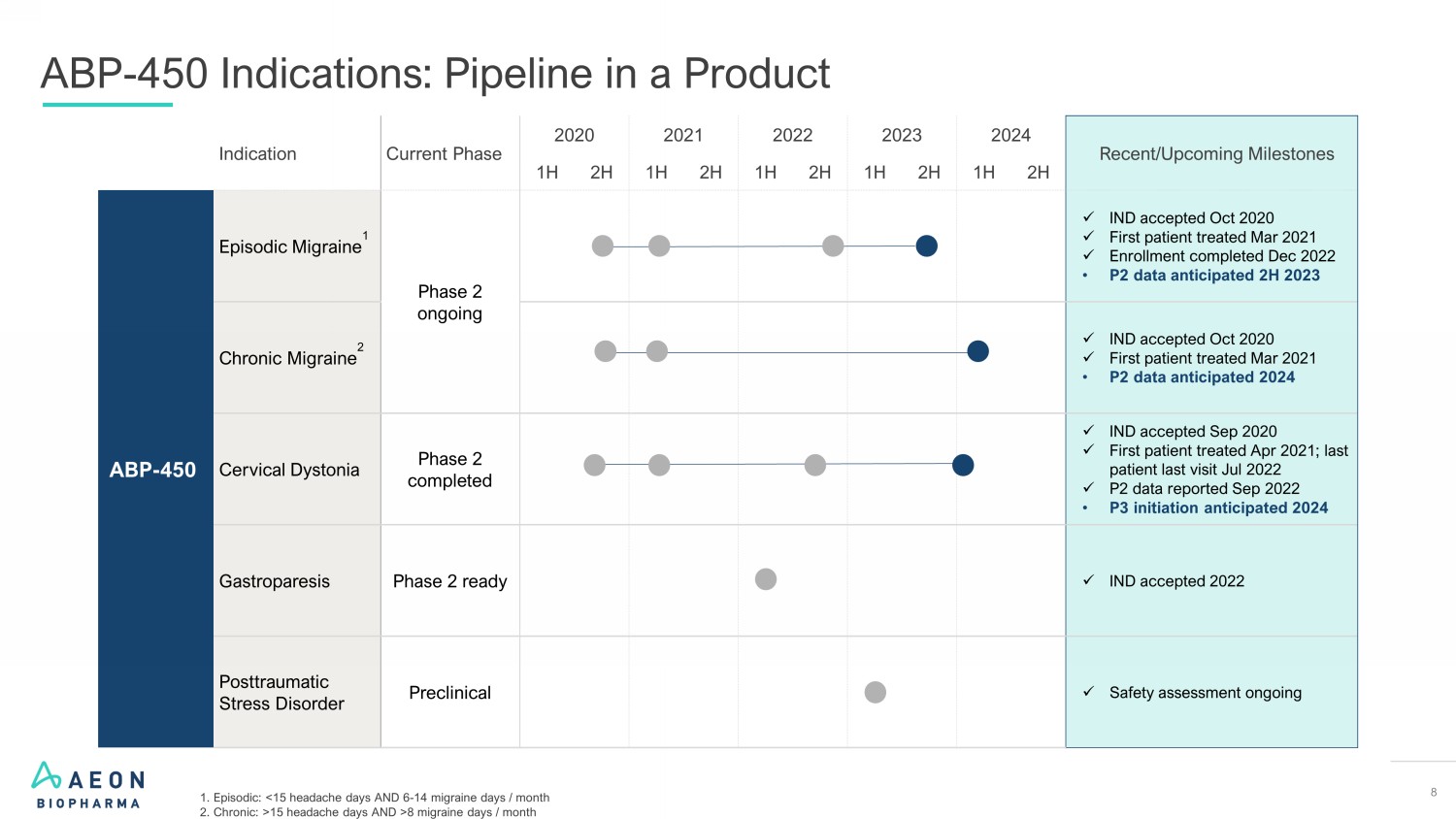
8 适应症当前阶段 2021 2022 2023 2023 2024 最近/即将到来的里程碑 1H 2H 1H 1H 2H 1H 2H ABP-450 发作性偏头痛 1 第 2 阶段正在进行中 x 2020 年 10 月接受临床治疗 x 2022 年 12 月预计 P2 数据已接受 2024 年下半年慢性偏头痛 2 x 2021 年 3 月已接受治疗 • P2 数据预计 2024 年宫颈肌张力障碍第 2 期已接受 x 2020 年 9 月接受临床试验 x 2021 年 9 月首次接受治疗 x 患者于 2021 年 4 月接受治疗;最后一次就诊患者最后一次就诊 2022 年 7 月 x P2 数据公布 2022 年 9 月 • P3 预计于 2024 年启动Gastroparesis 2 期就绪 x IND 已接受 2022 年创伤后应激障碍临床前 x 安全性评估正在进行中 ABP-450 适应症:产品在线 1.发作:15 天头痛和 8 天以上的偏头痛天数/月
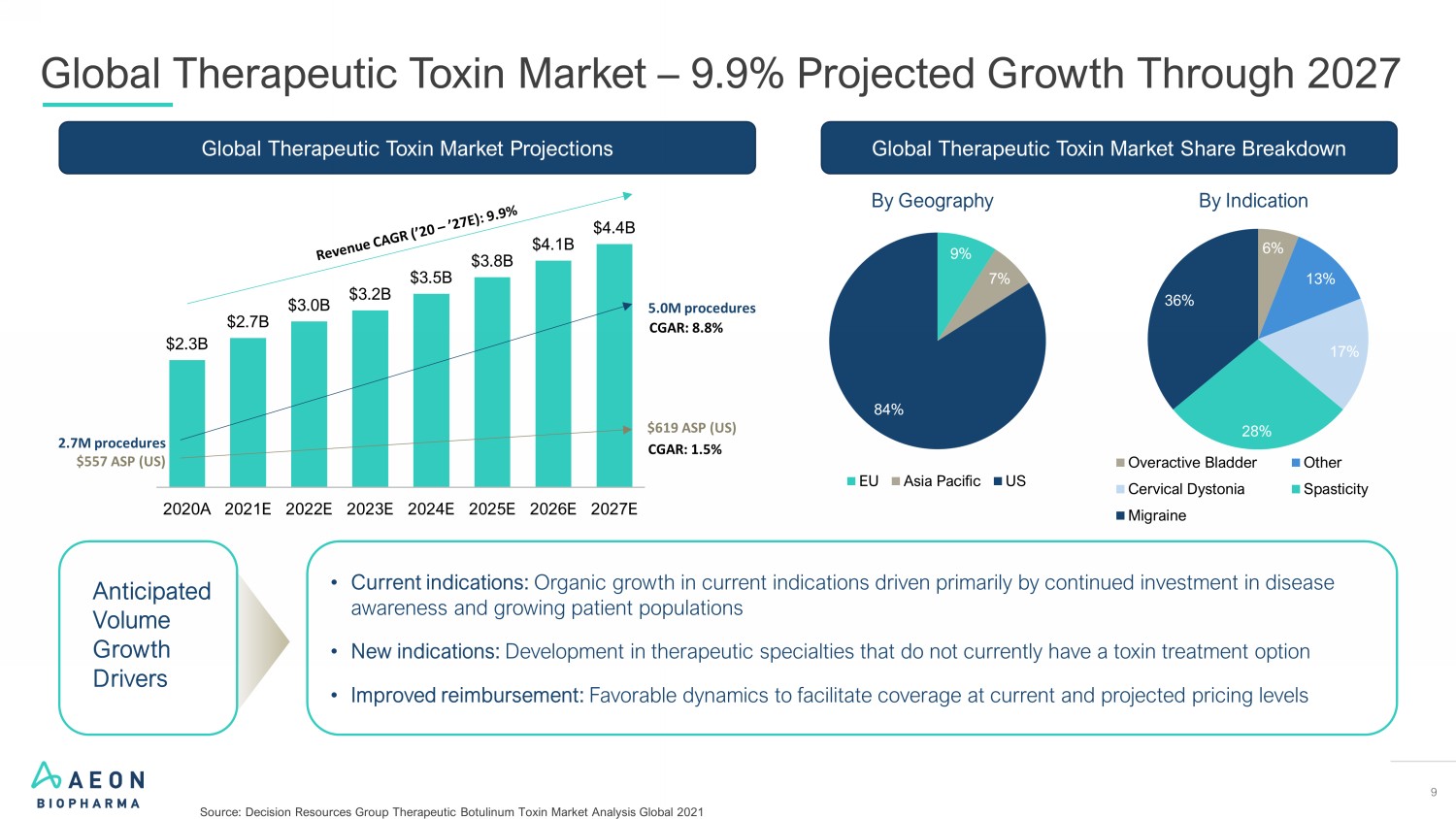
9 全球治疗毒素市场——预计到2027年将增长9.9% • 当前适应症:当前适应症的有机增长主要是由对疾病宣传的持续投资和患者群体的增长推动的 • 新适应症:目前没有毒素治疗选择的治疗专业的发展 • 报销改善:有利的动态促进了当前和预计定价水平的覆盖预期销量增长驱动因素 23B 27B 30B 35B 31.B 31.B 41 亿美元 41 亿美元 44 亿美元 2020A 2021E 2022E 2023E 2024E 2025E 2026E2027E 27M 手术 557 美元 ASP(美国)500 万例手术 619 美元 ASP(美国)CGAR:1.5% CGAR:8.8% 9% 7% 84% 欧盟亚太地区美国 6% 13% 17% 28% 36% 膀胱过度活跃其他宫颈肌张力障碍痉挛偏头痛全球治疗性毒素市场份额按地域划分全球治疗性毒素市场预测来源:决策资源集团2021年全球肉毒杆菌毒素市场分析
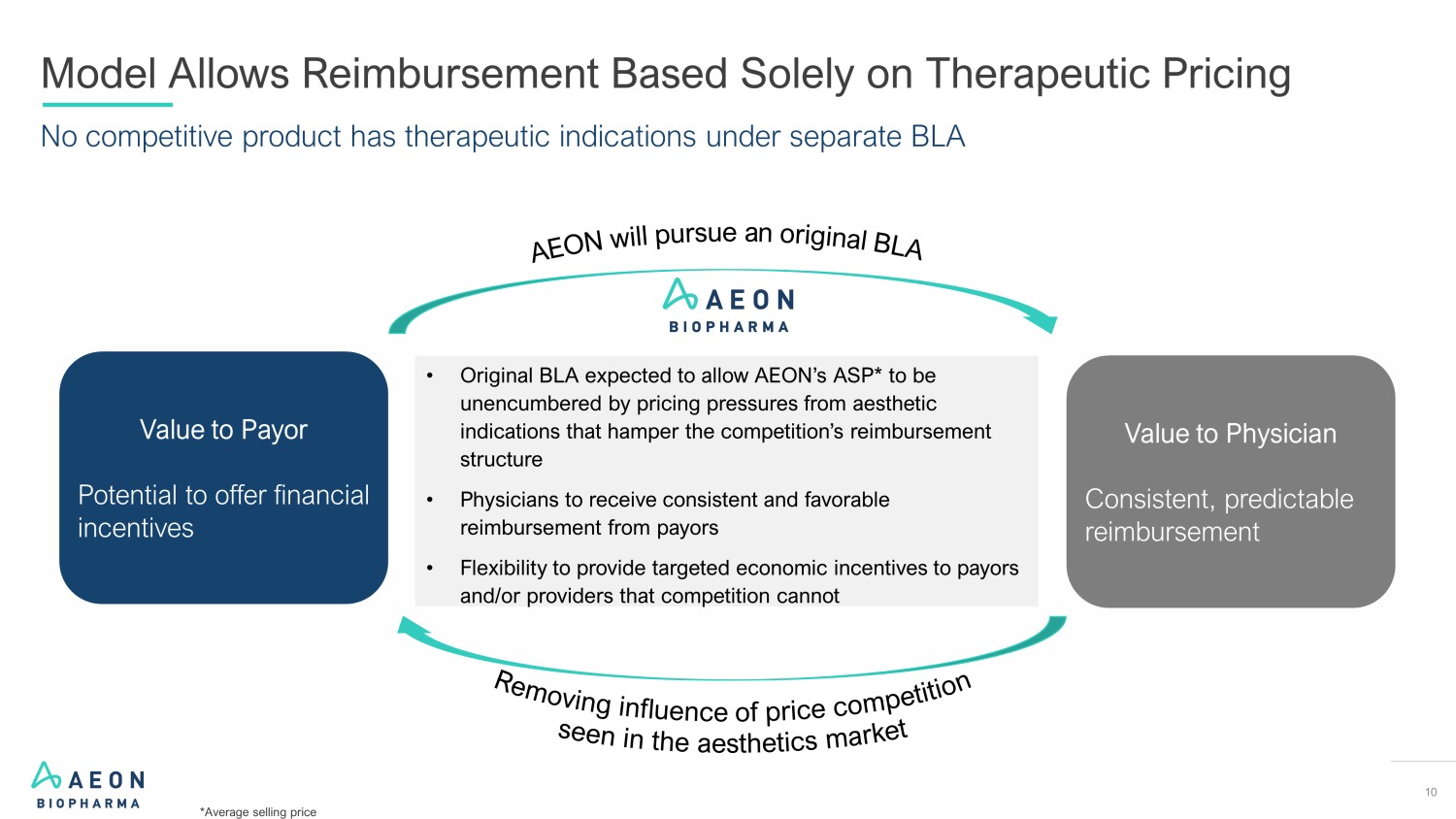
10 在单独的 BLA 模式下,任何竞争产品都没有治疗适应症允许仅根据治疗定价进行报销 *平均销售价格对医生的报销价值支付者价值有可能提供经济激励 • 原始 BLA 有望让AEON的 AEON的ASP*不受阻碍竞争报销结构的美学适应症的定价压力的阻碍 • 医生可以从付款人那里获得持续而优惠的报销 • 可以灵活地向医生提供有针对性的经济激励措施竞争对手无法做到的付款人和/或提供商

(偶发性和慢性预防)偏头痛

12 偏头痛市场来自新参与者的复苏使毒素受益在新产品推出和促销投资的推动下,新 cGRP 正在迅速扩大市场;偏头痛每年影响美国约 4000 万人,全球约 10 亿人,使其成为世界第三大流行的疾病 1 慢性偏头痛 • 头痛天数/月 15 天以上 • 约 400 万患者(112 亿美元市场)2 发作性偏头痛 • 6-14 天头痛/天月 • 约 940 万名患者(市场价值 185 亿美元)3 偏头痛市场加速 • 慢性偏头痛中的 Botox® 在此之后恢复了两位数的增长由于CGRP的推出和COVID的挑战,Botox® 仅对慢性偏头痛提出申诉,与同时具有慢性和发作适应症的 cgRP 相比,毒素表现良好 • 在第 2 阶段将发作性和慢性偏头痛患者包括在内,寻求比肉毒杆菌毒素® 更广泛的患者群体的标签 • ABP 450注射量更少且注射位置差异化的新型注射模式 • 有可能提高安全性和耐受性 • 偏头痛和宫颈肌张力障碍在商业受众中高度重合ABP-450 机会 1.偏头痛研究基金会。2.公司的估算基于2017年美国人口普查预测;戴蒙德,美国米格雷恩的诊断模式以及急性和预防性治疗:美国偏头痛患病与预防研究的结果(2006年);立顿,偏头痛诊断和治疗的障碍(2012年),假设220万daignose d患者每年接受四次治疗(两瓶),每瓶费用为634美元。Messali,《美国慢性偏头痛和发作性偏头痛的直接和间接成本:基于网络的调查》(2016年),假设365万名确诊患者每年接受四次治疗(两瓶),每瓶费用为634美元。4.DRG 报告,偏头痛疾病状况与预测,2020 年 12 月
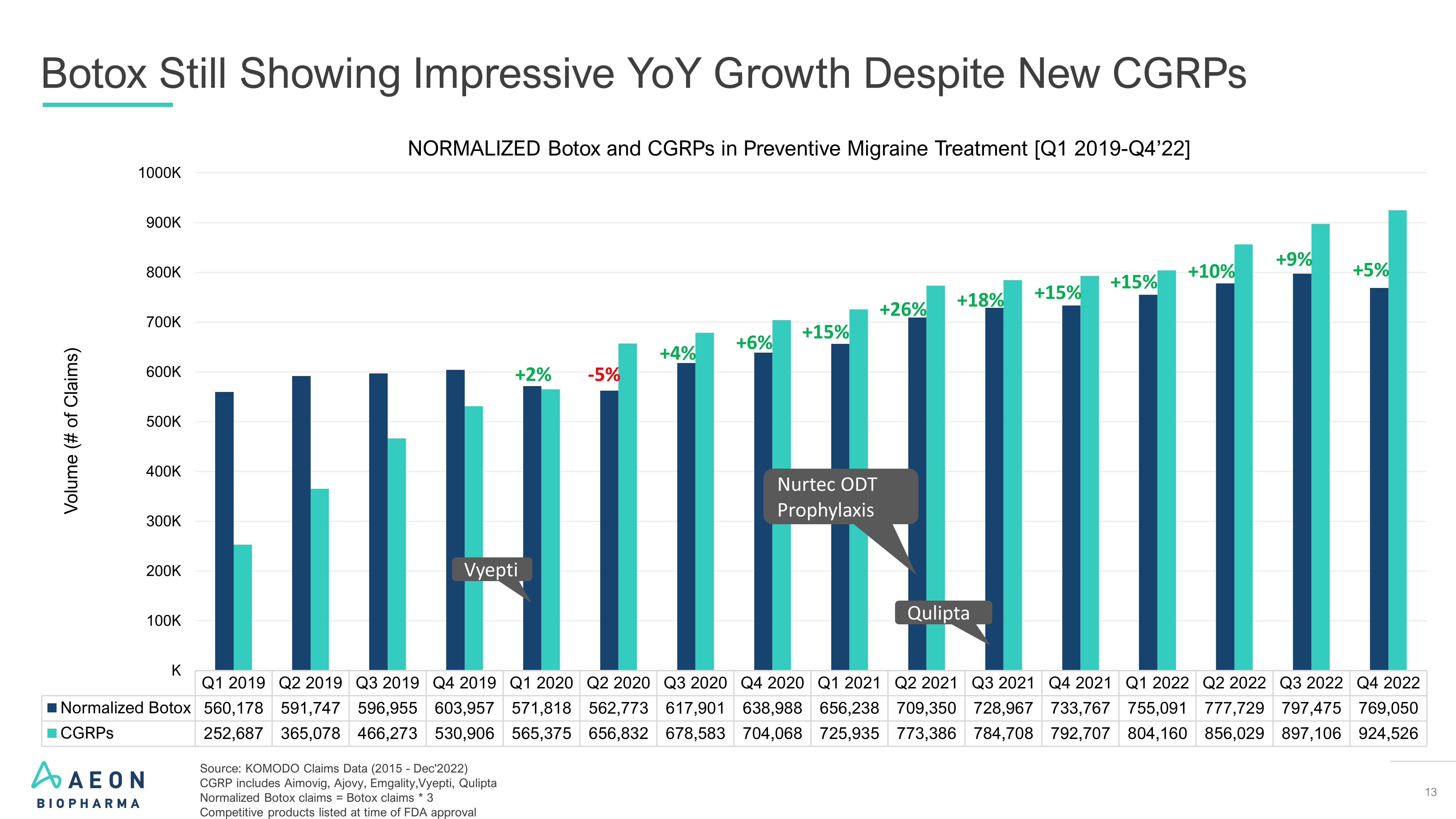
13 2019 年第 1 季度 2019 年第 2 季度 2019 年第 4 季度 2020 年第 2 季度 2020 年第 4 季度 2021 年第 2 季度 2022 年第 3 季度 2022 年第 4 季度标准化 botox 591,747 596,957 571,818 562,773 617,901 638,988 728,967 728,967 728,967 728,967 728,967 728,967 55,091 777,729 797,475 769,050 cGRPS 252,687 365,078 466,273 530,906 5656,832 678,068 725,386 794,708 792,707 804,160 897,106 924,526 K 100K 400K 500K 700K 800K 900K 1000K 预防性偏头痛治疗中的肉毒杆菌毒素和cGRP的正常化量(索赔数量) [2019 - Q4’22]尽管有新的 cGRP,但肉毒杆菌毒素仍显示出令人印象深刻的同比增长来源:KOMODO 索赔数据(2015 年至 2022 年 12 月)CGRP 包括 Aimovig、Ajovy、Emgality、Vyepti、Qulipta 标准化肉毒杆菌索赔 = 肉毒杆菌索赔 * 3 +9% +10% +15% +26% +6% +4% -5% +2% Qulipta Launch +5%
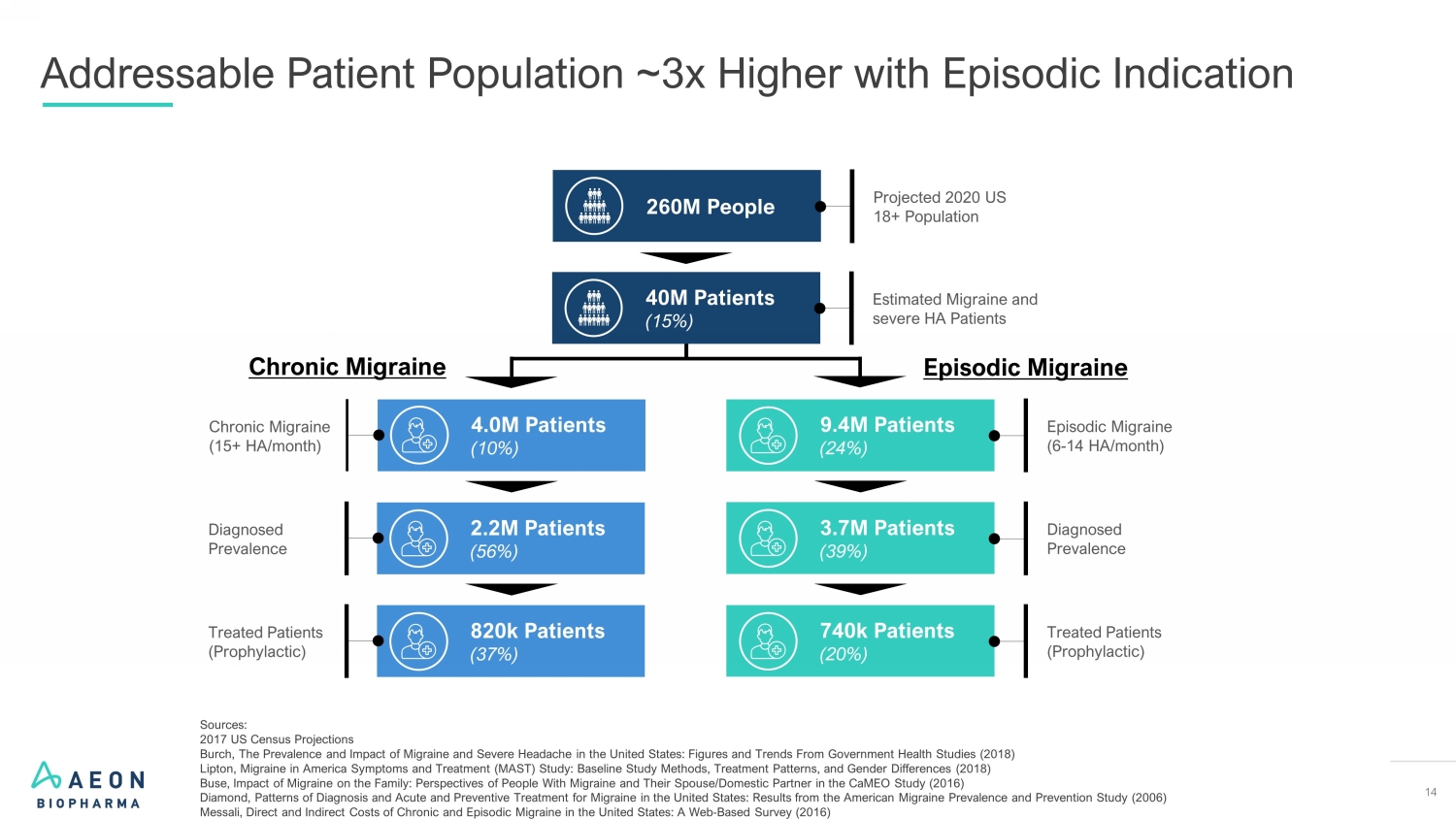
14 个有发作适应症的可寻址患者人数增加约 3 倍 160 万可寻址患者总数 160 万人 2020 年美国 18+ 人口 1 400 万患者 (15%) 估计偏头痛和重度 HA 患者 940 万患者 (24%) 偶发性偏头痛 (6-14 ha/月) 400 万患者 (10%) 慢性偏头痛 (15+ ha/月) 220万患者 (56%) 诊断患病率为 370 万患者 (39%) 患病率 82 万名患者(37%)接受治疗的患者(预防性)74 万名患者(20%)接受治疗的患者(预防性)慢性偏头痛发作性偏头痛 1. 2017 年美国人口普查预测 2。Burch,《美国偏头痛和严重头痛的患病率和影响:来自政府卫生研究的数据和趋势》(2018)3。Lipton,《美国的偏头痛症状与治疗(MAST)研究:基线研究方法、治疗模式和性别差异》(2018)4。Buse,《偏头痛对家庭的影响:偏头痛患者及其配偶/家庭伴侣的视角》(2016)5。戴蒙德,美国偏头痛的诊断模式以及急性和预防性治疗:美国偏头痛患病与预防研究的结果(2006)6。Messali,《美国慢性偏头痛和发作性偏头痛的直接和间接成本:基于网络的调查》(2016)

15 BOTOX PREEMPT2 1 慢性偏头痛的第 3 阶段 • 肉毒杆菌毒素和安慰剂的基线偏头痛天数与基线(CFB)的变化分别为 45% 和 33%,ABP-450 和安慰剂的预计CFB分别为45%和33% • 安慰剂和活性偏头痛之间的治疗效果约为1.3天 • 样本量为每组需要 91 名患者(所有 3 个手臂为 n=273)才能达到 80% 的统计功率 2 阶段发作性偏头痛 1 的终点预期https://headachejournal.onlinelibrary.wiley.com/doi/epdf/10.1111/j.1526-4610.2010.01678.x 统计功率和样本量假设预期基线(天)预计 CFB ABP-450 预计的 CFB 安慰剂效应大小标准。开发。可评估对象/Arm TOTAL N Power 10.5-4.73 (45%)-3.47 (33%)-1.3 3.1 91 273 80%

16 次发作性偏头痛 cgRP 的 3 期试验不适用于交叉试验比较;资料来源:包装说明书;Neurol Ther (2021) 10:469 — 497 BRand Generial Company 试验持续时间剂量主要终点 N 变化(天)与安慰剂的区别 p-value aimovig erenumab STRIVE 24 周 70 mg SC QM 每月偏头痛天数(从基线变为 4 至 6 个月)317-3.2-1.4 {}
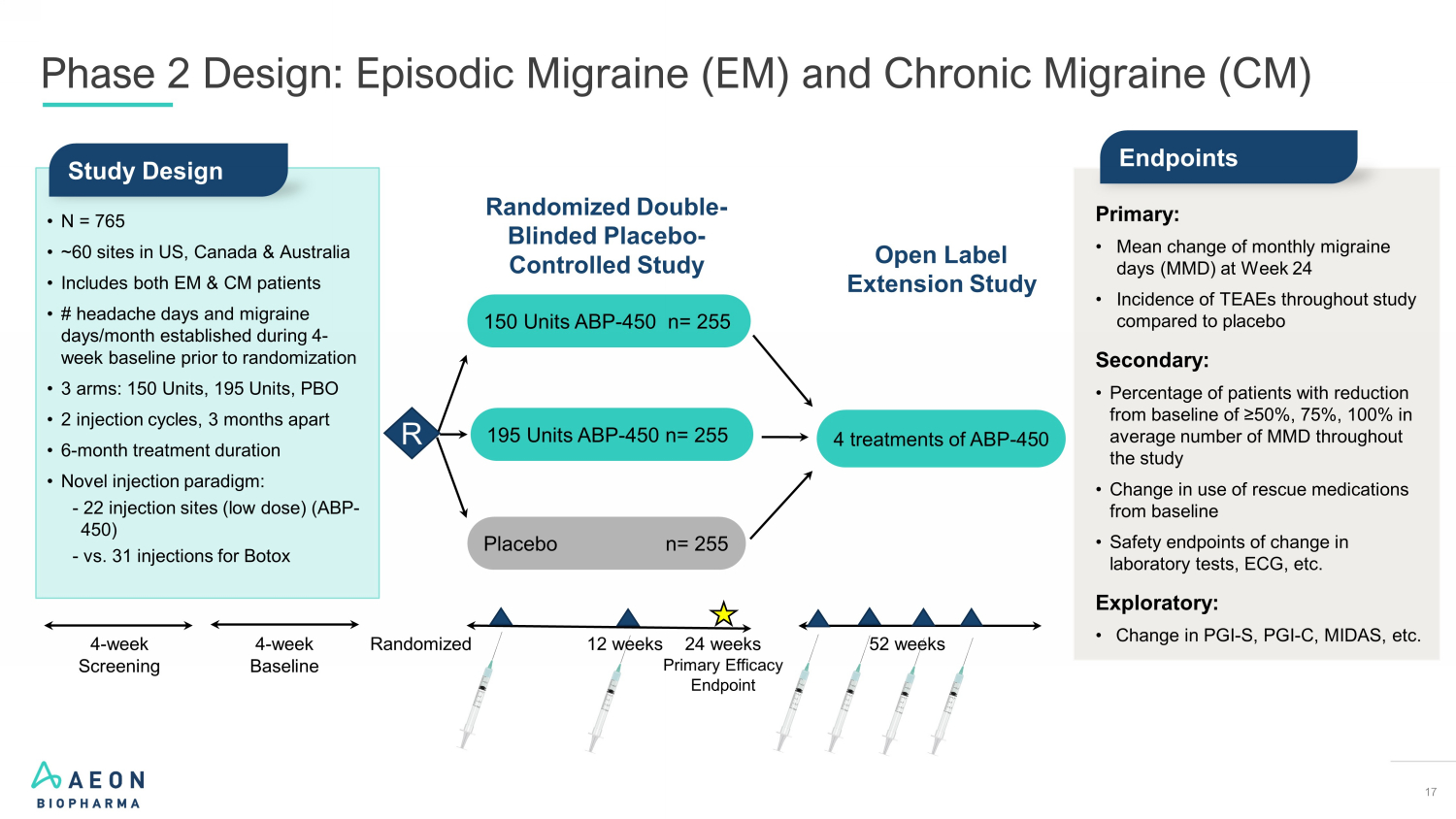
17 • N = 765 • 美国、加拿大和澳大利亚约 60 个部位 • 包括 EM 和 CM 患者 • 随机分组前 4 周基线期间确定的头痛天数和偏头痛天数/月数 • 3 组:150 个单位、195 个单位、PBO • 2 个注射周期,相隔 3 个月 • 6 个月的治疗时间 • 新注射模式:-22 个注射部位(低剂量)(ABP-450)-对比 Bototo的 31 次注射初级:• 第 24 周每月偏头痛天数(MMD)的平均变化 • 与安慰剂相比,整个研究中偏头痛天数(MMD)的平均变化率:• 偏头痛发病率减少的患者百分比整个研究的平均MMD数量的基线为≥50%、75%、100% • 救援药物使用量与基线相比的变化 • 实验室检测、心电图等变化的安全终点。探索性:• PGI-S、PGI-C、MIDAS 等的变化。安慰剂 n= 255 195 单位 ABP-450 n= 255 4 个单位 ABP-450 n= 255 4 个单位 ABP-450 n= 255 4 个单位 ABP-450 n= 255 4 个星期基线 4-一周筛查随机 R 终点随机化双盲安慰剂对照研究开放标签延伸研究 ABP 的 4 种治疗方法——450 52 周研究设计 12 周第 2 阶段设计:情景偏头痛 (EM) 和慢性偏头痛 (CM)
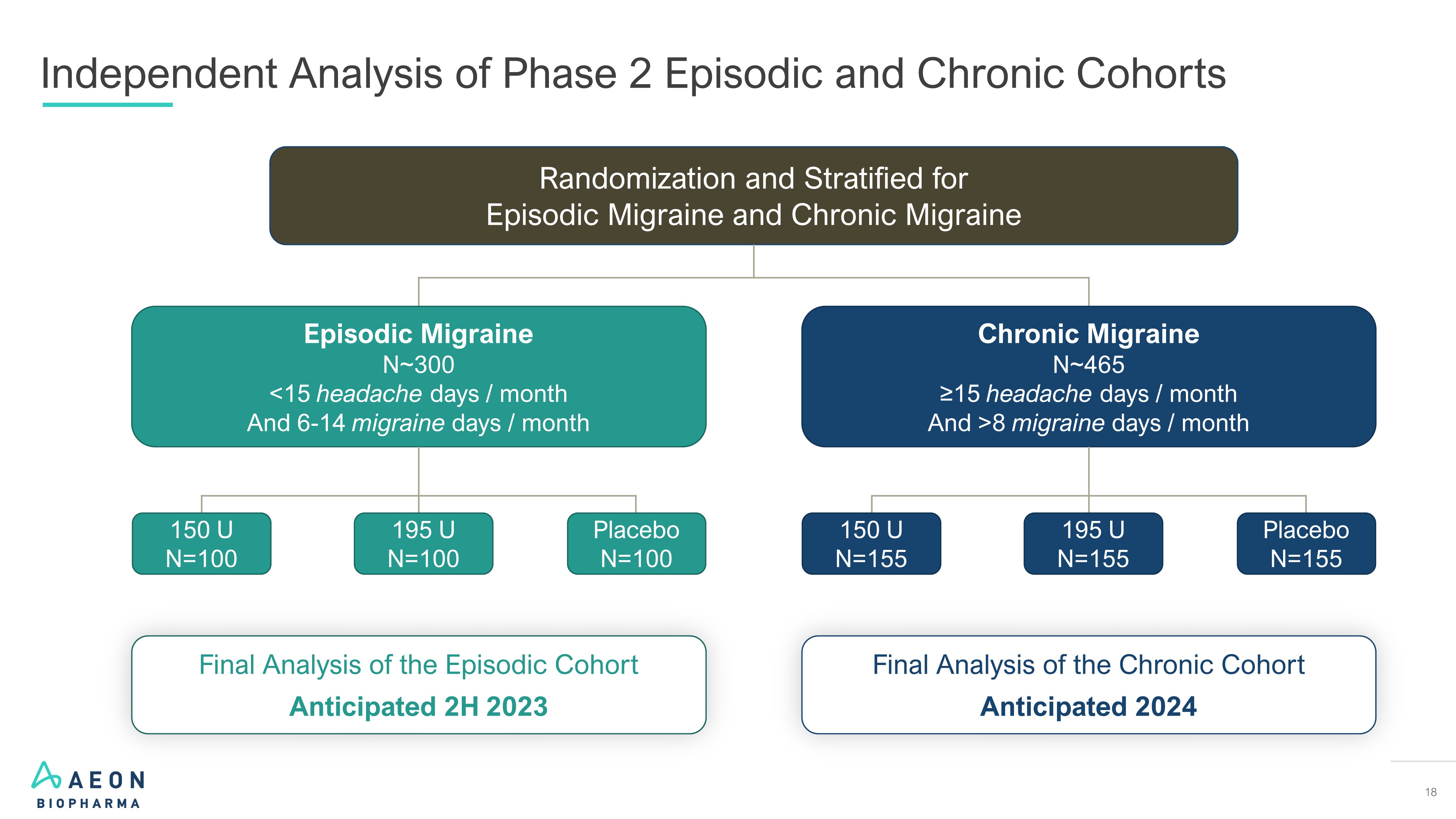
18 对发作性偏头痛和慢性偏头痛2期发作性偏头痛和慢性偏头痛随机分层的独立分析 N=300 8 偏头痛天数/月 150 U N=155 U N=155 安慰剂 N=155 发作队列的最终分析预计在 2023 年下半年对慢性队列的最终分析
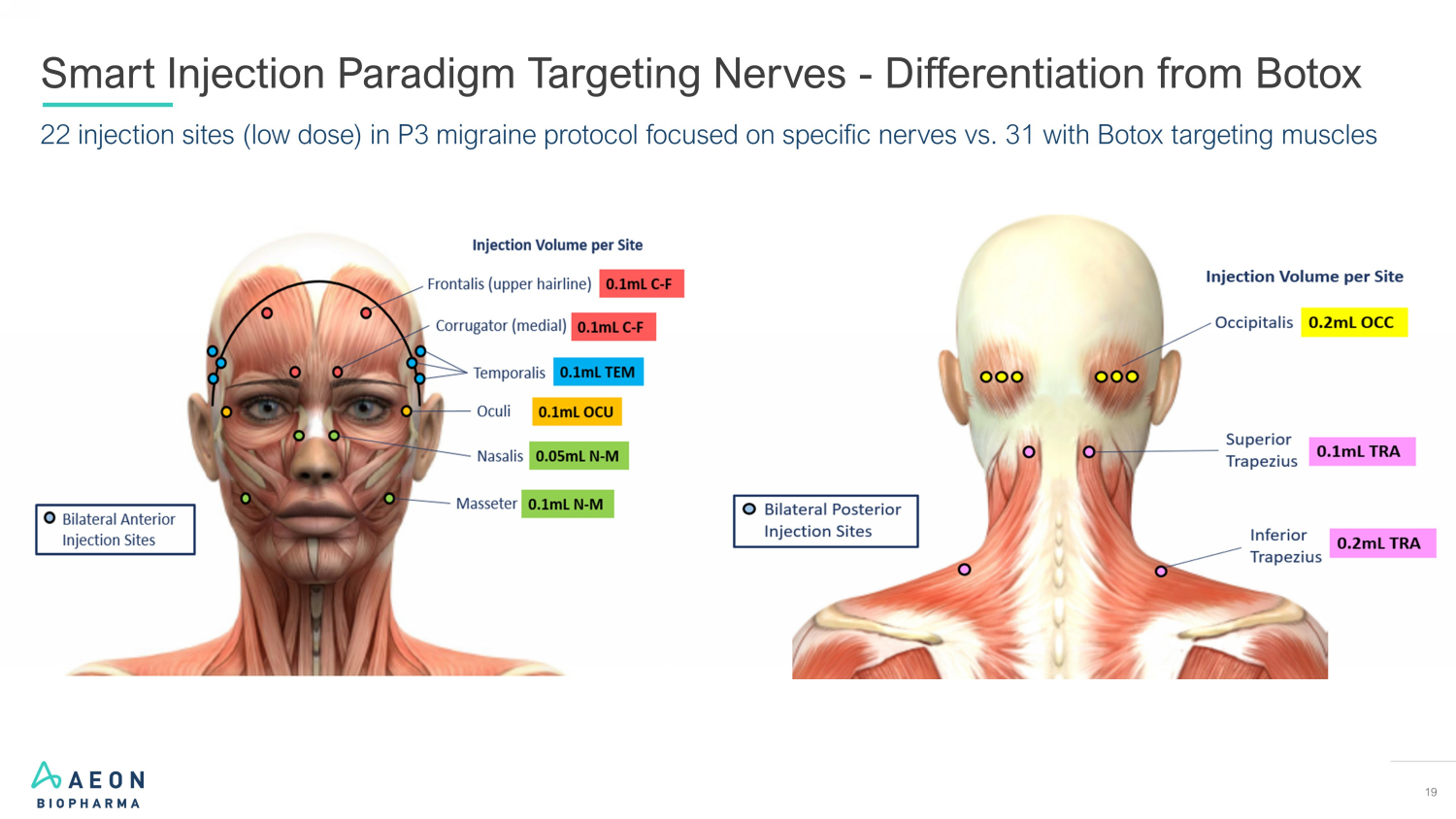
P3 偏头痛方案中有 19 22 个注射部位(低剂量)侧重于特定神经,而肉毒杆菌毒素靶向肌肉的 31 个 Smart Inshoting Paradigm 注射神经——与肉毒杆菌毒素的区别
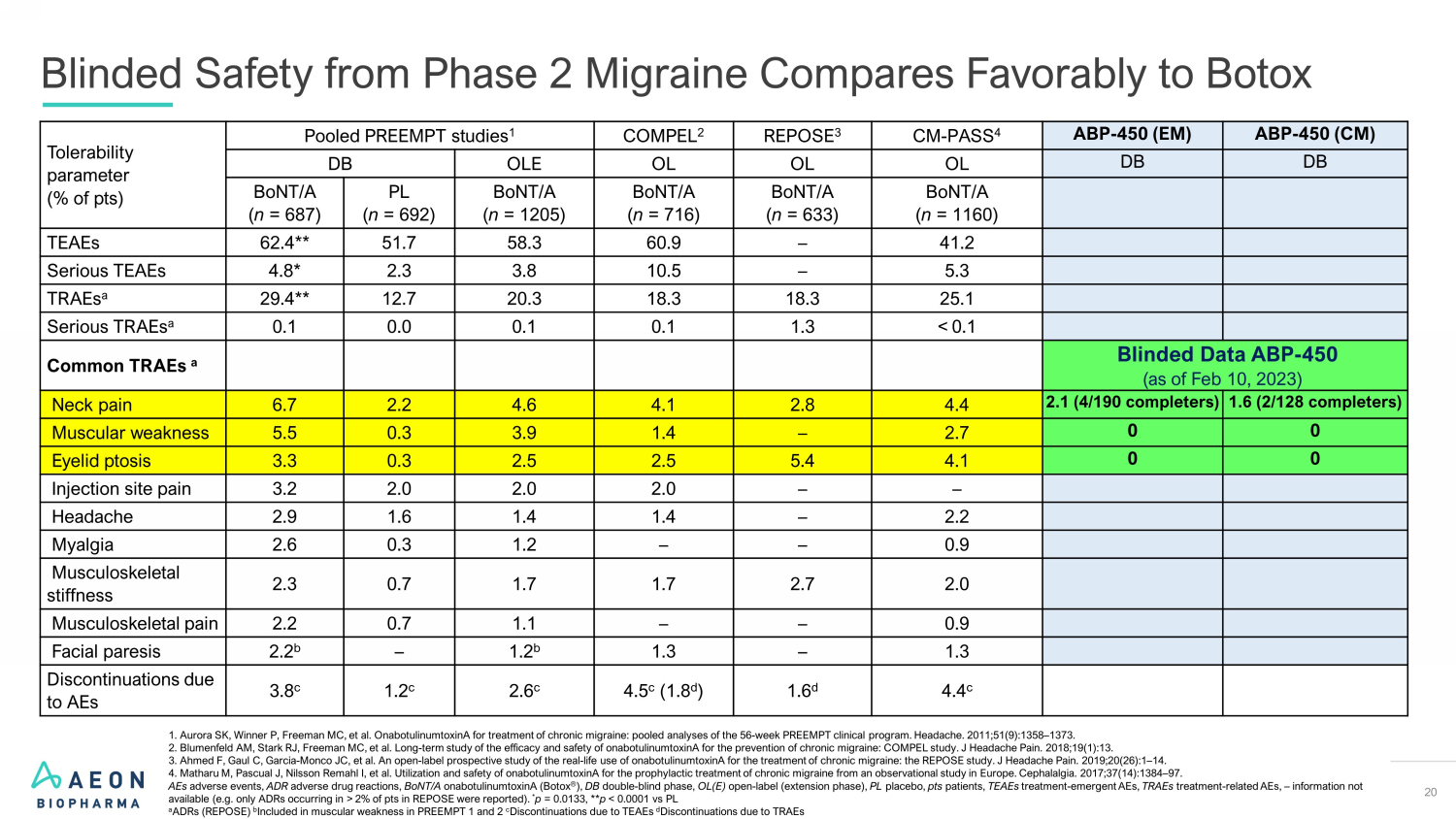
20 容忍度参数(百分比)Poled PREEMPT 研究 1 COMPEL 2 REPOSE 3 CM-PASS 4 ABP-450 (EM) ABP-450 (CM) DB OLE OL OL DB Bont/a (n = 692) bont/a (n = 633) bont/a (n = 633) bont/a (n = 633) bont/A (n = 633) bont/A (n = 633) bont/A (n = 633) bont/A (n = 633) bont/A (n = 633) bont/A (n = 633) bon= 1160) TEAE 62.4** 51.7 58.3 60.9 — 41.2 Serious TEAE 4.8* 2.3 3.8 10.5 — 5.3 traE a 29.4** 20.3 18.3 25.1 Serious traE a 0.1 0.1 0.1 1.3 的 repose 中有 2% 的点数被报告了)。* p = 0.0133,** p

胃轻瘫

22 Gastroparesis ABP 的机会——450 • 2019 年 FDA 行业指南 1 • 由于尚无明确、可靠的患者报告结果 (PRO),美国食品药品管理局建议将核心体征和症状列为终点。• 预计在 2024 年启动 2a 期研究 • 我们的主要终点衡量核心体征和症状在 12 周治疗期内与基线相比的变化 • 我们计划在单独的试验中评估特发性和糖尿病患者的潜在监管途径 • 定义为胃排空延迟 • 症状为慢性伴有发作性恶化 • 恶心、呕吐和疼痛是最令人不安的症状 • 既有特发性又有糖尿病(神经损伤会导致肠道肌肉功能受损)• 治疗选择非常有限;Reglan® 和 Gimoti tm(甲氧氯普胺)受限于 aES The Darsore • 约 400,000 名患者 2 • 约 900 亿美元的市场 • 未满足的需求高,竞争强度低 • 我们知道没有其他神经毒素寻求胃轻瘫适应症 • 数据来自研究者赞助的试验显示,内窥镜下注射沥青内注射神经毒素对神经毒素有积极反应特发性和糖尿病性胃轻瘫患者的幽门 ABP-450 机会 1. https://www.fda.gov/media/129880/download 2.公司的估计基于2017年美国人口普查预测;赛义德,《美国胃轻瘫的流行病学和诊断:基于人群的研究》。(2019);以及帕克曼,特发性胃轻瘫的临床特征因性别、体重、症状发作、胃排空延迟和胃轻瘫严重程度而异(2011 年)。
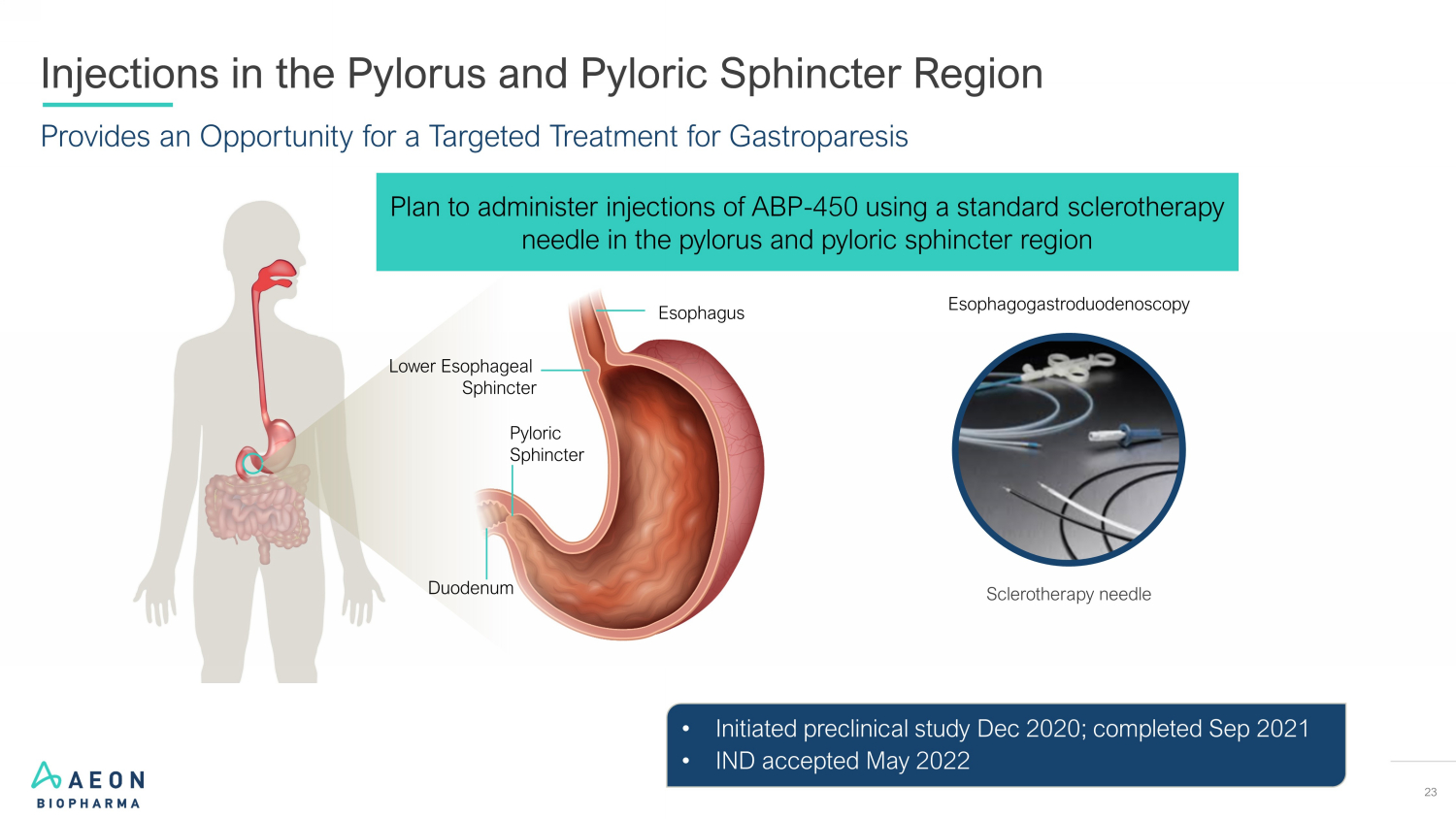
23 为幽门和幽门括约肌区域胃轻瘫注射提供机会硬化疗法针头食管胃十二指肠镜检查计划在幽门和幽门括约肌区域使用标准硬化疗法针头注射ABP-450 食管下食管括约肌幽门括约肌十二指肠 • 2020 年 12 月启动临床前研究;2021 年 9 月完成 • IND 于 2022 年 5 月接受

创伤后应激障碍(PTSD)

25 创伤后应激障碍(PTSD)• 创伤后应激障碍(PTSD)的定义很明确,具有广泛的疾病意识 • 一种可能发生在经历或目睹一个或多个创伤事件的人身上的精神障碍 • 症状类别包括入侵(非自愿记忆)、认知和情绪改变(负面想法和情绪)以及觉醒和反应改变(愤怒爆发)疾病 1 • 当前的 t 治疗包括认知行为疗法、药物(例如 SSRI、SNRI)和其他替代疗法 • 美国食品药品管理局已制定监管规定包括Zoloft和Paxil在内的多种药物的临床开发途径 • 许多经过验证的量表已经被广泛接受(例如CAPS、PCL-5、BDI)当前的治疗和监管途径 1。美国精神病学协会。https://www.psychiatry.org/patients-家庭/ptsd/what-is-ptsd。

26 与星状神经节相关的创伤后应激障碍来源:左图:Rae Olmsted KL、Bartoszek M、Mulvaney S 等。星状神经节阻滞治疗对创伤后应激障碍症状的影响:一项随机临床试验。JAMA Psychiatry。2020;77 (2): 130 — 138。doi: 10.1001/jamapsychiatry.2019.3474。右图:Levi、Ofir、Ariel Ben Yehuda、Daniel S. Pine 和 Yair Bar——Haim。“发人深省地审视轻度相关创伤后应激障碍的治疗效果。”《临床心理科学》10,第 4 期(2021):690 — 99。https://doi.org/10.1177/21677026211051314。星状神经节阻滞治疗对创伤后应激障碍症状的影响一项随机临床试验 Kristine L. Rae Olmsted,MSH;Michael Bartoszek,医学博士;Sean Mulvaney,医学博士;等人 JAMA Psychiatry。2020;77 (2): 130-138。关键要点问题:与虚假治疗相比,星状神经节阻滞在8周内降低创伤后应激障碍症状的严重程度如何?发现:在这项虚假对照随机临床试验中,相隔2周的2次星状神经节阻滞治疗可有效降低临床医生对DSM的创伤后应激障碍量表在8周内的总症状严重度评分为5分。接受星状神经节阻滞组的调整后的平均症状变化为−12. 6个百分点,而接受假治疗的组的调整后的平均症状变化为−6.1个百分点,差异显著。含义:星状神经节阻滞治疗作为创伤后应激障碍的辅助治疗方法值得进一步研究。冷静看待军人相关创伤后应激障碍的治疗有效性一项随机临床试验 Ofir Levi、Ariel Ben Yehuda、Yair Bar-Haim;等人临床心理科学。2021;10,no.4 摘要大约三分之二的创伤后应激障碍(PTSD)退伍军人在治疗后仍患有这种疾病。在现实世界的临床环境中,查明治疗的每种症状的有效性可以突出治疗强化和开发的相关领域。对709名患有创伤后应激障碍的退伍军人进行了创伤后应激障碍和抑郁症的基线和治疗后评估。创伤后应激障碍的缓解率为 39.4%。治疗对入侵症状的效果最差,对倒叙或对创伤特征记忆不佳没有影响。在汇款的退伍军人中,72.8%仍然符合至少一个集群的诊断标准。注意到抑郁症的临床疗效不佳;只有4. 1% 的患者在治疗后缓解。在现实世界中,创伤后应激障碍退伍军人的治疗效果有限。增强治疗反应可能需要提高提供者的忠诚度和患者对现有治疗的依从性,或者开发专门针对对现有治疗反应不佳的创伤后应激障碍症状的新疗法。AW0GR (A1)
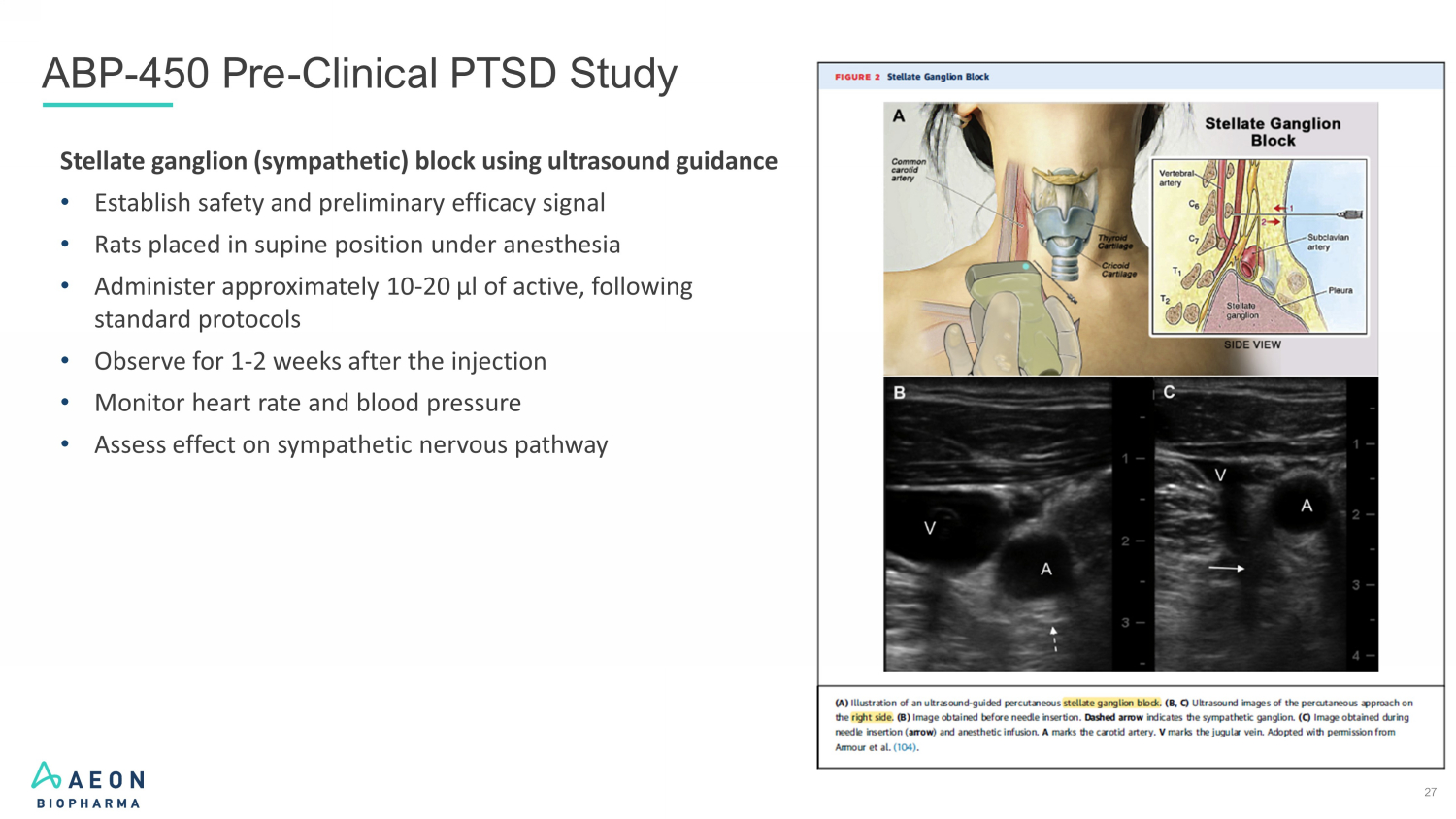
27 使用超声引导进行星状神经节(交感神经)阻滞 • 建立安全和初步疗效信号 • 麻醉下仰卧位的大鼠 • 按照标准方案给予大约 10-20 µl 活性物质 • 注射后观察 1-2 周 • 监测心率和血压 • 评估对交感神经通路的影响 ABP-450 临床前 PTSD StudyAW0 GR (A1)

宫颈肌张力障碍

29 宫颈肌张力障碍 ABP 的机会——450 • 具有有效发育的潜力 • 有可能允许参与部分标签上的运动障碍 • 有可能通过有针对性的临床项目利用更广泛的肌肉痉挛适应症和标签肌肉运动障碍的重要适应症 • 宫颈肌张力障碍是一种无法治愈的慢性疾病 • 颈部和肩部扭动作疼痛且虚弱 • 注射肉毒杆菌毒素是治疗的标准 • 已确立的结果衡量标准和监管途径 The Darsor •约50,000名患者 • 约3.6亿美元市场 • 2019年治疗性毒素市场销售额中约有40%用于各种肌肉运动障碍 • 预计第三阶段计划将包括与Botox® 进行头对头比较,以证明ABP在美国的市场机会——450来源:公司基于2017年美国人口普查预测 Defazio、宫颈肌张力障碍描述性流行病学(2013)美国神经病学会理查森的估计-爱沙尼亚治疗 (2017)
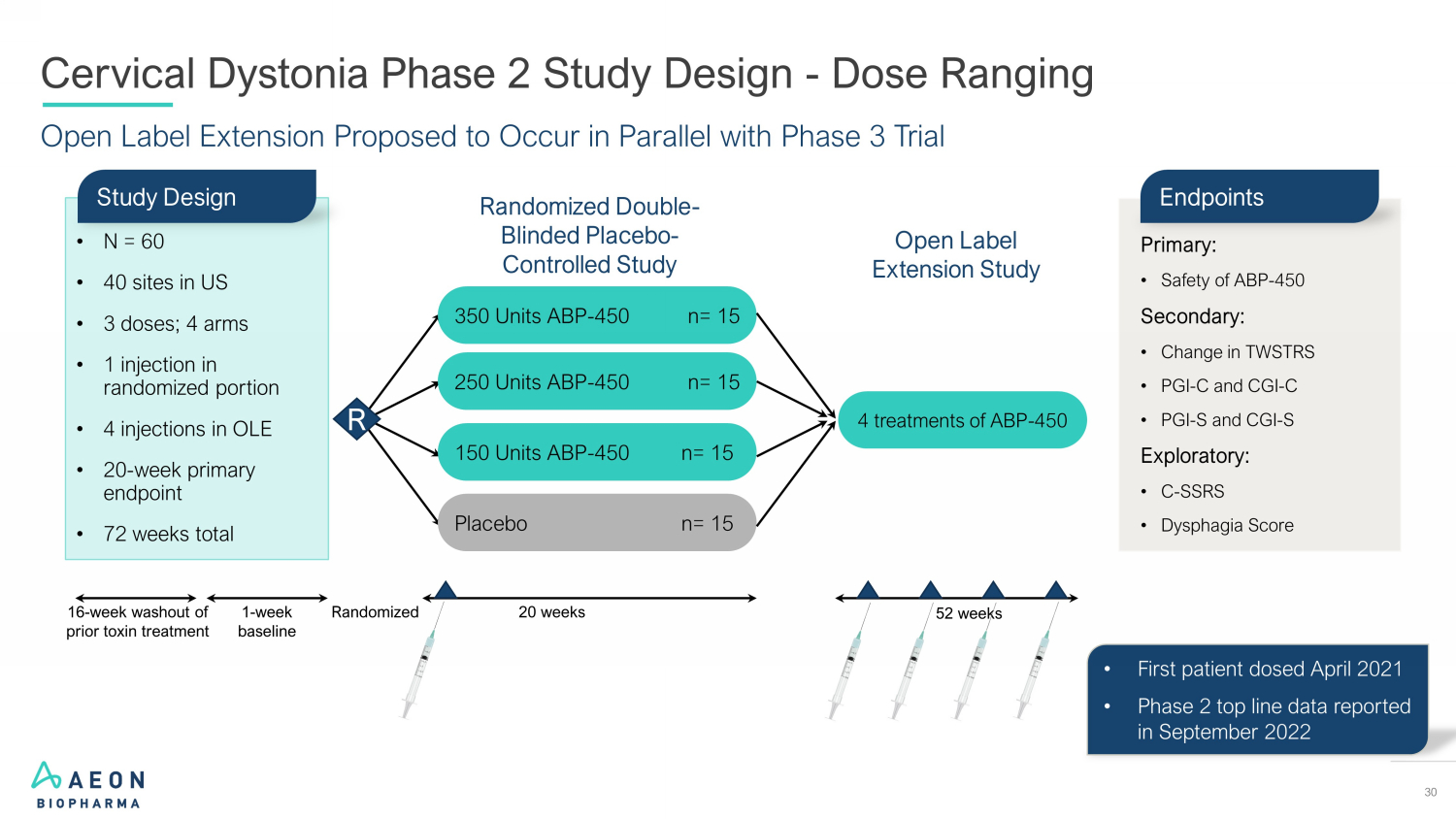
30 开放标签延期拟与 3 期临床试验宫颈肌张力障碍 2 期研究设计——剂量范围 • 2021 年 4 月首例患者给药 • 2022 年 9 月报告的第 2 期主要数据随机双盲安慰剂——对照研究 20 周随机 R 1-周基线 16 周——冲洗之前的毒素治疗开放标签延期研究安慰剂 n= 15 150 单位 ABP-450 nP-450 个单位 ABP-450 个单位 ABP-450 个单位 ABP-450 个单位 ABP-450 个单位 ABP-450 个单位 ABP-450 nP-450 个单位 ABP-450 个单位 = 15 350 单位 ABP-450 n= 15 4 次 ABP 治疗——450 52 周主要:• ABP 的安全性——450 次要:• TWSTRS 的变化 • PGI-C 和 CGI-C • PGI-S 和 CGI-S 探索性:• C-SSRS • 吞咽困难评分终点 • N = 60 • 美国 40 个地点 • 3 剂量;4 支手臂 • 随机部分注射 1 次 • OLE 注射 4 次 • 20 周主要终点 • 共 72 周研究设计设计

31 讨论和结论 • 2 期试验达到主要和其他关键终点,支持 ABP-450 在减少与 CD 相关的体征和症状方面的安全性和有效性。• ABP-450 显示出与治疗 CD 的其他肉毒毒素产品相似或低于其他肉毒杆菌毒素产品的不良反应发生率。• 因治疗而停药的次数为零-紧急不良事件 (TeaE) • 治疗率低——相关 TEAE (traE) • 零 dyaE 150 U 组出现吞咽病例,总体吞咽困难 (11%) 和肌肉无力 (6.7%) 发生率较低 • 所有 TRAE 均为轻度至严重程度为中度且本质为短暂性 • ABP-450 在治疗 CD 方面的疗效与其他肉毒毒素产品相似或更好。• 第 4 周 TWSTRS 在 150 U 中提高了 14.01 个百分点;250 U 中提高了 11.28 个百分点;350 U 在 350 U 中提高了 9.92 个百分点 — 低剂量组(150 U 和 250 U)的统计学意义,高剂量组(350 U 和 250 U)的数字有所改善) 与安慰剂对比 • 患者全球变化印象(PGI-C)在所有三个 ABP-450 剂量组中均比安慰剂有统计学上的显著改善 •临床全球变化印象(CGI-C)显示,与安慰剂相比,所有三个ABP-450剂量组的治疗效果持续时间均有统计学上的显著改善 • 150 U的中位治疗效果持续时间至少为20周,250 U的中位治疗持续时间为20周,350U的中位治疗持续时间为20周。

财务概览
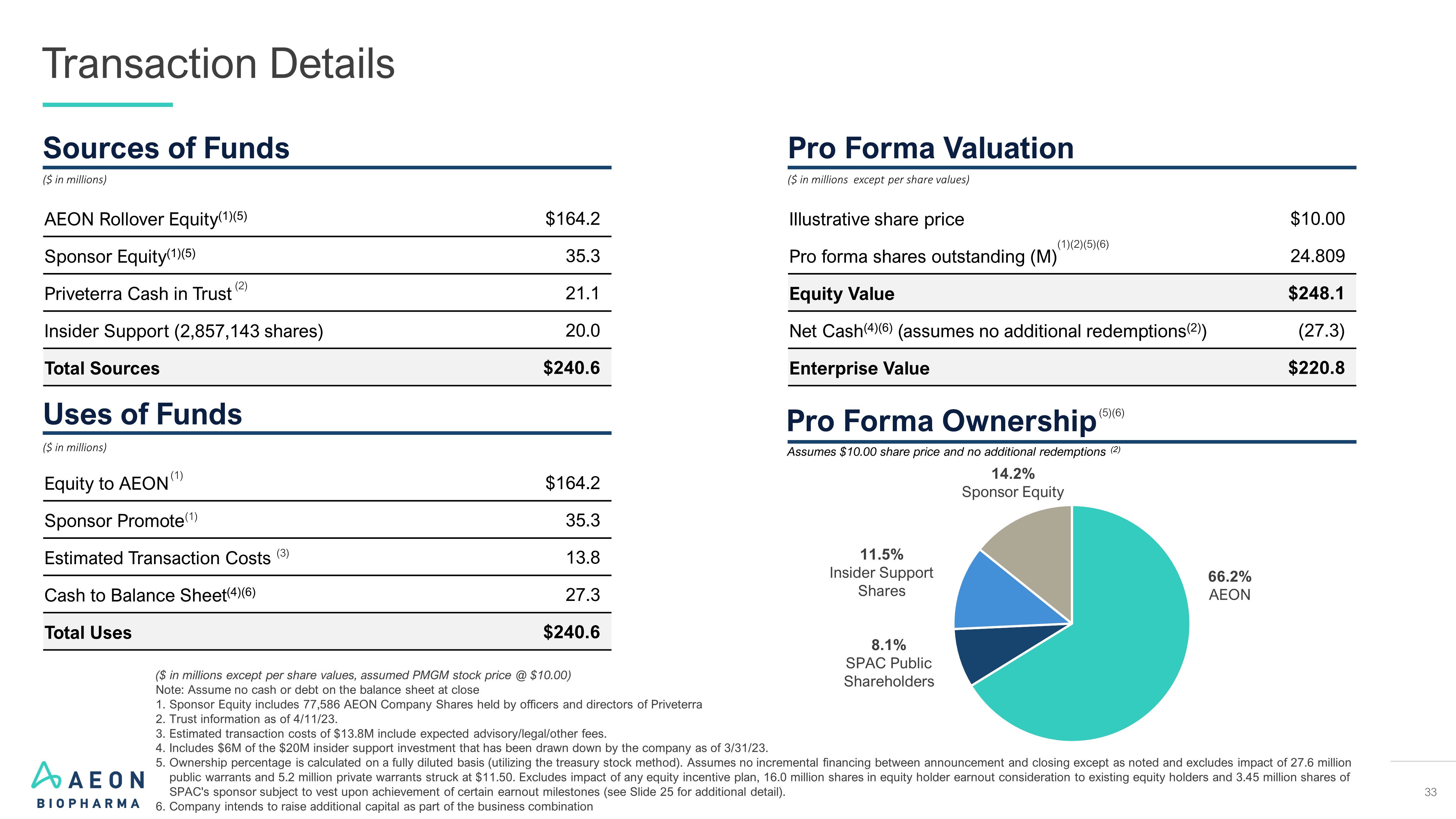
33 交易详情(以百万美元为单位,每股价值除外,假设 PMGM 股价 @ 10.00 美元)1.截至 23 年 3 月 31 日的信任信息。2.AEON Cash 截至 23 年 3 月 31 日,未经审计。3.所有权百分比在全面摊薄的基础上计算(使用库存股法)。假设除非另有说明,否则在宣布和收盘之间没有增加融资,并且不包括以11.50美元发行的2760万份公开认股权证和520万份私人认股权证的影响。不包括任何股权激励计划的影响、现有股权持有人的1600万股股权持有人盈利对价以及SPAC赞助商的345万股股票将在实现某些收益里程碑后归属(更多细节见幻灯片34)。预计交易成本为1,380万美元,包括预期的咨询/法律/其他费用。Pro Forma 估值说明股价 10.00 美元Pro forma 已发行股份 (M) 24.809 股权价值 248.1 美元净现金(假设没有额外赎回 (1))(30.9) 企业价值 217.2 美元(每股价值除外,以百万美元计)Pro Forma 所有权 8.1% SPAC 公众股东 13.9% 赞助商权益 66.5% AEON 假设股价为 10.00 美元,没有额外赎回 (1) 来源 of Funds AEON 展期权益 $165.0 赞助商权益 34.5 Priveterra Cash in Trust 20.0 AEON Cash 4.7 内幕支持(2,857,143 股)20.0 总来源 244.2 美元(百万美元)用途of Funds (3) (1) (2) AEON 股权 165.0 美元赞助商推广 34.5 预计交易成本 13.8 现金转资产负债表 30.9 总用途 244.2 美元 (4) (百万美元) (3) 11.5% Insider Support Shares
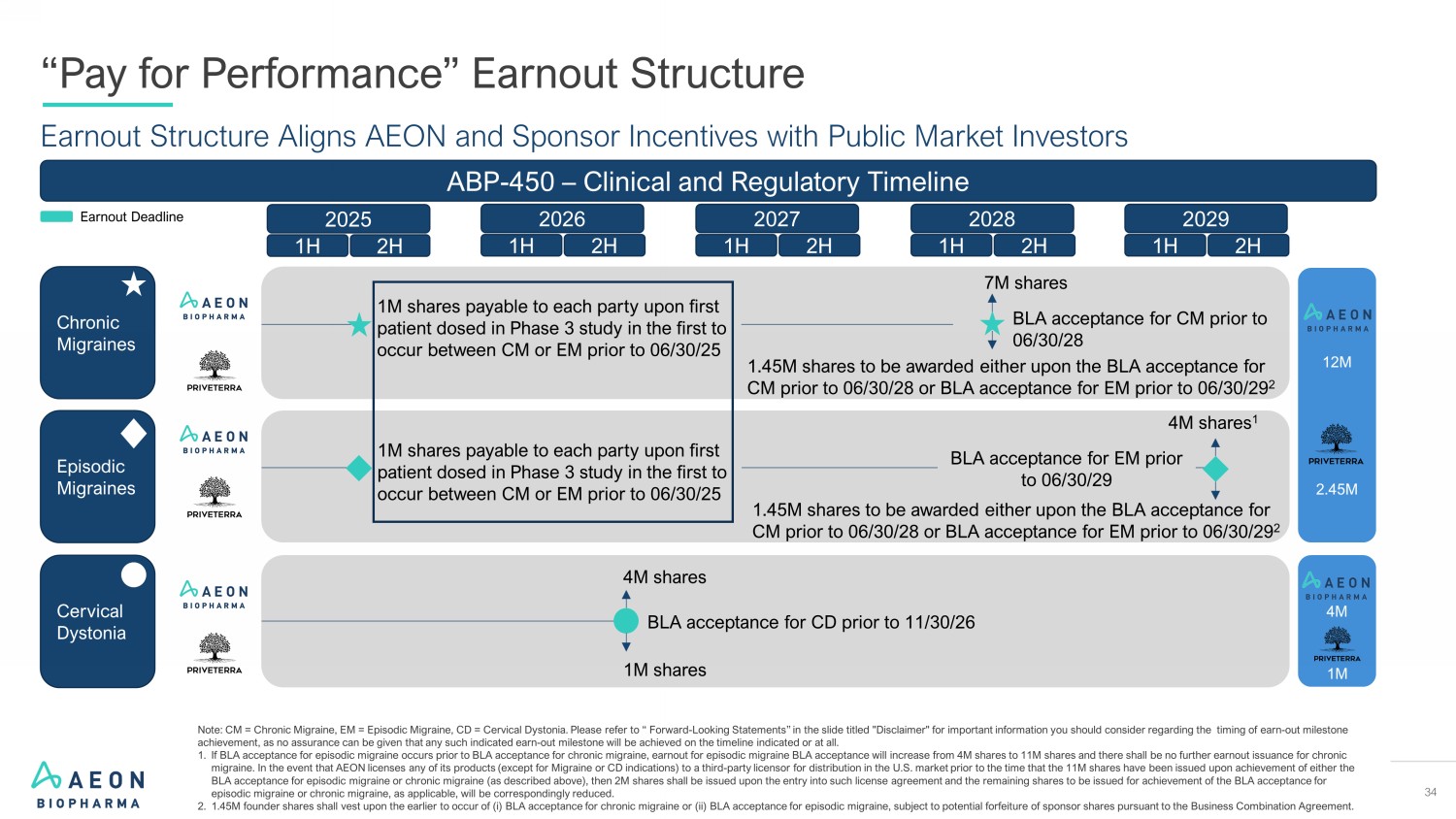
34 盈利结构使永旺和赞助商激励措施与公开市场投资者保持一致 “按绩效付费” 收益结构 ABP-450 — 临床和监管时间表 2025 下半年上半年 2027 年上半年 2028 下半年盈利截止日期 2 月 30 日之前 BLA 在 3 期研究中接受第一例患者在 CM 和 EM 之间给药,每方可获得 100 万股股票 06/30/25 7M 股票 Episodic Migarines 400M 股票 1 宫颈肌张力障碍 BLA 在 26 年 11 月 30 日之前获得 CD 的接受率 100 万股 400 万股 145 万 1M 4M 1.45M 股将在 28 年 6 月 30 日之前获得 BLA 接受 CM,或者在 29 年 6 月 30 日之前 BLA 接受新兴市场的 BLA 接受 2 100万股股票。在 25 年 6 月 30 日之前 CM 或 EM 之间的第一例患者给药,在 BLA 在 28 年 6 月 30 日之前接受 CM 或 BLA 在 29 年 6 月 30 日之前接受 BLA 接受 EM 后 2 BLA 29 年 6 月 30 日之前的 EM 注意:CM = 慢性偏头痛,EM = 发作性偏头痛,CD = 宫颈肌张力障碍。请参阅标题为 “免责声明” 的电子幻灯片中的 “前瞻性陈述”,了解在实现盈出里程碑的时机方面应考虑的重要信息,因为无法保证任何此类指定的盈出里程碑将在规定的时间表内实现或根本无法实现。1.如果BLA接受发作性偏头痛的时间早于BLA接受慢性偏头痛,则发作性偏头痛的收益BL A的接受率将从400万股增加到1100万股,并且不会进一步发行慢性偏头痛的盈利。如果AEON在BLA接受发作性偏头痛或慢性偏头痛(如上所述)后将其任何产品(偏头痛或慢性偏头痛适应症除外)许可给第三方许可方在美国市场分销,则应在该许可协议签订后发行200万股股票,剩余股份将发行以实现BLA的认可对于发作性偏头痛或慢性偏头痛,视情况而定,将相应减少。2. 1.45我的创始人股份应在 (i) BLA 接受慢性偏头痛或 (ii) BLA 接受 f 或发作性偏头痛的前提下归属,但根据业务合并协议,赞助商股份可能会被没收。
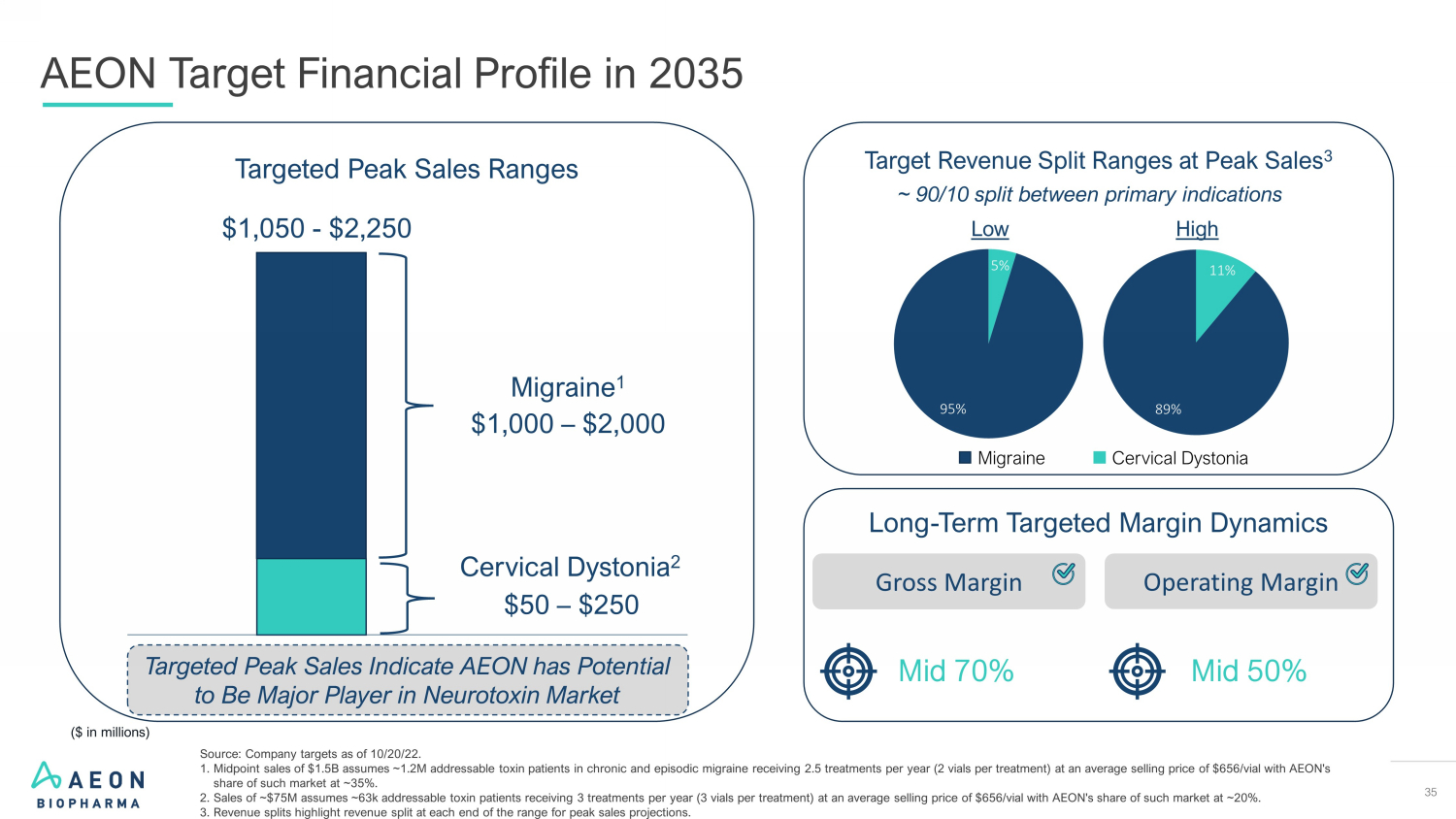
35 AEON Target 2035年的财务概况(百万美元)11% 89% 5% 95% 目标峰值销售范围目标收入分割范围 3 长期目标利润率动态中 50% 中70%偏头痛宫颈肌张力障碍 ~ 90/10 主要适应症之间的分配毛利率营业利润率目标峰值销售表明永旺有可能成为神经毒素市场的主要参与者 $1,050-$2,250 $1,000 — 2,000 美元 — 2,000 美元 — 250 美元 Dyine 1 Hurbain Stonia 2 Low High Source:公司的目标截至 22 年 10 月 20 日。1.中点销售额为15亿美元,假设约120万名慢性偏头痛和发作性偏头痛中可治疗的毒素患者每年接受2.5次治疗(每次治疗2瓶),平均销售价格为656美元/瓶,永旺在该市场的份额约为35%。销售额约为7500万美元,假设约6.3万名有针对性的毒素患者每年接受3次治疗(每次治疗3瓶),平均销售价格为656美元/瓶,AEON在该市场的份额约为20%。收入分割突出显示了区间两端的收入分配,以预测峰值销售额。
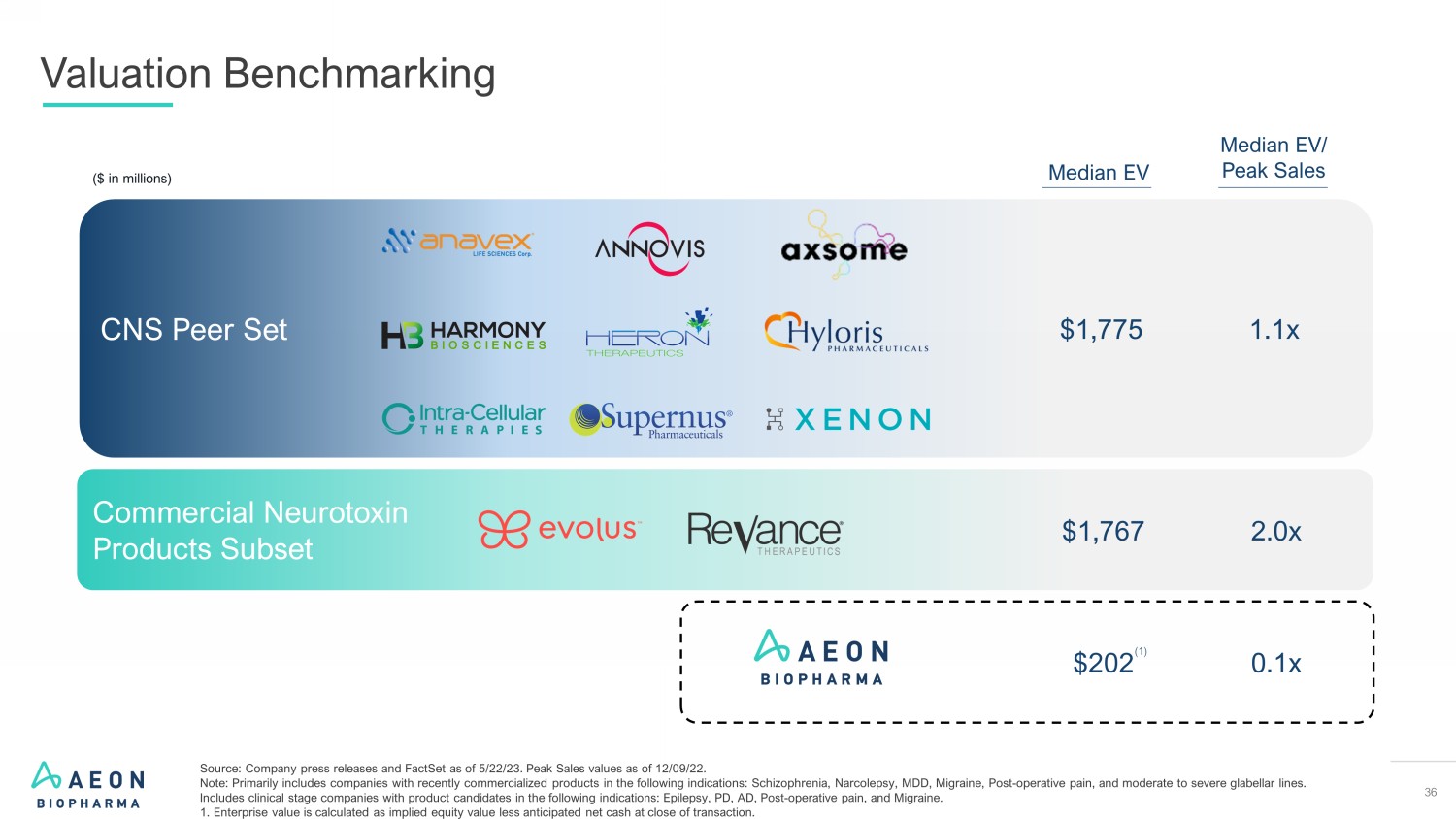
36 估值基准(百万美元)CNS同行集商用神经毒素产品子集中位数电动汽车/峰值销售额中位数为1,775 1.1x 1,767 2.0x 202 美元 0.1x (1) 来源:截至23年5月22日的公司新闻稿和FactSet。截至 22 年 9 月 12 日的峰值销售值。注意:主要包括最近将以下适应症产品商业化的公司:精神分裂症、Narcole psy、MDD、偏头痛、术后疼痛和中度至重度眉间纹。包括具有以下适应症的候选产品的临床阶段公司:癫痫、PD、AD、术后疼痛、和偏头痛。1.企业价值的计算方法是隐含权益价值减去交易结束时的预期净现金。
37 Investment Highlights 肉毒杆菌毒素已在数十种已公布的用途中显示出效用,ABP-450 有望获得 ABP 450;由于现有的美学 BLA(由 Evolus 单独持有)和制造基地获得 FDA、EMA 和加拿大卫生部批准的发作性偏头痛将使当前可治疗的患者群体增加近三倍(Botox® 仅适用于慢性偏头痛);ABP-450 2 期偏头痛研究包括慢性偏头痛和发作性偏头痛注射方案简化的患者有可能提高安全性和耐受性,有可能推行治疗毒素竞争对手目前不追求的传统药物定价模式,预计900kDa的肉毒杆菌毒素将促进医生采用管理团队拥有丰富的神经毒素商业和临床开发经验,这意味着自2019年以来对AEON的投资约为1.24亿美元强劲的发作性偏头痛市场扩张商业模式优势强大的领导力和赞助市场竞争的时机关键目标单一现有竞争对手已成熟市场(发作性偏头痛和慢性偏头痛);与美学市场不同,ABP-450的治疗重点将在产品到产品的基础上与市场领导者竞争,而不是与产品组合竞争 PTSD Opportunity 正在进行的临床前项目在解剖学的新部分中利用专有注射范例旨在提供IND支持的安全性和有效性数据;这种创新方法有可能在包括创伤后应激障碍在内的广泛的神经/心理学产品组合中发挥作用

附录

39 新进入者有效竞争 ABP 知识产权考虑因素的高壁垒——450 3 4 2 9 独家许可和供应协议 • 根据协议,大雄制造并向 AEON 提供 ABP-450 • 协议于 2019 年第四季度启动 • 已授予治疗适应症商业化独家许可 1 号协议所涵盖的治疗适应症美国专利正在申请的 PCT 国际专利正在申请的专利总数和专利如果已发放,专利将在 2040 年之前提供知识产权保护注:国家包括美国、加拿大、南非、澳大利亚、俄罗斯、欧盟、英国。
40个风险因素风险因素摘要公司的业务面临许多风险和不确定性,这些风险和不确定性代表了公司在成功实施战略和业务增长方面面临的挑战。以下是本演示文稿的附录,其中包括与公司使用相关的某些主要风险的摘要,但这些风险并不是公司现在面临或将来可能面临的唯一风险。您应仔细考虑讨论这些风险以及与公司业务和业务合并相关的其他风险,这些风险将包含在Priveterra提交的S-4表格注册声明中的委托书/招股说明书中。1.我们的运营历史有限,自成立以来已经蒙受了重大损失,预计在可预见的将来,我们将继续蒙受损失。如果我们实现了盈利,我们可能无法维持盈利。2.目前,我们未来的成功完全取决于我们唯一的候选产品ABP-450的成功和及时的监管批准和商业化。药品的开发和商业化受到广泛的监管,在我们计划及时或根本开发的任何适应症中,我们可能无法获得ABP-450的监管批准。临床产品开发涉及漫长、昂贵且不确定的过程。我们承担的费用可能超出我们的预期,或者在临床研究中遇到严重的延误或困难。4.在临床研究中注册和留住患者是一个昂贵且耗时的过程,由于我们无法控制的多种因素,可能会延迟、变得更加困难或不可能。如果我们在招收患者参加临床研究方面遇到延误或困难,我们可能会延迟或无法获得必要的监管批准。5.即使在这笔交易之后,我们仍需要额外的资金来为未来的运营提供资金,而未能在需要时以可接受的条件获得额外资本,或者根本无法获得额外的资本,可能会迫使我们推迟、限制、减少或终止运营。我们得出的结论是,自合并财务报表发布之日起一年内,我们没有足够的现金为我们的运营提供资金和履行到期的债务,因此,我们继续作为持续经营企业的能力存在重大疑问。7.ABP-450 可能会造成不良副作用或具有其他特性,这些特性可能会延迟或阻碍其在我们提出的任何治疗适应症中的监管批准,限制其商业潜力或在任何潜在的上市批准后导致严重的负面后果。其他各方涉及与 ABP-450 相同或几乎相同的肉毒杆菌毒素复合物的临床研究结果,或者我们进行的任何临床前研究的结果,可能无法预测我们的临床研究的未来结果。9.我们可能不时公布或发布的临床研究的中期或初步数据可能会随着更多可用的pa tie nt数据而发生变化,并且需要接受审核和验证程序,这可能会导致最终数据发生重大变化。10.由于我们的资源和资本渠道有限,我们必须优先开发ABP-450的某些治疗用途;这些决定可能被证明是错误的,可能会对我们的业务产生不利影响。11.我们可能无法成功获得专门考虑ABP-450的治疗用途的原始BLA。12.即使我们的任何拟议适应症获得监管部门的批准,ABP-450也可能无法获得医生、患者、第三方付款人和医学界其他人获得商业成功所必需的广泛市场认可。

41 风险因素(续)13.ABP-450,如果在任何当前提议或未来的治疗适应症中获得批准,将面临激烈的竞争,而我们未能有效竞争可能会阻碍我们实现显著的市场渗透和扩张。14.如果获得批准, ABP-450可能比预期的更早面临竞争. 15.如果我们无法自行或通过第三方建立销售和营销能力,那么如果在任何拟议的治疗适应症中获得批准,我们将无法成功地将ABP-450完全商业化,也无法产生产品收入。我们将需要扩大本组织的规模, 在管理这种增长方面我们可能会遇到困难. 17.我们的员工、独立承包商、顾问、商业合作者、主要调查员、供应商和其他年龄段的人可能从事不当行为或其他不当活动,包括不遵守监管标准和要求。18.如果对我们提起产品责任诉讼,我们可能会承担巨额责任,并且可能需要限制 ABP-450 的 comme rci 化。19.如果我们未能吸引和留住高级管理层和关键科学人员,我们可能无法在任何拟议的治疗适应症中成功开发出ABP-450,无法进行临床研究和商业化ABP-450。20。我们依靠《大雄协议》为我们提供在某些地区商业化和分销 ABP-450 的专有权利。大雄协议规定的任何重要权利(包括独家经营权)的终止或丧失都将对我们ABP-450的开发或商业化产生重大不利影响。21我们目前完全依靠大雄来制造ABP-450,因此,大雄的任何生产或其他问题都可能对我们产生不利影响。生物制剂的制造很复杂,Daewoong可能会在生产中遇到困难,这可能会影响我们为临床研究提供ABP-450供应的能力,我们获得上市批准的能力,或者我们获得产品的商业供应的能力,如果获得批准,这些供应可能会被推迟或停止。22.我们严重违反与 Medytox, Inc. 的许可和和解协议条款可能会对我们的业务产生重大不利影响。23.我们依赖并将继续依赖第三方和顾问来进行我们所有的临床前研究和临床研究。如果这些第三方或顾问未能成功履行合同职责或在预期的最后期限之前完成任务,我们可能无法获得ABP-450的监管批准。24.如果我们或我们当前或未来的任何许可方,包括大雄,无法维护、获得或保护与ABP-450相关的知识产权,我们可能无法在我们的市场上进行有效竞争。25.即使我们在任何治疗适应症中获得监管部门对ABP-450的批准,我们仍将受到持续的监管义务和持续的监管审查,这可能会导致大量额外费用,限制或延迟监管部门的批准,如果我们未能遵守适用的监管要求,我们将受到处罚。从理论上讲,ABP-450 如果在任何治疗适应症中获得批准,可能会受到标签和其他限制以及市场退出,如果我们未能遵守监管要求或我们的产品遇到意想不到的问题,我们可能会受到处罚。26.即使我们获得了上市批准,ABP-450在任何当前提出的或未来的治疗适应症中也可能无法获得保险和足够的报销,如果获得批准,这可能使我们很难以盈利的方式销售该产品。27.COVID-19 疫情已经并将继续对我们的运营以及我们的制造商、临床研究组织或 CRO 或其他与我们开展业务的第三方的业务或运营产生不利影响。
42 风险因素(续)28.第三方关于知识产权侵权、挪用或违规的索赔,或与我们可能获得或许可中的任何已颁发专利的无效或不可执行性相关的质疑,可能会阻碍或延迟我们的开发和商业化工作,或者以其他方式对我们的经营业绩产生不利影响。29.我们可能会卷入旨在保护或执行我们的知识产权或许可人的专利和其他知识产权的诉讼,这可能既昂贵又耗时。30.我们开发和商业化 ABP-450 和未来候选产品的权利在一定程度上受包括 Daewoong 在内的其他人授予我们的许可条款和条件的约束。如果我们未能遵守向第三方许可知识产权的协议中的义务,或者我们与许可方的业务关系中断,我们可能会失去对我们的业务至关重要的许可权。31.我们可能无法保护我们在世界各地的知识产权。32.如果我们无法保护商业秘密的机密性,我们的业务和竞争地位可能会受到损害。33.我们可能会被指控我们的员工、顾问或独立承包商错误地使用或披露了第三方的初步信息,或者主张了我们认为自己的知识产权的所有权。34.如果我们的商标和商品名称没有得到充分保护,那么我们可能无法在我们的利益商标中建立名称认可度,我们的业务可能会受到不利影响。35.知识产权不一定能解决所有潜在威胁。
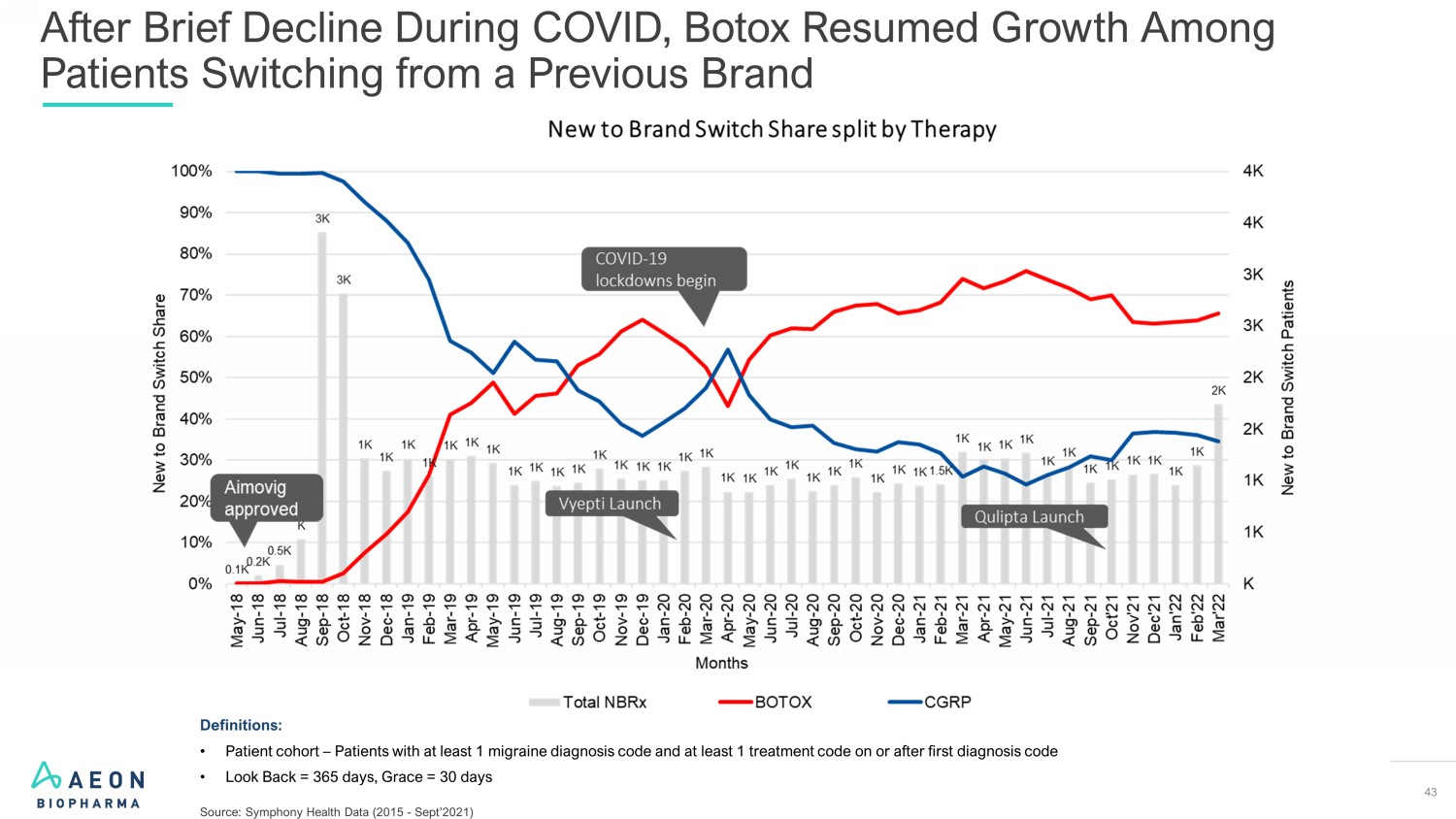
43 在COVID期间短暂下降之后,肉毒杆菌毒素在患者中恢复增长,不再使用先前的品牌定义:• 患者队列 — 至少有 1 个偏头痛诊断代码且在首次诊断代码上或之后至少有 1 个治疗代码的患者 • 回顾 = 365 天,Grace = 30 天来源:Symphony Health Data(2015-2021 年 9 月)

44 关键价值转折点治疗适应症原始 BLA 产品平台占有成熟市场,进入新适应症首次在成熟市场推出扩大治疗选择由成熟的 900 kDa 肉毒杆菌毒素复合物促进采用复制在已确定的治疗适应症上取得成功提高付款人和医生的价值医生从付款人那里获得持续和优惠的报销核心价值 BLA 和临床项目商业化验证模式扩大商业机会治疗性神经毒素市场的传统定价模式

45 顾问委员会具有高度相关的行业经验和成功记录经验丰富的顾问委员会安德鲁·布鲁门菲尔德、医学博士迈克尔·卡米莱里、医学博士 Chris Reist、偏头痛胃轻瘫神经/心理学博士 • 南加州头痛中心主任 • 委员会——获得美国精神病学和神经病学委员会神经病学认证,还获得了头痛医学认证。• 美国头痛学会头痛介入程序分会创始主席 • 广泛出版并有 60 多份同行评审出版物和 100 多份在头痛会议上发表海报 • 曾担任多项研究的首席研究员,经常在全国药物会议、医学会议、继续教育研讨会和社区活动上发表讲话。• 明尼苏达州罗切斯特的胃肠病学专家,在医学领域拥有超过 34 年的经验 • 梅奥诊所医学、药理学和生理学教授 • 梅奥诊所前发展主任 • 美国胃肠病学协会前主席 • 曾担任过几次会议 R01 和美国的复苏以及美国国立卫生研究院(NIH)的再投资法案(ARRA)资助 • 广泛出版并有 900 多篇同行评审出版物 • 荣获朱利叶斯·弗里登瓦尔德奖章,这是 AGA 因终身致力于胃肠病学而获得的最高荣誉 • 加州大学尔湾分校医学院精神病学和人类行为学教授兼解剖学和神经生物学名誉教授。• 研究兴趣包括成体干细胞、化学神经解剖学和神经解剖学和神经生物学荣誉教授电路、更高的大脑功能和大脑成像。• Sloan Scholar,资深人士富布赖特研究员,美国国立卫生研究院职业奖获得者,一系列荣誉学位和奖项获得者 • 五角大楼联合司令部 “认知与战争” 领域的主题专家。• 广泛发表并出现在许多纪录片、广播和电视节目中。Neuro/Psych James Fallon,博士 • 医学院精神病学与人类行为学名誉教授 • 研究精神科医生——弗吉尼亚州长滩医疗系统 • 目前他正在弗吉尼亚州长滩领导一个国防部项目,研究使用虚拟现实环境增加长期曝光率的潜在好处。• 广泛发表并有 100 多篇同行评审出版物 • 入选 2007-2019 年 “最佳医生” • 杰出医生 • 杰出人物美国精神病学协会会员 • 全国模范精神科医生奖精神病患者联盟 Del Stagg,监管机构/质量保证博士 • 在生物制药、医疗产品开发和监管事务方面有 40 多年的经验 • 之前的经验包括 Allergan、BD 和 Evolus • 负责药品、生物制剂(包括 Allergan 的 BOTOX®)的美国和国际监管部门审批 • 负责美国和国际监管部门对 Evolus® 的审批 • 众多成功进行首次公开募股的医疗产品公司的管理团队成员

46 Priveterra 赞助团队概述 • 以创新、透明度、长期关系和股东价值为驱动的专有投资论点的基本方法 • 过去二十年来在生命科学领域的良好往绩... 建立、运营和货币化投资 • 在收购和整合估值极具吸引力的公司方面拥有丰富的并购经验 • 成功实现新产品和技术商业化的历史 • 鲍勃·帕尔米萨诺将继续前进——前董事会职务 Robert Palmisano 已有 40 多年的历史独特而且在生命科学行业拥有丰富的经验,包括莱特医疗集团、ev3、Intralase Corp、MacroChem Corp 和 Summit Technology 的前总裁兼首席执行官 Vikram Malik 在金融领域拥有30多年的经验,曾在德意志银行和环球公司担任前投资银行副董事长——美国银行美林证券医疗技术主管 Oleg Grodnensky 在金融、战略咨询、投资、运营和公司领域工作超过 24 年科学行业 80 ~ 830 亿美元的并购总额已执行 26 约 160 亿美元的首次公开募股总额已执行 16 约 90 亿美元Tuck-ins/Integrations 完成了 5 个大约 100 亿美元的成功退出
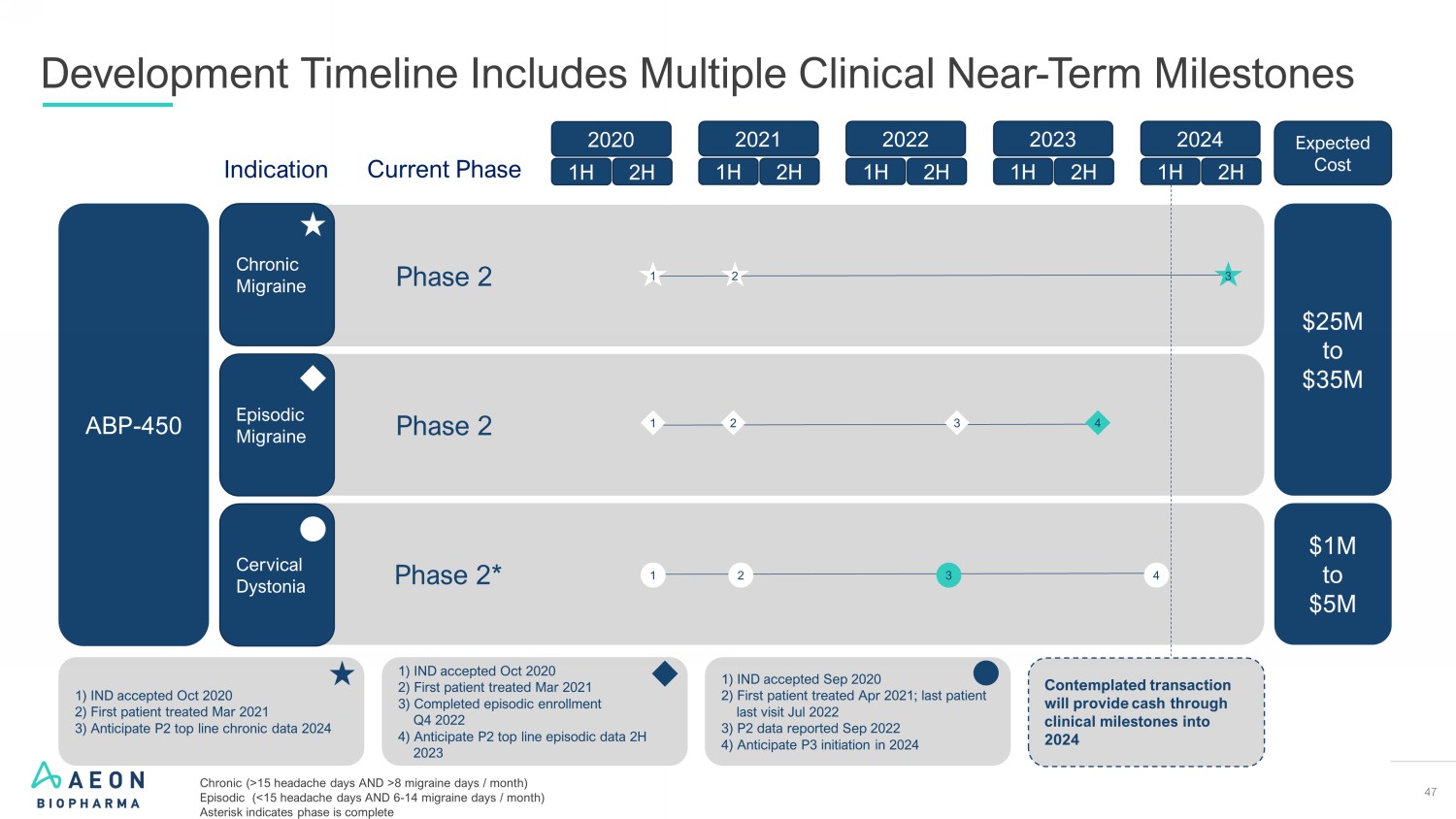
47 开发时间表包括多个临床近期里程碑慢性偏头痛发作性偏头痛适应症当前阶段 ABP-450 宫颈肌张力障碍 2 期 2* 2020 2H 2021 2H 2022 2H 1H 1 H 2023 2H 1H 1 2 3 1 1) 2022 年 10 月接受治疗的第一位患者 3) 预计 P2 第一季度发作数据 2H 2023 1 1 2 2 2 3 4 4) IND 2020 年 10 月接受 2) 第一位接受治疗的患者 2021 年 3 月 3) 预测 2024 年 P2 主要慢性数据 1) 2020 年 9 月接受 IND 接受 2) 第一位接受治疗的患者 2021 年 4 月;最后一位接受治疗的患者患者最后一次就诊 2022 年 7 月 3) 2022 年 9 月公布的 P2 数据 4) 预计在 2024 年启动 P3 预计将花费 2500 万美元至 350 万美元预计的交易将通过 2024 年 2024 年 2 小时 1H 的临床里程碑为慢性(>15 个头痛天和 >8 天偏头痛天/月)发作(

谢谢