目录表
美国证券交易委员会
华盛顿特区,邮编:20549
表格
|
根据1934年《证券交易法》第13或15(D)条 提交的年度报告。 截至本财政年度止 | |
|
根据1934年《证券交易法》第13节或第15(D)节提交的过渡报告。 关于从到的过渡期
|
委托文件编号:
(注册人的确切姓名在其章程中规定)
|
(述明或其他司法管辖权 公司或组织) |
(美国国税局雇主 识别号码) |
(主要执行机构地址和邮政编码)
(注册人电话号码,含 区号)
根据该法第12(B)条登记的证券:
| 每个班级的标题 | 交易代码 | 注册的每个交易所的名称 |
| 这个资本市场 | ||
| |
这个 |
根据该法第12(G)条登记的证券:
无
用复选标记
表示注册人是否为证券法第405条规定的知名经验丰富的发行人:YES☐
用复选标记
表示注册人是否不需要根据该法第13条或第15(D)条提交报告:是☐
用复选标记
表示注册人(1)是否在过去12个月内(或注册人被要求提交此类报告的较短时间内)提交了1934年《证券交易法》第13条或15(D)节要求提交的所有报告,以及(2)在过去90天内是否符合此类备案要求:
用复选标记
表示注册人是否在过去12个月内(或在注册人被要求提交此类文件的较短时间内)以电子方式提交了根据第
S-T条例(本章232.405节)规则405要求提交的每个交互数据文件:
用复选标记 表示注册人是大型加速申请者、加速申请者、非加速申请者、较小的报告公司还是新兴成长型公司。见《交易法》第12b-2条规则中“大型加速申报公司”、“加速申报公司”、“较小报告公司”和“新兴成长型公司”的定义。
| 大型加速文件服务器 | ☐ | 加速文件管理器 | ☐ |
| ☒ | 规模较小的报告公司 | ||
| 新兴成长型公司 |
如果是新兴成长型公司,用勾号表示注册人是否已选择不使用延长的过渡期来遵守根据《交易法》第13(A)节提供的任何新的或修订的财务会计准则。☐
用复选标记 表示注册人是否提交了一份报告,证明其管理层根据《萨班斯-奥克斯利法案》第404(B)条对其内部财务报告控制的有效性进行了评估,该内部控制是由编制 或发布其审计报告的注册会计师事务所进行的。☐
如果证券是根据该法第12(B)条登记的,应用复选标记表示登记人的财务报表是否反映了对以前发布的财务报表的错误更正。
用复选标记 表示这些错误更正中是否有任何重述需要根据§240.10D-1(B)对注册人的任何高管在相关恢复期间收到的基于激励的薪酬进行恢复分析。☐[1]
用复选标记表示注册人是否是空壳公司(如交易法规则12b-2所定义):
是,不是☐。
截至2022年6月30日,也就是注册人最近一个完整的第二财季的最后一个营业日,注册人的非关联公司持有的有投票权和无投票权普通股的总市值
基于注册人普通股在纳斯达克资本市场的收盘价0.8美元,约为$
截至2023年3月10日,注册人的普通股流通股数量为.
以引用方式并入的文件
为回应Form 10-K第三部分(第10、11、12、13和14项)所需的信息,现将注册人的最终委托书、信息说明书或2023年股东周年大会的Form 10-K年度报告修正案的部分内容合并于此。注册人打算 在注册人截至2022年12月31日的财政年度结束后120天内,以Form 10-K格式向证券交易委员会提交最终委托书、信息声明或对本年度报告的修正案。
___________________________
[1]根据美国证券交易委员会的指导意见,此空白复选框包含在本封面中,但在相关证券交易所上市标准通过并生效之前,不得对其进行任何披露。
Xenetic生物科学公司。
表格10-K的2022年年度报告
表格内容
| 第一部分 | 1 | ||
| 项目1 | 业务 | 1 | |
| 第1A项 | 风险因素 | 23 | |
| 项目1B | 未解决的员工意见 | 55 | |
| 项目2 | 属性 | 56 | |
| 第3项 | 法律诉讼 | 56 | |
| 项目4 | 煤矿安全信息披露 | 56 | |
| 第II部 | 57 | ||
| 第5项 | 注册人普通股市场、相关股东事项与发行人购买股权证券 | 57 | |
| 项目6 | [已保留] | 57 | |
| 第7项 | 管理层对财务状况和经营成果的探讨与分析 | 58 | |
| 第7A项 | 关于市场风险的定量和定性披露 | 66 | |
| 项目8 | 财务报表和补充数据 | 67 | |
| 项目9 | 会计与财务信息披露的变更与分歧 | 68 | |
| 第9A项 | 控制和程序 | 68 | |
| 项目9B | 其他信息 | 69 | |
| 项目9C | 关于妨碍检查的外国司法管辖区的披露 | 69 | |
| 第三部分 | 70 | ||
| 第10项 | 董事、高管与公司治理 | 70 | |
| 项目11 | 高管薪酬 | 70 | |
| 项目12 | 某些实益拥有人的担保所有权以及管理层和相关股东的事项 | 70 | |
| 第13项 | 某些关系和相关交易,以及董事的独立性 | 70 | |
| 项目14 | 首席会计费及服务 | 70 | |
| 第四部分 | 71 | ||
| 项目15 | 展品和财务报表附表 | 71 | |
| 项目16 | 表格10-K摘要 | 71 | |
| i |
有关前瞻性陈述的警示说明
本年度报告(以下简称“年度报告”)包含符合修订后的1934年证券交易法(“交易法”)第21E节和修订后的1933年证券法第27A节的前瞻性表述。除历史事实陈述外,本年度报告中包含的所有陈述,包括关于我们未来经营结果和财务状况、我们的业务战略和计划、未来收入、预计成本、前景和我们未来经营目标的陈述,均为前瞻性陈述 。这些前瞻性表述包括但不限于:冠状病毒或新冠肺炎全球大流行的挥之不去的影响及其应对措施,包括大流行对总体经济和市场状况的影响以及对我们的业务、经营业绩和财务状况的影响;地缘政治事件的预期影响,包括俄罗斯和乌克兰之间的冲突以及美国(下称“美国”)实施的相关制裁。合作安排的性质、时间和范围;根据合作安排的预期结果,包括根据合作安排获得监管机构批准的计划;我们候选药物商业化计划的结果;我们针对某些市场的计划,与第三方制造商合作, 并评估后续商业开发的其他候选药物,以及对我们候选药物的竞争的可能性和程度;我们计划推进创新的免疫肿瘤学技术,解决难以治疗的肿瘤适应症;对我们的脱氧核糖核酸酶(“DNase”)平台的期望 ,例如正在开发的DNase平台用于治疗实体肿瘤,旨在通过靶向中性粒细胞胞外陷阱(“Net”)来改善包括免疫疗法在内的现有治疗的结果,以及我们对优先考虑我们在这项新获得许可的技术上的努力和资源的期望;XCART的开发 ™嵌合抗原受体(“CAR”)T细胞(“XCART”)技术,并计划通过靶向单个患者恶性肿瘤细胞表面的独特B细胞受体 来开发基于细胞的疗法 用于治疗B细胞淋巴瘤;以及我们对我们的PolyXen的期望®平台,包括我们与生物技术和制药公司合作利用该平台的计划 及其在蛋白质或多肽疗法中的应用 及其应用,以改善下一代生物药物的半衰期和其他药学特性。
在某些情况下,这些 陈述可以通过诸如“可能”、“将”、“将”、“可能”、“应该”、“ ”、“预期”、“计划”、“预期”、“相信”、“估计”、“寻求”、“ ”、“大约”、“打算”、“预测”、“潜在”、“项目”或“继续”等术语来标识,“ 或此类术语和其他类似术语的否定。尽管我们相信本文中包含的前瞻性 陈述中反映的预期是合理的,但我们不能保证未来的结果、活动水平、业绩或成就。这些 陈述涉及已知和未知的风险和不确定因素,可能会导致我们或我们行业的结果、活动水平、业绩或成就与前瞻性陈述中明示或暗示的大不相同。
可能导致实际结果大相径庭的一些因素包括但不限于:
| · | 与CLS治疗有限公司(“CLS”)的交易和DNase平台的许可产生的意外成本、收费或支出; | |
| · | 在完成与CLS的交易和DNase平台的许可后,公司预期的财务业绩的不确定性; | |
| · | 未能实现DNase、XCART或PolyXen技术的预期潜力; | |
| · | 我们实施业务战略的能力; | |
| · | 未达到纳斯达克资本市场持续上市要求; | |
| · | 我们需要在未来筹集更多的营运资金,以便进一步发展我们的管道,并继续作为一家持续经营的企业; | |
| · | 我们为业务融资的能力; | |
| · | 我们成功执行、管理和整合关键收购和合并的能力; | |
| · | 产品开发和商业化风险,包括我们成功开发DNase技术的能力; |
| II |
| · | 不良安全结果和临床试验结果对我们疗法的影响; | |
| · | 我们有能力确保和维护我们技术的制造商; | |
| · | 新疗法和现有疗法的新用途对竞争环境的影响; | |
| · | 我们成功地将我们当前和未来的候选药物商业化的能力; | |
| · | 我们有能力实现与我们当前和未来的共同发展合作和战略安排相关的里程碑和其他付款; | |
| · | 我们依赖顾问、顾问、供应商和商业伙伴代表我们开展工作; | |
| · | 新技术对我们的候选药物和我们的竞争的影响; | |
| · | 政府机构的法律、法规发生变化; | |
| · | 中断或取消现有合同; | |
| · | 竞争性产品和定价的影响; | |
| · | 产品需求和市场接受度及风险; | |
| · | 拥有更多财力的竞争对手的存在; | |
| · | 按当前价格继续提供制造所用的用品或材料; | |
| · | 管理层执行计划和激励人员执行这些计划的能力; | |
| · | 我们吸引和留住关键人才的能力; | |
| · | 与我们的产品或公司本身有关的负面宣传; | |
| · | 与我们的知识产权有关的不利索赔; | |
| · | 采用新的会计准则或改变会计准则; | |
| · | 遵守适用于公共报告公司的法规和条例的固有成本,如2002年的《萨班斯-奥克斯利法案》; | |
| · | 公司未来可能进入的其他新业务; | |
| · | 一般经济和商业状况,以及通货膨胀趋势和金融市场不稳定或银行系统因银行倒闭而中断; | |
| · | 自然灾害或突发公共卫生事件,如新冠肺炎全球大流行,以及地缘政治事件,如俄罗斯入侵乌克兰,以及相关的制裁和其他经济中断或担忧,对我们的财务状况和经营业绩的影响;以及 | |
| · | 在我们的年度报告10-K表格的风险因素部分以及在随后提交给美国证券交易委员会(“美国证券交易委员会”)的文件中阐述的其他因素。 |
这些因素不一定是可能导致实际结果与本年度报告的前瞻性陈述中所表达的大不相同的所有重要因素。其他未知或不可预测的因素也可能对我们未来的结果产生实质性的不利影响,包括但不限于“风险因素”一节中讨论的那些因素。本 年度报告中的前瞻性陈述仅在本年度报告发布之日作出,我们不承担公开更新任何前瞻性 陈述以反映后续事件或情况的义务。我们打算让所有前瞻性陈述遵守《1995年私人证券诉讼改革法》中的安全港条款。
如本年度报告所用,除非另有说明,否则本报告中提及的“Xenetic”、“公司”、“我们”或“我们”均指Xenetic Biosciences,Inc.及其全资子公司。
我们的品牌和产品名称,包括但不限于XCART™,OncoHist™,PolyXen®,ErepoXen™ 和ImuXen™本年度报告中包含Xenetic Biosciences,Inc.和/或其在美国的子公司(美国或美国)的商标、注册商标或服务标志。以及其他一些国家。所有其他公司和产品名称可能是相关公司的商标。
| 三、 |
汇总风险因素
我们的业务面临着许多风险。除下面的摘要外,您还应仔细审阅本年度报告10-K表中的“风险因素”部分。 我们可能会受到其他风险和不确定因素的影响,这些风险和不确定因素目前尚不为我们所知,或我们目前认为这些风险和不确定因素无关紧要。这些风险应与本年度报告中的10-K表格中的其他信息一起阅读。与我们的业务相关的一些主要风险 包括:
| · | 我们从来没有盈利过,也可能永远不会实现或维持盈利。如果我们无法从我们的运营中产生足够的收入来支付费用,或者我们无法以商业合理的条款获得额外的融资,我们的业务、财务状况和运营结果可能会受到重大和不利的影响。 | |
| · | 我们将需要大量的额外资金来实现我们的目标。如果不能在需要时以可接受的条件获得必要的资本,或根本不能获得资金,可能会迫使我们推迟、限制或终止我们的产品开发努力、其他运营或商业化努力。 | |
| · | 筹集额外资本可能会对我们的股东造成稀释,限制我们的运营,或者要求我们放弃对我们的技术或候选药物的权利。 | |
| · | 我们未能满足纳斯达克资本市场的持续上市要求,可能会导致我们的普通股被摘牌。如果不能重新遵守纳斯达克上市规则,可能会影响我们普通股的市场价格和流动性,并降低我们的融资能力。 | |
| · | 我们的业务在很大程度上依赖于DNase肿瘤学平台的成功。 | |
| · | 我们在竞争极其激烈的环境中运营,不能保证竞争技术不会损害我们的业务发展。 | |
| · | 我们是一家开发包括候选药物和技术在内的医药产品的早期公司。鉴于这种发展的不确定性,我们的业务运营可能永远不会完全实现并为投资者创造价值。 | |
| · | 如果我们与我们的合作者或战略伙伴之间出现冲突,这些各方可能会为了他们的自身利益而行事,这可能会限制我们实施战略的能力。 | |
| · | 我们希望依赖第三方来进行、监督和监督我们的临床研究,如果这些第三方的表现不令人满意,可能会损害我们的业务。 | |
| · | 我们的合作者或战略合作伙伴可能决定采用替代技术,或者可能无法利用我们的技术开发商业上可行的产品,这将对我们的收入和我们开发这些产品的战略产生负面影响。 | |
| · | 我们可能会寻求建立更多的合作,如果我们不能在商业上合理的条件下建立合作,我们可能不得不改变我们的开发和商业化计划。 | |
| · | 如果我们达成一项或多项合作,我们可能被要求放弃对我们候选药物开发的重要权利和控制权,或者以其他方式受到不利条款的约束。 |
| 四. |
| · | 我们可能会发现很难将患者纳入我们的临床研究,这可能会推迟或阻止我们的药物产品的临床研究。 | |
| · | 我们可能会在临床试验的开始、登记或完成方面遇到重大延误,或者我们可能无法证明令相关监管机构满意的安全性和有效性,这可能会阻止我们及时将当前和未来的候选药物商业化(如果有的话)。 | |
| · | 如果我们完成了必要的临床前和临床研究,我们无法预测何时或是否会获得监管部门的批准,将候选药物商业化,或者批准的适应症可能比我们预期的更窄。 | |
| · | 如果我们获得了候选药物的监管批准,我们的候选药物将继续受到监管审查。 | |
| · | 任何当前或未来药品的商业成功将取决于医生、患者、第三方付款人和医学界其他人对市场的接受程度。 | |
| · | 开发中的候选药物的商业潜力很难预测。如果一种新的候选药物或技术的市场规模比我们预期的要小得多,它可能会对我们的收入、运营结果和财务状况产生重大的负面影响。 | |
| · | 如果我们的候选药物未能获得或保持足够的保险和报销,如果获得批准,可能会限制我们营销这些产品的能力,并降低我们创造收入的能力。 | |
| · | 我们可能会使用我们的财力和人力资源来追求特定的研究计划或候选药物,而不是利用可能更有利可图或成功可能性更大的计划或候选药物。 | |
| · | 我们可能不会成功地识别或发现更多的医药产品。 | |
| · | 我们候选药物的市场机会可能仅限于那些不符合或未能通过先前治疗的患者,而且可能很小。 | |
| · | 我们没有制造、销售、营销或分销能力,我们可能不得不投入大量资源来开发这些能力。 | |
| · | 我们对第三方的依赖要求我们分享我们的商业秘密,这增加了竞争对手发现这些秘密或我们的商业秘密被挪用或披露的可能性。 | |
| · | 如果我们不能充分保护或执行我们的知识产权,我们可能无法有效地运作。 | |
| · | 如果在法庭上受到质疑,针对我们候选药物的已颁发专利可能被认定为无效或不可执行。 | |
| · | 我们可能无法在世界各地保护我们的知识产权。 | |
| · | 如果我们侵犯了他人的知识产权,我们的业务和盈利能力可能会受到不利影响。 |
| v |
| · | 如果我们未能履行我们向第三方许可知识产权的协议中的义务,或者我们与许可人的业务关系受到干扰,我们可能会失去对我们的业务非常重要的许可权。 | |
| · | 我们可能会受到以下指控的影响:我们的员工、顾问或独立承包商错误地使用或披露了第三方的机密信息,或者我们的员工错误地使用或披露了其前雇主据称的商业秘密。 | |
| · | 我们可能会受到质疑我们的专利和其他知识产权的发明权或所有权的索赔。 | |
| · | 我们无法保护我们的机密信息和商业秘密,这将损害我们的业务和竞争地位。 | |
| · | 我们未来的成功取决于我们能否留住高管团队的主要成员、顾问和顾问,以及吸引、留住和激励合格人员的能力。 | |
| · | 我们将需要扩大我们的组织,我们可能会在管理这种增长方面遇到困难,这可能会扰乱我们的运营。 | |
| · | 我们是合作协议和其他重要协议的一方,这些协议包含复杂的商业条款,可能导致纠纷、诉讼或赔偿责任,可能对我们的业务、运营结果和财务状况产生不利影响。 | |
| · | 我们证券的市场价格可能波动很大,您可能无法出售我们的证券。 | |
| · | 我们的优先股拥有的权利、优先权和特权不属于我们普通股股东的权利,而且优先于普通股股东的权利,这可能导致我们优先股持有人的利益不同于我们普通股东的利益。 |
| VI |
第一部分
项目1--商务
概述
我们是一家生物制药公司,专注于推进创新的免疫肿瘤学技术,解决难以治疗的癌症。我们专有的DNase平台旨在通过针对Net来改善包括免疫疗法在内的现有治疗的结果,Net与癌症进展和对癌症治疗的耐药性有关 。我们于2022年4月获得了DNase肿瘤学平台的许可,并将我们的努力和资源用于这项新收购技术的开发 。
DNase平台是为靶向Net而设计的,Net是由包被组蛋白和其他蛋白质的细胞外染色质组成的网状结构。Net被激活的中性粒细胞排出,以应对微生物或促炎挑战。然而,过量生产或减少Net的清除可导致炎症和自身免疫病理的加重,以及在癌症生长和转移的情况下形成促肿瘤的利基环境。
我们计划在局部晚期或转移性实体肿瘤受试者中进行首例人类、多中心、剂量递增和IV型重组人脱氧核糖核酸酶I的剂量扩展研究。我们的全身性DNA酶计划最初的目标是数十亿美元的适应症,包括胰腺癌。胰腺癌早期诊断率低,死亡率高,五年生存预后差。症状通常是非特异性的,因此,胰腺癌通常直到晚期才被诊断出来。一旦疾病转移或扩散到其他器官,它就变得特别难以治疗。全球每年约有185,000人被诊断出患有这种疾病;2021年,美国国家癌症研究所的监测、流行病学和最终结果计划(SEER)估计,美国将有大约60,000人被诊断为胰腺癌。胰腺癌患者的总五年生存率为7-8%,是实体瘤恶性肿瘤中死亡率最高的;而在被诊断为转移性疾病的患者中,总的五年生存率仅为3%。最近的进展提高了许多癌症类型的存活率,但对胰腺癌患者并不有效,这突显了开发新的治疗方案的必要性。
此外,已经被诊断出患有转移性疾病的二线患者几乎没有治疗选择。唯一被批准用于二线患者的方案是奥尼维德®联合5FU和LV。对于这些接受二线治疗的IV期患者,中位总生存期仅为4.7个月(Macarulla 等人,胰腺2020)。
大量科学文献表明,NETs与癌症发病机制和癌症治疗(包括化疗、放射治疗和免疫治疗,如Checkpoint抑制剂和细胞治疗)的耐药性有关。在已发表的报告中,Net水平升高一直是与多种癌症患者预后不良相关的生物标志物。此外,对现有治疗药物的抵抗可能涉及Net释放免疫抑制信号因子,或Net产生的物理屏障,这可能会阻碍细胞毒性T细胞在肿瘤微环境中的渗透、活性和存活。已发表的临床前模型已经证明了系统地单独或与其他药物联合使用DNase在消除Net和防止肿瘤生长和转移方面的有效性。我们目前正专注于将我们的全身性DNA ase计划推进到临床,作为胰腺癌和局部晚期或转移性实体瘤的辅助治疗。
过继转移CAR T细胞已成为癌症免疫治疗中最有前途的进展之一。要成功治疗实体肿瘤,CAR T细胞必须能够在本身擅长免疫抑制并有利于肿瘤细胞存活的敌对肿瘤微环境中渗透、持续并保持抗肿瘤功能。最近设计CAR T的方法包括“装甲”CAR-T细胞,之所以被命名,是因为它们可以表达额外的因子来抵抗免疫抑制 或降解肿瘤细胞外基质的物理成分,包括网络。我们打算进行临床前研究,目的是证明装甲CAR T细胞以分泌DNA酶可以支持对实体瘤适应症的深度和持久性反应。设计用于识别癌症相关抗原的工程化CAR T细胞能够持续和选择性地杀死肿瘤细胞,并大幅降低肿瘤负担。CAR-T疗法在治疗血液系统恶性肿瘤方面取得了显着的临床成功,但迄今为止在实体瘤方面尚未取得成功。已发表的证据表明,除了免疫抑制因素外,Net形成的机械屏障还可以阻止T细胞穿透并阻断T细胞与肿瘤细胞的接触。
| 1 |
我们与比利时Wilition SARL有限公司(“Wilition”) 的合作是一项早期探索性计划,旨在评估Wilition的Nu.Q®技术与Xenetic的DNase-Armored CAR T平台的潜在组合,以开发可能针对多种实体癌症的专利采用细胞疗法,目前的CAR T细胞疗法对这些肿瘤显示出有限的效果或没有效果。根据合作协议的条款,Wilition将为一个研究项目提供资金,双方将分享合作产生的任何产品的商业化或许可收益。表观遗传学修饰的核小体存在于多种类型实体癌的肿瘤细胞表面和肿瘤微环境中,因此这些核小体可能代表着不限于单一癌症类型的可泛化的肿瘤抗原。Wilition的Nu.Q® 技术可以特异性识别和靶向表观遗传修饰的核小体,而我们的DNase-Armored CAR T平台旨在 增强实体肿瘤微环境中CAR T细胞的功能。
XCART是我们的个性化CAR T平台技术,旨在靶向患者特定的肿瘤新抗原,并已证明其在B细胞淋巴瘤中的作用机制。 XCART技术平台旨在利用成熟的筛选技术来识别选择性地与单个淋巴瘤患者恶性B细胞克隆表面的唯一B细胞受体(BCR)结合的多肽域。 这种BCR选择性靶向域被改造到CAR的抗原结合域中,从而创造了仅识别给定患者的恶性B细胞克隆的CAR T治疗 的可能性。我们相信,我们的个性化CAR T疗法有潜力为癌症患者提供比现有护理标准和目前批准的CAR T疗法更大的好处。我们已暂停 XCART平台的开发,因为我们优先考虑DNase平台,并打算将我们的资源集中在DNase程序的开发上。
此外,我们还与生物技术 和制药公司合作,开发我们的专有药物输送平台PolyXen,并根据血液凝血障碍领域的独家许可证安排收取特许权使用费。PolyXen是蛋白质和多肽药物输送的使能平台技术 。它使用生物聚合物聚唾液酸(“PSA”)来延长药物的半衰期,并潜在地提高治疗性多肽和蛋白质的稳定性。PSA链的附着位置和长度都可以通过改变分子的表观流体动力学半径来影响治疗性 ,这反过来又可以增强治疗性的许多生物学特性。它也可以用于小分子药物。
我们将我们的专利和专有技术 整合到目前正在与生物技术和制药行业合作开发的候选药物中,以创造我们相信 将比现有疗法更具药理学特性的下一代生物药物。我们的候选药物已由我们的研究活动或我们的合作者的研究活动产生,并处于开发阶段。因此,我们将继续投入大量资源用于我们的研发活动,并预计在不久的将来继续这样做。 到目前为止,我们的候选药物尚未在美国或任何其他国家或地区获得任何适用机构的监管营销授权或批准。
尽管我们拥有广泛的专利组合,但我们在2022年的内部努力的重点是我们DNase平台的许可和进步以及我们的XCART平台技术的开发 。
我们于2011年8月根据内华达州法律注册成立。我们直接或间接通过我们的全资子公司Hesperix S.A.(“Hesperix”)和 Xenetic Biosciences(英国)Xenetic UK(“Xenetic UK”)及其全资子公司Xenetic UK、Lipoxen Technologies Limited(“Lipoxen”)、Xenetic Bioscience,InCorporation and SymBioTec,GmbH(“SymBioTec”)拥有各种美国联邦商标注册和申请,以及未注册的商标和服务标记,包括但不限于XCART、OncoHist、 Polyxen、ErepoXen和Imuxen。
我们的战略
2022年4月,我们批准了DNase平台。 DNase平台旨在通过针对Net(有关技术的说明,请参阅“概述” 和“我们的技术和候选药物”)来改善现有治疗的结果,包括免疫疗法。我们现在的主要努力是将系统性DNA ase计划推向临床,作为胰腺癌和其他局部晚期或转移性实体肿瘤的辅助治疗 。我们的目标是通过改善反应和克服对检查点抑制剂、化疗和其他标准护理治疗的耐药性,为实体肿瘤的治疗提供解决方案。我们还打算寻求行业合作和潜在的许可 以开发用于其他用途和适应症的DNA ase。
| 2 |
我们打算在美国和欧洲酌情寻求孤儿药物指定和相关肿瘤学适应症的加速审批途径。如果我们的孤儿肿瘤药物 候选药物被授予孤儿药物称号,那么我们可能会受益于孤儿地位的某些关键优势,包括某些市场 排他性。
我们打算主要通过使用合同制造和合同研究组织(“CRO”)来推进我们的DNase 平台的开发,以便有效地 管理我们的资源。获得许可的候选药物的持续流水线增长和进展在一定程度上取决于我们 筹集足够资本、推进我们现有的共同开发合作和战略安排以及达成新的此类安排的能力。
业务发展
排他性再许可协议
于2022年4月26日,吾等与CLS订立独家 再许可协议(“再许可协议”),据此,吾等获得由CLS拥有或控制的若干 专利权及专有技术下的独家许可,以开发及商业化含有 脱氧核糖核酸酶用于治疗癌症的药物产品及方法(“再许可产品”)。根据再许可协议的条款,除其他事项外,我们 将独自负责并将尽商业上合理的努力,研究、开发和获得美国和某些欧洲市场的再授权产品的营销批准,并在获得营销批准后在相关市场将此类再授权产品 商业化。
作为根据分许可协议授予我们的许可和其他权利的代价,我们向CLS发行了375,000股我们的普通股(“分许可协议股份”),其中250,000股分许可协议股份直接发行给OPKO Health,Inc.(“OPKO”),而不是从CLS间接转让给OPKO的全资子公司EirGen Pharma Ltd.(“EirGen”),以履行CLS和EirGen之间的某些第三方合同 义务。此外,我们有义务向CLS支付高达13,000,000美元的现金作为潜在里程碑付款 ,以实现某些临床和监管里程碑,并根据某些监管里程碑的实现向CLS额外发行950,000股普通股。此外,我们有义务对许可期限内许可产品的净销售额(如再许可协议中定义的)支付从中位数到低两位数不等的分级版税,并支付我们从任何分被许可人 收到的一定对价的中低档百分比份额。
独家许可协议
2022年4月26日,我们与CLS签订了独家 许可协议(“许可协议”),根据该协议,我们获得了CLS拥有或控制的某些专利 权利和专有技术下的独家许可,以开发和商业化将DNase与CAR T疗法 结合在一起的药品和方法(“许可产品”)。根据许可协议的条款,我们将独家负责,并将尽商业上合理的努力,除其他事项外,研究、开发和获得许可产品在美国和某些欧洲市场的销售许可,并在获得销售许可后在相关市场将此类许可产品商业化。
考虑到许可协议授予我们的许可和其他权利,我们向CLS一次性支付了500,000美元的现金费用,向CLS发行了500,000股我们的普通股 ,并有义务支付高达13,000,000美元的现金作为潜在的里程碑付款,以实现每个许可产品的某些临床和监管里程碑。此外,我们有义务在版税期限内(如 许可协议所定义)对许可范围内的许可产品的净销售额支付从中位数到 低两位数不等的分级版税,并向我们从任何 分被许可人那里获得的一定对价的低两位数支付一定比例的份额。
| 3 |
专利转让与意志协作
2022年10月4日,我们完成了与Wilition和CLS合作的专利转让 。关于专利转让,吾等于2022年10月12日与特拉华州有限责任公司CLS Treeutics,LLC签订认购协议,据此,吾等同意向CLS LLC发行普通股,而CLS LLC同意认购850,000股普通股,作为CLS 及其关联方向我们转让CLS及其关联方拥有的某些专利权的代价。
2022年8月2日,我们宣布与Wilition进行研发合作,为癌症的治疗开发Nets靶向采用细胞疗法。该合作是一项早期探索性计划,旨在评估Wilition的Nu.Q® 技术测试与我们的DNase-Armored CAR T平台的潜在组合,以开发可能针对多种实体癌症的专利采用细胞疗法 。根据合作协议的条款,意志力将为一个研究项目提供资金,双方将分享合作产生的任何产品的商业化或许可收益。
Catalent
2022年6月30日,我们与Catalent Pharma Solutions LLC(“Catalent”)签订了一份工作说明书(以下简称“SOW”),概述了总体工作范围、时间表和定价,据此Catalent将向我们提供某些服务,以生产我们的重组蛋白质--人类脱氧核糖核酸酶I。
斯克里普斯研究公司
2023年3月17日,我们 与斯克里普斯研究公司签订了一项研究资助和期权协议(“协议”),根据该协议,我们已同意向斯克里普斯研究公司提供总额高达938,000美元的资金,用于资助与推进 公司的DNase肿瘤平台技术的临床前开发相关的研究。研究经费由我们根据商定的预算按月支付给斯克里普斯研究公司,该预算规定在协议签署之日支付约78,000美元的首付款,并在12个月内按月支付约78,000美元。根据《协议》,我们有权获得斯克里普斯研究公司在技术或专利权(如《协议》所定义)中的权利的全球独家许可,以及非独家、免版税、 不可转让的许可,以便在《协议》所规定的研究计划实施期间,仅为我们的内部研究目的制作和使用《TSRI技术》(如《协议》所定义)。
除非提前终止,否则本协议的有效期自本协议之日起持续十五(15)个月。本协议可由我们提前 提前30天书面通知Scripps Research,从生效日期(协议中的定义)后六(6)个月开始,或如果我们未能及时支付协议规定的到期款项,则由Scripps Research终止,但须提前30天书面通知以纠正此类 不付款的情况。如果另一方未能履行协议项下的任何义务或另一方破产,则任何一方均可进一步终止协议。
我们的技术和药物候选人
技术
我们将我们的专利和专有技术 整合到许多候选药物中,这些药物目前正在我们内部或与我们的生物技术和制药合作伙伴进行开发。 我们的目标是创造我们认为将是下一代生物药物和疗法的药物。虽然我们主要专注于研究和开发肿瘤药物,但我们也拥有合作伙伴正在开发的治疗其他疾病的药物的所有权和其他经济利益 。
在截至2022年12月31日的一年中,我们内部开发工作的重点是DNase肿瘤学平台的许可和发展,以及我们的XCART 技术的开发。我们没有积极致力于PolyXen或我们的任何其他技术的开发。
| 4 |
| DNA酶 |
DNase平台是针对Net而设计的,Net是由包被组蛋白和其他蛋白质的细胞外染色质组成的网状结构。Net被激活的中性粒细胞排出,以应对微生物或促炎挑战。然而,过量产生或减少Net的清除会导致炎症和自身免疫病理的加重,以及在癌症生长和转移的情况下产生促肿瘤的利基环境。
计划要点: | |
| · | 与CLS达成独家许可和再许可协议,以开发其介入性DNA酶平台,旨在改善包括免疫疗法在内的现有治疗的结果 ; | |
| · | 朝着人类研究的第一步迈进,目标是2024-2025年; | |
| · | 系统性DNA酶计划,最初目标是数十亿美元的适应症,包括胰腺癌和其他局部晚期或转移性实体肿瘤;以及 | |
| · | DNase-装甲车T计划处于临床前的早期开发阶段。 | |
| XCART | XCART技术平台是由其发起人设计的,旨在利用一种成熟的筛选技术来识别与单个患者恶性肿瘤细胞表面独特的BCR特异结合的多肽配体。然后将多肽插入CAR T细胞的抗原结合区域,随后的转导/转染过程被用于将患者的T细胞改造成CAR T形式,该形式重新引导患者的T细胞攻击肿瘤。从本质上讲,XCART筛选平台与典型的CAR T筛选方案相反,在CAR T筛选方案中,针对给定的靶点筛选高特异性抗体结构域的文库。在XCART筛选的情况下,目标本身是一个抗体结构域,因此其性质具有高度的特异性。XCART技术创造了个性化治疗淋巴瘤的可能性,利用具有抗原结合结构域的CAR,该结构域应该只识别并仅被特定患者的B细胞淋巴瘤的独特BCR识别。XCART的预期结果是有限的肿瘤外毒性,如B细胞再生障碍性贫血。我们目前暂停了XCART的进一步开发,因为我们将努力和资源集中在我们的DNase技术平台上。 |
| PolyXen | 一种能够实现的生物平台技术,旨在通过一种称为聚唾液酸化的过程将PSA化学地附着到药物分子上,从而延长药物分子在人体内的循环时间,从而创造出潜在的优秀的下一代候选治疗药物。PSA是一种生物聚合物,由唾液酸分子链组成,是人体的天然成分,尽管我们的PSA来自细菌来源。 |
研究、外部服务和协作
通过合作伙伴的努力,我们正在基于我们的DNase、XCART和PolyXen专利技术开发我们的下一代生物疗法和新型肿瘤学药物 流水线。 为了在有效管理我们的管理费用的同时做到这一点,我们依赖于合同制造商、CRO的服务和我们的战略合作 。我们目前没有内部研究设施来推行这些举措。因此,我们的技术和候选药物的持续流水线增长和进步取决于几个重要的合作和战略安排,包括我们与以下方面的安排:
| · |
Catalent,使生物制药、细胞、基因和消费者健康合作伙伴能够通过多种方式优化开发、推出和供应更好的患者治疗方法的全球领先企业;
| |
| · | Pharmsynz,包括其全资子公司SynBio LLC(“SynBio”),该公司是我们约2.9%普通股的实益所有者;以及 | |
| · | 斯克里普斯研究所(“斯克里普斯研究所”),世界上最大的私人非营利性研究机构之一。 |
因此,除了继续开发DNA酶技术,我们还对我们的合作者正在开发的用于治疗其他疾病的候选药物感兴趣。 我们可能会根据这些合作收取一些里程碑式的付款和版税组合,前提是这些药物 成功开发和营销。但是,除了与武田子许可下的版税付款,以及我们与Pharmsynz的合作协议下的潜在版税付款 外,我们预计短期内不会有任何里程碑或版税付款。 有关更多详细信息,请阅读下面标题为“重要合作和战略安排”的部分。
| 5 |
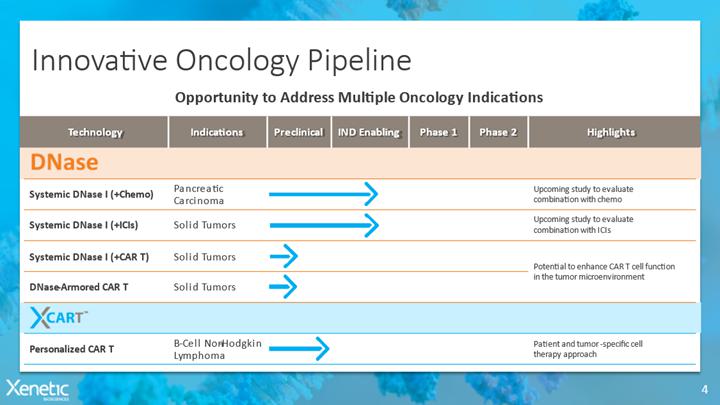
我们的候选药物管道
我们的产品线包含内部以及与我们的生物技术和制药合作伙伴正在开发的候选药物 。下表汇总了有关我们当前候选药物的关键信息 :

ErepoXen
ErepoXen,或多唾液酸促红细胞生成素(“PSA-EPO”), 使用我们的PolyXen平台技术治疗慢性肾脏病(“CKD”)患者的贫血。它旨在通过延长治疗药物在体内的循环半衰期来减少给药频率。我们不是在进行ErepoXen的临床开发,而是继续在我们的许可地区为候选药物提供许可外的机会。
我们与Pharmsynz 和血清研究所签署了合作协议,在有限的市场上开发和推出ErepoXen,根据协议,如果他们在这些努力中取得成功,我们将收取版税 。
| 6 |
Pharmsynz获得了监管部门的批准,将于2020年在俄罗斯开始ErepoXen(也称为Epolong)的第二(B)/第三阶段人体临床试验,并完成患者招募。2020年12月,Pharmsynz报告了这项临床试验的阳性数据,并于2021年2月在一份新闻稿中报告称,它已通过提交注册档案以获得俄罗斯的批准, 开始了Epolong的注册阶段。Pharmsynz在其新闻稿中报告说,预计俄罗斯阶段的注册活动将于2021年完成,最早将能够在2022年第一季度开始生产该产品。Pharmsynz已通知我们,它已收到一封回复信,其中指出了档案中的某些缺陷,并打算在更正后重新提交注册。
血清研究所在95名受试者中进行了ErepoXen的I期和II期临床试验。这些安全性试验没有重大的药物相关不良事件, 为我们提供了开始第二阶段重复给药的数据, 人用药物技术要求协调国际会议在澳大利亚、新西兰和南非针对未接受透析的CKD患者进行了ErepoXen的合规临床试验。我们完成了这项研究的三个队列,然后终止了研究。
此外,血清研究所在印度完成了ErepoXen针对中心透析患者的I/II期临床试验。血清研究所可能寻求利用Pharmsynz的试验数据和潜在的俄罗斯营销授权,请求豁免在印度进行的第三阶段临床试验,但须得到当地监管机构的批准。
管道扩展机会
在我们的许可下,我们的合作者可以在其本土市场 内运营,从而潜在地在广泛的治疗领域中生成与我们的技术相关的临床前和临床数据。根据这些协议,我们保留主要市场的所有权利,并共同拥有临床数据。因此,我们有机会在主要市场的开发和商业化决策过程中利用这些数据。
重要的合作和战略安排
武田
2017年10月,我们授予武田 向武田授予与本公司的PolyXen技术相关的某些专利的非排他性再许可的权利,这些专利之前是向武田独家许可的与治疗血液和出血疾病相关的产品。根据协议,武田 (I)于2017年11月向我们一次性支付了750万美元(7,500,000美元),(Ii)同意根据所涵盖产品在整个期限内的净销售额向我们支付个位数的版税。净销售额的特许权使用费支付从2019年末开始 。在截至2022年和2021年12月31日的年度内,公司分别将约170万美元和120万美元的特许权使用费记为收入,并基于某些承保产品净销售额的个位数特许权使用费。
Catalent
2022年6月30日,我们与Catalent 签订了一份SOW,概述了一般工作范围、时间表和定价,根据该协议,Catalent将向我们提供某些服务,以执行我们的重组蛋白质人类DNA I的cGMP制造。双方同意签订主服务协议(MSA) ,其中将包含管理SOW预期项目的条款和条件,并将取代包含Catalent标准条款和条件的SOW附录。此外,如果SOW和MSA中规定的特定于项目的条款和条件之间存在任何冲突,应以MSA条款和条件为准。在项目期限内, SOW计划的制造服务项目的估计总成本预计高达约500万美元(不包括某些费用和潜在的替代方案),项目的每个阶段都将与该 阶段的开始相关地单独开具发票。除非之前进行修订或终止,否则SOW计划的制造服务目前的目标是在2024年上半年完成。公司可在提前30天书面通知Catalent的情况下随时终止SOW。SOW还包含与机密性、保修、知识产权和赔偿等相关的惯例条款。
| 7 |
斯克里普斯研究公司
2020年5月15日,我们与斯克里普斯研究公司签订了一项研究资助和期权协议(“斯克里普斯协议”),根据该协议,我们同意向斯克里普斯研究公司提供总计300万美元的资金,用于资助与推进XCART临床前开发相关的研究。研究经费 由我们根据商定的预算按季度支付给斯克里普斯研究公司,该预算规定在斯克里普斯协议签订之日支付约300,000美元的首付款,随后在27个月内按季度支付约300,000美元 。根据斯克里普斯协议,斯克里普斯研究公司根据与斯克里普斯研究公司于2019年2月25日签订的、于2019年3月1日分配给我们的特定许可协议的条款,向我们授予了该领域内的任何 专利权或技术(如斯克里普斯协议所定义)的许可。此外,我们还可以选择获得 斯克里普斯研究公司在尚未授权给我们的技术或专利权中的全球独家许可,以及非独家、免版税、 不可转让的许可,以便在斯克里普斯协议预期的研究计划的执行期间,仅出于公司内部研究目的制造和使用斯克里普斯研究技术(如斯克里普斯协议中的定义)。在2022年第二季度,双方共同同意终止斯克里普斯协议项下的额外资金。因此,斯克里普斯研究公司同意根据协议继续开展工作,直到之前预付的资金用完为止。
PJSC药物合成
2009年11月,我们与Pharmsynz签订了合作研发许可协议(“Pharmsynz安排”),据此,我们向Pharmsynz授予了独家许可,允许其在某些地区开发、商业化和营销六种基于我们的PolyXen和ImuXen技术的候选产品 。作为交换,Pharmsynz授予我们独家许可,允许我们在Pharmsynz安排的范围内使用由Pharmsynz开发的任何临床前和临床数据,并自费在某些地区以外从事 候选药物的进一步研究、开发和商业化。
Pharmsynz完全负责为俄罗斯的研究和临床开发活动提供资金并进行自己的研究和临床开发。除特许权使用费外,Pharmynz协议没有规定任何里程碑或其他研究相关付款 。根据其中规定的条款和条件,Pharmynz安排应继续执行,直至终止为止。
2011年8月,我们与Pharmsynz的全资子公司SynBio签订了股票认购 和合作开发协议(“共同开发协议”) ,据此,我们授予SynBio独家许可,允许其利用基于SynBio的技术以及我们在俄罗斯和独联体的PolyXen、OncoHist和ImuXen平台技术的分子 开发、营销和商业化某些候选药物,在此统称为SynBio市场。作为我们授予SynBio该等许可权的交换,SynBio向我们授予了独家许可 ,允许我们使用SynBio产生的任何临床前和临床数据,并根据共同开发协议在SynBio市场以外的任何地区从事合作可能产生的商业候选产品的开发。
Synbio完全负责资助和开展其在俄罗斯的研究和临床开发活动。根据共同开发协议,除双方根据各自的技术提供各自的研究用品的费用外,没有为 规定的里程碑或其他与研究相关的付款。 提供这些费用是由于双方的便利,并不代表提供研究用品的持续或经常性义务。 在任何最终产品成功商业化后,我们有权在某些地区的销售中获得10%的特许权使用费 ,并向SynBio支付受共同开发协议条款限制的某些地区以外的销售的特许权使用费。在截至2022年12月31日和2021年12月31日的 年度,不存在与共同开发协议相关的供应服务收入 。共同开发协议继续有效,直到根据协议中规定的条款和条件终止为止。 SynBio于2021年12月20日将共同开发协议转让给其母公司Pharmynz。
见附注4重要的战略协作 为Pharmsynz在美国的股份所有权。
| 8 |
血清研究所
2011年8月,我们与血清研究所签订了合作研发协议(“血清协议”),向血清研究所提供了使用我们的PolyXen技术研发一种潜在的商业产品--聚唾液分析促红细胞生成素(“PSA-EPO”)的独家许可 。 血清研究所负责进行在某些预定区域内获得监管批准所需的所有临床前和临床试验,费用由血清研究所自费。塞缪尔研究所向我们支付版税,用于向塞缪尔研究所销售区域内的某些客户进行净销售额。对于我们在许可证期限内收到的净销售额,我们向血清研究所支付特许权使用费。根据合作安排,没有里程碑或其他与研究相关的付款到期。 血清协议继续有效,直到根据协议中规定的条款和条件终止为止。截至2022年12月31日,我们未开发任何商业产品,也未确认任何与此安排相关的版税收入或费用。截至2022年12月31日,Serve 研究所持有的股份不到我们已发行普通股总数的1%。
我们的知识产权
我们努力保护和加强对我们的业务具有重要商业意义的专有技术、发明和改进,包括寻求、维护和捍卫 专利权,无论是内部开发的还是从我们的合作者或其他第三方获得许可的。我们的政策是寻求保护我们的专有地位,其中包括在美国和美国以外的司法管辖区提交专利申请,涵盖我们的专有技术、发明、改进和候选产品,这些对我们业务的发展和实施非常重要。我们还依靠与我们的专有技术和产品候选相关的商业秘密和技术诀窍、持续创新和许可内机会来发展、加强和保持我们在肿瘤学领域的专有地位。我们还计划 依赖数据独占性、市场独占性和专利期延长(如果可用)。我们的商业成功将在一定程度上取决于我们是否有能力为我们的技术、发明和改进获得并维护专利和其他专有保护;保护我们商业秘密的机密性;获得并维护使用第三方拥有的知识产权的许可证;捍卫和执行我们的专有权利,包括我们未来可能拥有的任何专利;以及在不侵犯有效和可强制执行的专利和第三方其他专有权利的情况下运营。
我们的候选药物处于不同的开发阶段, 每种药物都受到美国专利商标局(“USPTO”)的专利保护和美国专利商标局(“USPTO”)的未决专利申请的保护, 在某些其他发达国家。我们的第一批专利于2021年开始到期,我们的PolyXen和OncoHist技术的大部分现有专利将在2025年至2030年之间到期。
我们的专利战略是在构成全球主要药品市场或可能生产药品的地点的司法管辖区内提交有关创新和改进的专利申请。就我们的主要专利组合而言,这些司法管辖区通常包括但不限于美国、英国、澳大利亚、日本、加拿大、韩国、中国、印度、俄罗斯和欧盟(“欧盟”)的某些其他国家/地区, 尽管我们不一定会在每个司法管辖区为每个专利家族提交专利申请。
截至2023年1月23日,我们通过我们的全资子公司Hesperix和Xenetic UK,以及Xenetic UK的全资子公司Lipoxen、XTI和SymBioTec,直接或间接地(例如,通过CLS的许可)拥有170多项美国和国际专利和正在进行的专利申请,涵盖了我们技术的各个方面。这一数字包括我们收购或申请的专利和专利申请,涉及我们的DNase和XCART平台技术的各个方面,包括我们在世界各地的所有权利和专利申请,与“针对癌症个性化治疗的文章和方法”相关的专利和专利申请,以及我们的PolyXen平台技术分别涵盖聚唾液酸化 和先进的聚合物共轭技术,以及我们的其他候选产品。更具体地说,我们的专利和专利申请涵盖癌症治疗、使用方法、聚合物结构、药物结合物、配方、聚合物和聚合物结合物的制造方法以及聚合物结合物的管理方法。
| 9 |
我们已经获得了某些疗法的专利保护,这些疗法使用我们的PolyXen技术将特定疗法与PSA联系起来。这些包括但不限于PSA-EPO、PSA-胰岛素和PSA-胰岛素样蛋白、下一代因子VIII候选蛋白SHP656(PSA-rFVIII)、PSA-DNase I和PSA-粒细胞集落刺激因子(PSA-GCSF)。更多的专利涉及制备与PSA相连的蛋白质的方法。这些方法专利包括那些在高pH溶液中将PSA与蛋白质连接的专利,以及使用通过打开和氧化唾液酸单元来生产唾液酸醛衍生物的工艺的专利。例如,我们有专利保护 可以在N端的PSA链接。
我们在PSA的生产和纯化过程中去除内毒素方面获得了专利保护。通过向PSA添加高pH 溶液和将多分散的离子电荷多糖(如PSA)分离成不同 平均分子量的级分的过程来去除内毒素。这是通过使用具有不同和恒定的离子强度和pH的柱和洗脱缓冲液来实现的,从而得到相对分子质量多分散度为1.1或更低的分级多糖。
我们的DNase技术也获得了专利保护,该技术包括使用DNase治疗癌症和改善癌症治疗相关的副作用 。DNA酶可以单独使用,也可以与癌症治疗药物联合使用。该产品组合和XCART产品组合 还涵盖了某些类型的CAR-T细胞的使用,无论是否添加DNA酶来治疗癌症。产品组合 进一步涵盖使用带有或不带有DNA酶的CAR-T细胞,这些细胞与免疫检查点抑制剂或调节剂一起使用来治疗癌症。
已颁发的专利可以提供不同的 期限保护,具体取决于专利申请的提交日期、专利颁发日期和专利在获得专利的国家/地区的法定期限。通常,为在美国提交的申请颁发的专利可以提供自最早生效日期起20年的排他性权利 。此外,在某些情况下,涵盖 或声称FDA批准的产品的已发布美国专利的期限可以延长,以重新获得因FDA监管 审查期而实际上丢失的部分期限,这称为专利期限延长。恢复期不得超过五年,包括恢复期在内的总专利期不得超过FDA批准后的14年。美国境外专利的期限根据外国司法管辖区的法律而有所不同,但通常也是自最早的有效申请日期起20年。但是, 专利提供的实际保护因产品而异,并取决于许多因素,包括专利的类型、覆盖范围、与监管相关的延期的可用性、特定国家 的合法补救措施的可用性以及专利的有效性和可执行性。
在某些情况下,如果我们使用受一项或多项专利保护的药物 ,我们开发和商业化技术的能力可能会受到我们获取这些专利药物的限制 。即使我们相信我们可以自由使用专利药物,我们也不能保证我们不会被指控或被确定侵犯第三方的权利,不会被禁止使用该药物或被发现对 损害赔偿负责。任何此类对访问权限或损害赔偿责任的限制都将对我们的业务、运营结果和财务状况产生实质性的不利影响。
像我们这样的制药和生物技术公司的专利地位是不确定的,涉及复杂的法律和事实问题。不能保证已颁发的专利将在法庭上保持有效和可强制执行。即使对于保持有效和可强制执行的专利,与获得此类判决相关的法律程序也是耗时和昂贵的。此外,已颁发的专利可能会受到反对或其他 诉讼程序的影响,这可能会导致专利被撤销或以修改后的形式(并可能以使专利没有商业相关性和/或广泛覆盖的形式)得到维护。此外,我们的竞争对手可能能够绕过或以其他方式绕过我们的专利设计。即使颁发并可强制执行专利,因为药品的开发和商业化可能会受到很大的延迟,专利可能会提前到期,并且在我们的专利所涵盖的产品商业化 之后,专利可能只提供短期的保护(如果有的话)。我们可能不得不参与美国专利商标局宣布的干预程序,这可能导致专利损失和/或我们的巨额成本。此外,我们理解,如果我们的任何未决专利申请没有发布, 或在发布后被视为无效,我们可能会失去宝贵的知识产权保护。
| 10 |
存在由第三方拥有的美国和外国专利权以及其他专有权利,涉及药物组合物和试剂、医疗器械和设备以及药物组合物的制备、包装和交付方法。我们无法确定这些权利中的哪些(如果有)将被存在这些权利的各个司法管辖区的当局视为与我们的技术相关,也不能确定地预测这些权利中的哪些(如果有)将被第三方主张或可能被第三方主张。我们可能会在针对任何此类索赔为自己和我们的合作伙伴辩护时产生巨大的 成本。此外,提出此类索赔的各方可能能够获得禁令或其他公平救济,这可能会有效地阻止我们在美国和其他国家/地区开发或销售我们的部分或全部产品,并可能导致获得巨额损害赔偿。如果发生侵权索赔,我们或我们的合作伙伴 可能需要从第三方获得一个或多个许可证。不能保证我们能够以合理的条款获得我们确定需要的任何技术的许可证 ,也不能保证我们可以开发或以其他方式获得替代技术。如果需要, 未能获得许可可能会对我们的业务、运营结果和财务状况产生重大不利影响。 此外,我们可能无法在商业合理的基础上获得与我们候选药物的开发相关的知识产权许可。 如果有的话。
我们的政策是要求我们的员工和 顾问、外部科学合作者、赞助研究人员和其他从我们那里获得机密信息的顾问在与我们开始雇佣或咨询关系时执行保密协议。这些协议规定, 个人在与我们的关系过程中开发或向其披露的所有机密信息均应保密,除非在特定情况下,否则不得向第三方披露。协议规定,由员工构思的所有发明应为我们的财产。然而,不能保证这些协议将在未经授权使用或披露此类信息的情况下为我们的商业秘密提供有意义的保护或足够的补救措施。
制造和供应
我们没有能力生产支持我们的候选药物开发计划所需的我们自己的材料,也不打算将此能力作为我们当前业务战略的一部分。我们目前与Catalent和血清研究所签订了协议,根据该协议,Catalent和血清研究所将生产临床材料,分别用于开发采用我们的DNase和PolyXen技术的候选药物,包括我们合作伙伴开发的候选药物。我们没有达成任何协议来生产用于开发我们的XCART技术的临床材料,如果需要,我们将寻找第三方制造商来满足我们的临床供应需求。
政府监管
一般信息
除其他事项外,美国联邦、州和地方及其他国家的政府当局对我们正在开发的产品的研究、开发、测试、制造、质量控制、审批、标签、包装、储存、记录保存、促销、广告、分销、营销和出口以及 进口等方面进行了广泛的监管。通常,新药必须通过NDA流程获得FDA的批准,新的生物制剂必须通过生物制品许可证申请(BLA)流程获得FDA的许可,然后才能在美国合法销售 。
美国监管机构
药物开发流程
在美国,FDA根据《联邦食品、药物和化妆品法》(FDCA)监管药品,对于生物制品,也根据《公共卫生服务法》(PHSA)及其实施条例进行监管。获得监管批准以及随后遵守适当的联邦、州、地方和外国法规和条例的过程需要花费大量的时间和财力。在产品开发过程、审批过程或审批后的任何时间未能遵守适用的美国要求 申请人可能会受到行政或司法制裁。这些制裁可能包括FDA拒绝批准待决申请、 撤回批准、吊销执照、临床封存、警告信或无标题信、产品召回、产品扣押、 完全或部分暂停生产或分销、禁令、罚款、拒绝政府合同、恢复原状、退还 或民事或刑事处罚。任何机构或司法执法行动都可能对我们产生实质性的不利影响。
| 11 |
FDA在一种药物或生物药物在美国上市前所需的程序 通常包括以下内容:
| · | 根据“良好实验室规范”(“GLP”)规定和其他适用规定完成临床前实验室测试、动物研究和配方研究; | |
| · | 向FDA提交IND,该IND必须在人体临床试验开始之前生效; | |
| · | 根据“良好临床实践”(“GCP”)规定进行充分和受控的人体临床试验,以确定拟用于其预期用途的药物的安全性和有效性; | |
| · | 向FDA提交NDA或BLA; | |
| · | 令人满意地完成FDA对生产药物的一个或多个制造设施的检查,以评估是否符合现行的良好制造规范(“cGMP”)要求,以确保设施、方法和控制足以保持药物的特性、强度、质量和纯度;以及 | |
| · | FDA对NDA或BLA的审查和批准。 |
药物或生物制造商也可能 受到批准后的监管要求。一旦确定要开发的候选药物,它将进入临床前测试阶段 。临床前测试包括对产品化学、毒性和配方的实验室评估,以及动物研究。IND赞助商必须将临床前测试的结果以及生产信息和分析数据作为IND的一部分提交给FDA 。赞助商还将包括一份协议,其中详细说明了临床试验第一阶段的目标、用于监测安全性的参数以及要评估的有效性标准(如果第一阶段适合进行疗效评估)。即使在IND提交之后,一些临床前试验也可能继续进行。IND在FDA收到后30天自动生效 ,除非FDA在30天内暂停临床试验。 在这种情况下,IND赞助商和FDA必须在临床试验开始之前解决任何悬而未决的问题。FDA还可以在临床试验之前或期间的任何时间实施临床搁置,原因是对正在进行的或拟议的临床试验存在安全担忧,或者不符合FDA的特定要求,在FDA通知赞助商已解除搁置之前,试验可能不会开始或继续进行。
所有临床试验必须在符合GCP规定的一名或多名合格研究人员的监督下进行。它们必须在详细说明试验目标、给药程序、受试者选择和排除标准以及安全和有效性标准的协议下进行,以进行评估。每个方案必须作为IND的一部分提交给FDA,如果发生任何严重和意想不到的不良事件,必须及时向FDA提交安全报告。参与临床试验的每个机构的机构评审委员会(IRB)(在某些情况下是独立的IRB)必须在该机构的临床试验开始之前审查和批准每个方案。作为审查的一部分,IRB还必须批准关于试验的信息和必须提供给每个试验受试者或其法律代表的同意书,监督研究直到完成,否则必须遵守IRB的规定。
人体临床试验通常分三个连续阶段进行 ,这些阶段可能重叠或合并:
| · | 第一阶段:该候选药物最初被引入健康人体,并进行安全性、剂量耐受性、吸收、代谢、分布和排泄测试。在一些治疗严重或危及生命的疾病(如癌症)的产品中,特别是当产品可能因其固有毒性而无法合乎道德地给健康志愿者服用时,最初的人体试验通常在患者身上进行。 | |
| · | 第二阶段:这一阶段涉及在有限的患者群体中进行临床试验,以确定可能的不良反应和安全风险,初步评估该产品对特定目标疾病的疗效,并确定剂量耐受性和适当剂量。 | |
| · | 第三阶段:临床试验是为了在地理分散的临床研究地点扩大患者群体中进一步评估剂量、临床疗效和安全性。这些临床试验旨在确定候选药物的总体风险-收益比,并在适当的情况下为产品标签提供充分的基础。 |
| 12 |
批准后试验,有时称为 第四阶段研究,可能会在最初的市场批准之后进行。这些试验用于从预期治疗适应症患者的治疗中获得更多经验。在某些情况下,FDA可以强制执行第四阶段临床试验,作为批准NDA或BLA的条件。
FDA或赞助商可以随时以各种理由暂停临床试验,包括发现研究对象面临不可接受的健康风险。 类似地,如果临床试验没有按照IRB的要求进行,或者如果药物与患者的意外严重伤害有关,IRB可以暂停或终止其机构对临床试验的批准。此外, 一些临床试验由赞助商组织的一个独立的合格专家小组监督,该小组称为数据安全监测 委员会。根据其章程,该小组可根据对试验的某些数据的访问,确定试验是否可以在指定的检查点进行。
在临床试验的同时,赞助商还必须 开发有关药物化学和物理特性的更多信息,并根据cGMP要求确定商业批量生产产品的工艺。制造工艺必须能够持续生产质量稳定的候选药物批次,此外,制造商还必须开发测试最终药物的特性、强度、质量和纯度的方法。此外,必须选择和测试适当的包装,并进行稳定性研究,以证明候选药物在保质期内不会发生不可接受的变质。
在IND处于活动状态且获得批准之前,赞助商必须至少每年向FDA提交总结自上次进展报告以来进行的临床试验和非临床研究结果的进展报告,以及必须向FDA提交书面的IND安全报告,包括严重的和意外的 不良事件、其他研究结果表明暴露于相同或类似药物的人体存在重大风险、动物试验或体外试验结果表明对人类有重大风险,以及与方案或研究人员手册中列出的结果相比,任何临床上重要的严重可疑不良反应发生率增加。
此外,还要求向公共注册机构报告正在进行的临床试验和已完成的试验结果。FDA监管产品的某些临床试验的赞助商必须注册并披露特定的临床试验信息,这些信息可在www.Clinicaltrials.gov上公开获得。与产品、患者群体、调查阶段、试验地点和调查人员以及临床试验的其他方面相关的信息 随后作为注册的一部分公开。赞助商还有义务在完成后讨论他们的临床试验结果。 这些试验的结果可以推迟到正在研究的新产品或新适应症获得批准后才公布。
美国市场审批流程
产品开发、临床前研究和其他非临床研究和临床试验的结果,以及对制造工艺的描述、对药物化学成分进行的分析测试、建议的标签和其他相关信息,将作为NDA或BLA的一部分提交给FDA,请求 批准该产品上市。提交保密协议或BLA需要支付使用费;在某些有限的情况下,可获得此类费用的豁免。FDA审查所有提交的NDA和BLA,以确保它们在接受备案之前足够完整 进行实质性审查。FDA可能会要求提供更多信息,而不是接受NDA或BLA 进行备案。在这种情况下,必须重新提交保密协议或BLA以及附加信息。重新提交的申请在FDA接受备案之前也要经过 审查。
一旦提交的申请被接受,FDA就开始进行深入的实质性审查。FDA可以将NDA或BLA提交给咨询委员会进行审查、评估和建议 是否应该批准申请以及在什么条件下批准。FDA不受咨询委员会的建议的约束,但它通常遵循这样的建议。审批过程漫长且往往很困难,如果不符合适用的监管标准或可能需要额外的临床或其他数据以及 信息,FDA可能拒绝批准NDA或BLA。即使提交了这样的数据和信息,FDA也可能最终决定NDA或BLA不符合批准标准 。FDA审查保密协议,除其他事项外,确定产品对于其预期用途是否安全有效,以及其制造是否符合cGMP,以确保和保持产品的特性、强度、质量和纯度。FDA审查BLA以确定产品是否安全、纯净和有效,以及制造、加工、包装或持有该产品的设施是否符合旨在确保产品持续安全、纯度和效力的标准。在批准保密协议或BLA之前,FDA将检查生产产品的一个或多个设施。
| 13 |
FDA对保密协议或BLA进行评估后,将 签发批准信或完整的回复信。批准函授权该药物的商业营销,并提供特定适应症的处方信息。一封完整的回复信表明申请的审查周期已经结束,目前的申请将不会获得批准。完整的回复信通常描述FDA确定的NDA或BLA中的具体缺陷,并可能需要额外的临床数据,例如额外的关键III期试验或与临床试验、非临床研究或生产相关的其他重要和耗时的要求。如果发出了完整的回复信, 赞助商必须重新提交保密协议或BLA,以解决信中确定的所有不足之处,或者撤回申请。即使提交了这样的数据和信息,FDA也可能判定NDA或BLA不符合批准标准。
如果产品获得监管部门的批准, 批准可能仅限于特定的疾病和剂量,或者使用适应症可能会受到限制,这可能会 限制产品的商业价值。此外,FDA可能要求赞助商进行第四阶段测试,包括临床试验,旨在NDA或BLA批准后进一步评估药物的安全性和有效性,并可能要求测试和监督计划,以监督已商业化的批准产品的安全性。FDA还可能在批准时附加其他条件,包括要求风险评估和缓解战略(“REMS”),以确保药物的安全使用。如果FDA得出结论认为需要REMS,NDA或BLA的赞助商必须提交一份建议的REMS。如果需要,FDA不会在没有批准的REMS的情况下批准NDA或BLA。REMS可以包括药物指南、医生沟通计划或确保安全使用的要素,如受限分发方法、患者登记和其他风险最小化工具。批准或营销方面的任何这些限制都可能限制产品的商业推广、分销、处方或分发。如果 不符合法规要求或在初始营销后出现问题,可能会撤回营销审批。
《孤儿药物法案》
《孤儿药品法》为制造商 提供激励措施,以开发和销售针对罕见病和病症的药物或生物制品,这些药物或生物制品适用于申请孤儿药物指定时在美国影响少于200,000人的罕见疾病或病症,或者针对美国患者人数超过200,000人且没有合理预期 将从美国的销售中收回的药物或生物制品。第一个获得FDA营销批准的孤儿药物开发商有权获得该产品在美国的七年独家营销期。然而,FDA认为临床上优于或不同于另一种批准的孤儿药物的药物,即使是相同的适应症, 也可能在七年的独家营销期内在美国获得批准。此外,孤儿药物的独家持有者应确保有足够数量的孤儿药物可供使用,以满足患者的需求。如果不这样做,可能会导致该药物的市场独家经营权被撤销。
儿科信息
根据2007年《儿科研究平等法》(“PREA”),NDA或BLAS或NDA或BLAS的补充剂必须包含数据,以评估该药物在所有相关儿科亚群中声称的适应症的安全性和有效性,并支持该药物对其安全有效的每个儿科亚群的剂量和给药。FDA可以批准推迟提交数据,或者给予全部或部分豁免。除非法规另有要求,否则PREA不适用于已被批准为孤儿药物指定的适应症的任何药物。《儿童最佳药品法》(BPCA)为NDA的赞助商提供了额外的六个月的市场独占期 ,条件是赞助商在规定的时间内提交FDA根据BPCA特别要求的儿科研究结果。《生物制品价格竞争与创新法案》规定,如果符合BPCA规定的条件,BLAS的赞助商可额外延长6个月的时间,以获得所有形式的含有BPCA规定的活性部分的生物制品的所有未到期的非专利市场独家经营权。
| 14 |
2012年7月9日签署成为法律的《食品和药物管理局安全与创新法案》(FDASIA)修订了FDCA。FDASIA要求计划 提交包含新活性成分、新适应症、新剂型、新给药方案或新给药途径的药物或生物制品的营销申请的赞助商必须在第二阶段会议结束后60天内或赞助商与FDA之间达成一致的情况下提交初步儿科研究计划(PSP)。初始PSP必须包括赞助者计划进行的一项或多项儿科研究的大纲,包括研究目标和设计、年龄组、相关终点和统计方法,或不包括此类详细信息的理由,以及任何推迟儿科评估或完全或部分免除提供儿科研究数据和支持信息的要求。FDA和赞助商必须就PSP达成协议 。如果需要根据从非临床研究、早期临床试验和/或其他临床开发计划收集的数据考虑儿科计划的变更,赞助商可以随时提交对商定的初始PSP的修正案。
加快发展和审查计划
FDA有一个快速通道计划,旨在 加快或促进审查符合特定标准的新药和生物制品的过程。具体地说,新药和生物制品如果旨在治疗严重或危及生命的疾病,并显示出解决该疾病未得到满足的医疗需求的潜力,则有资格获得快速通道指定。快速通道指定适用于 产品和正在研究的特定适应症的组合。新药或生物制剂的赞助商可在产品临床开发期间的任何时间要求FDA将该药物或生物制剂指定为快速通道产品。对于快速通道指定产品, FDA可以在提交完整的申请之前滚动考虑对营销申请的部分进行审查, 如果赞助商提供了提交申请部分的时间表,FDA同意接受申请的部分 并确定时间表是可接受的,赞助商在提交申请的第一部分时支付任何所需的使用费。
任何提交FDA上市的产品,包括快速通道计划,都可能符合FDA旨在加快开发和审查的其他类型计划的资格,例如 优先审查和加速审批。快速指定、优先审查和加速审批不会更改审批标准 ,但可能会加快开发或审批流程。在没有令人满意的替代疗法的情况下,或者与市场上销售的产品相比,在治疗、诊断或预防疾病方面有显著改善的情况下,任何产品都有可能 提供安全有效的治疗,才有资格优先审查。FDA将尝试将额外的资源用于评估指定优先审查的新药或生物制品的申请,以努力促进审查。此外, 产品可能有资格获得加速审批。被研究的药物或生物制品在治疗严重或危及生命的疾病方面的安全性和有效性,以及提供比现有治疗更有意义的治疗效果的药物或生物制品可能会获得加速批准 ,这意味着它们可能会根据充分且受控的临床试验确定产品 对合理地可能预测临床益处的替代终点有效,或基于对临床 终点的影响(而不是存活或不可逆转的发病率)而获得批准。作为批准的一项条件,FDA可以要求获得加速批准的药物或生物制品的赞助商进行充分和良好控制的上市后临床试验。此外,FDA目前 要求提前审批促销材料作为加速审批的条件,这可能会对产品的商业发布时间产生不利影响。如果FDA得出结论认为,被证明有效的药物只有在分销或使用受到限制的情况下才能安全使用,它将要求实施其认为必要的上市后限制,以确保药物的安全使用,例如(I)仅限于特定机构或具有特殊培训或经验的医生进行分销,或(Ii)以执行特定医疗程序为条件的分销。
FDASIA建立了一个新的药物和生物制品类别,称为“突破性疗法”,可能有资格获得突破性疗法称号。赞助商 可寻求FDA将一种药物或生物候选药物指定为“突破性疗法”,前提是该产品旨在单独或与一种或多种其他产品联合用于治疗严重或危及生命的疾病或状况,并且初步临床证据 表明该产品可能在一个或多个临床重要终点(如临床开发早期观察到的显著治疗效果)方面较现有疗法有显著改善。该指定包括Fast Track计划的所有功能, 以及更密集的FDA互动和指导。突破性治疗指定不同于加速批准和优先审查,如果符合相关标准,也可以授予同一药物优先审查。如果一种产品被指定为突破性疗法,FDA将加快此类药物的开发和审查。所有突破性治疗指定的申请将在收到后60天内进行审查,FDA将批准或拒绝该请求。
| 15 |
2016年颁布的《21世纪治疗法》为包括细胞和基因疗法在内的再生医学产品建立了一个新的快速审批计划。再生医学高级疗法(“RMAT”)计划建立了一个快速审查计划,以促进再生医学 疗法的开发和审查,以满足病情严重的患者未得到满足的医疗需求。如果研究药物符合再生医学疗法(如细胞疗法或基因疗法)的定义;(2)旨在治疗、修改、逆转或治愈严重疾病;以及(3)初步临床证据表明,再生医学疗法有可能解决此类疾病未得到满足的医疗需求,则有资格获得rmat 指定。RMAT指定的优势包括快速通道和突破性治疗指定计划的所有好处,包括与FDA的早期互动。
审批后要求
一旦获得批准,如果没有遵守监管要求或标准,或者产品上市后出现问题,FDA可能会撤回批准。 如果后来发现某个产品存在以前未知的问题,可能会导致该产品受到限制,甚至完全从市场上撤出 。批准后,对批准的产品的某些类型的更改,如增加新的适应症、某些 生产更改和额外的标签声明,需要接受FDA的进一步审查和批准。药品和生物制品制造商 以及参与生产和分销批准的药品和生物制品的其他实体必须向FDA和某些州机构注册其机构,并接受FDA和某些州机构的定期突击检查,以确保 遵守cGMP法规和其他法律法规。
美国专利期限恢复与市场排他性
生物制品价格竞争和创新法案,或BPCIA,修订了公共卫生服务法,授权FDA批准类似版本的创新生物制品,通常被称为生物仿制药。寻求批准生物相似物的竞争对手必须提交申请,以确定其分子与经批准的创新者生物高度相似,以及其他要求。然而,BPCIA禁止FDA在创新者生物制品获得初步营销批准后12年内根据该公司的数据批准生物相似申请。如果FDA要求创新者公司对该产品进行儿科临床研究,则这一12年的数据独占期可延长6个月,总计12年半。
根据FDA批准我们候选药物的时间、持续时间和具体情况,我们的一些美国专利可能有资格根据1984年的《药品价格竞争和专利期限恢复法》(通常称为《哈奇-瓦克斯曼修正案》)获得有限的专利期延长。Hatch-Waxman修正案 允许最长五年的专利恢复期限,作为在产品开发和FDA监管审查过程中失去的专利期的补偿。但是,专利期限的延长不能使专利的剩余期限从产品批准之日起总共超过14年。专利期延展期一般为IND生效日期至提交保密协议或BLA之日之间的时间的一半,加上NDA或BLA提交之日至该申请获得批准之间的时间,最长可延长5年。只有一项适用于批准的药物的专利有资格延期,延期申请必须在专利到期前提交。美国专利商标局与FDA协商,审查和批准任何专利期延长或恢复的申请。未来,我们打算申请延长我们目前拥有或许可的一项专利的专利期 ,以便根据临床试验的预期长度和相关保密协议或BLA的提交所涉及的其他因素,在合理获得的情况下将专利寿命延长到当前到期日之后。
| 16 |
FDCA 中的营销排他性条款还可能延迟某些营销申请的提交或审批。FDCA为第一个获得新化学实体保密协议批准的申请者提供了五年的非专利营销在美国的独家经营权。如果FDA以前没有批准过含有相同活性部分的任何其他新药,则药物是一种新的化学实体 ,该活性部分是负责该药物物质作用的分子或离子。在排他期内,FDA可能不接受另一家公司基于相同活性部分为另一种药物提交的简化新药申请 (ANDA)或505(B)(2)NDA,无论该药物 是用于与原始创新药物相同的适应症还是用于另一种适应症,如果申请人不拥有或没有 参考批准所需的所有数据的合法权利。然而,如果申请包含创新者NDA持有人向FDA列出的其中一项专利的专利无效或未侵权证明,则可以在四年后提交申请。如果FDA认为申请人进行或赞助的新的临床研究(生物利用度研究除外)对于批准 申请至关重要(例如,现有药物的新适应症、剂量或强度),则FDCA 还为NDA或现有NDA的补充物提供三年的市场排他性。这项为期三年的专营权仅涵盖该药物在新的临床研究基础上获得批准的修改 ,并不禁止FDA批准含有原适应症或使用条件的活性成分的药物的ANDA 。五年和三年的排他性不会推迟提交或批准完整的保密协议。然而,提交完整的保密协议的申请者将被要求进行或获得参考所有临床前研究和充分和良好控制的临床试验的权利,以证明安全性和有效性。
儿科专营权是美国BPCA规定的另一种监管市场专营权。如果赞助商按照上文“儿科信息”一节所述在儿童身上进行临床试验,则儿科专营权提供额外六个月的市场独家经营权。此外,如上文所述,孤儿药物专营权可能提供七年的市场专营期,但在某些情况下除外。
外国监管
除美国法规外,我们还将 遵守其他司法管辖区的各种法规,其中包括临床试验和任何商业销售 以及我们候选药物的分销。
无论我们的候选药物是否获得FDA批准,我们都必须在这些国家/地区开始 临床试验或上市之前获得外国监管机构的必要批准。美国以外的某些国家/地区也有类似的流程,即 要求在人类临床试验开始之前提交临床试验申请(“CTA”),这与IND非常相似。例如,在欧盟,CTA必须提交给每个国家的国家卫生当局和一个独立的伦理委员会,很像FDA和IRB。一旦CTA根据一个国家的要求获得批准,就可以继续进行临床研究开发。
管理进行临床试验、产品审批和许可、定价和报销的要求和流程因国家/地区而异。在所有情况下,临床试验均按照GCP以及源于《赫尔辛基宣言》的适用法规要求和伦理原则进行。
要在欧盟监管体系下获得监管机构对正在研究的 药物或生物制品的批准,我们必须提交上市授权申请。在美国用于提交保密协议或BLA的申请 类似于欧盟要求的申请,但不同的是,其中包括特定于国家/地区的文件要求。欧盟也为市场排他性提供了机会。例如,在欧洲联盟,在获得营销授权后,新的化学实体通常获得八年的数据独占权和额外的两年市场独占权。如果获得批准,数据排他性将阻止欧盟监管机构参考创新者的数据来评估通用应用程序。在额外的两年市场独占期内,可以提交通用营销授权,并可以参考创新者的数据,但在市场独占权到期 之前,不能销售任何仿制产品。但是,不能保证产品会被欧盟监管机构 视为新的化学实体,并且产品可能没有资格获得数据独占。在欧盟获得孤儿称号的产品可以获得十年的市场排他性,在此期间,相同适应症的类似医药产品不得投放市场 。孤儿产品还可以在欧盟获得额外两年的儿科研究市场排他性。 任何补充保护证书都不能基于孤儿适应症的儿科研究而获得延期。
| 17 |
欧盟指定“孤儿药品”的标准原则上与美国相似。根据(EC)141/2000号条例第3条,如果(1)一种药品用于诊断、预防或治疗危及生命或慢性衰弱的疾病,则可将该药品指定为孤儿。(2)(A)在提出申请时,这种情况在欧盟每10,000人中影响不超过5人,或者(B)如果没有孤儿身份的好处,产品将不会在欧盟产生足够的回报 以证明投资是合理的;以及(3)没有令人满意的诊断、预防或治疗这种情况的方法授权在欧盟销售,或者如果存在这种方法,产品将对受这种情况影响的人有重大好处,如(EC)847/2000条例所定义。孤儿医药产品有资格获得减费或减免费用等财政奖励,并在获得营销授权后,有权获得 经批准的治疗适应症的十年市场独家经营权。孤儿药品指定申请必须在申请上市前提交。 如果孤儿药物指定已被批准,申请人将获得上市授权申请的费用减免,但如果在提交上市授权时该指定仍在等待中,则不会。孤儿药物指定 不会在监管审查和审批过程中传递任何优势,也不会缩短监管审批过程的持续时间。
如果在第五年结束时确定该产品不再符合孤儿指定的标准,例如,如果该产品的利润足够高,不足以证明保持市场独占性是合理的,则10年的市场独占权可能会减少 至6年。此外,在下列情况下,可随时针对相同适应症的类似产品授予营销授权 :
| · | 第二个申请人可以证明,其产品虽然相似,但更安全、更有效或在临床上更优越; | |
| · | 申请人同意第二次申请孤儿药品的;或 | |
| · | 申请人不能提供足够的孤儿药品。 |
对于欧盟以外的其他国家/地区,例如东欧、拉丁美洲或亚洲的国家/地区,进行临床研究、产品许可或审批、定价和报销的要求因国家/地区而异。再次重申,在所有情况下,临床研究都是根据GCP以及源于《赫尔辛基宣言》的适用法规要求和伦理原则进行的。
如果我们未能遵守适用的外国监管要求,我们可能会受到罚款、暂停或撤回监管审批、产品召回、产品扣押、经营限制和刑事起诉等处罚。
其他监管事项
产品批准后的制造、销售、推广和其他活动 除了受FDA的监管外,还可能受到许多监管机构的监管,包括在美国的医疗保险和医疗补助服务中心、卫生与公众服务部的其他部门、药品执法管理局、消费品安全委员会、联邦贸易委员会、职业安全与健康管理局、环境保护局以及州和地方政府。在美国,销售、营销和科学/教育项目还必须遵守州和联邦的欺诈和滥用法律,包括州和联邦的反回扣、虚假声明、数据隐私 以及安全和医生支付透明度法律。定价和返点计划必须符合1990年《美国综合预算调节法》的联邦医疗保健计划(例如,医疗补助)返点要求,以及经2010年《医疗保健和教育调节法》修订的《患者保护法案》和《平价医疗法案》中的最新要求,统称为《平价医疗法案》, 以及2022年《降低通货膨胀法案》。如果向总务署联邦供应时间表的授权用户提供产品,则适用其他法律和要求。处理任何受控物质必须遵守美国《受控物质法》和《受控物质进出口法》。产品必须符合美国《防止毒物包装法》中适用的儿童保护包装要求。制造、销售、促销和其他活动也可能受到联邦和州消费者保护和不正当竞争法律的约束。
| 18 |
医药产品的分销受其他要求和法规的约束,包括旨在防止未经授权销售医药产品的广泛记录保存、许可、储存和安全要求。
未能遵守监管要求 可能使我们面临可能的法律或监管行动。根据具体情况,未能满足适用的法规要求 可能会导致刑事起诉、罚款或其他处罚、禁令、召回或扣押产品、完全或部分暂停生产、拒绝或撤回产品批准或拒绝允许公司签订供应合同,包括政府合同 。此外,即使一家公司遵守了FDA和其他要求,有关产品安全性或有效性的新信息也可能导致FDA修改或撤回产品批准。禁止或限制销售或撤回我们销售的未来产品 可能会以不利的方式对我们的业务产生重大影响。
法规的变更或现有法规的解释 可能会影响我们未来的业务,例如,要求:(I)更改我们的制造安排; (Ii)添加或修改产品标签;(Iii)召回或停产我们的产品;或(Iv)额外的记录保存 要求。如果强制实施任何此类变化,可能会对我们的业务运营产生不利影响。
报销
在国内和国外市场,任何经批准的产品的销售和报销在一定程度上将取决于第三方付款人支付此类产品成本的程度,如政府医疗计划、商业保险和托管医疗机构。这些第三方付款人越来越多地 挑战医疗产品和服务的价格,并实施控制以管理成本。控制医疗成本已成为联邦和州政府的优先事项,药品价格一直是这一努力的重点。各国政府对实施成本控制计划表现出了极大的兴趣,包括价格控制、对报销的限制以及对非专利产品的替代要求。例如,在美国,国会最近进行了几次调查,提出并颁布了联邦和州立法,旨在提高药品定价的透明度,审查定价与制造商患者计划之间的关系,降低联邦医疗保险下药品的成本,改革政府计划药品报销 方法。此外,2018年5月,特朗普政府制定了降低药品价格和 降低药品自付成本的《蓝图》,其中包含增加制造商竞争、增加某些联邦医疗保健计划的谈判能力、激励制造商降低其产品标价和降低消费者支付的药品自付成本的额外建议。虽然拜登政府没有继续这一努力,但它有权采取其他行动。2020年12月,特朗普政府发布了临时最终规则,重点是试图降低药品价格,包括 允许从加拿大进口某些药品,根据联邦医疗保险B部分对某些药品类别进行最惠国定价 ,以及通过修改美国联邦反回扣法规对联邦医疗保险D部分药品回扣计划进行修改。B部分最惠国规则于2021年1月4日被一名联邦法官阻止生效,称该规则过于仓促,没有为公众提供时间来根据《行政程序法》的要求发表评论。然后,在2021年12月29日,CMS发布了最终规则 ,正式废除了最惠国规则。还有悬而未决的诉讼要求暂缓对Medicare Part D药品 回扣计划和反回扣法规的更改。2021年1月30日,哥伦比亚特区地方法院批准了双方的 规定请求,将D部分返点规则的生效日期推迟到2023年1月1日。2022年8月7日,国会通过了《2022年通胀削减法案》,该法案将联邦医疗保险D部分药品退税计划和美国联邦反回扣法规的修改推迟到2032年1月实施。
此外,2022年的通胀降低法案可能会影响涵盖处方药的现有医疗保险计划。除其他相关条款外,2022年的《降低通货膨胀法案》允许联邦医疗保险计划通过设定某些“最高公平价格”,分别从2028年和2026年开始,直接协商联邦医疗保险B部分和D部分涵盖的某些高支出处方药的价格。此外,2022年的《减少通货膨胀法案》要求,如果联邦医疗保险计划涵盖的某些药品的价格上涨速度快于通货膨胀率,制造商必须向联邦政府支付回扣。
| 19 |
在州一级,立法机构越来越多地通过立法并实施旨在控制药品和生物产品定价的法规,包括价格或患者 报销限制、折扣、对某些产品准入的限制以及营销成本披露和透明度措施,在某些情况下,还鼓励从其他国家进口和批量购买。
在美国境内,如果我们未来获得适当的批准来销售我们的任何候选产品,我们可能会根据Medicaid、Medicare和公共卫生服务(PHS)药品定价计划为这些产品寻求批准和承保范围,还可能寻求将产品销售给联邦机构。医疗补助 是一项联邦和州联合计划,由各州管理,面向低收入和残疾受益人。根据Medicaid药品返点计划,制造商需要为州Medicaid计划报销的每单位产品支付返点。每种产品的返点金额是由法律规定的,如果某些价格的涨幅超过 通胀,可能会受到额外的折扣。联邦医疗保险是由联邦政府管理的一项联邦计划,涵盖65岁及以上的个人以及某些残疾人士。联邦医疗保险D部分为已登记的联邦医疗保险患者提供自我管理药物(即不需要由医生管理的药物)的保险。Medicare Part D由美国政府批准的私人处方药计划管理,每个药物计划都会为处方药的承保范围和定价建立自己的Medicare Part D处方,药物 计划可能会不时修改这些处方。联邦医疗保险B部分涵盖大多数在住院环境中使用的注射药物,以及由医院门诊部和医生办公室的有执照的医疗提供者管理的一些药物。Medicare B部分由Medicare 行政承包商管理,通常负责做出承保决定。根据某些付款调整和限制,Medicare通常根据制造商报告的平均销售价格的百分比来支付B部分承保药品的费用。药品 如果由联邦机构通过联邦供应时间表(FSS)购买,则可享受折扣定价。对于某些联邦机构承保和支付的药品,以及根据Medicaid、Medicare Part B 和PHS药品定价计划承保的药品,都需要参加FSS 。FSS定价定期与退伍军人事务部谈判。FSS定价 旨在不超过制造商对其产品向其最惠国非联邦客户收取的价格。此外,退伍军人管理局、国防部(包括军人及其家属通过TRICARE零售药房计划购买的药品)、海岸警卫队和小灵通购买的药品的价格 受定价上限(称为“联邦最高价格”)的限制,如果价格涨幅超过通胀,可能会受到额外折扣。为了维持医疗补助药品返点计划下的药品覆盖范围,制造商需要根据PHS药品定价计划向某些购买者提供折扣 。有资格获得折扣的购买者包括为经济困难患者提供不成比例服务的医院、社区卫生诊所和其他从PHS获得卫生服务赠款的实体。
2010年3月,美国国会颁布了《患者保护和平价医疗法案》和《医疗保健和教育协调法案》,或《平价医疗法案》,其中包括对政府医疗保健计划下药品的承保范围和支付方式进行的更改。自颁布以来,《平价医疗法案》的众多内容一直受到司法和国会的挑战,联邦政府的行政和立法部门 都在努力废除或取代《平价医疗法案》的某些方面。例如,前总裁·特朗普签署了 行政命令,旨在推迟实施《平价医疗法案》的某些条款,或以其他方式规避《平价医疗法案》规定的一些医疗保险要求。此外,美国国会已考虑立法, 将废除或废除并取代全部或部分《平价医疗法案》。虽然国会还没有通过全面的废除立法,但它已经制定了法律来修改《平价医疗法案》的某些条款,例如从2019年1月1日起取消对 不符合《平价医疗法案》个人购买医疗保险的规定的处罚,推迟实施某些强制收费,并增加参与联邦医疗保险部分的制药商所欠的销售点折扣。德克萨斯州一名地区法院法官裁定,《平价医疗法案》整体违宪,因为“个人强制令”已被国会废除,作为2017年减税和就业法案或税法的一部分。尽管最高法院在2021年6月裁定原告没有资格,但任何其他行政、立法或司法行动,如要“废除并取代”全部或部分《平价医疗法案》,可能会限制政府机构为医疗保健产品和服务支付的金额 ,这可能会导致对我们产品的需求减少或额外的定价压力,或者可能导致 大幅放松监管,这可能会使引入竞争产品和技术变得更加容易。
无论《平价医疗法案》条款的未来如何,国会将继续辩论一系列政策,这些政策可能会影响制药公司对产品收取的价格 或他们获得的报销金额。
| 20 |
环境监管
除了受到FDA的广泛监管外,我们还必须遵守适用于我们或我们的候选药物的环境法规。我们遵守适用于类似制药公司的环境法规的成本 微乎其微,因为我们目前没有也不打算从事任何候选药物的生产。我们目前使用非关联制造商来生产我们所有的候选药物材料,并从这些制造商那里接收最终材料,而我们在该过程的任何阶段都不参与制造 过程。
尽管我们相信我们使用、处理、储存和处置候选药物材料的安全程序 符合州和联邦法律法规所要求的环境标准,但我们不能完全消除这些材料造成意外污染或伤害的风险。我们不提供特定的保险单来减轻对我们或对环境的风险。
员工
截至2022年12月31日,我们雇用了四名全职员工 。我们没有与我们的员工签订任何集体谈判协议,我们的任何员工也不是任何工会的成员。
为了补充我们自己的专业人员,我们聘请了监管事务、药物警戒、流程工程、制造、质量保证、临床前和临床开发、会计和业务发展方面的专家。这些人包括科学顾问和独立顾问。
竞争
生物技术和制药行业的特点是技术进步迅速,竞争激烈,并高度重视专有产品。虽然我们相信我们的技术、开发经验和科学知识为我们提供了竞争优势,但我们面临着来自许多不同来源的潜在竞争,包括主要的制药、专业制药和生物技术公司、学术机构和政府机构以及公共和私人研究机构。我们成功开发和商业化的任何候选产品都将与现有疗法和未来可能推出的新疗法展开竞争。
我们的许多竞争对手可能在研发、制造、临床前测试、进行临床试验、获得监管批准、 和营销批准的产品方面拥有比我们多得多的财力和专业知识。制药、生物技术和诊断行业的合并和收购可能会导致更多的资源集中在我们数量较少的竞争对手中。这些竞争对手还在招聘和留住合格的科学和管理人员、为临床试验建立临床试验场地和患者登记 ,以及在获取与我们的计划互补或必要的技术方面与我们展开竞争。较小或处于早期阶段的公司 也可能成为重要的竞争对手,特别是通过与大型和成熟公司的协作安排。
影响我们所有候选产品成功的关键竞争因素 如果获得批准,可能是它们的疗效、安全性、副作用、便利性、价格、仿制药竞争水平、 以及政府和其他第三方付款人是否可以报销。
如果我们的竞争对手 开发和商业化比我们可能开发的任何产品更安全、更有效、副作用更少或更少、更方便或更便宜的产品,我们的商业机会可能会减少或消失。我们的竞争对手也可能比我们更快地获得FDA或其他监管机构对其产品的批准 ,这可能会使我们的竞争对手在我们能够进入市场之前建立强大的市场地位。此外,我们的竞争能力在许多情况下可能会受到保险公司或其他第三方付款人的影响 试图鼓励使用非专利产品。目前市场上有许多符合我们 正在追求的适应症的仿制药,预计未来几年将有更多的仿制药上市。如果我们的候选治疗产品 获得批准,我们预计它们的定价将显著高于竞争对手的仿制药。
| 21 |
治疗癌症患者最常见的方法是手术、放射治疗和药物治疗,包括化疗、激素治疗、免疫治疗和靶向药物治疗。市场上有多种治疗癌症的药物疗法。在许多情况下,这些药物联合使用以提高疗效。在一定程度上,如果我们的候选产品最终与现有药物或其他疗法结合使用或作为其辅助使用,则我们的候选产品 将无法与它们竞争。目前批准的一些药物疗法是品牌药物,受专利保护,其他药物 是仿制药。其中许多已获批准的药物都是久负盛名的疗法,被医生、患者和第三方付款人广泛接受。总体而言,尽管过去几十年来癌症的治疗取得了长足的进步,目前市场上的治疗方法也为许多患者提供了好处,但这些治疗方法在一定程度上都受到疗效和不良事件发生率的限制,而且没有一种方法能成功地治疗所有患者。因此,癌症的发病率和死亡率仍然居高不下。
胰腺癌和实体瘤的DNA酶
在胰腺癌领域,我们将与目前批准的为数不多的胰腺癌治疗方法竞争,包括胰腺导管腺癌(PDAC)。在第一行设置中,吉西他滨与阿布拉沙尼联合®或FOLFIRINOX方案是目前的治疗标准。对于二线转移患者,肿瘤学家现有的治疗方法选择有限。FDA批准的唯一二线药物是Onivyde®吉西他滨联合氟尿嘧啶(5FU)和亚叶酸钙(LV)治疗。除了化疗,默克的KEYTRUDA®被批准用于MSI-H癌症(约占所有病例的1%)和Lynparza®被批准用于维持BRCA突变的胰腺癌(约占所有病例的7%)。
在过去的几年里,用于晚期PDAC的化合物已经出现了一些晚期临床失败。这些失败的试验大多是基于一个有希望的终点。在PDAC开发的后期阶段,很少有化合物 。
对于其他实体肿瘤,有大量公司 正在开发旨在与已批准的免疫疗法(包括免疫检查点抑制剂)结合使用的治疗方法,以治疗各种实体肿瘤适应症。
B细胞淋巴瘤的XCART治疗
美国和欧盟批准了许多CAR T疗法,包括诺华公司的Kymriah(Tisagenlecleucel);Gilead Sciences,Inc.和Kite Pharma的Yescarta (Axicabagene Cilolucel)和Tecartus(Brexucagene Autolucel);百时美施贵宝(Bristol Myers Squibb)的Breyanzi(Lisocabagene Maraleucel)和Abecma(Idecabagene Vicleucel);以及Janssen的Carvykti(Ciltakabene Autolucel)。此外,有100多种CAR T疗法产品正在开发中,其中相当多是同种异体和现成的细胞疗法。此外,根据我们的CAR T疗法针对的疾病,我们可能面临来自CAR T疗法和其他 方法(如小分子和抗体)的兴趣适应症的竞争。基于T细胞的癌症治疗,如CAR T和TCR疗法,最近已成为学术机构和生物制药公司重要的研究和开发领域。
用于药物递送的PSA
目前相互竞争的平台包括聚乙二醇化、FC融合、白蛋白融合、HES化、PAS化和CTP融合,以及学术机构和其他从事药物开发的较小制药公司的平台。除了在药物产品、疗法、技术和流程的开发方面与大学和其他研究机构竞争外,我们还可能在从大学获得产品或技术的权利方面与其他公司竞争。
| 22 |
可用信息
我们的网站地址是www.xeneticBio.com。我们网站上的信息或可通过我们的网站访问的信息不是本10-K表格年度报告的一部分。我们的10-K表格的年度报告、10-Q表格的季度报告和8-K表格的当前报告以及对这些报告的修订可在我们以电子方式提交或提交到美国证券交易委员会后,在可行的情况下尽快免费在 上或通过我们的网站获取。美国证券交易委员会维护着一个互联网网站,其中包含有关我们在www.sec.gov上提交的文件的报告、委托书和信息声明以及其他信息。
除了根据交易法第13或15(D)节披露当前信息 以及对于FD法规要求通过我们的美国证券交易委员会备案文件披露的信息报告 外,我们还打算通过我们的投资者关系网站、新闻稿、公开会议 电话会议和网络广播来披露此类最新信息。
项目1A--风险因素
我们的业务面临许多风险。 除了本年度报告中包含的其他信息以及我们提交给美国证券交易委员会的其他公开文件外,您还应仔细考虑下面描述的风险和不确定性。以下任何风险都可能对我们的业务、财务状况、运营结果和前景产生重大不利影响,并导致我们普通股的交易价格下跌。
与我们的财务状况和资本金要求有关的风险
我们从来没有盈利过,也可能永远不会实现或维持盈利。如果我们无法从我们的运营中产生足够的收入来支付费用,或者我们无法 以商业合理的条款获得额外的融资,我们的业务、财务状况和运营结果可能会受到实质性的 和不利影响.
我们是一家临床阶段的生物制药公司,运营历史有限。医药产品和技术开发是一项投机性很强的工作,涉及很大程度的风险。我们没有产品被批准用于商业销售,到目前为止只产生了有限的收入。在2022年4月之前,我们主要关注与我们的XCART技术相关的临床前开发工作。随着2022年4月从CLS获得DNase肿瘤学平台的许可,我们现在的主要重点是通过合作机会或通过监管批准和商业化来推动该技术的发展。我们预计将继续产生大量研发费用和其他与我们持续运营相关的费用。因此,我们从未实现盈利,而且在可预见的未来可能无法实现盈利。 如果有的话。我们未来能否赚取利润,将视乎多项因素而定,包括:
| · | 资助与我们的候选药物和技术的研发、监管批准、商业化以及销售和营销相关的成本; | |
| · | 市场接受我们的候选药物和技术; | |
| · | 获取和开发新的候选药物和技术的成本; | |
| · | 将我们的候选药物推向市场的能力; | |
| · | 与我们的业务有关的一般和行政费用; | |
| · | 增加我们的研发成本; | |
| · | 与购买技术或其他资产有关的费用; | |
| · | 建立、维护和保护我们的知识产权; | |
| · | 吸引、聘用和留住合格人才;以及 | |
| · | 我们筹集额外资本的能力。 |
| 23 |
截至2022年12月31日,我们的累计赤字约为1.891亿美元。随着我们扩大研发活动以及商业化、营销和销售努力,我们预计会产生额外的重大运营亏损。我们还可能遇到不可预见的费用、困难、并发症、 延误和其他可能对我们的业务产生不利影响的未知因素。此外,由于与药品开发相关的许多风险和不确定性 ,包括我们当前的候选药物可能无法达到适用试验的临床终点 ,我们无法预测增加费用的时间或金额,以及我们是否或何时将实现或保持盈利。 如果我们无法从运营中产生足够的收入来支付费用,或者我们无法以商业合理的条款获得额外融资,我们的业务、财务状况和运营结果可能会受到实质性的不利影响。
我们将需要大量额外资金 来实现我们的目标。如果在需要时未能按可接受的条款获得必要的资金,或根本无法获得资金,可能会迫使我们推迟、限制或终止我们的产品开发工作、其他运营或商业化工作。
开发候选药物是一个昂贵、有风险且漫长的过程,我们预计与我们正在进行的活动相关的费用将会增加,特别是在我们继续研究和开发候选药物、启动临床试验并寻求上市批准的情况下。
截至2022年12月31日,我们拥有约1,310万美元的现金。我们预计,我们将需要额外的资金来开始和完成临床试验,获得监管部门对我们的候选药物的批准,并将其商业化,包括我们的其他临床前候选药物和未来的候选药物。但是,由于许多我们目前未知的因素,我们的运营计划可能会发生变化,我们可能需要比计划的更早寻求额外资金。额外的资金可以通过公共或私人股本或债务融资、第三方融资、营销和分销安排或其他合作、战略联盟和许可安排(或这些方法的组合)来获得。无论如何, 我们将需要更多资金来开展临床前和临床活动,寻求监管部门的批准,并将我们的长期候选药物商业化。 即使我们认为我们有足够的资金用于当前或未来的运营计划,如果市场条件有利或我们有特定的战略考虑,我们可能会 寻求额外的资本。
我们筹集额外资金的能力将取决于 金融、经济、政治和市场状况以及我们可能无法或有限控制的其他因素。持续的新冠肺炎疫情或其他因素(如地缘政治紧张局势,包括最近俄罗斯入侵乌克兰)以及由此产生的任何制裁、出口管制或其他限制性行动导致的市场波动 也可能对我们在需要时获得资本的能力产生不利影响。当我们需要额外资金时,我们可能无法以我们可以接受的条款和成本获得这些资金, 或者根本无法获得。
任何额外的筹款活动都可能使我们的管理层从日常活动中分心,这可能会对我们开发和商业化我们的候选药物的能力产生不利影响。 此外,我们不能保证未来的融资将以足够的金额或我们可以接受的条款提供(如果有的话)。 此外,任何融资条款可能会对我们股东的持股或权利产生负面影响,我们额外发行 证券(无论是股权还是债务),或发行此类证券的可能性,可能会导致我们股票的市场价格下跌。债务的产生可能导致固定支付义务的增加,我们可能需要同意某些限制性的 契约,例如对我们产生额外债务的能力的限制、对我们获取、销售或许可知识产权的能力的限制 以及可能对我们的业务开展能力产生不利影响的其他运营限制。
如果我们无法及时获得资金 ,我们可能需要大幅缩减、推迟或停止我们的临床前开发计划或任何候选药物的商业化 。我们也可能无法按预期扩大我们的业务或以其他方式利用我们的商机,这可能会损害我们的业务、财务状况和运营结果。
| 24 |
筹集额外资本可能会对我们的股东造成稀释,限制我们的运营,或者要求我们放弃对我们的技术或候选药物的权利。
在此之前,如果我们能够产生可观的产品收入,我们预计将通过股权和债务融资相结合的方式来满足我们的现金需求,并选择性地继续 进行合作、战略联盟和许可安排。我们目前没有任何承诺的外部资金来源 。在我们通过出售股权或可转换债务证券筹集额外资本的情况下,股权将被稀释,这些证券的条款可能包括清算或其他对我们股东权利产生不利影响的优惠。 债务融资可能涉及一些协议,其中包括限制或限制我们采取特定行动的能力的契约, 例如产生额外债务、进行资本支出或宣布股息。此类债务融资也可由我们全部或部分资产担保。
如果我们通过有选择地继续与第三方进行合作、战略联盟或许可安排来筹集资金,我们可能不得不放弃对我们的技术、未来收入流、研究计划或候选药物的额外有价值的 权利,或者我们可能不得不以可能对我们不利的条款授予许可证。如果我们无法在需要时通过股权或债务融资筹集更多资金,我们可能会被要求 推迟、限制、减少或终止我们的产品开发或未来的商业化努力,或者授予我们开发和营销我们原本更愿意自己开发和营销的候选药物的权利。如果我们无法通过协作、战略联盟或许可安排筹集更多资金,我们可能需要终止产品开发或未来的商业化努力 或完全停止运营。
与我们医药产品的发现和开发相关的风险
我们的业务在很大程度上依赖于DNase肿瘤学平台的成功。
我们的业务将在很大程度上取决于DNase肿瘤学平台的成功临床开发、监管批准和商业化。在我们被允许开始商业化之前,它将需要大量的临床开发和监管批准工作,如果有的话。我们已经并计划继续通过学术和战略合作来实施我们的临床开发战略。如果我们难以维持、 获得或无法按计划获得这些合作和其他学术合作,我们可能需要推迟、限制或终止任何正在进行或计划中的临床开发,这将对我们的业务产生不利影响。DNase和任何其他候选产品的临床试验以及 制造和营销将受到美国、欧盟和其他司法管辖区众多政府机构的广泛而严格的审查和监管 我们打算在这些司法管辖区测试和销售我们的候选产品 。在获得任何候选产品商业化销售的监管批准之前,我们必须通过 临床前测试和临床试验证明,该候选产品可安全有效地用于每个目标适应症,并有可能用于特定患者群体。这一过程可能需要多年时间,可能包括上市后研究和监督,这将需要我们目前筹集的收益之外的大量资源支出。在美国和欧盟批准的大量正在开发的药物 中,只有一小部分药物成功完成了FDA或欧洲药品管理局的监管审批流程 ,并已商业化。因此,即使我们能够获得必要的资金或找到学术合作伙伴或战略合作伙伴继续为我们的研究、开发和临床项目提供资金,我们也不能向您保证DNase 或我们的任何其他候选产品将成功开发或商业化。
| 25 |
我们是开发包括候选药物和技术在内的医药产品业务的早期公司。鉴于这种发展的不确定性,我们的业务 可能永远不会完全实现并为投资者创造价值。
我们已经投入了几乎所有的精力和财力来开发我们的产品,目前我们还没有任何获得市场批准的产品。到目前为止,我们的收入主要来自单一合作伙伴的协作和版税收入,而不是产品销售收入。我们创造产品收入的能力将取决于我们候选药物的成功开发和最终商业化 ,这可能在几年内不会发生。我们目前根据分许可协议产生版税收入,但没有任何 药品的销售收入,我们可能永远无法开发或商业化适销药。在我们从药品销售中获得任何收入之前,我们的每个候选药物都将需要开发、管理 开发和制造活动、在多个司法管辖区获得上市批准、获得制造供应、建立商业组织、大量投资和重大营销工作。我们 尚未证明有能力成功克服公司 在新的和快速发展的领域中经常遇到的许多风险和不确定性,特别是在制药领域。例如,要执行我们的业务计划,我们需要成功 :
| · | 为我们的候选药物执行开发活动,包括成功登记和完成临床试验; | |
| · | 为我们的候选药物的开发和商业化获得所需的市场批准; | |
| · | 获得并维护我们候选药物的专利和商业秘密保护或法规排他性; | |
| · | 保护、利用和扩大我们的知识产权组合; | |
| · | 建立和维护临床和商业制造能力,或与第三方制造商就临床和商业制造作出安排; | |
| · | 如果我们的候选药物获得批准,建立和保持强大的销售、分销和营销能力,无论是我们自己还是与战略合作伙伴合作; | |
| · | 如果我们的候选药物获得患者、医学界和第三方付款人的批准,则获得接受; | |
| · | 有效地与其他疗法竞争; | |
| · | 获得并维持医疗保险和适当的报销; | |
| · | 在我们的候选药物获得批准后,继续保持可接受的安全性; | |
| · | 发展和维护我们选择加入的任何战略关系(如果有的话); | |
| · | 执行和捍卫知识产权和索赔;以及 | |
| · | 随着临床前开发、临床试验、市场批准和商业化导致的成本和费用增加,管理我们的支出。 |
我们可能会发现很难在我们的临床研究中招募患者 ,这可能会推迟或阻止我们的药品的临床研究。
确定患者并使其有资格参与我们药品的临床研究,这对我们的成功至关重要。我们临床研究的时间取决于我们招募患者参与测试我们药品的速度。我们可能会遇到延误。如果患者因生物制药行业不良事件的负面宣传或其他 原因(包括类似患者群体的竞争性临床研究)而不愿参与我们的临床研究,则招募患者、进行研究和获得监管部门对潜在产品的批准的时间可能会推迟。这些延迟可能会导致成本增加、延迟推进我们的产品开发、延迟测试我们技术的有效性或完全终止临床研究。
| 26 |
我们可能无法识别、招募和招募足够数量的患者,或那些具有在研究中实现多样性所需或期望的特征的患者,以及时完成我们的临床 研究。患者入选受到许多因素的影响,包括:
| · | 正在调查的疾病的严重程度; | |
| · | 替代治疗的实际或感知可获得性; | |
| · | 患者群体的规模和性质; | |
| · | 有关试验的资格标准和设计; | |
| · | 接受研究的候选药物的感知风险和益处; | |
| · | 为潜在患者提供临床地点的近似性和可用性; | |
| · | 正在进行的潜在竞争药物的临床试验; | |
| · | 医生和患者对我们正在研究的候选药物相对于现有疗法或其他正在开发的产品的潜在优势的看法; | |
| · | 我们的CRO和我们的试验站点努力促进临床试验的及时登记; | |
| · | 医生的病人转介做法;以及 | |
| · | 需要在治疗期间和治疗后监测患者并充分收集患者数据。 |
如果我们不能招募足够数量的符合条件的患者参加FDA或其他监管机构要求的临床研究,我们可能无法启动或继续进行临床研究。我们在任何国家/地区成功启动、登记和完成临床研究的能力都会面临许多在国外开展业务所特有的风险,包括:
| · | 难以建立或管理与CRO和医生的关系; | |
| · | 进行临床研究的不同标准; | |
| · | 我们无法找到合格的本地顾问、医生和合作伙伴;以及 | |
| · | 遵守各种外国法律、医疗标准和监管要求的潜在负担,包括对药品和生物技术产品和治疗的监管。 |
如果我们难以招募足够数量的患者来按计划进行临床研究,我们可能需要推迟、限制或终止正在进行或计划中的临床研究, 任何此类研究都会对我们的业务产生不利影响。
| 27 |
我们可能会在临床试验的开始、登记或完成方面遇到重大延误,或者我们可能无法证明安全性和有效性,使相关监管机构满意,这可能会阻止我们及时将当前和未来的候选药物商业化(如果有的话)。
在获得监管部门批准销售我们当前和未来的候选药物之前,我们必须进行广泛的临床试验,以证明候选药物的安全性和有效性。我们不能保证任何临床研究将按计划进行或按计划完成, 如果有的话。一项或多项临床研究的失败可能发生在测试的任何阶段。可能妨碍成功或及时完成临床开发的事件包括:
| · | 延迟与监管机构就研究设计达成共识; | |
| · | 延迟与未来的CRO和临床研究地点就可接受的条款达成协议; | |
| · | 在每个临床研究地点延迟获得所需的IRB或独立伦理委员会的批准; | |
| · | 延迟招募合适的患者参与我们的临床研究; | |
| · | 由监管机构实施临床暂停,包括在检查我们的临床研究操作或研究地点之后; | |
| · | 我们的CRO、其他第三方或我们未能遵守临床研究要求; | |
| · | 未按照FDA的GCP或其他国家/地区适用的法规要求执行; | |
| · | 我们的候选药物的测试、验证、制造和交付到临床地点的延迟; | |
| · | 延迟让患者完全参与一项研究或返回治疗后随访; | |
| · | 临床研究地点或患者退出研究; | |
| · | 临床试验结果可能无法证明候选药物的安全性和/或有效性; | |
| · | 与候选药物有关的严重不良事件的发生,被认为超过了其潜在的好处;或 | |
| · | 需要修改或提交新的临床方案的法规要求和指南的变化。 |
任何无法成功完成临床前研究和临床试验的情况都可能导致我们的额外成本,或者削弱我们从产品销售、监管 以及商业化里程碑和版税中获得收入的能力。此外,如果我们对我们的候选药物进行生产或配方更改,我们 可能需要进行额外的研究,以将我们的修改后的候选药物与更早的版本连接起来。临床试验延迟还可能缩短我们可能拥有将候选药物商业化的独家权利的任何期限,或者允许我们的竞争对手在我们之前将产品 推向市场,这可能会削弱我们成功将候选药物商业化的能力,并可能损害我们的业务、财务状况、运营结果和前景。
如果我们的临床研究结果不确定 ,或者如果与我们的药品相关的安全问题或不良事件,我们可以:
| · | 延迟获得我们候选药物的上市批准或许可证,如果我们真的获得了它们的话; | |
| · | 获得批准的适应症或患者群体并不像预期或期望的那样广泛; | |
| · | 获得包括重大使用或分销限制或安全警告在内的标签的批准; | |
| · | 产品的使用方式可能会发生变化; | |
| · | 被要求进行额外的临床研究以支持批准或接受额外的上市后测试要求; | |
| · | 让监管部门撤回对该产品的批准,或以修改后的风险评估和缓解战略的形式对其分销施加限制; | |
| · | 附加标签说明,如警告或禁忌症; | |
| · | 被起诉;或 | |
| · | 我们的声誉受到了损害。 |
如上所述,上述任何事件都可能 阻止我们实现或维持市场对我们药品的接受程度,并削弱我们创造收入的能力。
| 28 |
如果我们完成必要的临床前研究和临床研究,我们无法预测何时或是否会获得监管部门批准将候选药物商业化,或者批准的范围可能比我们预期的更窄。
候选药物在 相关监管部门审查和批准之前不能商业化。即使我们的候选药物在临床研究中表现出安全性和 有效性,监管机构也可能无法及时完成审查过程,或者我们可能无法 获得监管部门的批准。如果FDA咨询委员会或其他监管咨询小组或机构 建议不批准或限制批准,可能会导致额外的延迟。此外,在产品开发、临床研究和审查过程中,我们可能会因未来立法或行政行动中的额外政府监管或监管机构政策的变化而受到延误或拒绝。监管机构也可以批准比要求的适应症更少或更有限的候选药物,也可以根据上市后研究的表现给予批准。此外,监管机构可能不会批准我们的候选药物成功商业化所必需或需要的标签声明。未能获得或延迟获得将候选药物商业化的监管批准将削弱我们的创收能力,并损害我们的 业务前景。
如果我们获得了候选药物的监管批准,我们的候选药物将继续受到监管审查。
如果我们的候选药物获得批准,它们将 遵守持续的法规要求,包括生产、标签、包装、储存、广告、促销、抽样、记录保存、 进行上市后研究以及提交安全性、有效性和其他上市后信息,包括美国的联邦和州 要求以及类似的外国监管机构的要求。
制造商和制造设施必须遵守FDA和类似的外国监管机构的广泛要求,包括确保质量控制和制造程序符合cGMP法规。因此,我们将接受持续的审查和检查,以评估对cGMP的遵守情况以及对任何保密协议、BLA或营销授权申请(MAA)中做出的承诺的遵守情况。因此,我们 以及我们的合作者和供应商必须继续在所有合规领域投入时间、金钱和精力,包括制造、生产和质量控制。
我们或我们的合作伙伴 为我们的候选药物获得的任何监管批准可能会受到产品上市的批准指示用途的限制或批准条件的限制,或者可能包含可能代价高昂的额外临床试验和监测的要求,以监控候选药物的安全性和有效性 。我们将被要求向FDA和类似的外国监管机构报告某些不良反应和生产问题(如果有)。任何涉及药品安全或与监管审查和批准相关的其他问题的新立法都可能导致产品开发或商业化的延迟,或增加确保合规的成本。我们将 必须遵守有关产品广告和促销的要求。有关处方 药品的促销信息受到各种法律和法规的限制,并且必须与产品 批准的标签中的信息一致。因此,我们不允许为未经批准的适应症或用途推广我们的产品。如果我们的 候选药物获得批准,我们必须提交新的或补充申请,并获得批准对已批准的 产品、产品标签或制造流程进行某些更改。我们还可以被要求进行上市后临床试验,以验证我们的产品在一般或特定患者亚组中的安全性和有效性。不成功的上市后研究或未能完成此类 研究可能会导致撤回营销审批。
| 29 |
如果监管机构发现获得批准的产品存在以前未知的 问题,例如意外严重性或频率的不良事件或我们的制造设施存在问题, 或者如果监管机构不同意产品的促销、营销或标签,该监管机构可能会对该产品或我们施加限制 ,包括要求该产品退出市场。如果我们未能遵守适用的监管要求,监管机构或执法机构可能会:
| · | 发出无标题和警告信; | |
| · | 施加民事或者刑事处罚的; | |
| · | 暂停、撤销监管审批或者吊销许可证的; | |
| · | 暂停或暂停我们正在进行的任何临床试验; | |
| · | 拒绝批准我们提交的待决申请或已批准申请的补充申请; | |
| · | 对我们的业务施加限制,包括关闭我们的制造设施;或 | |
| · | 扣押或扣留产品或要求召回产品。 |
政府对涉嫌违法的任何调查都可能需要我们花费大量时间和资源来回应,并可能产生负面宣传。任何未能遵守持续法规要求的行为都可能严重影响我们将产品商业化并从中获得收入的能力。如果实施监管制裁或撤销监管批准,公司价值和我们的经营业绩将受到负面影响 。
任何当前或未来药品的商业成功将取决于医生、患者、第三方付款人和医学界其他人 的市场接受程度。
即使获得必要的批准,我们药品的商业成功也将在一定程度上取决于医学界、患者和第三方付款人是否接受我们的药品 产品具有医疗用途、成本效益和安全性。我们或我们的合作伙伴向市场推出的任何药品可能无法 获得医生、患者、第三方付款人或医学界其他人的市场接受。这些药品的市场接受度 如果获准用于商业销售,将取决于许多因素,包括:
| · | 我们批准的候选药物与目前可用的产品相比的有效性; | |
| · | 患者是否愿意采用我们批准的候选药物来取代目前的治疗方法; | |
| · | 我们提供可接受的安全性和有效性证据的能力; | |
| · | 相对方便和容易管理; | |
| · | 任何不良副作用的流行率和严重程度; | |
| · | 限制与其他产品联合使用; | |
| · | 是否有替代治疗方法; | |
| · | 根据我们的候选药物和目标市场的概况,假设有竞争力或潜在的溢价要求,定价和成本效益; | |
| · | 我们或我们合作伙伴的销售和营销策略的有效性; | |
| · | 我们有能力获得足够的第三方保险或补偿;以及 | |
| · | 潜在的产品责任索赔。 |
即使一种潜在的产品在临床前和临床研究中表现出良好的 疗效和安全性,市场对该产品的接受度也要在该产品 上市后才能确定。我们教育医疗界和第三方付款人了解药品的好处的努力可能需要 大量资源,而且可能永远不会成功。如果这些产品没有达到足够的接受度,我们可能 不会产生显著的产品收入,也可能无法盈利。
| 30 |
开发中的候选药物的商业潜力很难预测。如果新候选药物或技术的市场规模明显小于我们预期的市场规模,可能会对我们的收入、运营结果和财务状况产生重大负面影响。
由于与其他可用技术或治疗方法相比的安全性和有效性等重要因素,很难估计药品的商业潜力 ,包括不断变化的护理标准、第三方付款人报销标准、患者和医生偏好、在漫长的药物开发过程中或商业引入后可能出现的竞争替代品的可用性,以及我们成功的候选药物在政府卫生部门批准后的仿制药版本的可用性 ,基于监管排他性到期或我们无法通过主张我们的专利来阻止仿制药版本上市。如果由于这些因素或其他因素,医药产品的市场潜力低于我们的预期,可能会对该医药产品的任何潜在合作伙伴关系的商业条款产生重大负面影响,或者,如果我们已经就该医药产品达成合作,则版税和里程碑付款的收入潜力可能会显著减少, 这将对我们的业务、财务状况和运营结果产生负面影响。
如果我们的候选药物未能获得或保持足够的保险和报销,如果获得批准,可能会限制我们营销这些产品的能力,并降低我们创造收入的能力 。
我们候选药物的成功,如果获得批准, 取决于第三方付款人是否提供足够的保险和报销。此外,由于我们的候选药物代表了治疗某些疾病的新方法,因此我们不能确保我们的候选药物将获得承保和报销,或准确地 估计我们的候选药物的潜在收入,也不能保证我们可能开发的任何产品都将获得承保和报销。
为其病情提供医疗服务的患者通常依靠第三方付款人来报销与其治疗相关的全部或部分费用。 政府医疗保健计划(如Medicare和Medicaid)和商业付款人的充足覆盖和报销对新产品的接受度 至关重要。
政府当局和第三方付款人,如私人健康保险公司和健康维护组织,决定他们将承保的药物和治疗以及报销金额 。第三方付款人的承保范围和报销可能取决于许多因素,包括第三方付款人对产品的使用是否符合以下条件的确定:
| · | 在其健康计划下有保障的福利; | |
| · | 安全、有效和医学上必要的; | |
| · | 适用于特定的患者; | |
| · | 具有成本效益;以及 | |
| · | 既不是试验性的,也不是调查性的。 |
在美国,为第三方付款人及其签约的药房福利经理管理此类付款人的处方 福利的第三方付款人及其签约的药房福利经理之间没有统一的承保和产品报销政策。因此,从政府或其他第三方获得产品的承保和报销审批是一个既耗时又昂贵的过程,这可能需要我们向每个支付方提供支持科学、临床和成本效益的数据,以逐个付款人的方式使用我们的产品,但不能保证将获得承保和充分的报销。 即使我们获得了特定产品的承保,所产生的报销付款率也可能不足以使我们实现或维持 盈利能力,或者可能需要患者发现无法接受的高共付额。此外,第三方付款人及其药房福利 经理可能不会为使用我们的基因修改产品后所需的长期后续评估提供保险或提供足够的报销。患者不太可能使用我们的候选药物,除非提供保险并且报销足以支付我们候选药物的很大一部分费用。与新批准的产品的保险范围和报销相关的不确定性很大。 目前很难预测第三方付款人将就我们的候选药物的承保范围和报销做出什么决定。
| 31 |
此外,美国和海外的政府和第三方付款人加大力度限制或降低医疗成本,可能会导致此类组织限制新批准产品的承保范围和报销水平,因此,他们可能无法为我们的候选药物 承保或提供足够的付款。由于 管理型医疗保健的趋势、医疗保健组织的影响力越来越大、成本控制举措和额外的立法变化,我们预计将面临与销售我们的任何候选药物相关的定价压力。
我们打算寻求批准在美国和选定的外国司法管辖区销售我们的候选药物 。如果我们的候选药物在一个或多个外国司法管辖区获得批准,我们将受到这些司法管辖区的规章制度的约束。在国外,药品 产品的定价受到政府管制和其他市场监管,这可能会对我们候选药品的定价和使用造成压力。 在这些国家/地区,在获得候选药物的上市批准后,与政府当局进行定价谈判可能需要相当长的时间。此外,我们候选药物的市场接受度和销量将在很大程度上取决于我们候选药物是否有足够的承保范围和第三方付款人的报销,并可能受到现有和未来医疗改革措施的影响 。如果我们的候选药物未能获得或保持足够的承保范围和报销,如果获得批准,可能会限制我们营销这些产品的能力,并降低我们创造收入的能力。
我们可能会使用我们的财务和人力资源 来追求特定的研究计划或候选药物,而无法利用可能更有利可图的计划或候选药物 或其成功的可能性更大。
由于我们的资源有限,我们可能会放弃 或推迟对某些计划、候选药物或后来证明具有更大商业潜力的适应症的机会的追求。我们的资源分配决策可能会导致我们无法利用可行的商业产品或有利可图的市场机会。 我们在候选药物当前和未来研发计划上的支出可能不会产生任何商业可行的产品。 如果我们没有准确评估特定候选药物的商业潜力或目标市场,我们可能会通过战略合作、许可或其他版税安排放弃对该候选药物有价值的 权利,而在这种情况下, 我们保留对该候选药物的独家开发和商业化权利会更有利,或者,我们可能会将内部 资源分配给某个治疗领域的候选药物,在该领域达成合作安排会更有利。 未能寻求具有更大商业潜力的机会或放弃候选药物的宝贵权利可能会对我们的业务、运营结果和前景产生不利影响。
我们可能无法成功识别或发现其他药品。
我们业务的成功主要取决于我们识别和开发医药产品的能力。由于多种原因,我们的研究计划可能无法确定用于临床开发的潜在药物 。我们的研究方法可能无法成功识别潜在的药品 ,或者我们的潜在的药品可能被证明具有有害的副作用,或者可能具有可能使产品无法销售或不太可能获得上市批准的其他特征。
如果发生上述任何事件,我们可能会被迫 放弃为一个或多个计划所做的开发工作,这将对我们的业务产生重大不利影响,并可能导致我们停止运营。识别新医药产品的研究项目需要大量的技术、财政和人力资源。我们可能会将我们的努力和资源集中在最终被证明不成功的潜在计划或药品上。 如果我们未能成功识别或发现其他药品,可能会对我们的业务、运营结果和前景产生不利影响。
| 32 |
我们的候选药物的市场机会可能仅限于那些没有资格接受或未能通过先前治疗的患者,而且可能很小。
癌症疗法有时被划分为一线、二线或三线,FDA通常最初只批准三线使用的新疗法。当癌症被发现得足够早时,一线治疗有时足以治愈癌症或延长生命,而不需要治愈。当一线治疗(通常包括化疗、激素治疗、手术或这些疗法的组合)被证明不成功时,可能会实施二线治疗。二线治疗通常包括更多的化疗、放射、抗体药物、肿瘤靶向小分子或这些药物的组合。三线治疗可以包括骨髓移植、抗体和小分子靶向治疗、更具侵入性的手术形式和新技术。在已批准治疗的市场上,我们预计最初将寻求批准我们的候选药物 作为对其他批准治疗失败的患者的后期治疗。随后,对于那些被证明是足够有益的药物(如果有的话),我们预计将寻求批准作为二线疗法和潜在的一线疗法,但不能保证我们的候选药物即使获得批准,也会被批准用于二线或一线疗法。此外,在获得二线或一线治疗的批准之前,我们可能需要进行额外的临床试验。
我们对患有我们要瞄准的癌症的人数,以及能够接受后期治疗的这些癌症患者的子集以及 有可能从我们的候选药物治疗中受益的人数的预测,都是基于我们的信念和估计。这些估计 来自各种来源,包括科学文献、诊所调查、患者基金会或市场研究, 可能被证明是不正确的。此外,新的研究可能会改变这些癌症的估计发病率或流行率。患者数量 可能会低于预期。此外,我们候选药物的潜在可寻址患者群体可能有限 ,或者可能无法接受我们候选药物的治疗。即使我们的候选药物获得了相当大的市场份额,如果没有获得监管部门对其他适应症的批准,我们可能永远无法实现盈利,包括用作一线或二线治疗 ,这可能会对我们的业务和运营结果产生不利影响。
临床试验可能无法证明我们候选药物的安全性和有效性,并可能阻止或显著推迟监管审批。
在获得NDA或BLA批准将候选药物商业化之前,我们必须通过严格控制的临床试验向FDA证明候选药物 既安全又有效,或者生物是安全、纯净和有效的。如果这些试验或未来的临床试验不成功,我们的业务和声誉可能会受到损害,我们的股票价格可能会受到不利影响。
临床失败可能发生在临床发展的任何阶段。临床试验可能会产生阴性或不确定的结果,我们或我们当前和未来的任何合作者可能会决定或监管机构可能要求我们进行额外的临床或临床前测试。我们将被要求通过严格控制的临床试验,用大量的 证据证明我们的候选药物在特定患者群体中的使用与各自的参考产品一样安全有效 ,然后我们才能寻求监管机构批准其商业销售。早期临床试验的成功 并不意味着未来更大规模的注册临床试验将会成功,因为后期临床试验的候选药物可能无法证明同等的安全性和有效性,令FDA和外国监管机构满意,尽管在初步临床试验中取得了进展 。在早期临床试验中显示出有希望的结果的候选药物仍可能在随后的验证性临床试验中失败。同样,临床前试验和早期临床试验的结果可能不能预测后续临床试验的成功,临床试验的中期结果也不一定能预测最终结果。制药行业的许多公司,包括那些拥有比我们更多的资源和经验的公司,在高级临床试验中遭遇了重大挫折,即使在早期的临床试验中取得了令人振奋的结果。
此外,临床试验的设计可以 确定其结果是否支持产品的批准,而临床试验设计中的缺陷可能在临床试验进展良好之前不会变得明显 。我们可能无法设计和执行临床试验来支持监管部门的批准。在 某些情况下,由于许多因素,同一候选药物的不同试验之间的安全性或有效性结果可能存在显著差异,这些因素包括但不限于试验方案的变化、患者群体的大小和类型的差异、对给药方案的坚持以及临床试验参与者的辍学率。
由于这些风险,我们的研发努力以及我们合作伙伴的努力可能不会产生任何商业上可行的产品。如果这些 开发工作的很大一部分没有成功完成,或者我们或我们的合作伙伴没有获得所需的监管批准,或者任何 批准的产品在商业上没有成功,我们可能不会产生显著的收入或盈利。
| 33 |
我们可能无法从FDA为我们的候选药物获得孤立药物指定 ,即使我们获得了此类指定,我们也可能无法保持与 孤立药物指定相关的好处,包括潜在的市场排他性。
根据《孤儿药品法》,FDA可以授予用于治疗罕见疾病或疾病的药物或生物的孤儿 药物名称,该药物或生物药物的定义是发生在美国患者人数 低于200,000人或美国患者人数超过200,000人,且没有合理的 期望通过在美国的销售收回药物或生物药物的开发成本。在美国,孤儿药物指定使一方有权获得财政激励,例如为临床试验费用提供赠款资金的机会、 税收优惠和用户费用减免。此外,如果具有孤儿药物指定的产品随后获得FDA针对其具有此类指定的疾病的第一个批准 ,则该产品有权获得孤儿药物独家经营权,这意味着FDA可能不会 批准任何其他申请,包括完整的NDA或BLA,在七年内销售相同的药物或生物制剂, 除非在有限的情况下,例如显示出相对于具有孤儿药物独占性的产品的临床优势,或者制造商 无法保证足够的产品数量。
我们可能寻求为我们的活性候选药物获得孤儿药物名称 ,以获得他们未来可能被批准的任何合格适应症。即使我们获得了这样的指定, 由于与开发药品相关的不确定性,我们可能不是第一个获得孤儿指定适应症的候选药物上市批准的公司。此外,如果我们 寻求批准比孤儿指定的适应症更广泛的适应症,则在美国的独家营销权可能会受到限制,或者如果FDA后来确定指定请求 存在重大缺陷,或者如果制造商无法保证足够数量的产品来满足这种罕见疾病或疾病患者的需求,则可能会失去独家营销权。此外,即使我们获得了产品的孤立药物排他性,这种排他性也可能无法 有效地保护该产品免受竞争,因为具有不同活性部分的不同药物可以被批准用于相同的 条件。即使在孤儿产品获得批准后,如果FDA得出结论认为后一种药物更安全、更有效或对患者护理有重大贡献,则FDA随后可以针对相同的情况批准具有相同活性部分的相同药物。孤儿 药物指定既不会缩短药物的开发时间或监管审查时间,也不会使该药物在监管审查或审批过程中具有任何优势。此外,即使我们为我们的候选药物寻求孤儿药物指定,我们也可能永远不会收到这样的指定。
医疗保健立法改革措施可能会对我们的业务和运营结果产生实质性的不利影响。
在美国和某些外国 司法管辖区,近年来有许多立法和监管法规以 方式改变了医疗保健系统,这可能会影响我们未来销售候选药物的盈利能力。
此外,联邦和州一级已经并将继续采取许多举措来寻求降低医疗成本。最重要的是,2010年3月,经《医疗保健和教育协调法案》(统称为《ACA》)修订的《患者保护和平价医疗法案》 被签署为法律,其中包括显著改变政府和私营保险公司为医疗保健融资的方式的措施。2017年1月,国会投票通过了2017财年预算决议,或预算决议,授权 实施废除ACA部分内容的立法。此外,2017年1月20日,前总裁·特朗普签署了一项行政命令,指示根据ACA拥有权力和责任的联邦机构放弃、推迟、授予豁免或推迟实施ACA中任何会给州、个人、医疗保健提供者、医疗保险公司或药品或医疗器械制造商带来财政或监管负担的条款。此外,2017年10月12日,前总裁·特朗普 发布了另一项行政命令,要求HHA以及劳工部和财政部的部长们考虑提出条例 或修改现有指导意见,以允许更多的雇主形成协会健康计划,允许其提供跨州保险,增加短期、有限期限的医疗保险计划的可用性,这些计划通常不受ACA的 要求的约束,并增加医疗报销安排的可用性和允许使用。2017年10月13日,司法部宣布,HHS立即停止向保险公司支付费用分摊减少付款,因为 确定这些付款没有被国会拨款。此外,2017年12月22日,前总裁·特朗普 签署了《减税和就业法案》(TCJA),使之成为法律,除了彻底改革联邦税收制度外,还从2019年1月1日起废除了与个人强制令相关的处罚。国会或美国的总裁也可以考虑随后的立法或行政行动,以取代、消除或重申ACA的内容。我们将继续评估ACA和任何未来修改、废除、取代或重申ACA的措施对我们业务的影响。
| 34 |
此外,2022年的通胀降低法案可能会影响涵盖处方药的现有医疗保险计划。除其他相关条款外,2022年的《降低通货膨胀法案》允许联邦医疗保险计划通过设定某些“最高公平价格”,分别从2028年和2026年开始,直接协商联邦医疗保险B部分和D部分涵盖的某些高支出处方药的价格。此外,2022年的《减少通货膨胀法案》要求,如果联邦医疗保险计划涵盖的某些药品的价格上涨速度快于通货膨胀率,制造商必须向联邦政府支付回扣。我们将继续评估2022年《降低通货膨胀法案》对我们业务的影响。
我们不能保证 持续的医疗改革辩论不会导致美国总裁的立法、法规、诉讼或行政行动对我们的业务不利。
未来可能提出和通过的法律及其他改革和成本控制措施 仍不确定,但可能包含限制我们为产品定价的能力的条款 和/或可能导致联邦医疗保险和其他医疗保健资金的进一步减少,这可能会对我们未来的客户以及我们创造收入、实现盈利或产品商业化的能力产生实质性的不利影响。
与我们对第三方的依赖相关的风险
我们可能会寻求建立更多的合作关系 ,如果我们不能以合理的商业条款建立合作关系,我们可能不得不改变我们的开发和商业化计划 。
我们的候选药物开发计划和候选药物的潜在商业化将需要大量额外的现金来支付费用。对于我们的一些候选药物, 我们可能会决定与其他制药和生物技术公司合作,开发这些候选药物并进行潜在的商业化 。
我们在寻找合适的合作伙伴方面面临着激烈的竞争。我们是否就任何其他协作达成最终协议将取决于我们对协作者的资源和专业知识的评估 、提议协作的条款和条件以及提议的协作者对许多因素的评估。这些因素可能包括临床试验的设计或结果、FDA或美国境外类似监管机构批准的可能性、候选药物的潜在市场、 制造候选药物并将其交付给患者的成本和复杂性、竞争药物的潜力、我们对技术所有权 存在的不确定性(如果在不考虑挑战的是非曲直的情况下对所有权提出挑战) 以及总体行业和市场状况。合作者还可以考虑可供合作的类似 适应症的替代候选药物或技术,以及此类合作是否会比我们与我们的候选药物合作更具吸引力。我们可能建立的任何其他合作或其他安排的条款可能对我们不利。
根据现有的协作协议,我们还可能受到限制,不能与潜在的协作者就某些条款签订未来的协议。协商和记录协作既复杂又耗时 。此外,大型制药公司之间最近发生了大量业务合并,导致未来潜在合作伙伴的数量减少。
我们可能无法以可接受的条款及时协商更多协作 ,或者根本无法协商。如果我们无法做到这一点,我们可能不得不削减我们正在寻求合作的候选药物的开发,减少或推迟其开发计划或我们的一个或多个其他开发计划,推迟 其潜在的商业化或缩小任何销售或营销活动的范围,或增加我们的支出并自费进行开发 或商业化活动。如果我们选择增加我们的支出来为开发或商业化活动提供资金 我们可能需要获得额外的资本,这些资本可能无法以可接受的条款提供给我们,或者根本无法获得。如果我们 没有足够的资金,我们可能无法进一步开发我们的候选药物或将其推向市场并产生产品收入。
| 35 |
如果我们与我们的合作者或战略合作伙伴之间出现冲突,这些各方可能会根据他们的自身利益行事,这可能会限制我们实施我们战略的能力。
如果我们的公司或学术合作伙伴或战略合作伙伴与我们发生冲突,对方可能会出于自身利益行事,这可能会限制我们实施我们的 战略的能力。我们的一些学术合作者和战略合作伙伴正在与我们合作的每个 领域进行多项产品开发工作。但是,我们的合作者或战略合作伙伴可能会单独或与其他人一起开发相关领域的产品,这些产品与这些合作的主题产品或潜在产品具有竞争力。 由合作者或战略合作伙伴开发的竞争产品,或者合作者或战略合作伙伴拥有 权利的竞争产品,可能会导致合作伙伴撤回对我们的候选药物的支持。
我们的一些合作者或战略合作伙伴 未来也可能成为我们的竞争对手。我们的合作者或战略合作伙伴可能开发竞争产品、阻止我们 与其竞争对手合作、未能及时获得监管批准、过早终止与我们的协议,或未能投入足够的资源用于产品的开发和商业化。这些发展中的任何一项都可能损害我们的产品开发努力,这可能会对我们的业务、运营结果和前景产生不利影响。
我们希望依靠第三方进行、监督和监督我们的临床研究,如果这些第三方的表现不令人满意,可能会损害我们的业务。
我们依赖CRO、临床研究人员和临床研究站点来确保我们的临床研究正确和及时地进行。我们将对CRO、临床研究人员和临床研究站点的绩效产生有限的影响,并且我们将仅控制我们CRO活动的某些方面。然而, 我们将负责确保我们的每项临床研究都是按照适用的协议、法律和 监管要求和科学标准进行的,我们对CRO的依赖不会免除我们的监管责任。 此外,这些第三方CRO、临床研究人员和临床研究地点使用的设施可能会受到 灾难性事件的负面影响,例如流行病,包括正在进行的新冠肺炎大流行、恐怖袭击、战争或其他武装冲突、地缘政治紧张局势,如俄罗斯和乌克兰之间持续的冲突以及相关的制裁和其他经济中断或担忧, 洪水或火灾等自然灾害或此类设施可能面临制造问题,例如在对此类设施进行监管检查后出现污染或监管问题。在这种情况下,我们可能需要找到合适的替代第三方设施并 建立合同关系,这可能不是现成的或按可接受的条款,这将导致额外的延迟和 增加的费用,包括额外所需的FDA批准的结果,并可能对我们的业务产生实质性的不利影响。
我们、我们的临床研究人员和我们的CRO 必须遵守FDA进行、记录和报告临床试验结果的GCP,以确保 数据和报告的结果是可信和准确的,并保护临床试验参与者的权利、完整性和机密性 。FDA通过对研究赞助商、主要研究人员和临床试验地点的定期检查来执行这些GCP。如果我们、我们的CRO或临床研究人员未能遵守适用的GCP,在我们的临床试验中生成的临床数据可能被认为是不可靠的,FDA可能会要求我们在批准任何上市申请之前进行额外的临床试验。 在检查后,FDA可能会确定我们的临床试验不符合GCP。此外,我们未来的临床试验将需要足够数量的测试对象来评估我们候选药物的安全性和有效性。因此,如果我们的CRO或临床调查人员未能遵守这些规定或未能招募足够数量的患者,我们可能会被要求重复此类 临床试验,这将推迟监管批准过程。
我们的CRO不是我们的员工,因此我们无法直接监控他们是否为我们的临床和非临床项目投入了足够的时间和资源,这些项目必须 分别按照GCP和GLP进行。这些CRO还可能与其他商业实体有关系,包括我们的竞争对手,他们可能还在为这些实体进行临床研究或其他药物开发活动,这可能会损害我们的竞争地位。如果我们的CRO未能成功履行其合同职责或义务,未能在预期期限内完成,或者由于未能遵守我们的临床方案或法规要求 (或任何其他原因)而导致他们获得的临床数据的质量或准确性受到影响,我们的临床研究可能会被延长、推迟或终止,我们可能无法获得监管部门对我们的药品的批准 ,或无法成功地将其商业化。因此,我们的财务业绩和药品的商业前景将受到损害,我们的成本可能会增加,我们的创收能力可能会被推迟。
我们还可能依赖其他第三方为我们可能进行的任何临床研究存储和分发我们的产品。如果我们的经销商出现任何业绩失误,都可能 推迟我们药品的临床开发或营销批准,或者如果获得批准,我们的产品将被商业化,从而造成额外的损失,并剥夺我们潜在的产品收入。
| 36 |
我们的合作者或战略合作伙伴 可能决定采用替代技术,或者可能无法使用我们的技术开发具有商业可行性的产品,这将对我们的收入和我们开发这些产品的战略产生负面影响。
我们的协作者或战略合作伙伴可能会采用 替代技术,这可能会降低我们产品的适销性。此外,由于我们当前或未来的合作者 或战略合作伙伴可能从事多个开发项目,他们可以选择将其资源转移到他们正在与我们合作的项目以外的项目 。如果他们这样做,这将推迟我们测试我们技术的能力,并将推迟或终止基于我们平台的潜在产品的开发。此外,我们的协作者和战略合作伙伴可以选择不开发由我们的协作和战略合作安排产生的产品,或者将足够的资源投入到这些产品的开发、制造、营销或销售中。如果未能根据我们与当前或未来合作伙伴的协议 开发候选药物并将其商业化,我们将无法获得未来的里程碑和特许权使用费付款,这将对我们的收入产生负面影响。
如果我们达成一项或多项合作, 我们可能被要求放弃对我们的候选药物开发的重要权利和控制权,或者受到 不利条款的约束。
我们未来进行的任何合作都可能 使我们面临许多风险,包括:
| · | 我们可能无法控制我们的合作者投入到我们候选药物的开发或商业化的资源的数量和时机; | |
| · | 合作者可以推迟临床试验,提供不足的资金,终止临床试验或放弃候选药物,重复或进行新的临床试验,或要求新版本的候选药物进行临床测试; | |
| · | 合作者不得对战略合作安排所产生的产品进行进一步的开发和商业化,或者可以选择停止研发计划; | |
| · | 合作者可能没有投入足够的资源来营销和分销我们的候选药物,从而限制了我们从这些产品中获得的潜在收入; | |
| · | 我们和我们的合作者之间可能会发生纠纷,导致我们候选药物的研究、开发或商业化的延迟或终止,或者导致昂贵的诉讼或仲裁,分散管理层的注意力并消耗资源; | |
| · | 合作者可能会遇到财务困难; | |
| · | 合作者可能无法正确维护或捍卫我们的知识产权,或可能以可能危及或使我们的专有信息无效或使我们面临潜在诉讼的方式使用我们的专有信息; | |
| · | 业务合并或协作者业务战略的重大变化也可能对协作者在任何安排下履行其义务的意愿或能力产生不利影响; | |
| · | 合作者可以决定独立或与包括我们的竞争对手在内的其他人合作开发竞争对手的候选药物;以及 | |
| · | 合作者可以终止该协议或允许其到期,这将推迟开发并可能增加我们候选药物的开发成本。 |
| 37 |
我们没有制造、销售、营销或分销能力,我们可能需要投入大量资源来开发这些能力。
我们没有内部制造能力。 因此,在制造方面,我们依赖第三方制造商。我们的战略基于利用合作伙伴的能力来开发和制造我们的产品,以便在制药市场上实现商业化,我们将依赖于与药物开发和制造合作者的合作。如果我们无法维持现有的协作安排或以商业上可接受的条款建立新的安排,我们将被要求进行产品制造和开发活动,费用由我们自己承担。这将增加我们的资本要求或要求我们限制开发活动的范围。 此外,我们在进行全面生物等效性或其他临床研究、准备和提交监管申请以及分销和营销药品方面经验有限或没有经验。因此,我们依赖合同方进行此类工作。 我们可能无法在可接受的财务条款下进行协作或聘请顾问或外部服务提供商来协助我们进行销售、市场营销和 分销职能。
如果我们的任何开发合作伙伴违反 协议或终止与我们的协议,或未能及时开展其合作活动,我们的药物产品的临床前和/或临床开发和/或商业化将被推迟,我们将被要求投入 额外资源用于产品开发和商业化或终止某些开发计划。此外,许可关系 可由我们的协作者自行决定终止,或在合同条款结束时终止,在某些情况下仅向我们发出有限的通知。终止合作安排可能会对我们的业务、财务状况和运营结果产生重大不利影响 。也不能保证不会在与第三方开发的任何技术的所有权方面产生争议。与合作者之间的这些和其他可能的分歧可能会导致我们药品的开发或商业化的延迟 ,或者可能导致诉讼或仲裁,这可能既耗时又昂贵,并可能对我们的业务、财务状况和运营结果产生重大不利影响。即使我们决定自己执行临床试验、销售、营销和分销职能,我们也可能面临一些额外的相关风险,包括:
| · | 我们可能无法吸引临床研究人员,无法建立有效的临床试验,也无法建立坚实的营销部门或销售队伍; | |
| · | 建立内部临床试验计划、市场营销部门或销售队伍的成本可能超过我们可用的财务资源,以及我们当前的任何候选产品(如果获得批准)或我们可能开发、许可或收购的任何其他药品所产生的收入;以及 | |
| · | 我们的直销和营销努力可能不会成功。 |
任何未能开展此类活动的行为都可能对我们的业务、财务状况和运营结果产生重大不利影响。
我们对第三方的依赖要求我们 共享我们的商业秘密,这增加了竞争对手发现这些秘密或我们的商业秘密被盗用或披露的可能性。
因为我们依赖第三方生产我们的医药产品,而且我们与各种组织和学术机构合作开发我们的医药产品,所以我们有时必须与他们分享商业秘密。我们寻求通过在开始研究或披露专有信息之前与我们的合作者、顾问、员工和顾问签订保密协议、材料转让协议、合作研究协议、咨询协议或其他类似协议来部分保护我们的专有技术。这些协议通常限制第三方使用或披露我们的机密信息的权利,例如 商业秘密。在与第三方合作时需要共享商业秘密和其他机密信息,这会增加 此类商业秘密被我们的竞争对手知晓、被无意中纳入其他人的技术或被披露或使用违反这些协议的风险。鉴于我们的专有地位在一定程度上基于我们的专有技术和商业秘密,竞争对手发现我们的商业秘密或其他未经授权的使用或披露将损害我们的竞争地位,并可能对我们的业务产生实质性的不利影响 。
| 38 |
此外,这些协议通常会限制我们的合作者、顾问、员工和顾问发布可能与我们的商业秘密相关的数据的能力。我们的学术 合作者通常有权发布数据,前提是提前通知我们,并可能将发布推迟指定的 时间,以保护我们因合作而产生的知识产权。在其他情况下,出版权由我们独家控制,尽管在某些情况下,我们可能会与其他各方共享这些权利。我们还可能进行联合研发计划,这些计划可能要求我们根据我们的研发合作伙伴或类似协议的条款共享商业秘密。 我们的竞争对手可能会通过违反这些协议、独立开发或发布包括我们的商业秘密在内的信息来发现我们的商业秘密 在发布时我们没有所有权或其他受保护的权利。竞争对手发现我们的商业秘密将损害我们的竞争地位,并对我们的业务产生不利影响。
我们的合同制造商在生产我们的产品时受到 严格的监管。我们所依赖的制造设施可能无法继续满足监管要求,并且产能有限。
我们目前与数量有限的 家供应商建立了生产我们的药品的关系。每个供应商可能需要许可证才能制造组件 如果此类流程不属于供应商或在公共领域内,并且我们可能无法转让或再许可我们可能拥有的与此类活动相关的知识产权 。
所有参与制备用于临床研究或商业销售的药物 产品的实体,包括我们现有的候选药物合同制造商,都受到广泛的监管。经批准用于商业销售或用于晚期临床研究的成品药品的成分必须按照cGMP生产。本规定管理生产过程和程序(包括记录保存) 以及质量体系的实施和运行,以控制和确保调查产品和批准销售的产品的质量 。对生产过程的不良控制可能会导致引入外来制剂或其他污染物,或在无意中 改变我们的药品的性能或稳定性,这些变化在最终产品测试中可能无法检测到。我们的合同 制造商必须及时提供支持NDA或BLA的所有必要文件,并必须遵守FDA通过其设施检查计划执行的GLP和cGMP规定。我们的部分或所有第三方承包商的设施和质量体系必须通过审批前检查,以符合适用的法规,作为监管部门批准我们的医药产品或任何其他潜在产品的条件。此外,监管当局可随时审核或检查与我们的医药产品或其他潜在产品或相关质量体系的制备有关的制造设施是否符合适用于正在进行的活动的法规。如果这些设施没有通过预先批准的工厂检查,FDA将不会批准该产品。
监管机构还可以在批准销售产品后的任何时间对我们的第三方承包商的制造设施进行审计。如果任何此类检查或 审核发现不符合适用法规,或者如果违反我们的产品规格或适用法规的行为是独立于此类检查或审核而发生的,我们或相关监管机构可能会要求我们或相关监管机构采取补救措施,这些措施对于我们或第三方来说可能是昂贵和/或耗时的,可能包括暂时或永久暂停临床 研究或商业销售,或暂时或永久关闭设施。对与我们签订合同的第三方实施的任何此类补救措施都可能对我们的业务造成实质性损害。
如果我们的第三方制造商未能保持监管合规性,FDA可以实施监管制裁,其中包括拒绝批准待处理的候选药物申请或撤销先前存在的批准。因此,我们的业务、财务状况和运营结果可能受到实质性损害 。
此外,如果一家经批准的制造商的供应中断 ,商业供应可能会严重中断。具备必要制造能力的制造商数量有限。此外,替代制造商需要通过NDA或BLA补充获得资格,这可能会导致进一步的延迟。如果依赖新的制造商进行商业生产,监管机构可能还需要进行额外的研究。更换制造商可能涉及大量成本,并可能导致我们所需的临床和商业时间表的延迟,这可能会对我们的业务和运营结果造成实质性损害。
| 39 |
这些因素可能导致我们药品的临床研究、监管提交、所需审批或商业化的延迟,和/或导致我们产生更高的 成本,阻碍我们的产品成功商业化。此外,如果我们的供应商未能满足合同要求, 并且我们无法获得一个或多个能够以基本相同的成本生产的替代供应商,我们的临床研究可能会延迟,或者我们可能会损失潜在的收入,这可能会对我们的业务和运营结果造成实质性的损害。
与我们的知识产权有关的风险
如果我们不能充分保护或执行我们的知识产权,我们可能无法有效运作。
我们的成功和竞争能力在很大程度上取决于我们的专利、专有配方和商标。不能保证我们的专利及相关商标和许可证不会受到挑战,并随后失效和/或取消。任何一个或全部专利或商标的无效或取消将严重损害我们的商业前景。此外,我们可能会发现有必要在法律上挑战侵犯我们的专利或商标或许可商标的各方,以加强我们的权利。不能保证任何 专利最终有效,也不能保证保护任何专利、商业秘密、专有技术或其他知识产权的努力会成功 。
像我们这样的制药和生物技术公司的专利地位是不确定的,涉及复杂的法律和事实问题。我们拥有众多美国和外国专利,以及多项正在申请的专利申请,涵盖了我们的候选药物和技术的各个方面。不能保证已颁发的专利 将在法庭上保持有效和可强制执行。即使对于被认定为有效和可强制执行的专利,与获得此类判决相关的法律程序也是耗时和昂贵的。此外,已颁发的专利可能会遭到反对或其他程序,这些程序可能会导致专利被撤销或以修改后的形式(以及可能以使专利不具有商业相关性和/或广泛覆盖范围的形式)得到维护。此外,我们的竞争对手可能能够绕过 ,或者绕过我们的专利进行设计。即使颁发了专利并可强制执行,因为制药产品的开发和商业化可能会受到很大的延迟,但专利可能会提前到期,并且在我们的专利所涵盖的产品商业化之后,如果有的话,也只能提供很短的保护期。我们可能不得不参与美国专利商标局宣布的干预程序,这可能会导致专利损失和/或给我们带来巨额成本。
我们已经提交了专利申请,并计划 提交更多的专利申请,涵盖我们候选药物和技术的各个方面。不能保证我们申请的专利申请真的会作为专利颁发,或者这样做具有商业相关性和/或广泛的覆盖面。 在专利颁发之前,专利申请中要求的覆盖面可以显著减少。索赔范围 对于我们与第三方达成许可交易的能力以及从我们的合作伙伴关系中获得版税的权利至关重要 。由于科学或专利文献中发现的发布往往滞后于此类发现的日期,因此我们无法 确定我们是我们的专利或专利申请所涵盖的发明的第一个发明者。此外,不能保证我们将是第一个提交针对某项发明的专利申请的公司。
在任何涉及知识产权(包括专利)的司法程序中出现不利结果,可能会使我们对第三方承担重大责任,需要从第三方或向第三方获得有争议的权利许可 ,或者要求我们停止使用有争议的技术。在我们向他人寻求知识产权许可的情况下, 我们可能无法在商业合理的基础上获得许可,从而引发对我们将我们的技术和/或产品自由商业化的能力的担忧。我们或我们的许可人或被许可人也可能无法识别在开发和商业化活动过程中产生的发明的可专利方面 ,否则将无法获得专利保护 。此外,在某些情况下,我们可能无权控制专利申请的准备、提交和起诉 (或维护专利),这些专利涵盖我们从第三方许可或许可给第三方的技术。我们依赖我们的许可方或 被许可方。因此,不得以符合我们业务最佳利益的方式起诉和强制执行这些专利和申请 。如果我们当前或未来的许可方或被许可方未能建立、维护或保护此类专利和其他知识产权,则此类权利可能会减少或取消。如果我们的许可人或被许可人在起诉、维护或强制执行任何专利权方面不完全合作或不同意我们的意见 ,此类专利权可能会受到损害。
如果不能充分保护或执行我们的知识产权 可能会对我们的业务、运营结果和前景产生重大不利影响。
| 40 |
适用于我们候选药物的已颁发专利 如果在法庭上受到质疑,可能会被认定为无效或不可执行。
如果我们或我们的许可合作伙伴之一对第三方提起法律诉讼,以强制执行覆盖我们的候选药物之一的专利,被告可以反诉 覆盖我们候选药物的专利无效和/或不可执行。在美国的专利诉讼中,被告声称无效和/或不可执行的反诉是司空见惯的。质疑有效性的理由可能是据称未能满足几个法定要求中的任何 ,包括缺乏新颖性、明显或无法实施。不可执行性断言的理由 可能是与专利起诉有关的人在起诉期间向美国专利商标局隐瞒相关信息或做出误导性声明的指控。第三方也可以向美国或国外的行政机构提出类似的索赔, 即使在诉讼范围之外也是如此。这类机制包括在外国司法管辖区的复审、赠款后审查和同等程序(例如,反对程序)。此类诉讼可能会导致我们的专利被撤销或修改,导致 这些专利不再涵盖我们的候选药物。法律断言无效和不可强制执行后的结果是不可预测的。 例如,关于有效性问题,我们不能确定没有无效的先前技术,而我们和专利审查员在起诉期间并不知道。如果被告以无效和/或不可执行的法律主张获胜, 我们将失去对候选药物的至少部分甚至全部专利保护。这种专利保护的丧失将对我们的业务产生实质性的不利影响。
我们可能无法在全球范围内保护我们的知识产权。
在全球所有国家/地区申请、起诉和保护候选药物专利的费用将高得令人望而却步,而且我们在美国以外的一些国家/地区的知识产权可能没有美国的知识产权那么广泛。此外,一些国家的法律对知识产权的保护程度不及美国的联邦和州法律。因此,我们可能无法 阻止第三方在美国以外的所有国家/地区实施我们的发明,或在美国或其他司法管辖区销售或进口使用我们的发明制造的产品。竞争对手可以在我们没有获得专利保护的司法管辖区使用我们的发明来开发自己的产品,此外,还可以将其他侵权产品出口到我们有专利保护但执法力度不如美国的地区 。这些产品可能会与我们的产品竞争,而我们的专利或其他知识产权可能无法有效或不足以阻止它们竞争。
许多公司在外国司法管辖区保护和捍卫知识产权方面遇到了重大问题 。某些国家的法律制度,特别是某些发展中国家的法律制度,不支持专利、商业秘密和其他知识产权保护的执行,尤其是与生物技术产品有关的保护,这可能使我们很难阻止侵犯我们的专利或销售 违反我们专有权的竞争产品。在外国司法管辖区强制执行我们的专利权的诉讼程序可能会导致巨额成本,并将我们的努力和注意力从我们业务的其他方面转移出去,可能会使我们的专利面临被无效或狭隘解释的风险,可能会使我们的专利申请面临无法颁发的风险,并可能引发第三方 对我们提出索赔。我们可能不会在我们发起的任何诉讼中获胜,而且如果有任何损害赔偿或其他补救措施, 可能没有商业意义。因此,我们在世界各地执行知识产权的努力可能不足以 从我们开发或许可的知识产权中获得显著的商业优势。
如果不能充分保护我们在世界各地的知识产权,可能会对我们的业务、运营结果和前景产生重大不利影响。
如果我们侵犯他人的知识产权 ,我们的业务和盈利能力可能会受到不利影响。
我们的商业成功还将在一定程度上取决于我们和我们的合作伙伴不侵犯他人的专利或专有权利。不能保证我们的合作伙伴使用或开发并由我们营销和销售的 技术和产品不会侵犯此类权利。如果发生此类侵权,并且我们和我们的合作伙伴都无法从相关第三方获得许可,则我们将 无法继续开发、制造、使用或销售任何此类侵权技术或产品。无法保证 是否提供第三方技术的必要许可证,或是否按商业上合理的条款提供许可证。在某些情况下,可能需要通过诉讼或其他程序来抗辩或主张侵权索赔,或确定第三方专有权利的范围和有效性。任何潜在的诉讼都可能导致我们的资源和资源的大量成本和转移, 可能会对我们产生实质性的不利影响。任何此类诉讼或诉讼中的不利结果可能会使我们承担重大责任,要求我们停止使用主题技术,或要求我们从第三方获得主题技术的许可,所有这些 都可能对我们的业务产生重大不利影响。
| 41 |
如果我们未能履行我们向第三方许可知识产权的协议中的义务 ,或者我们与许可方的业务关系中断 ,我们可能会失去对我们的业务非常重要的许可权。
我们是许多对我们的业务非常重要的知识产权许可协议的参与方,我们希望在未来签订更多许可协议。我们现有的 许可协议规定,我们预计未来的许可协议将对我们施加各种尽职调查、里程碑付款、版税和 其他义务。如果我们未能履行我们在这些协议下的义务,或者我们处于破产状态,许可方 可能有权终止许可,在这种情况下,我们将无法销售许可涵盖的产品。
我们可能需要从第三方获得许可证 以推进我们的研究,我们不时地这样做。我们可能无法以合理的成本或 合理的条款获得任何这些许可证(如果有的话)。在这种情况下,我们可能需要花费大量时间和资源来开发或许可替代技术 。如果我们无法做到这一点,我们可能无法开发受影响的候选药物,这可能会严重损害我们的业务。 我们不能保证不存在可能对我们当前的候选药物或未来产品强制执行的第三方专利,从而导致禁止销售,或者对于销售,我们有义务向第三方支付版税和/或其他形式的赔偿。
在许多情况下,我们许可的技术的专利诉讼完全由许可方控制。如果我们的许可方未能从他们那里获得并维护我们许可的专有 知识产权的专利或其他保护,我们可能会失去对知识产权的权利或与这些权利有关的专有权,而我们的竞争对手可以使用知识产权营销竞争产品。在某些情况下,我们控制由许可技术产生的专利的起诉。如果我们违反与此类起诉相关的任何义务,我们可能会对我们的许可合作伙伴承担重大责任。知识产权许可对我们的业务至关重要,涉及复杂的法律、商业和科学问题,并因我们行业科学发现的快速发展而变得复杂。根据许可协议,可能会在知识产权方面产生争议,包括:
| · | 根据许可协议授予的权利范围和其他与解释有关的问题; | |
| · | 我们的技术和工艺在多大程度上侵犯了不受许可协议约束的许可方的知识产权; | |
| · | 根据我们的合作开发关系,对专利和其他权利进行再许可; | |
| · | 我们在许可协议下的尽职义务,以及哪些活动满足这些尽职义务; | |
| · | 由我们的许可人、我们和我们的合作伙伴共同创造或使用知识产权而产生的发明和专有技术的所有权;以及 | |
| · | 专利技术发明的优先权。 |
如果我们 许可的知识产权纠纷阻碍或削弱了我们以可接受的条款维持当前许可安排的能力,我们可能无法成功 开发受影响的候选药物并将其商业化,这可能会对我们的业务产生重大不利影响。
我们可能会受到以下指控的影响:我们的员工、顾问或独立承包商错误地使用或披露了第三方的机密信息,或者我们的员工 错误地使用或披露了其前雇主声称的商业机密。
我们雇用的个人以前曾受雇于大学或其他生物技术或制药公司,包括我们的竞争对手或潜在竞争对手。我们可能会 被指我们或我们的员工、顾问或独立承包商无意中或以其他方式使用或泄露了我们员工的任何前雇主或其他第三方的知识产权,包括商业秘密或其他专有信息。 可能需要提起诉讼来抗辩这些索赔。如果我们未能为任何此类索赔辩护,除了支付金钱损失外, 我们可能会失去宝贵的知识产权或人员,这可能会对我们的业务造成不利影响。即使我们成功地对此类索赔进行了辩护,诉讼也可能导致巨额成本,并分散管理层和其他员工的注意力。
| 42 |
我们可能会受到质疑我们专利和其他知识产权的发明权或所有权的索赔。
我们还可能受到前员工、合作者或其他第三方对我们的专利或其他知识产权拥有所有权权益的索赔。我们未来可能会出现 所有权纠纷,例如,顾问或参与开发我们候选药物的其他人的义务冲突 。诉讼可能是必要的,以对抗这些和其他挑战库存或所有权的索赔。如果我们未能为任何此类索赔辩护,除了支付金钱损害赔偿外,我们还可能失去宝贵的知识产权,例如对宝贵知识产权的专有 所有权或使用权。这样的结果可能会对我们的业务产生实质性的不利影响。即使我们成功地对此类索赔进行了辩护,诉讼也可能导致巨额成本,并分散管理层和其他员工的注意力。
我们无法保护我们的机密信息和商业秘密,这将损害我们的业务和竞争地位。
除了为我们的一些技术和产品申请专利外,我们还依靠商业秘密,包括非专利的技术诀窍、技术和其他专有信息, 保持我们的竞争地位。我们寻求保护这些商业秘密,部分是通过与有权访问这些商业秘密的各方签订保密和保密协议,例如我们的员工、公司合作者、外部科学合作者、合同制造商、顾问、顾问和其他第三方。我们还与员工和顾问签订保密协议和发明或专利转让协议。这些各方中的任何一方都可能违反协议并泄露我们的专有信息,包括我们的商业秘密,我们可能无法就此类违规行为获得足够的补救措施。执行一方非法披露或挪用商业秘密的索赔是困难、昂贵和耗时的,结果是不可预测的。此外,美国国内外的一些法院可能不太愿意或不愿意保护商业秘密。如果竞争对手合法获取或独立开发了我们的任何商业秘密,我们将无权阻止该竞争对手使用该技术或信息与我们竞争,这可能会损害我们的竞争地位和业务。
我们可能会卷入保护 或强制执行我们的专利或我们许可方的专利的诉讼,这可能是昂贵、耗时和不成功的。
竞争对手可能会侵犯我们的专利或我们许可方的专利 。为了对抗侵权或未经授权的使用,我们可能会被要求提出侵权索赔,这可能是昂贵的 和耗时的。此外,在侵权诉讼中,法院可以裁定我们或我们的许可人的专利无效, 不可强制执行和/或未被侵权,或者可以以我们的专利不涵盖相关技术为理由拒绝阻止另一方使用相关技术。任何诉讼或辩护程序中的不利结果可能会使我们的一项或多项专利面临被无效或狭义解释的风险,并可能使我们的专利申请面临无法颁发的风险。
由第三方引发或由我们提起的干扰诉讼程序可能是必要的,以确定与我们的专利或专利申请或我们的许可人的那些专利或专利申请有关的发明的优先权。不利的结果可能要求我们停止使用相关技术或尝试从胜利方那里获得授权。如果胜利方不按商业上合理的条款向我们提供许可证,我们的业务可能会受到损害。我们的诉讼辩护或干预诉讼可能会失败,即使成功,也可能导致巨额成本,并分散我们的管理层和其他员工的注意力。我们可能无法单独或与我们的许可人一起防止盗用我们的知识产权 ,特别是在那些法律保护这些权利可能不如美国充分的国家。
此外,由于与知识产权诉讼相关的大量发现 ,我们的一些机密信息有可能在此类诉讼期间因披露而泄露。还可能公布听证结果、动议或其他临时程序或事态发展。如果证券分析师或投资者认为这些结果是负面的,可能会对我们普通股的价格产生实质性的不利影响。
| 43 |
美国专利法的变化可能会降低专利的整体价值,从而削弱我们保护产品的能力。
与其他生物制药公司一样,我们的成功在很大程度上依赖于知识产权,特别是专利。在生物技术行业获得和实施专利既涉及技术上的复杂性,也涉及法律上的复杂性,因此成本高、耗时长,而且本质上是不确定的。此外,美国已经制定并有望继续实施范围广泛的专利改革立法。此外,美国最高法院的某些裁决在某些情况下缩小了专利保护的范围,和/或在某些情况下削弱了专利所有者的权利。除了对我们未来获得专利的能力的不确定性增加之外,这种事件的组合 还造成了关于一旦获得专利的价值的不确定性。根据美国国会、联邦法院和USPTO的决定,管理专利的法律和法规可能会以不可预测的方式发生变化,从而削弱我们获得新专利或强制执行我们现有专利和未来可能获得的专利的能力。
专利改革立法可能会增加围绕起诉我们和我们许可方的专利申请以及执行或保护我们或我们的许可方颁发的专利的不确定性 和成本。2011年9月通过的《莱希-史密斯美国发明法》(《莱希-史密斯法案》)的条款对美国专利法进行了多项重大修改,其影响仍在显现。Leahy-Smith法案及其实施, 再加上任何新法规,可能会增加围绕我们专利申请的起诉以及我们已颁发专利的执行或保护的不确定性和成本,所有这些都可能对我们的业务和财务状况产生实质性的不利影响。
获得和维护我们的专利保护 取决于遵守政府专利机构施加的各种程序、文件提交、费用支付和其他要求,如果不符合这些要求,我们的专利保护可能会减少或取消。
专利和/或申请的定期维护费、续期费、年费和各种其他政府费用将在专利和/或申请的有效期内分几个阶段支付给USPTO和美国以外的各种政府专利机构。美国专利商标局和各种非美国政府专利代理机构要求在专利申请过程中遵守一些程序、文件、费用支付和其他类似条款。不遵守规定可能会导致专利或专利申请的放弃或失效,导致相关司法管辖区专利权的部分或全部丧失。在这种情况下,我们的竞争对手可能会进入市场, 这种情况将对我们的业务产生实质性的不利影响。
| 44 |
与我们的业务运营相关的风险
影响金融服务业的不利事态发展,例如涉及流动性、违约或金融机构或交易性交易对手违约的实际事件或担忧,可能会对公司当前和预计的业务运营及其财务状况和运营结果产生不利影响。
涉及流动性有限、违约、业绩不佳或其他不利发展的实际事件,影响金融机构、交易对手或金融服务业或整个金融服务业的其他公司,或对任何此类事件或其他类似风险的担忧或谣言,过去曾发生过,未来可能会导致整个市场的流动性问题。例如,2023年3月10日,硅谷银行(SVB)被加州金融保护和创新部关闭,后者指定联邦存款保险公司(FDIC)为接管人。同样,2023年3月12日,Signature Bank和Silvergate Capital Corp. 分别被卷入破产管理程序。尽管财政部、美联储和联邦存款保险公司的一份声明指出,SVB的所有储户在关闭仅一个营业日后即可提取其所有资金,包括无保险存款账户中的资金、信贷协议下的借款人、信贷协议下的借款人、信用证和某些其他金融工具、签名银行或被联邦存款保险公司接管的任何其他金融机构,但可能无法提取其中未提取的金额。我们 几乎所有现金都存放在SVB,其中大部分不会得到FDIC的保险,我们定期维护没有保险或超过FDIC保险限额的现金余额 。截至2023年3月13日,我们完全可以使用我们的资金。如果 无法使用我们的存款资金,可能会对我们的流动资金以及我们当前和/或预计的业务以及财务状况和运营结果产生重大不利影响。尽管我们不是SVB、签名或任何其他目前处于接管状态的金融机构的借款人或任何此类金融机构的一方,但如果我们的任何客户、供应商或与我们有业务往来的其他各方无法根据此类金融机构的此类工具或贷款安排获得资金, 这些各方向我们偿还债务或签订需要向我们支付额外款项的新商业安排的能力可能会受到不利影响。在这方面,SVB信贷协议和安排的交易对手以及信用证受益人等第三方可能会受到SVB关闭的直接影响,更广泛的金融服务业对流动性的担忧仍然存在不确定性。类似的影响过去也曾发生过,例如在2008-2010年金融危机期间。
通货膨胀和利率的快速上升导致以前发行的利率低于当前市场利率的政府债券的交易价值下降 。尽管美国财政部、联邦存款保险公司和联邦储备委员会已经宣布了一项计划,向以金融机构持有的某些此类政府证券为担保的金融机构提供高达250亿美元的贷款,以减轻此类工具销售的潜在损失风险,但金融机构对即时流动性的广泛需求或其他流动性需求可能会超出该计划的能力。此外,不能保证美国财政部、联邦存款保险公司和联邦储备委员会将来会在其他银行或金融机构关闭的情况下提供未投保资金的使用,也不能保证他们会及时这么做。
尽管我们评估我们的银行关系是必要或适当的,但我们获得资金来源和其他信贷安排的机会足以为我们当前和预计的未来业务运营提供资金或资本化 影响公司或整个金融服务业或整体经济的因素可能会严重损害我们的融资来源和其他信贷安排。这些因素可能包括流动性紧张或失败等事件, 根据各种金融、信贷或流动性协议或安排履行义务的能力,金融服务业或金融市场的中断或不稳定 ,或对金融服务业公司前景的担忧或负面预期。这些因素可能涉及与公司有财务或业务关系的金融机构或金融服务行业公司,但也可能包括涉及金融市场或金融服务行业的因素。
| 45 |
涉及 其中一个或多个因素的事件或问题的结果可能包括对我们当前和预计的业务运营以及我们的财务状况和运营结果产生的各种重大和不利影响。这些可能包括但不限于延迟获得存款或其他金融资产,或未投保的存款或其他金融资产的损失,或未投保的存款或其他金融资产的损失; 或终止现金管理安排和/或受现金管理安排约束的资金的延迟获取或实际损失。
投资者对美国或国际金融体系的担忧可能会导致不太有利的商业融资条款,包括更高的利率或成本以及更严格的财务和经营契约,或者对获得信贷和流动性来源的系统性限制,从而使我们更难以可接受的条款或根本不以可接受的条款获得融资。可用资金或现金和流动资金来源的任何减少,除其他风险外,可能会对我们履行运营费用、财务义务或履行其他义务的能力造成不利影响, 导致违反我们的财务和/或合同义务,或导致违反联邦或州工资和工时法。上述影响的任何 ,或上述因素或其他相关或类似因素导致的任何其他影响, 可能会对我们的流动资金、我们当前和/或预计的业务运营和财务状况以及 运营结果产生重大不利影响。
此外,宏观经济或金融服务业的任何进一步恶化都可能导致我们的客户或供应商亏损或违约,进而可能对我们当前和/或预期的业务运营以及运营结果和财务状况产生重大不利影响。例如,客户 可能在到期时无法付款、根据与我们的协议违约、破产或宣布破产,或者供应商可能 确定将不再作为客户与我们打交道。此外,客户或供应商可能会受到上述可能对公司造成重大不利影响的任何流动性或其他风险的不利影响,包括但不限于延迟获得或失去获得未投保存款的机会,或失去利用现有信贷安排的能力 涉及陷入困境或破产的金融机构。任何客户或供应商破产或资不抵债,或任何客户未能在到期时付款,或客户或供应商的任何违约或违约,或失去任何重要的供应商关系, 都可能导致公司的重大损失,并可能对我们的业务产生重大不利影响。
我们未来的成功取决于我们 留住高管团队主要成员、顾问和顾问以及吸引、留住和激励合格人员的能力。
我们高度依赖我们执行团队的主要成员,他们的服务的丧失可能会对我们目标的实现产生不利影响。为我们的业务招聘和留住其他 合格的员工、顾问和顾问,包括科学和技术人员,对我们的成功也至关重要。目前,我们的行业缺乏有技能的高管,这种情况很可能会持续下去。因此,对技能人才的竞争非常激烈,流失率可能很高。我们可能无法以可接受的条件吸引和留住人才 因为众多制药和生物技术公司在争夺拥有相似技能的人员。此外, 未能在临床前或临床研究中取得成功可能会使招聘和留住合格人员变得更具挑战性。无法招聘或失去任何高管、顾问或顾问的服务可能会阻碍我们研发目标的进展。
| 46 |
我们将需要扩展我们的组织 ,我们在管理这种增长时可能会遇到困难,这可能会中断我们的运营。
截至2022年12月31日,我们有四名全职员工 。随着我们的成熟,我们可能需要扩大我们的全职员工基础,并聘请更多的顾问和承包商。我们的管理层 可能需要将不成比例的注意力从我们的日常活动中转移出来,并投入大量时间 来管理这些增长活动。我们可能无法有效地管理我们业务的扩张,这可能会导致我们的基础设施薄弱、运营错误、失去商机、员工流失以及剩余员工的生产率下降 ,所有这些都可能对我们的业务、运营结果和前景产生实质性的不利影响。未来的任何增长都可能需要大量的资本支出,并可能从其他项目中转移财政资源,例如开发更多的候选药物 。如果我们的管理层不能有效地管理我们的增长,我们的费用增长可能会超过预期,我们创造和/或增长收入的能力可能会降低,我们可能无法实施我们的业务战略。我们未来的财务业绩 以及我们将候选药物商业化并有效竞争的能力将在一定程度上取决于我们有效管理未来任何增长的能力。
我们是合作协议和其他重要协议的一方,这些协议包含复杂的商业条款,可能会导致纠纷、诉讼或赔偿责任 ,这可能会对我们的业务、运营结果和财务状况产生不利影响。
我们目前从与生物技术和制药公司的合作协议中获得全部或大部分收入,并预计在可预见的未来获得这些收入。这些协作 协议包含复杂的商业条款,包括:
| · | 基于某些商业合理性绩效标准的临床开发和商业化义务,如果我们的合作伙伴的绩效的适当性发生争议,往往难以执行; | |
| · | 为合作的候选药物开发项目分配的人员和其他资源的研发绩效和报销义务; | |
| · | 临床和商业制造协议,其中一些协议是根据我们向合作伙伴提供的产品的实际成本定价的,成本分摊公式和方法复杂; | |
| · | 我们和我们的合作伙伴之间的知识产权所有权分配,用于在合作过程中开发的改进和新发明; | |
| · | 基于若干复杂变量的药品销售特许权使用费,包括净销售额计算、地理位置、专利权利要求覆盖范围、专利有效期、仿制药竞争对手、捆绑定价和其他因素;以及 | |
| · | 知识产权侵权、产品责任和某些其他索赔的赔偿义务。 |
我们可能会不时与第三方进行非正式的争议解决讨论,讨论如何正确解释我们协议中包含的复杂商业条款。 未来可能会出现或升级有关我们的协作协议、交易文档或第三方许可协议的一个或多个争议,最终可能导致昂贵的诉讼和对合同条款的不利解释,这将对我们的业务、财务状况和运营结果产生重大不利影响。
| 47 |
我们在竞争极其激烈的环境中运营 不能保证竞争技术不会损害我们的业务发展。
我们从事的是一个快速发展的领域。来自众多制药公司的竞争非常激烈,预计还会加剧。巨大且快速增长的肿瘤治疗市场可能会吸引新的进入者。许多生物技术和制药公司都专注于开发癌症治疗和免疫肿瘤技术。这些公司中的许多(如果不是全部)拥有比我们更多的财务和其他资源以及开发能力 。我们的许多竞争对手在承担产品的临床前和临床测试、获得监管批准以及制造和营销处方药产品方面也拥有更丰富的集体经验。不能保证我们正在开发的候选药物将比竞争对手的产品更有效或获得更大的市场接受度,也不能保证我们的竞争对手 不会成功开发出比我们正在开发的产品和技术更有效的产品和技术,或者不能保证我们的产品和技术会使我们的产品和技术竞争力降低或过时。此外,不能保证其他公司开发的新药或改进药不会使我们的药品变得多余或过时。
潜在的新会计准则或立法行动可能会对我们未来的财务状况或经营结果产生不利影响。
未来财务会计准则的变化 可能会在确认收入或费用的时间上造成不利的意外波动,并可能影响我们的财务状况 或经营业绩。未来可能会出现新的准则,并可能要求我们更改会计政策。 遵守不断变化的公司治理和公开披露法规可能会导致额外的费用。不断变化的与公司治理和公开披露相关的法律、法规和标准,包括2002年的《萨班斯-奥克斯利法案》(或《萨班斯-奥克斯利法案》)、新的《美国证券交易委员会》法规、上市公司会计监督委员会(简称PCAOB)标准和纳斯达克规则,正在给我们这样的公司 带来不确定性。由于这种不确定性和其他因素,保险、会计和审计成本很高。
我们的资本资源有限,目前我们的财务部门只有一名全职员工。我们依赖外部顾问来补充我们的内部专业知识,并致力于保持高标准的公司治理和公开披露。因此,我们打算投入所有合理的 必要资源来遵守不断发展的标准,这一投资可能会导致一般和行政费用的增加 ,并将管理时间和注意力从创收活动转移到合规活动。
与我们普通股相关的风险
我们未能满足纳斯达克资本市场持续上市的要求 可能导致我们的普通股被摘牌。如果不能重新遵守纳斯达克上市规则,可能会影响我们普通股的市场价格和流动性,并降低我们的融资能力。
目前,我们的普通股在纳斯达克资本市场进行交易。于2022年6月3日,吾等收到纳斯达克证券市场有限责任公司(“纳斯达克”)上市资格部 发出的书面通知(“通知”),通知吾等纳斯达克普通股的收市价已连续30个工作日低于1.00美元,因此吾等未能遵守“纳斯达克上市规则”第5550(A)(2)条对继续纳入纳斯达克资本市场的最低投标价格要求(“买入价要求”)。本通知对本公司普通股在纳斯达克资本市场上市没有立即 影响。
根据纳斯达克上市规则,我们有180个历日的期限,自通知日期起计,以重新遵守投标价格要求。因此,我们必须在2022年11月30日(“合规日期”)之前重新遵守投标价格要求。2022年12月1日,我们收到纳斯达克的信函 ,通知我们尽管公司普通股尚未恢复符合每股1.00美元的最低买入价要求,但纳斯达克已确定我们有资格再延长180个历日,或直到2023年5月29日,以恢复 合规。纳斯达克的决定乃基于本公司符合公开持有股份的市值持续上市要求及纳斯达克资本市场首次上市的所有其他适用要求(投标价格要求除外),以及吾等发出的书面通知,表示有意在第二合规期间通过进行反向 股票拆分来弥补不足之处。
| 48 |
如果在2023年5月29日之前的任何时间,纳斯达克普通股的收盘价至少连续10个工作日的收盘价达到或高于每股1.00美元,纳斯达克将发出书面通知,告知我们已经达到了出价要求。
我们将继续监控我们普通股的收盘价 ,并将考虑我们可用的选项来解决不足,并在分配的合规期内重新遵守投标价格要求 。然而,不能保证我们将能够重新遵守投标价格 要求,或以其他方式遵守纳斯达克上市规则。如果我们未能重新遵守纳斯达克上市规则,包括出价要求,我们可能会被摘牌,根据美国证券交易委员会的规定,我们的股票将被视为细价股,因此将受到对出售我们证券的经纪自营商施加额外销售实践要求的规则的约束。 这些要求给经纪自营商带来的额外负担可能会阻碍经纪自营商在我们的普通股中进行交易。这可能会严重限制我们普通股的市场流动性以及股东在二级市场上出售我们的证券的能力 。如果我们的普通股从纳斯达克资本市场退市,我们普通股的流动性将受到重大影响,这将降低我们普通股对投资者的吸引力,并导致我们普通股的 市场价格下跌。此外,如果我们不在大型交易所上市,我们可能很难筹集额外的资本。
我们证券的市场价格可能波动很大,您可能无法出售我们的证券。
在股票市场交易的公司一般都经历了极端的价格和成交量波动,这些波动往往与这些公司的经营业绩无关或不成比例 。无论我们的实际经营业绩如何,广泛的市场和行业因素都可能对我们证券的市场价格产生负面影响。
我们证券的市场价格可能会波动。 我们证券的价格可能会因各种因素而大幅波动,包括以下因素:
| · | 临床前或临床研究中的不良结果、延迟或搁置; | |
| · | 无法获得额外资金; | |
| · | 为我们的任何候选药物提交IND或BLA的任何延迟,以及与FDA对该IND或BLA的审查有关的任何不利发展或被认为是不利发展; | |
| · | 未能成功开发我们的候选药物; | |
| · | 未能维持我们现有的战略合作关系或进入新的合作关系; | |
| · | 我们或我们的许可方和战略合作伙伴未能起诉、维护或执行我们的知识产权; | |
| · | 适用于未来产品的法律或法规的变化; | |
| · | 无法为我们的候选药物获得足够的产品供应,或无法以可接受的价格这样做; | |
| · | 不利的监管决定; | |
| · | 竞争对手引进新产品、新服务或新技术; | |
| · | 未能达到或超过我们向公众提供的财务预测; | |
| · | 未能达到或超过投资界的财务预测; | |
| · | 公众、立法机构、监管机构和投资界对制药业的看法; | |
| · | 我们、我们的战略合作伙伴或我们的竞争对手宣布重大收购、战略合作伙伴关系、合资企业或资本承诺; | |
| · | 与专有权有关的争议或其他发展,包括专利、诉讼事项和我们为我们的技术获得专利保护的能力; | |
| · | 关键科学技术人员或管理人员的增减; | |
| · | 重大诉讼,包括专利或股东诉讼; | |
| · | 同类公司的市场估值变化; | |
| · | 我们或我们的股东将来出售我们的证券; | |
| · | 不利的经济条件,包括公共卫生问题(如冠状病毒爆发)和地缘政治事件(如俄罗斯入侵乌克兰)以及相关制裁和其他经济干扰或关切对一般经济活动的潜在不利影响;以及 | |
| · | 我们证券的交易量。 |
| 49 |
我们的优先股拥有不属于我们普通股股东的权利、优先权 和特权,这可能导致我们优先股持有人的利益 不同于我们普通股股东的利益。
我们优先股的持有人有权 获得清算优先权,使他们有权从我们可供分配给股东的资产中支付,然后才可以向任何普通股或任何系列优先股的持有人支付任何优先股级别低于此类优先股的优先股。清算优先权的存在可能会降低我们普通股的价值,使我们更难在未来的发行中出售普通股,或者阻止或推迟控制权的变更。此外,A系列优先股和B系列优先股的每股可转换为我们普通股的股票,受可发行上限的限制和某些调整,这可能会导致我们的普通股股东显著稀释 。优先股权利可能导致优先股持有者和我们普通股持有者之间的利益分歧。
未来发行普通股可能不会对我们的股东造成稀释。
截至2023年3月10日,我们约有1,520万股已发行普通股,不包括680万股与已发行优先股、认股权证、期权、限制性股票和普通股奖励相关的潜在摊薄普通股。
这些普通股的发行和这些普通股的出售,甚至这种发行和出售的可能性,可能会对我们普通股的市场价格产生压低作用,而这种普通股的发行将对我们的股东造成稀释。
我们可能会受到证券类诉讼的影响。
在过去,证券集体诉讼 经常是随着公司证券市场价格的下跌而对其提起的。这一风险与我们尤其相关,因为制药公司近年来经历了显著的股价波动。如果我们面临这样的诉讼, 可能会导致巨额成本,并转移管理层的注意力和资源,这可能会损害我们的业务。
我们的普通股或认股权证可能无法形成活跃、流动和有序的市场。
我们的普通股和认股权证在纳斯达克交易 。我们普通股或认购权证的活跃交易市场可能永远不会发展或持续下去。如果我们普通股或认购权证的活跃市场没有持续发展或持续,投资者可能很难在不压低市场价格的情况下出售股票或认购权证,投资者可能根本无法出售股票或认购权证。 不活跃的市场还可能削弱我们通过出售普通股或认购权证筹集资金的能力,并可能削弱我们以普通股或认购权证作为对价收购其他业务、应用程序或技术的能力,这反过来又可能对我们的业务产生重大不利影响。
我们已经与我们的股东签订了几项协议。
我们过去已经并可能继续与股东签订协议,这可能会导致利益冲突。此外,这些安排可能不是在与我们保持距离的情况下协商的,并且可能包含不符合我们最佳利益的条款和条件。
| 50 |
我们不打算为我们的普通股或优先股支付股息,因此任何回报都将限于我们股票的价值。
我们从未宣布或支付过普通股或优先股的任何现金股息。我们目前预计,我们将保留未来用于业务发展、运营和扩展的收益,在可预见的未来不会宣布或支付任何现金股息。因此,对普通股或优先股股东的任何回报将仅限于其股票的增值。
我们的公司章程、附则和内华达州修订条例的某些条款可能被视为具有反收购效力,这可能会导致我们普通股的市场价格下跌。
我们的公司章程、附则和内华达州修订案的某些条款可能被视为具有反收购效力。此类条款可能会延迟、阻止或阻止股东可能认为符合该股东最佳利益的要约收购或收购尝试,包括尝试 可能导致股东所持股份的市价溢价,从而导致我们普通股的市价下跌。
一般风险因素
我们的财务状况、经营结果、业务和现金流可能会受到不利的美国或全球经济状况的负面影响。
我们的财务状况、经营结果、业务和现金流可能会受到全球经济和全球金融市场总体状况以及经济稳定性不确定性的负面影响。全球经济经历了极端的波动和中断,包括公共卫生流行病和大流行,或其他传染病的爆发,如新冠肺炎大流行,以及国际冲突、恐怖主义或其他地缘政治事件,如俄罗斯入侵乌克兰,以及相关制裁和其他经济中断 或担忧。
例如,与一种新型冠状病毒(新冠肺炎)迅速增长的爆发有关的全球大流行已经并可能继续造成重大波动、 不确定性和经济混乱,包括资本市场的大幅波动。新冠肺炎疫情对我们的业务、运营、财务业绩和普通股交易价格的影响程度将取决于许多我们可能无法准确预测的不断变化的因素 。如果全球遏制新冠肺炎疫情的反应进一步升级或失败, 或者如果政府放松与疫情相关的限制的决定无效、过早或适得其反,我们可能会 对我们的业务、财务状况、运营结果和现金流产生实质性的不利影响。
此外,全球经济和金融市场也可能受到军事冲突、恐怖主义或其他地缘政治事件当前或预期影响的不利影响。 美国和其他国家为应对此类冲突而实施的制裁也可能对金融市场和全球经济造成不利影响,受影响国家或其他国家的经济对策可能会加剧市场和经济的不稳定。 2022年2月下旬,俄罗斯对乌克兰发起了重大军事行动。作为回应,美国和其他一些国家对俄罗斯实施了重大制裁和贸易行动,如果冲突继续或恶化,可能会实施进一步的制裁、贸易限制和其他报复行动。无法预测冲突的更广泛后果,包括与之相关的地缘政治紧张局势,以及美国和其他国家将在这方面采取的措施和报复行动,以及俄罗斯可能采取的任何应对措施或报复行动,这些都可能导致地区不稳定和地缘政治转变,并可能对全球贸易、货币汇率、地区经济和全球经济造成实质性不利影响。虽然很难预测前述任何一项对我们公司的影响,但针对冲突所采取的冲突和行动可能会增加我们的成本,扰乱我们的供应链,削弱我们在需要时以可接受的条件筹集或获得额外资本的能力(如果有的话),或者以其他方式对我们的业务、财务状况和运营结果产生不利影响。
| 51 |
不能保证信贷和金融市场的进一步恶化以及对经济状况的信心不会发生。严重或长期的经济低迷可能会给我们的业务带来各种风险,包括对我们可能开发的任何候选产品的需求减弱,以及我们在需要时以可接受的条件筹集额外资本的能力(如果有的话)。经济疲软或下滑也可能给我们的供应商带来压力,可能导致供应中断。如果股票和信贷市场恶化,可能会使任何必要的债务或股权融资变得更加困难,成本更高,摊薄程度也更高。如果不能以有利的条件及时获得任何必要的融资,可能会削弱我们实现增长战略的能力,可能会损害我们的财务业绩和股价,并可能要求我们推迟或放弃临床 开发计划。此外,我们当前或未来的服务提供商、制造商或其他协作者可能 无法挺过经济困难时期,这可能会直接影响我们按时和按预算实现运营目标的能力。 我们无法预测当前的经济环境和金融市场状况可能对我们的业务产生不利影响的所有方式。
我们使用潜在的未来运营亏损以及联邦和州NOL结转来抵消运营或公司合作产生的收入的应税收入的能力可能会受到限制 。
使用我们的NOL结转可能会受到限制 ,原因是未来的某些所有权变更或守则和其他税务机关规定的其他因素。TCJA改变了NOL结转的联邦递延税额和联邦NOL结转的使用规则。
如果我们的NOL结转有限,并且我们有 应纳税所得额超过该期间的可用NOL结转,我们将承担所得税责任,即使NOL结转 可能在到期前的未来几年可用。任何此类所得税负债都可能对我们未来的现金流、财务状况和财务业绩产生不利影响。
税制改革可能会对公司和我们的股东产生重大影响。
由于税法和法规的潜在变化或其解释的变化、税收法规的模糊性、事实解释的主观性 和其他因素,我们对有效税率和所得税资产负债的估计可能不正确,我们的财务报表可能会受到不利影响。本段第一句提到的这些因素的影响可能因时期而异 。
此外,我们缴纳的所得税金额 将接受美国联邦、州和地方税务机关以及非美国税务机关的持续审计。如果审计产生的付款或评估与我们的准备金不同,我们未来的结果可能包括对我们的纳税负债进行不利的调整,我们的财务 报表可能会受到不利影响。美国或其他司法管辖区税制的任何进一步重大变化 (包括下文进一步描述的国际收入征税变化)可能会对我们的财务报表产生不利影响。
政府可能会实施价格管制,这可能会对我们未来的盈利能力产生不利影响。
我们打算寻求批准在美国和其他司法管辖区销售我们的候选药物 。在一些外国国家和司法管辖区,特别是在欧盟,处方药的定价受到政府的管制。在这些国家/地区,在收到候选药物的上市批准后,与政府当局进行定价谈判可能需要相当长的时间。要在某些国家/地区获得报销或定价批准,我们可能需要进行临床试验,将我们候选药物的成本效益与 其他可用疗法进行比较,这既耗时又昂贵。如果我们未来的产品无法获得报销或在范围或金额上受到限制,或者如果定价设置在不令人满意的水平,我们可能无法实现或保持盈利。
| 52 |
我们的员工、首席调查人员、顾问和商业合作伙伴可能从事不当行为或其他不当活动,包括不遵守监管标准和要求以及内幕交易。
我们面临员工、主要调查人员、顾问和商业合作伙伴的欺诈或其他不当行为的风险。这些当事人的不当行为可能包括: 故意不遵守FDA和非美国监管机构的规定,向FDA和非美国监管机构提供准确的信息, 遵守美国和国外的医疗欺诈和滥用法律法规,准确报告财务信息或数据 或向我们披露未经授权的活动。特别是,医疗保健行业的销售、营销和业务安排受到旨在防止欺诈、不当行为、回扣、自我交易和其他滥用行为的广泛法律法规的约束。这些法律法规可能会限制或禁止各种定价、折扣、营销和促销、销售佣金、客户激励计划和其他业务安排。此类不当行为还可能涉及对在 临床研究过程中获得的信息的不当使用,这可能会导致监管制裁并对我们的声誉造成严重损害,或者可能导致监管机构 不批准我们的候选药物。并非总是能够识别和阻止员工的不当行为,我们为检测和防止此类行为而采取的预防措施可能无法有效控制未知或未管理的风险或损失,或保护我们免受因未能遵守这些法律或法规而引起的政府 调查或其他行动或诉讼。如果对我们采取任何此类行动,而我们未能成功为自己辩护或维护自己的权利,这些行动可能会对我们的业务产生重大的 影响,包括施加巨额罚款或其他制裁。
使用我们的候选药物可能会导致不良副作用。
与大多数生物制药产品一样,使用我们的候选药物可能与副作用或不良事件相关,这些副作用和不良事件的严重程度和频率可能会有所不同。任何时候都可能观察到与使用我们的候选药物相关的副作用或不良事件,包括在临床试验中或产品商业化之后,任何此类副作用或不良事件都可能对我们获得监管部门批准或销售我们的候选药物的能力产生负面影响。与使用我们的候选药物相关的副作用,如毒性或其他安全问题,可能需要我们进行额外的研究,或者停止这些候选药物的开发或销售,或者使我们面临产品责任诉讼, 将损害我们的业务。
不可预见的安全问题或不良事件的出现可能会导致监管机构要求我们对候选药物的安全性和有效性进行额外的临床前或临床试验 ,这是我们没有计划或预期的。我们无法向您保证,我们将及时或永远解决与任何产品相关的不良事件相关的问题,使FDA或任何监管机构满意,这些问题可能会损害我们的业务、前景和财务状况。我们也可能无意中未能在规定的 时间范围内报告我们知道的不良事件。我们也可能没有意识到我们已经意识到可报告的不良事件,特别是如果它没有作为不良事件报告给我们,或者如果它是意外的不良事件或在使用我们的产品时被及时删除。如果我们未能遵守我们的报告义务,FDA或其他外国监管机构可能会采取行动,包括刑事起诉、 施加民事罚款、扣押我们的产品或推迟批准或批准未来的产品。
| 53 |
我们面临潜在的产品责任, 如果针对我们的索赔成功,我们可能会招致重大责任和成本。如果使用我们的候选药物伤害了患者, 或者被认为伤害了患者,即使这种伤害与我们的候选药物无关,我们的监管批准可能会被撤销或 以其他方式受到负面影响,我们可能会受到代价高昂且具有破坏性的产品责任索赔。
在临床研究中使用我们的候选药物以及销售我们获得上市批准的任何产品都会使我们面临产品责任索赔的风险。产品责任 消费者、医疗保健提供商、制药公司或销售或以其他方式接触我们产品的其他人可能会对我们提出索赔 。我们的候选药物可能会引发不良反应的风险。如果我们不能成功抗辩 产品责任索赔,我们可能会招致巨额责任和成本。此外,无论优点或最终结果如何,产品 责任索赔可能会导致:
| · | 损害我们的商业声誉; | |
| · | 临床研究参与者退出; | |
| · | 因相关诉讼而产生的费用; | |
| · | 分散管理层对我们主要业务的注意力; | |
| · | 向患者或其他索赔人提供巨额金钱奖励; | |
| · | 无法将我们的候选药物商业化;以及 | |
| · | 减少了对我们候选药物的需求,如果被批准用于商业销售, |
所有这些都可能对我们的业务、运营结果和前景产生实质性的不利影响。
如果我们不遵守环境、健康和安全法律法规,我们可能会被罚款或罚款,或产生成本,这可能会对我们的业务成功产生实质性的不利影响 。
我们受到众多环境、健康和安全法律法规的约束,包括管理实验室程序以及危险材料和废物的处理、使用、储存、处理和处置的法律法规。我们的业务涉及使用危险和易燃材料,包括化学品和生物材料。我们的业务还会产生危险废物产品。我们通常与第三方签订处理这些材料和废物的合同。我们不能消除这些材料造成污染或伤害的风险。如果我们使用危险材料造成污染或伤害,我们可能会对由此造成的任何损害负责,任何责任都可能超出我们的资源范围。 我们还可能产生与民事或刑事罚款和处罚相关的巨额费用。
我们为员工因使用危险材料或其他工伤而受伤而可能产生的成本和费用,我们维持的工伤保险 可能无法为潜在的责任提供足够的保险。此外,为了遵守当前或未来的环境、健康和安全法律法规,我们可能会产生巨额成本。这些当前或未来的法律法规 可能会损害我们的研究、开发或生产努力。不遵守这些法律法规还可能导致巨额罚款、处罚或其他制裁,这可能会对我们的业务和运营结果产生实质性的不利影响。
非现金费用,如基于股票的支付 可能会对我们的运营结果产生不利影响。
我们记录与基于股票的支出相关的非现金费用,由于公司预计将继续发放基于股票的支付奖励,因此可能会大幅波动,并可能对我们的运营业绩产生不利影响 。
| 54 |
对现有标准和规则的不同解释 经常出现,可能会导致我们不得不重申之前报告的操作结果。
对会计政策的现有准则或对现有交易的会计处理方式的不同解释可能会导致我们不得不重新陈述之前报告的 运营结果。
我们的披露控制和程序可能无法 阻止或检测所有错误或欺诈行为。
我们必须遵守《交易法》的定期报告要求。任何披露控制和程序或内部控制和程序,无论构思和操作多么周密, 只能为实现控制系统的目标提供合理的、而不是绝对的保证。这些固有的限制包括 决策过程中的判断可能出错,以及故障可能因简单的错误或错误而发生的现实。此外,可以通过某些人的个人行为、两个或多个人的合谋或未经授权覆盖控制 来规避控制。因此,由于我们控制系统的固有局限性,由于错误或欺诈而导致的错误陈述可能会发生且未被发现,这可能会对我们的业务和运营结果产生实质性的不利影响。
我们的信息技术系统出现故障,包括网络安全攻击或其他数据安全事件,可能会严重扰乱我们的运营。
我们的运营在一定程度上取决于我们信息技术系统的持续表现。我们的信息技术系统可能容易受到物理或电子入侵、计算机病毒和类似中断的攻击。我们的信息技术系统故障可能会对我们的业务、盈利能力和财务状况产生不利影响。
成功的网络安全攻击或其他数据 安全事件可能导致机密或个人信息被盗用和/或丢失、造成系统中断 或部署攻击我们系统的恶意软件。网络安全攻击可能会在一段时间内未被察觉 。网络安全攻击或事件的发生可能导致业务中断,原因是我们的信息技术系统中断,或负面宣传导致我们的临床试验参与者、客户、股东和其他利益相关者的声誉受损,和/或增加了预防、应对或缓解网络安全事件的成本。此外,未经授权传播敏感个人信息或专有或机密信息可能使我们或其他第三方面临监管罚款 或处罚、诉讼和潜在责任,或以其他方式损害我们的业务。
我们是一家较小的报告公司, 适用于较小报告公司的报告要求降低可能会降低我们的普通股对投资者的吸引力。
我们是一家较小的报告公司(“SRC”), 这允许我们利用适用于其他不是SRC的上市公司的各种报告要求的豁免,包括不需要遵守经修订的2002年萨班斯-奥克斯利法案 第404条的审计师认证要求,减少了在我们的年度报告和定期报告和 代理报表中关于高管薪酬的披露义务,并在我们的年度报告和定期报告中仅提供两年的经审计财务报表。我们将继续作为SRC,直至(A)截至最近结束的第二财季的最后一个工作日,非关联公司持有的已发行普通股的总市值超过2.5亿美元,或(B)(1)我们的年收入超过1亿美元,(2)截至最近结束的第二财季的最后一个工作日,非关联公司持有的已发行普通股的总市值超过7亿美元。我们无法预测,如果我们依赖某些或所有这些豁免,投资者是否会发现我们的普通股吸引力下降。如果一些投资者因此发现我们的普通股吸引力下降,我们的普通股交易市场可能会变得不那么活跃,我们的股价可能会更加波动,可能会下跌。
项目1B--未解决的工作人员意见
不适用。
| 55 |
项目2--财产
我们在马萨诸塞州弗雷明翰康科德街945号租用办公空间 。租赁协议为期12个月,截止日期为2023年9月。我们相信,这个空间足以满足我们目前的需求,如果需要额外的空间,可以在附近以商业上的合理条件获得。
此外,我们还出租 360平方米。英国《金融时报》佛罗里达州迈阿密的办公空间。租赁的初始期限为12个月,从2016年12月1日开始 ,并已按年延长至2023年11月30日。我们相信,这个空间足以满足我们目前的需求 如果需要额外的空间,可以在现有空间内或附近以商业合理的条件获得。
项目3--法律诉讼
有时,我们 可能是诉讼的一方,并可能受到正常业务过程中附带索赔的影响。虽然诉讼和索赔的结果不能确定地预测,但我们目前相信这些普通课程事项的最终结果不会对我们的业务产生实质性的不利影响。无论结果如何,由于辩护和和解成本、管理资源转移和其他因素,诉讼可能会对我们产生不利影响。
截至2022年12月31日,管理层认为没有任何事项可能对我们的财务状况、经营业绩或现金流产生重大不利影响。
项目4--矿山安全披露
不适用。
| 56 |
第II部
项目5-注册人普通股市场、相关股东事项和发行人购买股权证券
我们的普通股和 普通股认购权证分别在纳斯达克资本市场(“纳斯达克”)上市,代码为“XBIO”和 “XBIOW”。
纪录持有人
截至2023年3月10日,我们共有426名普通股持有者。
分红
我们之前从未宣布或支付过普通股的任何现金股息。我们目前打算保留收益和利润(如果有的话)以支持我们的业务战略,在可预见的未来不打算支付任何现金股息。未来任何派发现金股息的决定将由本公司董事会自行决定,并将取决于本公司的财务状况、本公司的经营业绩、资本要求、一般业务状况以及董事会认为相关的任何其他因素。
股权薪酬计划信息
第5项所要求的关于根据股权补偿计划发行的授权证券的信息通过引用本表格10-K的第三部分第12项并入本文。
最近出售的未注册证券
没有。
回购发行人的股权证券
在截至2022年12月31日的季度内,我们没有回购任何流通股普通股。
第6项--[已保留]
保留。
| 57 |
第7项– 管理层对财务状况和经营成果的讨论与分析
业务概述
我们是一家生物制药公司,专注于推进创新的免疫肿瘤学技术,解决难以治疗的癌症。我们的DNase平台旨在通过针对Net来改善现有治疗的结果 ,包括免疫疗法。我们于2022年4月获得了DNase肿瘤学平台的许可,并预计 将优先考虑我们在开发这项新收购的技术上的努力和资源。我们目前专注于将我们的系统DNA ase计划推进到临床,作为胰腺癌和局部晚期或转移性实体肿瘤的辅助治疗。 我们还在开发我们的个性化嵌合抗原受体(CAR)T平台技术,XCART™, 开发针对单个患者恶性肿瘤细胞表面独特的B细胞受体的细胞疗法,用于治疗B细胞淋巴瘤。此外,我们还与生物技术和制药公司合作,开发我们的专有药物输送平台PolyXen,并根据血液凝血障碍领域的独家许可安排获得特许权使用费支付。
我们将我们的专利和专有技术 整合到目前正在与生物技术和制药行业合作开发的候选药物中,以创造我们相信 将比现有疗法更具药理学特性的下一代生物药物。我们的候选药物已由我们的研究活动或我们的合作者的研究活动产生,并处于开发阶段。因此,我们将继续投入大量资源用于我们的研发活动,并预计在不久的将来继续这样做。 到目前为止,我们的候选药物尚未在美国或任何其他国家或地区获得任何适用机构的监管营销授权或批准。根据将我们的PolyXen技术许可给行业合作伙伴的规定,我们将收到持续的版税。尽管我们拥有广泛的专利组合,但在截至2022年12月31日的一年中,我们内部努力的重点是我们DNase平台的许可和进步,以及我们XCART 平台技术的开发。
关键会计政策和估算
按照美国公认会计原则(“美国公认会计原则”)编制我们的财务报表要求我们作出估计、判断和假设,这些估计、判断和假设会影响在财务报表日期报告的资产和负债额,以及报告期内报告的收入、成本和费用。在持续的基础上,我们根据历史经验和我们认为在这种情况下合理的各种其他假设来评估我们的估计。这些评估的结果构成了对资产和负债的账面价值和报告的费用金额做出判断的基础 这些费用从其他来源看不出来 。由于未来事件及其影响无法确定,实际结果和结果可能与我们的估计、判断和假设大不相同。
管理层认为,以下会计估计对于全面理解和评估我们报告的财务结果是最关键的,它们需要管理层作出最困难的主观或复杂的判断,这是因为需要对本质上不确定的事项的影响进行估计。下面的叙述描述了这些关键的会计估计、判断和假设,以及如果实际结果与这些假设不同将产生的影响。
收入确认
我们与制药和生物技术合作伙伴签订了供应、许可和协作 协议,其中一些协议包括基于经批准的商业药品的潜在净销售额的版税协议。
| 58 |
我们根据会计准则编纂(“ASC”)主题606确认收入,与客户签订合同的收入(“ASC 606”)。本标准 适用于与客户签订的所有合同,属于其他标准范围的合同除外,如租赁、保险、协作安排和金融工具。根据ASC 606,实体在其客户获得对承诺商品或服务的控制权时确认收入,其金额反映了实体预期以这些商品或服务换取的对价 。为了确定实体确定属于ASC 606范围内的安排的收入确认,该实体执行以下五个步骤:(I)确定与客户的合同;(Ii)确定合同中的履约义务;(Iii)确定交易价格;(Iv)将交易价格分配给合同中的履约义务;以及(V)在某个时间点或随时间确认满足履约义务的收入。我们仅在以下情况下才将五步模型应用于合同: 很可能会收取它有权收取的对价,以换取它转让给客户的商品或服务。 在合同开始时,一旦合同被确定在ASC 606的范围内,我们就会评估 每个合同中承诺的商品或服务,确定哪些是履约义务,并评估每个承诺的商品或服务是否是不同的。然后,当履行义务得到履行时,我们将分配给相应履行义务的交易价格的金额确认为收入 。
作为对这些安排的会计处理的一部分,我们必须使用重大判断来确定:a)基于以上步骤(Ii)下的确定的履行义务的数量; b)以上步骤(Iii)下的交易价格;以及c)在以上步骤(Iv)中分配交易价格的 合同中确定的每一履行义务的独立销售价格。我们使用判断来确定是否应将里程碑或其他变量 对价计入交易价格,如下所述。交易价格按相对独立销售价格分配给每个履约义务 ,我们将收入确认为或在履行合同项下的履约义务时确认。在制定履约义务的独立价格时,我们会考虑适用的市场条件 和相关的实体特定因素,包括与客户谈判协议时考虑的因素和估计的 成本。我们通过评估用于确定独立销售价格的关键假设的变化是否会对多个履约义务之间的交易价格分配产生重大影响,来验证履约义务的独立销售价格 。我们确认合同资产或负债是因为我们的业绩(即,转移给客户的货物或服务)与客户的业绩(即,客户支付并无条件应支付的对价)之间的差异。
我们的许可协议条款可能包括 向协作合作伙伴交付IP许可。根据许可安排,我们可以通过不可退还的预付收据、开发和监管目标收据以及合作伙伴未来产品销售的版税收据组合获得补偿。我们预计 确认我们在许可和协作安排中收到的不可退还的预付许可付款以及开发和监管里程碑付款 ,其中包括未来义务,如供应义务,在我们根据每个相应安排的预期履约期内按比例计算。我们对预期履行绩效义务的期限做出最佳估计,其中可能包括技术转让援助、研究活动、临床开发活动以及从开发到产品商业化的制造活动 。鉴于这些协作安排的不确定性,需要做出重大判断来确定履约期的持续时间 。
当我们达成再许可我们的一些专利的安排时,我们将考虑履行义务,以确定在我们确定收入确认的适当方法和时间时,该安排是单一要素还是多个要素。我们考虑 的许可或再许可的条款,除了我们提供的服务、专利 国防成本、技术支持、市场营销或销售帮助等任何履行义务外,还会考虑价格调整或退款条款等元素,或可能构成可交付给它的额外 可更改收入确认时间的任何其他元素。收到的不可退还的预付许可和再许可费用, 继续履行或未来义务被视为与相关许可技术无关或敷衍了事, 在交付技术时确认为收入。
我们预计将根据基本合同条款确认销售期间的特许权使用费收入,前提是报告的销售额可以可靠地衡量,我们没有剩余的 履约义务,并且满足所有其他收入确认标准。我们预计,我们完成的与协作协议相关的研发服务的报销将在运营中确认为毛收入。我们的许可证 和与某些协作合作伙伴的协作协议还可以向我们提供未来的里程碑收据,仅根据相应协作合作伙伴在考虑截止日期延长或实现指定销量的情况下的表现 批准的药品。对于这类收据,我们希望根据适用的合同条款按履约或按比例在协议期限内将这些收据确认为收入。如果我们的持续履行或未来义务被视为无关紧要或敷衍了事,则这些收据也可被确认为收入。
| 59 |
研究和开发费用
研发费用是指在进行研发活动中发生的费用,包括薪酬福利、设施费用、管理费用、临床前开发、临床试验及相关临床制造费用、支付给合同研究机构(“CRO”)和合同制造机构(“CMO”)的费用以及其他外部费用。我们按已发生的 来计入研发成本。我们为研发服务预先支付不可退还的费用,因为发生了义务。归属于收购但未达到资本化标准的无形资产的价值 在收购时计入研发费用。根据许可协议支付的预付款将在收到许可时支出。许可协议项下的里程碑付款 在确定里程碑可能实现且相关金额可合理评估的期间内累计,并确认相应费用。
我们需要估算每个报告期的应计研究和开发费用。此流程包括审核未结合同和采购订单,与我们的人员进行沟通以确定已代表我们执行的服务,并在我们尚未收到发票或以其他方式通知实际成本时估计所执行的服务级别和服务产生的相关成本。我们的大多数服务提供商 按照预先确定的时间表或在达到合同里程碑时向我们开具欠款发票。但是,有些需要 预付款。我们根据当时已知的事实和情况,在财务报表中对截至每个资产负债表日期的应计费用进行估计。我们定期与服务提供商确认估计的准确性,并在必要时进行调整。 估计应计研究和开发费用的例子包括支付给下列人员的费用:
| · | 开展研发和临床前活动的合作伙伴; | |
| · | 与临床试验整体项目管理相关的项目经理; | |
| · | 与cGMP制造有关的cMOS; | |
| · | 与临床试验相关的CRO;以及 | |
| · | 与临床试验相关的调查网站。 |
我们根据我们与代表我们进行和管理临床试验的多个研究机构、CMO和CRO的报价和合同,对收到的服务和花费的努力进行估计,以此为基础支付与研发、临床前活动和临床试验相关的费用。这些 协议的财务条款有待协商,不同的合同会有所不同,可能会导致付款流程不均。在 中,可能会出现向供应商支付的款项超过所提供的服务级别并导致预付费用的情况。在应计服务费用时,我们估计将执行服务的时间段以及每段时间内的工作支出水平。如果服务执行的实际时间或工作水平与估计值不同,我们将相应调整应计或预付金额。 虽然我们预计我们的估计值不会与实际发生的金额有实质性差异,但我们对所执行服务的状态和时间的理解可能与实际状态和所执行服务的时间不同,并可能导致报告的金额 在任何特定时期过高或过低。到目前为止,我们之前对应计研究和开发费用的估计没有任何实质性调整。
基于股份的费用
基于股份的支出包括向员工和非员工授予期权 和限制性股票单位(“RSU”)以购买我们普通股的股份,向员工授予共同股权 计划奖励以及发行普通股以换取非员工提供的服务的协议。
| 60 |
基于股份的费用基于期权的估计公允价值或使用Black-Scholes期权定价模型计算。确定适当的公允价值模型和相关假设需要判断,包括估计股价波动和预期奖励条款。预期波动率 是根据公司的历史波动率估算的。如果无法获得奖励整个预期期限的公司数据,我们使用期权预期期限内我们的历史波动率和可比上市公司同业集团的加权平均值 。预期期限代表期权预期未平仓的时间。我们会在没收发生时而不是授予时对其进行处理。我们没有支付股息,也不预期在可预见的未来支付现金股息,因此,我们使用的预期股息收益率为零。无风险利率基于美国国债的利率,其到期日与奖励的估计预期期限一致。行使时,新发行的普通股股票将赎回股票期权 。当满足授予的归属和交收规定时,RSU将赎回我们普通股的新发行股票。
对于仅根据服务条件授予的员工期权,公允价值计量日期通常为授予之日,相关薪酬支出在奖励的必要归属期间以直线方式确认 。对于为交换公司运营中消耗的商品或服务而发行的非员工期权 ,公允价值计量日期为服务完成日期或绩效承诺达成日期中较早的日期。我们一般认为,股票期权的公允价值比所接受服务的公允价值更能可靠地计量。与授予非员工的股票期权相关的薪酬支出 在奖励的必要归属期间以直线基础确认。
认股权证
关于某些融资、咨询和合作安排,我们发行了认股权证,以购买我们普通股的股份。未清偿认股权证为独立票据,持有人不可出售或强制赎回,并归类为股权奖励。我们使用布莱克-斯科尔斯期权定价模型来衡量截至衡量日期的奖励的公允价值。与发行普通股一起向合作伙伴发行的认股权证最初按公允价值计入已发行普通股额外实收资本的减少额。
所有其他认股权证在必要的服务期内按公允价值 作为费用按直线计入,如果没有服务期或已提供服务,则在发行之日按公允价值记为费用。对于包含基于某些目标实现的归属触发因素的权证,我们应用 判断来估计实现这些目标的概率和时间。这些估计涉及固有的不确定性, 因此,如果实现这些目标的概率或时间发生变化,与费用相关的认股权证未来可能会有很大不同。对于与融资安排相关发行的权证,我们根据奖励和其他工具的相对公允价值分配收益。
无限期-活着的无形资产
在业务 合并、许可及其他交易中取得的资产及承担的负债一般于收购日期按各自的公允价值确认。在 收购时,我们一般使用“收益法”确定无形资产的公允价值,包括正在进行的研发(“IPR&D”)。收购的知识产权研发无形资产被视为无限期无形资产,直至完成或放弃相关的研究和开发工作。在公司的知识产权研发达到技术可行性之前,可能还需要进行大量的额外研究和开发。知识产权研发项目完成后,知识产权研发资产将在其预计使用寿命内进行摊销。
| 61 |
不确定的活着无形资产不会摊销 ,但至少每年或当商业环境的事件或变化表明账面价值可能不会减值时,对减值进行审查。我们的年度评估可能包括定性或定量分析,以确定其公允价值是否更有可能超过账面价值。在执行定性方法时,我们确定 事件或环境的存在是否导致我们确定无限活着的无形资产更有可能(即超过50%的可能性) 减值。如果我们选择首先评估定性因素,并确定无形资产减值的可能性不高于 ,则我们不需要采取进一步行动来测试减值。我们还可以选择绕过定性评估,仅执行量化减损测试,我们可以选择在某些 期间执行,而不是在其他期间执行。由于执行定性评估的选项不是永久性选择,因此我们在每次年度减值审查期间重新评估此选项。减值损失(如有)按无形资产的账面价值超出其公允价值计量。
无形资产极易受到减值费用的影响 ,尤其是用于知识产权研发的新收购资产。考虑到研发的高风险性质以及行业将开发化合物推向市场的成功率,知识产权研发减值费用可能在未来一段时间内发生。估计潜在减值的知识产权研发的公允价值对预测和假设的变化高度敏感,而假设的变化 可能会导致减值。
我们相信我们的估计和假设是合理的 ,在其他方面与市场参与者在其公允价值估计中使用的假设一致。但是,如果未来业绩 与我们的估计和假设不一致,那么我们可能会面临减值费用,这可能是实质性的。使用 不同的估计和判断可能会在我们的分析中产生非常不同的结果,并可能导致非常不同的资产 价值或费用。
新冠肺炎大流行的影响
2020年3月,世界卫生组织宣布发生全球大流行,这与一种新型冠状病毒株(新冠肺炎)的迅速爆发有关。疫情严重影响了美国的经济状况,在2020年3月上半月加速,并持续到2021年和2022年,因为联邦、州和地方政府对公共卫生危机采取了缓解措施,给美国经济带来了重大的不确定性。我们继续评估新冠肺炎疫情对我们业务的影响,尽管采取了社交距离和其他应对措施,但到目前为止还没有对我们的业务产生重大影响,新冠肺炎疫情对我们运营业绩和财务状况的最终影响取决于未来的事态发展,包括疫情持续时间和相关严重程度、接种疫苗的速度和速度,以及新冠肺炎新毒株的持续出现,如Delta和奥密克戎变种及其任何亚变种。以及它对宏观经济 情况的影响,这些情况是不确定的,目前无法预测。如果全球遏制新冠肺炎疫情的反应进一步升级或不成功,或者如果政府放松与疫情相关的限制的决定无效、过早或适得其反, 我们可能会对我们的业务、财务状况、运营结果和现金流产生实质性的不利影响。
乌克兰冲突对我军作战的影响
俄罗斯入侵乌克兰的短期和长期影响目前很难预测。实施制裁和反制裁可能对整个经济市场产生不利影响,并可能影响我们的业务、财务状况和运营结果。
| 62 |
经营成果
下表列出了截至2022年12月31日的年度与截至2021年12月31日的年度的经营历史业绩对比。
| 描述 | 2022 | 2021 | 增加 (减少) | 百分比 变化 | ||||||||||||
| 收入: | ||||||||||||||||
| 专利权使用费收入 | $ | 1,706,925 | $ | 1,160,692 | $ | 546,233 | 47.1% | |||||||||
| 运营成本和支出: | ||||||||||||||||
| 研发 | (4,770,834 | ) | (3,163,485 | ) | 1,607,349 | 50.8% | ||||||||||
| 一般和行政 | (3,653,999 | ) | (3,743,972 | ) | (89,973 | ) | (2.4 | )% | ||||||||
| 总运营成本和费用 | (8,424,833 | ) | (6,907,457 | ) | 1,517,376 | 22.0% | ||||||||||
| 运营亏损 | (6,717,908 | ) | (5,746,765 | ) | 971,143 | 16.9% | ||||||||||
| 其他收入(支出): | ||||||||||||||||
| 其他收入(费用) | (1,597 | ) | 1,119 | 2,716 | 242.7% | |||||||||||
| 利息收入,净额 | 167,152 | 100,467 | 66,685 | 66.4% | ||||||||||||
| 净亏损 | $ | (6,552,353 | ) | $ | (5,645,179 | ) | $ | 907,174 | 16.1% | |||||||
收入
截至2022年12月31日的年度收入增加了50万美元,增幅为47.1%,从截至2021年12月31日的年度的约120万美元增至170万美元。这一增长表明,与2021年同期相比,我们与武田的再许可协议相关的版税收入有所增加。
研发费用
总体而言,截至2022年12月31日的年度研发支出增加了160万美元,增幅为50.8%,与2021年同期的320万美元相比,增幅为50.8%,主要是由于知识产权研发支出为180万美元。在截至2022年12月31日的年度内,公司与公司的DNase平台许可相关的知识产权研发支出为180万美元。2021年没有类似的费用下表列出了我们在截至2022年12月31日和2021年12月31日的年度内按费用类别 产生的研发成本:
| Year ended December 31, | ||||||||
| 费用类别 | 2022 | 2021 | ||||||
| 知识产权研发费用 | $ | 1,793,750 | $ | – | ||||
| 外部服务和合同研究组织 | 2,314,513 | 2,497,190 | ||||||
| 薪金和工资 | 435,564 | 457,313 | ||||||
| 基于股份的费用 | 86,305 | 68,208 | ||||||
| 其他 | 140,702 | 140,774 | ||||||
| 研究与开发费用总额 | $ | 4,770,834 | $ | 3,163,485 | ||||
| 63 |
在480万美元的研发总支出中不包括180万美元的知识产权研发支出,在截至2022年12月31日的一年中,研发支出从截至2021年12月31日的320万美元下降了约20万美元,降幅为5.9%,至300万美元。外部服务和合同研究组织费用的减少主要是由于与我们的XCART技术平台相关的支出减少,但与许可相关的成本和我们与DNase平台相关的初始开发工作大大抵消了这一支出。我们 于2022年4月获得了DNase平台的许可,并希望将我们的精力和资源用于这项新收购的技术的开发。 因此,我们暂停了我们XCART技术平台的开发。
一般和行政费用
截至2022年12月31日的年度的一般和行政费用为370万美元,与前一年同期相比减少了约10万美元,或2.4%。这一下降主要是由于与我们知识产权组合相关的咨询和法律成本的减少,与2021年同期相比,在截至2022年12月31日的一年中,与CLS的DNase肿瘤学平台许可相关的法律成本大幅增加。
其他收入(费用)
截至2022年12月31日的年度,其他支出约为1,600美元,而2021年同期的其他收入约为1,100美元。其他费用的增加 主要是由于截至2022年12月31日的年度内,与2021年同期相比,外币汇率出现了不利的变化。
利息收入,净额
在截至2022年12月31日的一年中,利息收入净额增加到约 20万美元,而上一年同期约为10万美元。 这一增长主要是由于截至2022年12月31日的年度内,与2021年同期相比,投资资金的利率较高,导致利息收入增加。这一增长被Pharmsynz 贷款利息收入的下降部分抵消。
流动性与资本资源
在截至2022年12月31日的年度内,我们发生了约660万美元的净亏损 。截至2022年12月31日,我们的累计赤字约为1.891亿美元,而截至2021年12月31日的累计赤字约为1.825亿美元。截至2022年12月31日,营运资本约为1,260万美元,截至2021年12月31日,营运资本约为1,730万美元。在截至2022年12月31日的一年中,我们的营运资本减少了470万美元,主要原因是我们在截至2022年12月31日的年度的净亏损以及用于获得DNase肿瘤学平台许可证的50万美元的现金 。
我们的主要流动资金来源是现金。截至2022年12月31日,我们有大约1310万美元的现金和110万美元的流动负债。 截至2021年12月31日,我们有大约1820万美元的现金和140万美元的流动负债。
| 64 |
我们评估在财务报表发布之日起一年内,是否有 的情况或事件令人对我们作为持续经营企业的持续经营能力产生重大怀疑。自我们成立以来,我们已经发生了大量亏损,我们预计 在短期内将继续出现运营亏损。这些因素令人对我们作为持续经营企业的能力产生了极大的怀疑。我们相信,我们可以通过可能的公共或私募股权发行、债务融资、企业合作、关联方融资或其他方式获得资本资源,以继续作为一家持续经营的企业。我们相信,我们现有的资源将足以为我们的运营提供至少12个月的资金,从这些财务报表之日起算。但是,我们预计从长远来看,我们可能需要 更多资金来实施我们的业务计划。未来任何融资的条款、时间和范围将 取决于多个因素,包括我们临床开发计划取得的进展、我们识别并进入许可或其他战略安排的能力、我们继续在纳斯达克股票市场(“纳斯达克”)上市的能力,以及与金融、经济、地缘政治、行业和市场状况相关的 因素,其中许多因素是我们无法控制的。生物技术行业的资本市场可能非常不稳定,这使得未来任何融资的条款、时间和范围都不确定。于2022年6月3日,吾等 接获纳斯达克上市资格部发出书面通知(“通知”),通知吾等普通股的收市价已连续30个工作日低于1.00美元,因此未能遵守 根据纳斯达克上市规则第5550(A)(2)条(“买入价要求”)继续纳入纳斯达克资本市场的最低买入价要求。该通知对我们的普通股在纳斯达克资本市场的上市不会立即生效。 根据纳斯达克上市规则,我们自通知日期起有180个历日的期限来重新遵守投标价格要求 。因此,我们必须在2022年11月30日之前重新遵守投标价格要求,如果满足某些其他标准,则有资格获得额外的180个日历日的合规期。2022年12月1日,我们收到纳斯达克 的一封信,通知我们,尽管我们的普通股尚未重新达到每股1.00美元的最低买入价要求,但纳斯达克 已确定我们有资格再获得180个日历天期,即到2023年5月29日,以重新获得合规。纳斯达克的决定是基于本公司符合公开持有股份市值持续上市的要求和纳斯达克资本市场首次上市的所有其他适用要求(投标价格要求除外),以及我们发出的书面通知,表明我们打算在第二合规期内通过进行必要的反向股票拆分来弥补这一不足。
2023年3月10日,SVB被加州金融保护和创新部关闭,该部门指定FDIC为接管人。我们的现金主要是通过SVB维持的。2023年3月12日,美国财政部、美联储和FDIC推出了紧急措施,全面保护SVB的所有储户,并于2023年3月13日,我们完全可以使用我们在SVB的存款。因此,我们预计此类余额不会出现任何损失。
经营活动的现金流
截至2022年12月31日的经营活动中使用的现金流总额约为460万美元,这主要是由于我们在此期间的净亏损,与收购的知识产权研发和基于股份的费用相关的非现金费用部分抵消了 。此外,在截至2022年12月31日的年度内,流动负债减少。在截至2021年12月31日的一年中,用于经营活动的现金流量总计约470万美元,这主要是由于我们在此期间的净亏损,部分被与基于股票的费用相关的非现金费用所抵消。
投资活动产生的现金流
截至2022年12月31日的投资活动中使用的现金流总计500,000美元,这是为许可DNase肿瘤学平台而支付的现金。截至2021年12月31日的年度,没有来自投资活动的现金流。
融资活动产生的现金流
截至2022年12月31日的年度没有融资活动的现金流 。截至2021年12月31日止年度的融资活动现金流总额约为1,150万美元,即我们于2021年7月进行私募所得的净收益。
| 65 |
合同义务
合同义务是指与第三方协议下的未来现金承诺和负债,不包括我们无法合理预测其未来付款的或有负债。我们的合同义务源于办公空间的物业租赁。尽管我们对CMO服务负有义务,但 下表不包括根据我们与CMO的协议我们可能需要支付的潜在付款,因为根据这些协议,付款时间和实际支付的 金额可能会有所不同,具体取决于收到货物或服务的时间或某些义务的商定条款或金额的更改,而且这些协议可在公司书面通知后取消,因此不会产生长期的 债务。合同还可能包含难以预测的可变成本,因为它们基于登记的患者和临床试验地点等情况,这些情况可能会有所不同,因此也不包括在下表中。此外,以下所列债务的预期付款时间是根据当前信息估计的。
下表显示了我们截至2022年12月31日的合同义务,按类型汇总:
按期间到期的付款 截至2022年12月31日 | ||||||||||||||||||||
| 总计 | 少于 1年 | 1-3 年份 | 3-5 年份 | 更多 比 5年 | ||||||||||||||||
| 租赁义务 | $ | 28,524 | $ | 28,524 | $ | – | $ | – | $ | – | ||||||||||
| 总计 | $ | 28,524 | $ | 28,524 | $ | – | $ | – | $ | – | ||||||||||
最新会计准则
请参阅附注3,重要会计政策摘要项目8所附财务报表, 。
项目7A--关于市场风险的定量和定性披露
我们不需要提供本项目所需的信息 ,因为我们是一家较小的报告公司。
| 66 |
项目8--财务报表 和补充数据
| 独立注册会计师事务所报告(PCAOB ID |
F-1 |
| 截至2022年和2021年12月31日的合并资产负债表 | F-3 |
| 截至2022年12月31日和2021年12月31日止年度的综合全面亏损表 | F-4 |
| 截至2022年和2021年12月31日止年度股东权益综合报表 | F-5 |
| 截至2022年、2022年和2021年12月31日的合并现金流量表 | F-6 |
| 合并财务报表附注 | F-7 |
| 67 |
独立注册会计师事务所报告
致以下股东和董事会:
Xenetic生物科学公司。
对财务报表的几点看法
我们审计了所附的Xenetic Biosciences,Inc.(“贵公司”)截至2022年12月31日和2021年12月31日的综合资产负债表、截至2022年12月31日期间各年度的全面亏损、股东权益和现金流量的相关综合报表 以及相关附注(统称为“财务报表”)。我们认为,该等财务报表在各重大方面均公平地反映了本公司于2022年12月31日及2021年12月31日的财务状况,以及截至2022年12月31日止两个年度内各年度的经营业绩及现金流量,符合美国公认的会计原则。
意见基础
这些财务报表由公司管理层负责。我们的责任是根据我们的审计对公司的财务报表发表意见。我们 是一家在美国上市公司会计监督委员会(PCAOB)注册的公共会计师事务所,根据美国联邦证券法以及美国证券交易委员会和PCAOB的适用规则和法规,我们 必须与公司保持独立。
我们按照PCAOB的 标准进行审计。这些标准要求我们计划和执行审计,以获得关于财务报表是否没有重大错报的合理保证,无论是由于错误还是欺诈。本公司不需要,也没有聘请 对其财务报告的内部控制进行审计。作为我们审计的一部分,我们需要了解财务报告的内部控制,但不是为了对公司财务报告内部控制的有效性发表意见。因此,我们不表达这样的意见。
我们的审计包括执行程序以评估财务报表重大错报的风险(无论是由于错误还是欺诈),以及执行应对这些风险的程序。这些程序包括在测试基础上审查与财务报表中的金额和披露有关的证据。 我们的审计还包括评估所使用的会计原则和管理层做出的重大估计,以及评估财务报表的整体列报。我们相信,我们的审计为我们的观点提供了合理的基础。
关键审计事项
下文所述的关键审计事项是指当期对财务报表进行审计而产生的事项,这些事项已传达或要求传达给审计委员会:(1)涉及对财务报表具有重大意义的账目或披露,以及(2)涉及我们的 特别具有挑战性、主观性或复杂性的判断。关键审计事项的沟通不会以任何方式改变我们对整个财务报表的意见 ,我们也不会通过传达下面的关键审计事项,就关键审计事项或与其相关的账目或披露提供单独的意见 。
持续经营评估
有关事项的描述
我们将公司对 其持续经营能力的评估和相关披露确定为关键审计事项。本公司编制了未来现金流预测 ,其中涉及对关键变量的判断和估计,例如与不断发展的DNA ase技术相关的未来预期收入、特许权使用费收益和成本。审核上述公司的持续经营评估涉及核数师的高度判断,以评估公司持续经营分析中使用的现金流预测和其他假设的合理性。
如综合财务报表附注1所述,管理层相信本公司于批准该等财务报表之日有足够资金可供其使用,且自该等财务报表之日起可持续经营至少十二个月。 在作出此项评估时,管理层已考虑本公司现有资源。
| F-1 |
我们是如何在审计中解决这个问题的
我们评估了模型 中使用的假设,通过将管理层使用的假设与历史业绩、预算和公司的战略计划进行比较,来估计从我们的意见之日起未来12个月的未来现金流。我们还评估了关键假设,包括与收入、特许权使用费收益和现金流预测中的重大付款时间相关的假设,方法是将这些假设与历史数据和相关协议进行比较。我们对未来预期成本等关键假设进行了敏感性分析,以确定它们对未来现金流预测的影响。此外,我们还根据持续经营评估对公司的披露进行了评估。
收入确认高于特许权使用费收入
有关事项的描述
如综合财务报表附注3所述,本公司的收入来源包括根据经批准的商业医药产品的潜在净销售额与第三方签订的特许权使用费协议所得的特许权使用费收益,该净销售额基于估计可变对价。公司必须使用重要的 判断来确定何时报告的销售额可以可靠地衡量,公司没有剩余的业绩义务,并且满足所有其他 收入确认标准。公司的政策是,当预期的特许权使用费可以可靠地衡量时,将其确认为收入,这是在收到第三方报告后进行的。该公司通常在实际分受许可人销售之后的下一个季度收到这些报告。
我们确定执行与收入确认有关的程序,特别是与管理层将潜在净销售额估计为预期可变对价的程序有关的主要考虑因素是一项关键审计事项,在确定预期可变对价金额的最佳估计 时,管理层需要做出重大判断。这进而导致审计师在执行程序和评估审计证据时具有高度的判断力、主观性和努力 与管理层在与第三方的特许权使用费合同中确定预期可变对价以及管理层用来估计可变对价的最佳估计的判断有关。
我们是如何在审计中解决这个问题的
处理这一问题涉及执行程序和评估审计证据,以形成我们对合并财务报表的整体意见。这些程序包括评估管理层对第三方潜在净销售额的最佳估计,以确定可变对价。 这些程序还包括(I)评估和测试管理层使用的重要假设的合理性, (Ii)考虑历史或当前趋势,指出相对缺乏与预期 金额相关的历史经验,以及(Iii)获取和担保证据,包括从第三方收到的报告。
自2015年以来,我们一直担任本公司的审计师。
2023年3月22日
| F-2 |
Xenetic生物科学公司。
合并资产负债表
| 2022年12月31日 | 2021年12月31日 | |||||||
| 资产 | ||||||||
| 流动资产: | ||||||||
| 现金 | $ | $ | ||||||
| 预付费用和其他 | ||||||||
| 流动资产总额 | ||||||||
| 其他资产 | ||||||||
| 总资产 | $ | $ | ||||||
| 负债和股东权益 | ||||||||
| 流动负债: | ||||||||
| 应付帐款 | $ | $ | ||||||
| 应计费用和其他流动负债 | ||||||||
| 流动负债总额 | ||||||||
| 总负债 | ||||||||
| 承付款和或有事项(附注14) | ||||||||
| 股东权益: | ||||||||
| 优先股,授权股份 | ||||||||
| B系列,$面值:截至2022年12月31日和2021年12月31日的已发行和已发行股票 | ||||||||
| A系列,$面值:截至2022年12月31日和2021年12月31日的已发行和已发行股票 | ||||||||
| 普通股,$票面价值;和截至2022年12月31日和2021年12月31日授权的股票;和分别于2022年12月31日和2021年12月31日发行的股票;和分别截至2022年12月31日和2021年12月31日的流通股 | ||||||||
| 额外实收资本 | ||||||||
| 累计赤字 | ( | ) | ( | ) | ||||
| 累计其他综合收益 | ||||||||
| 库存股 | ( | ) | ( | ) | ||||
| 股东权益总额 | ||||||||
| 总负债和股东权益 | $ | $ | ||||||
附注是这些合并财务报表的组成部分。
| F-3 |
Xenetic生物科学公司。
综合全面损失表
在过去几年里 十二月三十一日, | ||||||||
| 2022 | 2021 | |||||||
| 收入 | ||||||||
| 专利权使用费收入 | $ | $ | ||||||
| 总收入 | ||||||||
| 运营成本和支出: | ||||||||
| 研发 | ( | ) | ( | ) | ||||
| 一般和行政 | ( | ) | ( | ) | ||||
| 总运营成本和费用 | ( | ) | ( | ) | ||||
| 运营亏损 | ( | ) | ( | ) | ||||
| 其他收入(支出): | ||||||||
| 其他收入(费用) | ( | ) | ||||||
| 利息收入,净额 | ||||||||
| 其他收入合计,净额 | ||||||||
| 净亏损 | $ | ( | ) | $ | ( | ) | ||
| 每股基本和摊薄净亏损 | $ | ) | $ | ) | ||||
| 加权平均普通股流通股、基本普通股和稀释普通股 | ||||||||
附注是这些合并财务报表的组成部分。
| F-4 |
Xenetic生物科学公司。
合并股东权益报表
| 优先股 | 普通股 | 累计 | ||||||||||||||||||||||||||||||||||
数 的 股票 | 帕尔 价值(0.001美元) | 数 的 股票 | 帕尔 价值(0.001美元) | 其他内容 已缴入 资本 | 累计赤字 | 其他综合 收入 | 库存股 | 总计 股东权益 | ||||||||||||||||||||||||||||
| 截至2021年1月1日的余额 | $ | $ | $ | $ | ( | ) | $ | $ | ( | ) | $ | |||||||||||||||||||||||||
| 普通股和认股权证的发行,扣除发行成本 | – | |||||||||||||||||||||||||||||||||||
| 行使预先出资的认股权证 | – | |||||||||||||||||||||||||||||||||||
| 行使认购权证 | – | ( | ) | |||||||||||||||||||||||||||||||||
| 基于股份的费用 | – | – | ||||||||||||||||||||||||||||||||||
| 向供应商发行普通股 | – | ( | ) | |||||||||||||||||||||||||||||||||
| 发行与权证收购相关的普通股 | – | ( | ) | ( | ) | |||||||||||||||||||||||||||||||
| 净亏损 | – | – | ( | ) | ( | ) | ||||||||||||||||||||||||||||||
| 截至2021年12月31日的余额 | $ | $ | $ | $ | ( | ) | $ | $ | ( | ) | $ | |||||||||||||||||||||||||
| 与购买正在进行的研究和开发有关的普通股的发行 | – | |||||||||||||||||||||||||||||||||||
| 行使认购权证 | – | ( | ) | |||||||||||||||||||||||||||||||||
| 基于股份的费用 | – | – | ||||||||||||||||||||||||||||||||||
| 净亏损 | – | – | ( | ) | ( | ) | ||||||||||||||||||||||||||||||
| 截至2022年12月31日的余额 | $ | $ | $ | $ | ( | ) | $ | $ | ( | ) | $ | |||||||||||||||||||||||||
附注是这些合并财务报表的组成部分。
| F-5 |
Xenetic生物科学公司。
合并现金流量表
| 截至12月31日止年度, | ||||||||
| 2022 | 2021 | |||||||
| 经营活动的现金流: | ||||||||
| 净亏损 | $ | ( | ) | $ | ( | ) | ||
| 对净亏损与经营活动中使用的现金净额进行的调整: | ||||||||
| 收购正在进行的研究和开发 | ||||||||
| 使用权资产摊销 | ||||||||
| 基于股份的费用 | ||||||||
| 经营性资产和负债变动情况: | ||||||||
| 预付费用和其他 | ( | ) | ||||||
| 其他长期资产 | ( | ) | ||||||
| 应付账款、应计费用和其他负债 | ( | ) | ||||||
| 用于经营活动的现金净额 | ( | ) | ( | ) | ||||
| 投资活动产生的现金流: | ||||||||
| 为收购正在进行的研发支付的净现金 | ( | ) | ||||||
| 用于投资活动的现金净额 | ( | ) | ||||||
| 融资活动的现金流: | ||||||||
| 发行普通股及认股权证所得款项净额 | ||||||||
| 行使认股权证所得收益 | ||||||||
| 融资活动提供的现金净额 | ||||||||
| 现金净变动额 | ( | ) | ||||||
| 期初现金 | ||||||||
| 期末现金 | $ | $ | ||||||
| 补充现金流信息: | ||||||||
| 支付利息的现金 | $ | $ | ||||||
| 非现金投融资活动补充日程表: | ||||||||
| 发行普通股以收购正在进行的研究和开发 | $ | $ | ||||||
| 向供应商发行普通股 | $ | $ | ||||||
| 发行与权证收购相关的普通股 | $ | $ | ||||||
| 通过无现金行使认购权证发行普通股 | $ | $ | ||||||
附注是这些合并财务报表的组成部分。
| F-6 |
Xenetic生物科学公司。
合并财务报表附注
| 1. | “公司”(The Company) |
背景
Xenetic Biosciences,Inc.(“Xenetic”或“公司”)成立于内华达州,总部设在马萨诸塞州弗雷明翰,是一家生物制药公司,专注于推进创新的免疫肿瘤技术,解决难以治疗的癌症。该公司专有的脱氧核糖核酸酶(DNase)平台旨在通过靶向中性粒细胞胞外陷阱(Net)来改善包括免疫疗法在内的现有治疗的结果,中性粒细胞细胞外陷阱(Net)与癌症进展和对癌症治疗的耐药性有关。Xenetic目前专注于将其系统DNA ase计划推进到临床,作为胰腺癌和局部晚期或转移性实体瘤的辅助治疗。XCART™该公司的个性化嵌合抗原受体(“CAR”)T平台技术是针对患者特定的肿瘤新抗原而设计的,并已证明其在B细胞淋巴瘤中的作用机制。此外,Xenetic还与生物技术和制药公司合作开发其专有药物输送平台, PolyXen®,并根据凝血障碍领域的独家许可安排收取特许权使用费。
公司直接或间接通过其全资子公司Hesperix S.A.(“Hesperix”)和Xenetic Biosciences(英国)Xenetic UK(“Xenetic UK”),以及Xenetic UK、Lipoxen Technologies Limited(“Lipoxen”)、Xenetic Bioscience,InCorporation和 SymBioTec,GmbH(“SymBioTec”)的全资子公司,拥有多个美国(“U.S.”)。联邦商标注册和申请 以及未注册商标和服务标记,包括但不限于XCART、OncoHist™、PolyXen、ErepoXen™和本年度报告中使用的ImuXen™。所有其他公司和产品名称可能是相关公司的商标 。
持续经营和管理层的计划
管理层评估在财务报表发出之日起一年内,是否有条件或事件(综合考虑)令人对本公司作为持续经营企业的能力产生重大怀疑。本公司自成立以来已出现巨额亏损,预计近期将继续出现经营亏损。这些因素令人对其作为持续经营企业的能力产生了极大的怀疑。本公司相信,它可以通过可能的公开或私募股权发行、债务融资、公司合作、关联方融资或其他方式获得资本资源,以继续经营下去。本公司相信,自 本财务报表之日起计,其现有资源将足以为本公司的营运提供至少十二个月的资金。然而,该公司预计,从长远来看,它可能需要额外的资本来实施其业务计划。 未来任何融资的条款、时间和范围将取决于几个因素,包括其产品开发计划取得的进展、其识别和进入许可或其他战略安排的能力、其继续在纳斯达克股票市场(“纳斯达克”)上市的能力,以及与金融、经济、地缘政治、行业和市场状况有关的因素,其中许多因素是其无法控制的。生物技术行业的资本市场可能非常不稳定,这使得未来任何融资的条款、时间和范围都不确定。2022年6月3日,本公司收到纳斯达克上市资格部发出的书面通知(“通知”),通知本公司其普通股的收盘价已连续30个工作日低于1.00美元,因此本公司未遵守“纳斯达克上市规则”第5550(A)(2)条对继续纳入纳斯达克资本市场的最低投标价格要求(“投标价格要求”)。本通知对本公司普通股在纳斯达克资本市场上市没有立即 影响。根据纳斯达克上市规则,本公司有 自通知日期起计180个历日的期间,以重新遵守投标价格要求。因此,公司 必须在2022年11月30日之前重新遵守投标价格要求,如果满足某些其他标准,则有资格额外获得180个日历日的合规期 。2022年12月1日,本公司收到纳斯达克的一封信,通知本公司,尽管 本公司的普通股尚未恢复符合每股1.00美元的最低买入价要求,但纳斯达克已确定 本公司有资格再延长180个历日,或到2023年5月29日才能恢复遵守。纳斯达克的厘定 乃基于本公司符合公开持有股份市值持续上市的要求及纳斯达克资本市场首次上市的所有其他适用要求(买入价要求除外),以及本公司发出书面通知 表示其有意于第二合规期内通过进行反向股票拆分以弥补不足之处。
| F-7 |
| 2. | 风险和不确定性 |
新冠肺炎大流行的影响
2020年3月,世界卫生组织宣布与一种新型冠状病毒株或新冠肺炎的爆发有关的全球大流行。随着联邦、州和地方政府采取缓解措施应对公共卫生危机,疫情对美国的经济状况产生了重大影响,在2020年3月上半月加速,并持续到2021年和2022年,给美国经济带来了重大不确定性。本公司继续评估新冠肺炎疫情对其业务的影响,虽然到目前为止, 尚未对本公司的运营造成重大影响,但本公司目前仍不确定此次 事件可能对本公司未来的运营产生的影响。新冠肺炎疫情对我们的业务、运营和财务业绩的影响程度将取决于许多不断变化的因素,我们可能无法准确预测这些因素,这种不确定性预计将持续一段时间。
乌克兰冲突对行动的影响
俄罗斯入侵乌克兰的短期和长期影响目前很难预测。实施制裁和反制裁可能对整个经济市场产生不利影响,并可能影响我们的业务、财务状况和运营结果。
| 3. | 重要会计政策摘要 |
合并原则
本公司的综合财务报表包括Hesperix、Xenetic UK和Xenetic UK的全资子公司Lipoxen、Xenetic Bioscience、InCorporation、 和SymBioTec的账目。所有重要的公司间余额和交易均已在合并中冲销。
某些前期金额已重新分类 以符合本期的列报方式。
预算的使用
综合财务报表及附注是根据美国公认会计原则(“美国公认会计原则”)编制的。根据美国公认会计原则编制财务报表要求管理层作出估计、判断和假设,这些估计、判断和假设会影响财务报表中报告的资产和负债额、收入、成本和费用以及附注中的披露。实际结果和结果可能与管理层的估计、判断和假设大不相同。
本位币变动
公司 境外子公司的本位币为美元。2014年公司迁至美国时,公司英国子公司的本位币从英镑改为美元。功能货币的变化是在预期的基础上应用的。因此,以前计入累计其他全面收益的任何损益保持不变。
| F-8 |
外币交易 笔
因汇率波动而产生的外币交易产生的已实现和未实现损益在综合全面损失表的“其他收入(费用)”中确认。以本位币以外的货币计价的货币资产和负债按资产负债表日的汇率重新计量为本位币,损益计入综合全面损失表。
金融工具的公允价值
会计准则编纂(“ASC”) 主题820,公允价值计量,公允价值定义为在计量日期在市场参与者之间有序交易中出售资产或转移负债所收取的价格。本公司采用以下公允价值层次结构,将用于计量公允价值的投入划分为三个等级,并根据可获得且对公允价值计量具有重要意义的最低等级的投入进行分类。一级投入是指报告实体在计量日期有能力获得的相同资产或负债在活跃的 市场上的报价。级别2利用非活跃市场中的报价、经纪商或交易商报价或具有合理价格透明度水平的替代定价来源。第三级投入是资产或负债的不可观察的投入,在计量日期,该资产或负债的市场活动很少(如果有的话)。截至2022年12月31日及2021年12月31日,本公司若干金融工具的账面价值因到期日较短而接近公允价值。见注9,公允价值计量,以讨论公司的公允价值计量。
现金和信用风险的集中度
本公司将自购买之日起90天或以下的所有高流动性投资 视为现金等价物。自购买之日起超过90天但自资产负债表之日起不到一年的原始到期日为 的投资归类为短期投资,而自资产负债表日起一年及以上的投资归类为长期投资。管理层在购买时确定其现金等价物和投资证券的适当分类,并在每个资产负债表日期重新评估此类确定。由于这些工具的短期性质,现金等价物的账面价值接近其公允价值。
可能使公司面临信用风险的金融工具主要包括存放在金融机构的现金,其余额经常超过联邦 保险限额。2023年3月10日,硅谷银行(SVB)被加州金融保护和创新部关闭,后者任命联邦存款保险公司(FDIC)为接管人。本公司的现金主要为SVB持有的货币市场基金。2023年3月12日,美国财政部、美联储和FDIC推出了紧急措施 以全面保护SVB的所有储户,2023年3月13日,我们完全可以使用我们在SVB的存款现金。因此,公司 预计不会出现任何与该等余额有关的损失。
财产和设备
本公司按 成本减去累计折旧的价格记录财产和设备。用于延长资产寿命或使用寿命的重大更新和改进支出 计入资本化。普通维修或维护性质的项目在发生时直接计入运营费用。公司 使用直线法计算资产的预计使用寿命内的折旧:
| 资产分类 | 预计使用寿命 | |
| 办公室和计算机设备 | ||
| 租赁权改进 | ||
| 家具和固定装置 |
本公司将报废或以其他方式处置的资产的成本与相应的累计折旧一起从相关账户中剔除,由此产生的收益或 损失将反映在经营结果中。
| F-9 |
无限期-活着的无形资产
在业务 合并、许可及其他交易中取得的资产及承担的负债一般于收购日期按各自的公允价值确认。在 收购时,我们一般使用“收益法”确定无形资产的公允价值,包括正在进行的研发(“IPR&D”)。收购的知识产权研发无形资产被视为无限期无形资产,在相关研究和开发工作完成或放弃之前不会摊销。在公司的知识产权研发达到技术可行性之前,可能还需要进行大量的额外研究和开发。知识产权研发项目完成后, 知识产权研发资产将在其预计使用寿命内摊销。
知识产权研发不摊销,但至少每年或当商业环境的事件或变化表明账面价值可能减值时,对减值进行审查。 公司还可以选择首先评估定性因素,以确定事件或情况的存在是否导致公司确定收购的知识产权研发受到损害的可能性更大(即超过50%) 。如果公司选择首先评估质量因素,并确定知识产权研发减值的可能性并不比未收购的更大,则公司无需采取进一步行动测试减值。公司还可以选择绕过定性评估,仅执行量化减值测试,公司可以选择在某些期间执行该测试 ,而不在其他期间执行。
减值损失(如有)按无形资产的账面价值超出其公允价值计量。
无形资产极易受到减值费用的影响 ,尤其是用于知识产权研发的新收购资产。考虑到研发的高风险性质以及行业将开发化合物推向市场的成功率,知识产权研发减值费用可能在未来一段时间内发生。估计 潜在减值的IPR&D的公允价值对预测和假设的变化高度敏感,假设的变化可能会导致减值。本公司相信其估计及假设均属合理,并在其他方面与市场参与者在估计公允价值时会采用的假设相符。然而,如果未来的结果与公司的估计和假设不一致,公司可能会面临减值费用,这可能是一笔重大费用。使用不同的估计 和判断可能在公司的分析中产生重大不同的结果,并可能导致重大不同的资产 价值或费用。
长期资产减值准备
当事件或环境变化显示资产或资产组的账面金额 可能无法完全收回时,本公司会审核应持有和使用的长期资产,包括财产和设备的减值。
可回收性评估 基于对资产或资产组的使用及其最终处置所产生的未贴现未来现金流量的估计。 减值(如果有的话)按资产的账面价值超出其公允价值的金额计算,通常使用贴现的 现金流量来确定公允价值。在截至2022年12月31日和2021年12月31日的年度内,没有记录到此类减值。
| F-10 |
收入确认
该公司与制药和生物技术合作伙伴签订供应、许可和合作协议,其中一些协议包括基于经批准的商业医药产品的潜在净销售额的特许权使用费协议。
公司根据ASC主题606确认收入,与客户签订合同的收入(“ASC 606”)。本标准适用于与客户签订的所有合同, 属于其他标准范围的合同除外,如租赁、保险、合作安排和金融工具。根据ASC 606,实体在其客户获得对承诺商品或服务的控制权时确认收入,其金额 反映了该实体预期以该等商品或服务换取的对价。为了确定实体确定在ASC 606范围内的安排的收入确认,该实体执行以下五个步骤:(I)确定与客户的合同;(Ii)确定合同中的履约义务;(Iii)确定交易价格;(Iv)将交易价格分配给合同中的履约义务;以及(V)在履行履约义务的时间点或时间上确认收入。公司仅在有可能收取其有权获得的对价以换取其转让给客户的商品或服务时,才将五步模式应用于合同。在合同开始时,一旦合同被确定在ASC 606的范围内,公司将评估每份合同中承诺的商品或服务,确定 属于履约义务的商品或服务,并评估每项承诺的商品或服务是否不同。然后,本公司将在履行履约义务时分配给相应履约义务的交易价格的金额确认为收入 。
作为此等安排的会计安排的一部分,本公司必须使用重大判断来确定:a)根据上文第(Br)(Ii)步的确定确定的履约义务的数量;b)上文第(Iii)步下的交易价格;以及c)上文第(Iv)步交易价格分配合同中确定的每项履约义务的独立售价。本公司使用判断来确定是否应将里程碑 或其他可变对价计入交易价格,如下所述。交易价格按相对独立销售价格分配给每项履约义务,公司在履行合同项下的 履约义务时确认收入。在制定履约义务的独立价格时,公司 会考虑适用的市场条件和相关实体特定的因素,包括与客户谈判 协议时考虑的因素和估计成本。本公司通过评估用于确定独立销售价格的关键假设的变化是否会对多个履约义务之间的交易价格分配产生重大影响,从而验证履约义务的独立销售价格。公司确认合同资产或负债,以弥补公司业绩(即,转让给客户的货物或服务)与客户业绩之间的差额 (即,客户支付并无条件应支付的对价)。
公司许可协议的条款 可能包括向协作合作伙伴交付知识产权许可。根据许可证安排,合作伙伴可通过不可退还的预付收据、开发和监管目标收据以及未来产品销售的版税收据组合获得补偿 。公司预计将确认公司在许可证和合作安排中收到的不可退还的预付许可证付款以及开发和监管里程碑付款 ,其中包括未来的义务,如供应义务,在公司根据各自安排的预期业绩期间按比例 。公司对公司预计履行公司业绩义务的时间做出最佳估计,包括技术转让援助、 研究活动、临床开发活动以及从产品开发到产品商业化的制造活动。鉴于这些协作安排的不确定性,需要做出重大判断来确定 实施期的持续时间。
当公司达成再许可其部分专利的安排时,在确定收入确认的适当方法和时间时,公司将考虑履行义务,以确定该安排是单一要素还是多要素 。除履行其向安排提供服务、专利保护费用、技术支持、营销或销售协助等 或任何其他可能构成可能改变收入确认时间的额外交付内容的 内容的任何履行义务外,公司还会考虑许可证的条款 或针对价格调整或退款条款等要素的子许可。收到的不可退还的预付许可和 分许可费用被视为与相关许可技术无关或敷衍了事的继续履行或未来义务,在交付技术时确认为收入。
| F-11 |
公司预计将根据基本合同条款在销售期内确认特许权使用费收入,前提是报告的销售额可以可靠地衡量,公司没有剩余的履约义务,并且满足所有其他收入确认标准。公司预计,公司完成的与合作协议相关的研究和开发服务的报销将在运营中确认为总收入 。公司与某些合作伙伴签订的许可协议和合作协议还可以规定未来向公司提供里程碑式的收据,完全基于各自合作伙伴在考虑截止日期延长时的表现 或达到批准药品的指定销售量。对于此类收据,公司希望将根据适用合同条款按履约或按比例在协议期限内赚取的收据确认为收入。 当公司的持续履行或未来义务被视为无关紧要或敷衍了事时,这些收据也可能被确认为收入。
另见注4,重要的战略协作.
研究和开发费用
研发费用是指在进行研发活动中发生的费用,包括薪酬福利、设施费用、管理费用、临床前开发、临床试验及相关临床制造费用、支付给合同研究机构(“CRO”)和合同制造机构(“CMO”)的费用以及其他外部费用。本公司用于支付已发生的研发费用。本公司为研发服务支付的前期费用不可退还,因为已产生 义务。归属于收购但未达到资本化标准的无形资产的价值在收购时计入研究和开发费用。根据许可协议支付的预付款将在收到许可时支出。里程碑 在确定里程碑可能实现且相关金额可合理评估的期间,根据许可协议应计付款,并确认相应的费用。
公司需要估算每个报告期的应计研究和开发费用。这一流程包括审查未结合同和采购订单,与公司人员沟通以确定已代表公司执行的服务,并在公司尚未收到发票或以其他方式通知公司实际成本时,估算执行的服务级别和服务产生的相关成本。本公司的大多数服务提供商都会按照预定的时间表或在达到合同里程碑时为所提供的服务开具欠款发票。但是, 有些需要预付款。本公司根据当时已知的事实和情况,在财务报表中对截至每个资产负债表日期的应计费用进行估计。公司定期与服务提供商确认估计的准确性,并在必要时进行调整。估计应计研究和开发费用的例子包括支付给下列人员的费用:
|
· · |
合作伙伴开展研发和临床前活动 ; 与临床试验的整体项目管理相关的项目经理; | |
| · | 与cGMP制造有关的cMOS; | |
| · | 与临床试验相关的CRO;以及 | |
| · | 与临床试验相关的调查网站。 |
本公司根据与代表本公司进行和管理临床试验的多个研究机构、CMO和CRO的报价和合同,对收到的服务和花费的努力进行的估计,作为与研究和开发、临床前活动、制造和临床试验相关的费用。这些协议的财务条款有待协商,不同的合同会有所不同,并可能导致不均衡的付款
流量。在某些情况下,向供应商支付的款项可能会超过所提供的服务水平,从而导致费用的预付款
。在应计服务费时,公司估计将提供服务的时间段和每段时间内要花费的努力程度。如果实际执行服务的时间或努力程度与估计值不同,公司将相应调整应计或预付金额。虽然预计其估计与实际发生的金额不会有实质性差异,但公司对所提供服务的状态和时间相对于实际状态和时间的理解可能会有所不同,并可能导致报告的金额在任何特定时期过高或过低。到目前为止,
公司对应计研发费用的先前估计没有任何重大调整。截至2022年12月31日、2022年12月31日和2021年12月31日,公司记录的累计计划费用约为$
| F-12 |
本公司以期权和限制性股票单位(“RSU”)的形式向雇员和非雇员授予以股份为基础的付款,以购买本公司的普通股股份,向雇员授予股份所有权计划(“JSOP”)奖励,以及发行普通股以换取非雇员提供的服务的协议。
基于股份的费用基于期权的估计公允价值或使用Black-Scholes期权定价模型计算。确定适当的公允价值模型和相关假设需要判断,包括估计股价波动和预期奖励条款。预期波动率 是根据公司的历史波动率估算的。在无法获得奖励的整个预期期限内的公司数据的范围内,公司使用本公司和可比上市公司的同行集团在期权预期期限内的历史波动性的加权平均。预期期限代表期权预计未完成的时间。 本公司在没收发生时而不是授予时对没收进行会计处理。本公司并未派发股息,亦不预期在可见未来派发现金股息,因此预期股息率为零。无风险利率 基于到期日与奖励预期期限一致的美国国债利率。行权时,新发行普通股的股票期权将被赎回。当符合授予的归属和结算条款时,RSU将赎回新发行的普通股股份。
对于仅根据服务条件授予的员工期权,公允价值计量日期通常为授予之日,相关薪酬支出在奖励的必要归属期间以直线方式确认 。对于为交换公司运营中消耗的商品或服务而发行的非员工期权 ,公允价值计量日期为服务完成日期或绩效承诺达成日期中较早的日期。本公司一般认为,股票期权的公允价值 比接受服务的公允价值更可靠地计量。与授予非员工的股票期权相关的薪酬支出 在奖励的必要归属期间以直线基础确认。
认股权证
关于某些融资、咨询和合作安排,本公司已发行认股权证购买其普通股股份。未偿还权证为独立工具,持有人不可出售或强制赎回,并分类为股权奖励。 本公司使用Black-Scholes期权定价模型计量截至计量日期的奖励的公允价值。在发行普通股的同时,向合作伙伴发行的认股权证最初按公允价值计入已发行普通股的额外实收资本的减少。所有其他认股权证均按公允价值在所需服务期内按直线计入费用,或在没有服务期或已提供服务的情况下于发行之日按公允价值计入费用。与正在进行的安排有关的授权证 在附注11中有更全面的说明,股东权益.
所得税
公司使用 资产负债法核算所得税。根据这一方法,递延税项资产和负债是根据因税务和财务报告目的对项目的不同处理而产生的暂时性差异确定的。递延税项资产及负债以 颁布税率计量,预期适用于该等暂时性差异可望扭转的年度的应税收入。此外,公司必须评估递延税项资产从未来应纳税所得额中扣除的可能性。本公司按季度评估其递延税项资产的可回收性。
| F-13 |
本公司计算每股基本净亏损的方法为:适用于普通股股东的净亏损除以期内公司已发行普通股的加权平均股数 。本公司在考虑期内已发行的股票期权的摊薄效应后计算每股摊薄净亏损,除非该等非参与证券具有反摊薄作用。本公司的JSOP 奖励在行使前被本公司视为库藏股,因此不影响本公司每股净亏损的计算 。截至2022年12月31日和2021年,每年都有大约颁发了JSOP奖项。
在截至2022年12月31日和2021年12月31日的年度内,由于公司的净亏损状况,每股基本净亏损和稀释后每股净亏损均相同。潜在摊薄、不参与的证券 未计入每股摊薄净亏损的计算,因为纳入这些证券将是反摊薄的。截至2022年12月31日和2021年12月31日,大约和潜在稀释证券分别被认为是反稀释证券。
细分市场信息
经营部门被确定为企业的组成部分 ,其独立的财务信息可供首席运营决策者(即公司首席执行官)进行评估,以就如何分配资源和评估业绩做出决策。公司 在一个运营部门中查看其运营并管理其业务。
租契
本公司根据 经营租约租赁行政设施。租赁协议可能包括租金假期、租金上涨条款和租户改善津贴。本公司根据ASU 2016-02对租赁进行会计处理,租赁(主题842)。ASU 2016-02要求承租人在开始之日确认除短期租赁外的所有租赁的租赁负债和使用权资产。见附注14,承付款和 或有以获取更多信息。
收购
该公司有从事收购交易的历史,这些交易要求公司评估该交易是否符合业务合并的标准。如果交易 不符合业务合并要求,则交易将被计入资产收购或资本重组,并且不确认商誉。如果收购符合企业合并的定义,本公司将收购价格(包括任何或有对价)分配给收购资产和于收购日期按其估计公允价值承担的负债,支付的收购价格超过收购净资产估计公允价值的任何部分计入商誉。 收购资产和承担负债的公允价值通常通过估计重置成本或 贴现现金流量估值方法确定。
本公司在厘定所收购有形资产的公允价值时,会考虑年龄、状况 及资产的经济使用年限等因素,估计以新资产取代该资产的成本。在确定所收购无形资产的公允价值时,本公司使用判断来估计适用的贴现率、增长率以及未来现金流的时间和金额。购置的资产和承担的负债的公允价值通常是在独立第三方专家的协助下确定的。
企业合并相关成本在发生成本的期间计入 。与资产收购相关的成本通常作为所收购资产成本的一部分进行资本化。
| F-14 |
最新会计准则
2016年6月,FASB发布了ASU 2016-13,金融工具-信用损失(主题326):金融工具信用损失的计量。该指导意见修改了对大多数金融资产和某些其他工具的信贷损失的计量和确认。修正案更新了按摊销成本计量和记录金融资产信贷损失的指导方针,将“已发生损失”模型替换为“预期损失”模型。这可能导致提早确认损失准备。ASU 2016-13适用于2022年12月15日之后开始的财年中较小的报告公共实体,但允许提前采用。公司将继续评估采用的影响,但我们预计这不会对我们的合并财务报表产生实质性影响。
| 4. | 重要的战略协作 |
武田药品工业株式会社(及其全资子公司武田)
2017年10月,本公司授予武田
授予与本公司的PolyXen技术相关的某些专利的非排他性再许可的权利,这些专利之前
独家授权给武田与治疗血液和出血疾病相关的产品。版税支付
约为$
Catalent Pharma Solutions LLC(“Catalent”)
2022年6月30日,公司与Catalent签订了一份工作说明书(SOW),概述了一般工作范围、时间表和定价,据此,Catalent将向公司提供某些服务,以执行公司重组蛋白质人DNA I的cGMP生产。双方
同意签订主服务协议(MSA),其中将包含管理SOW所预期项目的条款和条件,并将取代包含Catalent标准条款和条件的SOW附录。此外,如果SOW中规定的特定于项目的条款和条件与MSA之间存在任何冲突,则应以MSA条款和条件为准。在项目期限内,SOW计划的项目制造服务的估计总成本预计高达约500万美元(不包括某些费用和潜在的替代方案),项目的每个阶段都与该阶段的开始相关地单独开具发票。除非之前进行修订或终止,否则SOW计划的制造服务目前的目标是在2024年上半年完成。公司可在提前30天书面通知Catalent的情况下随时终止SOW。SOW还包含与保密、保证、知识产权和赔偿等相关的惯例条款。在截至2022年12月31日的年度内,公司向Catalent
支付了约$
| F-15 |
斯克里普斯研究公司
2020年5月15日,公司与斯克里普斯研究院(“斯克里普斯研究所”)签订了一项研究资助和期权协议(“斯克里普斯协议”),根据该协议,公司同意向斯克里普斯研究所提供总额高达300万美元的资金,以资助与推进XCART临床前开发有关的研究。研究经费由本公司根据商定的预算按季度支付给斯克里普斯研究公司,该预算规定在斯克里普斯协议签订之日向斯克里普斯研究公司支付首期约300,000美元,随后在27个月内按季度支付约300,000美元。根据斯克里普斯协议,斯克里普斯研究公司已根据与斯克里普斯研究公司于2019年2月25日签订的、于2019年3月1日转让给本公司的该特定许可协议的条款,向本公司
授予该领域内的任何专利权或技术(定义见斯克里普斯协议)
。此外,公司可以选择获得斯克里普斯研究公司在技术上的权利或尚未授权给公司的专利权的全球独家许可,以及非独家、免版税、不可转让的许可,使斯克里普斯研究技术(如斯克里普斯协议中的定义)在
执行斯克里普斯协议所设想的研究计划期间仅用于公司内部研究目的。在2022年第二季度,双方相互同意终止斯克里普斯协议项下的额外资金。因此,斯克里普斯研究公司同意继续根据该协议开展工作,直到之前预付的资金用完为止。该公司支付了$
PJSC药物合成
2009年11月,本公司与Pharmsynz签订了合作研发许可协议(“Pharmsynz安排”),据此,本公司向Pharmsynz授予独家许可,允许其在某些地区开发、商业化和营销基于本公司的PolyXen和ImuXen技术的六种候选产品。作为交换,Pharmsynz向该公司授予独家许可,允许其在Pharmsynz协议范围内使用Pharmsynz开发的任何临床前和临床数据,并在某些地区以外进行进一步研究、开发和商业化,费用由公司自费。
Pharmsynz直接或间接通过其全资子公司SynBio,LLC(“SynBio”)持有本公司约
2020年6月12日,本公司与Pharmsynz 签订了主服务协议(“Pharmsynz MSA”),以推进本公司针对B细胞恶性肿瘤的XCART技术 的开发。根据Pharmsynz MSA,Pharmsynz同意根据双方不时商定的工作指令提供服务,这些服务包括但不限于,充当公司的主要合同研究机构 ,以协助管理与俄罗斯和白俄罗斯多个学术机构的合作。根据每个工单中规定的预算和付款条件,公司需要支付Pharmsynz在提供服务时发生的合理费用、开支和传递成本。此外,如果工作订单规定了里程碑付款,则公司必须根据工作订单中规定的条款, 向Pharmsynz或Pharmsynz指定的第三方服务提供商支付此类付款,该里程碑付款可由公司自行决定以现金或公司普通股的股票支付。
| F-16 |
本公司和Pharmsynz于2020年6月12日根据Pharmsynz MSA执行了一份工作订单(“工作订单”),根据该工作订单,Pharmsynz同意根据该工作订单中规定的研究计划对本公司的XCART技术进行第一阶段研究。根据工作订单执行的活动预计需要大约20个月的时间,除非根据Pharmsynz MSA提前终止。
工作订单规定,在与第三方站点签订合同后,由Pharmsynz为额外的传递成本开具发票。此外,工作单规定,在达到工作单规定的与完成研究计划早期阶段相关的里程碑时,公司将支付或发行总额高达1,050,000美元的里程碑付款,或由公司自行
酌情支付或发行总计1,000,000股公司普通股。截至2022年12月31日,大约$
2021年10月12日,本公司与Pharmsynz签订了Pharmsynz MSA的第1号修正案(“MSA修正案”),终止了Pharmsynz MSA下的所有 工单。因此,不会在工单下执行进一步的服务,任何额外的 服务将包含在新的工单中。作为交换,公司与MSA修正案同时签订了新的工单(“第二工单”) 。根据第二份工作单的条款,Pharmynz应公司的书面要求提供某些列举的服务以支持公司开发其XCART技术,该工作可能是公司不时提出的 。
根据MSA修正案和第二工单,在进入第二工单时,公司一次性支付了$
2011年8月,SynBio与本公司签订了股票认购及合作开发协议(“共同开发协议”)。该公司向SynBio授予了 独家许可证,允许其利用基于SynBio技术的分子和该公司在俄罗斯和独联体的专有技术(PolyXen、OncoHist和ImuXen)开发、营销和商业化某些候选药物,这里统称为SynBio市场。作为回报,SynBio授予该公司独家许可证,允许其在某些商定的产品中使用SynBio产生的临床前和临床数据,并在SynBio市场以外的任何地区从事商业候选产品的开发。
Synbio独自负责资助和开展他们自己的研究和临床开发活动。除每家公司根据各自的技术提供各自的研究用品的费用外, 共同开发协议没有规定任何里程碑或其他与研究相关的付款。 提供时,这些费用是由于双方的便利,并不代表提供研究用品的持续或经常性义务。 在任何最终产品成功商业化后,公司有权在某些地区的销售中获得10%的特许权使用费 ,并根据共同开发协议的条款,向SynBio支付在该等地区以外的销售的特许权使用费。自2021年12月20日起,SynBio将共同开发协议转让给Pharmsynz。
到2022年12月31日,Pharmsynz继续从事研究和开发活动,没有产生任何商业产品。2020年12月,Pharmsynz报告了其Epolong的3期临床研究的阳性数据,Epolong是一种利用该公司的PolyXen技术治疗慢性肾脏疾病患者贫血的药物。2021年2月,Pharmsynz在一份新闻稿中报告称,它已经开始了Epolong的注册阶段,
提交了注册档案以获得俄罗斯的批准。Pharmsynz在其新闻稿中报告称,预计俄罗斯阶段的注册活动将于2021年完成,最早将能够在2022年第一季度开始生产该产品。Pharmsynz已通知本公司,它已收到一封回复信,指出档案中的某些缺陷,并打算在更正后重新提交注册。《公司》做到了
| F-17 |
印度血清研究所有限公司
2011年8月,公司与印度血清研究所有限公司(“血清研究所”)签订了合作研发协议,向血清研究所授予使用公司的PolyXen技术研发潜在商业产品Polysialylated Erythropoietin的独家许可。血清研究所负责进行在特定预定区域内获得监管批准所需的所有临床前和临床试验,费用由血清研究所自费。塞缪尔研究所向该公司支付版税,用于向塞缪尔研究所销售区域的某些客户进行净销售。根据合作安排,没有里程碑或其他与研究相关的 付款到期。
截至2022年12月31日,公司未开发任何商业产品 ,也未确认任何与该安排相关的特许权使用费收入或支出。截至2022年12月31日和2021年12月31日,血清研究所分别持有不到公司全部已发行普通股的股份 。
| 5. | 发牌安排 |
排他性再许可协议。
于2022年4月26日,本公司与CLS治疗有限公司(“CLS”)订立 独家再许可协议(“再许可协议”),据此,本公司获得独家许可,根据CLS拥有或控制的若干专利权及专有技术,开发及商业化使用DNA酶治疗癌症的 药物产品及方法(“再许可产品”)。 根据再许可协议的条款,本公司将独家负责,并应使用商业上合理的努力,其中包括,研究,在美国和某些欧洲市场开发并获得再授权产品的营销批准,并在获得营销批准后在相关市场将此类再授权产品商业化。
作为根据分许可协议授予公司的许可和其他权利的代价,公司向CLS颁发本公司普通股股份(“再许可协议股份”),其中250,000股再许可协议股份直接发行予OPKO Health,Inc.(“OPKO”) ,以代替由CLS间接转让给OPKO的全资附属公司EirGen Pharma Ltd.(“EirGen”),以履行CLS与EirGen之间的若干第三方合同义务。此外,本公司有责任向CLS支付最多13,000,000美元现金,作为实现某些临床和监管里程碑的潜在里程碑付款,并根据实现某些监管里程碑向CLS额外发行950,000股公司普通股。此外, 公司有义务对在许可期限内(如再许可协议中的定义)在许可范围内的许可产品的净销售额支付中位数-个位数到低-两位数不等的分级使用费,并在公司从任何分许可人收到的一定对价的 中低档青少年中支付一定比例的使用费。
独家许可协议
于2022年4月26日,本公司与CLS订立独家许可协议(“许可协议”),据此,本公司获得由CLS拥有或控制的若干专利权及专有技术下的独家许可,以开发及商业化结合DNase及CAR T疗法的医药产品及方法(“获许可产品”)。根据许可协议的条款,公司 将独家负责,并应尽商业上合理的努力,除其他事项外,研究、开发和获得许可产品在美国和某些欧洲市场的销售批准,并在获得销售批准后,将此类许可产品在相关市场进行商业化。
作为根据许可协议授予本公司的许可及其他权利的代价,本公司向CLS一次性支付$
| F-18 |
再许可和
许可协议的总对价约为$
专利转让与意志协作
2022年10月4日,该公司完成了与比利时威力SARL有限公司(“威力”)和CLS合作的专利转让。关于专利转让,本公司于2022年10月12日与特拉华州有限责任公司CLS Treeutics,LLC(“CLS LLC”)订立认购协议,据此,本公司同意向CLS LLC发行本公司普通股(“股份”),而CLS LLC同意认购850,000股本公司普通股(“股份”),作为CLS及其关连公司向本公司转让由CLS及其关连公司拥有的若干专利权的代价。
2022年8月2日,该公司宣布与Wilition进行研究和开发合作,开发以Net为目标的采用细胞疗法治疗癌症。Collaboration 是一个早期的探索性计划,旨在评估意志的Nu.Q的潜在组合®技术测试和 公司的DNase-Armored Car T平台,开发可能针对多种实体癌症的专利采用细胞疗法。根据合作协议的条款,Wilition将为一个研究项目提供资金,双方将分享合作产生的任何产品的商业化或许可收益。
专利转让的总代价约为50万美元,相当于利用收市价发行的850,000股普通股的公允价值
公司股票于截止日期的收盘价。由于专利权未来没有其他用途,公司记录了一笔约$的费用
该公司产生了大约$
| 6. | 财产和设备,净额 |
财产和设备,净额包括以下内容:
| 2022年12月31日 | 12月31日, 2021 | |||||||
| 办公室和计算机设备 | $ | $ | ||||||
| 家具和固定装置 | ||||||||
| 财产和设备--按成本计算 | ||||||||
| 减去累计折旧 | ( | ) | ||||||
| 财产和设备,净额 | $ | $ | ||||||
曾经有过
| F-19 |
| 7. | 其他资产 |
2016年,公司
与血清研究所达成协议,预付临床PSA用品,以换取该公司的普通股。截至2022年12月31日和2021年12月31日,公司已将美元
另见附注15,相关的 方交易以获得有关Pharmsynz贷款的描述。
| 8. | 应计费用 |
应计费用包括以下内容:
| 2022年12月31日 | 12月31日, 2021 | |||||||
| 应计薪资和福利 | $ | $ | ||||||
| 应计专业费用 | ||||||||
| 应计研究费用 | ||||||||
| 其他 | ||||||||
| 应计费用总额。 | $ | $ | ||||||
| 9. | 公允价值计量 |
ASC主题820,公允价值计量,
将公允价值定义为在计量日期在
市场参与者之间有序交易中出售一项资产或支付转移一项负债而收到的价格。本公司采用以下公允价值等级,将用于计量公允价值的投入划分为三个等级,并根据可获得的、对公允价值计量有重要意义的最低等级的投入在等级内进行分类。一级投入是指报告实体在计量日期有能力获得的相同资产或负债在活跃市场的报价
。第2级利用非活跃市场的报价、经纪商或交易商报价,或具有合理价格透明度的替代定价来源。第三级投入是资产或负债的不可观察的投入,在计量日期,资产或负债的市场活动很少(如果有的话)
。截至2022年12月31日和2021年12月31日,由于到期时间较短,本公司金融工具的账面价值接近公允价值。有几个
| 10. | 所得税 |
递延税项资产和负债是根据因税务和财务报告目的对项目的不同处理而产生的暂时性差异确定的。递延税 资产和负债采用制定的税率计量,预计适用于那些暂时性 差额有望逆转的年度的应纳税所得额。此外,公司必须评估递延税项资产从未来应纳税所得额中扣除的可能性。本公司已就本公司的递延税项资产提供全额估值津贴 因为本公司认为其递延税项资产更有可能无法变现。本公司按季度评估其递延税项资产的可回收性。截至2022年12月31日及2021年12月31日止年度并无所得税拨备(利益),因本公司迄今已出现亏损。
| F-20 |
所得税前亏损构成如下 :
| Year ended December 31, | ||||||||
| 2022 | 2021 | |||||||
| 国内(美国) | $ | ( | ) | $ | ( | ) | ||
| 外国(英国) | ||||||||
| 外国(德国) | ( | ) | ( | ) | ||||
| 外国(瑞士) | ( | ) | ( | ) | ||||
| 所得税前亏损 | $ | ( | ) | $ | ( | ) | ||
所得税优惠与美国公司税率(适用于公司所在国家/地区的税率)与净收益的对账如下:
| Year ended December 31, | ||||||||
| 2022 | 2021 | |||||||
| 联邦制 | $ | ( | ) | $ | ( | ) | ||
| 状态 | ( | ) | ( | ) | ||||
| 更改估值免税额 | ||||||||
| 永久差额,净额 | ||||||||
| 外币利差 | ( | ) | ( | ) | ||||
| 基于股份的支付,净额 | ||||||||
| 增强的研发税收抵免 | ( | ) | ( | ) | ||||
| 汇率变化 | ( | ) | ||||||
| 其他项目 | ( | ) | ( | ) | ||||
| 所得税净收益 | $ | $ | ||||||
| F-21 |
递延税项资产和负债反映了用于财务报告目的的资产和负债的账面价值与用于所得税目的的金额之间的暂时性差异所产生的税净影响。该公司递延税项资产的重要组成部分如下:
| Year ended December 31, | ||||||||
| 2022 | 2021 | |||||||
| 递延税项资产: | ||||||||
| 英国净营业亏损结转 | $ | $ | ||||||
| 英国资本损失结转 | ||||||||
| 美国联邦净营业亏损结转 | ||||||||
| 瑞士净营业亏损结转 | ||||||||
| 知识产权研发 | ||||||||
| 基于股份的支付 | ||||||||
| 增强的研发税收抵免 | ||||||||
| 德国净营业亏损结转 | ||||||||
| 资本化研究和实验支出 | ||||||||
| 美国各州净营业亏损结转 | ||||||||
| 其他 | ||||||||
| 租赁责任 | ||||||||
| 估值扣除前的递延税项资产总额 | ||||||||
| 递延税项资产的估值准备 | ( | ) | ( | ) | ||||
| 递延税项净资产 | ||||||||
| 递延税项负债: | ||||||||
| 使用权--资产租赁 | ( | ) | ||||||
| 递延税项负债总额 | ( | ) | ||||||
| 递延负债净额 | $ | $ | ||||||
截至2022年12月31日、2022年12月31日及2021年12月31日止年度,本公司的英国净营业亏损结转约为$
本公司使用其在美国产生的营业亏损结转和税收抵免来抵销未来应税收入的能力 受《美国国内税法》(以下简称《准则》)第382节的限制。如果发生守则中所述的某些所有权变更,这些限制可能会限制未来使用 营业亏损结转和税收抵免。未来股票所有权可能发生变化,这将对本公司使用营业亏损结转和税收抵免造成进一步限制。在这种情况下,公司可能被要求缴纳所得税,即使存在重大的经营亏损结转和税收抵免。
| F-22 |
公司使用其在英国产生的营业亏损结转和税收抵免的能力 受英国税法的限制。 这些法规可能会限制未来使用营业亏损结转:(I)如果所有权发生变化,公司经营的业务性质或行为发生变化,以及(Ii)在某些情况下,仅在业务性质或业务行为发生变化的情况下。在这种情况下,结转将不再可用于抵销未来的收入。
该公司利用其在德国和瑞士产生的营业亏损结转和税收抵免的能力也受到德国和瑞士税法的限制。如果所有权发生变化,这些规定可能会限制未来使用营业亏损结转。 在这种情况下,结转将不再可用于抵销未来的收入。
截至2022年12月31日和2021年12月31日,公司
公司在美国联邦税收管辖区、马萨诸塞州税收管辖区和某些外国税收管辖区提交所得税申报单。在截至2022年的日历纳税年度内,由于可用净营业亏损、结转亏损和研发税收抵免,公司将接受美国联邦、州、外国和地方所得税当局的审查
。截至2022年12月31日,国税局或任何其他税务机关尚未通知本公司任何审查
。该公司拥有
潜在的382限制
本公司的净营业亏损和税收 抵免结转将受到美国国税局的审查和可能的调整。本公司利用其净营业亏损(“NOL”)及研发信贷(“R&D”)结转的能力可能受到实质上的 限制,原因是根据守则第382节及国家类似条文的要求,所有权可能已发生或未来可能发生的变更。这些所有权变更可能会限制每年可分别用于抵消未来应税收入和税收的NOL和研发信贷结转金额 。一般而言,根据守则第382节的定义,所有权变更是指由某些股东或公众团体在三年内进行的一项或一系列交易,导致所有权变更超过公司已发行股票的50%。
本公司尚未完成评估 本公司自成为守则第382节所界定的亏损公司以来是否曾发生一次或多次所有权变更的研究,但 本公司认为很可能已发生所有权变更。如果公司经历了所有权变更,NOL和研发信贷结转的使用将受到年度限制,该限制首先通过将所有权变更时公司普通股的价值 乘以适用的长期免税税率确定,然后根据需要进行额外调整。任何此类限制都可能导致NOL或研发积分的一部分在使用前到期 。在研究完成且已知任何限制之前,任何金额都不会被视为不确定的税收状况或披露为未确认的税收优惠。任何因该等限制而在使用前到期的结转将从递延税项资产中剔除,并对估值免税额作出相应调整。由于估值拨备的存在,预计任何潜在限制不会对本公司的经营业绩产生重大影响。
主要税务管辖区(即马萨诸塞州联邦)可能会不时评估该公司的利息或罚款。截至2022年12月31日,公司没有未确认的重大税收优惠,也不需要对负债或运营进行调整。
| F-23 |
| 11. | 股东权益 |
普通股
公司普通股的每股股份使持有人有权就提交公司股东表决的所有事项投一票。普通股股东 在董事会宣布时有权获得股息。在本公司发生任何自愿或非自愿清算、解散或清盘的情况下,普通股持有人有权按比例分享本公司可供分配的资产。
授权份额增加
2022年12月21日,公司股东投票通过了公司章程修正案,将法定普通股增加到股份(“授权增持股份”)。本公司于2022年12月21日向内华达州州务卿提交本公司公司章程修订证书,以实施授权股份增加。
在市场(“自动取款机”)上提供
于2021年11月19日,本公司与作为独家销售代理(“Wainwright”)的H.C.Wainwright&Co.,LLC订立自动柜员机发售协议(“ATM协议”),根据该协议,本公司可不时透过Wainwright提供及出售其普通股股份,面值为$。每股 。股份的发售将根据2021年10月12日提交给美国证券交易委员会并于2021年10月22日宣布生效的S-3表格搁置登记声明(第333-260201号文件)和相关招股说明书进行,目前仅限于 其根据自动柜员机协议可以出售的不超过400万美元的证券,前提是本公司根据S-3表格I.B.6一般指示可以出售的证券数量可能受到限制。
根据自动柜员机协议,Wainwright可以根据证券法 颁布的第415条规则的定义,在销售中出售被视为“按市场”发行的股票,包括直接在或通过纳斯达克资本市场进行的销售。如果在单独的条款协议中达成一致,本公司可以Wainwright与本公司商定的收购价向Wainwright作为本金出售股份。Wainwright还可以在获得公司事先批准的情况下,以私下协商的交易方式出售股份。通过Wainwright出售股份(如有)将按本公司不时厘定的金额及时间作出,但本公司并无义务出售任何股份 本公司或Wainwright可随时暂停协议下的要约或终止协议。实际销售额将取决于本公司不时确定的各种因素,包括(其中包括)市场状况、本公司普通股的交易价格以及本公司对本公司适当资金来源的决定。根据自动柜员机协议的股份要约及出售将于(A)根据自动柜员机协议发行及出售所有 股份或(B)Wainwright或本公司根据自动柜员机协议的条款终止自动柜员机协议时终止。
股份于截至2022年12月31日及2021年12月31日止年度根据自动柜员机协议售出。该公司产生了$
| F-24 |
私募
于2021年7月26日,本公司就一项私募订立证券
购买协议,根据该协议,本公司根据纳斯达克规则以按市价定价
的私募方式发行及出售,(I)本公司普通股,面值$每股,(Ii)认股权证,购买总额为
B系列认股权证立即可以普通股每股0.001美元的价格行使。如果B系列认股权证持有人(及其附属公司)实益拥有4.99%以上的股份,则B系列认股权证持有人无权行使B系列认股权证的任何部分。根据B系列认股权证的条款,按行权生效后紧随已发行的普通股数量的百分比
确定。股东在通知本公司后,可增加或减少实益所有权限额规定,但实益所有权限额不得超过持有人行使认股权证后发行普通股后已发行普通股股数的9.99%
。任何提高实益拥有权限额的措施,将于通知送交本公司后第61天
才生效。B系列认股权证的内在价值约为#美元。. 在截至2021年12月31日的年度内,所有B系列购买认股权证普通股的股份
被行使,结果是$
A系列认股权证立即可按普通股每股3.30美元的价格行使。如果A系列认股权证持有人(及其附属公司)实益拥有4.99%以上的股份,则A系列认股权证持有人将无权行使A系列认股权证的任何部分。根据A系列认股权证的条款,按行权生效后紧接本公司普通股已发行股份数目的百分比
确定。持有人在通知本公司后,可增加或减少实益所有权限额条款,但实益所有权限额在任何情况下不得超过
持有人所持认股权证在紧接普通股发行生效后已发行普通股股数的9.99%。对实益所有权限额的任何提高将在向本公司交付通知
后第61天生效。本公司评估已发行认股权证的条款,并决定将该等认股权证分类为股权工具。这些认股权证于授出日期的公允价值估计为$每股,
,总计约$
A系列优先股
公司已指定
清算在 任何解散、清算或清盘后,无论是自愿还是非自愿,A系列优先股持有人将有权从公司资产中获得相当于A系列优先股的每股声明价值(经股票拆分、合并、重组等调整后)的金额 外加任何应计和未支付的股息,然后才对普通股或A系列优先股进行任何分配 。
| F-25 |
分红*A系列优先股的股东
有权获得非累积现金股息,年利率为
转换A系列优先股可随时根据其持有人的选择随时转换,并至少提前61天 通知本公司,A系列优先股以12股A系列优先股对1股普通股的比率计算。
救赎根据提前30天的书面通知,本公司可要求任何A系列优先股的持有人按A系列优先股12股转换为普通股的比率将任何或全部该等A系列优先股转换为普通股。
A系列优先股
有其他条款,涵盖股票股息和拆分、投票权、零碎股份和基本交易。截至2022年12月31日和2021年12月31日,大约有
B系列优先股
公司已指定
清算*在 任何解散、清算或清盘后,无论是自愿还是非自愿,B系列优先股持有人将有权 从公司资产中获得相当于B系列优先股每股声明价值的分配(根据股票拆分、组合、任何分派前,普通股或任何B系列优先股(包括A系列优先股)加上任何应计及未支付的股息,以及根据经修订及重述的指定证书当时到期应付的任何其他费用或违约金,应 对B系列优先股以下的普通股或任何系列优先股进行分配。就这一权利而言,根据修订和重述的指定证书进行的基本交易或控制权变更应构成清算。Xenetic将在任何股东会议前至少30天 向B系列优先股的每位持有人发出任何清算的书面通知,以批准此类清算,或如果不举行会议,则至少在清算日期前45天发出书面通知。
分红如果 受本公司董事会不时设立的任何已发行系列优先股的任何优先权利的规限,本公司B系列优先股的股份持有人 将有权从可用资金中获得本公司董事会可能不时宣布的有关本公司普通股股份(按折算基准)的非累积现金股息 。只要B系列优先股的任何股息仍未支付,本公司不得直接或间接支付或宣布任何股息,亦不得就任何初级证券(包括A系列优先股)作出任何分派,亦不得预留或用于购买或赎回任何与B系列优先股同等的初级证券或股份。
转换*B系列优先股可随时根据其持有人的选择权按一股优先股 股至约0.33股普通股的比率进行转换,但须遵守可发行的上限和下文所述的调整。有几个截至2022年和2021年12月31日止年度的B系列优先股转换。
| F-26 |
后续股权销售 。此外,B系列优先股具有基于棘轮价格的反稀释保护,在以低于B系列优先股规定价值的每股价格进行下一轮融资的情况下,受惯例的 分割。嵌入式转换选项不存在与主机仪器明确而密切相关的分支。
B系列优先股
有其他条款,涵盖股票股息和拆分、投票权、零碎股份和基本交易。截至2022年12月31日和2021年12月31日,大约有
与协作和咨询协议相关的授权书
关于本公司的某些合作协议和咨询安排,本公司已发行认股权证购买普通股 股票作为服务付款。在截至2021年12月31日的年度内,已授予或行使协作或咨询服务认股权证,所有未到期的协作认股权证 均已到期。结果,截至2022年12月31日和2021年12月31日,协作或咨询服务授权书尚未生效 。
与融资安排有关的认股权证
关于2021年7月的定向增发,该公司发行了A系列认股权证,购买了
此外,该公司已公开交易认股权证
以购买约
该公司还拥有未偿还的认股权证,可购买约
认股权证购买约
该公司有额外的未偿还债务和
股权融资权证,以购买总计约
| F-27 |
| 12. | 基于股份的费用 |
与股票期权、RSU和普通股奖励相关的基于股票的总费用约为$及$截至2022年12月31日和2021年12月31日止年度。 综合全面损失表中基于股份的费用分类如下:
| 截至十二月三十一日止的年度: | ||||||||
| 2022 | 2021 | |||||||
| 研发费用 | $ | $ | ||||||
| 一般和行政费用 | ||||||||
| $ | $ | |||||||
股票期权
本公司根据Xenetic Biosciences,Inc.修订和恢复的股权激励计划 (“股票计划”),以不同的归属条款向员工和非员工授予股票期权奖励和RSU 。本公司采用布莱克-斯科尔斯期权定价模型来计量股票期权奖励的公允价值,该模型 使用下表中所述的假设,包括无风险利率、预期期限、股价波动性、股息收益率和罚没率。无风险利率以授予时生效的美国国债收益率曲线为基础, 一个期限近似于期权的预期寿命。对于在2022年和2021年发行的股票期权,符合“普通”股票期权的条件,预期期限以简化方法为基础。本公司行使股票期权的历史有限, 无法为本公司估计员工和非员工股票期权的预期期限提供合理的基础。对于所有其他股票期权,公司根据公司临床项目的预期研发里程碑以及公司员工和非员工的行为来估计预期寿命。非员工 期权的预期寿命是期权的合同寿命。预期波动率是根据公司的实际波动率进行估计的。 由于公司数据在整个获奖预期期限内不可用,因此公司使用的价格波动率是基于公司历史波动率与具有与公司候选药物类似的治疗领域和非临床开发阶段的候选药物的可比上市公司的价格波动。由于本公司历来未曾宣派股息,且预期不会在期权的预期年期内宣派股息,因此本公司已应用预期股息 收益率为0%。本公司对发生的没收行为进行核算。
员工股票期权
在截至2022年12月31日和2021年12月31日的年度内, 和购买普通股的全部股票期权分别由本公司授予。每个期权的加权平均 授予日期公允价值为$及$,分别为。在截至2022年12月31日和2021年12月31日的年度内,行使了股票期权,没有任何期权到期。
在截至2022年12月31日和2021年12月31日的年度内, 和分别授予的股票期权总额,公允价值总额约为$及$ 截至2022年12月31日,大约有$与 预计将授予的员工股票期权相关的未确认的基于股票的付款。公司预计将在加权平均期间确认这笔费用,时间约为好几年了。
| F-28 |
布莱克-斯科尔斯期权 在截至2022年12月31日和2021年12月31日的年度内授予员工的期权定价模型中使用的主要假设如下:
| 截至十二月三十一日止的年度: | ||||||||
| 2022 | 2021 | |||||||
| 加权平均预期股息率(%) | ||||||||
| 加权平均预期波动率(%) | ||||||||
| 加权平均无风险利率(%) | ||||||||
| 期权的加权平均预期寿命(年) | ||||||||
| 加权平均行使价(美元) | ||||||||
以下是截至2022年12月31日和2021年12月31日的 年度员工股票期权活动摘要:
| 股份数量 | 加权的- 平均值 锻炼 价格 | 加权的- 平均值 剩余 生活 (年) | 集料 固有的 价值 | ||||||||||||
| 截至2021年1月1日的未偿还款项 | $ | $ | |||||||||||||
| 授与 | |||||||||||||||
| 过期 | |||||||||||||||
| 截至2021年12月31日的未偿还债务 | $ | $ | |||||||||||||
| 授与 | |||||||||||||||
| 过期 | |||||||||||||||
| 截至2022年12月31日的未偿还债务 | $ | $ | |||||||||||||
| 已归属或预计将于2022年12月31日归属 | $ | $ | |||||||||||||
| 自2021年12月31日起可行使 | $ | $ | |||||||||||||
| 自2022年12月31日起可行使 | $ | $ | |||||||||||||
| F-29 |
本公司截至2022年12月31日的非既得员工股票期权股票状况和截至2022年12月31日的年度变化摘要如下:
| 数量 股票 | 加权的- 平均值 授予日期 公允价值 | ||||||
| 截至2022年1月1日的余额 | $ | ||||||
| 授与 | $ | ||||||
| 被没收 | $ | ||||||
| 既得 | ( | ) | $ | ||||
| 截至2022年12月31日的余额 | $ | ||||||
限制性股票 个单位
确实有截至2022年12月31日和2021年12月31日的未偿还RSU 。RSU是完全授予的,授予日期的公允价值为$每股。 在截至2022年12月31日和2021年12月31日的年度内授予或到期的RSU。
非员工股票 期权
授予非员工的股票期权相关的基于股票的费用 被确认为服务是在直线基础上提供的。该公司认定,股票期权的公允价值比所接受服务的公允价值更可靠地计量。于截至2022年及2021年12月31日止年度内,本公司并无向非雇员授出购买 普通股的购股权。 在截至2022年12月31日和2021年12月31日的年度内行使了非雇员股票期权。 截至2022年12月31日和2021年12月31日的年度内与非员工期权相关的薪酬支出,因为所有 非员工股票期权于2020年12月31日全部归属。
以下是截至2022年12月31日和2021年12月31日的年度非员工股票期权活动摘要:
| 股份数量 | 加权的- 平均值 锻炼 价格 | 加权的- 平均值 剩余 生活 (年) | 集料 固有的 价值 | ||||||||||||
| 截至2021年1月1日的未偿还款项 | $ | $ | |||||||||||||
| 授与 | |||||||||||||||
| 过期 | ( | ) | |||||||||||||
| 截至2021年12月31日的未偿还债务 | $ | ||||||||||||||
| 授与 | |||||||||||||||
| 过期 | |||||||||||||||
| 截至2022年12月31日的未偿还债务 | $ | $ | |||||||||||||
| 已归属或预计将于2022年12月31日归属 | $ | $ | |||||||||||||
| 自2021年12月31日起可行使 | $ | $ | |||||||||||||
| 自2022年12月31日起可行使 | $ | $ | |||||||||||||
| F-30 |
普通股奖励
公司向非员工授予普通股奖励,以换取提供的服务。本公司使用所提供服务的公允价值或所授予奖励的公允价值来计量这些奖励的公允价值,以更可靠的可计量者为准。这些奖励的公允价值计量日期一般为服务完成之日。奖励的公允价值确认为以直线方式提供的服务 。在截至2022年12月31日和2021年12月31日的年度内,公司授予和发行的普通股奖励摘要如下:
| 股份数量 | |||
| 截至2021年1月1日的余额 | |||
| 授与 | |||
| 已发布 | ( | ) | |
| 截至2021年12月31日的余额 | |||
| 授与 | |||
| 已发布 | |||
| 截至2022年12月31日的余额 |
普通股奖励在截至2022年12月31日和2021年12月31日的 年内授予。截至2022年12月31日,普通股奖励余额尚未发放。
共同持股计划
截至2022年12月31日和2021年12月31日,大约有 JSOP奖颁发给了两名前高级管理人员,并尚未完成。根据JSOP计划,本公司的股份由参与的高管和JSOP信托的受托人以公平市价共同购买,该等股份由JSOP信托持有。对于美国公认会计原则的目的,奖励作为员工期权进行估值,并作为库存股记录为股本减少,直到员工 行使为止。JSOP奖励是完全授予的,没有到期日。有几个截至2022年12月31日和2021年12月31日的 年内的薪酬费用。
| 13. | 员工福利计划 |
公司有一个明确的401(K)储蓄计划(“401(K)计划”)。401(K)计划基本上涵盖了所有美国员工,并允许
参与者在税前基础上延期支付部分年度薪酬或进行税后贡献。公司对401(K)计划的贡献可由董事会酌情决定。在截至2022年12月31日和2021年12月31日的年度内,公司
贡献了约$
| F-31 |
| 14. | 承付款和或有事项 |
租契
公司在开始时确定
安排是否为租赁。在……上面
与我们的经营租赁相关的补充现金流信息和非现金 活动如下:
截至的年度 十二月三十一日, | 截至的年度 十二月三十一日, | |||||||
| 2022 | 2021 | |||||||
| 经营现金流信息: | ||||||||
| 为计入租赁负债的金额支付的现金 | $ | $ | ||||||
与我们的经营租赁相关的补充资产负债表信息如下:
| 资产负债表分类 | 十二月三十一日, 2022 | 十二月三十一日, 2021 | ||||||||
| 使用权资产-ST | 预付费用和其他 | $ | $ | |||||||
| 流动租赁负债 | 应计费用和其他流动负债 | $ | $ | |||||||
本公司未将ASU
2016-02的规定适用于其在佛罗里达州迈阿密的办公空间租赁。有效
| 15. | 关联方交易 |
本公司已与血清研究所和Pharmynz签订了各种研究、开发、许可和供应协议,各自都是关联方,其关系、所有权、交易性质和交易性质在这些脚注的其他部分中披露。请参阅附注4,重要的战略协作, 和注7,其他资产,了解有关与也是关联方的协作合作伙伴的安排的详细信息。
| F-32 |
于2019年第四季度,本公司与Pharmsynz订立贷款协议(“Pharmsynz贷款”),据此,本公司向Pharmsynz提供本金总额最高达$。
自2021年1月23日起,本公司与Pharmsynz、Kevelt和SynBio签订了贷款协议第一修正案和其他贷款文件(“Pharmsynz贷款延期”)
,将Pharmsynz贷款的偿还条款和到期日修改为2022年1月。名为
的Pharmsynz贷款延期条款为两(2)笔相等的每月本金付款$
自2021年8月31日起,本公司与Pharmsynz、Kevelt和SynBio签订了贷款协议第二修正案和其他贷款文件(“第二次Pharmsynz贷款延期”),将Pharmsynz贷款的偿还条款和到期日修改为2022年7月。第二次Pharmsynz贷款延期的条款要求预付费用$
本公司于2022年10月31日与Pharmsynz、Kevelt和SynBio签订了《贷款协议第三修正案》和其他贷款文件(“第三次Pharmsynz贷款延期”),主要是为了将Pharmsynz贷款的偿还条款和到期日修改至2023年5月31日。第三次贷款延期的条款要求在签署第三次延期贷款时支付一定的本金、利息和费用。
此外,第三次延期贷款要求在2022年11月30日至2023年5月31日期间分七(7)
个月分期偿还剩余本金和利息,以及某些其他条款和条件。经修订的Pharmsynz贷款的所有其他条款仍然有效。虽然Pharmsynz已根据第三次贷款延期支付了某些款项,但第三次贷款延期所需的所有本金和利息尚未支付。因此,公司已将截至2022年12月31日和2021年12月31日的应收贷款归类为长期贷款。本公司评估了贷款的可收回性
并确定本公司在美国持有的抵押品,包括由Pharmynz和SynBio拥有的本公司的所有普通股和优先股,足以支持偿还未偿还本金余额。截至2022年12月31日和2021年12月31日,约为$
2022年4月,本公司与CLS签订了附注5所述的若干 协议。本公司董事之一Roger Kornberg是CLS科学顾问 董事会的成员。然而,Kornberg先生并不拥有CLS的任何股权,亦不会因该等协议拟进行的交易而获得任何经济利益。我们的董事之一Adam Logal先生是OPKO首席财务官、首席会计官兼财务主管高级副总裁。
| F-33 |
| 16. | 后续事件 |
本公司对自资产负债表日起至财务报表发布之日止的事项进行审核,并确定除下文所述事项外,并无该等事项需要在财务报表中确认或披露。
斯克里普斯研究公司
2023年3月17日,公司与斯克里普斯研究公司签订了一项研究资助和期权协议(“协议”),根据该协议,公司同意向斯克里普斯研究公司提供总额高达938,000美元的资金,用于资助与推进公司的DNase肿瘤平台技术的临床前开发有关的研究。研究经费由本公司根据商定的预算按月支付给斯克里普斯研究公司,该预算规定在协议签订之日支付约78,000美元的首付款,并在12个月内按月支付约78,000美元。根据该协议,该公司有权获得Scripps Research在技术或专利权(如协议定义)中的权利的全球独家许可,以及非独家、 免版税、不可转让的许可,以便在执行协议预期的研究计划期间,仅为公司内部的研究目的制造和使用TSRI技术(如协议定义)。
除非提前终止,否则本协议的有效期自本协议之日起持续十五(15)个月。本协议可由公司提前30天书面通知斯克里普斯研究公司,从生效日期(协议中的定义)后六(6)个月开始,或由斯克里普斯研究公司终止。如果公司未能及时支付本协议规定的到期款项,须提前30天书面通知解决此类不付款问题。 如果另一方未能履行协议项下的任何义务或另一方破产,则任何一方均可进一步终止协议。
硅谷银行
SVB于2023年3月10日被加州金融保护和创新部关闭,并任命FDIC为接管人。该公司主要与SVB保持现金。2023年3月12日,美国财政部、美联储和FDIC推出了紧急措施,全面保护SVB的所有储户,并于2023年3月13日,我们 完全可以使用我们在SVB的存款现金。因此,公司预计此类余额不会出现任何损失.
| F-34 |
项目9--会计和财务披露方面的变更和与会计师的分歧
不适用。
项目9A--控制和程序
评估披露控制和程序
我们的管理层在首席执行官和首席财务官的参与下,评估了截至本年度报告10-K表格所涵盖期间结束时,我们的披露控制和程序的有效性,这些程序由1934年修订的《证券交易法》(以下简称《交易法》)下的规则13a-15(E)和规则15d-15(E)所定义。
基于此评估,包括首席执行官和首席财务官在内的我们的管理层得出结论,截至2022年12月31日,我们的披露 控制和程序设计在合理的保证水平,并有效地提供合理的保证, 我们根据交易所法案提交或提交的报告中要求我们披露的信息在美国证券交易委员会规则和表格中指定的时间段内得到记录、处理、汇总和报告,并且此类信息经过积累并传达给我们的 管理层,包括我们的主要高管和主要财务官,或视情况执行类似职能的人员。 以便及时做出有关所需披露的决定。
管理层关于财务报告内部控制的报告
我们的管理层负责建立和维护对财务报告的充分内部控制,这一术语在《交易法》规则13a-15(F)中有定义。在我们的首席执行官和首席财务官的参与下,管理层在我们的监督下, 对截至本年度报告10-K表格所涵盖的期末的财务报告内部控制的设计和有效性进行了评估。在对财务报告的内部控制进行评估时,管理层使用了#年由特雷德韦委员会赞助组织委员会(“COSO”)制定的标准内部控制--综合框架(2013框架)。基于这一评估,我们的管理层得出结论,截至本Form 10-K年度报告所涵盖的期间结束时,我们对财务报告的内部控制是基于#年特雷德韦委员会COSO 提出的标准而有效的内部控制--综合框架。
本年度报告不包括我所注册会计师事务所关于财务报告内部控制的认证报告。根据《多德-弗兰克华尔街改革和消费者保护法》第989G节规定的对非加速申请者的豁免,管理层的报告不受我们注册会计师事务所的认证。
财务报告内部控制的变化
在本10-K年度报告所涵盖的季度期间,我们对财务报告的内部控制没有发生任何变化 对财务报告的内部控制产生了重大影响,或有合理的可能性对财务报告的内部控制产生重大影响。
| 68 |
对控制和程序有效性的限制
在设计和评估披露控制和程序时,管理层认识到,任何控制和程序,无论设计和操作有多好,都只能提供实现预期控制目标的合理保证。公司对财务报告的内部控制包括符合以下条件的政策和程序:
| (1) | 与保存合理详细、准确和公平地反映公司资产的交易和处置的记录有关; |
| (2) | 提供合理保证,保证必要时记录交易,以便根据公认的会计原则编制财务报表,并且公司的收支仅根据公司管理层和董事的授权进行; |
| (3) | 就防止或及时发现可能对财务报表产生重大影响的未经授权收购、使用或处置公司资产提供合理保证。 |
管理层,包括公司主要行政人员和主要财务人员,或执行类似职能的人员,并不期望公司的内部控制能够防止或发现所有错误和所有欺诈行为。一个控制系统,无论设计得多么好,运行得多么好,只能提供合理的保证,而不是绝对的保证,保证控制系统的目标得以实现。此外,控制系统的设计必须反映这样一个事实,即存在资源限制,并且控制的好处必须被视为相对于其成本。由于所有控制系统的固有局限性,任何对内部控制的评价都不能提供绝对保证 所有控制问题和舞弊事件(如果有的话)都已被发现。此外,对未来 期间控制有效性的任何评估都有可能会因为业务条件的变化而导致这些内部控制变得不充分,或者 对政策或程序的遵守程度可能会恶化。
项目9B--其他资料
斯克里普斯研究公司
2023年3月17日,公司与斯克里普斯研究公司签订了一项研究资助和期权协议(“协议”),根据该协议,公司同意向斯克里普斯研究公司提供总额高达938,000美元的资金,用于资助与推进公司的DNase肿瘤平台技术的临床前开发有关的研究。研究经费由本公司根据商定的预算按月支付给斯克里普斯研究公司,该预算规定在协议签订之日支付约78,000美元的首付款,并在12个月内按月支付约78,000美元。根据该协议,该公司有权获得Scripps Research在技术或专利权(如协议定义)中的权利的全球独家许可,以及非独家、 免版税、不可转让的许可,以便在执行协议预期的研究计划期间,仅为公司内部的研究目的制造和使用TSRI技术(如协议定义)。
除非提前终止,否则本协议的有效期自本协议之日起持续十五(15)个月。本协议可由公司提前30天书面通知斯克里普斯研究公司终止,终止日期从生效日期(协议定义)后六(6)个月开始;如果公司 未能及时支付根据协议到期的款项,则可由斯克里普斯研究公司终止,但须提前30天书面通知以纠正此类不付款行为。如果另一方未能履行 协议规定的任何义务或另一方破产,则协议可由任何一方进一步终止。
该协议的副本 将作为证据提交给公司截至2023年3月31日的三个月期间的10-Q季度报告。
项目9C--关于阻止检查的外国司法管辖区的披露
不适用。
| 69 |
第 第三部分
项目10--董事、执行干事和公司治理
本项目要求的信息将在截至2022年12月31日的公司会计年度结束后120天内提交给美国证券交易委员会的与公司2023年股东年会相关的最终委托书或信息说明书中阐述,并通过引用并入本文,或将包含在本年度报告的10-K表格修正案中。
项目11--高管薪酬
本项目要求的信息将在截至2022年12月31日的公司会计年度结束后120天内提交给美国证券交易委员会的与公司2023年股东年会相关的最终委托书或信息说明书中阐述,并通过引用并入本文,或将包含在本年度报告的10-K表格修正案中。
项目12--某些受益所有人和管理层的担保所有权及相关股东事项
本项目要求的信息将在截至2022年12月31日的公司会计年度结束后120天内提交给美国证券交易委员会的与公司2023年股东年会相关的最终委托书或信息说明书中阐述,并通过引用并入本文,或将包含在本年度报告的10-K表格修正案中。
第13项-某些关系和相关交易,以及董事独立性
本项目要求的信息将在截至2022年12月31日的公司会计年度结束后120天内提交给美国证券交易委员会的与公司2023年股东年会相关的最终委托书或信息说明书中阐述,并通过引用并入本文,或将包含在本年度报告的10-K表格修正案中。
项目14--主要会计费和 服务
本项目要求的信息将在截至2022年12月31日的公司会计年度结束后120天内提交给美国证券交易委员会的与公司2023年股东年会相关的最终委托书或信息说明书中阐述,并通过引用并入本文,或将包含在本年度报告的10-K表格修正案中。
| 70 |
第四部分
项目15--证物和财务报表 附表
| (a) | 以下是作为本年度报告10-K表格的一部分而提交的: | |
| · | 合并财务报表:报告本项要求的合并财务报表和独立注册会计师事务所报告列入第二部分第八项; | |
| · | 财务报表明细表:所有附表都被省略,因为它们不适用或不需要,或者因为所要求的信息显示在合并财务报表或其附注中。 | |
| (b) | 展品:以表格10-K的形式与本年度报告一起提交或提供的展品或通过引用并入本文的展品列于第72页开始的《展品索引》中,该页通过引用并入本文。 | |
项目16--表格10-K摘要
不适用。
| 71 |
展品索引
| 展品 不是的。 | 附件 索引 | 表格 | 提交日期 | 展品 数 | 归档 特此声明 | |||||
| 3.1 | 《公司章程》 | S-1 | 11/21/2011 | 3.1 | ||||||
| 3.2 | 公司章程修正案证书 | 8-K | 02/12/2013 | 3.1 | ||||||
| 3.3 | 公司章程修正案证书 | 8-K | 02/27/2013 | 3.1 | ||||||
| 3.4 | 公司章程修正案证书 | 10-Q | 01/10/2014 | 3.1 | ||||||
| 3.5 | 根据NRS 78.209变更证书 | 10-Q | 01/10/2014 | 3.2 | ||||||
| 3.6 | 公司章程修正案证书 | 8-K | 09/30/2015 | 3.1 | ||||||
| 3.7 | 修订 并重新制定附例 | 8-K | 02/27/2017 | 3.1 | ||||||
| 3.8 | 经修订和重新确定的A系列优先股的优先股、权利和限制指定证书表格 | S-1/A | 10/27/2016 | 3.8 | ||||||
| 3.9 | 第二份B系列优先股优先股、权利和限制指定证书的修订和重新发布 | S-1/A | 10/31/2016 | 3.9 | ||||||
| 3.10 | 根据NRS 78.209变更证书 | 8-K | 06/24/2019 | 3.1 | ||||||
| 3.11 | 公司章程修正案证书 | 8-K | 06/24/2019 | 3.2 | ||||||
| 3.12 | 公司章程修正案证书 | 10-K | 03/16/2021 | 3.12 | ||||||
| 3.13 | 公司章程修正案证书 | 10-K | 03/16/2021 | 3.13 | ||||||
| 3.14 | 公司章程修订证书 | X | ||||||||
| 4.1 | 根据1934年《证券交易法》第12条登记的注册人证券说明 | X | ||||||||
| 4.2 | 注册人普通股证书表格 | S-1/A | 07/14/2016 | 4.1 | ||||||
| 4.3 | 注册 Xenetic Bioscience,Inc.和OJSC Pharmynz之间的权利协议,日期为2015年7月1日 | 8-K | 07/08/2015 | 10.3 | ||||||
| 4.4 | 登记权协议第一修正案表格 | 8-K | 11/16/2015 | 10.8 | ||||||
| 4.5 | 普通股认购权证表格 | 8-K | 06/25/2019 | 4.1 | ||||||
| 4.6 | 普通股认购权证表格 | 8-K | 07/22/2019 | 4.2 | ||||||
| 4.7 | A系列认股权证表格 | 8-K | 07/28/2021 | 4.1 | ||||||
| 10.1† | 修订后的Xenetic Biosciences,Inc.股权激励计划表格,经修订,自2021年12月7日起生效 | DEF14A | 10/15/2021 | 附录A | ||||||
| 10.2# | Lipoxen plc、Lipoxen Technologies Ltd和SynBio LLC于2011年8月4日签署的共同开发协议和独家许可条款 | 10-K/A | 02/18/2015 | 10.18 | ||||||
| 10.3 | Xenetic Biosciences(UK)Limited(前身为Lipoxen plc)、Lipoxen Technologies Limited、SynBio LLC和上市股份公司Pharmsynz于2021年12月17日签订的共同开发协议和独家许可条款的续签 | 10-K | 03/22/2022 | 10.3 | ||||||
| 10.4## | Lipoxen Technologies Limited与上市股份公司Pharmynz之间的独家许可协议,日期为2021年12月20日 | 10-K | 03/22/2022 | 10.4 |
| 72 |
| 展品 不是的。 | 附件 索引 | 表格 | 提交日期 | 展品 数 | 归档 特此声明 | |||||
| 10.5# | SynBio LLC和Lipoxen plc于2011年8月4日就Lipoxen plc股本中普通股的认购协议 | 10-K/A | 02/18/2015 | 10.19 | ||||||
| 10.6# | 合作,日期为2009年11月11日的Pharmsynz ZAO和Lipoxen Technologies Ltd.之间的许可和开发协议。 | 10-K/A | 02/18/2015 | 10.20 | ||||||
| 10.7# | Lipoxen plc、Lipoxen Technologies Ltd和印度血清研究所有限公司之间的独家专利和专有技术许可和制造协议,日期为2011年8月4日 | 10-K/A | 02/18/2015 | 10.21 | ||||||
| 10.8 | Dmitry Genkin、FDS Pharma、Lipoxen Technologies Limited和Xenetic Biosciences Inc.之间的知识产权转让。 | 10-K | 04/15/2015 | 10.1 | ||||||
| 10.9† | Xenetic Biosciences,Inc.和Jeffrey Eisenberg之间的雇佣协议,日期为2016年12月1日 | 8-K | 12/6/2016 | 10.1 | ||||||
| 10.10† | Xenetic Biosciences,Inc.和Curtis Lockshin之间的雇佣协议,日期为2017年1月1日 | 8-K | 01/04/2017 | 10.1 | ||||||
| 10.11† | Xenetic Biosciences,Inc.与詹姆斯·F·帕斯洛于2017年3月23日签署的雇佣协议 | 8-K | 04/04/2017 | 10.1 | ||||||
| 10.12† | Xenetic Biosciences,Inc.及其每位董事和高管之间的赔偿协议格式 | 10-Q | 08/14/2017 | 10.1 | ||||||
| 10.13† | Xenetic Biosciences,Inc.与Jeffrey Eisenberg于2017年10月26日修订并重新签署的雇佣协议 | 10-K | 03/30/2018 | 10.45 | ||||||
| 10.14# | Xenetic Biosciences,Inc.、Baxalta Inc.、Baxalta US Inc.和Baxalta GmbH之间签订的、日期为2017年10月27日的再许可协议的权利 | 10-K | 03/30/2018 | 10.46 | ||||||
| 10.15 | Xenetic Biosciences,Inc.与OPKO PharmPharmticals,LLC之间的转让协议,日期为2019年3月1日 | 8-K/A | 05/20/2019 | 10.1 | ||||||
| 10.16 | 转让协议第一次修正案,日期为2019年6月7日 | 8-K | 06/13/2019 | 10.1 | ||||||
| 10.17 | 转让协议第二修正案,日期:2019年6月24日 | 8-K | 06/24/2019 | 10.1 | ||||||
| 10.18 | 第三次《转让协议修正案》,日期为2019年7月15日 | 8-K | 07/16/2019 | 10.1 | ||||||
| 10.19 | Xenetic Biosciences,Inc.和某些购买者之间签署的同意书表格,日期为2019年6月24日 | 8-K | 06/25/2019 | 10.1 | ||||||
| 10.20 | Xenetic Biosciences,Inc.和帝国股票转让公司之间的授权代理协议,日期为2019年7月19日 | 8-K | 07/22/2019 | 10.1 | ||||||
| 10.21 | Xenetic Biosciences,Inc.和某些购买者之间的同意协议,日期为2019年7月16日 | 8-K | 07/16/2019 | 10.1 | ||||||
| 10.22† | 信函协议格式 。任命非雇员、独立董事为遗传生物科学公司 | 10-K | 03/26/2020 | 10.51 | ||||||
| 10.23† | Xenetic Biosciences,Inc.股票期权授予通知表格 | 10-K | 03/26/2020 | 10.52 | ||||||
| 10.24† | Xenetic生物科学公司股票期权授予通知,日期为2019年12月4日,由Jeffrey Eisenberg和Xenetic Biosciences,Inc. | 10-K | 03/26/2020 | 10.53 | ||||||
| 10.25## | 研究 公司与斯克里普斯研究所于2020年5月15日签署的资金和期权协议 | 10-Q | 08/12/2020 | 10.1 |
| 73 |
| 展品 不是的。 | 附件 索引 | 表格 | 提交日期 | 展品 数 | 归档 特此声明 | |||||
| 10.26## | 公司与PJSC Pharmynz于2020年6月12日签订的Master服务协议 | 10-Q | 08/12/2020 | 10.2 | ||||||
| 10.27## | 本公司与PJSC Pharmynz于2021年10月12日签订的主服务协议修正案1 | 10-K | 03/22/2022 | 10.28 | ||||||
| 10.28## | 公司与PJSC Pharmynz于2021年10月12日签订的主服务协议的第二份工作单 | 10-K | 03/22/2022 | 10.29 | ||||||
| 10.29 | 本公司及其其他各方于2021年7月26日签署的《证券购买协议》表格 | 8-K | 7/28/2021 | 10.1 | ||||||
| 10.30 | 登记权利协议表格,日期为2021年7月26日,由本公司及其其他各方签署 | 8-K | 7/28/2021 | 10.2 | ||||||
| 10.31 | Xenetic Biosciences,Inc.与持有人之间的信函协议书格式,日期为2021年11月15日 | 8-K | 11/16/2021 | 10.1 | ||||||
| 10.32 | 在Xenetic Biosciences,Inc.和H.C.Wainwright&Co.,LLC之间的市场发售协议,日期为2021年11月19日 | 8-K | 11/19/2021 | 1.1 | ||||||
| 10.33## | Xenetic Biosciences,Inc.与CLS治疗有限公司之间的独家再许可协议,日期为2022年4月26日 | 10-Q | 8/11/2022 | 10.1 | ||||||
| 10.34## | Xenetic Biosciences,Inc.与CLS治疗有限公司的独家许可协议,日期为2022年4月26日 | 10-Q | 8/11/2022 | 10.2 | ||||||
| 10.35 | Xenetic Biosciences,Inc.与CLS治疗有限公司的认购协议格式,日期为2022年4月26日 | 10-Q | 8/11/2022 | 10.3 | ||||||
| 10.36## | Xenetic Biosciences,Inc.和Catalent Pharma Solutions,LLC之间的工作声明,日期为2022年6月30日 | 10-Q | 8/11/2022 | 10.4 | ||||||
| 21.1 | 附属公司名单 | X | ||||||||
| 23.1 | Marcum LLP的同意 | X | ||||||||
| 24.1 | 授权书(包括在签名页上) | X | ||||||||
| 31.1 | 根据规则第13a-14(A)条或规则第15d-14(A)条的要求认证特等执行干事 | X | ||||||||
| 31.2 | 根据细则13a-14(A)或细则15d-14(A)的要求认证首席财务干事 | X | ||||||||
| 32.1* | 《美国法典》第18编第36章第13a-14(B)条或第15d-14(B)条和第1350节第13a-14(B)条或第15d-14(B)条所要求的首席执行官和首席财务官证书(《美国法典》第18编第1350节) | X | ||||||||
| 101.INS | 内联XBRL实例文档。 | X | ||||||||
| 101.SCH | 内联XBRL分类扩展 架构文档。 | X | ||||||||
| 101.CAL | 内联XBRL分类扩展 计算链接库文档。 | X | ||||||||
| 101.DEF | 内联XBRL分类扩展 定义Linkbase文档。 | X | ||||||||
| 101.LAB | 内联XBRL分类扩展 标签Linkbase文档。 | X | ||||||||
| 101.PRE | 内联XRBL分类扩展 演示Linkbase文档。 | X | ||||||||
| 104 | 封面交互式 数据文件(嵌入内联XBRL文档中) | X |
|
† #
## |
指管理合同或任何补偿性计划、合同或安排。 已向证券和交易委员会提出申请,要求对本文件中包含的某些机密材料进行保密处理。已要求保密处理的 遗漏材料已单独提交给美国证券交易委员会。 根据修订后的《1933年证券法》S-K条例第601(B)(10)项,本展品中用方括号和星号标记的部分已被省略,因为它们(I)不是实质性的,(Ii)如果公开披露可能会对注册人造成竞争损害。如果委员会或其工作人员提出要求,登记人承诺迅速提供未经编辑的展品副本作为补充。 |
| * | 本证明不视为为1934年证券交易法(修订)第18节的目的而提交,或以其他方式承担该节的责任,也不应被视为通过引用纳入根据1933年证券法(修订后)或1934年证券交易法(修订后)提交的任何文件。 |
| 74 |
签名
根据1934年《证券交易法》第13或15(D)节的要求,注册人已正式授权以下签署人代表其签署本报告。
| Xenetic生物科学公司。 | ||
| 日期:3月22, 2023 | 发信人: | 杰弗里·F·艾森伯格 |
| 杰弗里·F·艾森伯格 | ||
| 首席执行官 |
授权书和签名
我们,以下签署的Xenetic Biosciences,Inc.的高级管理人员和董事,特此分别组成并任命我们真正合法的代理人Jeffrey F.Eisenberg,他拥有全面的权力,以我们的名义以下列身份签署对本报告的所有修订,并总体上以我们的名义和代表我们以此类身份做一切事情,使Xenetic Biosciences,Inc.能够遵守经修订的1934年证券交易法的条款和证券交易委员会的所有要求。
根据1934年《证券交易法》的要求 ,本报告已于2023年3月22日由以下注册人以下列身份签署。
| 签名 | 标题 | |
| 杰弗里·F·艾森伯格 |
董事首席执行官兼首席执行官 (首席行政官) | |
| 杰弗里·F·艾森伯格 | ||
| 日期:3月22, 2023 | ||
| /s/詹姆斯·帕斯洛 | 首席财务官 | |
| 詹姆斯·帕斯洛 | (首席财务官和首席会计官) | |
| 日期:3月22, 2023 | ||
| /s/Grigory Borisenko | 董事 | |
| 格里戈里·鲍里森科 | ||
| 日期:3月22, 2023 | ||
| /s/詹姆斯·卡拉维 | 董事 | |
| 詹姆斯·卡拉维 | ||
| 日期:3月22, 2023 | ||
| /s/Firdaus JAL Dastoor | 董事 | |
| 菲尔道斯·贾尔·达斯图尔 | ||
| 日期:2023年3月22日 | ||
| 罗杰·科恩伯格 | 董事 | |
| 罗杰·科恩伯格 | ||
| 日期:2023年3月22日 | ||
| /s/Adam Logal | 董事 | |
| 亚当·洛格尔 | ||
| 日期:3月22, 2023 | ||
| /s/Alexey Vinogradov | 董事 | |
| 阿列克谢·维诺格拉多夫 | ||
| 日期:3月22, 2023 |
| 75 |