新闻稿

第二季度的强劲执行推动了2022年全年指南的升级,并提供了丰富的免疫学和罕见病研发新闻流
巴黎,2022年7月28日
在Dupixent®、罕见病、疫苗和CHC的推动下,按恒定汇率计算,2022年第二季度销售额增长8.1%
•受Dupixent®(19.63亿欧元,+43.4%)和罕见病两位数增长的推动,专业护理增长了21.6%
•由于旅行和Booster疫苗的强劲反弹以及PPH特许经营权的持续增长,疫苗上涨了8.7%
•尽管与 COVID-19 相关的对 Lovenox® 的需求有所减少,但通用药品的核心资产仍实现了 6.0% 的增长
•受咳嗽和感冒、过敏和消化系统健康的推动,CHC连续第五个季度实现增长(+ 9.1%)
按恒定汇率计算,2022年第二季度业务每股收益(1)增长16.7%,这得益于销售额增加和利润率的提高
•由于效率提高和EUROAPI解散带来的利润率提高,BOI利润率增长了1.3个百分点至27.2%
•第二季度末节省了26亿欧元,其中大部分再投资于增长驱动力和研发
•业务每股收益(1)为1.73欧元,按报告计算增长25.4%,按CER计算增长16.7%
•国际财务报告准则每股收益为0.94欧元(下降2.1%)
企业社会责任战略的进展
•赛诺菲全球健康部门启动了一项服务不足地区的医疗解决方案基金,并启动了Impact®,这是一个新品牌,致力于非营利性地向40个低收入国家的高危人群分发30种赛诺菲产品
•Valyou计划通过降低美国未投保患者的胰岛素自付费用,继续改善获得胰岛素的机会
•赛诺菲将其范围3温室气体减排目标上调至2030年-30%,推出了低能耗强度疫苗设施
研发转型的关键里程碑和监管成果
•Efanesoctocog alfa,第一种获得 FDA A型血友病突破性疗法称号的 VIII 因子疗法
•Dupixent® 在美国获准作为首款针对 12 岁及以上嗜酸性食管炎的成人和儿童的治疗药物,以及首款针对 6 个月至 5 岁患有中度至重度特应性皮炎的儿童的生物药物
•美国食品和药物管理局接受 Dupixent® 作为结节性瘙痒症成年人的优先审查
•Nexviadyme® 和 XenpozymeTM 已获得欧盟批准
•下一代 COVID-19 助推器在对抗包括 Omicron 在内的令人担忧的变种时表现出强劲的效果
2022年全年企业每股收益指引向上修正
•赛诺菲现在预计,除非出现不可预见的重大不利事件,否则按CER计算,2022年业务每股收益(1)将增长约15%(2)。按2022年7月的平均汇率计算,货币对2022年企业每股收益的积极影响估计在+ 7.5%至+ 8.5%之间
赛诺菲首席执行官保罗·哈德森评论说:
“我们在第二季度的业绩再次以我们的主要增长驱动因素的销售额增加和出色的财务业绩为标志,这促使我们上调了全年业务每股收益预期。值得注意的是,我们看到了专业护理业务的显著增长势头,这主要是由Dupixent® 推动的。在我们继续增加研发投资的同时,我们实现了重要的研发里程碑,例如Dupixent® 在其第四个疾病适应症嗜酸性食管炎中获得批准。本月早些时候,我们有机会在ISTH上展示了efanesoctog alfa的变革潜力,efanesoctocog alfa是第一种获得美国食品药品管理局突破性疗法称号的A型血友病替代因子替代疗法。我们在推进全面整合的社会影响力战略方面也取得了长足的进展,特别是在平价准入方面,推出了Impact®,这是一个专门用于非营利分销的品牌,旨在确保在40个低收入国家安全分销30种赛诺菲药品。随着我们继续提前实现Play to Win战略,我们对下半年的业务前景充满信心,因此,我们重申了在2022年实现投资回报率30%的目标的承诺。”
| | | | | | | | | | | | | | | | | | | | |
| Q2 2022 | 改变 | 改变
在 CER | H1 2022 | 改变 | 改变
在 CER |
| 国际财务报告准则报告的净销售额 | €10,116m | +15.7% | +8.1% | €19,790m | +14.2% | +8.4% |
| 报告的《国际财务报告准则》净收益 | €1,175m | -1.9% | _ | €3,184m | +15.2% | — |
| 国际财务报告准则每股收益报告 | €0.94 | -2.1% | _ | €2.55 | +15.4% | — |
自由现金流 (3) | €1,535m | +7.5% | _ | €3,242m | -3.3% | — |
| 企业营业收入 | €2,753m | +21.5% | +13.2% | €5,818m | +18.7% | +12.7% |
业务净收益 (1) | €2,170m | +25.4% | +16.6% | €4,594m | +22.6% | +16.3% |
企业每股收益 (1) | €1.73 | +25.4% | +16.7% | €3.68 | +22.7% | +16.3% |
除非另有说明(定义见附录9),否则净销售额的变化以固定汇率(CER)表示。(1)为了促进对运营业绩的理解,赛诺菲对业务净利润表进行了评论。企业净收入是非公认会计准则财务指标(定义见附录9)。附录3中提供了2022年第二季度的合并损益表,附录4列出了报告的国际财务报告准则净收益与企业净收益的对账;(2)2021年业务每股收益为6.56欧元;(3)自由现金流是非公认会计准则财务指标(定义见附录9)。
2022年第二季度和上半年赛诺菲销售额
----------------------------
除非另有说明,否则本新闻稿中所有销售额的百分比变化均在CER1中列出
---------------------
2022年第二季度,赛诺菲的销售额为101.16亿欧元,据报告增长了15.7%。汇率变动产生了7.6个百分点的积极影响,这主要是由于美元。在CER,公司的销售额增长了8.1%。
2022年上半年,赛诺菲的销售额达到197.9亿欧元,据报告增长了14.2%。汇率变动产生了5.8个百分点的积极影响。在CER,公司的销售额增长了8.4%。
全球业务部门
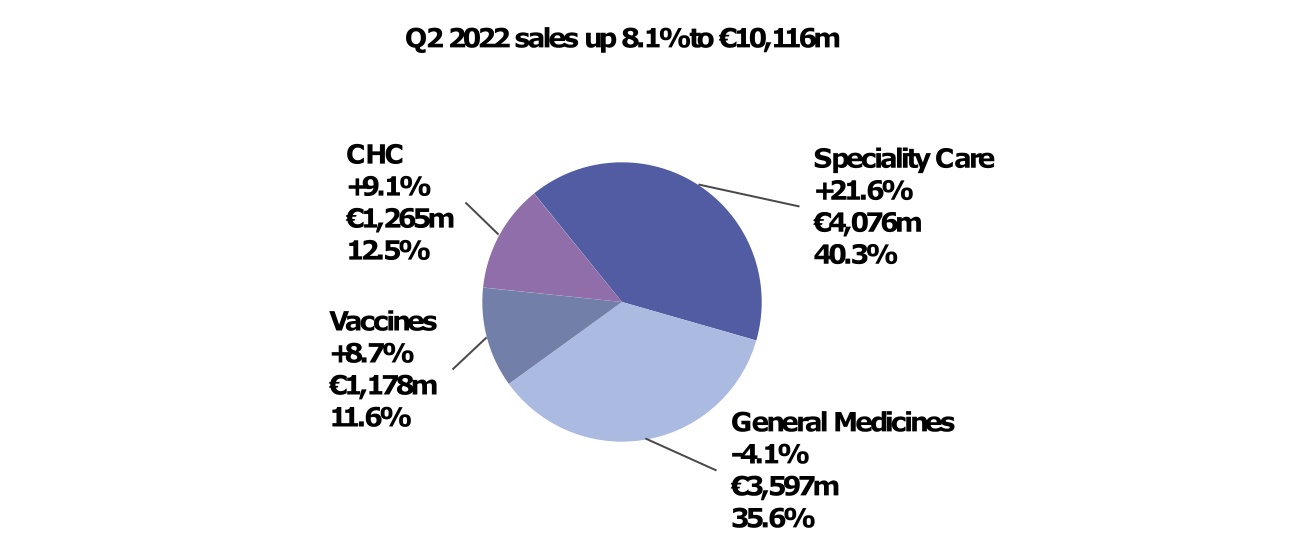
按全球业务部门划分的2022年第二季度净销售额(按CER变动;百万欧元;占总销售额的百分比)
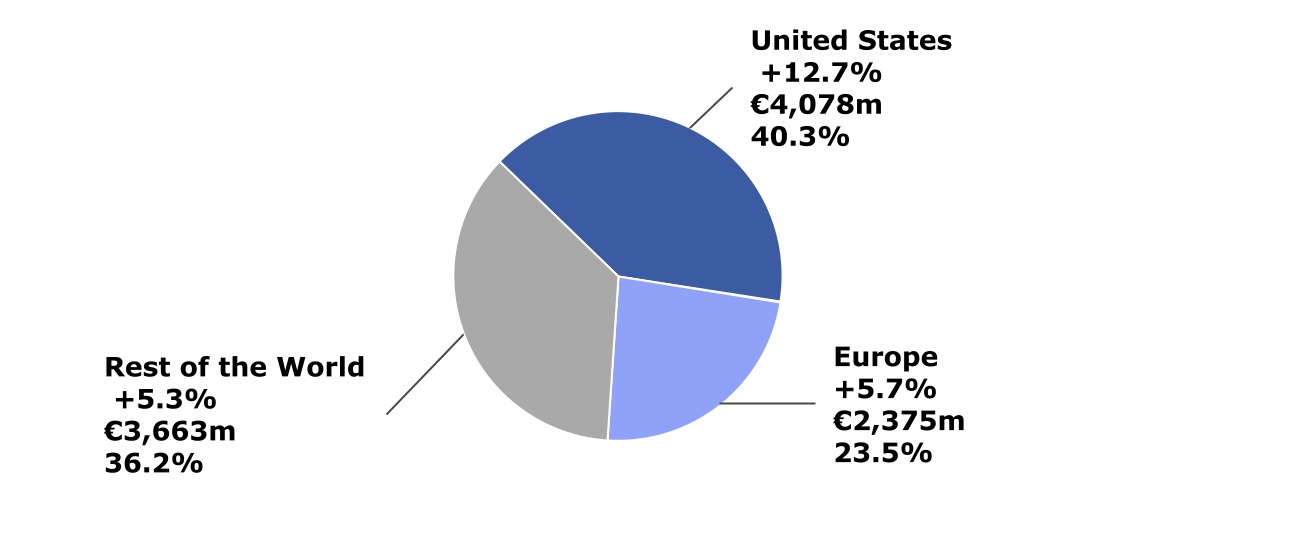
按地理区域划分的2022年第二季度净销售额(按CER变动;百万欧元;占总销售额的百分比)
2022年第二季度营业收入
第二季度业务营业收入(BOI)增长了21.5%,达到27.53亿欧元。在CER,投资回报率增长了13.2%。投资回报率与净销售额的比率增长了1.3个百分点至27.2%(按恒定汇率计算为27.1%)。上半年,投资回报率增长了18.7%,达到58.18亿欧元。在CER,投资回报率增长了12.7%。企业营业收入与净销售额的比率增长了1.1个百分点至29.4%(按CER计算为29.4%)。
1 财务指标的定义见附录9。
药品
第二季度药品销售额增长7.9%,达到76.73亿欧元,这主要是由专业护理产品组合(增长21.6%)以及Dupixent® 的持续强劲表现所推动,而普通药品的销售额下降了4.1%。2022年上半年,药品销售额增长了7.7%,达到149.99亿欧元,这反映了特种护理和普通药物核心资产的强劲表现。
专业护理
Dupixent
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
Total Dupixent® | 1,963 | | +43.4 | % | 3,577 | | +44.4 | % |
第二季度,Dupixent®(与Regeneron合作)的销售额增长了43.4%,达到19.63亿欧元。在美国,Dupixent® 销售额为14.77亿欧元(增长37.9%),这得益于成人、青少年和6至11岁儿童对特应性皮炎(AD)的持续强劲需求,12岁及以上患者和6至11岁儿童对哮喘的持续吸收,以及伴有鼻息肉的慢性鼻窦炎(crsWnP)。Dupixent® 处方总量(TRx)增长了38%(同比),新品牌处方(NBRx)增长了23%。在欧洲,第二季度Dupixent® 的销售额增长了56.6%,达到2.39亿欧元,这反映了AD、哮喘和CrsWNP的持续增长。在世界其他地区,第二季度销售额达到2.47亿欧元,增长65.3%。Dupixent® 上半年的销售额达到35.77亿欧元,增长44.4%。
神经病学和免疫学
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在CER | H1 2022 | 改变
在CER |
Aubagio® | 526 | | -2.2 | % | 1,017 | | -4.4 | % |
Lemtrada® | 20 | | 0.0 | % | 45 | | 0.0 | % |
Kevzara® | 77 | | +30.4 | % | 172 | | +46.0 | % |
全神经病学和免疫学 | 623 | | +1.1 | % | 1,234 | | +0.7 | % |
在第二季度和上半年,神经病学和免疫学的销售额分别增长了1.1%(至6.23亿欧元)和0.7%,这得益于Kevzara® 的强劲增长,但Aubagio® 销售额的下降部分抵消了这一增长。
Aubagio® 销售额在第二季度下降了2.2%,至5.26亿欧元,这是由于竞争压力和价格双重导致美国和世界其他地区的销售额下降,但部分被欧洲的增长所抵消。
由于全球对IL-6受体阻滞剂的需求暂时增加,第二季度Kevzara®(与Regeneron合作)的销售额增长了30.4%,达到7700万欧元。
罕见病
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
Myozyme®/Lumizyme® | 252 | | -3.6 | % | 487 | | -3.3 | % |
Fabrazyme® | 238 | | +9.3 | % | 458 | | +5.8 | % |
Cerezyme® | 202 | | +18.8 | % | 367 | | +5.5 | % |
Cerdelga® | 72 | | +11.5 | % | 139 | | +7.3 | % |
Aldurazyme® | 64 | | +7.0 | % | 133 | | +4.9 | % |
Nexviazyme® | 43 | | – | 73 | – |
| 其他罕见病 | 20 | | -13.0 | % | 38 | | -13.6 | % |
| 总罕见病 | 891 | | +11.6 | % | 1,695 | | +6.7 | % |
第二季度,罕见病销售额增长了11.6%,达到8.91亿欧元,这得益于高彻、法布里和庞培特许经营权的增长。世界其他地区的销售受益于有利的购买模式。罕见病上半年的销售额增长了6.7%,这反映了所有三个地理区域和所有核心品牌的增长。
Pompe特许经营权(Myozyme® /Lumizyme® + Nexviazyme®)第二季度的销售额增长了12.0%,达到2.95亿欧元,这主要是由于这三个地区的新增患者累积以及优惠的购买
世界其他地区的模式以及Nexviazyme® 的崛起。Myozyme® /Lumizyme® 的销售额下降了3.6%,至2.52亿欧元,这主要反映了Nexviazyme® 在美国向Nexviazyme® 的转换。Nexviazyme®(于2021年8月在美国推出,2021年11月在日本推出)在第二季度的销售额为4,300万欧元(其中在美国销售3700万欧元)。
高彻特许经营权(Cerezyme® + Cerdelga®)的销售额在第二季度增长了16.8%(至2.74亿欧元)。在世界其他地区的推动下,Cerezyme® 的销售额增长了18.8%,达到2.02亿欧元,这反映了良好的购买模式。同时,Cerdelga® 的销售额增长了11.5%,这得益于转换和新患者累积。
第二季度Fabrazyme® 的销售额增长了9.3%,达到2.38亿欧元,这主要是由这三个地理区域的增长推动的。
XenpozymeTM(alfa olipudase alfa)于6月在日本上市,是第一种也是唯一一种治疗酸性鞘磷脂酶非中枢神经系统(CNS)表现的酶替代疗法。
肿瘤学
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
Jevtana® | 105 | | -15.8 | % | 203 | | -20.8 | % |
Sarclisa® | 64 | | +52.5 | % | 129 | | +67.6 | % |
Fasturtec® | 46 | | +7.7 | % | 86 | | +8.1 | % |
Libtayo® | 47 | | +36.4 | % | 88 | | +44.1 | % |
| 全肿瘤学 | 263 | | +8.0 | % | 507 | | +7.4 | % |
肿瘤学第二季度和上半年的销售额分别增长了8.0%(至2.63亿欧元)和7.4%,这主要是由Sarclisa® 推动的,它抵消了欧洲Jevtana® 仿制药竞争的影响。
2021年3月底,部分欧洲市场进入仿制药竞争(下降73.3%),第二季度Jevtana® 销售额下降了15.8%,至1.05亿欧元。在美国,销售额增长了8.2%,Jevtana® 目前受四项橙皮书列出的专利保护:7,241,907美元、8,927,592美元、10,583,110美元和10,716,777美元。赛诺菲在美国特拉华特区地方法院根据Hatch-Waxman对声称拥有'110专利、'777专利和'592专利的仿制药申请人提起了专利侵权诉讼。赛诺菲已与一些被告达成和解协议,针对其余被告的诉讼仍在进行中。为期3天的审判定于2023年1月开始,其余被告同意在地方法院作出有利于被告的裁决之前或审后简报会结束四个月后,不推出任何仿制卡巴齐他赛产品。Jevtana® 还获得了与CARD临床研究相关的监管数据独家授权,该研究将于2023年12月到期。
第二季度Sarclisa® 销售额为6400万欧元,增长52.5%,主要受美国(3000万欧元,增长62.5%)和日本的业绩推动。
赛诺菲重组了与Regeneron Pharmicals的免疫肿瘤学合作,根据经修订和重述的许可和合作协议,向Regeneron Pharmicals授予了Libtayo® 的全球独家许可权,该协议转让了开发、商业化和制造Libtayo® 的权利。赛诺菲将从2022年第三季度起停止整合Libtayo® 的非美国销售额。
罕见血液病
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
Eloctate® | 153 | | -3.5 | % | 291 | | -3.2 | % |
Alprolix® | 129 | | +16.0 | % | 237 | | +9.0 | % |
Cablivi® | 51 | | +4.3 | % | 97 | | +9.5 | % |
enjaymoTM | 3 | | – | 4 | | – |
| 总罕见血液病 | 336 | | +5.5 | % | 629 | | +3.7 | % |
第二季度,罕见血液病的特许经营销售额增长了5.5%(3.36亿欧元),这主要反映了Alprolix® 的增长被Eloctate® 销售额的下降部分抵消。在Alprolix® 和Cablivi® 的推动下,上半年的特许经营销售额增长了3.7%。
第二季度Eloctate® 的销售额为1.53亿欧元,下降了3.5%,这反映了竞争环境导致美国和世界其他地区的销售额下降。
受美国以及世界其他地区增长的推动,Alprolix® 第二季度销售额增长了16.0%,达到1.29亿欧元。
在美国增长的支持下,第二季度Cablivi® 的销售额增长了4.3%,达到5100万欧元。在欧洲的销售额稳定在2400万欧元。
Enjaymo™ 是首款获批的冷凝素病患者治疗药物(于2月在美国获批),其第二季度销售额为300万欧元。
普通药物
第二季度通用药品销售额下降4.1%,至35.97亿欧元。经投资组合精简后不包括 EUROAPI2 第三方销售(2022年第二季度和2021年第二季度),受核心资产持续表现的推动,销售额下降了1.0%。第二季度工业销售额为1.33亿欧元,下降33.3%,这反映了自5月10日以来EUROAPI第三方销售额的下滑。
通用药品上半年的销售额下降了2.3%(不包括精简投资组合在内的销售额下降了1.6%)。上半年,核心资产销售占普通药品销售额的43.6%,而2021年同期为40.2%。
核心资产
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
Lovenox® * | 337 | | -10.9 | % | 714 | | -9.5 | % |
Toujeo® | 267 | | +2.4 | % | 541 | | +4.4 | % |
Plavix® | 247 | | 0.0 | % | 508 | | 0.0 | % |
Praluent® | 128 | | +147.9 | % | 197 | | +79.8 | % |
胸腺球蛋白® | 113 | | +12.0 | % | 210 | | +12.8 | % |
Multaq® | 91 | | +2.5 | % | 178 | | +7.9 | % |
Mozobil® | 66 | | +6.9 | % | 124 | | +6.4 | % |
Soliqua® | 53 | | +4.3 | % | 106 | | +10.0 | % |
Rezurock® | 43 | | – | 84 | | – |
| 其他 | 266 | | -3.5 | % | 543 | | -0.8 | % |
| 核心资产总额 | 1,611 | | +6.0 | % | 3,205 | | +5.3 | % |
*不包括汽车仿制药
第二季度,核心资产3的销售额增长了6.0%,达到16.11亿欧元,这得益于Praluent® 和胸腺球蛋白® 的增长以及Rezurock® 的强劲表现,但Lovenox® 销售额的下降部分抵消了这一增长。上半年,核心资产销售额增长了5.3%,达到32.05亿欧元,这得益于Praluent®、Thymoglobulin® 和Soliqua® 的两位数增长以及Rezurock® 的贡献。
第二季度Lovenox® 销售额下降了10.9%,至3.37亿欧元,这反映了2021年的较高比较基数,这是由于 COVID-19 相关需求和生物仿制药渗透率提高所致。
第二季度Toujeo® 销售额增长了2.4%,达到2.67亿欧元,这反映了美国和欧洲的增长被预计从今年5月起在中国实施的胰岛素批量采购(VBP)所部分抵消。
赛诺菲于11月参与了中国基础胰岛素类似物的VBP招标,并凭借Toujeo® 和Lantus® 成为A组的中标者之一。赛诺菲预计,2022年,其在中国的glargine销售额将下降不超过30%,这要归因于销量增加和价格大幅降低。在中国,第二季度和上半年Toujeo® /Lantus® 的销售额分别为1.01亿欧元(下降24,2%)和2.94亿欧元(下降5,3%)。
Plavix® 第二季度销售额稳定在2.47亿欧元,这反映了中国销量的持续增长(销售额增长了19.1%,至1.25亿欧元),这抵消了欧洲和日本销售额的下降,在这些国家,该产品受到4月初强制降价的影响。
Praluent® 第二季度销售额为1.28亿欧元,增长147.9%。Praluent® 在美国的销售额与总净额的调整有关,因为自联盟重组以来,Regeneron现在已合并了美国的销售额。不包括美国,第二季度Praluent® 的销售额增长了47.9%,这得益于欧洲的业绩以及自2022年1月起纳入NDRL后中国的加速增长。
Multaq® 第二季度销售额增长了2.5%,达到9,100万欧元,反映了美国和世界其他地区的增长。
2. 自5月10日起,EUROAPI第三方销售额已脱节
3 赛诺菲已优先考虑其通用药品投资组合中的核心资产,这些资产具有差异化和/或成熟的概况,这些资产在关键市场具有重大增长机会。核心资产包括Toujeo、Soliqua、Praluent、Multaq、Lovenox、Plavix等,2021年的总销售额为576.8万欧元
第二季度Soliqua® 销售额增长了4.3%,达到5300万欧元,这得益于世界其他地区的增长(增长33.3%),这足以抵消美国销售额的下降。
Rezurock® 第二季度的销售额为4,300万欧元。自推出以来,已有超过1000名患者接受了Rezurock®(占当前可治疗患者群体的25%)的治疗,持续率极高。Rezurock® 在美国的处方覆盖范围广泛,覆盖了全国约80%的生命。
非核心资产
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
Lantus® * | 600 | | -12.1 | % | 1,271 | | -6.7 | % |
Aprovel® /Avapro® | 120 | | +13.1 | % | 245 | | +15.5 | % |
| 其他非核心资产 | 1,133 | | -8.5 | % | 2,320 | | -7.9 | % |
| 非核心资产总额 | 1,853 | | -8.6 | % | 3,836 | | -6.4 | % |
第二季度,非核心资产销售额下降8.6%,至18.53亿欧元,这反映了投资组合的精简(-1.9个百分点),以及中国的VBP对Lantus® 以及Eloxatin® 和Taxotere® 销售的影响。上半年,非核心资产销售额下降了6.4%,不包括投资组合精简,下降了4.8%(-1.6个百分点)。
Lantus® 的销售额为6亿欧元,第二季度下降了12.1%。在美国,受处方损失以及基础胰岛素市场整体萎缩的影响,销售额下降了19.0%。在世界其他地区,销售额下降了8.2%,这反映了中国从今年5月开始实施胰岛素VBP。
第二季度Aprovel® /Avapro® 的销售额增长了13.1%,达到1.2亿欧元,这得益于去年世界其他地区从供应限制中恢复过来。
制药业务营业收入
第二季度,药品的业务营业收入(BOI)增长了17.9%,达到28.26亿欧元(按恒定汇率增长10.4%)。投资回报率与净销售额的比率增长了0.7个百分点至36.8%(按CER计算为37.0%),反映了毛利率的提高。
制药公司上半年的业务营业收入增长了15.2%,至56.57亿欧元(按恒定汇率增长9.6%)。投资回报率与净销售额的比率增长了0.5个百分点至37.7%(按CER计算为37.9%)。
疫苗
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
脊髓灰质炎/百日咳/Hib 疫苗 (包括 Hexaxim®/Hexyon®、Pentacel®、Pentaxim® 和 Imovax®) | 589 | | +7.9 | % | 1,202 | | +9.1 | % |
脑膜炎疫苗 (包括 Menactra®、MenquadFi®) | 153 | | -24.7 | % | 265 | | -21.3 | % |
加强疫苗(包括 Adacel®) | 152 | | +32.1 | % | 261 | | +18.4 | % |
| 旅行和流行疫苗 | 145 | | +83.8 | % | 243 | | +73.7 | % |
流感疫苗 (包括 Fluzone® HD/ Efluelda®、Fluzone®、Flublok®、Vaxigrip®) | 115 | | -5.9 | % | 181 | | -10.7 | % |
| 其他疫苗 | 24 | | +29.4 | % | 46 | | +20.0% |
| 疫苗总数 | 1,178 | | +8.7 | % | 2,198 | | +7.8 | % |
第二季度和上半年疫苗销售额分别增长了8.7%(至11.78亿欧元)和7.8%,这得益于脊髓灰质炎/百日咳/Hib疫苗的销售以及旅行和Booster疫苗的逐步恢复。
在第二季度,脊髓灰质炎/百日咳/乙型流感嗜血杆菌(PPH)疫苗的销售额增长了7.9%,达到5.89亿欧元,这得益于Pentaxim® 在中国的强劲增长,这要归因于市场增长和一些库存增加。在美国,PPH 的销售受到以下因素的影响
Vaxelis® 的市场份额不断增长。提醒一下,Vaxelis® 的市场销售不合并,利润由赛诺菲和默沙东平均分配。
第二季度脑膜炎销售额下降了24.7%,至1.53亿欧元,这反映了美国疾病预防控制中心的库存波动和拉丁美洲销售额的下降。
在 COVID-19 疫情之后美国和欧洲逐步复苏的推动下,第二季度加强疫苗的销售额增长了32.1%,达到1.52亿欧元。
第二季度旅行和地方性疫苗继续复苏,销售额增长了83.8%,达到1.45亿欧元,反映了所有地区的增长。
第二季度流感疫苗销售额下降了5.9%,至1.15亿欧元,这反映了受不利阶段影响的南半球销售下降,但与2021年销售相关的欧洲回报储备逆转部分抵消了这一下降。
疫苗业务营业收入
在第二季度,业务营业收入(BOI)与去年同期相比增长了26.5%(按恒定汇率计算增长14.6%),达到2.86亿欧元,这反映了尽管与Translate Bio和mRNA卓越中心相关的研发费用有所增加,但销售增长强劲。投资回报率与净销售额的比率为24.3%(按恒定汇率计算为23.3%),而2021年同期为22.1%。
2022年上半年,疫苗投资回报率下降了2.5%(按恒定汇率下降9.9%),至5.82亿欧元,这反映了第一三共在2021年第一季度记录的付款。投资回报率与净销售额的比率为26.5%(按恒定汇率计算为25.8%),而2021年上半年的比例为30.8%,不包括第一三共的付款,为24.7%)。
消费者医疗保健
| | | | | | | | | | | | | | |
| 净销售额(百万欧元) | Q2 2022 | 改变 在 CER | H1 2022 | 改变 在 CER |
| 过敏 | 192 | | +16.2 | % | 418 | | +13.4 | % |
| 咳嗽和感冒 | 98 | | +74.5 | % | 219 | | +96.4 | % |
| 疼痛护理 | 304 | | +5.8 | % | 618 | | +13.8 | % |
| 消化健康 | 336 | | +9.3 | % | 661 | | +11.5 | % |
| 身心健康 | 142 | | +1.5% | 296 | | +8,3% |
| 个人护理 | 149 | | +5.5 | % | 279 | | +1.6 | % |
| 非核心 /其他 | 44 | | -29.0 | % | 102 | | -22.3 | % |
| 全面的消费者医疗保健 | 1,265 | | +9.1 | % | 2,593 | | +13.1 | % |
在第二季度,消费者医疗保健(CHC)的销售额增长了9.1%,达到12.65亿欧元,这得益于欧洲和拉丁美洲的两位数增长。这一表现归因于包括 COVID-19 在内的强劲季节推动了对咳嗽和感冒产品的强劲需求,以及消化健康、过敏和止痛护理类别的增长。这种全球表现包括3.5个百分点的积极价格影响(ppt)。非核心产品的撤资在第二季度产生了1.4个百分点的负面影响。上半年CHC的销售额增长了13.1%,这要归因于强烈的咳嗽和寒冷季节,以及止痛护理、消化健康和过敏类别的增长,这足以抵消非核心产品的撤资(影响为-1.0个百分点)。
在美国,第二季度CHC销售额增长了3.1%,达到3.35亿欧元,这要归因于过敏症的两位数增长,个人护理品类的个位数增长被消化健康销售额的下降部分抵消。
在欧洲,第二季度CHC销售额增长了17.9%,达到3.75亿欧元,这主要反映了咳嗽和感冒、过敏和消化健康类别的强劲增长。
在世界其他地区,受所有主要类别增长的支持,第二季度CHC销售额增长了6.8%,达到5.55亿欧元。
CHC 业务营业收入
在第二季度,CHC的业务营业收入(BOI)增长了25.5%(按CER计算增长17.5%),达到4.23亿欧元。与去年相比,投资回报率与净销售额的比率增长了2.5个百分点至33.4%(按CER计算为33.3%),这反映了强劲的销售增长。上半年,CHC的投资回报率增长了39.4%(按CER计算增长33.9%),至10.19亿欧元,这要归因于强劲的销售增长和与之相关的资本收益增加
剥离非战略资产。投资回报率与净销售额的比率增长了6.1个百分点至39.3%(按CER计算为39.3%)。
按地理区域划分的公司销售额
| | | | | | | | | | | | | | |
| 赛诺菲销售额(百万欧元) | Q2 2022 | 改变
在 CER | H1 2022 | 改变
在 CER |
| 美国 | 4,078 | | +12.7 | % | 7,562 | | +12.4 | % |
| 欧洲 | 2,375 | | +5.7 | % | 4,767 | | +6.2 | % |
| 世界其他地区 | 3,663 | | +5.3 | % | 7,461 | | +6.2 | % |
| 其中中国 | 798 | | +11.2 | % | 1,699 | | +12.3% |
| 其中日本 | 403 | | +6.6 | % | 836 | | +4.0 | % |
| 其中巴西 | 243 | | +4.1 | % | 503 | | -3.5 | % |
其中俄罗斯 | 156 | | -14.1 | % | 341 | | +10.3% |
| 赛诺菲总销售额 | 10,116 | | +8.1 | % | 19,790 | | +8.4 | % |
受Dupixent® 推动的专业护理强劲表现的支持,美国第二季度和上半年的销售额分别增长了12.7%(至40.78亿欧元)和12.4%。
在欧洲,第二季度和上半年的销售额分别增长了5.7%(至23.75亿欧元)和6.2%,这主要是由Dupixent® 的业绩以及疫苗和CHC的强劲增长所推动的。
在世界其他地区,第二季度和上半年的销售额分别增长了5.3%(至36.63亿欧元)和6.2%,这反映了Dupixent® 推动的专业护理业绩以及疫苗和CHC销售额的增长。在中国的销售额增长了11.2%,达到7.98亿欧元,这主要是由于Dupixent®、Plavix® 和疫苗的增长被VBP的影响部分抵消了这一增长。在日本,受Dupixent® 和Sarclisa® 的推动,第二季度的销售额增长了6.6%,达到4.03亿欧元,这足以抵消Plavix® 销售额的下降。在俄罗斯,在第一季度药房和患者层面的库存前所未有之后,第二季度的销售额下降了14.1%,至1.56亿。3月,赛诺菲停止了与其在俄罗斯供应基本和改变生活的药物和疫苗无关的任何新支出。这包括所有广告和促销支出。
2022年第二季度末的研发最新情况
监管更新
•美国食品药品监督管理局(FDA)已批准每周300毫克的Dupixent®(dupilumab),用于治疗12岁及以上患有嗜酸性食管炎(EoE)的成人和青少年。获得批准后,Dupixent成为美国第一种也是唯一一种专门用于治疗EoE的药物。
•美国食品和药物管理局已批准Dupixent® 用于患有中度至重度特应性皮炎的6个月至5岁的儿童,这些儿童无法通过局部处方疗法充分控制疾病,或者不建议使用这些疗法。
•欧盟委员会扩大了Dupixent® 在欧盟的上市许可,用于治疗6至11岁的儿童,作为2型炎症的附加维持疗法,其特征是血液嗜酸性粒细胞升高和/或分数呼出的一氧化氮(FeNO)升高,中至高剂量的吸入性皮质类固醇(ICS)以及另一种用于维持治疗的药物无法充分控制这些患者。
•美国食品和药物管理局已同意优先审查Dupixent® 的补充生物制剂许可申请(sBLa),该申请用于治疗成人结节性瘙痒(PN),这是一种导致极度瘙痒和皮肤损伤的慢性炎症性皮肤病。
•欧盟委员会已批准Xenpozyme®(alpudase alfa)作为第一种也是唯一一种治疗A/B型或B型ASMD儿童和成人患者非中枢神经系统(CNS)酸性鞘磷脂酶缺乏症(ASMD)表现的酶替代疗法。鉴于ASMD社区的医疗需求尚未得到满足,欧洲药品管理局(EMA)授予Xenpozyme® Priority® Priority® 药品(PRIME)名称。
•欧盟委员会已经批准了Nexviadyme®(α-avalglucosidase alfa)的上市许可,这是一种酶替代疗法(ERT),用于长期治疗晚发和婴儿发作的庞贝病,这是一种罕见的、进行性的、使人衰弱的肌肉疾病。自2006年欧盟委员会批准上市名为Myozyme® 的α葡萄糖苷酶以来,Nexviadyme® 是欧洲第一种也是唯一一种新批准的庞贝病药物。提醒一下,2021年11月,人用药品委员会(CHMP)发布了一项意见,不授予阿尔法雪崩葡萄糖苷酶新活性物质(NAS)地位。2022年4月,孤儿药产品委员会(COMP)还建议将Nexviadyme® 从孤儿药品社区登记册(OMP)中删除。
投资组合更新
第 3 阶段:
•根据关键的 XTEND-1 三期研究的数据,美国食品药品管理局已授予efanesoctog alfa(BIVV001)突破性疗法称号,用于治疗甲型血友病(一种罕见且危及生命的出血性疾病)患者。赛诺菲和索比合作开发和商业化efanesoctocog alfa。
•根据独立审查委员会的评估,IKEMA对复发多发性骨髓瘤患者进行Sarclisa®(伊沙妥昔单抗)联合使用卡非佐米和地塞米松(Kd)的临床试验的最新结果显示,中位无进展存活率(MPF)为35.7个月,而单独接受Kd治疗的患者为19.2个月。
•两项评估venglustat治疗法布里病和高歇氏病3型作用的研究已经开始并招募了第一批参与者。
•对nirsevimab关键的3期MELODY和2b期试验的预先设定合并分析结果显示,对在足月出生或早产儿进入第一个呼吸道病毒季节的婴儿中,由呼吸道合胞病毒(RSV)引起的医疗辅助下呼吸道感染(与安慰剂相比相对风险降低)为79.5%。
•在 VAT08 第 2 阶段试验中,赛诺菲-葛兰素史克下一代候选疫苗(一种含有 D614 和 β(B.1.351)菌株的二价疫苗的阳性数据显示,在奥密克戎变种高度循环的环境下,对有症状的 COVID-19 的疗效为 64.7%,对奥密克龙证实的有症状的病例的疗效为 72%。在以前血清反应阳性的人群中,它对症状感染的总体疗效为75.1%,在Omicron确诊的有症状的病例中,其总体疗效为93.2%。
•对赛诺菲-葛兰素史克下一代 COVID-19 助推剂候选药物(一种含有 Beta (B.1.351) 变体的单价配方,进行的 VAT02 队列 2 研究引起了显著提高
针对先前接种过mRNA COVID-19 疫苗的成年人中,针对多种关注变体(对抗D614母体病毒增加15倍,β毒株增加30倍,对BA.1增加40倍)的抗体滴度高于基线。
•与此同时,由巴黎公共援助组织(AP-HP)进行的独立COVIDBOOST(VAT013)研究表明,在使用两剂辉瑞-BioNTech的Comirnaty疫苗进行初步疫苗接种后,赛诺菲-葛兰素史克下一代增强疫苗产生的免疫反应比辉瑞-BioNTech的加强剂或赛诺菲-葛兰素史克第一代加强剂更高。结合 VAT08 第 2 阶段研究,这些数据有力地表明赛诺菲-葛兰素史克的下一代基于 Beta 的增强剂有可能成为对公共卫生需求的相关回应。
•2022年5月,赛诺菲告知参与托乐鲁替尼治疗多发性硬化症(MS)和重症肌无力(MG)的三期研究的研究人员,在这些试验中发现了有限数量的药物性肝损伤(DILI)病例。这些事件发生在给药后的三个月内,是在现有的肝脏监测中发现的,大多数事件被确定为同时出现并发症,历史上已知容易导致药物引起的肝损伤。重要的是,在所有病例停药后,用于监测肝损伤的实验室值的上升是可逆的。同月,对研究方案进行了修订,以增加监测频率,并将已存在肝功能障碍危险因素的患者排除在入组范围之外。6月下旬,美国食品药品管理局对托乐鲁替尼用于多发性硬化症和重组的3期研究进行了部分临床搁置。结果,美国的新注册被暂停,在美国参加试验不到60天的参与者被暂停了研究药物。同时,全球有超过两千名先前入组的患者继续接受托勒布鲁替尼治疗。7月初,美国食品和药物管理局向赛诺菲发出书面通知,要求提供与临床安全数据和一些临床前数据的额外分析有关的信息。赛诺菲有信心努力在9月底之前向原子能机构提供所要求的信息。提交回复后,美国食品和药物管理局可能需要长达30天的时间才能就是否同意解除部分临床搁置做出决定,这最早可能在第四季度作出。同时,在大多数国家,临床项目的注册仍在继续,修订后的研究方案,包括加强安全监测。自5月份更新的协议生效以来,已有近190名患者入组,这些患者迄今没有出现肝损伤的迹象。赛诺菲预计将在今年年底之前完成RRMS研究机构GEMINI I和GEMINI II的招募工作。赛诺菲正在与世界各地的独立数据监测委员会成员和调查人员密切合作,评估这些安全措施的有效性。基于托乐布鲁替尼强有力的pH2b疗效数据和风险缓解措施,赛诺菲对托勒布鲁替尼作为多发性硬化症患者具有潜在变革性的口服治疗选择的未来仍然充满信心
第 2 阶段:
•评估 SAR445088 治疗抗体介导排斥反应的研究已经开始并招募了第一批参与者。
•评估 SAR443820 治疗肌萎缩性侧索硬化症的安全性和有效性的研究已开始入组。
•评估利扎布替尼对经过大量预处理的免疫血小板减少症(ITP)成人的安全性、药代动力学和临床活性的1/2期剂量发现研究的阳性结果发表在《新英格兰医学杂志》上。结果表明,使用rilzabrutinib进行治疗可以快速持久地增加血小板数量,并支持可接受的安全性。
•评估研究中的miRNA-21 lamidersen(也称为 SAR339375)对Alport综合征疗效的研究因未能满足预先规定的徒劳标准而中止。
•花生过敏中Dupixent® 的开发已停止。
第 1 阶段:
•评估单独使用 SAR446309(使用Amunix获得,以前称为 AMX-818)以及与pembrolizumab联合使用对患有局部晚期或转移性 HER2 表达癌症的成年参与者的安全性和有效性的研究已开始入组。
随着乌克兰的战争,赛诺菲调整了其在该地区的临床试验实施情况。该公司决定停止为俄罗斯和白俄罗斯正在进行的临床试验招募任何新的患者,尽管它将继续治疗已经入组的患者。在乌克兰,赛诺菲正在尽其所能提供支持
并提供目前参加赛诺菲赞助的临床试验的患者,包括将他们转移到乌克兰境内或邻国。由于预计可能会丢失数据,赛诺菲已启动新的临床站点,并在未受战争影响的地区,扩大了患者注册人数。这可能会导致多发性硬化症和慢性阻塞性肺病(COPD)关键试验的初步完成日期发生变化,先前公布的提交时间表保持不变。
截至2022年6月30日的研发渠道更新可在赛诺菲的网站上查阅:
https://www.sanofi.com/en/science-and-innovation/research-and-development
企业社会责任战略的实施进展情况
赛诺菲在改善药品供应方面继续取得进展
赛诺菲全球健康部门宣布设立基金并推出Impact®
赛诺菲全球健康宣布推出Impact®,这是赛诺菲生产的新护理药物标准品牌,专门用于非营利组织向世界上最贫困国家的高危人群分发。Impact® 品牌包括胰岛素、格列本脲和奥沙利铂等,将使30种赛诺菲药物能够在40个低收入国家安全分销。这些药物被世界卫生组织视为必不可少的药物,涵盖了广泛的治疗领域,包括糖尿病、心血管疾病、结核病、疟疾和癌症。
该公司还宣布设立影响力基金,该基金将支持初创公司和其他创新者,他们可以在服务不足的地区为可持续医疗保健提供可扩展的解决方案。通过提供包容性企业融资和技术援助,该基金将补充GHU的使命,即利用全球、区域和地方投资,支持医疗保健专业人员的培训,并帮助社区运行可持续医疗体系。
赛诺菲扩大了美国服务不足社区的使用渠道
在美国,没有保险的糖尿病患者将能够从赛诺菲的Insulins Valyou储蓄计划中获得赛诺菲胰岛素(Lantus、甘精胰岛素 U-100、Toujeo、Admelog和Apidra),持有效处方,固定价格为35美元,为期30天的供应量。这是对胰岛素Valyou储蓄计划的增强。此前,该计划以99美元的价格提供30天的赛诺菲胰岛素供应,最多十盒SoloStar笔和/或10毫升小瓶或5盒Max SoloStar笔。
Insulins Valyou储蓄计划自2018年启动以来,已帮助成千上万的糖尿病患者节省了处方费用。2021年,胰岛素Valyou储蓄计划的使用次数超过97,000次,为糖尿病患者提供了超过3700万美元的储蓄。
此更新旨在为参与该计划的个人提供更多优惠。
赛诺菲加入诺华的希望之灯计划,以解决临床试验、健康和教育领域的种族不平等问题
赛诺菲自豪地宣布与希望之灯计划合作,以解决健康和教育差异的根本原因,并在制药行业的研发中创造更大的多样性、公平性和包容性。
历史上,种族和族裔少数群体在临床研究中一直处于边缘地位。赛诺菲认识到并支持改变这种状况并帮助纠正临床试验参与方面的这种差异的紧迫性。
希望之标于2021年7月启动,由诺华和诺华美国基金会承诺提供3370万美元,最初是与莫尔豪斯医学院和其他26所历史悠久的黑人学院和大学、瑟古德·马歇尔学院基金、Coursera和全国医学会合作的10年合作,共同努力增加临床试验参与者和研究人员的多样性;改善获得高质量教育和有前途的工作机会;解决用于诊断的数据标准中固有的偏见并治疗疾病;并找到为严重影响有色人种社区健康的环境和气候问题提供切实可行的解决方案。
赛诺菲在限制对环境的影响方面继续取得进展
CO2 范围 3 减排新目标
随着赛诺菲旨在最大限度地减少包括气候变化在内的环境影响的雄心勃勃的战略取得重要进展,该公司决定升级其范围3的温室气体(GHG)减排目标,将其从最初的-14%提高到2030年的-30%,这是其到2030年实现碳中和目标的一部分。
上个2021年第三季度,赛诺菲承诺到2030年在所有业务及其整个价值链中实现碳中和,并在2050年之前实现温室气体净零排放,将公司的目标日期比其在 COP21 和《巴黎协定》之后于2015年做出的承诺提前了20年。作为该目标的一部分,到2030年,运营(范围1和2)的温室气体减排目标与2019年基准相比设定为-55%,价值链(范围3)的温室气体减排目标为-14%。这些目标得到了基于科学的目标倡议(SBTi)的验证。去年5月,赛诺菲向SBTI提交了净零目标和升级后的范围3减排目标以供验证。
新加坡的进化疫苗设施:低能耗和 100% 的电气化设计
建立碳中和之路不仅涉及设施改造或优化,还涉及设计环境足迹最低的新工厂。
我们在新加坡的新疫苗设施最大限度地提高了能源效率,包括所有过程的能量回收,并且 100% 电气化,燃气锅炉由热泵取代,所有过程均采用能量回收。所有可用的表面都配备了太阳能电池板以产生可再生电力。剩余的电力供应将来自可再生替代方案,例如长期电力购买协议和可再生能源证书,目标是根据赛诺菲 RE100 的承诺,到2030年实现100%的可再生电力。
ESG 控制面板
2020年,随着赛诺菲重申其企业社会责任雄心,公司审查并更新了其举措组合。下图显示的数字突显了赛诺菲综合企业社会责任战略实施的持续进展。
除非另有说明,否则数据以年初至今计算
实惠的访问权限
赛诺菲全球健康是公司内部于2021年4月成立的非营利机构,旨在为40个最低收入国家的患者提供涵盖广泛治疗领域的30种赛诺菲药物。除了提供的产品外,赛诺菲全球健康还致力于整合计划,确保长期为患者提供最佳的护理管理。
赛诺菲还致力于帮助1,000名无法获得治疗的罕见疾病患者,并将每年捐赠100,000瓶药物用于治疗。这延续了赛诺菲30年来对患有罕见疾病的患者的承诺,例如法布里病、高歇病或庞贝病,这些疾病的治疗机会往往有限。
关于准入的第三项举措是为所有新产品制定全球准入计划,在推出后的两年内在选定的相关市场上市。
| | | | | | | | |
实惠的访问权限 | | |
赛诺菲全球健康 |
| Q1 2022 | Q2 2022 |
疟疾 | •1,024,170 名患者接受了治疗 •8 个国家
| •1,693,770 名患者接受了治疗 •10 个国家 |
肺结核 | •35,094 名患者接受了治疗 •11 个国家
| •76,634 名患者接受了治疗 •13 个国家 |
NCD | •46,300 名患者接受了治疗 •12 个国家 | •85,956 名患者接受了治疗 •21 个国家 |
捐赠罕见病药瓶 |
| Q1 2022 | Q2 2022 |
| # 接受治疗的患者 | 998 | 1,015 |
| #Vials 捐赠了 | 22,682 | 51,370 |
全球访问计划 |
| Q1 2022 | Q2 2022 |
访问计划数量 | 试点阶段和蓝图已完成 |
针对未满足的需求进行研发
赛诺菲继续努力抗击脊髓灰质炎和昏睡病,这是其解决全球健康问题的两项传统计划。
赛诺菲从一开始就参与了对抗脊髓灰质炎的斗争,并将继续在脊髓灰质炎疫苗的交付中发挥关键作用。该公司还承诺与世卫组织合作,到2030年消除昏睡病。
赛诺菲研发目标的一部分是开发创新药物以消除儿童癌症死亡
| | | | | | | | |
针对未满足的需求进行研发 |
根除脊髓灰质炎 |
| Q1 2022 | Q2 2022 |
# 已提供脊髓灰质炎灭活疫苗 (IPV) 剂量 | 为全球疫苗免疫联盟国家向联合国儿童基金会提供了1600万剂IPV疫苗 | 为全球疫苗免疫联盟国家向联合国儿童基金会提供了2700万剂IPV疫苗
|
消除昏睡病
|
| 2020 财年 | 2021 财年 |
# 接受测试的患者 | 160 万 | 2 百万 |
# 接受治疗的患者 | 663 | 805 |
儿科癌症治疗开发 |
| Q1 2022 | Q2 2022 |
已识别的资产数量 | 临床研究方案准备的 2 项资产中的 1 项 | •临床前评估中有 1 项资产 •临床研究方案准备中有 1 项资产 |
地球护理
为了更好地保护资源,赛诺菲计划在2027年之前拆除其注射器疫苗的所有塑料吸塑包装。此外,该公司承诺到2025年对所有新产品进行生态设计。为了到2030年将其温室气体排放量减少55%,赛诺菲的所有基地都将使用100%的可再生能源电力,该公司已设定了到2030年实现其车队碳中和的目标。
| | | | | | | | | | | |
星球护理 |
无水泡疫苗 |
| Q1 2021 | Q2 2022 |
% 无泡注射器疫苗 | 生产的无泡疫苗有 29%
| 数据每年更新一次 |
生态设计 |
| Q1 2021 | Q2 2022 |
生命周期分析 (LCA) 的数量 | 4 个 LCA 已完成,1 个正在进行中 生态设计数字解决方案项目启动
| 5 个 LCA 已完成,3 个正在进行中 生态设计数字解决方案项目正在进行中 |
范围 1 和 2 排放 |
| Q1 2021 | Q2 2022 |
与 2019 年相比,温室气体减少 | -26% | -27% |
可再生电力
|
| Q1 2021 | Q2 2022 |
来自可再生能源的电力消耗百分比 | 60%1 | 60% |
环保车队 |
| Q1 2021 | Q2 2022 |
环保车队占总车队的百分比 | 28.7% 的生态舰队 | 30.4% 生态舰队 |
1. 分拆EUROAPI后重新计算了基线
工作场所内外
作为一家跨国公司,赛诺菲致力于确保其领导者反映其所服务的社区和患者。公司致力于继续培育一个所有员工都有平等机会在公司内部担任责任职位的组织。赛诺菲的目标是到2025年让40%的女性担任高级管理职位,50%的女性担任高级领导职位。赛诺菲将继续参与其经营所在社区的社会和经济活动。最后,赛诺菲正在将其对社会的承诺嵌入其领导者的职业发展道路中,以增强其决策的社会影响力。
| | | | | | | | | | | | | | |
工作场所内外 |
| Q1 2021 | Q2 2022 |
多元化的高级领导层 |
女性百分比 | 35.1% 的高管 我们的高级领导者中有40.4%是女性 | 35.9% 的高管 我们的高级领导者中有41.1%是女性 |
与社区互动 |
| Q1 2021 | Q2 2022 |
# 志愿者 | 4,975 名志愿者 | 1,998 名志愿者 |
# 小时 | 26,906 小时 | 12,687 小时 |
从领袖到公民 |
| Q1 2021 | Q2 2022 |
关键绩效指标 | 计划于2022年推出 |
ESG 评级
近几个月来,赛诺菲社会影响力战略的持续实施使该公司在大多数ESG排名中的排名或等级出现了一系列积极的更新。
2022年第二季度和上半年财务业绩
企业净收入4
2022年第二季度,赛诺菲的净销售额为101.16亿欧元,增长了15.7%(按恒定汇率计算增长8.1%)。上半年的净销售额为197.9亿欧元,增长14.2%(按恒定汇率增长8.4%)。
第二季度其他收入增长了108.0%(按恒定汇率计算增长85.0%),达到6.26亿欧元,其中包括非赛诺菲产品的VaxServe销售额增长了3.93亿欧元(按恒定汇率增长53.5%)。上半年,其他收入增长了68.6%(按恒定汇率计算增长54.7%),达到10.05亿欧元,其中包括VaxServe非赛诺菲产品的销售额6.79亿欧元(按恒定汇率增长35.0%)。
第二季度毛利增长了21.1%(按恒定汇率计算增长12.2%),至74.93亿欧元。与2021年同期相比,毛利率增长了3.3个百分点至74.1%,这反映了在有利的产品组合和效率提高的推动下,药品毛利率的强劲提高(从74.9%提高到78.5%)。疫苗毛利率从56.5%提高到59.3%。CHC的毛利率为66.3%,增长0.3个百分点。在上半年,毛利率增长了2.6个百分点至74.1%(按CER计算为73.6%),这得益于药品和效率的提高。
第二季度研发(R&D)支出增长了18.8%(按CER计算增长12,8%),至16.58亿欧元,这反映了药品优先资产开发和疫苗支出增加。上半年,研发费用增长了18.2%,达到31.47亿欧元(按恒定汇率计算增长13.4%)。
第二季度销售一般和管理费用(SG&A)增长了10.1%,至25.74亿欧元。在CER,销售和收购支出增长了2.8%,这反映了对专业护理增长驱动力的商业投资增加,以及对开支的严格控制。在第二季度,销售和收购占销售额的比率与去年同期相比下降了1.3个百分点至25.4%。上半年,销售和收购支出增长了9.3%,达到49.53亿欧元(按恒定汇率计算增长3.5%),与2021年同期相比,销售和收购与销售额的比率下降了1.1个百分点,至25.0%。
第二季度和上半年的运营支出为42.32亿欧元(按恒定汇率计算增长13.4%和6.6%)和81亿欧元(按恒定汇率增长12.6%和7.2%)。
第二季度扣除支出后的其他当前营业收入为-5.23亿欧元,而2021年第二季度为-1.98亿欧元。扣除支出后的其他当前营业收入包括6.21亿欧元的支出(2021年第二季度的支出为3.07亿欧元),相当于单克隆抗体联盟Regeneron的利润份额,Regeneron对开发成本的报销以及Regeneron产生的商业化相关费用的报销。在第二季度,该项目还包括与普通药品投资组合精简相关的2400万欧元净资本收益,而2021年同期为4700万欧元。2022年上半年,扣除支出后的其他当前营业收入为-7.88亿欧元,而2021年同期为-2.99亿欧元,其中包括与精简投资组合相关的2.56亿欧元净资本收益,而2021年同期为1.03亿欧元。2022年上半年与Regeneron的单克隆抗体联盟相关的支出为10.98亿欧元,而2021年同期为5.86亿欧元(更多细节见附录7)。
第二季度和上半年的员工利润份额为2500万欧元和5,500万欧元,而2021年同期分别为1,700万欧元和2600万欧元,其中包括与VaxelistM相关的美国利润份额。
第二季度业务营业收入4(BOI)增长了21.5%,至27.53亿欧元。在CER,投资回报率增长了13.2%。投资回报率与净销售额的比率增长了1.3个百分点至27.2%,这主要反映了毛利率的提高。上半年,业务营业收入为58.18亿欧元,增长18.7%(按CER计算增长12.7%)。上半年,节省了2.3亿欧元,其中200欧元来自工业事务部,并全部再投资于关键研发项目。上半年,企业营业收入与净销售额的比率增长了1.1个百分点至29.4%(按CER计算为29.4%)。
2022年第二季度和上半年的净财务支出分别为-7700万欧元和-1.55亿欧元,而2021年同期为-7,600万欧元和-1.6亿欧元。
2022年第二季度和上半年的有效税率为19.0%,而去年同期为21.0%。赛诺菲预计,到2022年,其有效税率将达到19%左右。
第二季度业务净收入4增长了25.4%,达到21.7亿欧元,按恒定汇率计算增长了16.6%。与2021年第二季度相比,企业净收入与净销售额的比率增长了1.7个百分点至21.5%。2022年上半年,业务净收入增长了22.6%,达到45.94亿欧元,按恒定汇率计算增长了16.3%。与2021年同期相比,企业净收入与净销售额的比率增长了1.6个百分点至23.2%。
4参见2022年第二季度合并损益表附录3;财务指标定义见附录9,参见附录4以报告企业净收益的国际财务报告准则净收益对账。
2022年第二季度,每股业务收益4(每股收益)为1.73欧元,按报告计算增长25.4%(按恒定汇率增长16.7%)。平均已发行股票数量为12.508亿股,而2021年第二季度为12.513亿股。2022年上半年,每股业务收益8为3.68欧元,按报告计算增长22.7%,按恒定汇率计算增长16.3%。平均已发行股票数量为12.50亿股,而2021年上半年为12.503亿股。
报告的《国际财务报告准则》净收益与企业净收益的对账(见附录4)
2022年上半年,国际财务报告准则的净收入为31.84亿欧元。不包括在业务净收入中的主要项目是:
•9.1亿欧元的摊销费用涉及被收购公司的无形资产(主要是Genzyme:2.73亿欧元,Bioverativ:1.81亿欧元,勃林格殷格翰CHC业务:9500万欧元,Ablynx:8400万欧元,Kadmon:7700万欧元)以及收购的无形资产(许可证/产品:5700万欧元)。这些项目对公司没有现金影响。
•无形资产减值8700万欧元。
•与精简计划相关的重组成本和类似项目为7.92亿欧元。
•由上述项目产生的5.73亿欧元的税收影响,主要包括无形资产摊销和减值产生的2.18亿欧元递延税,以及与重组成本和类似项目相关的1.99亿欧元(见附录4)。
EUROAPI 分拆对赛诺菲国际财务报告准则账户的影响
“其他收益和亏损,诉讼” 一栏包括2022年5月10日EUROAPI股票实物分配后的1,000万欧元税前解除合并收益。
当天,赛诺菲失去了控制权,停止巩固EUROAPI。赛诺菲取消了EUROAPI账面净值资产的100%,包括商誉,12.27亿欧元。其他影响是:
•减持7.93亿欧元的股权,相当于按当时在泛欧交易所观察到的EUROAPI市场份额计算的实物分配的公允价值,
•2022年6月17日从法国政府通过其法国科技主权基金EPIC BPIFrance以1.5亿欧元收购的EUROAPI12%的股本中获利,
•按公允价值计量的EUROAPI留存权益为4.13亿欧元。
“税收收入” 额度包括EUROAPI交易后的1.02亿欧元收益。
资本分配
2022年上半年,扣除营运资金(-7.1亿欧元)和资本支出(-6.96亿欧元)的净变动,重组、收购和处置前的自由现金流下降了17.6%,至37.35亿欧元。在收购5(-4.19亿欧元)、出售收益5(5.41亿欧元)以及与重组和类似项目相关的付款(-6.15亿欧元)之后,自由现金流6下降了3.3%,至32.42亿欧元。收购Amunix(-8.75亿欧元)后,赛诺菲支付的股息(-41.68亿欧元),净负债从2021年12月31日的99.83亿欧元增加到2022年6月30日的121.9亿欧元(扣除68.99亿欧元的现金和现金等价物)。
5 每笔交易不超过5亿欧元(包括与交易相关的所有付款)。
6 非公认会计准则财务指标(定义见附录9)。
前瞻性陈述
本新闻稿包含经修订的1995年《私人证券诉讼改革法》中定义的前瞻性陈述。前瞻性陈述是不是历史事实的陈述。这些陈述包括预测和估计及其基本假设,有关未来财务业绩、事件、运营、服务、产品开发和潜力的计划、目标、意图和预期的陈述,以及有关未来业绩的陈述。前瞻性陈述通常由 “期望”、“预期”、“相信”、“打算”、“估计”、“计划” 和类似表述来识别。尽管赛诺菲管理层认为此类前瞻性陈述中反映的预期是合理的,但提醒投资者,前瞻性信息和陈述存在各种风险和不确定性,其中许多风险和不确定性难以预测,通常超出赛诺菲的控制范围,这可能导致实际业绩和发展与前瞻性信息和陈述所表达、暗示或预测的业绩和发展存在重大差异。除其他外,这些风险和不确定性包括研发固有的不确定性、未来的临床数据和分析,包括上市后的分析、监管机构(例如FDA或EMA)关于是否及何时批准任何此类候选产品可能申请的任何药物、设备或生物学应用的决定,以及他们关于标签和其他可能影响此类候选产品可用性或商业潜力的事项的决定,候选产品如果获得批准的事实可能不会在商业上取得成功、替代疗法的未来批准和商业成功、赛诺菲从外部增长机会中受益、完成关联交易和/或获得监管许可的能力、与知识产权和任何相关的未决或未来诉讼相关的风险以及此类诉讼的最终结果、汇率和现行利率的趋势、动荡的经济和市场状况、成本控制举措及其后续变化,以及 COVID-19 将产生的影响关系到我们、我们的客户、供应商、供应商和其他业务伙伴,以及其中任何一个的财务状况,以及我们的员工和整个全球经济的状况。COVID-19 对上述任何内容的任何实质性影响也可能对我们产生不利影响。这种情况正在迅速变化,可能会产生我们目前尚未意识到的额外影响,并可能加剧先前确定的其他风险。风险和不确定性还包括赛诺菲在向美国证券交易委员会和AMF提交的公开文件中讨论或确定的不确定性,包括赛诺菲截至2021年12月31日止年度的20-F表年度报告中 “风险因素” 和 “关于前瞻性陈述的警示性声明” 中列出的不确定性。除适用法律的要求外,赛诺菲不承担任何更新或修改任何前瞻性信息或陈述的义务。
附录
| | | | | |
附录 1: | 按GBU、特许经营、地理区域和产品划分的2022年第二季度和上半年的销售额 |
附录二: | 2022年第二季度和上半年企业净损益表 |
附录 3: | 2022年第二季度和上半年合并损益表 |
附录 4: | 报告的《国际财务报告准则》净收益与企业净收入的对账 |
附录 5: | 净负债的变化 |
| |
| |
| 附录 6: | 简化的合并资产负债表 |
| 附录 7: | 扣除支出后的其他当期营业收入 — Regeneron Alliances |
附录 8: | 货币敏感度 |
附录 9: | 非公认会计准则财务指标的定义 |
媒体关系
Sandrine Guendoul | + 33 6 25 25 09 14 25 | sandrine.guendoul@sanofi.com
Sally Bain | + 1 617 834 6026 | sally.bain@sanofi.com
Chrystel Baude | + 33 6 70 98 70 59 | chrystel.baude@sanofi.com
埃文·伯兰德 | +1 215 432 0234 | evan.berland@sanofi.com
尼古拉斯·奥布里斯特 | + 33 6 77 21 27 55 | nicolas.obrist@sanofi.com
Victor Rouault | + 33 6 70 93 71 40 | victor.rouault@sanofi.com
凯特·康威 | + 1 508 364 4931 | kate.conway@sanofi.com
投资者关系
Eva Schaefer-Jansen | + 33 7 86 80 56 39 | eva.schaefer-jansen@sanofi.com
Arnaud Delépine | + 33 6 73 69 36 93 | arnaud.delepine@sanofi.com
Corentine Driancourt | + 33 6 40 56 92 21 | corentine.driancourt@sanofi.com
Felix Lauscher | + 1 908 612 7239 | felix.lauscher@sanofi.com
普里亚·南杜里 | +1 617 764 6418 | priya.nanduri@sanofi.com
Nathalie Pham | + 33 7 85 93 30 17 | nathalie.pham@sanofi.com
附录1:按GBU、特许经营、地理区域和产品划分的2022年第二季度和上半年的净销售额
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年第二季度(百万欧元) | 总销售额 | % CER | % 已报告 | | 美国 | % CER | | 欧洲 | % CER | | 世界其他地区 | % CER |
| Dupixent | 1,963 | +43.4 | % | +57.9 | % | | 1,477 | +37.9 | % | | 239 | +56.6 | % | | 247 | +65.3 | % |
| 奥巴吉奥 | 526 | -2.2 | % | +6.5 | % | | 360 | -2.8 | % | | 137 | +3.0 | % | | 29 | -17.1 | % |
| 莱姆特拉达 | 20 | 0.0 | % | +5.3 | % | | 8 | -30.0 | % | | 6 | 0.0 | % | | 6 | +100.0 | % |
| Kevzara | 77 | +30.4 | % | +37.5 | % | | 40 | +40.0 | % | | 25 | +25.0 | % | | 12 | +18.2 | % |
| 神经病学和免疫学 | 623 | +1.1 | % | +9.5 | % | | 408 | -0.6 | % | | 168 | +5.7 | % | | 47 | -2.0 | % |
| Cerezyme | 202 | +18.8 | % | +22.4 | % | | 49 | 0.0 | % | | 66 | +8.2 | % | | 87 | +42.6 | % |
| Cerdelga | 72 | +11.5 | % | +18.0 | % | | 39 | +9.4 | % | | 28 | +12.0 | % | | 5 | +25.0 | % |
| Myozyme | 252 | -3.6 | % | +1.6 | % | | 81 | -21.7 | % | | 103 | +1.0 | % | | 68 | +18.5 | % |
| Nexviazyme | 43 | +3900.0 | % | +4200.0 | % | | 37 | 0.0 | % | | 2 | +100.0 | % | | 4 | 0.0 | % |
| Fabrazyme | 238 | +9.3 | % | +16.7 | % | | 116 | +6.2 | % | | 58 | +7.4 | % | | 64 | +17.0 | % |
| Aldurazyme | 64 | +7.0 | % | +12.3 | % | | 16 | 0.0 | % | | 21 | +10.0 | % | | 27 | +8.7 | % |
| 罕见病 | 891 | +11.6 | % | +17.4 | % | | 338 | +7.6 | % | | 279 | +6.5 | % | | 274 | +22.9 | % |
| 杰夫塔纳 | 105 | -15.8 | % | -7.9 | % | | 74 | +8.2 | % | | 8 | -73.3 | % | | 23 | -4.3 | % |
| Fasturtec | 46 | +7.7 | % | +17.9 | % | | 30 | +18.2 | % | | 12 | +9.1 | % | | 4 | -33.3 | % |
| Libtayo | 47 | +36.4 | % | +42.4 | % | | — | 0.0 | % | | 36 | +38.5 | % | | 11 | +28.6 | % |
| Sarclisa | 64 | +52.5 | % | +60.0 | % | | 30 | +62.5 | % | | 16 | +14.3 | % | | 18 | +90.0 | % |
| 肿瘤学 | 263 | +8.0 | % | +16.4 | % | | 134 | +19.2 | % | | 72 | -11.1 | % | | 57 | +17.4 | % |
| Alprolix | 129 | +16.0 | % | +29.0 | % | | 106 | +12.0 | % | | — | 0.0 | % | | 23 | +35.3 | % |
| Eloctate | 153 | -3.5 | % | +6.3 | % | | 124 | -3.5 | % | | — | 0.0 | % | | 29 | -3.2 | % |
| Cablivi | 51 | +4.3 | % | +10.9 | % | | 26 | +9.5 | % | | 24 | 0.0 | % | | 1 | 0.0 | % |
| 罕见血液病 | 336 | +5.5 | % | +15.9 | % | | 259 | +5.1 | % | | 24 | 0.0 | % | | 53 | +10.4 | % |
| 专业护理 | 4,076 | +21.6 | % | +32.0 | % | | 2,616 | +21.4 | % | | 782 | +15.2 | % | | 678 | +30.9 | % |
| | | | | | | | | | | | |
| 洛文诺克斯 | 337 | -10.9 | % | -8.2 | % | | 2 | -50.0 | % | | 168 | -7.7 | % | | 167 | -13.7 | % |
| Toujeo | 267 | +2.4 | % | +8.1 | % | | 70 | +5.2 | % | | 107 | +6.9 | % | | 90 | -4.5 | % |
| Plavix | 247 | 0.0 | % | +5.6 | % | | 2 | -33.3 | % | | 26 | -16.1 | % | | 219 | +3.0 | % |
| Multaq | 91 | +2.5 | % | +15.2 | % | | 82 | +2.9 | % | | 4 | -33.3 | % | | 5 | +66.7 | % |
| 胸腺球蛋白 | 113 | +12.0 | % | +22.8 | % | | 65 | +3.6 | % | | 9 | +12.5 | % | | 39 | +27.6 | % |
| Mozobil | 66 | +6.9 | % | +13.8 | % | | 40 | +9.4 | % | | 16 | +6.7 | % | | 10 | 0.0 | % |
| Praluent | 128 | +147.9 | % | +166.7 | % | | 55 | 0.0 | % | | 55 | +41.0 | % | | 18 | +77.8 | % |
| soliqua/iglarLixi | 53 | +4.3 | % | +15.2 | % | | 26 | -11.1 | % | | 7 | +14.3 | % | | 20 | +33.3 | % |
| Rezurock | 43 | 0.0 | % | 0.0 | % | | 43 | 0.0 | % | | — | 0.0 | % | | — | 0.0 | % |
| 其他核心资产 | 266 | -3.5 | % | +3.5 | % | | 47 | -35.8 | % | | 87 | -2.2 | % | | 132 | +17.0 | % |
| 核心资产 | 1,611 | +6.0 | % | +12.8 | % | | 432 | +21.3 | % | | 479 | +0.6 | % | | 700 | +2.4 | % |
| 兰图斯 | 600 | -12.1 | % | -5.8 | % | | 217 | -19.0 | % | | 111 | -7.4 | % | | 272 | -8.2 | % |
| Aprovel | 120 | +13.1 | % | +21.2 | % | | 2 | +100.0 | % | | 21 | -12.5 | % | | 97 | +20.3 | % |
| 其他非核心资产 | 1,133 | -8.5 | % | -4.8 | % | | 101 | -10.1 | % | | 293 | -11.3 | % | | 739 | -7.1 | % |
| 非核心资产 | 1,853 | -8.6 | % | -3.8 | % | | 320 | -16.0 | % | | 425 | -10.4 | % | | 1,108 | -5.5 | % |
| 工业销售 | 133 | -33.3 | % | -30.7 | % | | 3 | -84.6 | % | | 126 | -30.7 | % | | 4 | 0.0 | % |
| 普通药物 | 3,597 | -4.1 | % | +1.4 | % | | 755 | +0.3 | % | | 1,030 | -8.9 | % | | 1,812 | -2.6 | % |
| | | | | | | | | | | | |
| 药品 | 7,673 | +7.9 | % | +15.7 | % | | 3,371 | +16.0 | % | | 1,812 | +0.1 | % | | 2,490 | +4.9 | % |
| | | | | | | | | | | | |
| 脊髓灰质炎/百日咳/乙型流感嗜血杆菌 | 589 | +7.9 | % | +13.3 | % | | 99 | -17.0 | % | | 83 | +23.9 | % | | 407 | +12.4 | % |
| 加强疫苗 | 152 | +32.1 | % | +43.4 | % | | 91 | +24.6 | % | | 43 | +34.4 | % | | 18 | +77.8 | % |
| 脑膜炎 | 153 | -24.7 | % | -17.7 | % | | 109 | -26.7 | % | | 4 | +300.0 | % | | 40 | -25.9 | % |
| 流感疫苗 | 115 | -5.9 | % | -3.4 | % | | — | 0.0 | % | | 33 | +266.7 | % | | 82 | -28.2 | % |
| 旅行和流行疫苗 | 145 | +83.8 | % | +95.9 | % | | 51 | +100.0 | % | | 25 | +200.0 | % | | 69 | +54.5 | % |
| 疫苗 | 1,178 | +8.7 | % | +15.3 | % | | 372 | -3.5 | % | | 188 | +59.8 | % | | 618 | +5.5 | % |
| | | | | | | | | | | | |
| 过敏 | 192 | +16.2 | % | +29.7 | % | | 118 | +11.7 | % | | 20 | +25.0 | % | | 54 | +23.7 | % |
| 咳嗽和感冒 | 98 | +74.5 | % | +78.2 | % | | — | 0.0 | % | | 56 | +166.7 | % | | 42 | +17.6 | % |
| 疼痛护理 | 304 | +5.8 | % | +10.5 | % | | 57 | -2.0 | % | | 138 | +7.8 | % | | 109 | +7.3 | % |
| 消化健康 | 336 | +9.3 | % | +15.9 | % | | 33 | -19.4 | % | | 112 | +18.9 | % | | 191 | +10.1 | % |
| 身体健康 | 85 | +2.6 | % | +9.0 | % | | — | 0.0 | % | | 5 | 0.0 | % | | 80 | +2.7 | % |
| 心理健康 | 57 | 0.0 | % | +5.6 | % | | 12 | -8.3 | % | | 26 | 0.0 | % | | 19 | +6.3 | % |
| 个人护理 | 149 | +5.5 | % | +17.3 | % | | 113 | +6.3 | % | | — | -100.0 | % | | 36 | +6.5 | % |
| 非核心 /其他 | 44 | -29.0 | % | -29.0 | % | | 2 | -100.0 | % | | 18 | -33.3 | % | | 24 | -27.8 | % |
| 消费者医疗保健 | 1,265 | +9.1 | % | +16.2 | % | | 335 | +3.1 | % | | 375 | +17.9 | % | | 555 | +6.8 | % |
| | | | | | | | | | | | |
| 公司 | 10,116 | +8.1 | % | +15.7 | % | | 4,078 | +12.7 | % | | 2,375 | +5.7 | % | | 3,663 | +5.3 | % |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年上半年(百万欧元) | 总销售额 | % CER | % 已报告 | | 美国 | % CER | | 欧洲 | % CER | | 世界其他地区 | % CER |
| Dupixent | 3,577 | +44.4 | % | +56.2 | % | | 2,653 | +38.0 | % | | 450 | +55.0 | % | | 474 | +75.5 | % |
| 奥巴吉奥 | 1,017 | -4.4 | % | +2.3 | % | | 689 | -6.3 | % | | 269 | +1.5 | % | | 59 | -9.4 | % |
| 莱姆特拉达 | 45 | 0.0 | % | +4.7 | % | | 19 | -15.0 | % | | 12 | +9.1 | % | | 14 | +16.7 | % |
| Kevzara | 172 | +46.0 | % | +52.2 | % | | 90 | +64.0 | % | | 53 | +29.3 | % | | 29 | +36.4 | % |
| 神经病学和免疫学 | 1,234 | +0.7 | % | +7.3 | % | | 798 | -1.8 | % | | 334 | +5.4 | % | | 102 | +4.1 | % |
| Cerezyme | 367 | +5.5 | % | +7.0 | % | | 94 | +2.4 | % | | 126 | +1.6 | % | | 147 | +11.0 | % |
| Cerdelga | 139 | +7.3 | % | +13.0 | % | | 75 | +6.3 | % | | 55 | +7.8 | % | | 9 | +12.5 | % |
| Myozyme | 487 | -3.3 | % | +0.8 | % | | 163 | -17.8 | % | | 206 | +2.5 | % | | 118 | +10.7 | % |
| Nexviazyme | 73 | +6700.0 | % | +7200.0 | % | | 63 | 0.0 | % | | 3 | +200.0 | % | | 7 | 0.0 | % |
| Fabrazyme | 458 | +5.8 | % | +11.2 | % | | 221 | +5.3 | % | | 116 | +4.5 | % | | 121 | +8.1 | % |
| Aldurazyme | 133 | +4.9 | % | +8.1 | % | | 29 | 0.0 | % | | 45 | +4.7 | % | | 59 | +7.4 | % |
| 罕见病 | 1,695 | +6.7 | % | +10.9 | % | | 645 | +7.4 | % | | 553 | +4.2 | % | | 497 | +9.0 | % |
| 杰夫塔纳 | 203 | -20.8 | % | -15.4 | % | | 142 | +8.4 | % | | 19 | -74.7 | % | | 42 | -8.7 | % |
| Fasturtec | 86 | +8.1 | % | +16.2 | % | | 54 | +14.0 | % | | 24 | +9.1 | % | | 8 | -22.2 | % |
| Libtayo | 88 | +44.1 | % | +49.2 | % | | — | 0.0 | % | | 70 | +43.8 | % | | 18 | +45.5 | % |
| Sarclisa | 129 | +67.6 | % | +74.3 | % | | 55 | +78.6 | % | | 38 | +40.7 | % | | 36 | +89.5 | % |
| 肿瘤学 | 507 | +7.4 | % | +13.4 | % | | 251 | +20.0 | % | | 151 | -12.8 | % | | 105 | +20.0 | % |
| Alprolix | 237 | +9.0 | % | +18.5 | % | | 198 | +10.5 | % | | — | 0.0 | % | | 39 | +2.6 | % |
| Eloctate | 291 | -3.2 | % | +4.7 | % | | 232 | -2.8 | % | | — | 0.0 | % | | 59 | -4.8 | % |
| Cablivi | 97 | +9.5 | % | +15.5 | % | | 48 | +2.3 | % | | 47 | +17.5 | % | | 2 | 0.0 | % |
| 罕见血液病 | 629 | +3.7 | % | +11.9 | % | | 482 | +3.8 | % | | 47 | +17.5 | % | | 100 | -2.0 | % |
| 专业护理 | 7,642 | +19.8 | % | +27.8 | % | | 4,829 | +20.4 | % | | 1,535 | +13.6 | % | | 1,278 | +25.7 | % |
| | | | | | | | | | | | |
| 洛文诺克斯 | 714 | -9.5 | % | -7.0 | % | | 7 | -60.0 | % | | 353 | -4.1 | % | | 354 | -12.7 | % |
| Toujeo | 541 | +4.4 | % | +8.2 | % | | 128 | -4.2 | % | | 211 | +8.2 | % | | 202 | +5.9 | % |
| Plavix | 508 | 0.0 | % | +4.7 | % | | 5 | -20.0 | % | | 52 | -13.3 | % | | 451 | +2.1 | % |
| Multaq | 178 | +7.9 | % | +17.9 | % | | 160 | +9.8 | % | | 9 | -25.0 | % | | 9 | +28.6 | % |
| 胸腺球蛋白 | 210 | +12.8 | % | +22.1 | % | | 121 | +7.9 | % | | 17 | +6.3 | % | | 72 | +23.6 | % |
| Mozobil | 124 | +6.4 | % | +12.7 | % | | 71 | +6.7 | % | | 31 | +6.9 | % | | 22 | +4.8 | % |
| Praluent | 197 | +79.8 | % | +89.4 | % | | 55 | +860.0 | % | | 108 | +42.7 | % | | 34 | +33.3 | % |
| soliqua/iglarLixi | 106 | +10.0 | % | +17.8 | % | | 56 | -3.8 | % | | 15 | +7.1 | % | | 35 | +43.5 | % |
| Rezurock | 84 | 0.0 | % | 0.0 | % | | 84 | 0.0 | % | | — | 0.0 | % | | — | 0.0 | % |
| 其他核心资产 | 543 | -0.8 | % | +4.0 | % | | 86 | -36.6 | % | | 182 | +4.0 | % | | 275 | +15.2 | % |
| 核心资产 | 3,205 | +5.3 | % | +10.4 | % | | 773 | +13.4 | % | | 978 | +3.5 | % | | 1,454 | +2.9 | % |
| 兰图斯 | 1,271 | -6.7 | % | -1.4 | % | | 425 | -10.3 | % | | 223 | -9.3 | % | | 623 | -3.3 | % |
| Aprovel | 245 | +15.5 | % | +22.5 | % | | 3 | 0.0 | % | | 42 | -10.6 | % | | 200 | +24.0 | % |
| 其他非核心资产 | 2,320 | -7.9 | % | -5.2 | % | | 196 | -6.3 | % | | 593 | -10.1 | % | | 1,531 | -7.3 | % |
| 非核心资产 | 3,836 | -6.4 | % | -2.5 | % | | 624 | -9.0 | % | | 858 | -9.9 | % | | 2,354 | -4.2 | % |
| 工业销售 | 316 | -18.9 | % | -16.8 | % | | 13 | -54.2 | % | | 294 | -13.7 | % | | 9 | -61.9 | % |
| 普通药物 | 7,357 | -2.3 | % | +1.9 | % | | 1,410 | +1.0 | % | | 2,130 | -4.8 | % | | 3,817 | -2.0 | % |
| | | | | | | | | | | | |
| 药品 | 14,999 | +7.7 | % | +13.7 | % | | 6,239 | +15.4 | % | | 3,665 | +2.1 | % | | 5,095 | +3.9 | % |
| | | | | | | | | | | | |
| 脊髓灰质炎/百日咳/乙型流感嗜血杆菌 | 1,202 | +9.1 | % | +14.2 | % | | 224 | -15.4 | % | | 161 | +11.0 | % | | 817 | +17.5 | % |
| 加强疫苗 | 261 | +18.4 | % | +26.7 | % | | 144 | +15.0 | % | | 74 | +12.1 | % | | 43 | +48.1 | % |
| 脑膜炎 | 265 | -21.3 | % | -15.6 | % | | 185 | -19.3 | % | | 6 | +500.0 | % | | 74 | -30.2 | % |
| 流感疫苗 | 181 | -10.7 | % | -7.7 | % | | 12 | 0.0 | % | | 37 | +105.6 | % | | 132 | -28.7 | % |
| 旅行和流行疫苗 | 243 | +73.7 | % | +82.7 | % | | 74 | +83.3 | % | | 42 | +215.4 | % | | 127 | +47.6 | % |
| 疫苗 | 2,198 | +7.8 | % | +13.5 | % | | 678 | -2.1 | % | | 321 | +31.1 | % | | 1,199 | +8.2 | % |
| | | | | | | | | | | | |
| 过敏 | 418 | +13.4 | % | +21.9 | % | | 249 | +13.5 | % | | 37 | +8.8 | % | | 132 | +14.7 | % |
| 咳嗽和感冒 | 219 | +96.4 | % | +99.1 | % | | — | 0.0 | % | | 122 | +165.2 | % | | 97 | +46.9 | % |
| 疼痛护理 | 618 | +13.8 | % | +17.0 | % | | 103 | +2.2 | % | | 289 | +15.6 | % | | 226 | +17.1 | % |
| 消化健康 | 661 | +11.5 | % | +15.4 | % | | 62 | -8.2 | % | | 224 | +12.0 | % | | 375 | +15.1 | % |
| 身体健康 | 173 | +5.0 | % | +8.8 | % | | — | 0.0 | % | | 11 | -15.4 | % | | 162 | +6.8 | % |
| 心理健康 | 123 | +13.1 | % | +15.0 | % | | 24 | -4.3 | % | | 60 | +9.1 | % | | 39 | +34.5 | % |
| 个人护理 | 279 | +1.6 | % | +10.7 | % | | 209 | -0.5 | % | | 1 | -50.0 | % | | 69 | +10.2 | % |
| 非核心 /其他 | 102 | -22.3 | % | -21.5 | % | | (2) | -175.0 | % | | 37 | -32.1 | % | | 67 | -6.8 | % |
| 消费者医疗保健 | 2,593 | +13.1 | % | +17.8 | % | | 645 | +2.6 | % | | 781 | +19.4 | % | | 1,167 | +14.9 | % |
| | | | | | | | | | | | |
| 公司 | 19,790 | +8.4 | % | +14.2 | % | | 7,562 | +12.4 | % | | 4,767 | +6.2 | % | | 7,461 | +6.2 | % |
附录 2:企业净损益表
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022 年第二季度 | 药品 | 疫苗 | 消费者医疗保健 | 其他 (1) | 道达尔集团 |
| 百万欧元 | Q2 2022 | Q2 2021 (2) | 改变 | Q2 2022 | Q2 2021 (2) | 改变 | Q2 2022 | Q2 2021 (2) | 改变 | Q2 2022 | Q2 2021 (2) | 改变 | Q2 2022 | Q2 2021 (2) | 改变 |
| 净销售额 | 7,673 | 6,633 | 15.7% | 1,178 | 1,022 | 15.3% | 1,265 | 1,089 | 16.2% | — | — | —% | 10,116 | 8,744 | 15.7% |
| 其他收入 | 191 | 58 | 229,3% | 418 | 230 | 81,7% | 16 | 13 | 23.1% | 1 | — | —% | 626 | 301 | 108,0% |
| 销售成本 | (1,844) | (1,725) | 6,9% | (897) | (675) | 32,9% | (442) | (383) | 15.4% | (66) | (75) | (12.0)% | (3,249) | (2,858) | 13.7% |
| 占净销售额的百分比 | (24,0%) | (26.0)% | | (76,1%) | (66.0)% | | (34.9)% | (35.2)% | | | | | (32,1%) | (32.7)% | |
| 毛利 | 6,020 | 4,966 | 21.2% | 699 | 577 | 21.1% | 839 | 719 | 16.7% | (65) | (75) | (13.3)% | 7,493 | 6,187 | 21.1% |
| 占净销售额的百分比 | 78.5% | 74.9% | | 59.3% | 56.5% | | 66.3% | 66.0% | | | | | 74.1% | 70.8% | |
| 研究和开发费用 | (1,277) | (1,061) | 20.4% | (227) | (171) | 32.7% | (45) | (41) | 9.8% | (109) | (123) | (11.4)% | (1,658) | (1,396) | 18.8% |
| 占净销售额的百分比 | (16.6)% | (16.0)% | | (19.3)% | (16.7)% | | (3.6)% | (3.8)% | | | | | (16.4)% | (16.0)% | |
| 销售和一般费用 | (1,440) | (1,293) | 11.4% | (197) | (189) | 4.2% | (370) | (356) | 3.9% | (567) | (499) | 13.6% | (2,574) | (2,337) | 10.1% |
| 占净销售额的百分比 | (18.8)% | (19.5)% | | (16.7)% | (18.5)% | | (29.2)% | (32.7)% | | | | | (25.4)% | (26.7)% | |
| 其他当期营业收入/支出 | (475) | (213) | | 2 | — | | (9) | 13 | | (41) | 2 | | (523) | (198) | |
| 联营公司*和合资企业的利润/亏损份额 | 8 | 6 | | 9 | 9 | | 8 | 2 | | — | — | | 25 | 17 | |
| 归属于非控股权益的净收益 | (10) | (8) | | — | — | | — | — | | — | — | | (10) | (8) | |
| 企业营业收入 | 2,826 | 2,397 | 17.9% | 286 | 226 | 26.5% | 423 | 337 | 25.5% | (782) | (695) | 12.5% | 2,753 | 2,265 | 21.5% |
| 占净销售额的百分比 | 36.8% | 36.1% | | 24.3% | 22.1% | | 33.4% | 30.9% | | | | | 27.2% | 25.9% | |
| | | | | | | | | | | | | | | |
| | | | 财务收入和支出 | (77) | (76) | |
| | | | 所得税支出 | | | | | (506) | (458) | |
| | | | 税率** | | | | | 19.0% | 21.0% | |
| | | | 业务净收入 | | | | | 2,170 | 1,731 | 25.4% |
| | | | 占净销售额的百分比 | | | | | 21.5% | 19.8% | |
| | | | | | | | | | | |
| | | | 企业收益/股份(单位:欧元)*** | 1.73 | 1.38 | 25.4% |
* 扣除税款。
** 根据税前业务收入、关联公司和非控股权益确定。
*** 基于2022年第二季度平均已发行12.508亿股和2021年第二季度12.513亿股的平均流通股数。
(1) 其他包括全球支持职能(财务、人力资源、信息解决方案与技术、赛诺菲商业服务等)的费用。
(2) 包括2021年4月IFRIC最终议程决定对服务期福利分配的影响。
附录 2:企业净损益表
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| 2022年半年 | 药品 | 疫苗 | 消费者医疗保健 | 其他 (1) | 道达尔集团 | | | | |
| 百万欧元 | 6M 2022 | 6M 2021 (2) | 改变 | 6M 2022 | 6M 2021 (2) | 改变 | 6M 2022 | 6M 2021 (2) | 改变 | 6M 2022 | 6M 2021 (2) | 改变 | 6M 2022 | 6M 2021 (2) | 改变 | | | | |
| 净销售额 | 14,999 | 13,196 | 13.7% | 2,198 | 1,937 | 13.5% | 2,593 | 2,202 | 17.8% | — | — | —% | 19,790 | 17,335 | 14.2% | | | | |
| 其他收入 | 266 | 108 | 146.3% | 707 | 461 | 53.4% | 30 | 27 | 11.1% | 2 | — | —% | 1,005 | 596 | 68.6% | | | | |
| 销售成本 | (3,539) | (3,404) | 4.0% | (1,578) | (1,254) | 25.8% | (890) | (753) | 18.2% | (120) | (131) | (8.4)% | (6,127) | (5,542) | 10.6% | | | | |
| 占净销售额的百分比 | (23.6)% | (25.8)% | | (71.8)% | (64.7)% | | (34.3)% | (34.2)% | | | | | (31.0)% | (32.0)% | | | | | |
| 毛利 | 11,726 | 9,900 | 18.4% | 1,327 | 1,144 | 16.0% | 1,733 | 1,476 | 17.4% | (118) | (131) | (9.9)% | 14,668 | 12,389 | 18.4% | | | | |
| 占净销售额的百分比 | 78.2% | 75.0% | | 60.4% | 59.1% | | 66.8% | 67.0% | | | | | 74.1% | 71.5% | | | | | |
| 研究和开发费用 | (2,442) | (2,040) | 19.7% | (412) | (316) | 30.4% | (81) | (69) | 17.4% | (212) | (238) | (10.9)% | (3,147) | (2,663) | 18.2% | | | | |
| 占净销售额的百分比 | (16.3)% | (15.5)% | | (18.7)% | (16.3)% | | (3.1)% | (3.1)% | | | | | (15.9)% | (15.4)% | | | | | |
| 销售和一般费用 | (2,748) | (2,481) | 10.8% | (367) | (359) | 2.2% | (752) | (700) | 7.4% | (1,086) | (991) | 9.6% | (4,953) | (4,531) | 9.3% | | | | |
| 占净销售额的百分比 | (18.3)% | (18.8)% | | (16.7)% | (18.5)% | | (29.0)% | (31.8)% | | | | | (25.0)% | (26.1)% | | | | | |
| 其他当期营业收入/支出 | (886) | (465) | | 9 | 120 | | 113 | 23 | | (24) | 23 | | (788) | (299) | | | | | |
| 关联公司*和合资企业的利润/亏损份额 | 22 | 13 | | 25 | 8 | | 8 | 5 | | — | — | | 55 | 26 | | | | | |
| 归属于非控股权益的净收益 | (15) | (16) | | — | — | | (2) | (4) | | — | — | | (17) | (20) | | | | | |
企业营业收入 | 5,657 | 4,911 | 15.2% | 582 | 597 | -2.5% | 1,019 | 731 | 39.4% | (1,440) | (1,337) | 7.7% | 5,818 | 4,902 | 18.7% | | | | |
| 占净销售额的百分比 | 37.7% | 37.2% | | 26.5% | 30.8% | | 39.3% | 33.2% | | | | | 29.4% | 28.3% | | | | | |
| | | | | | | | | | | | | | | | | | | |
| | | | | | | 财务收入和支出 | (155) | (160) | | | | | |
| | | | | | | 所得税支出 | | (1,069) | (995) | | | | | |
| | | | | | | 税率** | | 19.0% | 21.0% | | | | | |
| | | | | | | 业务净收入 | | 4,594 | 3,747 | 22.6% | | | | |
| | | | | | | 占净销售额的百分比 | | 23.2% | 21.6% | | | | | |
| | | | | | | | | | | | | | | |
| | | | | | | 企业收益/股份(单位:欧元)*** | 3.68 | 3.00 | 22.7% | | | | |
* 扣除税款。
** 根据税前业务收入、关联公司和非控股权益确定。
*** 基于2022年上半年平均已发行12.50亿股和2021年上半年12.503亿股已发行股票的平均数量。
(1) 其他包括全球支持职能(财务、人力资源、信息解决方案与技术、赛诺菲商业服务等)的费用。
(2) 包括2021年4月IFRIC最终议程决定对服务期福利分配的影响。
附录 3:合并损益表
| | | | | | | | | | | | | | |
| 百万欧元 | Q2 2022 | Q2 2021 (1) | 到2022年 | 到 2021 年 (1) |
| 净销售额 | 10,116 | | 8,744 | | 19,790 | | 17,335 | |
| 其他收入 | 626 | | 301 | | 1,005 | | 596 | |
| 销售成本 | (3,250) | | (2,858) | | (6,130) | | (5,542) | |
| 毛利 | 7,492 | | 6,187 | | 14,665 | | 12,389 | |
| 研究和开发费用 | (1,658) | | (1,396) | | (3,147) | | (2,663) | |
| 销售和一般费用 | (2,574) | | (2,337) | | (4,953) | | (4,531) | |
| 其他营业收入 | 26 | | 143 | | 416 | | 410 | |
| 其他运营费用 | (549) | | (341) | | (1,204) | | (709) | |
| 无形资产的摊销 | (461) | | (386) | | (910) | | (775) | |
无形资产减值 | (82) | | (176) | | (87) | | (178) | |
| 或有对价的公允价值重新计量 | (21) | | 32 | | (17) | | (4) | |
| 重组成本和类似项目 | (617) | | (187) | | (792) | | (343) | |
其他得失和诉讼 | (124) | | — | | (142) | | — | |
| | | | |
| 营业收入 | 1,432 | | 1,539 | | 3,829 | | 3,596 | |
| 财务费用 | (101) | | (89) | | (189) | | (188) | |
| 财务收入 | 24 | | 14 | | 34 | | 28 | |
| 税前收入、联营企业和合资企业 | 1,355 | | 1,463 | | 3,674 | | 3,436 | |
| 所得税支出 | (163) | | (274) | | (495) | | (678) | |
| 联营企业和合资企业的利润/(亏损)份额 | 28 | | 17 | | 58 | | 26 | |
| | | | |
| | | | |
| 净收入 | 1,220 | | 1,206 | | 3,237 | | 2,784 | |
| 归属于非控股权益的净收益 | 45 | | 8 | | 53 | | 20 | |
| 归属于赛诺菲股东的净收益 | 1,175 | | 1,198 | | 3,184 | | 2,764 | |
| 平均已发行股票数量(百万) | 1,250.8 | | 1,251.3 | | 1,250.0 | | 1,250.3 | |
| | | | |
| 国际财务报告准则每股收益(单位:欧元) | 0.94 | | 0.96 | | 2.55 | | 2.21 | |
(1) 包括IFRIC2021年3月的最终议程决定对配置或定制软件即服务(SaaS)安排中使用的应用程序软件的成本以及2021年4月对服务期收益归因的影响。
附录4:归属于赛诺菲股东的净收益与业务净收益的对账
| | | | | | | | | | | | | | |
| 百万欧元 | Q2 2022 | Q2 2021 (1) | 到2022年 | 到 2021 年 (1) |
| 归属于赛诺菲股东的净收益 | 1,175 | | 1,198 | | 3,184 | | 2,764 | |
无形资产摊销 (2) | 461 | | 386 | | 910 | | 775 | |
无形资产减值 | 82 | | 176 | | 87 | | 178 | |
| 或有对价的公允价值重新计量 | 21 | | (32) | | 17 | | 4 | |
| 收购对库存的影响所产生的费用 | — | | — | | 3 | | — | |
| 重组成本和类似项目 | 617 | | 187 | | 792 | | 343 | |
其他得失和诉讼 | 124 | | — | | 142 | | — | |
| | | | |
| 上面列出的项目的税收影响: | (341) | | (183) | | (573) | | (316) | |
| 无形资产的摊销和减值 | (122) | | (140) | | (218) | | (230) | |
| 或有对价的公允价值重新计量 | (11) | | 4 | | (18) | | 3 | |
| | | | |
| 重组成本和类似项目 | (153) | | (47) | | (199) | | (89) | |
| | | | |
| 其他税收影响 | (55) | | — | | (138) | | — | |
| | | | |
| 其他物品 | 31 | | (1) | | 32 | | (1) | |
| | | | |
| | | | |
| | | | |
| 业务净收入 | 2,170 | | 1,731 | | 4,594 | | 3,747 | |
国际财务报告准则每股收益 (3)(以欧元计) | 0.94 | | 0.96 | | 2.55 | | 2.21 | |
(1) 包括IFRIC2021年3月的最终议程决定对配置或定制软件即服务(SaaS)安排中使用的应用程序软件的成本以及2021年4月对服务期收益归因的影响。
(2)其中与作为业务合并一部分的无形资产重新评估所产生的摊销费用有关:2022年第二季度为4.28亿欧元,2021年第二季度为3.67亿欧元。
(3) 第二季度:基于2022年第二季度平均流通股数12.508亿股和2021年第二季度12.513亿股。
HY:根据2022年上半年平均已发行12.50亿股和上半年12.503亿股的平均已发行股票数量计算
2021.
附录5:净负债的变化
| | | | | | | | | | | |
| 百万欧元 | H1 2022 | H1 2021 | (1) |
| 业务净收入 | 4,594 | | 3,747 | | |
| 不动产、厂房、设备和软件的折旧、摊销和减值 | 771 | | 708 | | |
| 其他物品 | (224) | | 142 | | |
| 运营现金流 | 5,141 | | 4,597 | | |
| 营运资金的变化 | (710) | | 611 | | |
| 购置不动产、厂房和设备及软件 | (696) | | (673) | | |
| 重组、收购和处置前的自由现金流 | 3,735 | | 4,535 | | |
收购无形资产、投资和其他长期金融资产 (2) | (419) | | (902) | | |
| 已支付的重组费用和类似项目 | (615) | | (526) | | |
处置不动产、厂房和设备、无形资产和其他非流动资产扣除税款后的收益 (2) | 541 | | 247 | | |
| 自由现金流 | 3,242 | | 3,354 | | |
收购合并企业投资,包括 假定债务 (3) | (941) | | (984) | | |
资产处置扣除税款后的收益 (3) | 101 | | — | | |
| | | |
| | | |
| 赛诺菲股票的发行 | 40 | | 23 | | |
| 收购库存股 | (360) | | (140) | | |
| 向赛诺菲股东支付的股息 | (4,168) | | (4,008) | | |
| 其他物品 | (121) | | 78 | | |
| 净负债的变化 | (2,207) | | (1,677) | | |
| 期初 | 9,983 | | 8,790 | | |
| 结清净债务 | 12,190 | | 10,467 | | |
(1) 包括IFRIC2021年3月的最终议程决定对配置或定制软件即服务(SaaS)安排中使用的应用程序软件的成本以及2021年4月对服务期收益归因的影响。
(2) 自由现金流包括每笔交易上限不超过5亿欧元的投资和撤资(包括与交易相关的所有付款)。
(3) 包括每笔交易上限超过5亿欧元的交易(包括与交易相关的所有付款)。
附录 6:简化的合并资产负债表
| | | | | | | | | | | | | | | | | | | | | | | |
| 资产(百万欧元) | 2022年6月30日 | 2021年12月31日 | | 负债和权益(百万欧元) | 2022年6月30日 | 2021年12月31日 | |
| | | | 归属于赛诺菲股权持有人的权益 | 70,951 | 68,681 | |
| | | | 归属于非控股权益的权益 | 353 | 350 | |
| | | | 权益总额 | 71,304 | 69,031 | |
| | | | 长期债务 | 15,942 | 17,123 | |
| 不动产、厂房和设备-自有资产 | 9,767 | 10,028 | | 非流动租赁负债 | 2,001 | 1,839 | |
| 使用权资产 | 1,875 | 1,948 | | 与业务合并和非控股权益相关的非流动负债 | 742 | 577 | |
| | | | | | | |
| | | | | | | |
| 无形资产(包括商誉) | 72,533 | 69,463 | | 非流动准备金和其他非流动负债 | 6,181 | 6,721 | |
| 非流动所得税资产 | 187 | 175 | | 非流动所得税负债 | 2,029 | 2,039 | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| 非流动金融资产以及对联营公司和递延所得税资产的投资 | 8,818 | 7,975 | | 递延所得税负债 | 1,550 | 1,617 | |
| 非流动资产 | 93,180 | 89,589 | | 非流动负债 | 28,445 | 29,916 | |
| | | | | | | |
| | | | | | | |
| | | | 应付账款和其他流动负债 | 18,233 | 17,397 | |
| | | | 与业务合并和非控股权益相关的流动负债 | 90 | 137 | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| 库存、应收账款和其他流动资产 | 20,923 | 19,854 | | 当前所得税负债 | 443 | 309 | |
| 当前所得税资产 | 538 | 612 | | 当期租赁负债 | 231 | 269 | |
| 现金和现金等价物 | 6,899 | 10,098 | | 短期债务和长期债务的流动部分 | 3,063 | 3,183 | |
| 流动资产 | 28,360 | 30,564 | | 流动负债 | 22,060 | 21,295 | |
| 持有待出售或交换的资产 | 286 | 89 | | 与持有待出售或交换的资产相关的负债 | 17 | 0 | |
| 总资产 | 121,826 | 120,242 | | 权益和负债总额 | 121,826 | 120,242 | |
| | | | | | | |
附录7:扣除支出后的其他当期营业收入 — Regeneron Alliances
| | | | | | | | |
| 百万欧元 | H1 2022 | H1 2021 |
单克隆抗体联盟 | | |
与损益分成相关的收入和支出 | (979) | (521) |
Regeneron 支付的额外利润份额与开发成本有关 | 97 | 51 |
Regeneron 商业运营费用报销 | (216) | (116) |
总计:单克隆抗体联盟 | (1,098) | (586) |
免疫肿瘤学联盟 | | |
全面免疫肿瘤学联盟 | 36 | 37 |
其他 Regeneron | | |
与 Regeneron(主要是 Zaltrap®)相关的其他总数 | (6) | (6) |
| Total Regeneron 联盟 | (1,068) | (555) |
附录 8:货币敏感度
2022年企业每股收益货币敏感度
| | | | | | | | |
| 货币 | 变体 | 企业每股收益灵敏度 |
| 美元 | +0.05 美元/欧元 | -欧元 0.14 |
| 日元 | +5 日元/欧元 | -0.02 欧元 |
| 中国元 | +0.2 人民币/欧元 | -0.02 欧元 |
| 巴西雷亚尔 | +0.4 巴西雷亚尔/欧元 | -欧元 0.01 |
| 俄罗斯卢布 | +10 卢布/欧元 | -0.02 欧元 |
2022年第二季度销售额的货币敞口
| | | | | | | | | | | |
| 货币 | Q2 2022 | | |
| 我们 $ | 41.4 | % | | |
| 欧元 € | 20.4 | % | | |
| 中国元 | 7.3 | % | | |
| 日元 | 3.9 | % | | |
| 巴西雷亚尔 | 2.2 | % | | |
| 墨西哥比索 | 1.7 | % | | |
| 澳大利亚元 $ | 1.5 | % | | |
| 俄罗斯卢布 | 1.4 | % | | |
| 加拿大元 | 1.3 | % | | |
| 英镑 | 1.3 | % | | |
| 其他 | 17.6 | % | | |
货币平均汇率
| | | | | | | | | | | | | | | | | | | | |
| Q2 2021 | Q2 2022 | 改变 | | | | | |
| €/$ | 1.21 | | 1.07 | | -11.7 | % | | | | | |
| 欧元/日元 | 131.91 | | 138.14 | | +4.7 | % | | | | | |
| 欧元/元 | 7.79 | | 7.06 | | -9.4 | % | | | | | |
| 欧元/雷亚尔 | 6.39 | | 5.24 | | -18.0 | % | | | | | |
| 欧元/卢布 | 89.49 | | 71.40 | | -20.2 | % | | | | | |
附录 9:非公认会计准则财务指标的定义
按固定汇率 (CER) 计算的公司销售额
当我们提到 “按固定汇率”(CER)计算的净销售额变化时,这意味着我们排除了汇率变动的影响。
我们通过使用前一时期的汇率重新计算相关时期的净销售额来消除汇率的影响。
2022年第二季度和上半年按固定汇率计算的净销售额与公司销售额的对账
| | | | | | | | |
| 百万欧元 | Q2 2022 | H1 2022 |
| 净销售额 | 10,116 | | 19,790 | |
| 汇率的影响 | 661 | | 1,002 | |
| 按固定汇率计算的公司销售额 | 9,455 | | 18,788 | |
业务净收入
赛诺菲发布了一项重要的非公认会计准则指标。业务净收益定义为归属于赛诺菲股东的净收益,不包括:
•摊销无形资产,
•无形资产减值,
•重新计量与业务合并或处置相关的或有对价的公允价值,
•收购对库存的影响所产生的费用
•与收购相关的其他影响(包括收购对关联公司和合资企业的影响),
•重组成本和类似项目(1),
•其他损益(包括处置非流动资产的损益(1)),
•与诉讼相关的费用或条款 (1),
•与上述项目相关的税收影响以及重大税收纠纷的影响,
•归属于与上述项目相关的非控股权益的净收益。
(1) 在合并财务报表附注B.19和B.20中列报的重组成本和类似项目以及处置损益和诉讼损益。
自由现金流
自由现金流是一项非公认会计准则财务指标,由我们的管理层审查,我们认为它为衡量公司运营产生的净现金提供了有用的信息,可用于战略投资1(扣除撤资1)、债务偿还和股东资本回报。自由现金流由经折旧、摊销和减值调整后的企业净收入、扣除股息后的关联公司和合资企业的损益份额、处置损益、包括养老金和其他离职后福利在内的准备金的净变动、递延税、基于股份的支出和其他非现金项目等准备金的净变动来确定。它包括扣除处置收益2后的营运资金、资本支出和其他资产收购的净变动2,以及与重组和类似项目相关的付款。自由现金流不是国际财务报告准则定义的,它不能替代国际财务报告准则经营活动中总净现金流量的衡量标准。
1 交易金额超过每笔交易5亿欧元的上限(包括与交易相关的所有付款)。
2 每笔交易的上限不超过5亿欧元(包括与交易相关的所有付款)。
从运营活动提供/(用于)的净现金与自由现金流的对账
| | | | | | | | |
| 百万欧元 | H1 2022 | H1 2021 (2) |
合并现金流量表中由/(用于)经营活动提供的净现金 (1) | 3,825 | | 4,727 | |
| 购置财产、厂房、设备和软件 | (696) | | (673) | |
收购无形资产、投资和其他长期金融资产 (3) | (419) | | (902) | |
处置不动产、厂房和设备、无形资产和其他非流动资产扣除税款后的收益 (3) | 541 | | 247 | |
偿还租赁负债 | (137) | | (106) | |
| 其他 | 128 | | 61 | |
自由现金流 (4) | 3,242 | | 3,354 | |
1 与自由现金流最直接比较的《国际财务报告准则》。
2 包括2021年3月IFRIC最终议程决定对配置或定制软件即服务(SaaS)安排中使用的应用程序软件的成本以及2021年4月对服务期收益归因的影响。
3 笔交易,每笔交易不超过5亿欧元。
4 非国际财务报告准则指标(见附录9中的定义)。