美国
美国证券交易委员会
华盛顿特区,20549
表格
截至本财政年度止
或
由_至_的过渡期
委托文件编号:
(注册人的确切姓名载于其章程)
|
||
(述明或其他司法管辖权 |
|
(税务局雇主 |
|
||
(主要行政办公室地址) |
|
(邮政编码) |
注册人的电话号码,包括区号:(
根据该法第12(B)条登记的证券:
每节课的标题 |
|
交易代码 |
|
注册的每个交易所的名称 |
|
|
这个 |
||
认股权证,以每股11.50美元收购普通股的一半 |
|
CLNNW |
|
纳斯达克资本市场 |
根据该法第12(G)条登记的证券:没有。
如果注册人是证券法规则405中定义的知名经验丰富的发行人,请用复选标记表示。是的☐
如果注册人不需要根据交易法第13节或第15(D)节提交报告,请用复选标记表示。是的☐
用复选标记表示注册人(1)是否在过去12个月内(或注册人被要求提交此类报告的较短时间内)提交了1934年《证券交易法》第13条或15(D)节所要求的所有报告,以及(2)在过去90天内是否符合此类提交要求。
用复选标记表示注册人是否在过去12个月内(或在注册人被要求提交此类文件的较短时间内)以电子方式提交了根据S-T规则第405条(本章232.405节)要求提交的每个交互数据文件。
用复选标记表示注册人是大型加速申报公司、加速申报公司、非加速申报公司、较小的报告公司或新兴成长型公司。请参阅《交易法》第12b-2条规则中“大型加速申报公司”、“加速申报公司”、“较小申报公司”和“新兴成长型公司”的定义。
大型加速文件服务器 |
☐ |
加速文件管理器 |
☐ |
☒ |
规模较小的报告公司 |
||
|
|
新兴成长型公司 |
如果是新兴成长型公司,用勾号表示注册人是否选择不使用延长的过渡期来遵守根据交易所法案第13(A)节提供的任何新的或修订的财务会计准则。
用复选标记表示注册人是否提交了一份报告,证明其管理层根据《萨班斯-奥克斯利法案》(《美国联邦法典》第15编,第7262(B)节)第404(B)条对其财务报告的内部控制的有效性进行了评估,该评估是由编制或发布其审计报告的注册会计师事务所进行的。
用复选标记表示注册人是否是空壳公司(如《交易法》第12b-2条所定义)。是,☐不是
截至2021年6月30日,也就是注册人最近完成的第二财季的最后一个营业日,非关联公司持有的注册人普通股的总市值约为$
截至2022年3月8日,注册人普通股的流通股数量为
以引用方式并入的文件
注册人的最终委托书中与其2022年股东年会有关的部分通过引用并入本年度报告的Form 10-K第III部分。最终委托书将在与本报告相关的财政年度结束后120天内提交给美国证券交易委员会。
Clene Inc.
截至2021年12月31日的Form 10-K年度报告
第一部分 |
|
3 |
|
第1项。 |
业务 |
|
5 |
第1A项。 |
风险因素 |
|
47 |
项目1B。 |
未解决的员工意见 |
|
79 |
第二项。 |
属性 |
|
79 |
第三项。 |
法律诉讼 |
|
79 |
第四项。 |
煤矿安全信息披露 |
|
79 |
|
|
|
|
第二部分 |
|
80 |
|
第五项。 |
注册人普通股市场、相关股东事项与发行人购买股权证券 |
|
80 |
第六项。 |
[已保留] |
|
80 |
第7项。 |
管理层对财务状况和经营成果的探讨与分析 |
|
81 |
第7A项。 |
关于市场风险的定量和定性披露 |
|
92 |
第八项。 |
财务报表和补充数据 |
|
93 |
第九项。 |
会计与财务信息披露的变更与分歧 |
|
94 |
第9A项。 |
控制和程序 |
|
94 |
项目9B。 |
其他信息 |
|
95 |
项目9C。 |
关于妨碍检查的外国司法管辖区的披露 |
|
95 |
|
|
|
|
第三部分 |
|
96 |
|
第10项。 |
董事、高管与公司治理 |
|
96 |
第11项。 |
高管薪酬 |
|
96 |
第12项。 |
某些实益拥有人的担保所有权以及管理层和相关股东的事项 |
|
96 |
第13项。 |
某些关系和相关交易,以及董事的独立性 |
|
96 |
第14项。 |
首席会计师费用及服务 |
|
96 |
|
|
|
|
第四部分 |
|
97 |
|
第15项。 |
展品和财务报表附表 |
|
97 |
第16项。 |
表格10-K摘要 |
|
98 |
2
目录表
第一部分
在本10-K表格年度报告(“年度报告”)中,“公司”以及对“我们”、“我们”或类似内容的提及应理解为对Clene Inc.及其合并子公司的提及。
有关前瞻性陈述的警示说明
就联邦证券法而言,本年度报告中的某些陈述可能构成“前瞻性陈述”。我们的前瞻性陈述包括但不限于有关我们或我们的管理团队对我们未来业务的期望、希望、信念、意图或战略的陈述。此外,任何提及未来事件或情况的预测、预测或其他特征,包括任何基本假设的陈述,均为前瞻性陈述。词语“预期”、“相信”、“考虑”、“继续”、“可能”、“估计”、“预期”、“打算”、“可能”、“可能”、“计划”、“可能”、“潜在”、“预测”、“项目”、“应该”、“将会”、“将会”以及类似的表述可以识别前瞻性陈述。但没有这些话并不意味着一份声明不具有前瞻性。本年度报告中的前瞻性陈述可能包括,例如,关于以下方面的陈述:
这些前瞻性陈述代表了我们截至本年度报告日期的观点,涉及许多判断、风险和不确定因素。我们预计随后发生的事件和事态发展将导致我们的观点发生变化。我们没有义务更新前瞻性陈述,以反映它们作出之后的事件或情况,无论是由于新信息、未来事件或其他原因,除非适用的证券法可能要求这样做。因此,不应将前瞻性陈述视为代表我们截至随后任何日期的观点。
由于许多已知和未知的风险和不确定性,我们的实际结果或表现可能与这些前瞻性陈述中明示或暗示的结果或表现大不相同。可能导致实际结果不同的一些因素包括:
3
目录表
此外,“我们相信”的声明和类似的声明反映了我们对相关主题的信念和意见。这些陈述是基于截至本年度报告日期我们掌握的信息,虽然我们认为这些信息构成了此类陈述的合理基础,但这些信息可能是有限或不完整的,我们的陈述不应被解读为表明我们已对所有可能获得的相关信息进行了详尽的调查或审查。这些陈述本质上是不确定的,提醒您不要过度依赖这些陈述。
与我们的业务相关的重大风险摘要
我们的业务受到许多重大风险和其他风险的影响,在做出投资决定之前,您应该意识到这些风险。这些风险在题为“风险因素”的一节中有更全面的讨论。除其他外,这些风险包括:
4
目录表
项目1.BU粘性
概述
我们是一家临床阶段的制药公司,致力于新型清洁表面纳米技术(CSN)的发现、开发和商业化®“)治疗学。CSN®治疗药物由过渡元素的原子组成,当这些元素以纳米晶体的形式组装时,具有异常高的独特催化活性,而这些相同元素中没有以块状形式存在。这些催化活动驱动、支持和维持患病、应激和受损细胞内有益的代谢和能量细胞反应。
我们受专利保护的专有地位使我们有潜力开发一条广泛而深入的新型CSN管道®治疗对人类健康有很大影响的一系列疾病。我们从2013年开始,创新了一个电晶体化学药物开发平台,该平台借鉴了纳米技术、等离子体和量子物理、材料科学和生物化学的进步。我们的平台工艺导致纳米晶体具有刻面表面,没有伴随其他生产方法的化学表面修饰。许多传统的纳米颗粒合成方法都涉及到在颗粒表面不可避免地沉积潜在的有毒有机残留物和稳定的表面活性剂。合成既无毒又高度催化的稳定纳米晶体已经克服了在利用过渡金属催化活性用于治疗方面的这一重大障碍。
我们清洁的表面纳米晶体显示出比其他商业上可用的纳米粒子高出许多倍的催化活性,这些纳米粒子是使用各种技术生产的,我们已经进行了比较评估。我们有多种候选药物,在神经学、传染病和肿瘤学方面有潜在的应用。我们目前的努力集中于解决两个领域尚未得到满足的高度医疗需求:第一,与包括肌萎缩侧索硬化症(ALS)、多发性硬化症(MS)和帕金森病(PD)在内的中枢神经系统疾病有关的需求;第二,与新冠肺炎相关的需求,这是一种高度传染性的病毒性呼吸道疾病,会严重,有时甚至致命。
克雷恩方法
克雷恩的药物开发方法是专注于创新和科学驱动.
战略和领导力
我们的管理团队是成功执行这一战略计划和实现我们的商业模式的关键。我们卓越的团队为他们提供了广泛的专业知识和行业经验,使他们能够熟练而有效地领导公司。执行团队成员在科学创新、早期和后期药物开发、商业化、营销以及知识产权的产生和保护方面建立了良好的记录。
我们对CSN的创新®治疗候选药物使我们处于治疗一系列高影响、高需求的人类疾病的新药开发的前沿。当我们领导CSN的发展时®治疗公司,我们的业务战略可以概括为以下几点:
5
目录表
知识产权、商业秘密和制造业
我们是我们制造工艺、设备和药物的唯一发明者。这些发明受到全球150多项专利的全面知识产权组合的保护,另外还有大约20项专利正在申请中。更多细节见“-知识产权”。这些专利涉及(1)制造我们的CSN的设备®治疗药物候选,(2)使用这些装置所涉及的过程,(3)在这些装置中制造的候选药物,以及(4)候选药物的使用方法。除了美国的申请外(“U.S.”)和外国专利,我们将继续通过使用商标、商业秘密、版权保护和持续的技术创新来保护和维护我们的专利地位。例如,我们投入了多年的密集研究和开发来微调我们的生产和交付过程,以期能够一致、可靠和负担得起地生产我们的候选药物,包括CNM-Au8®,以满足大规模需求。我们认为,在不违反我们的知识产权保护的情况下,任何反向工程或以其他方式复制我们的发现的尝试都将对潜在竞争对手构成极大的挑战。
我们还专注于建立一个强大和相关的商业秘密组合。我们的商业秘密组合自始至终都与我们的水性产品的液体处理和加工有关。以我们的主要资产CNM-Au8为例®,含有至少一种加工增强剂的高纯水进入生产设备,在那里它暴露在等离子体调节步骤中。等离子体调节的确切性质会影响其他成分,这些成分会成为流动水的一部分,从而影响后续的晶体生长过程。同样,电极设计、配置和操作的许多细节也影响发生在每组电极上的电化学晶体生长过程。同样,每个槽设备的许多设计和操作方面都直接影响发生在每个电极组上的电化学晶体生长过程。最后,晶体生长后液体处理的各个方面,如浓缩和填充,都是至关重要的,以免向液体中引入任何污染物,这可能会改变纳米晶体的表面,从而增加毒性和/或对生物催化过程的效果产生不利影响。我们继续探索在我们产品的设计、生产、控制和制造的各个方面扩大我们的商业秘密组合的其他方法。
我们的制造工厂在生产我们的CSN时符合严格的国际良好制造流程(GMP)标准®治疗学。此外,我们目前正在增加我们的制造设施空间,以满足预期的商业需求,如果我们的候选药物之一被批准用于商业销售。随着我们继续满足对我们产品的预期未来需求,我们拥有扩大和扩大生产的专业知识。
产品
我们的CSN®候选治疗药物旨在解决几个疾病领域高度未得到满足的医疗需求,包括:
除了开发具有催化活性、刻面、表面清洁的纳米晶体外,我们的电子晶体化学平台还可以生产各种过渡元素的离子溶液,包括银、锌和其他元素-这些元素在治疗疾病方面已被证明具有历史实用价值。
6
目录表
补充剂
我们的专利电化学制造平台进一步使我们能够开发极低浓度的膳食补充剂,以促进广大人群的健康和福祉。这些膳食补充剂可以有很大的不同,包括不同组成、形状和大小的纳米晶体以及具有不同金属成分的离子溶液。
膳食补充剂通过我们的全资子公司dOrbary,Inc.(“dOrbary”),或通过股东和关联方4Life Research LLC(“4Life”)的独家许可证进行营销和分销。这些措施包括:
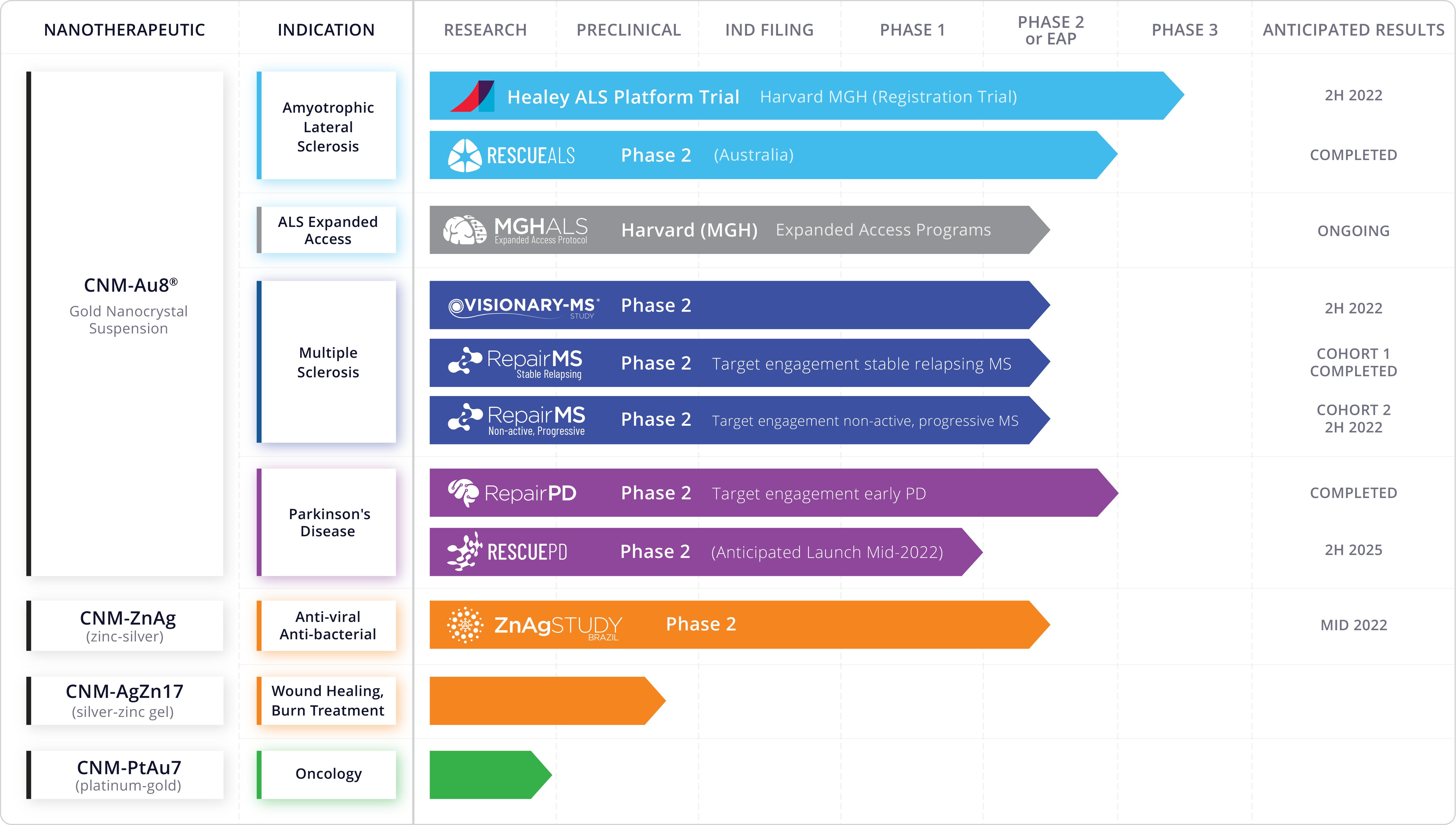
临床开发管道
CNM-AU8®:我们有一个2/3阶段的注册临床试验,Healey ALS平台试验,目前正在进行中,以确定CNM-Au8的安全性和有效性®肌萎缩侧索硬化症患者。我们完成了RESPECT-ALS,这是一项第二阶段的概念验证临床试验,以评估CNM-Au8的有效性、安全性、药代动力学和药效学®在早期有症状的ALS患者中。我们还完成了Repair-PD和Repair-MS的第一个剂量队列,两个开放标记的研究人员盲目第二阶段临床试验,证明了CNM-Au8的靶向参与®对大脑能量代谢物的影响。修复-MS将继续启动
7
目录表
第二个剂量队列的成员。此外,我们还进行了治疗慢性视神经病变视觉通路缺陷的第二阶段临床试验Visionary-MS,以评估CNM-Au8的有效性、安全性、耐受性和药代动力学。®对于稳定复发的MS患者的再髓鞘形成,我们支持为ALS患者提供两个EAP。最初的EAP于2019年9月与马萨诸塞州综合医院的Sean M.Healey&AMG中心(“Healey Center”)合作推出,适用于ALS,目前对新参与者关闭,但仍在进行中。第二个EAP与Healey ALS平台试验一起在三个参与的临床站点实施。最后,我们预计在2022年年中推出RESPECT-PD,这是治疗PD患者的第二阶段临床试验。
CNM-ZnAg:我们目前正在进行一项第二阶段临床试验,以确定锌银液体溶液治疗新冠肺炎的有效性和安全性。
下面的图表反映了我们主要候选药物的各个阶段。

我们的CSN®治疗平台
我们已经开发了一种新的制药技术,CSN®治疗学。通过将电化学、纳米技术、等离子体和量子物理、材料科学和生物化学的概念结合起来,我们创造和改进了一种专有的电结晶方法,这种方法可以在过渡元素的纳米晶体中产生单一或多个成分,这些纳米晶体表面干净,具有高度的刻面,并且具有生物催化活性。这些纳米晶体可以浓缩成水悬浮液并口服。我们还能够利用我们的电化学制造平台生产各种过渡元素的离子溶液。一旦进入胃肠道系统,纳米晶体就会进入血流,并在肝脏、肾脏和脾等器官中蓄积,较少的纳米晶体穿过血脑屏障,到达脑、脊髓和脑脊液。纳米晶体可以在体内保持几天的活性,然后通过肝胆-粪便系统和泌尿系统被清除。
一旦进入体内,CSN®治疗药物穿过细胞膜进入细胞,在那里它们直接在生物系统内捐赠和接收电子。通过这种方式,每个纳米晶体充当一个有效的催化剂,可以驱动、支持和维持患病、应激和受损细胞内有益的代谢和能量细胞反应。我们认为,这些基于纳米晶体的催化治疗药物代表了一种全新的药物开发方法,与小分子药物和大分子生物制品的标准范例有很大不同。与局限于单一靶点或特定信号通路的传统药理学方法不同,我们的技术平台生产了金属纳米晶体,这些纳米晶体通过多种细胞类型的多模式活动跨越多种疾病而受益。通过利用细胞催化剂支持细胞内的能量反应,我们相信这项技术代表着在治疗神经退化和与能量衰竭相关的相关疾病的潜在病理生理学方面取得的革命性进展。
8
目录表
下面的图1显示了使用我们的CSN可以生产的纳米晶体的种类的例子®治疗平台。
图1.代表性CSN®治疗性纳米晶

图1.金纳米晶体(CNM-AU8)常见晶型的代表性透射电子显微镜®)由我们的CSN产生®治疗平台。插图是线框,说明每个经典形状:A,五角形双金字塔;B,四面体;C,六角双金字塔。这些纳米晶的直径为10-13 nm。
具有催化活性的纳米晶
催化剂降低了化学反应的活化能,从而加快了反应的速度,而不会在反应中消耗。在这样做时,它不会改变底物和产物的平衡,它可以催化正向和反向反应,直到达到动态平衡或底物和产物的平衡。
已经发现了金属纳米晶的几种工业用途,但据我们所知,我们相信我们是目前唯一家开发催化活性纳米晶来直接调节生物系统作为治疗药物候选的公司。在我们发明CSN之前®在治疗平台上,用于制造稳定纳米颗粒的方法需要使用有机溶剂或封顶剂,这会污染纳米颗粒的表面,并且基本上很难去除。关于这些纳米颗粒的毒性,文献中有多个相互矛盾的报告,从据说无毒到对活体有高度毒性。我们认为,这种一致性的缺乏可能是由于不同的纳米颗粒制剂被有机试剂污染的程度不同,导致了观察到的毒性效应。由于我们的电晶体化学方法不涉及使用任何有机溶剂或还原化学品,我们观察到我们的纳米晶体在生物体中具有比使用其他方法制备的纳米颗粒更高的催化活性。使用我们的主要资产CNM-Au8完成的所有毒理学研究®,已经导致了NOAEL的发现。
过渡金属纳米晶是表面催化剂。与酶不同的是,酶是通过活性中心结合口袋降低激活能的蛋白质催化剂,而金属纳米晶体在其表面进行催化活性,在那里它们充当异常有效的电子供体和接受者。因此,未经修饰、清洁、没有污染化学物质的表面对催化活性极其重要。纳米晶体的小面和顶点是发生电子交换的表面区。金属纳米晶对葡萄糖、抗坏血酸或含能代谢物烟酰胺腺嘌呤二核苷酸(NAD)的氧化反应具有多种不同的催化活性,包括超氧化物歧化酶、过氧化氢酶和过氧化氢酶样活性。图2是催化的图解,显示了一个单一的金纳米晶体将背景中的烟酰胺腺嘌呤二核苷酸氢化物(NADH)分子转化为前景中的NAD。金纳米晶体被描述为电子储存库,因为它们的表面可以很容易地每秒接受和释放数千个电子,以便催化生化反应,使它们能够将反应速度加速到极高的水平。例如,在室温下,NADH向NAD的转化通常非常缓慢。添加我们的金纳米晶悬浮液CNM-AU8®,我们观察到NADH转化为NAD的速度非常快。重要的是,NAD反应通过一种称为糖酵解的反应,在线粒体和细胞质中驱动三磷酸腺苷(“ATP”)的产生。ATP是所有生物中能量的通用货币;如果没有能力将NADH转换为NAD,反之亦然,细胞将很快耗尽ATP能量储存并死亡。CSN®治疗学捕捉刻面、表面清洁的纳米晶体的自然、非凡的催化活性,以产生对细胞具有高能量或保护价值的代谢物。
9
目录表
图2.催化活性纳米晶机理表示

图2.催化活性图解(不是按比例)。五角形双锥体金纳米晶体与其电子云一起表示该纳米晶体与与其表面相互作用的衬底快速交换电子的能力。在背景中,绘制为黑色化学球棒图形的NADH分子被催化转化为前景中亮粉色球棒图形的NAD。左边的粉色和蓝色线粒体可以利用可用的NAD生成ATP(Ella Maru绘制)。
我们对中枢神经系统疾病的关注
在过去的几十年里,传统的小分子和生物药物开发方法在解决神经系统疾病的尝试中遭受了严重挫折。造成这些挫折的一个可能因素是这些疾病本身背后的多因素机制,这些机制足够复杂,它们可能不适合“一种药物、一种靶点”的疾病修改。面对这些失败,我们相信我们的纳米晶体药物开发的新范式是有利的,它生产出具有独特催化、多模式作用机制的新型药物。
现在有多条证据表明,精力衰竭是神经退行性疾病的关键因素。神经元及其相关的支持细胞,特别是少突胶质细胞,是人体中能量消耗最高的细胞之一:大脑只占人体体重的2%,但它消耗了人体代谢能量的20%以上。随着人类年龄的增长,我们的细胞将食物转化为能量的能力变得不那么有效。最终,神经系统对三磷酸腺苷的需求超过了细胞的供应能力,结果,神经元开始衰竭,随后死亡。遗传和环境因素决定了哪些神经元类型在任何个体中最容易受到能量衰竭的影响。在帕金森病中,多巴胺能和其他类型的神经细胞表现为线粒体衰竭,导致能量产生受损。在肌萎缩侧索硬化症中,线粒体功能障碍被认为是散发性和家族性肌萎缩侧索硬化症的标志,几种肌萎缩侧索硬化症的遗传原因变异与神经元能量代谢失调有关。在多发性硬化症中,能够重新髓鞘损伤的轴突的细胞被证明处于新陈代谢压力下,使它们无法经历修复受损髓鞘的耗能过程。
临床前研究表明,CNM-Au8®纳米晶体跨越血脑屏障,潜在地保护多种中枢神经系统细胞类型。在多项临床前研究中,我们已经证明这些中枢神经系统细胞可能在几个方面从催化活性纳米晶体中受益:OL获得足以驱动髓鞘产生的能量提升;多巴胺能神经元、海马神经元和皮质神经元改善能量生产和利用,足以提高生存和维持功能,以应对多种疾病相关应激源。来自肌萎缩侧索硬化症患者的人星形胶质细胞在共培养时具有杀死运动神经元的能力,当共培养的运动神经元被CNM-Au8处理时,这些运动神经元的毒性显著降低。®。就其本质而言,具有催化能力的多面、表面清洁的纳米晶体避开了过去困扰中枢神经系统药物开发领域的许多挑战。重要的是,它们的催化机制产生了几种有用的能量代谢物,同时减少了有害物质的存在。这些机制非常适合于解决神经退行性疾病在多个层面和多种中枢神经系统细胞类型中发生的复杂故障。
10
目录表
CSN的创新®治疗是,我们相信我们有能力应对由多种中枢神经系统疾病带来的最重大挑战。与“一药一靶”的模式不同,表面清洁的多面体纳米晶通过多种机制增强细胞的能量状态,同时独立地减少氧化应激,刺激中枢神经系统细胞内的蛋白质稳态。每个纳米晶体能够每秒交换数千个电子,潜在地解决了疾病中枢神经系统细胞的缺陷,而不会进一步耗尽其内部能量储存的细胞。我们相信我们的数据表明CSN®因此,治疗学支持细胞并补充细胞的能量缺乏。换句话说,我们的研究表明,CSN®治疗公司为中枢神经系统的细胞提供正常运作所需的基本能量块。
CSN的市场潜力®神经退行性疾病的治疗学
尽管治疗需求迫切,神经退行性疾病治疗有巨大的市场机会,但有效的治疗方法有限。目前FDA批准的ALS治疗药物对疾病的修改作用非常有限。我们估计到2029年,全球肌萎缩侧索硬化症的销售额将超过10亿美元。此外,截至2016年,全球约有220万多发性硬化症患者,我们估计市场规模约为230亿美元。目前,没有现有的治疗方法可以促进非活动性进展性多发性硬化症患者的髓鞘再生,也没有被证明可以改善非活动性进展性多发性硬化症患者的功能。非活动性进行性多发性硬化症患者约占所有多发性硬化症患者的三分之一,他们遭受进行性功能丧失、生活质量严重下降和寿命缩短的困扰。最后,目前还没有针对帕金森病的疾病修正疗法。所有现有的帕金森病治疗方法都仅限于改善症状,没有一种方法被证明可以防止或减缓多巴胺能神经元的丢失。截至2016年,全球约有610万PD患者,我们估计到2026年,这一市场将达到约60亿美元。如果目前正在进行的临床试验提供了重新髓鞘形成的证据或证明神经功能得到改善,CSN®治疗公司在治疗肌萎缩侧索硬化症、多发性硬化症或帕金森病方面将有巨大的商业销售潜力。
全世界还没有一种批准的多发性硬化症药物被证明对髓鞘再生和神经保护有效果。CNM-AU8®其针对中枢神经系统疾病的髓鞘再生和神经保护的作用机制,加上市场对安全有效治疗的迫切需求,为我们提供了我们认为具有巨大市场潜力的先发优势,用于治疗中枢神经系统疾病。我们最先进的CSN®候选治疗药物CNM-Au8®,已经开发出来,以解决在治疗中枢神经系统疾病,肌萎缩侧索硬化症,多发性硬化症和帕金森病中未得到满足的重大医疗需求。肌萎缩侧索硬化症、多发性肌萎缩侧索硬化症和帕金森氏症都严重影响了患有这些疾病的人的健康和寿命,导致对疾病修正治疗的巨大需求。
CNM-AU8®肌萎缩侧索硬化症、多发性硬化和帕金森病能量代谢的恢复
概述
CNM-AU8®是一种浓缩的、口服的纯金纳米晶体悬浮液,在用碳酸氢钠缓冲的制药级水中。单次60毫升的剂量在30毫克时含有超过100万亿个纳米晶体。CNM-AU8的中位FERET直径®纳米晶体约为13纳米,每个纳米晶体平均由大约70,000个金原子组成。CNM-AU8®的催化机制,直接给予和/或接受电子,提高细胞的能量反应速度,而不需要细胞的相关能量投资,从而增加细胞的净能量能力。CNM-AU8®治疗结果是改善了中枢神经系统细胞内的能量代谢。通过这一机制,CNM-Au8®可能保护包括OL和/或神经元在内的多种神经元和胶质细胞免受氧化、炎症、低氧和兴奋性毒性损伤,潜在地导致增强髓鞘形成和改善神经元存活,同时保护轴突和突触的完整性。
标准ICH M3(R2)毒理学研究在CNM-AU8上进行®在四种动物中,没有产生毒性发现,导致NOAEL发现,直到最大可行剂量。口服单次和多次递增剂量CNM-Au8的首例人体1期临床试验®然后在86名健康的人类志愿者中进行了研究。所有剂量(不超过90毫克/天)的CNM-Au8®都被很好地容忍了。安全性作为第二阶段救援-肌萎缩侧索硬化症试验的一部分进行了调查,没有显著的不良结果。治疗中出现的不良事件主要被评为轻度至中度严重和一过性。未评估与主动药物治疗有关的严重不良事件(“SAE”)。
CNM-AU8®已获得监管部门批准,可以进行旨在评估CNM-Au8安全性和有效性的第二阶段临床试验®对于大脑代谢物的靶参与以及功能和生理的改善,表明重新髓鞘形成和神经保护。CNM-Au8每次临床试验详情®以下是《CNM-AU8临床发展计划》中给出的®作为治疗疾病的药物“一节为每个适应症。
11
目录表
行动机制
CNM-AU8®通过催化作用改善能量,减少有害的ROS,并通过神经系统细胞中的热休克蛋白-1途径诱导蛋白质动态平衡。这些独特的作用机制导致了一系列有益的影响,如图3所示。
图3.催化生物学作用机制
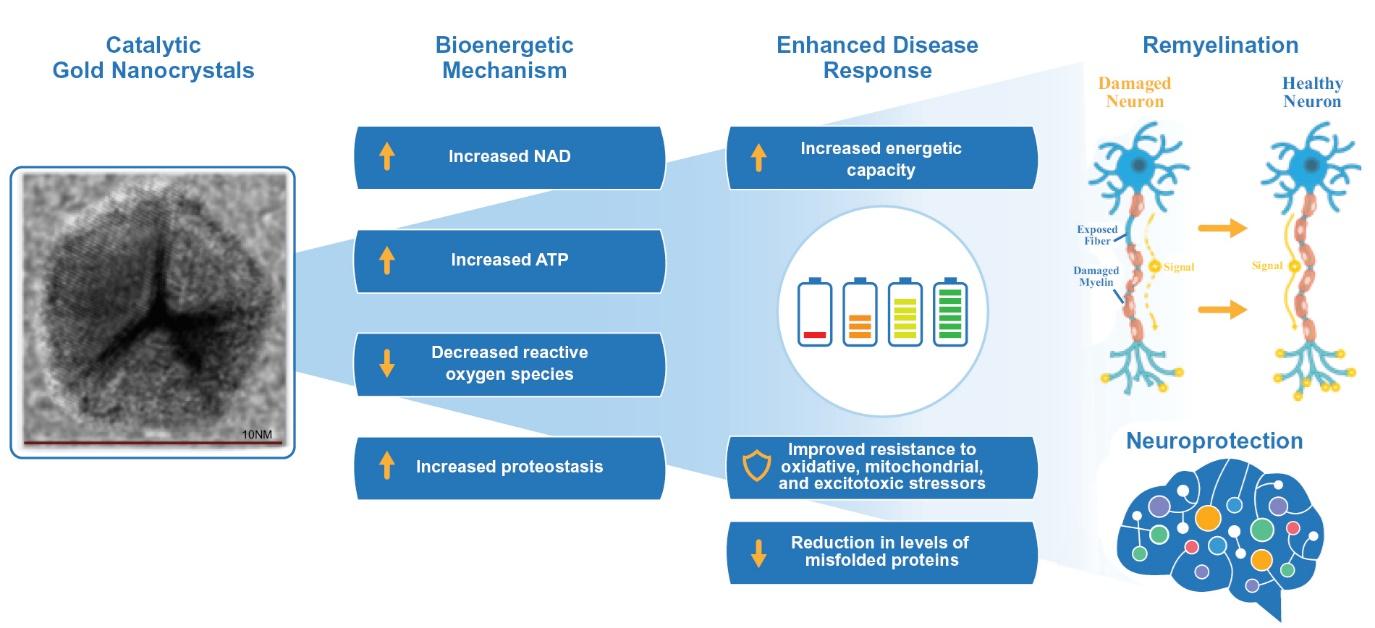
图3.CNM-AU8®介导的催化提高了细胞的能量能力,降低了氧化应激,导致NAD和ATP的产生增加,并通过热休克因子1途径增加了蛋白抑制活性。总而言之,这些活动导致神经元、OL和星形胶质细胞的一连串增强的疾病反应,这些细胞类型最容易受到能量缺乏的影响。CNM-AU8®从而在ALS、MS和PD等神经退行性疾病中介导重新髓鞘形成和神经保护作用。
CNM-Au8催化的关键代谢产物之一®是烟酰胺腺嘌呤二核苷酸(NAD)的氧化形式+”) (Fig. 4). NAD+及其还原的伴侣NADH对于在活细胞中驱动细胞能量ATP生成反应至关重要(图4A)。脑成像研究表明,NAD的比例+TO NADH通常随着年龄的增长而降低。降低NAD+血液和大脑中的水平都与精神分裂症、多发性硬化症、帕金森病和亨廷顿病等神经系统疾病有关。助推NAD+神经退行性疾病临床前模型的活性一直显示出有益的抗衰老和神经保护作用。CNM-AU8®对NADH直接氧化成NAD的催化活性比我们测试过的任何其他商业可获得的金纳米粒子都要高(图4C,D)。我们已经证明用CNM-Au8处理培养的神经系统细胞®增加他们的NAD蜂窝池+和ATP,证明CNM-AU8®增强中枢神经系统细胞的能量能力(图4E,F)。这种对ATP(图4F)的优化使OL能够增加髓鞘的产生,并帮助许多其他类型的中枢神经系统细胞抵御环境和疾病相关的应激因素,否则这些应激因素将导致它们死亡。
图4所示的统计分析是通过单因素方差分析(“ANOVA”)进行的,以比较每个处理组的平均值与车辆对照组的平均值(针对多次比较进行了校正)。P值(图4e,F)表示在一般假设组之间没有差异(零假设)的情况下,获得至少与分析中观察到的结果一样极端的测试结果的概率。P值越低(小),观测的统计意义越大,零假设为真的可能性就越小。科学界和监管机构,如FDA,通常认为p值在0.05或更小的情况下,在独立临床试验中复制时是显著的。持续的统计学意义显著的临床前结果,如本文所述,用于支持调查性新药应用(“NDA”),以调查研究产品的临床效果。
许多神经退行性疾病共有的一个重要应激源是当神经元的能量需求开始超过其产生足够的ATP以执行正常功能的能力时,有害的ROS在神经元内积累。由ROS积累引起的慢性氧化应激可以压倒通常严格调节ROS水平的线粒体系统。过量的ROS积累破坏细胞膜,导致钙离子失衡,最终导致细胞死亡。
12
目录表
图4.NAD氧化和生物效应对ATP和NAD的影响+
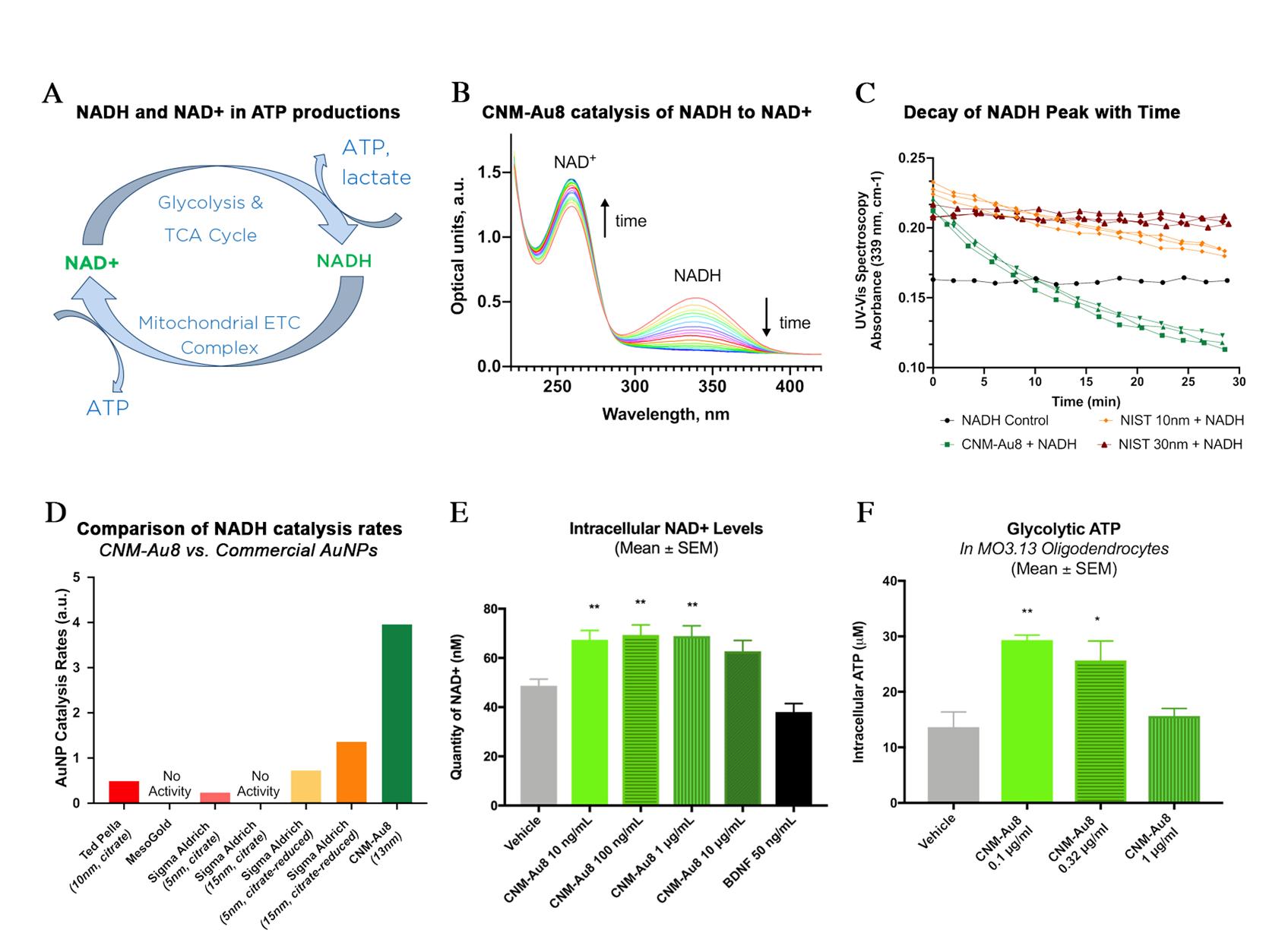
图4.CNM-Au8的高能催化作用®。NAD-NADH还原-氧化偶联在ATP生成反应、糖酵解和线粒体电子传递链氧化磷酸化中都起着关键作用。用紫外-可见光谱表征了CNM-Au8的催化活性®随着时间的推移。随着反应的进行,nadh被消耗,如在340 nm处的nadh吸收峰的减少所证明的那样,而nad+如NAD的相应增加所示+在260 nm处有吸收峰。C,CNM-AU8的NADH吸收峰衰减速率较大®比柠檬酸还原的金,直径10 nm(橙色)和30 nm(红色)的纳米颗粒(从美国国家标准与技术研究所购买)更好,表明CNM-Au8®在相同的反应条件下,其催化速率至少是美国国家标准与技术研究所比较器的三倍。D,CNM-AU8的催化速率®明显优于几种商业上可获得的金纳米粒子。Sigma Aldrich提供不含反应物的“柠檬酸还原”金纳米颗粒,其中使用额外的程序来清洁反应物的表面。“柠檬酸盐”金纳米粒子悬浮液中可能仍有残留的反应物。E,蜂窝NAD+对CNM-AU8的反应水平增加®原代啮齿动物神经元-神经胶质共培养的治疗。原代培养的啮齿动物OL细胞对CNM-Au8的反应使细胞ATP水平升高®治疗。面板E-F,显示的数量为组平均值+/−扫描电子显微镜。使用经多次比较校正的单因素方差分析来比较每个处理组的平均值与赋形剂对照组的平均值;用星号表示在统计学上显著差异的处理组和赋形剂:*p
除了促进NAD+神经系统细胞内浓度CNM-AU8®通过直接催化ROS的还原,直接作用于ROS的还原(图5)。CNM-AU8®具有抗氧化催化活性,并已被证明以类似超氧化物歧化酶的方式直接还原氧自由基,以及转化过氧化氢(H2O2“)以类似过氧化氢酶的方式转化为水和氧气(图5A,B)。CNM-Au8的抗氧化活性®已经在原代小鼠OL培养中得到证实,在这些培养中,ROS的基础水平随着处理而降低(图5C)。在PD中体外培养模型中,用神经毒素1-甲基-4-苯基吡啶(MPP)处理原代鼠多巴胺能细胞产生的ROS降低对CNM-Au8的反应®在MPP存在的情况下进行治疗(图5D)。图5所示的统计分析由单因素方差分析进行,以比较每个处理组的平均值与车辆控制的平均值(针对多次比较进行了校正)。P值(图5C,D)表示获得
13
目录表
测试结果至少与在化验中观察到的结果一样极端,在一般假设组之间没有差异的情况下(零假设)。
之前针对神经退行性疾病的药物开发工作包括许多抗氧化剂,但所有这些都没有显示出改善疾病的效果。我们相信CNM-AU8®保持在与标准抗氧化剂不同的类别,因为据我们所知,没有其他抗氧化剂表现出催化能力增加能量代谢产物NAD+和ATP,同时独立催化降低ROS。
图5.活性氧物种的减少
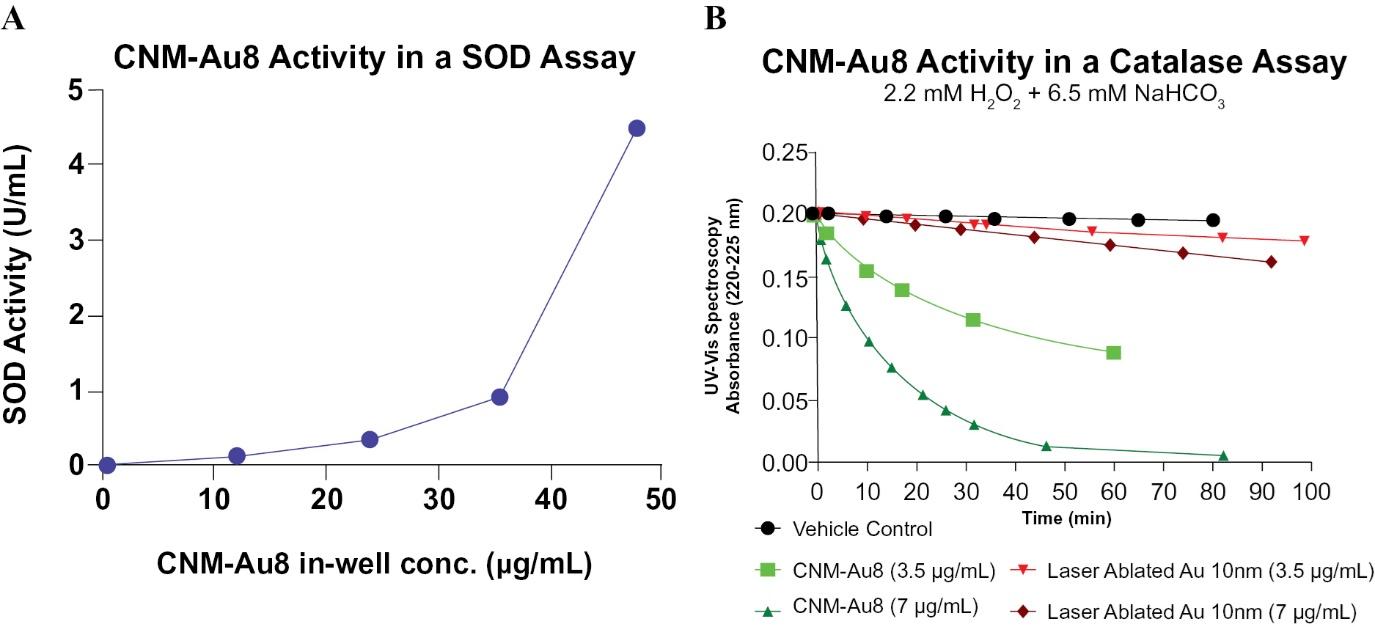

图5.CNM-AU8®是一种催化活性抗氧化剂。CNM-Au8细胞的A,SOD样活性®用超氧化物歧化酶比色试剂盒(开曼化学)测定超氧阴离子自由基。B,H的吸收峰衰减2O2就像H的置换一样2O2在CNM-AU8现场进行®(绿色)或直径相近的对比AUNPs(红色)或无金色(黑色)。C、D、神经毒素(MPP+CNM-Au8对原代E15大鼠共培养的线粒体应激和多巴胺能神经元死亡的保护作用®(绿色),由+细胞数量(未显示),ROS减少,通过用CELLROX绿色信号(细胞液氧化环境的标志)荧光的多巴胺(TH)细胞的分数来衡量,以及线粒体膜电位的增加(MitoTracker Red CMXRos)(D)。面板C-D,数量显示为组平均值+/−扫描电子显微镜。采用多次比较校正的单因素方差分析方法比较各治疗组MPP与CNM-AU8的均数®单用Mpp(4μM)治疗组的平均值;各治疗组间差异有统计学意义®治疗组单用MPP治疗
14
目录表
用星号表示:*p
以前在神经退行性疾病领域的药物开发努力将错误折叠的蛋白质聚集体作为疾病的有毒驱动因素;例如,帕金森病中的α-突触核蛋白,阿尔茨海默病中的淀粉样β蛋白,以及肌萎缩侧索硬化症中的TAR DNA结合蛋白43(TDP-43)。CNM-Au8作用机制的重要组成部分®在PD和ALS的细胞模型中,它分别具有剂量依赖性地减少聚集的α-突触核蛋白和TDP-43的能力(图6)。我们认为,这种活性至少部分归因于热休克因子1途径的20个基因转录的强劲诱导,我们在OLS中观察到对CNM-Au8的反应®治疗(Robinson等人)在Sci Rep 10,1936(2020)的动物模型中,表面清洁的多面纳米晶金的纳米催化活性增强了髓鞘再生(Sci Rep 10,1936(2020)),这是由于对NAD上调的间接细胞反应,已被证明激活自噬和蛋白抑制反应。
综上所述,CNM-Au8®通过其催化活性展示了一种新的作用机制,包括:
图6.错误折叠的蛋白质聚集物减少
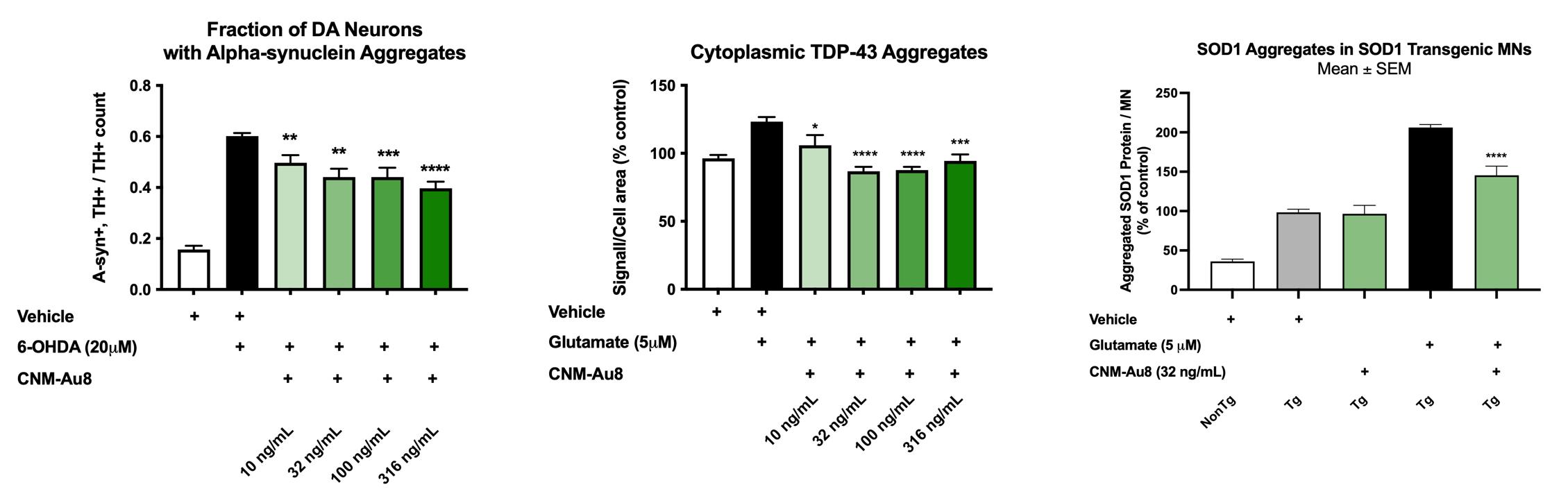
图6显示了在帕金森病(图6A)、散发性和家族性肌萎缩侧索硬化症(图6B)和家族性SOD1ALS(图6C)中典型的多巴胺能和脊髓运动神经元中三种不同类型的蛋白质聚集体的剂量依赖性减少。在每一种检测中,CNM-AU8®处理都伴随着神经元存活和轴突网络保存的剂量依赖性增加。这些结果表明,在代表不同神经退行性疾病的体外模型中,CNM-AU8®减少了有毒蛋白质聚集体的数量。组指标绘的+/-扫描电子显微镜。*第
CNM-AU8的安全性和容错性®
我们完成了CNM-Au8的第一阶段人体研究®2016年,证明它对进一步的临床开发是安全的,并评估不同剂量浓度下的药代动力学曲线。
试验设计。CNM-Au8的一期首例人体研究®是一项随机、安慰剂对照、双盲、逐步递增的单剂量和多剂量研究,以评估CNM-Au8的安全性、耐受性和药代动力学®在健康的男性和女性志愿者中。这项研究分为两个阶段:单次递增剂量(“SAD”)阶段和多次递增剂量(“MAD”)阶段。首先进行SAD阶段,然后是研究的MAD阶段。
15
目录表
安全。安全评估显示没有重大发现。根据报告的治疗紧急不良事件(“TEAE”)的频率,本研究中使用的所有剂量都被确定为耐受性良好。服用安慰剂的患者TEAE发生率(86%)高于服用CNM-AU8的患者®SAD和MAD时相加给药组(75%)。没有受试者因TEAES而中断研究,任何治疗组都没有SAEs的报道。最常见的TEAE几乎完全是1级(轻度)严重和短暂的。最常见的TEAE包括头痛、嗜睡、疲劳、腹痛、腹泻、恶心和头晕。
药物动力学。MAD时相药动学分析显示,21天结束时,15、30、60、90 mg组的血金最大浓度分别为1.53、1.98、2.35、3.33 ng/mL。药代动力学分析表明,CNM-Au8®半衰期为14-21天。研究结束时,人类的药物暴露水平等于或超过了在动物模型中证明了神经保护和髓鞘再生功效的同等暴露水平。
结论。首次人体安全性结果显示,服用CNM-Au8后没有安全信号®人类的临床使用剂量和药物暴露水平等于或超过在动物模型中展示神经保护和髓鞘再生功效的同等暴露水平。
在成功完成CNM-Au8的第一阶段研究后®,我们进行了CNM-AU8®进入多个第二阶段临床试验,旨在测试CNM-Au8的疗效®在特定的疾病指征中。基于我们临床前髓鞘再生和神经保护数据的安全性和强度,我们已经启动了一项2/3期注册临床试验,Healey ALS平台试验,目前正在进行中,以确定CNM-Au8的安全性和有效性®肌萎缩侧索硬化症患者。我们完成了RESPECT-ALS,这是一项第二阶段的概念验证临床试验,以评估CNM-Au8的有效性、安全性、药代动力学和药效学®在早期有症状的ALS患者中。我们还完成了Repair-PD和Repair-MS的第一个剂量队列,两个开放标记的研究人员盲目第二阶段临床试验,证明了CNM-Au8的靶向参与®对大脑能量代谢物的影响。Repair-MS将继续启动第二个剂量队列。此外,我们正在进行一项名为Visionary-MS的第二阶段临床试验,用于治疗慢性视神经病变的视觉通路缺陷,以评估CNM-Au8的有效性、安全性、耐受性和药代动力学®对于稳定复发的MS患者的再髓鞘形成,我们支持为ALS患者提供两个EAP。最初的EAP是与马萨诸塞州综合医院的希利ALS中心合作于2019年9月推出的。第二个EAP与Healey ALS平台试验一起在三个参与的临床站点实施。在我们正在进行的2期和2/3期临床试验和我们的EAP中,我们正在积累越来越多的人类安全暴露。到目前为止,在盲法的基础上,我们还没有看到令人担忧或限制剂量的安全信号,两个独立的数据安全监测委员会监督我们的随机双盲安慰剂对照试验,建议在对安全数据进行无盲评估后继续进行试验。
肌萎缩侧索硬化症
肌萎缩侧索硬化市场机遇
肌萎缩侧索硬化症是一种成人起病的、进行性和致命性的神经肌肉系统退行性疾病,导致肌肉无力和瘫痪,在最初诊断后三到五年内导致死亡。在美国,ALS影响着超过15,000名患者,是最常见的成人起病的进行性运动神经元病。肌萎缩侧索硬化症涉及脊髓和大脑中负责控制随意肌肉运动的运动神经元的进行性退化。在肌萎缩侧索硬化症中,运动神经元的这种进行性丧失会导致肌肉无力、肌肉质量丧失,以及无法控制运动。尽管FDA批准了两种治疗肌萎缩侧索硬化症的药物,利鲁唑和依达拉奉,但这两种药物都不能实质性地阻止或逆转这种疾病的进展性质。大多数肌萎缩侧索硬化症患者的发病年龄在40至60岁之间,男性更为常见。65岁以后,男女发病率差异缩小。
肌萎缩侧索硬化症的治疗现状及局限性
目前的ALS治疗方法主要是姑息性的,目的只是暂时缓解症状,而不是解决潜在的疾病进展。例如,一种治疗呼吸功能丧失的方法是无创呼吸机,这是ALS相关死亡的最常见原因。尽管迫切需要一种有效的疾病修正疗法,制药业也做出了重大研究努力来满足这一需求,但临床成功有限,迄今为止还没有批准根治性疗法。有两种FDA批准的治疗ALS的药物:抗谷氨酸能药物利鲁唑和自由基清除剂依达拉奉。然而,这两种治疗方法都被认为具有有限的疾病修改效果,因为利鲁唑平均只将参与者的寿命延长两到三个月,而依达拉奉则减缓ALSFRS-R的下降
16
目录表
评分,一种临床上衡量功能下降的指标,只在一小部分处于疾病早期的参与者中进行。此外,FDA已经批准了Amylyx制药公司提交的与其药物AMX0035有关的NDA申请的优先审查,这是基于一项第二阶段临床试验,根据ALSFRS-R评分,AMX0035在6个月的随机阶段结束时,临床下降率在统计上显著减少。欧洲药品管理局(“EMA”)目前也在审查AMX0035的商业化潜力。显然,开发安全有效的ALS疾病修改疗法是一种迫切的、尚未得到满足的需求。
CNM-AU8的潜在优势®对于ALS
我们相信CNM-AU8®有可能成为治疗肌萎缩侧索硬化症的一流纳米治疗药物。在ALS的人诱导多能干细胞(IPSC)模型中,CNM-Au8®与利鲁唑相比,显示出明显更好的人类运动神经元保护。此外,CNM-Au8的口服给药®对于ALS模型小鼠,这些动物的平均寿命延长了三倍以上,这归因于文献中报道的依达拉奉或利鲁唑治疗。而依达拉奉的作用机制与CNM-Au8有一个相似的成分®,即减少氧化应激,我们认为活性的重要区别在于CNM-Au8®证明了其具有增强患病神经元的能量活性以及显著降低氧化应激的潜力。此外,我们认为,包括肌萎缩侧索硬化症在内的许多神经退行性疾病的复杂性要求一种具有多种活性的治疗药物,这种药物可以增强多种中枢神经系统细胞类型的能量分布;为此,CNM-Au8®可能是唯一适合于应对这种复杂和破坏性疾病带来的治疗挑战的药物。
肌萎缩侧索硬化症非临床药理神经保护研究综述
运动神经元在肌萎缩侧索硬化症的过程中逐渐退化。CNM-Au8对运动神经元的神经保护作用®, 体外培养首先使用神经保护分析。用谷氨酸刺激大鼠运动神经元,或用对运动神经元有毒性的淀粉样β1-42肽(“A-β”)刺激大鼠运动神经元。在阿尔茨海默病中,A-β聚集体参与淀粉样斑块的形成。CNM-AU8®用谷氨酸或A-β刺激运动神经元的治疗可增加存活运动神经元的数量,并以剂量依赖的方式保存轴突网络。
显示神经毒性的错误折叠蛋白的聚集是包括ALS在内的许多神经退行性疾病的标志。在90%以上的ALS病例中,运动神经元中错误定位的胞浆TDP-43的积聚与ALS有关,并且TDP-43聚集体被证明扰乱了运动神经元的细胞功能。在神经元-神经胶质细胞共培养实验中,将谷氨酸或A-β应用于大鼠运动神经元,会导致TDP-43聚集在运动神经元的细胞质中。CNM-Au8治疗谷氨酸或A-β刺激的运动神经元®显著减少TDP-43聚集体的积累,并呈剂量依赖关系。
除了动物模型,IPSCs已经成为一种使用人类来源细胞进行神经退行性疾病建模的新技术。IPSCs可以从人的皮肤或血液样本中产生,然后在体外分化为星形胶质细胞和运动神经元。使用这项技术,ALS患者来源的星形胶质细胞被证明对正常健康的人类运动神经元具有毒性。CNM-AU8简介®对于这些中毒的ALS患者,星形胶质细胞-运动神经元共培养显著地、剂量依赖地挽救了人类运动神经元,并保存了运动神经元轴突网络。总之,这些结果表明,CNM-AU8®在几种不同的模型中发挥运动神经元保护作用,包括对兴奋性毒性应激、A-β毒性和毒性星形胶质细胞的反应。
CNM-AU8的疗效观察®在一个体内ALS动物模型,分别用转基因(SOD)进行了两项研究1G93A)小鼠模型品系,模拟人类SOD1家族形式的ALS。在一项使用快速进展的超氧化物歧化酶的研究中1G93A动物,CNM-AU8®经处理的动物表现出脑干萎缩和脑干空泡化的显着减少,通常在未处理的超氧化物歧化酶中可见1G93A老鼠。在使用进展较慢的超氧化物歧化酶的研究中1G93A动物,CNM-AU8®经处理的动物在许多行为和功能测试中显示出显著的治疗效果,包括总体临床评分、重量保持、静态杆状定位时间和平均车轮运行速度。CNM-AU8细胞的中位生存期®用药的动物比用药的对照组多了23天(大约是动物预期寿命的20%)。
CNM-Au8的临床研究进展®作为治疗ALS的疾病修饰药
ALS的孤儿药物状况
FDA授予CNM-Au8孤儿药物称号®2019年5月用于治疗肌萎缩侧索硬化。在FDA指定孤儿药物后,赞助商可能有资格获得FDA管理的七年孤儿药物独家经营权、研发费用的部分税收抵免、潜在的研发拨款、免除FDA的费用以及FDA的协议援助。
17
目录表
救援-肌萎缩侧索硬化症
这是一项关于CNM-Au8的有效性、安全性、药代动力学和药效学的2期随机、双盲、安慰剂对照试验®在早期的ALS患者中。这项试验在45名登记参与者中进行了36周。该试验以1:1的比例随机选择接受CNM-Au8治疗的患者®每天服用30毫克或在标准护理(利鲁唑)的基础上服用匹配的安慰剂。试验的主要终点是运动单位编号指数总和从基线到第36周的百分比变化。次要终点是用力肺活量(FVC)的变化和MUNIX值到36周的绝对变化。探索性终点包括ALS疾病进展的多种临床相关测量,ALS功能评定量表修订版(ALSFRS-R)6分下降,ALS特定生活质量(ALSSQOL-SF),以及额外的临床和神经生理学终点。2021年11月2日,我们公布了ASPLE-ALS试验的一线结果。虽然试验在36周时没有达到munix和fvc的主要或次要终点,但在第12周观察到munix终点的疗效信号(图10A,p=0.057)。此外,在肢体起病ALS的子集中的预定分析中,CNM-AU8®MUNIX12周时有显著疗效(p=0.0385),36周时有改善趋势(p=0.0741)(图7b)。肢体起病的肌萎缩侧索硬化症约占肌萎缩侧索硬化症患者的70%。MUnix是一种神经生理学生物标记物,它估计服务于选定肌肉的功能较低的运动神经元的数量。在试验36周期间,临床相关的探查终点显示CNM-AU8有显著的益处®治疗包括,减缓肌萎缩侧索硬化症的疾病进展(图7E,p=0.0125),降低ALSFRS-R下降6点的参与者的比例(图7D,p=0.035),以及提高ALSSQOL-SF的生活质量(图7C,p=0.018)。汇总数据如下图所示。此外,CNM-AU8®接受治疗的参与者在呼吸功能和运动功能的各项指标上始终显示出方向性的益处(即较少的下降),尽管不是很明显。救援-ALS试验的长期延长显示,与使用经过验证的ENCALS预测模型对整个试验人群的预期生存进行比较时,有证据表明潜在的生存益处(图7F;Westeneng等人)。柳叶刀神经。2018年5月;17(5):423-433)。CNM-AU8®通过36周的每日口服剂量被发现耐受性良好。没有与CNM-AU8有关的SAE报告®治疗。治疗后出现的不良事件的严重程度主要为轻度至中度。最常报告的与CNM-AU8相关的不良事件®治疗包括吸入性肺炎3例,一过性胃肠道不适2例。总而言之,我们认为这些数据表明,有利于CNM-AU8的风险-收益比是可以接受的®并显示出患有肌萎缩侧索硬化症的患者病情进展缓慢的迹象。
18
目录表
图7.救援结果-ALS
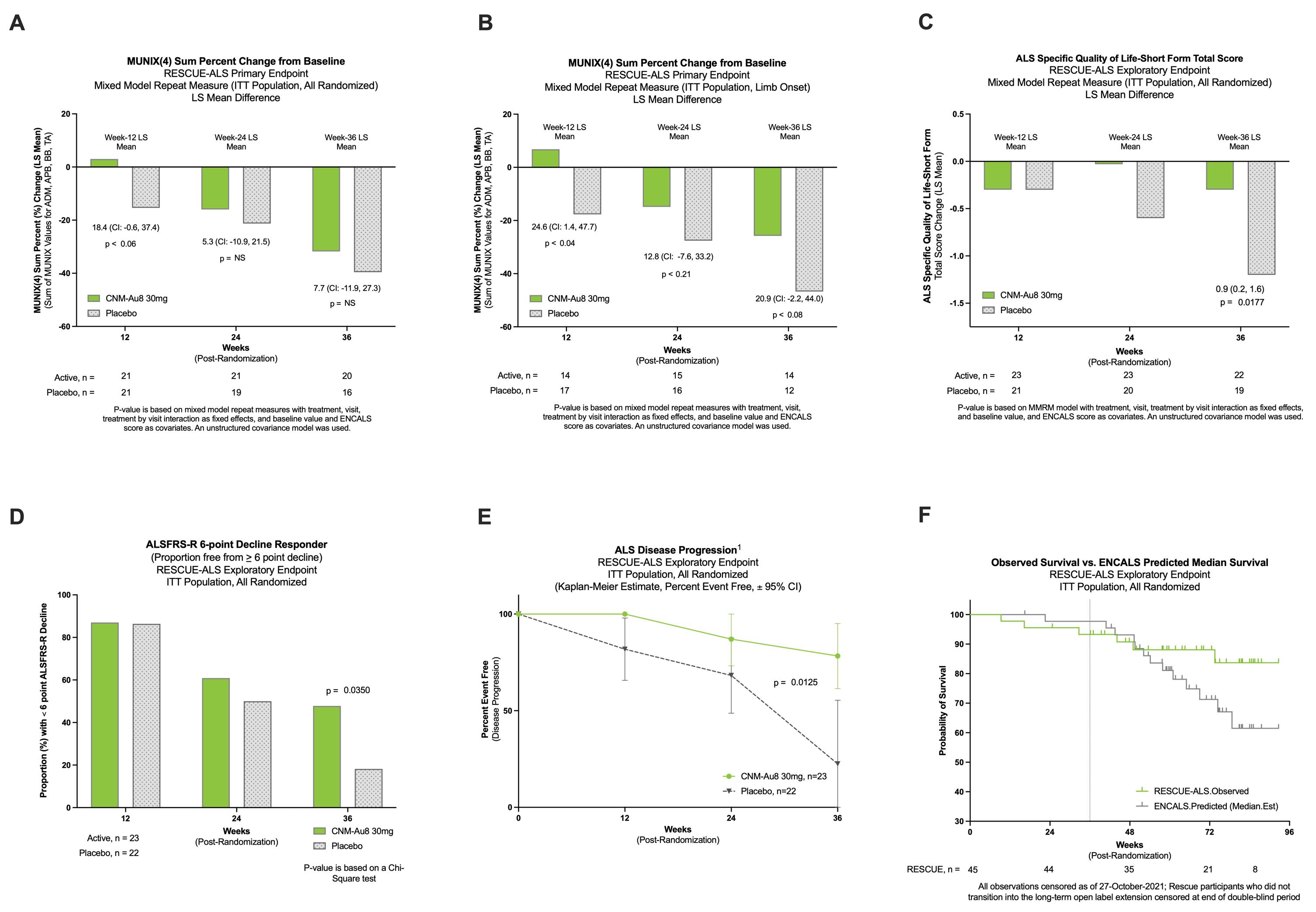
救援-肌萎缩侧索硬化症由FightMND提供了大量资金,为我们提供了140万澳元的赠款。一般来说,Fight MND的赠款条款包括在CNM-AU8商业化的情况下偿还收到的资金®在澳大利亚,用于治疗肌萎缩侧索硬化症的未来净销售额最高可达原始赠款金额140万澳元的个位数中位数倍数。根据与患者登记目标相关的业绩里程碑的实现情况,分配资金。临床试验活动的所有知识产权均归我们所有。
Healey ALS平台试验
2019年9月,马萨诸塞州综合医院的希利ALS中心选择了CNM-AU8®作为首批纳入ALS治疗平台试验的三种药物之一。Healey ALS平台试验将测试前景看好的实验性疗法,其设计允许同时测试多种药物,以便快速识别和加快ALS新疗法的开发,同时提供缩短试验时间、降低成本和增加患者参与度的优势。该试验包括来自慈善捐赠者和希利中心的大量财政支持,并提供来自东北肌萎缩侧索硬化症财团的54个美国ALS临床试验点的专家。
该试验是一项2/3期、多中心、双盲、安慰剂对照的注册临床试验,旨在评估CNM-Au8的安全性、有效性、药代动力学和药效学®治疗肌萎缩侧索硬化症。参与者在积极治疗和安慰剂之间随机分配3:1,其中积极治疗平均分配给低剂量(30 Mg)的CNM-Au8®和大剂量(60 Mg)CNM-Au8®。主要终点是从基线到第24周的ALSFRS-R评分的变化率,计划的次要终点是缓慢肺活量和手持测力测量的变化。研究终点包括基于存活率和ALSFRS-R评分从基线到第24周的变化的联合排名评分、嗓音病理测量以及基于生物流体的药效学和代谢标记物。
19
目录表
我们直接向Healey中心支付这项试验的临床实施费用;不会有额外的许可费或里程碑要求。Healey ALS平台试验的IND由马萨诸塞州综合医院举办。我们拥有所有CNM-AU8®数据,而安慰剂数据将在平台试验中的不同治疗方案中共享。注册于2021年11月完成,CNM-Au8的主要结果®预计将于2022年下半年完成。
扩展访问计划
基于对CNM-Au8潜力的兴趣®为了延缓ALS患者的疾病进展,马萨诸塞州综合医院的临床专家要求使用CNM-Au8®在两个EAP中。EAP是一种途径,用于患有立即危及生命的情况或严重疾病或状况的患者,在没有类似或令人满意的替代治疗方案时,获得研究医疗产品(药物、生物或医疗设备)在临床试验之外进行治疗。在美国,要符合EAP的资格,应满足以下条件:(I)患者患有严重疾病或状况,或其生命立即受到疾病或状况的威胁;(Ii)没有类似或令人满意的替代疗法来诊断、监测或治疗疾病或状况;(Iii)患者不可能参加临床试验;(Iv)潜在的患者利益证明治疗的潜在风险是合理的;以及(V)提供研究用医疗产品不会干扰可能支持医疗产品开发或治疗适应症营销批准的研究试验。EAP是根据向FDA提交的研究协议进行的,并于2019年9月和2021年9月开始。EAP将收集ALS患者的安全性和药代动力学数据,因为标准的纳入和排除标准,ALS患者本来没有资格进行临床试验。
截至2022年2月18日,已有56名参与者参加了2019年9月开始的EAP,暴露时间长达125周。目前,根据该议定书,有33名参与者是活跃的。截至2022年2月18日,已有14名参与者参加了2021年9月开始的EAP,暴露时间长达约20周。目前,根据该协议,所有14名参与者都是活跃的。EAP为FDA审查提供了额外的安全数据,并将被视为CNM-AU8安全数据包的一部分®,并可能提供关于NDA提交的支持性长期安全数据,如果Healey ALS平台试验产生统计上显著的治疗益处。
多发性硬化
微软的市场机会
多发性硬化症是一种中枢神经系统的炎症性和退行性疾病,涉及免疫介导的大脑、视神经和脊髓的破坏。多发性硬化症是由自身免疫攻击髓鞘造成的,髓鞘是包裹神经元轴突的保护性覆盖物。当髓鞘被自体炎症免疫攻击破坏时,神经元会受到损害,最终可能会死亡,导致运动症状、认知障碍、视觉障碍和其他神经损伤。
多发性硬化症通常始于20岁至40岁之间,是年轻人非创伤性残疾的主要原因。女性受到影响的频率大约是男性的三倍,除了不太常见的原发-进行性疾病的个人,那里没有性别优势。MS是最常见的炎症性脱髓鞘疾病,其患病率差异很大,从北美和欧洲的高发病率到东亚和撒哈拉以南非洲的低发病率。美国国家多发性硬化症协会最近领导的一项研究估计,美国 大约有800,000人患有多发性硬化症。尽管目前有可用的疾病修饰疗法,但大约26%的多发性硬化症患者已经发展成一种非活跃的进行性疾病,针对这种疾病,获得批准的有效治疗方法有限,导致严重的生活质量损失。
多发性硬化症的诊断主要是临床诊断,辅以放射学检查(例如磁共振成像)。其他诊断方法包括血液测试、诱发电位测试、腰椎穿刺术和光学相干断层扫描,这是一项检查MS对视网膜神经细胞和轴突健康影响的新技术。利用磁共振成像,多发性硬化症临床隔离综合征的新诊断分类已被纳入更新的2017年国际(麦克唐纳)标准。诊断技术的不断改进可能会增加诊断为多发性硬化症的患者数量。
多发性硬化症目前的治疗方法和局限性
目前所有治疗多发性硬化症的药物要么治疗多发性硬化症引起的症状,要么减轻自身免疫介导的炎症程度。这些药物通常被称为疾病修正疗法(“DMT”)。目前批准的几乎所有DMT都被批准用于治疗复发形式的多发性硬化症(“RMS”)。它们通常通过免疫抑制或免疫调节发挥作用,从而将自身免疫相关的对髓鞘的攻击降至最低。免疫调节型DMT可降低炎症性发作的风险,称为“复发”,并可减缓发作患者(即“活跃”患者)的残疾发展。因此,DMT可能会降低RMS转化为继发性进展性MS的风险。较新的DMT已被证明显著减少了自身免疫介导的攻击,并延缓了活动期患者的疾病进展。然而,没有可用的药物可以减少正在进行的功能丧失(即疾病进展)。
20
目录表
非活动期(不再发作的)多发性硬化症患者。没有一种被批准的DMT能在临床上改善MS病变中受损和脱髓鞘的轴突的重新髓鞘形成。目前可用于治疗多发性硬化症的DMT包括:注射用药、Avonex(干扰素-β-1a)、倍他龙(干扰素-β-1b)、Extavia(干扰素-β-1b)、Copaxone(醋酸格列酮)、Pregridy(聚乙二醇乙型干扰素-1a)、Rebif(干扰素-1a)、非专利等效物(醋酸谷氨酰胺注射剂、格拉托巴(醋酸格拉替拉默);口服药物、Aubagio(特氟米特)、Gilenya(Fingolimod)、Tecfidera(富马酸二甲酯)、Mavenclad(Cladriine)、Mayzent(Siponimod);输液用药、Lemtrada(Alemtuzumab)、Novantrone(Mitoxantrone)、Ocrevus(Ocrelizumab)和Tysabri(Natalizumab)。多发性硬化症的治疗进展与新的B细胞去除疗法,包括奥曲珠单抗,已在很大程度上改善了炎症性疾病的活动,其衡量标准是复发风险的降低和MRI检测到的新的Gd增强性(炎症)损害的发生。然而,尽管这些药物稳定了活动期MS患者的疾病活动,但总体功能并未显示出显著改善。重要的是,对于迄今已获批准的DMT来说,疗效和安全性通常是负相关的。
人们对更好的治疗策略的需求越来越大。尽管目前治疗多发性硬化症的药物可以降低炎症发作的风险,并减缓一些多发性硬化症患者的疾病进展,但患者对药物的反应可能是可变的和次优的。对于非活动期多发性硬化症患者,没有可用的DMT可以显著改变他们的进行性恶化。此外,目前MS药物的副作用从轻微到严重不等,这可能会导致患者依从性降低。
CNM-AU8的潜在优势®对于MS
我们相信CNM-AU8®有可能成为针对CNM-Au8女士的全球一流的重新髓鞘形成和神经保护性疾病修改纳米治疗药物®通过增强受到疾病攻击的神经元和OL的能量活动来支持神经功能。与目前免疫调节的MS DMTs不同,CNM-AU8®被认为通过改善能量、减少有害的ROS和诱导保护性热休克蛋白机制直接支持神经保护和髓鞘再形成。CNM-AU8®口服,可穿透血脑屏障,迄今具有良好的安全性、耐受性和毒理学特征。交替使用或与标准免疫调节性DMT一起使用,CNM-AU8®治疗可能会改善患者的生活质量,并有可能逆转疾病的进展,因为它增强了受到疾病攻击的神经元和OL的能量活动,即使是在炎症发作得到很好控制的患者中也是如此。
多发性硬化症的非临床药理学研究综述
髓鞘形成是一个复杂的过程,导致轴突被含有特殊蛋白质和脂类的OL膜包裹。由此产生的髓鞘为轴突提供代谢支持,并促进轴突的电传导,这反过来又允许中枢神经系统处理运动、感觉和更高级别的认知功能。在活跃的髓鞘形成过程中,OL每分钟合成约100,000个蛋白质,每秒合成数千个新的脂肪分子,这反映了生成生物量所需的巨大能量投资,并使这种细胞类型成为体内对能量要求最高的细胞之一。在多发性硬化症中,髓鞘被自身免疫介导的炎症攻击破坏,其轴突曾经受到髓鞘保护和支持的神经元受到破坏,最终可能死亡。已知OL前体细胞存在于MS病变附近,并可在再髓鞘形成中发挥作用,但研究表明,这些细胞能量受损,再髓鞘形成在大多数中枢神经系统病变中次之。
在活着的多发性硬化症患者的大脑中发现了能量缺陷31磷核磁共振波谱(“31P-MRS“)。在MS患者的尸检脑中,MS病变附近的OL前体细胞显示线粒体复合体活性受损和其他能量缺陷。这些能量缺陷在多发性硬化症疾病进展中起着关键作用。CNM-AU8®是专为直接解决这些重要的病理生理机制而设计的。
我们考察了CNM-AU8的性能®为了解决OL能量缺乏,诱导重新髓鞘形成,并恢复功能活动和运动行为,在涉及到体外培养和体内检测CNM-AU8的方法®功效。这项工作已作为同行评议的出版物发表在《科学报告》上,并在此作简要总结。
离体原代OL前体细胞的实验表明CNM-Au8对髓鞘的产生有很强的诱导作用®。CNM-AU8细胞的RNAseq分析®经处理的OL前体细胞表明,已知的髓鞘基因的多种转录本上调,糖酵解活性和ATP产生也增加。几项体内实验也证明了口服CNM-Au8®结果在使用铜酮或溶血磷脂治疗的动物的大脑和脊髓中增加了重新髓鞘形成,这两种已知的药物通过不同的机制剥夺神经元的髓鞘(Robinson等人)。SCI代表2020年2月11日;10(1):1936)。在Robinson等人的同行评议出版物中进行了全面描述。无论是口服铜试剂还是立体注射溶血磷脂,都是导致胼胝体脱髓鞘或脊髓脱髓鞘的常用技术。通过在啮齿类动物的食物中加入这种试剂,铜必利酮是一种铜络合剂,可以在包括胼胝体在内的多个大脑区域内特异性地导致成熟的OL死亡。喂服铜试剂引起的最大脱髓鞘
21
目录表
通常发生在五周内,可以用透射电子显微镜进行目视监测和量化。溶血磷脂注射会导致脊髓局部区域内髓鞘的快速降解,在损伤后一天内,使用Luxol Fast Blue或甲苯胺髓鞘染色光镜观察,也可以用病变的透射电子显微镜观察,以便在接下来的几周内观察诱导的损伤内的再髓鞘形成。无论采用哪一种技术,如果要将胼胝体或脊髓重新髓鞘化为髓鞘,则需要将存活的OL前体细胞迁移到脱髓鞘部位,将这些细胞分化为成熟的有髓鞘的OL,并在这一高能量要求的过程中迅速产生特殊的蛋白质和脂类,以形成包裹在轴突周围的新的髓鞘膜。多重独立体内用铜酮或溶血磷脂作为脱髓鞘试剂进行再髓鞘试验,以证明CNM-Au8的再髓鞘能力。®。例如,CNM-AU8®在开始给药的同时预防性提供,或仅在给药两周后才提供治疗性的,以便在给药前开始脱髓鞘®。在这两种情况下,CNM-AU8®在受影响的大脑区域中,髓鞘的恢复比使用药物治疗的对照组更好。此外,提供CNM-Au8的动物®只有在完全脱髓鞘(整整五周的铜比林治疗)发生后,才有证据表明他们大脑中成熟髓鞘标志物的表达水平高于载体对照组,这表明CNM-AU8®不是阻断铜试剂的作用,而是通过刺激OL的分化来诱导恢复。溶血磷脂实验也证实了类似的结果,表明被完全不同的机制破坏的髓鞘可以通过每天口服CNM-Au8来恢复®溶血磷脂局部脱髓鞘后1-2周。CNM-AU8治疗®不仅显著改善了实验动物大脑中有髓轴突的定量检测,而且在开场测试和运动学分析中也改善了小鼠的行为和功能运动。例如,对587张透射电子显微镜图像中有髓轴突和无髓轴突的数量进行了量化,平均每个治疗组84张图像(每个治疗组15只小鼠,总共7个治疗组),显示出统计学意义(p®通过灌胃与处理过的车辆、喂饲铜试剂的对照组进行比较。在使用溶血磷脂的独立脱髓鞘模型研究中,用CNM-Au8治疗受损动物®与对照组相比,注射LPC后皮损内有髓轴突的平均增加43%(p=0.15,CNM-Au8的非配对t检验®将处理过的大鼠转移到交通工具处理过的对照组)。最后,在铜试剂介导的粗大和精细运动行为脱髓鞘模型研究中,接受治疗性交付CNM-AU8的那组动物®在开阔领域和精细运动动力学评估中都显示出可检测到的行为改善。主成分分析显示CNM-AU8与CNM-AU8的步态指标无统计学差异(P=0.47®与假治疗组相比,治疗组和假治疗组有显著差异(p=0.032;双因素方差分析)。
图8显示了观察到的CNM-Au8诱导髓鞘形成的例子®从所选内容体外培养和体内Robinson等人报道的实验。这些研究是由我们全额资助的,是西北大学、乔治华盛顿大学的学术研究人员以及各种其他学术顾问和我们员工合作的结果。
22
目录表
图8.重新髓鞘形成摘要
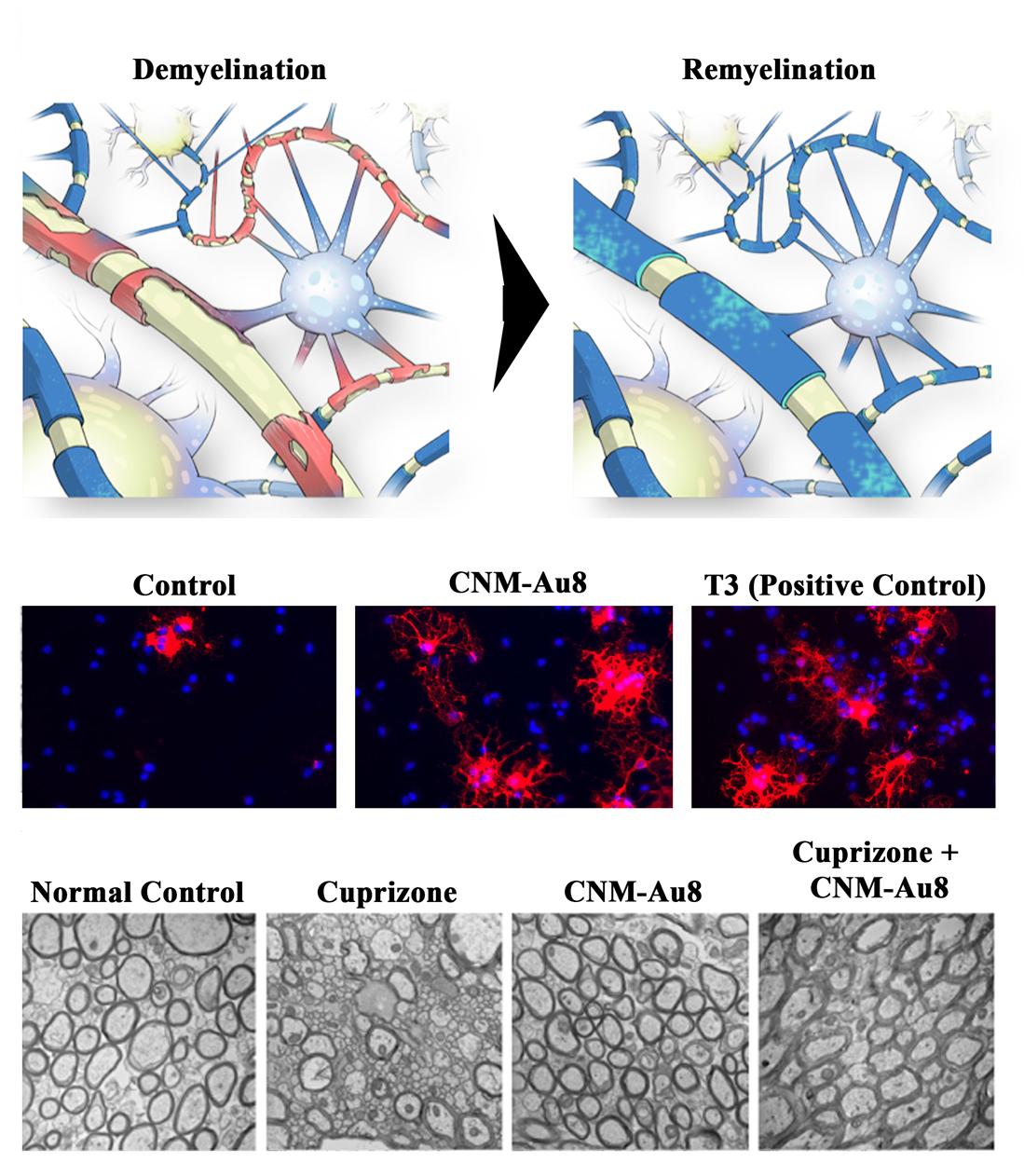
图8.CNM-AU8髓鞘形成活性总结®。左上一行:MS中出现的神经元轴突脱髓鞘(红色)(黄色)的插图右:OL(蓝色细胞)提供的沿轴突恢复的髓鞘(蓝色)插图。中排:分离的原代小鼠OL前体,经载体对照处理(左),3μg/mLCNM-AU8®,或阳性对照和髓鞘诱导剂三碘甲腺原氨酸。细胞被固定并染色为髓鞘碱性蛋白(MBP),红色是成熟髓鞘的标志,核染色DAPI为蓝色,以显示视野中所有OL前体细胞的存在。在CNM-AU8中可以看到更多表达MBP的细胞®处理过的细胞与载体处理过的细胞相比。下排:从左至右:不使用铜试剂,铜试剂,连续5周,CNM-Au8处理的小鼠痂状体切片的透射电子图像®五周,或五周的铜试剂和CNM-Au8®在这五周中的最后三周。在每一张显微照片中,髓鞘可被视为暗环。铜试剂治疗破坏髓鞘,而CNM-AU8®仅靠治疗并不能改变髓鞘。CNM-AU8®治疗经铜试剂处理的动物后,这些动物大脑中的髓鞘得以恢复。
CNM-Au8的临床研究进展®作为治疗多发性硬化症的疾病修正药物
基于我们的CNM-Au8一期临床试验的安全性研究结果®和我们强大的临床前再髓鞘形成数据,我们已经启动了两个第二阶段临床试验,以调查CNM-Au8的效果®在MS患者中。
有远见的-MS
Visionary-MS临床试验于2018年12月启动,是一项正在进行的双盲、随机、安慰剂对照的第二阶段试验,评估两剂CNM-Au8的疗效和安全性®作为一种再生髓鞘和神经保护疗法,用于患有稳定的RMS伴慢性视力障碍的人。登记的参与者必须有慢性视神经病变,定义为视力损害,在登记前六个月内没有急性视神经炎发作,以及稳定(非活动性)疾病,定义为
23
目录表
因为在入院前的三个月内,多发性硬化症没有复发。伴发免疫调节性MS DMT是允许的。参与者被随机分配到低剂量CNM-Au8®(15毫克/天),大剂量CNM-Au8®(30毫克/天),或匹配的安慰剂。主要终点是从基线到第24周的低对比度字母敏锐度(LCLA)的改善。探查终点包括OCT、多焦VEP波幅和潜伏期、全视野VEP波幅和潜伏期、MRI终点、视功能(高对比度)和生活质量/扩展残疾状态量表(EDSS)。
对比度是物体与其背景相比所包含的亮度或暗度。由眼睛区分的对比度的最小差异称为对比度阈值,通常报告为其倒数值,也称为对比度敏感度(1/对比度阈值)。因此,如果患者需要大量的对比度来识别对象,则他们的对比度敏感度较差,并且该测量的数值较低。对比度敏感度可以被认为是一种光谱,因为无论是否存在视力障碍,白色背景上的黑色字母比白色字母上对比度较低的灰色字母更容易识别。对比度阈值是个体从背景中辨别对象所需的最小对比度,对于多发性硬化症患者来说,即使在两组人的视力(在高对比度下测量)相同的情况下,对比度阈值也会高于健康人。对比度敏感度是一种光谱,可能会引起个人对比度阈值的更微妙的变化,而高对比度视觉敏锐度则无法做到这一点。LCLA测试不同空间频率的低对比度视力,这些频率可能特别受到个体复杂视觉通路中特定神经间连接受损的影响。
在Visionary-MS试验中,所有参与者都保持在双盲、安慰剂对照的治疗期间,直到最后一名参与者完成第24周。通过这种方式,将为试验中的大多数患者生成双盲、安慰剂对照的数据,直至第48周,从而提高试验评估CNM-Au8长期效果的能力®在临床终点上。TGA、加拿大卫生部和FDA都批准了这项试验的进行。截至2022年2月1日,73名参与者参加了Visionary-MS试验,在双盲期内接触该研究产品长达48周。从随机化到开放标签延长的长期治疗超过117周。
Visionary-MS的初步、中期、盲目疗效结果最近作为海报在2022年2月24-26日举行的2022年美国多发性硬化症治疗和研究委员会(ACTRIMS)论坛上公布。最初的73名参与者,包括53名试验持续时间长达48周的参与者的结果显示,在整个人群中,与临床相关的、暴露相关的平均标准LCLA改善,以及其他修改的多发性硬化症功能复合子量表(“(M)MSFC”)的综合组合,包括符号数字模式测试(SDMT,认知)、9-Hole Peg测试(9HPT,上肢功能)和计时25英尺步行(T25FWT,步态)。这些盲目的中期分析将试验治疗期间(M)MSFC得分的变化与患有轻度疾病的试验参与者的基线值进行了比较,试验参与者的基线EDSS得分为1.5或更低。这些参与者的基线分数被选为一个比较器,因为他们表现出的神经损伤比总试验人群的神经损伤更少,提供了一个有效的比较组来评估总试验人群随时间的变化。从基线到48周,将MSFC的四个子量表(LCLA、SDMT、9HPT和T25FW)的变化与这组轻度疾病对照组的基线分数进行比较。这些比较是在每个试验时间点(12、24、36和48周)进行的。在每次访问中,总体试验人群(随机2:1有效CNM-AU8®与对照组相比,(混合效应模型;p®在多发性硬化症患者中推动有意义的神经改善的潜力。此外,我们认为这些观察结果是值得注意的,因为从包括MS结局评估联盟(MSOAC)(Goldman等人)在内的数据集报告的MS患者中,LCLA、SDMT、9HPT和T25FW预计将长期下降。神经病学。2019年11月19日;93(21):e1921-e1931)。MSOAC包括从14个独立的MS临床试验中获得的预期获得的RMS患者水平的数据,包括超过12,776名参与者,合并到一个数据库中,并跟踪长达24个月。当将LCLA、SDMT、9HPT和T25FW作为多维测量而不是单独分析时,这些性能测量中的任何一个的进展都比常用的MS EDSS更敏感,并且在RMS患者中显示出长期的下降。在整个试验人群中观察到的增加的平均改善(CNM-AU8®和安慰剂)可能对CNM-Au8有积极的临床疗效®与MSOAC数据中出版物报告的预期下降形成对比。图9为截至2022年2月14日所有就诊记录的所有前瞻性多发性硬化症(如低剂量、高剂量、安慰剂)的所有试验参与者每12周间隔观察到的平均LCLA变化和综合MSFC平均6分量Z分数变化的摘要,并表明在试验过程中不断改善。
24
目录表
图9.Visionary-MS标准化LCLA和集成(M)MSFC Z-Score的平均值与基线的变化

首页--期刊主要分类--期刊细介绍--期刊题录与文摘--期刊详细文摘内容德克萨斯州霍拉代/美利坚合众国、坎珀敦、新南威尔士州/澳大利亚、宾夕法尼亚州费城/美利坚合众国、霍拉代/美利坚合众国。在2022年2月24日至26日举行的2022年ACTRIMS论坛上发表的“Visionary-MS:CNM-Au8,用于治疗慢性视神经病变的催化活性纳米金混悬液的第二阶段临床试验的更新”。
来自Visionary-MS的可用盲法安全数据表明,CNM-Au8®耐受性良好,大多数不良事件的严重程度都很轻。没有与研究产品相关的SAE(例如,安慰剂,CNM-AU8®)到目前为止都有报道。最常见的不良反应包括头痛、上呼吸道感染和喉咙痛。由于与COVID大流行相关的挑战,Visionary-MS试验将提前结束。在Visionary-MS试验有序结束后,预计2022年下半年将有完整的非盲法试验结果。
修复-MS和修复-PD
两个阶段2,中枢神经系统成像临床试验,修复-MS和修复-PD,通过测量口服CNM-Au8对MS和PD患者大脑能量代谢产物的影响来证明中枢神经系统靶点参与体内。这些能量代谢物是非侵入性和半定量的测量,利用31用7特斯拉(“7T”)磁共振扫描仪进行P-MRS成像。维修试验正在德克萨斯西南大学进行,该中心具有进行和分析7T的专门能力31P-MRS成像研究。这两项修复试验都获得了FDA的临床批准,并于2019年12月(REPAIR-PD)/2020年1月(REPAIR-MS)开始,并于2021年8月公布了REPAIR-PD和第一个修复剂量队列-MS的完整数据。我们招募了13名参与者参加Repair-PD试验,并接触了CNM-Au8®在暴露于CNM-Au8的Repair-MS试验中,长达21周的13名复发MS参与者®长达18周。修复-MS和修复-PD是单中心、仅有效的序贯小组研究,考察CNM-Au8的脑代谢效应、安全性、药代动力学和药效学®在筛查后15年内被诊断为多发性硬化症的患者或在筛查后3年内被诊断为帕金森病的患者。修复-PD已经完成了第一个剂量队列,由于机构限制,计划的第二个队列将不会被登记。Repair-MS将继续启动第二次给药队列,最多15名非活动性进展性MS参与者。
在修复程序中,使用全体积头部线圈采集~600个体素的全脑频谱波形,空间分辨率为2厘米3对于以下代谢物:NAD POOL(两者均为NAD+和NADH一起)、三磷酸腺苷-α、三磷酸肌酸、三磷酸腺苷-γ、磷酸肌酸、细胞外和细胞内无机磷、尿苷二磷酸葡萄糖、磷胆碱(PC)、磷乙醇胺,
25
目录表
甘油磷胆碱和甘油磷乙醇胺。在同一患者队列中使用部分容量的头部线圈来测量单个NAD的枕顶水平+和NADH磷代谢产物测定NAD的比例+/nadh。
对Repair-MS和Repair-PD的前两个已完成剂量队列的预先指定的综合分析于2021年8月5日公布,并在2021年9月17日至22日举行的MDS虚拟大会上以口头演示的形式提交。对于主要终点的结果,大脑NAD的平均变化+/NADH比率(氧化和还原形式的NAD的比率),显示在CNM-AU8治疗12周后,平均增加了0.589个单位(10.4%)®(P=0.037,配对t检验),对Repair-PD和Repair-MS试验进行预先指定的综合分析。关键次要端点,与NAD中的基线相比的平均变化+总NAD池中的部分和NADH部分与主要终点一致,表明NAD+NADH分数增加(p=0.026),NADH分数减少(p=0.026)。这些姊妹试验的个体结果表明,NAD的改善具有一致的统计趋势+Repair-PD和Repair-MS的NADH比值分别为p=0.11和p=0.14。
对预先指定的探索终点的分析表明,动态平衡是通过基本的能量代谢产物实现的,包括三磷酸腺苷、细胞磷(“PI”)(输入))、pC和磷酸化潜能指数(“ATP-?/ADP*pI(输入)“)。对于这些代谢物和指数,从基线到治疗第12周结束时的百分比变化与基线水平显著负相关,因此基线水平相对较低的参与者表现出增加,而基线水平相对较高的受试者表现出再平衡效应,水平下降到基线人群平均水平。这种关系是在两个试验的综合基础上观察到的,并且分别在REPAIR-PD和REPAIR-MS中独立观察到:2 = 0.82, p 2=0.71p=0.0011),磷酸化电位(r2 = 0.72, p = 0.0002; r2 = 0.68, p = 0.0019), PC (r2 = 0.78, p 2 = 0.54, p = 0.0095), and Pi(输入) (r2 = 0.42, p = 0.017; r2 = 0.48, p = 0.018).
下面的图10显示了通过部分体积线圈分析(主要终点)的NAD/NADH比率的变化,以及综合综合分析中的关键次要终点的变化。
图10.Repair-MS和Repair-PD的综合结果
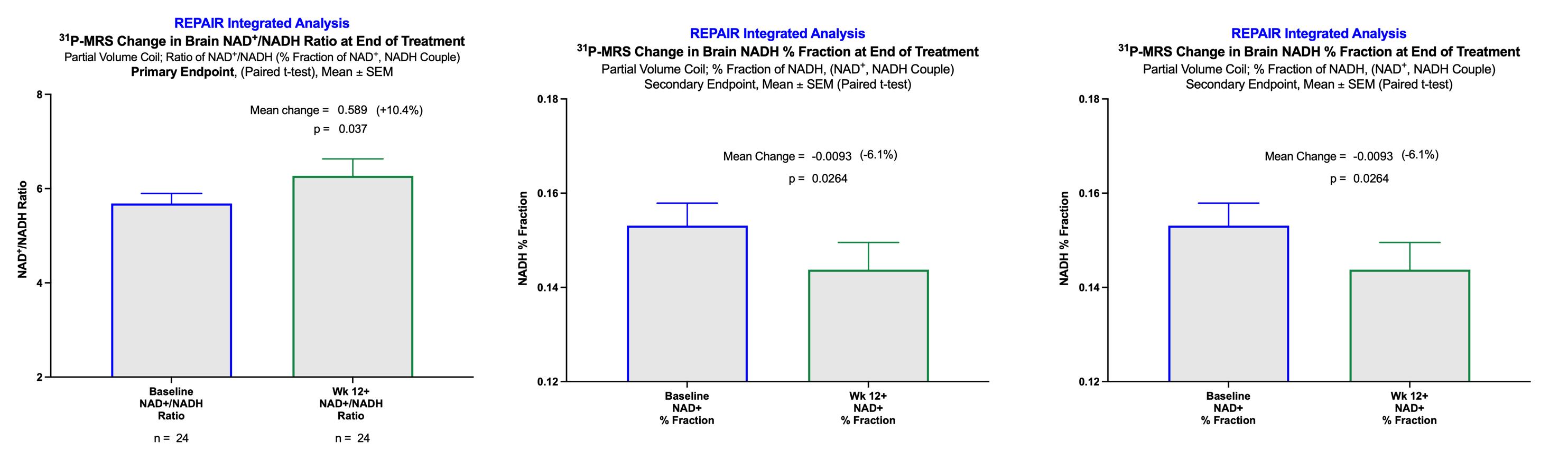
帕金森氏病
PD市场机遇
帕金森病是一种慢性进行性神经退行性疾病,主要表现为多巴胺能神经元的进行性丧失。黑质中脑的区域。多巴胺能神经元的退化导致静止性震颤、运动迟缓、肢体僵硬、步态和平衡问题,以及由于更广泛的神经元丢失而日益公认的认知和行为改变。除了衰老之外,遗传和环境因素都被认为是导致帕金森病发生的原因,而衰老是发展这种疾病的最重要的风险因素。大约每100名60岁以上的人中就有一人受到帕金森病的影响。
帕金森病的现有治疗方法及局限性
虽然已经批准了一些帕金森病的治疗方法,如多巴胺激动剂、COMT和MAO-B抑制剂,以及脑深部刺激,但这些治疗方法仅限于改善症状。目前还没有可用的治疗方法来防止多巴胺能神经元的破坏。多巴胺能神经功能丧失的不可避免的进展会导致症状的逐渐恶化,“开”(运动障碍)和“关”(僵硬)症状变得越来越难以管理。此外,长期使用左旋多巴,一种用于治疗帕金森症状的常用处方多巴胺前体,通常会导致运动障碍,其本身就会变成
26
目录表
正在禁用。尽管在过去的几十年里做出了巨大的努力,但目前还没有针对帕金森病的疾病修饰或神经保护疗法。一种改变或减缓临床进展,从而改善帕金森病健康和寿命的治疗方法,将解决一个非常重要的未得到满足的需求。
神经元能量衰竭是帕金森病的基础,表现为线粒体和溶酶体功能受损,神经元对谷氨酸毒性的敏感性,氧化应激积累,清除错误折叠蛋白的自噬失败,以及与本病相关的突触完整性丧失。因此,与CNM-Au8一样,细胞能量效率的提高是可能的®,代表了这种疾病的一个重要的、以前没有解决的治疗靶点。
CNM-AU8的潜在优势®对于PD
我们相信CNM-AU8®有可能成为全球一流的治疗帕金森病的纳米治疗药物。虽然目前治疗帕金森病的方法是为了刺激存活的多巴胺能神经元以产生部分功能效应,但没有一种疗法能阻止多巴胺能神经元不可避免的退化,从而改变疾病的发展过程。我们的非临床研究表明,CNM-Au8®在使用各种毒素和应激源造成的各种与疾病相关的侮辱中,对多巴胺能神经元具有强大的神经保护作用。此外,CNM-AU8®可能具有比现有批准的产品更好的耐受性,如治疗PD的常用药物,如左旋多巴/卡比多巴,这些药物在长期使用后会导致运动障碍的风险。
帕金森病的非临床药理学及一般神经保护研究综述
兴奋毒性损伤、氧化应激和错误折叠的α-突触核蛋白的积累是与帕金森病相关的能量通路失败的特征。为了确定CNM-AU8是否®可以作为帕金森病的神经保护剂,我们进行了一系列体外培养和体内旨在测试CNM-AU8疗效的研究®保护不同类型的神经细胞免受各种与帕金森病相关的疾病应激源的伤害。
CNM-AU8的潜力®首次证明在帕金森氏病特异性细胞模型中提供神经保护体外培养。用1-甲基-4-苯基-1,2,3,6-四氢吡啶(MPTP)刺激原代培养的大鼠多巴胺能细胞,MPTP被代谢成其活性形式MPP+)或6-羟基多巴胺(“6-OHDA”),这两种毒素都是多巴胺能神经元特有的毒素。CNM-Au8治疗原代神经元-神经胶质细胞共培养的实验研究®以剂量依赖的方式增加存活的多巴胺能神经元的数量,并通过各种指标影响神经元健康的整体改善,包括轴突网络的保存、氧化应激的减少、线粒体染色的增加和α-突触核蛋白聚集体的减少。CNM-Au8的活性®然后在标准的6-OHDA单侧帕金森病损毁模型中进行测试。损毁大鼠和假对照组分别口服赋形剂或CNM-Au8®在纹状体损伤建立后的4周(损伤后2周)或6周(损伤后1天)。CNM-AU8带来显著的功能改进®在阿朴吗啡诱导的行为旋转和圆柱状爪子放置试验中都显示了治疗作用。此外,在CNM-Au8纹状体内检测到大量存活的多巴胺能神经元®-与车辆控制相比,治疗的肢端动物。这些研究独立地证明了CNM-AU8®在帕金森病的临床前模型中,治疗具有强大的神经保护特性。
CNM-Au8的临床研究进展®作为治疗帕金森病的疾病修饰药
维修-PD
我们启动了第二阶段修复-PD临床试验,通过测量口服CNM-Au8的效果来确定CNS靶向结合®如前所述,帕金森病患者的脑能量代谢产物。Repair-PD试验是在德克萨斯大学西南分校进行的。REPAIR-PD试验获得FDA批准用于临床,并于2019年12月开始。Repair-PD试验结束时,13名随机参与者完成了第一次给药队列。在维修计划第二阶段开放标签试验中,CNM-AU8®已经展示了治疗多发性硬化症和帕金森病的靶向参与。
REPAIR-PD的结果在2021年9月17日至22日举行的2021年MDS虚拟大会上公布。对于主要终点的结果,大脑NAD的平均变化+/NADH比率(氧化和还原形式的NAD的比率),显示在CNM-AU8治疗12周后平均增加了0.386个单位(6.8%)®(P=0.1077,配对t检验)。关键次要端点,与NAD中的基线相比的平均变化+总NAD池的部分和NADH部分与显示NAD的主要终点一致+NADH分数增加(p=0.1336),NADH分数减少(p=0.1336)。探索性终点,包括从BL到EOS访问的百分比变化,显示了关键能量标记物的变化与BL水平高度相关。平均而言,能量代谢物水平低于BL值的患者在EOS就诊时全脑代谢物水平显著增加,而BL值高于BL值的平均正常化水平的患者。重要的是,这种关系在三磷酸腺苷水平上观察到(r2 = 0.8158; p 2 = 0.7218; p = 0.0002), and several other 31P代谢物,表明CNM-Au8具有体内平衡作用®关于大脑能量学。TEAE被评定为轻微和短暂的。没有SAE,也没有参与者经历临床上显著的实验室异常。这些结果
27
目录表
有力地证明了帕金森病患者大脑中的靶点参与,并提供了第一个临床证据,证明了CNM-Au8的催化作用®脑部能量代谢物。有关详细信息,请参阅上面的“-Repair-MS和Repair-PD”部分。
救援-PD
计划进行第二阶段临床试验,以调查CNM-Au8的疗效®关于延缓或预防帕金森病患者的疾病进展。RESPECT-PD试验将跟踪PD患者以确定CNM-Au8的疗效®关于稳定疾病活动作为一种神经保护疗法。救援-PD试验计划于2022年年中开始,预计试验启动后36个月内会有结果。
其他CSN®流水线中的治疗学
另外三种候选药物正处于支持IND的不同研究阶段。利用我们的CSN®在治疗药物开发平台上,我们开发了基于过渡元素银和锌(CNM-ZnAg)的额外候选药物,用于抗病毒/抗细菌和伤口愈合(CNM-AgZn17),以及用于肿瘤应用的金和铂(CNM-PtAu7)。
治疗新冠肺炎的广谱抗病毒抗菌剂--纳米锌银
CNM-ZnAg是一种口服给药、广谱抗病毒和抗菌药物。它的配方是锌(锌)的离子溶液+2)和银(银+)与有限的存在(0纳米粒子,都是使用CSN产生的®平台,不涉及用于生成锌和银化合物的传统无机合成方法。整合锌-银离子溶液的理论基础是公认的锌和银(作为独立实体)在抗微生物和抗病毒疾病治疗方面的历史活动。来自其他实验室的内部和外部的初步开发研究表明,当锌2+和银+同时给药,它们表现出协同抗病毒和抗菌性能,这是锌2+或银牌+,或Ag0纳米颗粒是单独给药的。
在人体内,锌是人体必需的结构成分
基于ICH M3(R2)指南的CNM-ZNAg标准毒理学程序已经完成。对CNM-ZNAg的毒性进行了评价,以达到最大可行剂量的高浓度给药,每天4次,连续给药大鼠28天和犬7天。在所有研究中,没有死亡,没有与测试品相关的临床观察,也没有对体重、食物消耗量、血液学终点、临床病理结果、凝血时间、尿液分析或尿液化学的影响。标准体内对啮齿动物的遗传毒性研究,包括2天的彗星试验和28天的微核网织红细胞评估,显示测试品对遗传毒性没有影响。
之前,一家之前的公司对这种膳食补充剂进行了为期七天的人体耐受性研究,以确定40名健康人类志愿者的安全性和耐受性。没有自我报告的不良事件,实验室评估表明,体重、血压、心率、肝酶(AST/ALT)、血糖或血脂(总胆固醇、低密度脂蛋白/高密度脂蛋白、甘油三酯)与基线相比没有显著变化。在7天的服药期内,没有发现与服用膳食补充剂相关的安全发现。
纳米锌银治疗新冠肺炎的临床研究进展
新冠肺炎是一种迅速出现的呼吸道疾病,导致相当大的发病率和死亡率。严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)是引起新冠肺炎的病毒感染。新冠肺炎的症状多种多样,大多数感染者都会出现不同程度的呼吸窘迫、发热、咳嗽、喉咙痛、身体不适、肌痛、恶心、腹泻、嗅觉障碍和嗅觉障碍。由于这种疾病的国际感染率和潜在的严重性质,
28
目录表
2020年3月11日,世界卫生组织将新冠肺炎定为大流行。因此,迫切需要降低新冠肺炎感染者的发病率和改善康复时间,这是一个重大的未得到满足的医疗需求。
由于世界范围内的迫切需求,我们基于CNM锌Ag可能提供免疫支持的假设,决定迅速开发CNM锌Ag作为治疗新冠肺炎的候选药物。在有限的基础上,已经提供了一种膳食补充剂版本的锌银来支持免疫健康。使用该膳食补充剂的初步非对照观察病例系列得出的结果表明,对聚合酶链式反应确诊的患者口服锌银,新冠肺炎感染可以改善患者的幸福感,限制疾病持续时间。以下是对美国一家工业食品加工设施及其相关集合住房爆发新冠肺炎疫情的大型案例系列研究的结果。62名公司员工和管理人员自愿每天口服锌银膳食补充剂(在隔离和集体住房中),完成标准化的每日症状调查,并在开始锌银治疗前和服用锌银补充剂后7天再次进行SARS-CoV-2聚合酶链式反应检测。研究人群主要是西班牙裔(74%)。平均年龄33.6岁(10.8岁),其中84%为男性。通过聚合酶链式反应检测,27名受试者在补充前被确认为SARS-CoV-2阳性。在治疗开始时聚合酶链式反应阳性确诊为SARS-CoV-2的受试者中,44%的患者在补充治疗7天后转为聚合酶链式反应阴性(图11A)。在开始治疗前35名SARS-CoV-2聚合酶链式反应阴性的受试者中,88%的患者在治疗7天后重复检测SARS-CoV-2阴性。在27名SARS-CoV-2阳性患者中,24名报告的症状与新冠肺炎一致,一般自我报告为轻度至中度强度。症状解决(图11A), 聚合酶链式反应检测到病毒清除(图11C)在锌银治疗开始后迅速下降,这与参与者对变化的总体印象(图11B)的显着改善一致。第7天的症状消退率(~75%)似乎定性地高于在可比的新冠肺炎非住院有症状患者群体中完成的一项研究的安慰剂改善率(~50%)(图11d,Skipper等人)。我是安·实习生。 2020 Jul 16;M20-4207).
29
目录表
图11.感染或接触新冠肺炎的食品加工设施工人的聚合酶链式反应状况和症状变化
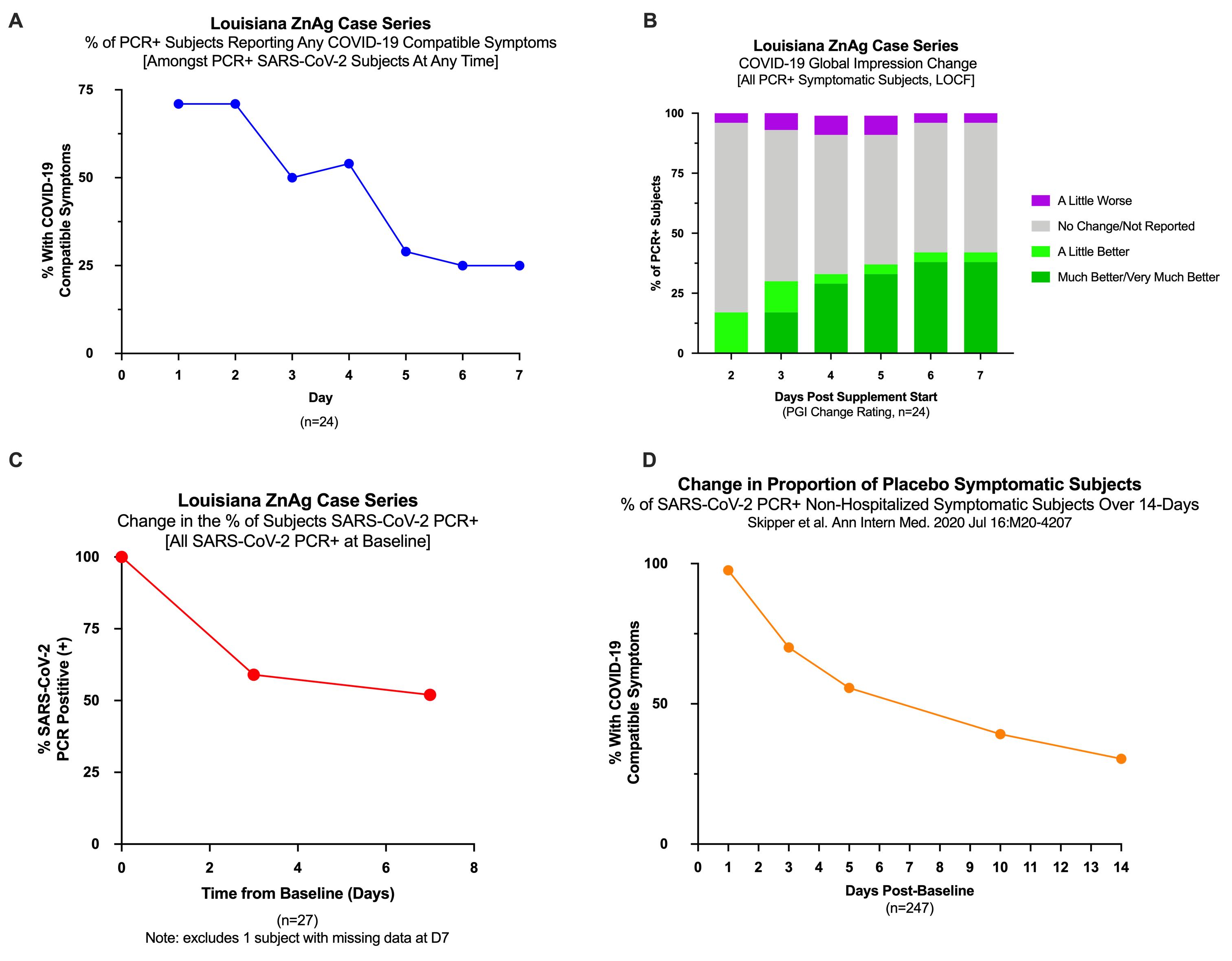
考虑到潜在的临床疗效,加上动物毒理学或初步的人类耐受性研究没有确定的安全信号,我们正在进行一项随机、安慰剂对照的临床试验,以确定CNM锌Ag对改善新冠肺炎症状的有效性和安全性。这项临床试验正在巴西进行,截至2022年2月,已完全纳入276名受试者。巴西代表着这样一个地理位置:大量的新冠肺炎病例,强大的临床基础设施和临床试验经验,合理的经济成本,以及对参与新冠肺炎临床研究参与者的有限竞争。这项试验是一项随机、双盲、安慰剂对照的CNM-ZNAg试验,旨在减少在第28天住院的发生率(主要终点),并缩短经聚合酶链式反应确诊的SARS-CoV-19受试者症状消失的时间(次要终点)。该试验将评估两种不同剂量的CNM-ZnAg,并将其与安慰剂进行联合分析。试验结果预计将于2022年年中公布。
用于创面愈合和烧伤治疗的CNM-AgZn17
CNM-AgZn17由银和锌的离子溶液组成,在聚合物凝胶配方中用于皮肤局部应用。我们已经在体外实验中证明了CNM-AgZn17对常见和耐药的金黄色葡萄球菌等常见病原体具有广泛的抗病毒和抗菌活性。我们还在糖尿病创面愈合的动物模型中显示了增强创面愈合的益处,并在烧伤愈合过程中减少了疤痕的形成。
我们目前正在完成一项标准的动物毒理学计划,以证明安全性,以便推进第一次人类剂量研究。我们已经进行了GLP局部应用的皮肤毒性研究,预计将于2023年完成。受制于
30
目录表
随着这些毒理学发现和其他结果的监管文件的公布,我们预计在2023年底之前启动一项标准的1期皮肤首例人体安全性研究,使用CNM-AgZn17进行单次递增剂量和多次递增剂量队列。这项研究的目标将是证明CNM-AgZn17的安全性足以推进到第二阶段的临床计划。鉴于到目前为止CNM-AgZ17显示出的多种临床前益处,我们设想了一个专注于治愈烧伤和/或手术伤口的临床计划,预计将于2024年启动。
CNM-PtAu7-我们的肿瘤学靶向纳米治疗
CNM-PtAu7是一种由合金金和铂组成的新型纳米晶体的悬浮液。我们已经证明,CNM-PtAu7处理人乳腺癌细胞株EFM-19和MT-3可以诱导促凋亡基因的表达,抑制抗凋亡基因的表达,这与抗肿瘤作用是一致的。我们进一步证明了与电子传输链活性相关的基因下调,这也可能抑制肿瘤的活性。关于CNM-PtAu7抗肿瘤作用的进一步研究计划在更多的恶性细胞系中进行。CNM-PtAu7已在全球所有主要市场获得专利,包括美国、欧洲、中国、新加坡和日本。
研究与开发
概述
我们对我们的研发计划投入了大量资金。我们的研究和开发活动对于获得和保持CSN开发领域公认的全球领导者的地位至关重要®治疗学。我们的研发计划是继续创新具有催化活性的新型纳米晶体和金属过渡元素的离子悬浮液,这些纳米晶体和离子悬浮液具有公认的医疗价值,以及未被探索或尚未发现的物理化学和催化性能。
我们已经在内部开发了对我们的研发过程至关重要的所有技术,并通过适当的知识产权保护来保护这些技术,并将继续这样做。我们通过马里兰州工厂的内部研发团队开展研究活动,并参与外部临床研究合作,以支持我们的研发活动。
内部研究与开发
我们的内部或内部研发活动由一群经验丰富的研究科学家、材料科学家、工程师、分子生物学家、医生、临床试验操作专家以及在生物制药行业拥有深厚专业知识的管理团队执行。我们的内部研发团队拥有从药物发现到临床前开发再到临床试验设计和实施的全方位能力。我们相信我们的内部研发团队经验丰富、合格,将使我们能够实现开发创新CSN并将其商业化的长期目标®为世界各地的患者提供治疗。我们的内部研发团队通过四个子团队进行职能运作:(1)研究工程团队,(2)生物科学发现团队,(3)非临床开发团队,和(4)临床开发团队,它们通力合作,确保我们的研发工作取得成功。
我们的研究工程团队负责新CSN的开发和优化®治疗候选药物,以及开发技术流程和基础设施,以确保我们CSN的可重复化学、制造和控制(CMC)批量生产®治疗候选人。我们的研究工程团队成员拥有化学、材料科学和工程、电气工程和固体物理方面的博士和/或硕士学位。我们的研究工程团队负责人拥有电气工程学位,并在我们的电晶体化学平台的设计中发挥了重要作用,包括我们用来生产CSN的各种连续流动装置。®治疗学。
我们的生物科学发现团队负责CSN的初步表征®治疗,进行生物测试,并通过体外和体内测试评估候选药物的活性和毒性。我们的生物发现团队评估CSN®一旦我们的研究工程团队完成了初步开发,就可以选择治疗候选药物。这个团队由一位经验丰富的研究科学家领导,他是一名医学博士,拥有分子科学博士学位。我们的生物发现团队与我们的研究工程团队密切合作,完善我们的CSN®候选者选择,例如基于结构特征,以优化我们的CSN的生物效应®候选治疗学。
我们的非临床开发团队负责开发完整的非临床动物药理学、毒理学和安全性研究数据集,这足以支持向人类研究伦理委员会(“HREC”)和政府监管机构提交监管文件,以便获得在人体研究中使用的批准。我们的非临床开发团队与我们的生物科学发现团队和临床开发团队合作,将我们的发现转化为动物,并为最终的患者研究做准备。该团队还领导我们与大学和学术界的外部合作研究活动
31
目录表
专家。我们的非临床开发团队由一位拥有斯坦福大学发育生物学博士学位和剑桥大学遗传学科学硕士学位的研究科学家领导,她曾在剑桥大学担任马歇尔学者。她也是犹他大学医学院的兼职教员。
我们的临床开发团队由首席医疗官领导,他是一名获得董事会认证的神经科医生,也是美国神经病学学会会员。一旦我们的CSN®候选治疗药物已经证明了足够的安全性和毒理学结果,可以进入人体研究,临床开发团队设计、实施并监督我们临床试验的操作进行。临床试验旨在证明我们的CSN®治疗学在治疗疾病方面是安全有效的。
外包研发
与行业实践一致,我们还将某些研究和开发外包给关键的学术合作伙伴、非临床研究组织和第三方CRO。我们与拥有髓鞘形成和神经保护专业知识的重点学术大学的专家合作。这些大学的合作者进行了动物实验,以证明CNM-Au8的效果®在动物和基于细胞的体外试验中的髓鞘再生和神经保护的治疗。为了支持我们的研究工作,我们与位于ALS的约翰·霍普金斯大学、剑桥大学的髓鞘相关实验、西北大学的髓鞘相关实验、乔治华盛顿大学的髓鞘相关实验以及爱丁堡大学的髓鞘相关研究的学术专家进行了合作。一般来说,我们将大部分毒理学、药理学和毒代动力学研究外包给非临床的专家CRO。
为了最大限度地提高运营灵活性和效率,我们聘请了行业领先的CRO来管理、实施和支持我们的临床试验,并补充我们的内部研发能力。我们采用严格的程序来选择CRO为我们进行研究;选择是基于在中枢神经系统疾病领域的质量、声誉和研究经验。除了CRO提供的服务和产品的广度、深度和质量外,在临床试验管理方面,我们还强调CRO有能力促进最佳选址、及时招募患者和有效地进行复杂的临床试验。我们的CRO在其研究的职能领域内得到了广泛的认可。
我们与CRO和我们的外部合作伙伴就每个临床试验或非临床研究项目签订单独的协议。所有CRO和其他外部研究合作者都是独立的第三方。与我们的主要CRO和外部合作伙伴签订的服务协议的主要条款摘要如下:
我们通过各种活动监控和评估我们的CRO和外部研究合作伙伴,包括现场访问、持续的项目团队审查和/或第三方评估员的评估。我们通过保持强有力的质量控制措施,努力实现临床试验的卓越。我们履行核心职能,如临床开发战略制定和内部方案设计,并对临床试验管理的关键职能进行控制和监督。我们定期进行现场访问,以监督网站的启动、患者招募和数据质量监控,除非受到新冠肺炎相关研究限制的限制。我们还聘请第三方顾问进行临床试验审计。通过内部数据审查进一步评估数据质量,包括医疗审查、文件审查和监测报告审查。我们不会与没有围绕数据隐私和保障措施建立流程以确保通过临床试验合规的供应商合作。我们与CRO和其他外部研究伙伴保持着稳定的关系。
临床试验管理
为了支持我们的临床试验,我们的内部临床试验团队为我们的临床试验设计、实施、收集和分析数据。当需要额外的服务来支持临床试验时,我们会对潜在的供应商和CRO进行可行性和资格评估。这些供应商通过审查其目前的运营结构和既定程序进行审查,
32
目录表
关于研究、适应症或人群的知识和经验,以及参与临床站点的过去反馈。我们的内部临床开发团队监督CRO的关键临床活动,如患者资格审查、医疗数据审查和SAE审查,以确保这些CRO的表现符合我们的规程和适用法律,从而保护我们临床试验数据的完整性和真实性。我们的内部临床开发团队与CRO举行会议,通过跟踪临床进展并解决潜在问题和风险来评估CRO的表现。
助学金
我们从多个组织获得了赠款,包括国家多发性硬化症协会、澳大利亚注册的非营利性慈善机构FightMND和迈克尔·J·福克斯基金会,他们总共向我们发放了总计约230万美元的赠款。我们还获得了对Healey ALS平台试验的间接资金支持,该试验由马萨诸塞州综合医院管理,正在进行CNM-Au8的平台试验®与其他药物相比,成本要低得多,如果我们以合理的市场价格进行设计类似的研究。
这些赠款包括以下条款:
2019年12月,我们从国防部管理的美国国会指导的医学研究计划获得了130万美元的拨款,我们决定不接受。我们将我们的决定通知了国防部,拨款从2021年7月19日起终止。这笔赠款没有在任何时期的财务报表中确认,也没有对我们的财务状况、经营业绩或任何时期的现金流产生影响。
制造业
我们生产CSN®在我们位于美国马里兰州东北部的自己的生产设施(“东北设施”),基于完全由我们发明的新的制造工艺和设备。东北工厂符合GMP,我们运营着一个ISO8级的洁净室,其中包含我们发明并获得专利的专门的电晶体化学设备,或连续流动槽设备,以生产我们的CSN®治疗用高纯度的原料。在我们目前的经营规模下,我们生产过程中的金纳米晶体悬浮液,我们的铅资产CNM-Au8的活性药物成分(“原料药”)®,持续进行。我们相信,我们目前的原料药生产能力完全足以满足我们正在进行的第二阶段和第二/3阶段临床试验对研发和供应的需求,我们相信我们的工艺可以进行扩展,以实现早期商业上可行的数量。
我们于2021年9月开始租赁位于美国马里兰州埃尔克顿的74,210平方英尺的生产设施(“埃尔克顿设施”),该设施位于东北工厂以北几英里处。Elkton工厂正在重新开发,以支持我们独特的制造需求,并将使我们能够大幅提高我们的制造能力,为2022年下半年预期发布的2/3阶段Healey ALS平台试验评估CNM-AU8的数据做准备®作为治疗肌萎缩侧索硬化症的方法。我们还签订了一份从2022年2月开始的租约,将我们的东北工厂从大约21,000平方英尺扩大到32,603平方英尺,以进一步提高我们的制造能力。我们相信,我们的技术专长和能力完全足以扩大产能,以支持预期的增长和预期的商业化。我们还制定了一项分阶段计划,随着对我们产品的需求增加,大幅扩大我们的生产流程和能力,以满足商业营销需求。我们相信,我们目前的生产环境已经使我们成为领先的世界级CSN制造商®考虑到质量、成本、可管理性、可扩充性和可控性,我们的设施、设备和流程将符合国际惯例,并支持我们的长期战略计划。
33
目录表
通过多年的密集研究和开发,我们已经对我们的生产和交付过程进行了微调,使我们能够始终如一地、可靠地和负担得起地生产我们的核心候选药物,包括CNM-Au8®。我们还投入了相当多的时间和大量资源来完善处理和存储系统,以保持我们纳米晶体悬浮液的稳定性和有效性。一般而言,CSN的制造工艺®治疗包括以下步骤:
许可证安排
2018年,我们与4Life建立了许可协议和独家供应协议,4Life是一家国际保健品供应商,也是我们的股东之一。
根据这项许可协议,我们向4Life授予独家许可,涉及我们的电化学晶体化学技术平台生产的极低浓度银、金和其他类似的极低浓度非药物补充剂产品。这一独家许可不包括4Life对其拥有非独家权利的锌银。4Life被允许在全球范围内开发、制造、制造、使用、销售和商业化膳食补充剂领域的特许产品和某些人类内部或外部使用的非药物产品,这些产品含有通过我们的电化学制造技术形成的基于金属的成分。4Life将在监管部门批准其作为营养矿物质补充剂销售后,利用其合理勤奋的商业努力将产品推向某些商业市场。本许可协议的初始期限从2018年8月31日开始,并将持续到4Life于2020年7月1日向市场推出第一个营养补充剂许可产品后的五年。经双方同意,许可协议可续期五年。许可协议到期后,协议中的排他性条款将转换为非排他性条款。许可协议只有在双方相互同意的情况下才能终止,或在任何一方违反协议而导致根据适用法律终止协议的情况下终止。
根据独家供应协议,4Life将独家向我们购买授权产品,我们将通过4Life独家销售授权产品,但并非通过4Life独家销售的锌银除外。在未来发生某些事件时,4Life可以根据许可协议获得独家制造许可产品的权利,但不适用于此权利的锌银除外。独家供应协议的初始期限于2018年8月31日开始,将持续到最低销售开始日期后五年,双方商定的最低销售开始日期为2021年4月。经双方同意,独家供应协议可再续期五年。4 Life可以因由终止独家供应协议,原因包括拒绝、未治愈的重大违约、资不抵债、破产、为债权人的利益而进行的一般转让、未能提供财务和运营能力的合理保证、长期无法补救的不可抗力,以及没有适当地通知控制权的变化。我们可以终止独家供应协议的情况下,拒绝,未治愈的重大违约,资不抵债,破产或一般转让债权人的利益由4Life。
在商业销售时,4Life根据4Life的产品总销售额篮子的大小向我们支付个位数的版税。根据许可协议,特许权使用费按季度支付,直至许可协议终止。此外,4Life
34
目录表
将向我们支付完全负担的制造费用,外加保证的两位数利润率。我们开始供应KHC46(黄金系数)和低剂量锌银溶液(锌因数)在本许可协议下的2020年上半年。
到目前为止,我们还没有授权我们的电晶体化学平台,任何CSN®治疗公司或任何候选药物转让给任何其他党派。
原材料的来源和可获得性
某些关键原材料可从市场上数量有限的供应商处获得。请参阅“风险因素-我们的业务依赖于原材料的使用,这些原材料的供应减少或成本增加或此类原材料的任何质量问题都可能对我们的业务、财务状况、运营结果和前景产生实质性的不利影响了解更多信息。
竞争
虽然治疗中枢神经系统疾病的方法竞争激烈,变化频繁,但目前还没有FDA批准的治疗方法具有支持患者髓鞘再生和神经保护的机制。CNM-AU8®其髓鞘再生和神经保护的核心作用为我们治疗中枢神经系统疾病提供了全球独一无二的先发优势。再加上我们扩大的知识产权组合,我们相信,对于进入髓鞘再生和神经保护疗法市场的任何潜在竞争对手来说,要在不违反我们的知识产权保护的情况下复制我们的努力将是具有挑战性的。
知识产权
我们的知识产权通过广泛的全球专利、机构专业知识和经验以及专业技术诀窍得到保护,这使我们能够保持在CSN发展方面的领先地位。®治疗高度医疗需要的疾病。
截至2021年12月31日,我们在全球已获得150多项专利,全球约有20项专利正在申请中。我们有世界范围的权利来保护我们的CSN,从而将其商业化®并相信,我们已颁发的和正在申请的专利将提供足够的保护,确保我们CSN未来的商业潜力®治疗学。
我们已在美国(美国)、澳大利亚(AU)、巴西(BR)、加拿大(CA)、中国(CN)申请并获得专利。欧洲专利局(EP),包括比利时(BE)、瑞士(CH)、德国(DE)、丹麦(DK)、芬兰(FI)、法国(FR)、英国(GB)、冰岛(IS)、爱尔兰(IE)、意大利(IT)、匈牙利(HU)、荷兰(NL)、挪威(NO)、波兰(PL)、葡萄牙(PT)、西班牙(ES)、瑞典(SE)、斯洛文尼亚(SI)和土耳其(TR);埃及(EG);印度(IN);印度尼西亚(ID);以色列(IL);日本(JP);韩国(KR)、墨西哥(MX)、新西兰(NZ)、菲律宾(PH)、俄罗斯(RU)、塞舌尔(SC)、新加坡(SG)和阿拉伯联合酋长国(AE);拥有多个基本专利家族保护我们的CSN®治疗学。下表列出了与我们的CSN相关的授权专利系列材料®治疗学。
描述 |
|
管辖权 |
|
申请日期(美国) |
|
授予日期(美国) |
用于处理液体并在液体、装置和纳米颗粒以及由此产生的纳米颗粒/液体溶液中制造某些成分(例如纳米颗粒)的连续方法(这些专利涉及CNM-AU8®和锌银) |
|
已发出:美国(4)、AU(3)、CA(2)、CN、ID、IL、IN、JP(2)、KR、MX、PH;BE、DK、ES、FI、FR、DE、HU、IE、IT、NL、NO、PL、PT、SE、SI、SC、CH、TR、GB 批准: 待定:美国,EP |
|
July 11, 2007 |
|
2013年12月31日 2017年8月29日 2018年10月9日 2013年9月24日 July 12, 2016 这些专利的到期日期将在适用的外国司法管辖区于2028年到期,在美国将于2030年到期。* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
35
目录表
处理液体并在液体、装置和纳米颗粒及其纳米颗粒/液体溶液中制造某些成分(例如纳米颗粒)的连续方法 |
|
已发出: U.S. (3) 待定: U.S. |
|
2009年1月14日 |
|
2013年9月24日 July 12, 2016 2019年10月15日 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
连续、半连续和间歇处理液体并在液体、装置和纳米颗粒以及纳米颗粒/液体溶液和胶体中制造某些成分(例如纳米颗粒)的方法(这些专利涉及CNM-Au8®和锌银) |
|
已发出:美国(3)、AU、CA、CN、IN、IS、JP、KR;CH、DE、DK、FI、FR、IE、NL、NO、SE、GB 允许: 待定:极压 |
|
2009年1月15日 |
|
June 30, 2015 July 31, 2018 May 18, 2021 这些专利的到期日将于2030年在美国和适用的外国司法管辖区* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
医疗用新型金基纳米晶及其电化学制造方法(这些专利涉及CNM-Au8®) |
|
已发出:美国(3)、AE、AU(4)、BR、CA、CN、ID、IN、IL、JP(4)、KR(3)、MX、PH、RU、SG(2);CH、DE、DK、ES、FI、FR、GB、IE、IT、NL、NO、SE 允许:声发射 待定: AU, MX, PH, SG, U.S. (2) |
|
July 8, 2009 |
|
March 28, 2017 2019年10月22日 April 20, 2021 这些专利的到期日将于2030年在美国和适用的外国司法管辖区* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
新型金-铂基双金属纳米晶体悬浮液,其电化学制造方法及其用途(这些专利不涉及本文中任何特别命名的候选产品) |
|
已发出:美国、AE、AU、CA、CN、ID、IL、IN、JP、KR(2)、MX、新西兰、PH、RU、SG;CH、DE、DK、ES、FI、FR、GB、IE、IT、NL、NO、SE。 待定:BR,美国 |
|
March 30, 2011 |
|
July 12, 2016 这些专利的到期日将分别于2030年在美国和2032年在适用的外国司法管辖区* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
治疗某些脱髓鞘和髓鞘障碍和/或促进髓鞘再生的方法和治疗(这些专利涉及CNM-Au8®) |
|
已发出:Au、ID、IL、JP、MX、NZ(2)、PH、RU、SG(2);BE、DK、FI、FR、DE、HU、IE、IT、NL、NO、PT、SE、SI、CH、TR、GB 批准: 允许:KR 待定:BR、CA、CN、IN、JP |
|
北美 |
|
北美 这些专利的到期日将于2033年在美国和适用的外国司法管辖区*
|
|
|
|
|
|
|
|
*到期日期不包括某些国家/地区可能的专利延期。
到目前为止,我们没有参与任何可能受到威胁或悬而未决的知识产权诉讼,我们也没有收到任何关于侵犯知识产权的索赔的通知,我们可能是索赔人或答辩人。
政府监管
FDA和联邦、州和地方各级以及外国的其他监管机构,除其他外,广泛管理研究、开发、测试、制造、质量控制、进口、出口、安全、有效性、标签、
36
目录表
药品的包装、储存、分销、记录保存、审批、广告、促销、营销、审批后监控和审批后报告,例如我们正在开发的药品。我们与第三方承包商一起,必须遵守我们希望进行研究或寻求CNM-AU8批准或许可的国家的管理监管机构的各种临床前、临床和商业批准要求。®或任何未来的毒品候选人。
FDA药品审批流程
在美国,FDA根据《联邦食品、药物和化妆品法》以及执行法规和指南对药品进行监管。FDA在候选药物在美国上市之前所需的程序通常包括以下几个方面:
临床前和临床发展
在美国开始对候选药物进行第一次临床试验之前,我们必须向FDA提交IND申请。IND申请是FDA授权给人类使用研究用新药产品的请求。IND提交的中心焦点是临床试验的总体研究计划和方案。IND还包括动物和体外培养评估候选药物的毒理学、药代动力学、药理学和药效学特征的研究;CMC信息;以及任何可用人类数据或文献,以支持研究产品的使用。IND必须在人体临床试验开始前生效。IND在FDA收到后30天自动生效,除非FDA在30天内对拟议的临床试验提出安全担忧或其他问题。在这种情况下,IND可能会被临床搁置,直到IND赞助商和FDA解决了悬而未决的关切或问题。因此,提交IND可能会导致FDA授权开始临床试验,也可能不会。
临床试验涉及根据GCP和保护人类研究对象的规定,在合格研究人员的监督下向人类受试者管理研究产品,包括要求所有研究对象就其参与任何临床试验提供自愿知情同意。临床试验是在临床试验方案下进行的,其中详细说明了试验的目标、用于监测安全性的参数和要评估的有效性标准。在产品开发期间进行的每个后续临床试验和后续的任何方案修改都必须单独提交给现有的IND。对于新的适应症,可能需要单独的新IND。IRB必须在临床试验开始之前审查和批准任何临床试验的计划及其知情同意书,并必须监督试验直到完成。通常,每个机构或临床站点都有自己的IRB。IRB负责确保人类受试者的权利和隐私得到维护。监管当局、IRB或赞助商可随时以各种理由暂停临床试验,包括发现受试者面临不可接受的健康风险,或试验不太可能达到其声明的目标。一些研究还包括由临床试验赞助商组织的由合格专家组成的独立小组DSMB的监督,该小组根据对试验的某些数据的访问,授权临床试验是否可以在指定的检查点进行。如果dsmb确定存在
37
目录表
受试者存在不可接受的安全风险或其他理由,如没有疗效证明。还有关于向公共注册机构报告正在进行的临床试验和临床试验结果的要求。为了批准NDA,人体临床试验通常分三个连续阶段进行(可能重叠或合并):
在某些情况下,FDA可能会要求,或者公司可能会自愿在产品获得批准后进行额外的临床试验,以获得有关该产品的更多信息。这些研究被称为第4阶段研究,可以作为批准NDA的条件来实施。在临床试验的同时,公司可能会完成额外的动物研究,开发关于候选药物生物学特性的更多信息,并必须根据当前的GMP要求最终确定商业批量生产产品的过程。制造过程必须能够始终如一地生产高质量的候选药物批次,除其他外,还必须开发测试最终产品的特性、强度、质量和纯度的方法。此外,必须选择和测试适当的包装,并进行稳定性研究,以证明候选药物在保质期内没有发生不可接受的变质。
像我们这样的制药公司,在向FDA作出重大虚假或欺诈性陈述、向FDA或任何其他政府实体的人员提供或提供任何被禁止的报酬、酬金或其他有价值的东西,或其他行为、陈述或不作为的情况下,受制于各种法律(包括《美国法典》第21编第335a,335b条或第335c,42 U.S.C.第1320a-7条的规定)禁止雇用或使用的个人的雇用或使用,或其他行为、陈述或不作为,这些行为、陈述或不作为受FDA政策的约束。和非法小费“在56 FED中提出。注册46191(1991年9月10日),雇用此类个人,或在开发和监管申请过程中发生此类违规行为,可能会阻止或推迟对保密协议的任何批准。
保密协议的提交、审查和批准
假设根据所有适用的法规要求成功完成了所有要求的测试,则非临床研究和临床试验的结果将作为NDA的一部分提交给FDA,请求批准将该产品用于一个或多个适应症。保密协议必须包括从相关的临床前研究和临床试验中获得的所有相关数据,包括否定或模糊的结果以及积极的发现,以及与产品的CMC相关的详细信息,以及建议的标签等。提交保密协议需要向FDA支付一笔可观的申请使用费(除非适用于豁免或豁免)。
一旦提交了保密协议,FDA的目标是在接受备案申请后10个月内审查标准申请(60天程序),或者,如果申请符合优先审查资格,则在FDA接受备案申请后6个月内审查。在标准审查和优先审查中,FDA对补充信息或澄清的要求可以显著延长审查过程。FDA审查保密协议,以确定产品是否安全有效,以及其制造、加工、包装或持有的设施是否符合旨在确保产品持续安全性和有效性的标准。FDA可能会召集一个咨询委员会,就申请审查问题提供临床见解。在批准保密协议之前,FDA通常会检查生产产品的一个或多个设施。FDA不会批准申请,除非它确定制造工艺和设施符合GMP要求,并足以确保产品在所要求的规格下一致生产。此外,在批准NDA之前,FDA通常会检查一个或多个临床地点,以确保符合GCP。如果FDA确定申请、制造工艺或制造设施不可接受,它将在提交的文件中列出不足之处,并经常要求提供额外的测试或信息。尽管提交了任何要求的补充信息,FDA最终可能会决定该申请不符合批准的监管标准。
38
目录表
在FDA对NDA进行评估并对将生产研究产品和/或其药物的制造设施进行检查后,FDA可以出具批准信或完整的回复信。批准函授权该产品的商业营销,并提供特定适应症的具体处方信息。一封完整的回复信将描述FDA在NDA中发现的所有缺陷,但如果FDA确定支持申请的数据不足以支持批准,FDA可以在没有首先进行所需检查、测试提交的产品批次和/或审查拟议标签的情况下发布完整的回复信。在发布完整的回复信时,FDA可以建议申请人可能采取的行动,以解决任何调查结果,并将NDA置于批准的条件下,包括要求提供更多信息或澄清。如果不符合适用的监管标准,FDA可以推迟或拒绝批准NDA,要求额外的测试或信息和/或要求上市后测试和监督以监测产品的安全性或有效性。
如果一种产品获得监管部门的批准,这种批准将被授予特定的适应症,并可能导致对该产品可能上市的指定用途的限制。例如,FDA可能会批准具有风险评估和缓解战略(“REMS”)的NDA,以确保产品的好处大于其风险。REMS是一种安全策略,用于管理与产品相关的已知或潜在严重风险,并通过管理此类药物的安全使用使患者能够继续获得这些药物,可能包括药物指南、医生沟通计划或确保安全使用的要素,如受限分配方法、患者登记和其他风险最小化工具。FDA还可能以改变拟议的标签或制定适当的控制和规范等为条件进行批准。一旦获得批准,如果没有保持对上市前和上市后要求的遵守,或者如果产品进入市场后出现问题,FDA可能会撤回产品批准。FDA可能要求进行一项或多项第4阶段上市后研究和监测,以进一步评估和监测产品在商业化后的安全性和有效性,并可能根据这些上市后研究的结果限制产品的进一步销售。
加快发展和审查计划
提交FDA审批的候选药物的上市申请可能符合FDA旨在加快FDA审查和批准过程的计划的资格,例如优先审查、快速通道指定、突破性疗法和加速批准。
如果一种产品有可能在没有令人满意的替代疗法的情况下提供安全有效的治疗,或者与市场上销售的产品相比,在治疗、诊断或预防严重疾病或状况方面有显著改善,则该产品有资格获得优先审查。对于含有新分子实体的产品,优先审查指定意味着FDA的目标是在60天申请日后6个月内对上市申请采取行动(而标准审查为10个月)。
为了有资格获得快速通道认证,FDA必须根据赞助商的请求,确定一种产品旨在治疗严重或危及生命的疾病或状况,并证明有潜力通过提供一种不存在的疗法或基于疗效或安全因素的可能优于现有疗法的疗法来满足未满足的医疗需求。快速通道指定为与FDA审查团队进行更频繁的互动提供了机会,以加快产品的开发和审查。FDA还可以在提交完整的申请之前滚动审查快速通道产品的NDA部分,前提是赞助商和FDA就提交申请部分的时间表达成一致,并且赞助商在提交NDA的第一部分时支付任何必要的使用费。在提交保密协议的最后部分之前,审查时钟不会开始。
此外,根据2012年7月颁布的FDA安全和创新法案的规定,赞助商可以请求将候选药物指定为“突破性疗法”。突破性疗法被定义为一种旨在单独或与一种或多种其他药物联合治疗严重或危及生命的疾病或状况的药物,初步临床证据表明,该药物可能在一个或多个临床重要终点显示出比现有疗法显著的改善,例如在临床开发早期观察到的实质性治疗效果。被指定为突破性疗法的药物也有资格获得加速批准。FDA必须采取某些行动,如及时召开会议和提供建议,以加快批准突破性疗法的申请的开发和审查。
此外,在治疗严重或危及生命的疾病或状况方面的安全性和有效性而研究的产品,如果确定该产品对合理地可能预测临床益处的替代终点有效,或者对可以比不可逆转的发病率或死亡率更早地测量的临床终点有效,并且考虑到病情的严重性、稀有性或流行率以及可用或缺乏替代治疗,合理地预测对不可逆转的发病率或死亡率或其他临床益处的影响,则可获得加速批准。作为加速批准的条件,fda通常会要求赞助商进行充分和良好控制的上市后临床试验,以验证和描述预期的
39
目录表
对不可逆转的发病率或死亡率或其他临床益处的影响。作为加速批准的条件,FDA目前还要求预先批准促销材料,这可能会对产品商业推出的时间产生不利影响。
即使一种产品符合一个或多个这些计划的条件,FDA也可能在以后决定该产品不再符合资格条件,或者决定FDA审查和批准的时间段不会缩短。此外,优先审查、快速通道指定、突破性治疗指定和加速批准不会改变批准的标准,但可能会加快开发或批准过程。
孤儿药物名称
根据《孤儿药品法》,FDA可以将一种用于治疗罕见疾病或状况的药物授予孤儿称号,这种疾病或状况在美国影响不到20万人,或者在美国影响超过20万人,而在美国,无法合理预期在美国开发和提供治疗这种疾病或状况的药物的成本将从该药物在美国的销售中收回。在提交保密协议之前,必须请求指定为孤儿。在FDA授予孤儿称号后,FDA公开披露了治疗剂的通用身份及其潜在的孤儿用途。孤儿药物指定本身不会在监管审查或批准过程中传递任何优势,也不会自动缩短监管审查或批准过程的持续时间。然而,被授予孤儿地位的药物允许赞助商获得税收抵免和用户费用减免。
如果一种被指定为孤儿的产品随后获得了FDA对其具有这种指定的疾病的第一次批准,该产品有权获得孤儿药物排他性,这意味着FDA可能不会批准任何其他申请,包括完整的NDA,在七年内销售相同适应症的同一产品,除非在有限的情况下,例如显示出相对于具有孤儿药物排他性的产品的临床优势。孤儿药物排他性并不阻止FDA批准针对相同疾病或状况的不同药物,或针对不同疾病或状况的相同药物。指定的孤儿产品如果被批准用于比其获得孤儿指定的指示更广泛的用途,则不得获得孤儿排他性。此外,如果FDA后来确定指定请求存在重大缺陷,或者如果制造商无法保证足够数量的产品来满足这种罕见疾病或疾病患者的需求,则可能会失去在美国的独家营销权。
审批后要求
我们根据FDA批准制造或分销的任何产品都受到FDA普遍和持续的监管,其中包括与质量控制和质量保证、记录保存、不良事件报告、定期报告、产品抽样和分销以及产品广告和促销相关的要求。在批准后,对批准的产品的大多数更改,如增加新的适应症或其他标签声明,都要经过FDA的审查和批准。还有持续的使用费要求,根据这一要求,FDA对批准的NDA中确定的每种产品进行年度计划费用评估。制造商及其分包商被要求向FDA和某些州机构登记他们的机构并列出他们生产的药品,并接受FDA和某些州机构的定期突击检查,以确保其符合GMP,这对我们施加了某些程序和文件要求。对制造工艺的更改受到严格的监管,根据更改的重要性,可能需要FDA事先批准才能实施。FDA的法规还要求调查和纠正任何偏离GMP的情况,并对我们和它可能决定使用的任何第三方制造商或包装商提出报告要求。因此,制造商必须继续在生产和质量控制方面花费时间、金钱和精力,以保持符合GMP和其他方面的法规遵从性。
如果没有遵守监管要求和标准,或者如果产品上市后出现问题,FDA可能会撤回批准。后来发现产品存在以前未知的问题,包括预料不到的严重程度或频率的不良事件,或生产工艺,或未能遵守监管要求,可能会导致修订批准的标签以添加新的安全信息;实施上市后研究或临床试验以评估新的安全风险;或根据REMS计划实施分销限制或其他限制。除其他外,其他潜在后果包括:
40
目录表
FDA严格监管药品和生物制品的营销、标签、广告和促销。公司只能提出与FDA批准的药物的安全性、有效性和使用条件有关的声明,并根据批准的标签的规定进行。FDA和其他机构积极执行禁止推广非标签用途的法律法规。不遵守这些要求可能会导致负面宣传、警告信、改正广告,以及潜在的民事和刑事处罚。医生可能会为合法获得的产品开具处方,用于产品标签中未描述的用途,以及与我们测试和FDA批准的用途不同的用途。这种标签外的使用在医学专科中很常见。医生可能会认为,在不同的情况下,这种非标签使用是许多患者的最佳治疗方法。FDA不规范医生在选择治疗时的行为。然而,FDA确实限制了制造商在产品标签外使用问题上的沟通。
其他美国医保法和合规性要求
在美国,我们目前和未来的业务除受FDA的监管外,还须受联邦、州和地方当局的监管,包括但不限于,隶属于美国卫生与公众服务部(HHS)的联邦医疗保险和医疗补助服务中心(CMS),以及HHS的其他部门(如监察长办公室、民权办公室和卫生资源与服务管理局)、美国司法部(DoJ)、司法部内的个别联邦检察官办公室,以及州和地方政府。例如,我们的临床研究、销售、营销和科学/教育资助计划必须遵守《社会保障法》(如《反回扣法》)、《虚假申报法》、《反欺诈法》的反欺诈条款,以及实施《健康保险携带和责任法案》(HIPAA)、《药品供应链安全法案》(“DSCSA”)和类似的州法律的隐私和安全条款。我们的业务运营以及与调查人员、医疗专业人员、顾问、第三方付款人、患者和客户的当前和未来安排可能受到联邦政府以及我们开展业务所在州和外国司法管辖区当局的医疗法律、法规和执法的约束。这些法律管辖但不限于州和联邦反回扣、欺诈和滥用、患者经纪、虚假声明、隐私和安全、价格报告、药品分销和医生阳光法律。我们的一些商业前活动受到其中一些法律的约束。
除其他事项外,联邦反回扣法规禁止任何个人或实体故意或故意以现金或实物直接或间接、公开或隐蔽地提供、支付、索要或接受任何报酬,以诱导或作为购买、租赁、订购或安排购买、租赁、订购或安排购买、租赁或订购根据Medicare、Medicaid或其他联邦医疗保健计划可全部或部分报销的任何物品或服务的回报。薪酬一词被广泛解读为包括任何有价值的东西。反回扣法规被解释为适用于治疗产品制造商与处方者、购买者和处方经理之间的安排。有一些法定例外和监管避风港保护某些活动不被起诉。例外和安全港的范围很窄,涉及可能被指控旨在诱使开处方、购买或推荐的报酬的做法,如果不符合例外或安全港的资格,可能会受到审查。没有满足特定适用的法定例外或监管安全港的所有要求,并不意味着这种行为本身就是《反回扣条例》所规定的非法行为。取而代之的是,将根据对其所有事实和情况的累积审查,逐案评估这一安排的合法性。我们的做法可能在所有情况下都不符合法定例外或监管安全港保护的所有标准。
此外,2010年的《患者保护和平价医疗法》修正了《反回扣法令》中的意图标准,2010年的《保健和教育和解法案》(统称为《平价医疗法》)将其修正为更严格的标准,规定个人或实体不再需要实际了解该法令或违反该法令的具体意图即可实施违法行为。违反反回扣法规可能会导致巨额的民事和刑事罚款和处罚,监禁,并被排除在联邦医疗保健计划之外。此外,就联邦《虚假申报法》(下文讨论)而言,包括因违反联邦《反回扣条例》而产生的物品或服务的索赔构成虚假或欺诈性索赔。此外,几个州也有类似的州级反回扣法规。
联邦虚假索赔和民事金钱惩罚法,包括《虚假索赔法》,施加了重大处罚,可由普通公民通过民事诉讼强制执行,禁止任何个人或实体故意向联邦政府提交或导致提交虚假或欺诈性的付款或批准索赔,包括联邦医疗保险和医疗补助等联邦医疗保健计划,故意制作、使用或导致制作或使用与向联邦政府的虚假或欺诈性索赔有关的虚假记录或陈述,或故意作出虚假陈述以不正当方式避免,减少或隐瞒向联邦政府支付金钱的义务。索赔包括对提交给美国政府的金钱或财产的“任何请求或要求”。例如,从历史上看,制药和其他医疗保健公司根据这些法律被起诉,因为它们被指控向客户免费提供产品,并期望客户向联邦政府收取账单。
41
目录表
产品的计划。其他公司也被起诉,因为这些公司营销产品用于未经批准的、标签外的用途,因此通常是不报销的,从而导致提交虚假声明。违反联邦民事虚假索赔法案的处罚可能包括高达政府实际损害赔偿的三倍,外加重大强制性民事处罚,以及被排除在联邦医疗保健计划之外。
HIPAA制定了额外的联邦刑法,除其他事项外,禁止故意和故意执行或试图执行计划,以虚假或欺诈性的借口、陈述或承诺的方式诈骗或获取任何医疗福利计划(包括私人第三方付款人)拥有或控制或保管的任何金钱或财产,故意阻碍对医疗违规行为的刑事调查,以及明知和故意通过诡计、计划或装置、重大事实或作出任何与提供或支付医疗福利、项目或服务有关的重大虚假、虚构或欺诈性陈述。与反回扣法规一样,HIPAA下某些医疗欺诈法规的意图标准不需要实际了解法规或违反法规的特定意图才能实施违规。
我们可能会受到联邦政府和我们开展业务所在州的数据隐私和安全法规的约束。经《健康信息技术促进经济和临床健康法》(“HITECH”)及其实施条例修订的HIPAA对个人可识别健康信息的隐私、安全和传输提出了要求。除其他事项外,HITECH使HIPAA的隐私和安全标准直接适用于商业伙伴,即创建、接收、维护或传输与代表覆盖实体及其覆盖分包商提供服务相关的受保护健康信息的独立承包商或覆盖实体的代理。HITECH还创建了四个新的民事罚款等级,修订了HIPAA,使民事和刑事处罚直接适用于商业伙伴,并赋予州总检察长新的权力,可以向联邦法院提起民事诉讼,要求损害赔偿或禁制令,以执行HIPAA,并寻求与提起联邦民事诉讼相关的律师费和费用。此外,许多州法律在特定情况下管理健康信息的隐私和安全,其中许多法律在很大程度上彼此不同,往往没有被HIPAA先发制人,可能具有比HIPAA更具禁止性的效果,从而使合规工作复杂化。
此外,联邦《医生支付阳光法案》及其实施条例要求,在Medicare、Medicaid或儿童健康保险计划(某些例外情况除外)下可以获得付款的某些药品、器械、生物和医疗用品制造商每年向CMS报告与向医生(定义为包括医生、牙医、验光师、足科医生和脊椎按摩师)和教学医院,或应其请求或代表其要求或代表其指定的实体或个人支付或分配给医生(定义为包括医生、牙医、验光师、足科医生和脊椎按摩师)的某些付款或其他价值转移有关的信息。医生和教学医院,并每年报告医生及其直系亲属持有的某些所有权和投资权益。如果报道不准确,可能会受到处罚。从2022年开始,适用的制造商还将被要求报告有关前一年向医生助理、护士执业人员、临床护士专家、麻醉师助理、注册护士麻醉师和注册助产士支付和转移价值的此类信息。此外,许多州都有类似于上述联邦法律的法规或法规,这些法规或法规的范围可能更广,可能适用于任何付款人。我们还可能受到州法律的约束,州法律要求制药公司遵守制药行业的自愿合规指南和联邦政府颁布的相关合规指南,和/或州法律要求药品制造商报告与向医生和其他医疗保健提供者支付和其他价值转移、药品定价或营销支出有关的信息。这些法律可能在很大程度上彼此不同,从而使遵约工作进一步复杂化。另外, 如果我们在国外有业务运营或在其他国家和司法管辖区销售我们的任何产品,包括加拿大或欧盟,我们可能会受到额外的监管。
有朝一日,我们可能会开发出一种产品,一旦获得批准,就可以由医生进行管理。根据当前适用的美国法律,某些通常不是自行给药的产品(包括注射药物)可能有资格通过Medicare B部分享受Medicare的保险。Medicare B部分是原始Medicare的一部分,原始Medicare是为老年人和残疾人提供医疗福利的联邦医疗计划,涵盖门诊服务和用品,包括某些对治疗受益人的健康状况是医学上必要的生物制药产品。作为制造商合格药品获得联邦医疗保险B部分报销的条件之一,制造商必须参加其他政府医疗保健计划,包括医疗补助药品返点计划和340B药品定价计划。医疗补助药品退税计划要求制药商与卫生与公众服务部部长签订并生效一项全国性退税协议,作为各州获得联邦匹配资金的条件,用于制造商向医疗补助患者提供的门诊药物。根据340B药品定价计划,制造商必须将折扣扩大到参与该计划的实体。
此外,许多制药商必须计算并向政府报告某些价格报告指标,如平均销售价格和最佳价格。在某些情况下,当这些指标没有准确和及时地提交时,可能会适用处罚。此外,这些药品的价格可能会通过政府医疗保健计划或私人付款人要求的强制性折扣或回扣,以及未来法律的任何放松来降低,这些法律目前限制从销售价格低于美国的国家进口药品。很难预测未来联邦医疗保险覆盖范围和报销政策将如何应用于我们的产品
42
目录表
而且,不同联邦医疗计划的覆盖范围和报销情况并不总是一致的。联邦医疗保险报销率还可能反映出对联邦医疗保险计划施加的预算限制。
为了以商业方式分销产品,我们必须遵守州法律,该法律要求对一个州的药品制造商和批发商进行登记,包括在某些州将产品运往该州的制造商和经销商,即使这些制造商或经销商在该州没有营业地点。联邦政府和一些州还要求制造商和分销商保留有关分销链中产品历史的记录。联邦法律要求制造商向后续供应链合作伙伴提供产品跟踪信息。DSCSA管理着某些处方药在美国分销时的追踪系统。DSCSA的目标是保护消费者免受可能是假冒、受污染、被盗或掺假的药品的影响。法律要求制造商在每次药品所有权转让之前或在每次转让时,向随后的所有者提供交易历史、交易信息和交易对账单。在召回或询问潜在非法产品的情况下,制造商必须能够提供有关其产品的交易历史和交易信息的信息。违反DSCSA的行为可能会导致罚款或监禁。此外,许多州对制造商进行监管,并强制执行记录保存和许可证要求。
几个州已经颁布了立法,要求制药和生物技术公司建立营销合规计划,向州政府提交定期报告,定期公开销售、营销、定价、临床试验和其他活动,和/或注册其销售代表,并禁止药店和其他医疗保健实体向制药和生物技术公司提供某些医生处方数据用于销售和营销,并禁止某些其他销售和营销行为。我们的所有活动都可能受到联邦和州消费者保护以及不正当竞争法律的约束。
确保与第三方的业务安排符合适用的医疗法律和法规是一项代价高昂的努力。如果我们的业务被发现违反了上述任何联邦和州医疗保健法律或任何其他当前或未来适用于我们的政府法规,我们可能会受到惩罚,包括但不限于民事、刑事和/或行政上的重大处罚、损害赔偿、罚款、交还、监禁、被排除在政府计划之外,如Medicare和Medicaid、禁令、由个人举报人以政府名义提起的私人诉讼,或拒绝允许我们签订政府合同、合同损害、声誉损害、行政负担、利润减少和未来收入,如果我们受到公司诚信协议或其他协议的约束,以解决有关不遵守这些法律的指控,以及我们业务的缩减或重组,则需要承担额外的报告义务和监督,任何这些都可能对我们的业务运营能力和我们的运营结果产生不利影响。
承保范围、定价和报销
对于我们可能获得监管批准的任何候选药物的覆盖范围和报销状态,存在很大的不确定性。在美国和国外市场,我们获得监管部门批准进行商业销售的任何产品的销售,在一定程度上将取决于第三方付款人为此类产品提供保险的程度和建立足够的补偿水平。在美国,第三方付款人包括联邦和州医疗保健计划、私人管理的医疗保健提供者、医疗保险公司和其他组织。政府医疗保健计划(如美国的联邦医疗保险和医疗补助)和商业支付者的充分覆盖和报销对于新产品的接受度至关重要。
我们成功地将任何产品商业化的能力还将在一定程度上取决于第三方付款人为这些产品和相关治疗提供保险和补偿的程度,第三方付款人决定他们将支付哪些治疗费用并建立补偿水平。第三方付款人的承保范围和报销可能取决于许多因素,包括第三方付款人对使用治疗性药物的决定:
我们不能确保我们商业化的任何产品都有保险或报销,如果有保险和报销,报销水平是多少。覆盖范围也可能比FDA或类似的外国监管机构批准该产品的目的更有限。报销可能会影响我们获得监管部门批准的任何产品的需求或价格。
43
目录表
第三方付款人除了质疑医疗产品、治疗和服务的安全性和有效性外,还越来越多地挑战价格,检查医疗必要性,审查成本效益。为我们的产品获得报销可能特别困难,因为品牌药物和在医生监督下使用的药物往往价格较高。我们可能需要进行昂贵的药物经济学研究,以证明我们产品的医疗必要性和成本效益,以及获得FDA批准所需的成本。我们的候选药物可能不被付款人认为是医学上必要的或具有成本效益的。从政府或其他第三方付款人那里获得产品的承保和报销批准是一个既耗时又昂贵的过程,这可能需要我们向每个付款人提供支持科学、临床和成本效益的数据,以便在逐个付款人的基础上使用我们的产品,但不能保证获得保险和足够的报销。付款人决定为产品提供保险并不意味着将批准足够的偿还率。此外,一个付款人决定为一种产品提供保险并不能保证其他付款人也会为该产品提供保险。可能无法获得足够的第三方报销,使我们能够维持足够的价格水平,以实现其在产品开发方面的投资的适当回报。如果无法获得报销或仅在有限的水平上获得报销,我们可能无法成功将我们成功开发的任何候选药物商业化。
其他国家也有不同的定价和报销方案。例如,在欧盟,各国政府通过其定价和报销规则以及对国家医疗体系的控制来影响生物制药产品的价格,这些体系为消费者支付了生物制药产品的大部分成本。一些法域实行正面清单和负面清单制度,只有在商定了补偿价格后,才能销售产品。为了获得报销或定价批准,其中一些国家可能要求完成临床试验,将特定候选药物的成本效益与目前可用的疗法进行比较。其他成员国允许公司制定自己的药品价格,但监控公司的利润。医疗成本的下行压力变得很大。因此,对新产品的进入设置了越来越高的壁垒。此外,在一些国家,来自低价市场的跨境进口对一国国内的定价施加了商业压力。
如果政府和第三方付款人不能提供足够的保险和补偿,我们获得监管部门批准用于商业销售的任何候选药物的适销性可能会受到影响。此外,美国的政治和经济压力以及立法变化增加了药品定价的压力,我们预计这种压力将继续增加。医疗费用普遍上涨,特别是处方药、医疗器械和外科手术程序等治疗费用上涨的下行压力变得非常大。承保政策和第三方报销费率可能随时发生变化。即使我们获得监管部门批准的一个或多个产品获得了有利的承保和报销状态,未来也可能实施不太有利的承保政策和报销费率。
医疗改革
在美国和一些外国司法管辖区,已经并将继续有关于医疗保健系统的几项立法和监管改革和拟议的改革,这些改革可能会阻止或推迟候选药物的上市批准,限制或规范批准后的活动,并影响获得上市批准的候选药物的有利可图销售的能力。在美国和其他地方的政策制定者和支付者中,有很大的兴趣推动医疗系统的改革,其既定目标是控制医疗成本、提高质量和/或扩大准入。在美国,制药业一直是这些努力的重点,并受到重大立法倡议的重大影响。
《平价医疗法案》的一些条款尚未实施,《平价医疗法案》的某些方面受到了法律和政治挑战。例如,2021年6月17日,美国最高法院驳回了一项基于程序理由的挑战,该挑战辩称,《平价医疗法案》整体违宪,因为“个人授权”已被国会废除。因此,《平价医疗法案》将以目前的形式继续有效。此外,在美国最高法院做出裁决之前,拜登总统于2021年1月28日发布了一项行政命令,启动了一个特殊的投保期,目的是通过平价医疗法案市场获得医疗保险,该市场从2021年2月15日开始,一直开放到2021年8月15日。行政命令还指示某些政府机构审查和重新考虑限制获得医疗保健的现有政策和规则,包括重新审查医疗补助示范项目和豁免计划,包括工作要求,以及通过医疗补助或《平价医疗法案》为获得医疗保险造成不必要障碍的政策。《平价医疗法案》有可能在未来受到司法或国会的挑战。目前尚不清楚任何此类挑战和拜登政府的医疗改革措施将如何影响《平价医疗法案》和我们的业务。
可能会通过进一步的立法或监管,可能会损害我们的业务、财务状况和运营结果。自《平价医疗法》颁布以来,还提出并通过了其他立法修改。例如,2011年8月,奥巴马总统签署了《2011年预算控制法案》,其中包括对医疗保险提供者支付的每一财年2%的总减幅,该法案从2013年4月1日开始生效,除非国会采取进一步行动,否则将一直有效到2030年。然而,新冠肺炎的救济立法从5月1日起暂停了2%的联邦医疗保险自动减支,
44
目录表
2020年至2021年12月31日。2013年1月,《2012年美国纳税人救济法》签署成为法律,其中包括进一步减少了对包括医院、成像中心和癌症治疗中心在内的几类提供者的医疗保险支付,并将政府追回向提供者多付款项的诉讼时效从三年延长到五年。此外,2021年3月11日,拜登总统签署了《2021年美国救援计划法案》,从2024年1月1日起,取消了针对单一来源和创新多来源药物的法定医疗补助药品退税上限,目前该上限为药品平均制造商价格的100%。
此外,美国对特殊药品定价做法的立法和执法兴趣也越来越大。具体地说,美国国会最近进行了几次调查,并提出了一项联邦立法,旨在提高药品定价的透明度,降低联邦医疗保险下处方药的成本,审查定价与制造商患者计划之间的关系,以及改革政府计划的药品报销方法。国会表示,将继续寻求新的立法和/或行政措施来控制药品成本。此外,根据最近的一项行政命令,拜登政府表示打算采取某些政策举措来降低药品价格。作为对拜登行政命令的回应,2021年9月9日,HHS发布了一份应对高药价的综合计划,其中概述了药品定价改革的原则,并列出了国会可以采取的各种潜在立法政策,以及HHS可以采取的潜在行政行动来推进这些原则。尚未最后确定实施这些原则的立法或行政行动。此外,国会正在考虑将药品定价作为预算协调过程的一部分。美国个别州也越来越积极地通过立法和实施旨在控制生物制药产品定价的法规,包括价格或患者报销限制、折扣、对某些产品准入和营销成本披露的限制以及透明度措施,在某些情况下,旨在鼓励从其他国家进口和批量采购。
《反海外腐败法》
《反海外腐败法》禁止任何美国个人或企业直接或间接向任何外国官员、政党或候选人支付、提供或授权支付或提供任何有价值的东西,目的是影响外国实体的任何行为或决定,以帮助个人或企业获得或保留业务。《反海外腐败法》还要求证券在美国上市的公司遵守会计条款,这些条款要求我们保存准确和公平地反映公司(包括国际子公司)所有交易的账簿和记录,并为国际业务设计和维护适当的内部会计控制系统。
《就业法案》
我们符合《证券法》第2(A)(19)节所界定的“新兴成长型公司”的资格,该条款经《就业法案》修订。因此,只要我们继续是一家新兴成长型公司,我们就有资格并可能利用某些适用于其他非新兴成长型公司的上市公司的各种报告要求的豁免,包括(I)根据萨班斯-奥克斯利法案第404(B)条关于财务报告的内部控制的审计师认证要求的豁免,(Ii)豁免薪酬发言权、频率发言权和黄金降落伞投票要求,以及(Iii)在我们的定期报告和委托书中关于高管薪酬的披露义务减少。
我们将一直是一家新兴的成长型公司,直到:(I)财政年度的最后一天(A)托特纳姆收购第一有限公司(“托特纳姆”)首次公开募股结束五周年之后,(B)我们的年总收入至少为10.7亿美元,或(C)根据1934年《交易法》,我们被视为“大型加速申报公司”,如果截至我们最近完成的第二财季的最后一个营业日,非关联公司持有的我们普通股的市值超过7亿美元,就会发生这种情况;或(Ii)我们在之前三年期间发行了超过10亿美元的不可转换债务证券的日期。
此外,《就业法案》规定,新兴成长型公司可以利用延长的过渡期来遵守新的或修订后的会计准则。这允许新兴成长型公司推迟采用某些会计准则,直到这些准则适用于私营公司。我们已选择利用这一延长的过渡期,因此,我们可能会在非上市公司需要采用新的或修订的会计准则的相关日期采用该等准则,而不是其他上市公司所要求的日期。因此,我们的财务报表可能无法与截至上市公司生效日期遵守新的或修订的会计声明的公司进行比较。
较小的报告公司状态
我们也是一家“较小的报告公司”,因为截至2021年6月30日,我们非关联公司持有的股票市值不到7亿美元,在截至2021年12月31日的财年中,我们的年收入不到1亿美元。我们可以
45
目录表
在任何一年中,如果(I)在最近结束的财年中截至6月30日,非关联公司持有的我们股票的市值低于2.5亿美元,或(Ii)在最近结束的财年中,我们的年收入低于1亿美元,并且截至6月30日,非关联公司持有的我们股票的市值低于7亿美元,则在任何给定的年度内,我们仍是一家规模较小的报告公司。如果我们是一家较小的报告公司,当我们不再是一家新兴的成长型公司时,我们可能会继续依赖较小的报告公司可以获得的某些披露要求的豁免。具体地说,作为一家较小的报告公司,我们可能会选择在我们的Form 10-K年度报告中只公布最近两个财政年度的经审计财务报表,与新兴成长型公司类似,较小的报告公司减少了有关高管薪酬的披露义务。
附加法规
除上述规定外,有关环境保护和有害物质的州和联邦法律,包括《职业安全与健康法》、《资源保护与回收法》和《有毒物质控制法》,都会影响我们的业务。这些法律和其他法律规范了我们对各种生物和化学物质的使用、处理和处置,这些物质和化学物质用于我们的业务,以及由我们的业务产生的废物。如果我们的运营导致环境污染或使个人暴露在危险物质中,我们可能会承担损害赔偿和政府罚款的责任。我们相信,我们在实质上遵守了适用的环境法律,继续遵守这些法律不会对我们的业务产生实质性的不利影响。然而,我们无法预测这些法律的变化可能会如何影响我们未来的运营。
其他规例
我们还受到许多联邦、州和地方法律的约束,这些法律涉及安全工作条件、制造实践、环境保护、火灾危险控制和危险或潜在危险物质的处置。我们现在或将来遵守这些法律和法规可能会产生巨大的成本。
员工与人力资本资源
截至2021年12月31日,我们共有102名员工,其中95人是全职员工,主要分布在犹他州和马里兰州。下表按角色列出了我们的员工:
部门 |
|
员工人数 |
|
|
占总数的百分比 |
|
||
制造业 |
|
|
37 |
|
|
|
35 |
% |
临床 |
|
|
11 |
|
|
|
11 |
% |
质量控制与生物分析 |
|
|
11 |
|
|
|
11 |
% |
微生物学实验室 |
|
|
8 |
|
|
|
8 |
% |
研究与开发 |
|
|
7 |
|
|
|
7 |
% |
高级管理层 |
|
|
7 |
|
|
|
7 |
% |
质量保证 |
|
|
8 |
|
|
|
8 |
% |
金融 |
|
|
5 |
|
|
|
5 |
% |
人力资源 |
|
|
4 |
|
|
|
4 |
% |
资讯科技 |
|
|
1 |
|
|
|
1 |
% |
营销 |
|
|
3 |
|
|
|
3 |
% |
总计 |
|
|
102 |
|
|
|
100 |
% |
我们的员工没有工会代表,也没有集体谈判协议的覆盖范围,我们相信我们与员工的关系很好。
我们的人力资本资源目标包括,如适用,识别、招聘、留住、激励和整合我们现有的和更多的员工。我们股权激励计划的主要目的是通过授予基于股票的薪酬奖励和基于现金的绩效奖金奖励来吸引、留住和激励选定的员工、顾问和董事。
企业信息
我们主要执行办公室的邮寄地址是犹他州盐湖城G50套房南米罗克大道6550号,邮编是84121,我们的电话号码是(801)6769695。我们的网站地址是Https://clene.com。本公司网站所载或可从本公司网站取得的资料并未纳入本年度报告内,阁下不应将其视为本年度报告的一部分。我们在本年度报告中包括我们的网站地址,仅作为不活跃的文本参考。
46
目录表
第1A项。风险因素主因子
投资我们的证券涉及高度风险。在决定是否投资我们的证券之前,您应仔细考虑以下描述的风险和不确定性,以及本年度报告中的其他信息,包括我们的综合财务报表和相关说明以及“管理层对财务状况和经营结果的讨论和分析”。这些风险因素中描述的一个或多个事件或情况的发生,单独或与其他事件或情况结合在一起,可能会对我们的业务、声誉、收入、财务状况、运营结果和未来前景产生重大不利影响,在这种情况下,我们普通股的市场价格可能会下跌,您可能会损失部分或全部投资。上文概述和下文所述的风险和不确定性并非详尽无遗,也不是我们面临的唯一风险和不确定性。我们目前不知道或我们目前认为无关紧要的其他风险和不确定性也可能损害我们的业务运营。本年度报告还包含涉及风险和不确定因素的前瞻性陈述,请参阅“有关前瞻性陈述的警示说明”。由于多种因素,包括下面描述的风险,我们的实际结果可能与我们的预期结果大不相同。
与我们的商业和工业有关的风险
我们在很大程度上依赖于我们候选药物在未来的成功商业化,这可能无法实现或可能经历重大延误。
作为一家新的生物制药企业,我们目前没有任何可用于商业销售的药物,也没有任何已被监管部门批准销售的药物。我们已经投入了大量的精力和财力来研发我们的主要候选药物CNM-Au8®,一种催化活性的金纳米晶体悬浮液,在早期研究中已显示出治疗ALS、MS和PD患者的潜力。我们在未来创造收入和盈利的能力在很大程度上取决于CNM-Au8产生的未来销售额®以及我们的候选药物,这反过来又取决于我们目前正在临床开发的治疗神经疾病患者的候选药物的成功研发、监管批准、商业化和销售。我们还在基于我们的技术开发尚未进入人体试验的新药。我们候选药物的最终成功取决于我们实现某些里程碑,包括但不限于:
如果我们不能及时实现这些里程碑中的一个或多个,或者根本不能实现,我们可能会在获得候选药物的批准和/或成功将其商业化方面遇到重大延误,这将对我们的业务造成实质性损害,我们可能无法产生足够的收入和现金流来继续运营。
即使我们能够从未来任何候选药物的销售中获得收入,我们也可能无法盈利,可能需要获得额外的资金才能继续运营。任何所需的资金可能不会以优惠条款提供,或者根本不会。如果我们无法实现盈利或无法持续盈利,那么我们可能无法继续按计划运营,并可能被迫减少运营。即使我们确实实现了盈利,我们也可能无法维持或提高季度或年度的盈利能力。我们未能实现并保持盈利将显著降低我们的价值,并可能削弱我们筹集资金、扩大业务或继续运营的能力,这反过来可能对我们的业务、财务状况和运营结果产生不利影响。
47
目录表
我们目前没有从候选药物的商业销售中产生任何收入,我们可能不会像预期的那样盈利,或者根本不会盈利。
我们的主要业务是研发,如果成功,还可以销售候选药物。由于我们所有的候选药物仍处于研究和开发阶段,我们目前没有从销售候选药物中获得收入,我们记录了持续的重大净亏损。我们产生了与膳食(矿物质)补充剂供应协议相关的微不足道的收入;然而,这些收入预计不会对我们未来的收入产生实质性贡献。如果由于未能完成临床试验、获得监管批准、进行商业规模生产或任何其他原因,我们未能按计划将我们的候选药物商业化,我们可能会在通过商业销售我们的候选药物产生收入和实现利润方面遇到重大延误或失败。
此外,我们预计未来将产生巨大的成本,特别是在研究和开发以及我们候选药物的商业化方面。截至2021年12月31日和2020年12月31日的年度,研发支出总额分别为2840万美元和1520万美元。随着目前正在进行临床前研究的候选药物进入临床试验阶段,与这些候选药物相关的成本可能会显著增加。未来,随着我们将更多的候选药物进入临床试验阶段,对商业化产品进行更多的临床试验以扩大其用途,并对我们的候选药物进行商业化生产,与此类操作相关的成本可能会大幅增加。
当我们在竞争激烈的制药市场运营时,我们争先于竞争对手将我们的候选药物商业化,这给我们带来了产生研发和其他费用的压力,这可能会对我们的盈利能力产生负面影响。另一方面,如果我们的商业化候选药物获得批准,可能会由于竞争、市场需求不足、产品缺陷或任何其他原因而无法实现其销售潜力。因此,即使我们未来开始从商业化候选药物的销售中获得收入,我们可能在很长一段时间内仍不会盈利,或者根本不会盈利。
自成立以来,我们已经发生了重大的净亏损和净运营现金流出,预计在可预见的未来将继续出现重大的净亏损。
对生物制药药物开发的投资具有很高的投机性。它需要大量的前期资本支出和巨大的风险,即候选药物可能无法获得监管部门的批准或在商业上可行。我们继续产生与我们正在进行的业务相关的巨额费用。自成立以来,我们已经蒙受了巨大的损失。截至2021年12月31日及2020年12月31日止年度,本公司录得营运亏损5,000万美元及2,020万美元,截至2021年12月31日及2020年12月31日止年度分别录得净亏损970万美元及1,930万美元。截至2021年12月31日,我们的累计赤字为1.633亿美元。具体内容见《管理层对财务状况和经营成果的讨论与分析》。我们几乎所有的运营亏损都是由于与我们的研发计划相关的成本和与我们的运营相关的行政费用造成的,我们预计未来我们的研发费用将继续增加。
我们预计在可预见的未来将继续遭受亏损,随着我们继续扩大我们的候选药物的开发并寻求监管部门的批准,以及我们继续建立我们的商业化和销售队伍,以预期我们的晚期候选药物可能在未来推出,我们预计这些损失将会增加。通常情况下,一种新药从药物发现阶段到可用于治疗患者需要许多年的时间。此外,我们将继续产生与上市公司运营相关的成本,并支持我们作为发展阶段或商业阶段的制药公司的发展。我们未来净亏损的规模将在一定程度上取决于我们药物开发计划的数量和范围以及这些计划的相关成本、任何经批准的产品的商业化成本、我们产生收入的能力以及我们通过与第三方的安排支付或收到的里程碑和其他付款的时间和金额。如果我们的任何候选药物在临床试验中失败,或者没有获得监管部门的批准,或者如果获得批准,未能获得市场接受,我们可能永远不会盈利。如果我们不能实现并保持盈利,我们的价值将大幅下降,并削弱我们筹集资金、保持研发努力、扩大业务或继续运营的能力。
我们继续经营下去的能力要求我们获得足够的资金来资助我们的运营,这些资金可能无法以可接受的条件获得,或者根本无法获得。如果不能在需要时获得这一必要的资本,可能会迫使我们推迟、限制、减少或终止我们的药物开发或商业化努力。
截至2021年12月31日,我们的现金和限制性现金总额为5030万美元,累计赤字为1.633亿美元。在截至2021年12月31日和2020年12月31日的年度内,我们在运营活动中使用的现金净额分别为3460万美元和1890万美元。在可预见的未来,我们预计在经营活动中将继续出现亏损并使用现金。具体内容请参见《管理层对财务状况和经营成果的讨论与分析--流动性与资本资源》。我们的长期运营需要获得额外的资本来为我们的运营提供资金。作为我们正在进行的业务计划的一部分,我们将继续寻求通过股权融资筹集额外资本,并可能寻求债务融资或其他资本来源,我们可能会尝试
48
目录表
与第三方合作开发我们的候选药物并将其商业化。我们可能无法以可接受的条件获得资本,或者根本无法获得资本。任何融资条款都可能对我们股东的持股或权利产生不利影响。根据我们当前业务计划的结果,我们可能需要实施成本节约措施,包括可能推迟或减少研发计划和商业化努力,最早将于2022年第三季度开始。目前,在没有额外资本的情况下,我们相信我们有足够的资源为我们持续运营到2023年第二季度提供资金。除其他因素外,这些因素可能会令人对我们继续经营下去的能力产生极大的怀疑。
我们的经营历史有限,这可能会使我们很难评估目前的业务和预测我们未来的业绩。
我们是一家成立于2012年12月的生物制药公司,专注于发现和开发治疗神经疾病和其他疾病的创新药物。我们有限的运营历史,特别是考虑到纳米晶体疗法领域的快速发展,可能会使我们很难评估我们目前的业务和预测我们未来的业绩。
对生物制药产品开发的投资具有很高的投机性,因为它需要大量的前期资本支出,并存在重大风险,即任何潜在的候选药物将无法证明足够的疗效或可接受的安全性,无法获得监管部门的批准,无法在商业上可行。作为一项相对较新的业务,我们还没有表现出有能力以商业规模制造药物,没有能力安排第三方代表我们这样做,也没有能力进行成功商业化所需的销售和营销活动。我们没有任何产品被批准用于商业销售,也没有从产品销售中获得任何收入。此外,作为一家经营历史有限的企业,我们可能会遇到早期生物制药公司在快速发展的领域经常遇到的不可预见的费用、困难、并发症、延误等已知和未知的因素和风险。因此,您对我们目前的业务或未来的成功或生存能力所做的任何评估,都可能不像我们有更长的运营历史并能够减少上述一些不确定性时那样准确。此外,我们有限的财务记录,尚未从我们预期的未来主要业务中获得任何收入,对您评估我们的业务可能具有有限的参考价值。
我们可能会在成功管理我们的增长和扩大业务方面遇到困难,这可能会对我们的业务、财务状况、运营结果和前景产生不利影响。
随着我们寻求通过临床试验推进我们的候选药物,我们将需要扩大我们的开发、监管、合规、制造、营销和销售能力,或者与第三方签订合同,为我们提供这些能力。随着我们业务的扩大,我们预计将需要管理与各种战略合作伙伴、供应商和其他第三方的更多关系。未来的增长将给我们的管理层成员带来巨大的额外责任。我们未来的财务业绩以及我们将候选药物商业化并有效竞争的能力,在一定程度上将取决于我们有效管理未来任何增长的能力。为此,我们必须能够有效地管理我们的开发工作和临床试验,并招聘、培训和整合更多的临床、监管、制造、财务、法律、管理、行政以及销售和营销人员。我们可能无法完成这些任务,如果我们不能完成其中任何一项任务,可能会阻碍我们的成功增长,并可能损害我们的业务、财务状况、运营结果和前景。
政府法规或与制药和生物技术行业相关的做法的变化,包括潜在的医疗改革,可能会减少对我们的候选药物的需求,或者使我们的候选药物获得监管批准并将其商业化变得更加困难。
近年来,美国国会、总统、行政部门和州立法机构考虑了各种类型的医疗改革,以控制不断增长的医疗成本。类似的改革运动也发生在欧洲和亚洲的部分地区。医疗改革立法还可能增加药物开发和商业化的成本,或者限制上市药物的报销,这可能会限制新药开发的利润。这可能会对制药和生物技术公司的研发支出产生不利影响,进而可能减少我们在美国和其他国家的商机。我们无法预测未来会采纳什么改革建议,如果有的话。
如果我们或我们可能聘用的任何CRO未能遵守环境、健康和安全法律法规,我们可能会受到罚款或处罚,或产生可能对我们的业务、财务状况、运营结果和前景产生重大不利影响的成本。
我们和某些与我们签约的第三方,如我们的第三方CRO,受到许多环境、健康和安全法律法规的约束,包括管理实验室程序以及危险材料和废物的处理、使用、储存、处理和处置的法律法规。此外,我们未来的建设项目可能需要与负责环境保护、健康和安全的有关行政部门完成一些监管程序,才能投入运营。我们的行动涉及使用危险和易燃材料,包括化学品和生物材料。我们的业务还会产生危险废物产品。我们通常与第三方签订合同,处理这些材料,并
49
目录表
浪费。我们不能完全消除这些材料造成污染或伤害的风险。如果我们使用危险材料造成污染或伤害,我们可能要对由此造成的任何损害负责,任何责任都可能超出我们的资源范围。
虽然我们维持工人补偿保险,以支付因使用或接触危险材料而导致员工受伤的成本和费用,但该保险可能不能提供足够的保险来应对潜在的责任。我们不为可能因我们储存、使用或处置生物或危险材料而对我们提出的环境责任或有毒侵权索赔维持保险。
此外,适用于我们和我们的第三方承包商的环境、健康和安全法律法规可能会发生变化,并在未来提出更严格的要求。因此,我们可能需要支付巨额费用来遵守未来的环境、健康和安全法律法规。这些现行或未来的法律法规可能会损害我们的研究、开发或生产努力。不遵守这些法律法规也可能导致巨额罚款、处罚或其他制裁,这可能会对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。
我们的内部计算机系统,或我们可能聘请的任何CRO或其他第三方承包商或顾问使用的系统,可能会出现故障或遭遇安全漏洞。
尽管实施了安全措施,但我们的内部计算机系统以及我们的CRO和其他承包商和顾问的计算机系统很容易受到计算机病毒和未经授权访问的破坏。尽管据我们所知,到目前为止,我们还没有经历过任何重大的系统故障或安全漏洞,但如果发生这样的事件并导致我们的运营中断,可能会导致我们的开发计划和业务运营的重大中断。
在我们的正常业务过程中,我们收集和存储敏感数据,其中包括受法律保护的患者健康信息、员工的个人身份信息、知识产权和专有业务信息。我们利用现场系统和外包供应商来管理和维护我们的应用程序和数据。这些应用程序和数据包含各种业务关键型信息,包括研发信息、商业信息以及商业和金融信息。由于信息系统、网络和其他技术对我们的许多运营活动至关重要,我们的系统或向我们提供信息系统、网络或其他服务的供应商的系统关闭或服务中断会带来越来越大的风险。此类中断可能是由以下事件引起的:计算机黑客攻击、网络钓鱼攻击、勒索软件、传播计算机病毒、蠕虫和其他破坏性或破坏性软件、拒绝服务攻击和其他恶意活动,以及由我们的员工、承包商、顾问、业务合作伙伴和/或其他第三方的疏忽或故意行为(如错误或盗窃)、供应链攻击、停电、自然灾害(包括极端天气)、恐怖袭击或其他类似事件造成的安全事件。此类事件可能会对我们和我们的业务产生不利影响,包括数据丢失和设备和数据损坏。此外,系统冗余可能无效或不足,我们的灾难恢复规划可能不足以涵盖所有可能发生的情况。重大事件可能导致我们的运营中断、声誉受损或收入损失。此外,我们可能没有足够的保险范围来补偿与此类事件相关的任何损失。
我们可能会面临因盗用、误用、泄露、篡改或故意或意外泄露或丢失我们和供应商的信息系统和网络中维护的信息(包括员工和患者的个人信息以及公司和供应商的机密数据)而导致的风险。此外,外部各方可能试图渗透我们或我们供应商的系统,或以欺诈手段诱使我们的人员或我们供应商的人员披露敏感信息,以便访问我们的数据和/或系统。与其他公司一样,我们的数据和系统有时会受到威胁,今后也会继续受到威胁,包括恶意代码和病毒、网络钓鱼和其他网络攻击。随着时间的推移,这些威胁的数量和复杂性不断增加。如果我们的信息技术系统或供应商的信息技术系统发生重大破坏,市场对我们安全措施有效性的看法可能会受到损害,我们的声誉和信誉可能会受到损害。我们可能需要花费大量的资金和其他资源来修复或更换信息系统或网络。
此外,尽管我们作出了努力,但不能完全消除发生这些事件的可能性。随着我们将更多的信息系统外包给供应商,与付款人和患者进行更多的电子交易,以及更多地依赖基于云的信息系统,相关的安全风险将会增加,我们将需要花费额外的资源来保护我们的技术和信息系统。
我们还可能被要求遵守法律、法规、规则、行业标准和其他要求我们维护个人数据安全的法律义务。我们还可能有合同和其他法律义务将安全事件通知客户、合作者或其他相关利益相关者。如果不能预防或减轻网络攻击,可能会导致未经授权访问数据,包括专有和个人信息。大多数司法管辖区都制定了法律,要求公司在涉及某些类型的数据的安全漏洞时通知个人、监管机构和其他人。这样的披露代价高昂,可能导致负面影响
50
目录表
宣传,可能会导致我们的客户或合作伙伴或其他相关利益相关者对我们的安全措施的有效性失去信心,并要求我们花费大量资本和其他资源来应对和/或缓解实际或预期的安全事件所造成的问题。此外,应对网络安全事件或缓解任何已发现的安全漏洞的成本可能会很高,包括补救此类事件的影响、支付赎金、从备份中恢复数据以及执行数据分析以确定哪些数据可能受到攻击的成本。此外,我们控制或补救安全事件或任何被利用来导致事件的漏洞的努力可能不会成功,而控制或补救它们的努力和任何相关失败可能会导致中断、延迟、损害我们的声誉,并增加我们的保险覆盖范围。
此外,安全漏洞导致的监管响应或诉讼可能会对我们的业务产生不利影响。未经授权访问我们的信息技术系统可能会导致与我们的客户、合作者或其他相关利益相关者提起诉讼,或政府实体采取监管行动。这些诉讼可能迫使我们花费金钱进行辩护或和解,分散管理层的时间和注意力,增加我们的经营成本,或对我们的声誉造成不利影响。我们可能被要求从根本上改变我们的业务活动和做法,以应对此类诉讼,这可能会对我们的业务产生不利影响。如果发生安全漏洞,并且我们的数据或我们的合作者的数据的保密性、完整性或可用性被破坏,我们可能会招致重大责任,这可能会对我们的业务产生负面影响,并损害我们的声誉。
此外,我们的保险可能不足以覆盖与此类事件相关的损失,而且在任何情况下,此类保险可能不包括我们因应对和补救安全漏洞而可能招致的所有类型的成本、费用或根本不包括损失。如果对我们提出的一项或多项超出我们可用保险范围的大额索赔获得成功,或导致我们的保单发生变化(包括增加保费或实施大额免赔额或共同保险要求),可能会对我们的业务产生不利影响。此外,我们不能确定我们现有的保险范围和错误和遗漏保险将继续以可接受的条款提供,或者我们的保险公司不会拒绝未来的任何索赔。
我们自己制造我们所有的候选药物,并打算自己制造大多数(如果不是全部)任何已批准的药物,这可能会对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。
我们目前在美国有制造设施,并可能在其他市场建立更多的制造设施,以扩大我们的制造能力。由于许多因素,包括监管要求,这些设施可能会遇到意想不到的延误和费用。如果我们的新设施的建设、监管评估和/或审批被推迟,如果获得批准,我们可能无法生产足够数量的候选药物,这将限制我们的开发和商业化活动以及我们的增长机会。与建造或维护我们的设施相关的成本超支可能需要我们从其他来源筹集额外资金,这些资金可能不会以优惠的条件提供,或者根本不能获得。
我们制造过程中使用的许多设备都是我们开发和制造的,在短时间内购买或制造合适的替代品将是困难的,甚至是不可能的。此外,对于这些设备中的大部分,我们没有足够数量的备件或没有备件可用。如果某些设备损坏、丢失或无法使用,我们将不得不建造新的部件,这可能需要相当长的时间,导致我们至少部分生产作业暂时停止。此外,我们不断寻求进一步微调和发展我们的先进制造技术和工艺控制,以充分利用我们的设施。制造技术的进步可能会使我们的设施和设备不足,在这种情况下,我们可能会失去任何竞争优势。
为了使我们的候选药物的生产数量达到我们认为将满足预期市场需求所需的数量,如果获得批准,我们将需要在目前的生产水平上大幅增加或“扩大”生产过程。扩大规模过程的一个重要部分将包括寻找方法来提高我们生产过程的自动化和半自动化,这将需要额外的研发、投资、潜在的新监管批准以及与第三方的合作,其中一些可能不会成功。如果我们无法或延迟扩大规模,或者如果这样做的成本对我们来说在经济上不可行,我们可能无法生产足够数量的批准候选药物来满足未来的任何需求。
延迟完成和接受监管部门对我们制造设施的批准可能会推迟我们的开发计划或商业化努力,这可能会损害我们的业务。
我们的生产设施将接受各种监管机构的持续定期检查,包括FDA、EMA、中国国家医疗产品管理局(“NMPA”)、加拿大卫生部和澳大利亚治疗用品管理局(“TGA”)或其他类似监管机构,以确保符合GMP。如果我们不遵守并记录我们对GMP或其他法规要求的遵守,可能会导致临床或商业用途产品供应的重大延迟,并可能导致临床试验的终止或暂停,或者可能延迟或阻止提交或批准我们候选药物的上市申请或我们的药物的商业化(如果获得批准)。我们还可能在以下方面遇到问题:
51
目录表
不遵守适用的法规也可能导致对我们施加制裁,包括罚款、禁令、民事处罚、要求暂停或搁置我们的一项或多项临床试验、监管机构未能批准我们的候选药物上市、延迟、暂停或撤回批准、供应中断、执照吊销、扣押或召回我们的候选药物、运营限制以及民事或刑事起诉,任何这些都可能损害我们的业务。
损坏、破坏或中断我们制造设施的生产将对我们的业务和前景产生负面影响。
如果我们的制造设施或其中的设备被损坏或摧毁,我们可能无法迅速或廉价地更换我们的制造能力或根本无法更换。如果设施或设备暂时或长期丢失,我们可能无法将生产转移给第三方。即使我们可以将生产转移给第三方,转移也可能是昂贵和耗时的,特别是因为新工厂需要遵守必要的监管要求,而且我们在销售在新工厂生产的任何药物之前都需要监管机构的批准。如果我们的任何候选药物获得批准并成功商业化,这样的事件可能会推迟我们的临床试验或减少我们的产品销售。我们制造设施的任何制造操作中断都可能导致我们无法满足临床试验或商业化的要求。任何妨碍我们及时制造候选药物的能力的中断都可能对我们的业务、财务状况、运营结果和前景造成实质性损害。
目前,我们为我们的财产和设备提供保险,保险金额为我们认为合理的。然而,我们的保险覆盖范围可能不会报销我们,或者可能不足以报销我们可能遭受的任何费用或损失。如果发生灾难性事件或我们的制造设施或工艺出现故障,我们可能无法满足对候选药物的要求。
严重的通货膨胀可能会对我们的业务、财务状况和运营结果产生不利影响。
通货膨胀会增加我们的成本,包括工资成本,从而对我们产生不利影响。严重的通货膨胀往往伴随着更高的利率。通胀和利率的任何大幅上升都可能对我们的业务、财务状况和经营业绩产生重大不利影响。
我们未来的成功有赖于我们留住关键高管以及吸引、培训、留住和激励合格和高技能人才的能力。
我们高度依赖我们的联合创始人兼首席科学官Mark Mortenson、我们的首席执行官兼总裁Rob Etherington以及我们管理和科学团队的其他主要成员。我们不为我们的任何高管或其他员工提供“关键人物”保险。失去我们的任何高管、其他关键员工和其他科学顾问的服务,以及我们无法找到合适的替代者,可能会导致产品开发的延迟,并损害我们的业务。
未来招聘和留住合格的科学、技术、临床、制造、销售和营销人员也将是我们成功的关键。此外,我们依赖第三方顾问和顾问,包括科学和临床顾问,帮助我们制定我们的发现、临床开发、运营和商业化战略。失去高管或其他关键员工和顾问的服务可能会阻碍我们实现研发和商业化目标,并严重损害我们成功实施业务战略的能力。
我们从某些税收和财务激励中受益,这些激励措施到期或发生变化可能会对我们的盈利能力产生不利影响。
我们受益于某些税收待遇,以及与我们的研发成本相关的税收优惠。我们通过美国、澳大利亚和马里兰州的研发税收抵免获得可退还的税收抵免。在美国,研发抵免被用来抵消美国工资单上的联邦就业税。在澳大利亚,我们获得了43.5%的研发扣除额的可退税抵免。在马里兰州,我们获得了基础研究和开发费用3%的税收抵免,以符合条件的研发费用和马里兰州的基本金额为准,用于抵消州收入
52
目录表
税收,并可适用于随后几年的税收,直到使用抵免或抵免可结转七年。我们还在马里兰州享受州个人财产税和销售税的免税,以及马里兰州企业区招聘和创造就业的税收抵免。
此外,当前或未来适用于我们的税收待遇、税收优惠、税收优惠和财政奖励可能会因许多因素而改变、终止或以其他方式不可用,这些因素包括政府政策或相关政府当局的行政决定的变化。由于政府政策的潜在变化,我们不能确定未来我们将获得的政府拨款水平。我们的税后盈利能力和现金流可能会受到这些或其他因素中的一个或多个的不利影响。
我们利用净营业亏损来抵消未来应税收入的能力可能会受到一定的限制。
自成立以来,我们遭受了巨额亏损,预计不会在不久的将来实现盈利,如果有的话。在我们继续产生应税亏损的情况下,未使用的亏损将结转以抵消未来的应税收入(如果有的话)。截至2021年12月31日,我们有1.101亿美元的美国联邦净营业亏损(“NOL”)结转,可用于减少未来的应税收入,并有一个无限期的结转期,但其用途限于相当于年度应纳税所得额80%的年度扣减。此外,截至2021年12月31日,我们有7,710万美元的国家NOL结转,这些结转可能用于减少未来的应税收入,其中6,420万美元有无限期结转,而其余1,290万美元将在2032年后开始到期。截至2021年12月31日,我们还有260万美元的研发税收抵免结转,可用于减少未来的纳税义务,并在2032年后的不同日期到期。
根据经冠状病毒援助、救济和经济安全法案或CARE法案修订的美国联邦税收立法,通常被称为减税和就业法案(TCJA),在2017年12月31日之后的应税年度和未来应税年度发生的美国联邦NOL可以无限期结转,但此类美国联邦NOL在2020年12月31之后开始的应税年度产生的扣除是有限的。目前还不确定各州将如何回应TCJA和CARE法案。此外,根据修订后的1986年《国内税法》第382条和州法律的相应条款,如果一家公司在三年内经历了按价值计算其股权所有权发生超过50%的“所有权变更”,则该公司使用变更前的净资产结转和其他变更前的税收属性来抵消变更后的收入或税款的能力可能会受到限制。根据1986年《国税法》第382条的规定,任何未来发行的股权证券,以及自我们成立以来发生的其他交易,都可能引发这样的所有权变更。我们还没有进行一项研究,以评估是否发生了此类所有权变更。我们可能会经历所有权的变化,因为我们的股票所有权随后发生了变化,其中一些可能是我们无法控制的。如果所有权发生变化,我们使用NOL结转的能力受到实质性限制,这将损害我们的财务状况和运营结果,因为它实际上增加了我们未来的纳税义务。
税法的变化可能会对我们产生不利影响,美国国税局或法院可能不同意我们的纳税立场,这可能会对我们的财务状况或我们普通股的价值产生不利影响。
2017年12月22日颁布的TCJA对美国税法产生了重大影响,包括改变了美国对某些类型的企业收入征税的方式,并将美国联邦企业所得税税率降至21%。它还对一些税收优惠施加了新的限制,包括扣除或商业利息、使用净营业亏损结转、对外国收入征税和外国税收抵免等。
为应对新冠肺炎疫情,2020年3月27日颁布的《CARE法案》进一步修订了1986年的《国税法》,包括对TCJA所做的某些修改,一般是临时的。此外,国税局(“IRS”)尚未就TCJA和CARE法案所作更改的一些重要问题发布指导意见。在缺乏这种指导的情况下,我们将对一些悬而未决的问题采取立场。不能保证美国国税局或法院会同意我们的立场,在这种情况下,可能会征收可能对我们的业务、现金流或财务业绩产生不利影响的税收处罚和利息。
此外,本届政府可能会提议对美国税法进行重大修改,其中一些或全部可能会通过。这类立法的通过,以及对现有司法判决或国税局当前立场的改变或修改,可能会极大地改变本年度报告中所述的税务处理方式,可能会有追溯力。我们无法预测美国国会或任何其他立法机构是否会颁布新的税收立法,美国国税局或任何其他税务当局是否会发布新的法规或其他指导意见,也无法预测此类立法或法规可能对我们或我们的财务状况产生什么影响。不能保证未来税法的变化不会大幅提高企业所得税税率、对扣除、抵免或其他税收优惠施加新的限制,或做出可能对我们的业务、现金流或财务业绩产生不利影响的其他变化。
53
目录表
我们的财务状况和运营可能会受到新冠肺炎疫情的不利影响。
由新型冠状病毒SARS-CoV-2引起的呼吸道疾病新冠肺炎的暴发已在全球蔓延,导致许多国家的政府采取措施,通过隔离、严格的旅行限制、加强边境检查等措施来减缓疫情的传播。疫情的爆发和政府为应对新冠肺炎大流行而采取的措施,对企业和商业产生了直接和间接的重大影响。新冠肺炎疫情的未来发展及其对我们业务和运营的影响是不确定的。
我们、我们的CRO、临床研究人员、第三方供应商和临床站点可能会遇到候选药物供应中断和/或采购对我们的研发活动至关重要的物品,包括制造我们的候选药物所用的原材料、我们的临床试验或临床前研究中使用的医疗和实验室用品或用于临床前试验的动物,在每个情况下,由于应对新冠肺炎大流行的持续努力,可能会出现供应短缺的情况。新冠肺炎大流行对供应链的任何中断,或未来任何潜在的爆发,都可能对我们的临床试验计划和业务运营产生重大不利影响。
此外,我们已经并将寻求在位于许多受新冠肺炎疫情影响的地区的地点招募患者参加我们的临床试验,因此,我们的试验受到了影响。此外,即使网站正在积极招募,如果患者受到新冠肺炎病毒的影响,或者因为新冠肺炎疫情而害怕访问或旅行到临床试验网站,我们在正在进行的和计划中的临床试验中可能会面临招募或留住患者的困难。长期推迟或关闭我们的试验登记或患者中止可能会对我们的临床试验计划和时间表产生实质性的不利影响。
应对新冠肺炎疫情可能会重新分配我们在监管和知识产权事务方面的资源,从而对我们获得监管批准和保护我们知识产权的能力产生不利影响。此外,由于旨在限制面对面互动的措施,我们可能会面临监管会议和审批的障碍。
新冠肺炎疫情对我们的供应商为我们的候选药物提供材料、在我们的临床试验中招募或留住患者或我们收集患者数据的能力产生的任何负面影响都可能导致临床试验活动的代价高昂的延误,这可能会对我们获得监管部门批准并在获得批准后将我们的候选药物商业化的能力产生不利影响,增加我们的运营费用,并对我们的财务业绩产生实质性的不利影响。
新冠肺炎疫情对全球经济产生了重大影响。新冠肺炎疫情对我们的业务、临床前研究和临床试验的影响程度将取决于未来的事态发展,这些事态发展具有很高的不确定性,无法自信地预测,例如疾病的最终地理传播、新冠肺炎大流行的持续时间、美国和其他国家的旅行限制和社会距离、企业关闭或商业中断,以及美国和其他国家采取的控制和治疗疾病的行动的有效性。新冠肺炎大流行的全球爆发继续演变,我们的临床试验的进行可能继续受到不利影响,尽管采取了任何努力来减轻这种影响。新冠肺炎疫情有可能对我们的业务、财务状况、运营结果和前景产生不利影响。详见《管理层对财务状况和经营成果的讨论与分析--新冠肺炎疫情的影响》。
我们已经发现了财务报告内部控制中的重大弱点。如果我们不能纠正这些重大弱点,或者如果我们在未来经历更多的重大弱点,或者以其他方式未能维持有效的内部控制系统,我们可能无法准确或及时地报告我们的财务状况或经营结果,这可能会对投资者对我们的信心产生不利影响,从而影响我们的普通股价值。
对财务报告的有效内部控制对于我们提供可靠的财务报告是必要的,并与适当的披露控制和程序一起旨在防止欺诈。任何未能实施所需的新的或改进的控制措施,或在执行过程中遇到的困难,都可能导致我们无法履行我们的报告义务。此外,我们根据《萨班斯-奥克斯利法案》第404条进行的任何测试,或我们的独立注册会计师事务所在需要时进行的任何后续测试,都可能揭示我们在财务报告内部控制方面的缺陷,这些缺陷被认为是重大缺陷或重大弱点,或可能需要对我们的财务报表进行前瞻性或追溯性更改,或发现需要进一步关注或改进的其他领域。较差的内部控制也可能导致投资者对我们报告的财务信息失去信心,这可能会对我们普通股的交易价格产生负面影响。
在对截至2021年和2020年12月31日的财务报表进行审计时,我们的管理层发现了财务报告内部控制中的重大弱点。重大缺陷是指财务报告的内部控制存在缺陷或缺陷的组合,使得我们的年度或中期财务报表的重大错报有合理的可能性无法及时防止或发现。发现的重大弱点与我们没有设计或维持一个与我们的财务报告相称的有效控制环境有关。
54
目录表
要求。我们控制环境中的这一缺陷导致了与我们财务报告内部控制活动以及信息和通信有关的以下其他重大缺陷:
上述控制缺陷中的每一个都可能导致一个或多个账户余额或披露的错报,从而导致年度或中期合并财务报表的重大错报,而这些错报是无法预防或发现的。因此,我们的管理层已经确定,上述每一项控制缺陷都构成重大弱点。
虽然我们已开始采取措施解决重大弱点,但这些措施的实施可能不能完全解决我们在财务报告内部控制方面的重大弱点和不足,我们也不能得出这些问题已得到完全补救的结论。随着我们继续评估并努力改进我们对财务报告的内部控制,管理层可能会确定有必要采取额外或不同的措施来解决控制缺陷或对补救计划的修改。此外,在未来,我们可能会确定我们还有更多的实质性弱点。我们未能纠正重大弱点或未能发现和解决任何其他重大弱点或控制缺陷,可能会导致我们的财务报表不准确,还可能削弱我们及时遵守适用的财务报告要求和相关监管文件的能力,这可能会导致投资者对我们报告的财务信息失去信心,这可能会导致我们普通股的市场价格波动和下跌。
根据第404条,在反向资本重组后,我们作为幸存实体,必须提交一份关于我们财务报告内部控制有效性的报告,包括由我们的独立注册会计师事务所出具的关于财务报告内部控制的认证报告。然而,尽管我们仍然是一家新兴的成长型公司,我们将不会被要求包括由我们的独立注册会计师事务所发布的关于财务报告的内部控制的认证报告。为了在规定的时间内遵守第404条,我们将参与记录和评估我们对财务报告的内部控制的过程,这既昂贵又具有挑战性。在这方面,我们将需要继续提供内部资源,可能聘请外部顾问,并通过详细的工作计划,以评估和记录财务报告内部控制的充分性,继续酌情采取步骤改进控制程序,通过测试验证控制措施是否如文件所述发挥作用,并实施财务报告内部控制的持续报告和改进程序。尽管我们做出了努力,但我们和我们的独立注册会计师事务所都有可能在规定的时间框架内得出结论,证明我们对财务报告的内部控制是有效的,符合第404条的要求。这可能会对投资者对我们的信心产生不利影响,从而影响我们普通股的价值。
我们的候选药物及其作为商业产品的可行性存在很大的不确定性。
金属纳米晶体治疗候选药物,如我们的铅产品CNM-Au8®被认为是潜在治疗神经系统疾病和其他疾病的新兴和新颖的研究产品。我们正在开发CNM-AU8®用于治疗神经系统疾病,如肌萎缩侧索硬化症、多发性硬化症和帕金森病,通过髓鞘再生和/或与某些生物反应催化有关的神经保护机制。目前还没有被批准的髓鞘再生疗法,神经保护治疗对这些适应症的影响的证据到目前为止还很有限。由于用于治疗这些适应症的促进髓鞘再生和神经保护的纳米晶体疗法的开发的临床试验数据和先例有限,我们的临床试验的设计或结果很有可能不能令人满意,无法支持监管部门的批准。此外,关于金属纳米晶体药物上市授权的监管先例通常有限或没有,也没有适当区分批准的纳米晶体产品标签的监管框架。我们的铅金属纳米晶候选药物CNM-Au8®,含有完全由高纯金单独制成的纳米晶体。目前尚不清楚监管部门将如何识别或分类CNM-Au8的活性部分®包括它是否被归类为新的化学实体或类似的名称。不能从黄金中获得充分区分的活性部分分类通常可能会限制CNM-AU8®以及我们的候选药物永远不会实现盈利。
55
目录表
此外,纳米晶体疗法的作用机制还不完全清楚,在临床试验中可能会观察到不良事件或副作用,并由医生在未来与患者使用相关的情况下报告。如果这些不良事件或副作用被证明是重大的,它们可能会阻碍我们的候选药物通过临床试验的能力,或者它们可能超过患者从使用我们的候选药物中获得的好处,这两者都可能阻止我们的候选药物实现盈利。
我们的候选药物不会被代谢,可能会在长期使用后在体内积累,这使得长期服用我们的候选药物的长期效果不确定。尽管截至本年度报告日期,我们候选药物的所有当前毒理学研究都已得出无不良反应的水平,但我们尚未完成生殖或致癌研究,我们需要在未来完成这些研究。这些研究的任何负面结果都可能对我们的业务、运营结果、财务状况和前景产生实质性的不利影响。
此外,纳米晶体疗法的临床试验结果可能会揭示出严重的、不可接受的严重程度和不良副作用的流行。任何此类副作用都可能对我们获得监管部门批准的能力产生不利影响。例如,FDA、NMPA、加拿大卫生部、TGA、EMA或其他类似机构可以命令我们暂停或终止我们的研究,或停止我们候选药物的进一步临床开发或拒绝批准。此外,任何与药物有关的不良副作用都可能影响患者招募或纳入患者完成试验的能力,或者可能导致潜在的产品责任索赔。这些情况中的任何一种都可能严重损害我们的业务、财务状况、经营结果和前景。
我们之前没有获得任何候选药物的监管批准,我们可能无法获得或可能延迟获得任何我们的候选药物的监管批准。
我们的业务在很大程度上取决于我们能否及时完成候选药物的开发、获得监管部门的批准并成功商业化。在没有获得FDA、NMPA、加拿大卫生部、TGA、EMA和其他类似监管机构的监管批准之前,我们不能将候选药物商业化。获得监管部门批准所需的时间是不可预测的,但通常需要数年时间才能开始临床前研究和临床试验,并取决于许多因素,包括监管部门的相当大的酌情决定权。此外,在候选药物的临床开发过程中,批准政策、法规或获得批准所需的临床数据的类型和数量可能会发生变化,并可能因司法管辖区而异。
我们的候选药物可能会因为许多原因而无法获得监管部门的批准,包括:
FDA、NMPA、TGA、Health Canada、EMA或类似的监管机构可能需要更多信息,包括额外的临床前或临床数据,以支持批准,这可能会推迟或阻止批准和我们的商业化计划,或者我们可能决定放弃开发计划。
56
目录表
新的或意想不到的不良事件,或监管要求和指南的变化也可能发生,我们可能需要修改提交给适用监管机构的临床试验方案,以反映这些变化。修正案可能要求我们向IRBs或HRECs重新提交临床试验方案进行重新检查,这可能会影响临床试验的成本、时间或成功完成。
如果我们的任何候选药物的临床试验延迟完成或终止,该候选药物的商业前景将受到损害,我们从这些候选药物中创造产品销售收入的能力将被推迟。此外,完成临床试验的任何延误都将增加我们的成本,减缓我们的候选药物开发和审批过程,并危及我们开始产品销售和为该产品创造相关收入的能力。任何这些情况都可能对我们的业务、财务状况、经营结果和前景造成重大损害。此外,许多导致或导致临床试验开始或完成延迟的因素最终也可能导致我们的候选药物被拒绝获得监管部门的批准。
我们可能无法成功识别、发现、开发或许可新药候选药物。
由于几个原因,我们不能保证我们将成功地确定临床开发的潜在候选药物。例如,我们的研究方法可能无法成功识别潜在的候选药物,或者我们确定的那些可能被证明具有有害副作用或其他特征,使其无法上市或不太可能获得监管批准。我们通过我们专有的电晶体化学药物开发平台为发现工作投入了大量资源,然而,我们不能保证我们将成功地识别出更多潜在的候选药物,或者我们将能够成功地识别并获得来自其他各方的具有高潜力的新候选药物的许可。
继续开发我们的候选药物以获得更多适应症,并确定新的候选药物和药物靶标的研究计划需要大量的技术、财政和人力资源。我们的研究计划最初可能在确定潜在适应症和/或候选药物方面表现出希望,但由于多种原因未能产生临床开发结果,包括:
因此,不能保证我们能够通过内部研究计划为我们的候选药物确定额外的治疗机会或开发合适的潜在候选药物,这可能会对我们未来的增长、业务、财务状况、运营结果和前景产生实质性的不利影响。我们可能会将我们的努力和资源集中在潜在的候选药物或其他最终被证明是不成功的潜在计划上。
候选药物的临床前和临床开发涉及一个漫长而昂贵的过程,结果不确定,我们无法预测我们是否或何时能够成功地开发任何候选药物或将其商业化。
对于我们每个候选药物来说,都有失败的风险。在获得监管部门批准销售我们的任何候选药物之前,我们必须完成临床前研究,然后进行广泛的临床试验,以证明我们的候选药物在人体上的安全性和有效性。很难预测我们的候选药物何时或是否会在人体上证明有效和安全,或获得监管部门的批准。我们针对一些候选药物的内部发现计划正处于开发的早期阶段,在商业化之前将需要大量投资和监管批准。在我们获得FDA、NMPA、TGA、加拿大卫生部、EMA或类似监管机构的监管批准之前,我们不被允许营销或推广我们的任何候选药物,而且我们的任何候选药物可能永远不会获得这样的监管批准。
如果临床试验被暂停或终止,我们可能会遇到监管延误,如果临床试验被我们暂停或终止,或者根据需要,由进行此类试验的机构的IRBs或伦理委员会、由DSMB(为监测正在进行的临床试验而成立的独立专家小组)暂停或终止,或由FDA、NMPA、TGA、加拿大卫生部、EMA或其他监管机构暂停或终止。此类主管部门可能会因一系列因素而暂停或终止临床试验,这些因素包括:(1)未能按照法规要求或适用的临床规程进行临床试验,(2)FDA、NMPA、TGA、加拿大卫生部、EMA或其他监管机构对临床试验操作或试验地点进行检查,导致实施临床暂停、不可预见的安全问题或不良副作用,(3)未能证明使用某种药物的益处,(4)政府法规或行政措施的变化,或(5)缺乏足够的资金来继续临床试验。导致延误的许多因素
57
目录表
临床试验的开始或完成也可能最终导致我们的候选药物被拒绝获得监管部门的批准。此外,FDA、NMPA、TGA、Health Canada、EMA或其他监管机构可能不同意我们的临床试验设计或我们对临床试验数据的解释,或者即使在任何监管机构对我们的临床试验设计进行审查和评论后,也可能更改审批要求。
临床前研究和临床试验费用昂贵,难以设计和实施,可能需要多年才能完成。此外,临床前和临床数据往往容易受到不同解释和分析的影响,许多公司认为他们的候选药物在临床前研究和临床试验中表现令人满意,但仍未能获得监管机构对其候选药物的批准。我们候选药物未来的临床试验可能不会成功。
临床试验的开始取决于与FDA、NMPA、TGA、加拿大卫生部、EMA和/或其他监管机构正在进行的讨论的基础上最终确定试验设计。FDA、NMPA、TGA、Health Canada、EMA和其他监管机构可能会改变他们对试验设计或临床终点可接受性的立场,这可能要求我们完成额外的临床试验或施加我们目前预期不到的批准条件。成功完成我们的临床试验是向FDA、NMPA、TGA、加拿大卫生部、EMA和/或其他监管机构提交每个候选药物的保密协议(或类似申请),从而最终批准我们的候选药物并进行商业营销的先决条件。我们不知道我们候选药物的临床试验是否会如期完成,如果可以的话。
早期临床试验的结果可能不能预测后期临床试验的结果。
我们候选药物的临床前研究和早期临床试验的结果可能不能预测后期临床试验的结果。尽管在临床前研究和初步临床试验中取得了进展,但临床试验后期阶段的候选药物可能无法显示出预期的安全性和有效性特征。由于这些和其他原因,未来的临床试验结果可能不会有利。
在某些情况下,由于许多因素,同一候选药物的不同试验之间的安全性和/或有效性结果可能存在显著差异,这些因素包括方案中规定的试验程序的变化、患者群体的大小和类型的差异,包括遗传差异、患者对给药方案的依从性以及临床试验参与者的辍学率。随着候选药物的开发从临床前到早期和后期的临床试验走向批准和商业化,开发计划的各个方面,如生产和配方,通常都会在过程中进行更改,以努力优化过程和结果。这样的变化有可能无法实现这些预期目标。在我们进行的任何试验中,由于临床试验地点的数量较多,以及此类试验涉及的国家/地区和语言较多,因此结果可能与早期试验不同。任何这些变化都可能使计划中的临床试验或我们可能启动的其他未来临床试验的结果更难预测,并可能导致我们的候选药物表现不同,这可能会推迟临床试验的完成,推迟我们候选药物的批准,和/或危及我们开始候选药物商业化的能力。
我们候选药物的临床试验可能无法证明令监管机构满意的安全性和有效性,或者可能不会产生积极的结果,这可能会导致我们在完成或最终无法完成我们候选药物的开发和商业化过程中产生额外的成本或经历延迟。
在获得销售我们的候选药物的监管批准之前,我们必须进行广泛的临床试验,以证明我们的候选药物在人体上的安全性和有效性。在临床试验期间或临床试验的结果中,我们可能会遇到许多意想不到的事件,这些事件可能会推迟或阻止我们获得监管部门的批准或使我们的候选药物商业化,包括:
58
目录表
如果我们被要求对我们的候选药物进行超出我们目前预期的额外临床试验或其他测试,如果我们无法成功完成对我们候选药物的临床试验或其他测试,如果这些试验或测试的结果不呈阳性或仅略呈阳性,或者如果它们引起安全问题,我们可能会(I)延迟获得对我们的候选药物的监管批准;(Ii)根本没有获得监管批准;(Iii)获得批准的适应症并不像预期的那样广泛;(Iv)在获得监管批准后将药物从市场上移除;(V)须遵守额外的上市后测试规定;(Vi)须受药物分销或使用方式的限制;或(Vii)无法获得药物使用的补偿。
重大的临床试验延迟也可能增加我们的开发成本,并可能缩短我们拥有将候选药物商业化的独家权利或允许我们的竞争对手在我们之前将药物推向市场的任何期限。这可能会削弱我们将候选药物商业化的能力,并可能损害我们的业务和运营结果。
如果我们在招募患者参加临床试验时遇到困难,我们候选药物的临床试验可能会推迟或受到其他不利影响。
根据他们的方案及时完成临床试验,除其他外,取决于我们能否招募足够数量的患者留在试验中,直到我们的结论。由于各种原因,我们在临床试验中招募患者时可能会遇到困难,包括:
如果我们不能及时完成临床试验,将推迟我们候选药物的批准和商业化,损害我们候选药物的商业表现,从而损害我们的业务和运营结果。
59
目录表
如果我们无法获得所需的监管批准或在获得监管批准方面遇到延误,我们将无法将我们的候选药物商业化,我们的创收能力将受到实质性损害。
在获得用于目标适应症的任何候选药物的商业销售的监管批准之前,我们必须在临床前研究和良好控制的临床试验中证明,并就美国的批准而言,使FDA满意地证明,用于该目标适应症的候选药物是安全和有效的,并且制造设施、工艺和控制是足够的。除了临床前和临床数据外,NDA还必须包括候选药物的CMC的重要信息。获得保密协议的批准是一个漫长、昂贵和不确定的过程,可能无法获得批准。在我们向FDA提交保密协议后,FDA决定是接受还是拒绝提交的申请。我们不能确定任何提交的材料是否会被FDA接受备案和审查。
我们还没有证明有能力为我们的候选药物申请或获得监管部门的批准。例如,我们没有准备监管机构提交所需材料或导航监管审批流程的经验。因此,我们为候选药物成功提交保密协议并获得监管批准的能力可能会比我们是一家在获得监管批准方面有经验的公司涉及更多固有风险、时间更长、成本更高。
美国以外的监管机构,如美国国家药品监督管理局、TGA、加拿大卫生部和EMA,也有批准用于商业销售的药物的要求,我们在这些地区上市之前必须遵守这些要求。各国的监管要求可能有很大差异,可能会推迟或阻止我们的候选药物的推出。在一个国家进行的临床试验可能不会被其他国家的监管部门接受,在一个国家获得监管批准并不意味着将在任何其他国家获得监管批准。审批流程因国家/地区而异,可能涉及额外的产品测试和验证,以及额外的行政审查期限。寻求非美国监管机构的批准可能需要额外的非临床研究或临床试验,这可能是昂贵和耗时的。非美国监管审批过程可能包括与获得FDA批准相关的所有风险。由于所有这些原因,我们可能不会及时获得非美国监管部门的批准,如果有的话。
无论是在美国国内还是国外,开发候选药物、获得监管批准并将其商业化的过程都是漫长、复杂和昂贵的,而且永远不能保证获得批准。即使我们的候选药物成功获得监管部门的批准,任何批准都可能大大限制批准的使用适应症,或要求在产品标签上包括预防措施、禁忌症或警告,或要求昂贵且耗时的批准后临床试验或监测作为批准条件。在我们的候选药物的任何商业销售获得批准后,对该药物的某些更改,如制造工艺的更改和额外的标签声明,可能需要接受FDA、NMPA、TGA、加拿大卫生部、EMA和类似监管机构的额外审查和批准。此外,我们任何候选药物的监管批准都可能被撤回。如果我们无法在一个或多个司法管辖区获得对我们候选药物的监管批准,或者任何批准包含重大限制,我们的目标市场将会减少,我们实现候选药物全部市场潜力的能力将受到损害。此外,我们可能无法获得足够的资金或产生足够的收入和现金流来继续开发任何其他候选药物。
对于我们的任何候选药物,可能不会授予有利的称号,或者如果授予,可能会在以后撤回,并且可能不会导致更快的开发或监管审查或批准。
我们目前没有快速通道称号或突破性疗法称号,但未来可能会寻求一个或多个此类称号。
如果一种药物用于治疗严重或危及生命的疾病,并且该药物显示出解决该疾病未得到满足的医疗需求的潜力,药物赞助商可以申请FDA快速通道认证。FDA在决定是否授予这一称号时拥有广泛的自由裁量权。即使我们相信某个特定的候选药物有资格获得这一指定,我们也不能保证FDA会决定批准它。即使我们确实获得了快速通道认证,我们也可能不会比传统的FDA程序更快地经历开发、审查或批准过程。如果FDA认为我们的临床开发计划的数据不再支持快速通道指定,它可能会撤回该指定。许多获得快速通道指定的药物未能获得FDA的批准。
突破疗法被定义为一种旨在单独或与一种或多种其他药物联合治疗严重或危及生命的疾病或状况的药物,初步临床证据表明,该药物可能在一个或多个临床重要终点显示出比现有疗法显著的改善,例如在临床开发早期观察到的实质性治疗效果。对于被指定为突破性疗法的药物,FDA和赞助商之间的互动和沟通可以帮助确定最有效的开发路径。
60
目录表
FDA有权将其指定为突破性疗法。因此,即使我们认为,在完成早期临床试验后,我们的一种候选药物符合被指定为突破性疗法的标准,FDA也可能不同意,而决定不授予该称号。在任何情况下,与根据FDA传统程序考虑批准的药物相比,收到候选药物的突破性治疗指定可能不会导致更快的开发、审查或批准过程,也不能确保FDA最终批准。此外,即使我们的一个或多个候选药物有资格成为突破性疗法,FDA稍后也可能决定这些候选药物不再符合资格条件。
虽然我们已经获得了FDA对CNM-AU8的孤儿药物名称®对于ALS的治疗,我们可能不会从这样的指定中意识到任何好处,它不会增加获得批准的机会。
FDA批准了我们的主要候选药物CNM-Au8为孤儿药物®,用于治疗肌萎缩侧索硬化症。包括美国和欧盟在内的一些司法管辖区的监管机构可能会将患者人数相对较少的药物指定为孤儿药物。根据《孤儿药品法》,如果一种药物是用于治疗罕见疾病或疾病的药物,通常被定义为在美国患者人数少于20万人的疾病,或者在美国影响超过20万人的疾病,并且没有合理的预期可以通过在美国的销售收回用于该适应症的产品的研发成本,则FDA可以将该药物指定为孤儿药物。通常,如果具有孤儿药物名称的药物随后获得了具有该名称的适应症的第一次监管批准,该药物有权享有一段市场排他期,这使得FDA或EMA不能在排他期内批准同一药物的同一适应症的另一营销申请。适用期限在美国为7年,在欧盟为10年。如果一种药物不再符合孤儿药物指定的标准,或者如果该药物的利润足够高,从而不再有理由获得市场排他性,那么欧洲的排他性期限可以缩短到六年。如果FDA或EMA确定指定请求存在重大缺陷,或者如果制造商无法保证足够数量的药物来满足患有罕见疾病或疾病的患者的需求,则可能会失去孤儿药物的排他性。
虽然我们已经获得了CNM-AU8的孤儿药物名称®对于美国ALS的治疗,并可能获得其他候选药物或适应症的相同称号,如果获得批准,该称号可能无法有效保护候选药物免受竞争,因为不同的药物可以被批准用于相同的情况,相同的药物可以被批准用于不同的情况,但可以在标签外用于我们可能获得的任何孤儿适应症。即使在一种孤儿药物获得批准后,如果FDA得出结论认为,后一种药物在临床上更优越,因为它被证明更安全、更有效,或者对患者护理做出了重大贡献,那么FDA随后可以批准一种在其他情况下是相同药物的药物。
我们的任何候选药物,如果获得批准,都将继续受到持续或额外的监管义务和监管审查的约束,这可能会导致大量额外费用,如果我们未能遵守监管要求或我们的候选药物遇到意想不到的问题,我们可能会受到惩罚。
我们的任何候选药物,如果获得批准,都将受到制造、标签、包装、储存、广告、促销、采样、记录保存、进行上市后研究以及提交安全性、有效性和其他上市后信息方面的持续或额外的监管要求,包括美国的联邦和州要求以及欧盟、中国、澳大利亚和其他市场的类似监管机构的要求。
制造商和制造商的工厂必须遵守FDA、NMPA、TGA、加拿大卫生部、EMA和其他类似监管机构的广泛要求,以确保质量控制和制造程序符合GMP。因此,如果我们未来要建立制造设施,我们将受到持续的审查和检查,以评估对GMP的遵守情况以及对任何NDA、其他营销申请和之前对任何检查意见的回应中做出的承诺的遵守情况。因此,我们和其他与我们合作的人必须继续在监管合规的所有领域花费时间、金钱和精力,包括制造、生产和质量控制。
我们为候选药物获得的任何批准可能会受到该药物可能上市的批准指示用途的限制或批准条件的限制,这可能会对该药物的商业潜力产生不利影响,或包含对可能代价高昂的上市后测试和监测的要求,以监测该候选药物的安全性和有效性。FDA、NMPA、TGA、Health Canada、EMA或类似的监管机构也可能要求风险评估缓解战略计划作为我们候选药物批准或批准后的条件。此外,如果FDA、NMPA、TGA、Health Canada、EMA或类似的监管机构批准了我们的候选药物,我们将必须遵守要求,例如,对于我们在批准后进行的任何临床试验,包括提交安全性和其他上市后信息和报告、注册,以及继续遵守GMP和GCP。
FDA和其他监管机构严格监管投放市场的产品的营销、标签、广告和促销。只能根据批准的适应症和按照批准的标签的规定推广药物。FDA、NMPA、TGA、Health Canada、EMA等监管部门积极执行法律法规
61
目录表
禁止推广标签外使用,以及被发现不当推广标签外使用的公司可能会受到重罚和执法行动。
即使我们能够将任何批准的候选药物商业化,这些药物也可能受到国家或其他第三方报销做法或不利的定价法规的约束,这可能会损害我们的业务。
监管新治疗产品的监管审批、定价和报销的法规因国家而异。在欧洲、加拿大、澳大利亚、中国和中国以外的一些市场,处方药的定价即使在获得初步批准后,仍然受到政府的持续控制。因此,我们可能会在特定国家获得药品的监管批准,但随后会受到价格法规的约束,这些法规会推迟我们的药物的商业推出,并对我们的收入产生负面影响。
我们能否成功地将任何已批准的候选药物商业化,还将在一定程度上取决于政府卫生行政部门、私人健康保险公司和其他组织对这些药物和相关治疗的报销程度。
全球医疗行业的一个主要趋势是成本控制。政府当局和这些第三方付款人试图通过限制特定药物的覆盖范围和报销金额来控制成本。
在美国,第三方付款人之间没有统一的药品保险和报销政策。因此,从政府或其他第三方付款人那里获得药物的承保和报销批准是一个既耗时又昂贵的过程,这可能需要我们向每个付款人提供科学、临床和成本效益数据,以逐个支付者的基础上支持我们未来批准的药物的使用,而不能保证获得保险和足够的报销。即使我们获得了特定药物的保险,由此产生的报销率可能不足以使我们实现或维持盈利,或者可能需要患者认为不可接受的高得令人无法接受的共同支付。此外,第三方付款人可能不会覆盖我们未来批准的候选药物使用后所需的长期后续评估,也不会为其提供足够的补偿。患者不太可能使用我们未来批准的任何药物,除非提供保险,并且报销足以支付药物成本的很大一部分。由于我们的一些候选药物可能比传统的小分子疗法有更高的商品成本,并且可能需要长期的后续评估,因此覆盖范围和报销率可能不足以使我们实现盈利的风险可能更大。
越来越多的第三方付款人要求公司在标价的基础上向他们提供预定的折扣,并对医疗产品的定价提出挑战。我们不能保证我们商业化的任何批准的候选药物都可以得到报销,如果可以报销,报销的水平是多少。报销可能会影响我们商业化的任何经批准的候选药物的需求或价格。如果无法获得报销或仅限于有限的水平,我们可能无法成功地将我们成功开发的任何候选药物商业化。
在获得批准的候选药物的报销方面可能会有很大的延误,覆盖范围可能比FDA、NMPA、TGA、加拿大卫生部、EMA或其他类似监管机构批准候选药物的目的更有限。此外,有资格获得补偿并不意味着任何药物在所有情况下都会得到支付,或者支付的费率将覆盖我们的成本,包括研究、开发、制造、销售和分销。如果适用,新药的临时付款也可能不足以支付我们的成本,并且可能不会成为永久性的。付款率可能会因药物的使用和临床环境的不同而有所不同,可能是基于已经报销的低成本药物所允许的付款,并可能被并入其他服务的现有付款中。药品净价可能会因为政府医疗保健计划或私人付款人要求的强制性折扣或回扣,以及未来法律的任何弱化而降低,这些法律目前限制从那些国家进口药品,在这些国家,药品的销售价格可能低于美国。我们无法迅速从政府资助的和私人付款人那里获得任何未来批准的候选药物和我们开发的任何新药的保险和有利可图的支付率,这可能会对我们的业务、经营业绩和整体财务状况产生实质性的不利影响。
我们打算单独或与合作伙伴一起寻求批准,以便在美国、中国、欧盟、澳大利亚、加拿大和其他司法管辖区销售我们的候选药物。在中国、澳大利亚、加拿大和欧盟,药品的定价受到政府的控制,在获得上市监管批准后,可能需要相当长的时间才能获得未来批准的药品报销。我们未来批准的任何候选药物的市场接受度和销量将在很大程度上取决于第三方药物支付者是否提供足够的保险和报销,并可能受到现有和未来医疗改革措施的影响。
62
目录表
我们的候选药物如果在未来获得批准,可能无法达到医生、患者、第三方付款人和医学界其他人对商业成功所需的市场接受度,候选药物的市场机会可能比我们估计的要小。
我们的候选药物如果在未来获得批准,可能无法获得医生、患者、第三方付款人和医学界其他人的足够市场接受。例如,目前的多发性硬化症治疗方法在医学界得到了很好的确立,医生可能会继续依赖这些治疗方法,将我们正在进行临床试验的相同或类似适应症的候选药物排除在外。此外,医生、患者和第三方付款人可能更喜欢其他新产品而不是我们的产品。如果我们的候选药物没有达到足够的接受度,我们可能不会产生显著的产品销售收入,我们也可能无法盈利。如果我们的候选药物获准用于商业销售,市场的接受程度将取决于许多因素,包括:
如果我们商业化的任何已批准的候选药物未能获得医生、患者、医院、治疗中心或医学界其他人的市场接受,我们将无法产生可观的收入。即使未来任何已批准的候选药物获得市场接受,如果推出比我们的候选药物更受欢迎、更具成本效益或使我们的候选药物过时的新产品或技术,我们可能无法随着时间的推移保持市场接受度。
如果我们的候选药物导致或被认为导致不良副作用,可能会导致延迟或无法获得监管部门的批准或对已批准标签的商业概况进行限制。
我们的候选药物引起的不良副作用可能会导致我们或监管机构中断、推迟或停止临床试验,并可能导致更严格的标签,或者推迟或拒绝FDA、NMPA、TGA、加拿大卫生部、EMA或其他监管机构的监管批准。如果我们候选药物的正在进行的临床试验结果显示严重程度高且无法接受且普遍存在不良副作用,我们候选药物的临床试验可能会被暂停或终止,FDA、NMPA、TGA、加拿大卫生部、EMA或类似的监管机构可以命令我们停止进一步开发我们的候选药物或拒绝批准我们的候选药物的任何或所有目标适应症。与药物相关的副作用可能会影响患者招募或纳入患者完成临床试验的能力,或导致潜在的产品责任索赔。任何这些情况都可能对我们的业务、财务状况和前景造成重大损害。
临床试验评估了潜在患者群体的样本。由于患者数量和暴露时间有限,我们的候选药物的罕见和严重副作用可能只有在接触候选药物的患者数量显著增加时才会被发现。如果我们的候选药物获得监管部门的批准,而我们或其他人发现这些药物(或任何其他类似药物)引起的不良副作用,或者这些候选药物的效果不如之前认为的那样有效,可能会导致一些潜在的重大负面后果,包括:
63
目录表
任何这些事件都可能阻止我们实现或维持市场对受影响的候选药物的接受程度,如果获得批准,可能会大幅增加我们的药物商业化成本,并显著影响我们成功将我们的药物商业化并创造收入的能力。
药品不良反应和标签外使用我们产品的负面结果可能会对我们的商业声誉、产品品牌名称、商业运营、财务状况(包括我们普通股的价值)造成实质性损害,并使我们承担责任。
在药品市场上分销或销售的产品可能会受到标签外药物使用的影响。标签外药物使用是指根据适应症、患者群体、剂量强度或频率或其他使用条件开出的产品,与监管部门批准的用法和标签不符。即使FDA、NMPA、TGA、Health Canada、EMA和其他类似的监管机构积极执行禁止推广标签外使用的法律和法规,我们的产品仍然存在标签外药物使用的风险,并且在未经主管当局批准的患者群体或剂量中使用。在标签外使用我们的产品可能效果不佳或完全无效,并可能导致药物不良反应。任何这些事件都可能造成负面宣传,严重损害我们的商业声誉、产品品牌、商业运营和财务状况,包括我们普通股的价值。此外,这可能会对我们的产品商业化能力产生负面影响,因为它可能会影响第三方付款人对我们产品的报销和处方安置决定。这些事件还可能使我们承担责任,导致或导致我们临床试验进度的延迟,还可能最终导致我们的候选药物无法获得监管部门的批准。
在标签外使用我们的产品可能会使我们面临政府调查或起诉。
执行法律法规以禁止标签外使用的监管机构可以调查我们的产品是否被标签外使用。即使我们采取措施防止我们的产品进行标签外促销,这也不一定能阻止监管或检察机构对我们进行调查和采取行动,就像我们从事标签外促销一样。
作为一家公司,我们没有推出和营销药物的经验。如果我们无法发展销售、营销和分销能力,或与第三方达成销售、营销和分销协议或安排,我们可能无法成功地将任何药物商业化,如果获得批准,或产生候选药物的销售收入。
如果获得批准,我们还没有展示出有能力推出任何候选药物并将其商业化。因此,我们成功地将任何批准的药物商业化的能力可能会比我们是一家具有推出和营销药物经验的公司带来更多固有风险、花费更长的时间和更高的成本。
我们将不得不与其他制药和生物制药公司竞争,以招聘、聘用、培训和留住营销和销售人员。我们必须为我们批准的任何或所有药物发展内部销售、营销和商业分销能力,或者就我们批准的药物的销售和营销寻求合作安排。然而,我们不能保证我们将能够发展这种分销能力或建立或维持这种合作安排,或者如果我们能够做到这一点,也不能保证他们将拥有有效的销售队伍。我们获得的任何收入都将取决于这些第三方的努力。我们将很少或根本无法控制这些第三方的营销和销售活动,如果获得批准,我们的产品销售收入可能会低于我们自己将任何批准的药物商业化,或者我们可能在未来根本无法产生任何产品销售收入。
64
目录表
我们面临着来自其他制药和生物技术公司的激烈竞争,如果我们不能有效竞争,我们的经营业绩可能会受到影响。
新药的开发和商业化竞争激烈。我们面临着来自世界各地的大型制药公司、专业制药公司和生物技术公司的竞争。目前有许多大型制药和生物技术公司营销和销售药物,或正在开发用于治疗神经系统疾病和其他疾病的药物,我们正在将药物商业化或开发候选药物。潜在的竞争对手还包括学术机构、政府机构和其他进行研究、寻求专利保护并为研究、开发、制造和商业化建立合作安排的公共和私人研究组织。
如果我们的竞争对手开发和商业化比我们可能商业化或商业化的任何药物更安全、更有效、副作用更少或更少、更方便或更便宜的药物,我们的商业机会可能会减少或消失。我们的竞争对手也可能比我们更快地获得FDA、NMPA、TGA、Health Canada、EMA或其他类似监管机构对其药物的批准,这可能会导致我们的竞争对手在我们能够进入市场之前建立强大的市场地位和/或可能减缓我们的监管批准。
我们现在或未来的许多竞争对手在研发、制造、临床前测试、进行临床试验、获得监管批准和营销批准的药物方面比我们拥有更多的财务资源和专业知识。制药和生物技术行业的合并和收购可能导致更多的资源集中在我们数量较少的竞争对手身上。规模较小的公司和其他初创公司也可能成为重要的竞争对手,特别是通过与大型和成熟公司的合作安排。这些第三方在招聘和留住合格的科学和管理人员、建立临床试验场地和临床试验的患者登记,以及在获取与我们的计划互补或必要的技术方面与我们竞争。
我们可能直接或间接受到美国和其他司法管辖区适用的反回扣法、虚假申报法、医生支付透明度法、隐私和安全法、欺诈和滥用法或类似的医疗保健和安全法律法规的约束,这可能使我们面临刑事制裁、民事处罚、合同损害、声誉损害以及利润和未来收入减少。
在我们获得监管批准的任何产品的推荐和处方中,医疗保健提供者、医生和其他人扮演着主要角色。如果我们的任何候选药物获得了FDA的批准,并开始在美国将这些药物商业化,我们的业务可能会受到各种联邦和州欺诈和滥用法律的约束,包括但不限于联邦反回扣法规、联邦虚假索赔法案和医生支付阳光法律法规。这些法律可能会影响我们拟议的销售、营销和教育计划等。此外,我们可能受到联邦政府和我们开展业务所在州的患者隐私法规的约束。适用的联邦和州医疗保健法律法规的限制包括:
65
目录表
此外,除其他外,我们还受制于上述每一项医疗法律的州和非美国等价物,其中一些法律的范围可能更广,可能适用于由任何来源报销的医疗服务,而不仅仅是政府付款人,包括私人保险公司。此外,一些州通过了法律,要求制药公司遵守2003年4月总监察长办公室关于制药制造商的合规计划指南和/或其他自愿的行业行为准则。几个州还实施了其他营销限制,或要求制药公司向该州进行营销或价格披露。对于遵守这些州的要求需要什么是模棱两可的,如果我们不遵守适用的州法律要求,我们可能会受到惩罚。
违反欺诈和滥用法律的行为可能会受到刑事和/或民事制裁,包括惩罚、罚款和/或排除或暂停联邦和州医疗保健计划,如联邦医疗保险和医疗补助,以及禁止与美国政府签订合同。
美国政府和美国法院都没有就欺诈和滥用法律对潜在责任的限制提供明确的指导,因为这些法律可能适用于我们的业务。执法当局越来越注重执行这些法律,经常使用新的和创造性的法律理论,我们的一些做法可能会受到这些法律的挑战。确保我们与第三方的业务安排符合适用的医疗法律和法规的努力将涉及大量成本。无论合规努力如何,政府当局可能会得出结论,我们的业务实践可能不符合当前或未来涉及适用欺诈和滥用或其他医疗保健法律和法规的现行或未来法规、法规或判例法。此外,根据联邦《虚假申报法》以及几个州的虚假申报法,个人有权代表美国政府提起诉讼。如果对我们采取任何此类行动,对此类行动进行防御,即使成功,也会分散我们和我们的关键人员对我们核心任务的注意力,并可能造成巨大代价。如果我们没有成功地为自己辩护或维护我们的权利,这些行动可能会对我们的业务产生重大影响,包括施加民事、刑事和行政处罚、损害赔偿、交还、罚款、可能被排除在参与Medicare、Medicaid和其他联邦医疗保健计划之外、合同损害、声誉损害、利润和未来收益减少以及我们的业务削减,任何这些都可能对我们的业务运营能力和运营结果产生不利影响。此外, 我们在美国境外批准的任何药物的批准和商业化,也可能会使我们受到上述医疗保健法以及其他非美国法律的非美国对等法律以及美国《反海外腐败法》的约束。
如果我们预期与之开展业务的任何医生或其他提供者或实体被发现不遵守适用法律,他们可能会受到刑事、民事或行政制裁,包括被排除在政府资助的医疗保健计划之外,这也可能对我们的业务产生不利影响。
我们可能会面临当前法规和未来立法的变化带来的困难。
在美国和一些外国司法管辖区,已经并将继续有关于医疗保健系统的几项立法和监管改革和拟议的改革,这些改革可能会阻止或推迟候选药物的上市批准,限制或规范批准后的活动,并影响获得上市批准的候选药物的有利可图销售的能力。在美国和其他地方的政策制定者和支付者中,有很大的兴趣推动医疗系统的改革,其既定目标是控制医疗成本、提高质量和/或扩大准入。在美国,制药业一直是这些努力的重点,并受到重大立法倡议的重大影响。
例如,《平价医疗法案》极大地改变了政府和私营保险公司的医疗融资和提供方式。在《平价医疗法案》中,对制药和生物技术行业具有重要意义的条款如下:除其他事项外,使生物产品受到低成本生物仿制药的潜在竞争,创建了一种新的方法,根据该方法,对符合以下条件的药品计算制造商在医疗补助药品回扣计划下欠下的回扣
66
目录表
吸入法、注入法、注入法、植入法或注射法,提高医疗补助药品返点计划下制造商所欠的最低医疗补助返点,并将返点计划扩大到登记在医疗补助管理型护理组织中的个人,建立对某些品牌处方药制造商的年费和税收,并创建新的联邦医疗保险D部分覆盖缺口折扣计划,制造商必须同意在其覆盖间隔期内向符合条件的受益人提供适用品牌药物谈判价格的70%的销售点折扣,作为制造商的门诊药物纳入联邦医疗保险D部分的条件。
《平价医疗法案》的一些条款尚未实施,《平价医疗法案》的某些方面受到了法律和政治挑战。例如,2021年6月17日,美国最高法院驳回了一项基于程序理由的挑战,该挑战辩称,《平价医疗法案》整体违宪,因为“个人授权”已被国会废除。因此,《平价医疗法案》将以目前的形式继续有效。此外,在美国最高法院做出裁决之前,拜登总统于2021年1月28日发布了一项行政命令,启动了一个特殊的投保期,目的是通过平价医疗法案市场获得医疗保险,该市场从2021年2月15日开始,一直开放到2021年8月15日。行政命令还指示某些政府机构审查和重新考虑限制获得医疗保健的现有政策和规则,包括重新审查医疗补助示范项目和豁免计划,包括工作要求,以及通过医疗补助或《平价医疗法案》为获得医疗保险造成不必要障碍的政策。《平价医疗法案》有可能在未来受到司法或国会的挑战。目前尚不清楚任何此类挑战和拜登政府的医疗改革措施将如何影响《平价医疗法案》和我们的业务。
可能会通过进一步的立法或监管,可能会损害我们的业务、财务状况和运营结果。自《平价医疗法》颁布以来,还提出并通过了其他立法修改。例如,2011年8月,奥巴马总统签署了《2011年预算控制法案》,其中包括对医疗保险提供者支付的每一财年2%的总减幅,该法案从2013年4月1日起生效。然而,新冠肺炎的救济立法暂停了从2020年5月1日到2021年12月31日的2%的联邦医疗保险自动减支。2013年1月,《2012年美国纳税人救济法》签署成为法律,其中包括进一步减少了对包括医院、成像中心和癌症治疗中心在内的几类提供者的医疗保险支付,并将政府追回向提供者多付款项的诉讼时效从三年延长到五年。此外,2021年3月11日,拜登总统签署了《2021年美国救援计划法案》,从2024年1月1日起,取消了针对单一来源和创新多来源药物的法定医疗补助药品退税上限,目前该上限为药品平均制造商价格的100%。
此外,美国对特殊药品定价做法的立法和执法兴趣也越来越大。具体地说,美国国会最近进行了几次调查,并提出了一项联邦立法,旨在提高药品定价的透明度,降低联邦医疗保险下处方药的成本,审查定价与制造商患者计划之间的关系,以及改革政府计划的药品报销方法。国会表示,将继续寻求新的立法和/或行政措施来控制药品成本。此外,根据最近的一项行政命令,拜登政府表示打算采取某些政策举措来降低药品价格。作为对拜登行政命令的回应,2021年9月9日,HHS发布了一份应对高药价的综合计划,其中概述了药品定价改革的原则,并列出了国会可以采取的各种潜在立法政策,以及HHS可以采取的潜在行政行动来推进这些原则。尚未最后确定实施这些原则的立法或行政行动。此外,国会正在考虑将药品定价作为预算协调过程的一部分。美国个别州也越来越积极地通过立法和实施旨在控制生物制药产品定价的法规,包括价格或患者报销限制、折扣、对某些产品准入和营销成本披露的限制以及透明度措施,在某些情况下,旨在鼓励从其他国家进口和批量采购。
我们预计,如果《平价医疗法案》基本上维持目前的形式,将继续对我们获得批准的任何产品的承保范围和价格造成额外的下行压力,并可能严重损害我们的业务。医疗保险和其他政府计划报销的任何减少都可能导致私人支付者支付的类似减少。此外,实施成本控制措施或其他医疗改革可能会阻止我们创造收入、实现盈利或将我们的产品商业化。这些改革可能会对我们可能成功开发并获得监管批准的候选药物的预期收入产生不利影响,并可能影响我们的整体财务状况和开发候选药物的能力。
任何未能进行适当的质量控制和质量保证的行为都将对我们的业务和财务业绩产生重大不利影响。
我们的候选药物和任何药物的生产,如果获得批准,应遵守适用的法律、法规和GMP。这些规定管理生产过程和程序,包括记录保存和质量的实施和运作
67
目录表
管理体系,以控制和确保调查产品和批准销售的产品的质量。我们在生产过程的每个阶段都实行严格的质量控制,以符合这些要求。我们在整个生产过程中进行广泛的测试,以确保我们的候选药物的安全性和有效性。然而,我们可能会检测到未放行产品的生产没有遵守我们的生产程序,或者我们生产过程中使用的原材料没有按照GMP或其他规定收集并储存的情况,导致确定应销毁涉案产品。
此外,如果我们未能遵守法律、法规和GMP的相关质量控制要求,我们的产品供应可能会中断,这可能会推迟或阻止此类产品的进一步销售,这可能会对我们的业务和财务业绩产生实质性的不利影响。
此外,在扩展活动期间可能会出现质量问题。如果我们不能在大批量生产过程中成功地确保我们产品的一致性和高质量,我们的产品的销售可能无法得到促进,这可能会对我们的业务和财务业绩产生实质性的不利影响。
我们可能会探索在全球范围内许可商业化权利或其他形式的合作,这将使我们面临额外的风险。
非美国市场是我们增长战略的重要组成部分。我们最初打算重点关注美国、欧盟、加拿大、澳大利亚、日本、韩国和中国的机会。如果我们无法在这些或其他市场获得许可证或与第三方达成合作安排,或者如果这些安排不成功,我们的创收增长潜力将受到不利影响。此外,国际业务关系使我们面临额外的风险,这些风险可能会对我们实现或维持盈利业务的能力产生重大不利影响,包括:
这些风险和其他风险可能会对我们从国际市场获得或维持收入的能力产生重大不利影响,并可能对我们的业务、财务状况、运营结果和前景产生重大不利影响。
非法和/或平行进口和假冒药品可能会减少对我们未来批准的候选药物的需求,并可能对我们的声誉和业务产生负面影响。
从政府价格管制或其他市场动态导致价格较低的国家进口竞争产品,无论是政府政策授权的还是非法的,如果获得批准,可能会对我们未来的任何药物的需求产生不利影响,
68
目录表
反过来,如果我们将产品商业化,可能会对我们的销售和盈利能力产生不利影响。根据美国、中国、欧盟、澳大利亚和其他司法管辖区的现行法律,未经批准的外国进口处方药是非法的。然而,随着患者获得这些价格较低的进口产品的能力继续增长,非法进口可能会继续发生,甚至增加。此外,从价格较低的市场跨境进口(平行进口)到价格较高的市场,如果获得批准,可能会损害我们未来药物的销售,并对一个或多个市场的定价施加商业压力。此外,如果获得批准,政府主管部门可能会扩大消费者进口我们未来药物的低价版本或从我们运营的国家以外的竞争产品进口的能力。未来任何增加消费者从我们运营的国家以外的国家获得低价药品的立法或法规都可能对我们的业务产生实质性的不利影响。
在药品市场分销或销售的某些产品可能在没有适当许可证或批准的情况下制造,或者可能在其内容或制造商方面被欺诈性地贴错标签。这些产品通常被称为假冒药品。假冒药品控制和执法系统,特别是在中国等发展中市场,可能不足以阻止或消除仿制我们产品的假冒药品的制造和销售。由于在许多情况下,假冒药品的外观与正品非常相似,但通常以较低的价格出售,如果获得批准,假冒产品可能会迅速侵蚀对我们未来药品的需求。我们的声誉和业务可能会因为以我们或我们的合作者的品牌名销售的假冒药品而受到损害。此外,仓库、工厂或运输途中的库存被盗,这些库存没有妥善储存,并通过未经授权的渠道出售,可能会对患者安全以及我们的声誉和业务产生不利影响。
我们依赖第三方进行临床前研究和临床试验,我们必须与合作者有效合作,开发我们的候选药物。如果这些第三方不能成功地履行合同职责或在预期的最后期限前完成,我们可能无法获得监管部门对我们的候选药物的批准或将其商业化,我们的业务可能会受到实质性损害。
我们依赖并计划继续依赖第三方CRO和第三方供应商为我们正在进行的临床前和临床项目监测、收集样本、分析样本、报告数据和管理数据。我们依赖这些第三方来执行我们的临床前研究和临床试验。虽然我们只控制他们活动的某些方面,但我们有责任确保我们的每项研究都按照适用的议定书、法律和法规要求以及科学标准进行,并且我们对CRO的依赖不会免除我们的监管责任。我们、我们的CRO、支持我们临床计划的第三方供应商以及我们的临床研究人员都必须遵守GCP,GCP是FDA、NMPA、TGA、加拿大卫生部、EMA和其他类似监管机构对我们临床开发中的所有药物执行的法规和指南。如果我们、我们的任何CRO、第三方供应商或临床研究人员未能遵守适用的GCP,在我们的临床试验中产生的临床数据可能被认为是不可靠的,FDA、NMPA、TGA、加拿大卫生部、EMA或类似的监管机构可能会要求我们在批准我们的营销申请之前进行额外的临床试验。此外,我们的关键临床试验必须使用GMP生产的产品进行。我们或任何第三方未能遵守这些规定可能导致我们不得不重复临床试验,这将推迟监管批准过程。
如果我们与这些第三方的任何关系终止,我们可能无法与其他CRO、供应商或临床研究人员达成安排,或以商业合理的条款这样做。此外,我们的CRO不是我们的员工,除了根据我们与此类CRO达成的协议向我们提供的补救措施外,我们无法控制他们是否将足够的时间和资源投入到我们正在进行的临床和其他项目中。如果CRO未能成功履行其合同职责或义务或未能在预期期限内完成,如果CRO需要更换CRO,或者如果他们或我们的临床研究人员获得的临床数据的质量或准确性因未能遵守我们的临床方案、法规要求或其他原因而受到影响,我们的临床试验可能会被延长、推迟或终止,我们可能无法获得监管部门对我们的候选药物的批准或成功将其商业化。其结果是,我们的运营结果和我们药品的任何商业前景都将受到损害,我们的成本将增加,我们创造收入的能力将被推迟。
更换或增加额外的CRO或临床研究人员涉及额外的成本和延误,这可能会严重影响我们满足预期临床开发时间表的能力。不能保证我们未来不会遇到这些延误,也不能保证这些延误或挑战不会对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。
我们未来创造收入的能力取决于我们与合作者有效合作开发我们的候选药物的能力,包括获得监管部门的批准。如果获得批准,我们与合作伙伴的安排将是成功将产品推向市场并将其商业化的关键。我们在各个方面都依赖合作伙伴,包括承担研发计划、进行临床试验、管理或协助监管申报和审批过程,以及协助我们的商业化努力。我们不控制我们的合作者,我们不能确保这些第三方将充分和及时地履行他们对我们的所有义务。如果他们未能成功完成剩余的研究,或者根本没有完成,这将延误、不利影响或阻止监管部门的批准。我们不能保证我们的任何合作者的表现都令人满意
69
目录表
如果我们的任何合作者违反或终止了与我们的协议,我们可能无法成功地将候选药物商业化,这可能会对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。
我们的CRO、临床研究人员和第三方供应商也可能受到新冠肺炎疫情的影响。见--我们的财务状况和经营业绩可能会受到新冠肺炎疫情的不利影响。
我们已经进行了研究合作,并可能在未来形成或寻求合作、合资企业或战略联盟或达成许可安排,而我们可能没有意识到此类合作、联盟或许可安排的好处。
我们可能会结成或寻求战略联盟,建立合资企业或合作,或与第三方达成许可协议,我们相信这将补充或加强我们关于我们的候选药物和我们可能开发的任何未来候选药物的开发和商业化努力。这些关系中的任何一种都可能要求我们产生非经常性和其他成本,增加我们的短期和长期支出,扰乱我们的管理和业务,或者发行稀释我们现有股东的证券。
虽然我们已经与一些世界领先的学术机构和研究中心达成了合作研究安排,并正在与中枢神经系统疾病领域的关键科学家合作,但我们在寻找合适的战略合作伙伴方面面临着激烈的竞争,谈判过程既耗时又复杂。此外,我们为我们的候选药物建立战略合作伙伴关系或其他替代安排的努力可能不会成功,因为它们可能被认为处于合作努力的开发阶段太早,第三方可能不认为我们的候选药物具有展示安全性和有效性或商业可行性的必要潜力。如果我们与第三方合作开发和商业化候选药物,如果获得批准,我们可以预期将对该候选药物未来成功的部分或全部控制权让给第三方。对于我们可能寻求从第三方获得许可的任何候选药物,我们可能面临来自其他制药或生物技术公司的激烈竞争,这些公司拥有比我们更多的资源或能力,而我们达成的任何协议可能都不会产生预期的好处。
此外,涉及我们候选药物的合作面临许多风险,其中可能包括:
因此,如果我们不能成功地将这些产品与我们现有的运营和公司文化相结合,我们可能无法实现当前或未来的任何研究合作、战略合作伙伴关系或第三方药物潜在许可的好处,这可能会推迟我们的时间表或以其他方式对我们的业务产生不利影响。我们也不能确定,在战略上
70
目录表
交易或许可,我们将获得证明此类交易合理的收入或净收入。如果我们不能及时以可接受的条款与合适的合作伙伴达成协议,或者根本无法达成协议,我们可能不得不削减我们的一种候选药物的开发,减少或推迟我们的开发计划或一个或多个未来的开发计划,推迟我们潜在的商业化或缩小任何销售或营销活动的范围,或者增加我们的支出,并自费进行开发或商业化活动。如果我们选择自己资助和从事开发或商业化活动,我们可能需要获得更多的专业知识和额外的资本,而这些可能是我们无法接受的条件或根本无法获得的。如果我们未能达成合作,并且没有足够的资金或专业知识来开展必要的开发和商业化活动,我们可能无法进一步开发我们的候选药物,或者如果获得批准,将无法将它们推向市场并产生产品销售收入,这将损害我们的业务、财务状况、运营结果和前景。
我们的业务依赖于原材料的使用,而这些原材料的供应减少或成本增加或此类原材料的任何质量问题都可能对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。
为了生产我们的产品,我们必须以商业上可以接受的价格及时获得足够数量的高质量原材料。某些关键原材料,如高纯金和其他过渡元素制成的电线,可以从市场上有限数量的供应商那里获得。因此,任何生产中断或我们的供应商无法生产足够数量的药物来满足我们的需求,都可能损害我们日常运营业务和继续研究和开发未来候选药物的能力。此外,如果获得批准,我们预计随着业务规模的扩大和产品的商业化,对此类材料的需求将会增加,我们不能保证现有供应商有能力满足我们的需求。我们还面临材料成本增加的风险,我们可能无法将其转嫁给客户,因此我们的盈利能力可能会降低。此外,尽管我们在制造过程中使用这类材料之前已经对它们实施了质量检查程序,并要求我们的供应商保持高质量标准,但我们不能保证我们能够以高质量标准确保足够数量的原材料,也不能保证我们使用的供应中的所有质量问题都能被检测出来。例如,如果我们使用的高纯净水以任何方式受到损害,它可能会导致整个批次无法使用,或者根据杂质的性质,可能会对患者造成危险。此外,我们不能向您保证,第三方将能够维护和续签其运营所需的所有许可证、许可证和批准,或遵守所有适用的法律和法规。如果他们不这样做,可能会导致他们的业务运营中断, 这反过来可能导致我们所使用的原材料短缺。如果我们无法获得足够的原材料,我们的产品质量因此受到影响,我们可能不得不推迟临床试验和监管申报,召回我们的产品,受到产品责任索赔的影响,未能遵守持续的监管要求,并产生重大成本来纠正此类问题,这可能对我们的业务、财务状况、运营结果和前景产生重大不利影响。
如果我们无法通过知识产权为我们的候选药物获得并保持足够的专利保护,或者如果获得的知识产权范围不够广泛,第三方可能会开发和商业化与我们的产品类似或相同的产品,我们成功将批准的药物商业化的能力可能会受到不利影响。
我们的成功在很大程度上取决于我们通过获得、维护和执行我们的知识产权(包括专利权)来保护我们的专有技术、临床试验中的候选药物以及市场上已批准的药物(如果获得批准)免受竞争的能力。我们寻求保护我们认为具有商业重要性的候选药物和技术,方法是在最重要的商业市场提交专利申请,包括美国、中国、欧洲、加拿大、日本、韩国和其他国家/地区,依靠商业秘密或药品监管保护,或采用这些方法的组合。然而,专利起诉过程昂贵、耗时和复杂,我们可能无法以合理的成本或及时提交、起诉、维持、执行或许可所有必要或可取的专利申请。我们也有可能在获得专利保护为时已晚之前,无法确定我们的研发成果中可申请专利的方面。因此,我们可能无法阻止竞争对手在所有这些领域和地区开发竞争药物并将其商业化。
专利可能被宣布无效,专利申请可能因多种原因而不被批准,包括已知或未知的先前技术、专利申请中的缺陷或基础发明或技术缺乏新颖性。尽管我们与有权获取我们研发成果的机密或可申请专利的方面的各方签订了保密和保密协议,例如我们的员工、公司合作者、外部科学合作者、合同制造商、顾问、顾问和任何其他第三方,但这些各方中的任何一方都可能违反此类协议,并在提交专利申请之前披露此类成果,从而危及我们寻求专利保护的能力。此外,科学文献中的发现发表往往落后于实际发现,美国和其他司法管辖区的专利申请通常在申请后18个月才公布,或者在某些情况下根本不公布。因此,我们不能确定我们是第一个在我们的专利或未决专利申请中要求保护的发明,或者我们是第一个为此类发明申请专利保护的公司。此外,中国、欧洲专利局和美国都采用了先申请专利的制度,在这种制度下,谁先申请专利,谁就会
71
目录表
如果满足所有其他可专利性要求,则授予该专利。在先申请制度下,第三方可以被授予与我们发明的技术有关的专利。
专利申请中权利要求的覆盖范围可以在专利发布前大幅缩小,权利要求的范围在专利发布后可以重新解释。即使我们目前或将来许可或拥有的专利申请以专利的形式发布,它们也不会以将为我们提供任何有意义的保护、阻止竞争对手或其他第三方与我们竞争或以其他方式为我们提供任何竞争优势的形式发布。此外,生物技术和制药公司的专利地位普遍高度不确定,涉及复杂的法律和事实问题,近年来一直是许多诉讼的对象。因此,我们的专利权的颁发、范围、有效性、可执行性和商业价值都具有高度的不确定性。
专利的颁发对于我们的发明性、范围、有效性或可执行性并不是决定性的,我们的专利可能会在任何国家的法院或专利局受到挑战。我们可能会将现有技术的第三方预发行提交给美国专利商标局(USPTO),或者参与反对、派生、撤销、重新审查、授权后和各方间在外国司法管辖区对我们的专利权或其他人的专利权提出质疑的审查、干预程序或类似程序。任何此类提交、诉讼或诉讼中的不利裁决可能会缩小我们专利权的范围或使其无效,允许第三方将我们的技术或批准的药物商业化并在不支付费用的情况下与我们直接竞争,或者导致我们无法在不侵犯、挪用或以其他方式侵犯第三方专利权的情况下生产或商业化候选药物和批准的药物。此外,我们可能不得不参与美国专利商标局宣布的干扰程序,以确定发明的优先权,或在授予后的挑战程序中,例如在外国专利局的异议中,挑战我们的发明的优先权或我们的专利和专利申请的其他可专利性特征。此类挑战可能导致专利权的丧失、排他性的丧失,或专利主张的缩小、无效或无法执行,这可能会限制我们阻止他人使用类似或相同的技术和产品或将其商业化的能力,或限制我们的技术和候选药物的专利保护期限。即使最终结果对我们有利,这样的程序也可能导致大量成本,并需要我们的科学家和管理层花费大量时间。因此,我们不知道我们的任何技术或候选药物是否会受到有效和可执行的专利的保护或继续受到保护。我们的竞争对手或其他第三方可能能够通过以非侵权方式开发类似或替代技术或产品来规避我们的专利。
此外,尽管可能有各种延期,但专利的有效期及其提供的保护是有限的。例如,已批准的疗法可能在相关专利到期后面临仿制药的竞争,或者如果它们甚至在到期之前就被挑战和失效。仿制药制造商可能会在法庭上挑战我们专利的范围、有效性或可执行性,我们可能无法成功地执行或捍卫这些知识产权,因此可能无法独家开发或营销相关产品,这将对该产品的任何潜在销售产生重大不利影响。我们的候选药物的已颁发专利和未决专利申请,如果已颁发,预计将在本年度报告的“商业-知识产权”中描述的不同日期到期。在我们已颁发的专利或我们未决专利申请中可能颁发的专利到期后,我们将无法向潜在竞争对手主张此类专利权,我们的业务和运营结果可能会受到不利影响。
考虑到新药候选药物的开发、测试和监管审查所需的时间,保护这些候选药物的专利可能会在这些药物商业化之前或之后不久到期。因此,我们的专利和专利申请可能没有为我们提供足够的权利,以排除其他人将与我们的产品相似或相同的产品商业化。此外,我们的一些专利和专利申请未来可能会与第三方共同拥有。如果我们无法获得任何第三方共同所有人在此类专利或专利申请中的权益的独家许可,这些共同所有人可能能够将他们的权利许可给其他第三方,包括我们的竞争对手,而我们的竞争对手可以销售竞争产品和技术。此外,我们可能需要我们专利的任何此类共同所有人的合作,以便针对第三方强制执行此类专利,而此类合作可能不会提供给我们。上述任何一项都可能对我们的竞争地位、业务、财务状况、经营结果和前景产生重大不利影响。
我们可能无法在世界各地保护我们的知识产权,也无法防止第三方的不公平竞争。
在全球所有国家/地区申请、起诉、维护和保护候选药物的专利对我们来说可能非常昂贵,而且我们在一些非美国国家的知识产权的范围和力度可能与美国不同。此外,某些非美国国家的法律对知识产权的保护程度与美国法律不同。因此,我们可能无法阻止第三方在美国以外的所有国家/地区实施我们的发明。或在美国或非美国司法管辖区销售或进口使用我们的发明制造的药物。竞争对手可能会在我们没有获得专利保护的司法管辖区使用我们的技术来开发他们自己的药物,此外,可能会将其他侵权药物出口到我们有专利保护但执法权不如美国司法管辖区的其他司法管辖区
72
目录表
这些药物可能与我们未来批准的药物竞争,我们的专利权或其他知识产权可能不能有效或不足以阻止它们竞争。
我们可能会卷入保护或执行我们的知识产权的诉讼,这可能是昂贵、耗时和不成功的。如果在法庭上或在美国专利商标局或类似的非美国当局提出质疑,我们与我们的药物相关的专利权可能被认定为无效或不可执行。
竞争对手可能侵犯我们的专利权,或挪用或以其他方式侵犯我们的知识产权。为了打击侵权或未经授权的使用,未来可能需要提起诉讼,以强制或捍卫我们的知识产权,保护我们的商业秘密,或确定我们自己的知识产权或其他人的专有权利的有效性和范围。知识产权的执行或保护可能既昂贵又耗时。我们对被认为侵权者提出的任何索赔也可能促使这些当事人对我们提出反索赔,声称我们侵犯了他们的知识产权。我们目前和潜在的许多竞争对手都有能力投入比我们更多的资源来执行和/或保护他们的知识产权。因此,尽管我们做出了努力,但我们可能无法阻止第三方侵犯或挪用我们的知识产权。任何诉讼程序中的不利结果可能会使我们的专利以及未来可能从我们未决的专利申请中颁发的任何专利面临被无效、无法强制执行或被狭隘地解释的风险。此外,由于知识产权诉讼需要大量的披露,在这类诉讼期间,我们的一些机密信息可能会因披露而被泄露。
在美国的专利诉讼中,被告在地区法院或专利商标和上诉委员会中声称专利无效或不可强制执行的反诉是司空见惯的,第三方可以基于多种理由断言专利无效或不可强制执行。第三方也可以向美国或国外的行政机构提出类似的索赔,即使在诉讼范围之外也是如此。这些机制包括单方面重新考试,各方间在非美国司法管辖区的审查、授予后审查、派生和同等程序,如反对程序。这类诉讼可能会导致我们的专利被撤销或修改,使其不再涵盖和保护我们的候选药物。在法律上断言无效和不可执行之后的结果是不可预测的。例如,关于我们专利的有效性,我们不能确定没有我们、我们的专利律师和专利审查员在起诉期间不知道的无效的先前技术。如果被告以无效和/或不可执行性的法律主张获胜,我们将失去对候选药物的至少部分甚至全部专利保护。这种专利保护的丧失可能会对我们的业务产生实质性的不利影响。
我们可能无法防止我们的商业秘密或机密信息被盗用,特别是在法律可能不像美国那样充分保护这些权利的国家。此外,由于与知识产权诉讼相关的大量发现,在此类诉讼期间,我们的一些机密信息可能会因披露而被泄露。
如果我们因侵犯第三方的知识产权而被起诉,这类诉讼可能代价高昂且耗时,并可能阻止或推迟我们的候选药物的开发或商业化。
我们的商业成功在一定程度上取决于我们避免侵犯第三方的专利和其他知识产权。我们知道,在我们正在开发候选药物的领域中,存在着属于第三方的其他已颁发专利。也可能有我们目前不知道的第三方专利或专利申请,考虑到我们运营的动态领域,很可能会颁发与我们业务的某些方面相关的额外专利。在生物技术和制药业中,一般都有大量涉及专利和其他知识产权的诉讼和其他索赔和程序。随着生物技术和制药行业的扩张以及更多专利的颁发,我们的候选药物可能会引发侵犯他人专利权的索赔的风险增加。
第三方可能会断言我们使用技术侵犯了他们的专利或其他专有权利。对这些索赔的辩护,无论其是非曲直,都可能涉及巨额诉讼费用,并转移我们的技术人员、管理人员或两者的正常责任。如果第三方成功起诉我们侵犯他们的知识产权,我们可能会受到禁令或其他衡平法救济,这可能会阻止我们开发和商业化我们的一个或多个候选药物。我们还可能不得不支付大量损害赔偿,包括故意侵权情况下的三倍损害赔偿金和律师费,或者重新设计我们的侵权候选药物,这可能是不可能的,或者需要大量的时间和成本。如果在任何此类诉讼中出现不利结果,甚至在没有诉讼的情况下,我们可能需要从第三方获得许可证,以推进我们的研究或允许我们的候选药物商业化。任何这样的许可证都可能在合理的条款下无法获得,或者根本无法获得。如果我们无法获得这样的许可证,我们将无法进一步开发和商业化我们的一个或多个候选药物,这可能会严重损害我们的业务。我们也可以选择签订许可协议,以了结专利侵权索赔或在诉讼前解决纠纷,任何此类许可协议都可能要求我们支付版税和其他费用,这可能会严重损害我们的业务。
73
目录表
知识产权诉讼可能会导致不利的宣传,损害我们的声誉,增加我们的运营损失,导致我们普通股的市场价格下跌。
在任何知识产权诉讼过程中,可能会公布听证会、动议或其他临时程序或事态发展的结果,如果证券分析师或投资者认为这些结果是负面的,可能会对我们普通股的市场价格产生重大不利影响。此类诉讼或诉讼可能大幅增加我们的运营亏损,并减少可用于开发活动或任何未来销售、营销或分销活动的资源。我们可能没有足够的财政或其他资源来适当地进行此类诉讼或法律程序。我们的一些竞争对手可能比我们更有效地承担这类诉讼或诉讼的费用,因为他们有更多的财政资源。专利诉讼或其他诉讼的发起和继续所产生的不确定性可能会对我们在市场上的竞争能力产生重大不利影响。
获得和维护我们的专利保护有赖于遵守政府专利机构提出的各种程序、文件提交、费用支付和其他要求,如果不符合这些要求,我们的专利保护可能会减少或取消。
任何已颁发专利的定期维护费应每年向美国专利商标局和大多数外国司法管辖区支付,或在专利有效期内分几个阶段支付。美国专利商标局和各种非政府专利机构要求在专利申请过程中遵守一些程序、文件、费用支付和其他类似条款。虽然在许多情况下,根据适用的规则,通过支付滞纳金或通过其他方式可以纠正疏忽失效,但在某些情况下,不遵守规定可能会导致专利或专利申请的放弃或失效,从而导致相关法域的专利权部分或全部丧失。可能导致专利或专利申请被放弃或失效的不合规事件包括未能在规定的期限内对官方行动做出回应,未支付费用,以及未能适当地使其合法化并提交正式文件。在这种情况下,我们的竞争对手可能会进入市场,这将对我们的业务产生实质性的不利影响。
如果我们没有为我们可能开发的任何候选药物获得专利期限延长和数据排他性,我们的业务可能会受到实质性损害。
根据FDA对我们可能开发的任何候选药物的上市批准的时间、期限和细节,我们的一项或多项美国专利可能有资格根据1984年的药品价格竞争和专利期限恢复行动或Hatch Waxman修正案获得有限的专利期延长。Hatch Waxman修正案允许专利展期最长为五年,作为对临床试验和FDA监管审查过程中失去的专利期的补偿。在其他外国法域也可能存在类似的延展权。一项专利期限的延长不得超过自药品批准之日起共计十四年的时间,只能延长一项专利,并且只能延长涉及批准的药物、其使用方法或者制造方法的权利要求。但是,我们可能因为在测试阶段或监管审查过程中未能进行尽职调查、未能在适用的最后期限内提出申请、未能在相关专利到期前提出申请或未能满足适用的要求等原因而无法获得延期。此外,专利保护的适用期限或范围可能比我们要求的要短。此外,除了新的试点方案外,中国还没有建立专利期限延长制度,试点方案的实施可能不会很快发生。因此,我们在中国拥有的专利还没有资格因在临床试验和监管审查过程中失去的专利期而被延长。如果我们无法获得专利期限的延长,或者如果任何此类延长的期限比我们要求的要短,我们的竞争对手可能会在我们的专利到期后获得竞争产品的批准,我们的业务、财务状况、运营结果和前景可能会受到实质性损害。
专利法的改变可能会降低专利的总体价值,从而削弱我们保护候选药物的能力。
美国最近颁布并正在实施范围广泛的专利改革立法。美国最高法院最近的裁决缩小了某些情况下可获得的专利保护范围,并在某些情况下削弱了专利所有者的权利。除了对我们未来获得专利的能力的不确定性增加之外,这种事件的结合也造成了对一旦获得专利的价值(如果有的话)的不确定性。根据美国国会、联邦法院和美国专利商标局的决定,管理专利的法律和法规可能会以不可预测的方式发生变化,从而削弱我们获得新专利或强制执行我们现有的专利和未来可能获得的专利的能力。外国司法管辖区的法律可能会有类似的变化,可能会影响我们的专利权或其他知识产权的价值。
如果我们不能保护我们的商业秘密的机密性,我们的商业和竞争地位将受到损害。
除了我们已颁发的专利和未决的专利申请外,我们还依赖商业秘密,包括未获专利的技术诀窍、技术和其他专有信息,以保持我们的竞争地位并保护我们的候选药物。我们寻求
74
目录表
保护这些商业秘密,部分方法是与有权接触这些商业秘密的各方签订保密和保密协议,如我们的员工、企业合作者、外部科学合作者、赞助研究人员、顾问、顾问和其他第三方。我们还与我们的员工和顾问签订保密和发明或专利转让协议。然而,这些各方中的任何一方都可能违反此类协议并披露我们的专有信息,我们可能无法就此类违规行为获得足够的补救措施。强制执行一方非法披露或挪用商业秘密的主张可能是困难、昂贵、耗时的,结果是不可预测的。如果我们的任何商业秘密被竞争对手合法获取或独立开发,我们将无权阻止竞争对手使用该技术或信息与我们竞争,我们的竞争地位将受到损害。
我们可能会受到指控,称我们的员工错误地使用或披露了其前雇主所谓的商业秘密。
我们的许多员工,包括我们的高级管理人员,以前曾受雇于其他生物技术或制药公司,包括我们的竞争对手或潜在竞争对手。其中一些员工,包括我们的每一位高级管理层成员,都签署了与以前的雇佣有关的所有权、保密和竞业禁止协议。尽管我们努力确保我们的员工在为我们工作时不使用他人的专有信息或专有技术,但我们可能会受到指控,即我们或这些员工使用或披露了任何此类员工前雇主的知识产权,包括商业秘密或其他专有信息。我们不知道有任何与这些事项或与我们高级管理层的协议有关的威胁或悬而未决的索赔,但未来可能需要提起诉讼来抗辩此类索赔。如果我们不能为任何此类索赔辩护,除了支付金钱损害赔偿外,我们还可能失去宝贵的知识产权或人员。即使我们成功地对这类索赔进行了辩护,诉讼也可能导致巨额成本,并分散管理层的注意力。
知识产权不一定能保护我们免受对我们竞争优势的所有潜在威胁。
我们的知识产权所提供的未来保护程度是不确定的,因为知识产权具有局限性,可能无法充分保护我们的业务,或使我们能够保持竞争优势。以下示例是说明性的:
75
目录表
与企业反向资本重组和整合相关的风险
作为一家上市公司,我们已经产生了显著增加的费用和行政负担,这可能会对我们的业务、财务状况和运营结果产生不利影响。
作为一家新上市公司,特别是在我们不再是一家新兴的成长型公司或规模较小的报告公司之后,我们作为上市公司已经并将继续面临更多的法律、会计、行政和其他成本和支出,这些成本和支出是我们作为私人公司没有发生的。萨班斯-奥克斯利法案,包括第404条的要求,以及后来由美国证券交易委员会(“美国证券交易委员会”)实施的规则和法规,2010年的多德-弗兰克华尔街改革和消费者保护法及其颁布和即将颁布的规则和法规,上市公司会计监督委员会和证券交易所,要求上市公司承担额外的报告和其他义务。遵守上市公司的要求增加了成本,并使某些活动更加耗时。其中一些要求要求我们进行我们以前没有做过的活动。我们的管理层和其他人员也已经并将继续投入大量时间来实施这些合规倡议。此外,还产生了与美国证券交易委员会报告要求相关的额外费用。此外,如果在遵守这些要求方面发现任何问题(例如,如果审计师发现财务报告的内部控制存在重大缺陷或重大缺陷),我们可能会产生纠正这些问题的额外费用, 而这些问题的存在可能会对我们的声誉或投资者对我们的看法产生不利影响。购买董事和高级职员责任险的费用也更高。作为一家上市公司,与我们的地位相关的风险可能会使我们更难吸引和留住合格的人担任董事会成员或高管。这些细则和条例规定的额外报告和其他义务增加了法律和财务合规成本以及相关法律、会计和行政活动的成本。这些增加的成本要求我们转移大量资金,否则这些资金本可以用于扩大我们的业务和实现战略目标。股东和第三方的宣传努力也可能促使治理和报告要求发生更多变化,这可能会进一步增加成本。
我们符合《证券法》所指的新兴成长型公司和较小报告公司的资格,如果我们利用新兴成长型公司可获得的某些披露要求豁免,可能会降低我们的普通股对投资者的吸引力,并可能使我们的业绩更难与其他上市公司的业绩进行比较。
我们符合《证券法》第2(A)(19)节所界定的“新兴成长型公司”的资格,该条款经《就业法案》修订。因此,只要我们继续是一家新兴成长型公司,我们就有资格并可能利用某些适用于其他非新兴成长型公司的上市公司的各种报告要求的豁免,包括(I)根据萨班斯-奥克斯利法案第404(B)条关于财务报告的内部控制的审计师认证要求的豁免,(Ii)豁免薪酬发言权、频率发言权和黄金降落伞投票要求,以及(Iii)在我们的定期报告和委托书中关于高管薪酬的披露义务减少。我们将一直是一家新兴的成长型公司,直到:(I)财政年度的最后一天(A)托特纳姆首次公开募股(IPO)结束五周年后,(B)我们的年总收入至少为10.7亿美元,或(C)根据《交易法》,我们被视为“大型加速申报公司”,如果截至我们最近完成的第二财季最后一个营业日,非关联公司持有的我们普通股的市值超过7.00亿美元,就会发生这种情况;或(Ii)我们在之前三年期间发行了超过10亿美元的不可转换债务证券的日期。
此外,《就业法案》规定,新兴成长型公司可以利用延长的过渡期来遵守新的或修订后的会计准则。这允许新兴成长型公司推迟采用某些会计准则,直到这些准则适用于私营公司。我们已选择利用这一延长的过渡期,因此,我们可能会在非上市公司需要采用新的或修订的会计准则的相关日期采用该等准则,而不是其他上市公司所要求的日期。因此,我们的财务报表可能无法与截至上市公司生效日期遵守新的或修订的会计声明的公司进行比较。
此外,由于截至2021年6月30日,我们非关联公司持有的股票市值不到7亿美元,在截至2021年12月31日的财年中,我们的年收入不到1亿美元,因此我们也是一家“较小的报告公司”。在任何一年,如果(I)在最近结束的财年中截至6月30日,非关联公司持有的我们股票的市值低于2.5亿美元,或(Ii)在最近结束的财年中,我们的年收入低于1亿美元,并且截至6月30日,非关联公司持有的股票的市值低于7亿美元,我们可能仍然是一家规模较小的报告公司。如果我们是一家较小的报告公司,当我们不再是一家新兴的成长型公司时,我们可能会继续依赖较小的报告公司可以获得的某些披露要求的豁免。具体地说,作为一家较小的报告公司,我们可能会选择在我们的Form 10-K年度报告中只公布最近两个财政年度的经审计财务报表,与新兴成长型公司类似,较小的报告公司减少了有关高管薪酬的披露义务。
76
目录表
我们无法预测投资者是否会因为我们依赖这些豁免而发现我们的普通股吸引力下降。如果一些投资者因此发现我们的普通股吸引力下降,我们的普通股交易市场可能会变得不那么活跃,我们的股价可能会更加波动。
与我们普通股相关的风险
我们修订和重述的公司注册证书以及修订和重述的章程中的条款可能会使合并、要约收购或代理权竞争变得困难,从而压低我们普通股的交易价格。
我们修订和重述的公司注册证书以及修订和重述的章程中的条款可能会阻止、推迟或阻止股东可能认为有利的合并、收购或其他控制权变化,包括股东可能因持有我们的普通股股份而获得溢价的交易。这些条款还可能限制投资者未来可能愿意为我们普通股股票支付的价格,从而压低我们普通股的市场价格。这些规定包括:
我们修订和重述的公司注册证书以及修订和重述的章程中的这些和其他条款可能会使股东或潜在收购者更难获得对我们董事会的控制权或发起当时董事会反对的行动,包括推迟或阻碍合并、要约收购或委托书竞争。这些条款的存在可能会对我们普通股的价格产生负面影响,并限制股东在公司交易中实现价值的机会。
我们未来发行的债务或股权证券可能会对我们普通股的市场价格产生不利影响。
未来,我们可能会尝试通过增发普通股或发行债务或其他股权证券(包括商业票据、中期票据、优先或次级票据、可转换为股权的债务证券或优先股)来获得融资或进一步增加资本资源。未来的临床试验、商业化努力和收购可能需要大量额外资本,而不是运营现金。我们预计将通过额外发行股票、公司债务和/或运营现金的组合来获得收购所需的资本。
增发普通股或其他股权证券或可转换为股权的证券可能会稀释我们现有股东的经济和投票权,或降低我们普通股的市场价格,或两者兼而有之。清算后,此类债务证券和优先股的持有人以及其他借款的贷款人将优先于普通股持有人获得我们可用资产的分配。可转换为股权的债务证券可根据转换比率进行调整,根据这些调整,某些事件可能会增加转换后可发行的股权证券的数量。优先股如果发行,可能会优先于清算分配或优先于股息支付,这可能会限制我们向普通股持有人支付股息的能力。我们在未来的任何发行中发行证券的决定将取决于市场状况和其他我们无法控制的因素,这些因素可能会对我们未来发行的金额、时间和性质产生不利影响。
77
目录表
一般风险因素
不能保证我们将能够遵守纳斯达克的持续上市标准。
如果纳斯达克因未能达到纳斯达克的上市标准而将我们的普通股或认股权证在其交易所退市,我们和我们的股东可能面临重大的不利后果,包括:
我们普通股的价格可能会波动。
一般的股票市场和生物技术股票市场都经历了极端的波动。与在全国证券交易所交易并拥有大量公开流通股的较大、较成熟的公司的股票相比,像我们这样的较小公司的普通股市场具有显著的价格波动,而我们普通股的股价比这些较大、较成熟的公司的股票价格更不稳定,并将在无限期的未来继续存在。
我们普通股的价格可能会因各种因素而波动,包括:
无论我们的经营业绩如何,这些市场和行业因素都可能大幅降低我们普通股的市场价格。
78
目录表
项目1B。未解决的员工意见
不适用。
第二项。属性
到目前为止,我们还没有任何自有物业。我们从美国的独立第三方那里租赁了许多物业。我们租用的盐湖城总部用于金融、临床开发、临床运营、转化医学和业务运营。我们租用的马里兰州东北部工厂用于制造和研发活动。我们新租赁的马里兰州埃尔克顿工厂将用于提高我们的制造能力。我们认为,我们的设施对于目前的目的是适当和充足的,我们的生产能力得到了很大程度的利用。
以下摘要阐述了我们租赁物业的详细情况:
第3项。法律诉讼
我们目前不是任何实质性法律程序的一方。然而,在正常的业务过程中,我们可能会不时地卷入法律程序。我们无法预测任何此类法律程序的结果,尽管存在潜在的结果,但由于辩护和和解成本、管理资源转移和其他因素,其存在可能对我们产生不利影响。截至本年度报告日期,吾等并不知悉有任何针对吾等、吾等高级职员或吾等董事的未决或威胁诉讼或行政诉讼,可能会对吾等的业务、财务状况或经营业绩造成重大不利影响。
项目4。煤矿安全信息披露
不适用。
79
目录表
第二部分
第五项。注册人普通股市场、相关股东事项与发行人购买股权证券
市场信息
我们的普通股和公开交易的权证在纳斯达克上交易,代码分别为“CLNN”和“CLNNW”。
持有者
截至2022年3月8日,我们的普通股共有63,138,351股已发行和流通股,由80名登记在册的股东持有。登记在册的股东数量是从我们的转让代理的记录中确定的,不包括其股份以各种证券经纪人、交易商和注册结算机构的名义持有的受益所有者。
分红
我们打算保留所有可用资金和未来的任何收益,为我们业务的增长和发展提供资金。我们从未宣布或支付过普通股的现金股利,在可预见的未来,我们也不打算支付现金股利。我们宣布分红的能力受到我们签订的融资条款或其他协议的限制。未来的债务或其他融资安排也可能包含禁止或限制我们普通股可能宣布或支付的股息金额的条款。投资者不应期望获得现金股利而购买我们的普通股。
未来宣布派息的任何决定将由本公司董事会酌情决定,并将取决于本公司的财务状况、经营结果、资本要求、一般业务状况以及本公司董事会可能认为相关的其他因素。
最近出售的未注册证券
2021年2月1日,在我们2020股票计划的注册声明生效之前,我们向我们的员工、顾问和其他服务提供商授予了期权,根据我们的2020股票计划,我们可以每股6.55美元的行使价购买我们总计130,000股普通股。此次发行的依据是第4(A)(2)节规定的《证券法》登记要求的豁免。
发行人及关联购买人购买股权证券
没有。
项目6. [已保留]
80
目录表
第7项。管理层对财务状况和经营成果的探讨与分析
以下对本公司财务状况和经营结果的讨论和分析应与本年度报告Form 10-K中其他部分包含的合并财务报表和相关附注一起阅读。本讨论包含前瞻性陈述,反映了我们目前对可能影响我们未来财务状况或经营结果的事件和财务趋势的预期、希望、信念、意图、战略、估计和假设。实际结果和事件的时间可能与这些前瞻性陈述中所载的大不相同,原因包括本年度报告10-K表格中其他部分“有关前瞻性陈述的警示说明”和“风险因素”章节中讨论的那些因素。除文意另有所指外,就本节而言,术语“我们”、“我们”、“公司”或“我们”意指Clene Inc.及其合并子公司的业务和运营。
业务概述
我们是一家临床阶段的制药公司,致力于新型清洁表面纳米技术(CSN)的发现、开发和商业化®“)治疗学。CSN®治疗药物由过渡元素的原子组成,当这些元素以纳米晶体的形式组装时,具有异常高的独特催化活性,而这些相同元素中没有以块状形式存在。这些催化活动驱动、支持和维持患病、应激和受损细胞内有益的代谢和能量细胞反应。
我们受专利保护的专有地位使我们有潜力开发一条广泛而深入的新型CSN管道®治疗对人类健康有很大影响的一系列疾病。我们从2013年开始,创新了一个电晶体化学药物开发平台,该平台借鉴了纳米技术、等离子体和量子物理、材料科学和生物化学的进步。我们的平台工艺产生了具有刻面结构和表面的纳米晶体,这些结构和表面没有伴随其他生产方法的化学表面修饰。许多传统的纳米颗粒合成方法都涉及到在颗粒表面不可避免地沉积潜在的有毒有机残留物和稳定的表面活性剂。合成既无毒又高度催化的稳定纳米晶体已经克服了在利用过渡金属催化活性用于人类治疗方面的这一重大障碍。
我们的清洁表面纳米晶体的催化活性比我们已经比较评估的其他多种商业可获得的纳米粒子高出许多倍,这些纳米粒子是使用各种技术生产的。我们现在拥有多种药物资产,目前正在开发和/或临床试验中,应用于神经学、传染病和肿瘤学。我们的开发和临床工作目前集中在两个领域,解决尚未得到满足的高度医疗需求:第一,与中枢神经系统疾病相关的需求,包括肌萎缩侧索硬化症(ALS)、多发性硬化症(MS)和帕金森病(PD);第二,与新冠肺炎相关的需求,这是一种高度传染性的病毒性呼吸道疾病,具有严重的、有时是致命的并存。
我们目前没有批准用于商业销售的药物,也没有从药物销售中获得任何收入。自成立以来,我们从未盈利,每年都出现运营亏损。我们通过我们的全资子公司dOrbary,Inc.,或通过股东和关联方4Life Research LLC(“4Life”)的独家许可,从膳食补充剂的销售中获得收入。我们预计这些收入与我们的运营费用以及我们预计从我们候选药物的潜在未来销售中产生的收入相比都是很小的,我们目前正在进行临床试验。截至2021年12月31日和2020年12月31日,我们的运营亏损总额分别为5,000万美元和2,020万美元。截至2021年12月31日和2020年12月31日,我们的累计赤字分别为1.633亿美元和1.536亿美元。
我们预计将继续投资于产品开发、销售和营销,并预计未来将出现更多亏损,为我们的运营和进行产品研发提供资金。我们还认识到需要筹集额外资本来全面实施我们的业务计划。我们业务计划的长期延续有赖于从我们的产品中产生足够的收入来抵消开支和资本支出。如果我们不能产生足够的收入并无法获得资金,我们将被迫推迟、减少或取消部分或全部研发计划、产品组合扩展、商业化努力或资本支出,这可能会对我们的业务前景、满足长期流动性需求的能力产生不利影响,或者我们可能无法继续运营。
我们临床项目的最新发展
我们有一个2/3阶段的注册临床试验,Healey ALS平台试验,目前正在进行中,以确定CNM-Au8的安全性和有效性® 肌萎缩侧索硬化症患者。CNM-AU8结果® 预计将于2022年下半年完成。我们完成了Repair-MS和Repair-PD的第一个剂量队列,这是两个开放标记、研究者盲目的第二阶段临床试验,证明了CNM-Au8的靶向参与®对大脑能量代谢物的影响。REPAIR-MS将在2022年继续启动第二个剂量队列。此外,我们正在进行一项名为Visionary-MS的第二阶段临床试验,用于治疗慢性视神经病变的视觉通路缺陷,以评估CNM-Au8的有效性、安全性、耐受性和药代动力学®对于稳定复发的MS患者的再髓鞘形成,由于与COVID大流行相关的挑战,Visionary-MS试验将提前结束。完全非盲目的结果
81
目录表
这项研究的结果预计将在2022年下半年进行。我们预计将于2022年年中推出RESPECT-PD,这是一项治疗PD患者的第二阶段临床试验。最后,我们目前正在进行一项第二阶段的临床试验,以确定锌银液治疗新冠肺炎的有效性和安全性。
我们还支持为肌萎缩侧索硬化症患者提供两个扩展接入计划(“EAP”)。最初的EAP是与马萨诸塞州总医院的Sean M.Healey&AMG ALS中心合作于2019年9月推出的,该项目对新注册人员关闭,但仍在为现有参与者提供服务。第二个EAP最近与Healey ALS平台试验一起在三个参与的临床站点实施。
新冠肺炎大流行的影响
新冠肺炎疫情始于2019年12月,目前已在全球范围内蔓延,已导致多国政府采取措施减缓新冠肺炎疫情的蔓延。新冠肺炎疫情和政府采取的应对措施对企业和商业产生了直接和间接的重大影响,因为出现了劳动力短缺,供应链中断,设施和生产暂停。新冠肺炎疫情的未来发展及其对我们业务和运营的影响仍然不确定。新冠肺炎大流行可能会影响我们启动和完成临床前研究的能力,推迟未来临床试验的启动,扰乱监管活动,或对我们的业务和运营产生其他不利影响。特别是,我们和我们的第三方合同研究机构(“CRO”)面临的中断可能会影响我们启动和完成临床前研究的能力,导致生产中断,或在临床试验地点造成延误。新冠肺炎疫情已经对金融市场造成了重大干扰,并可能继续造成此类干扰,这可能会影响我们筹集更多资金支持运营的能力。此外,新冠肺炎疫情对全球经济产生了重大影响,可能会对我们的业务和运营产生不利影响。
我们正在监测新冠肺炎疫情对我们的业务和财务报表的潜在影响。虽然新冠肺炎疫情导致了各种研究限制,并暂停了我们的某些临床试验,但这些影响是暂时的,到目前为止,我们还没有因为新冠肺炎疫情而经历重大业务中断或资产账面价值减值损失。我们不知道有任何具体的相关事件或情况需要我们修改财务报表中反映的估计。新冠肺炎疫情将在多大程度上直接或间接影响我们的业务、运营结果和财务状况,包括计划及未来的临床试验和研发成本,将取决于极不确定的未来发展,包括可能出现的有关新冠肺炎的新信息、采取的遏制或治疗措施以及相关影响的持续时间和强度。
Tottenham和Clene Nanomedine的反向资本重组
于2020年12月30日(“截止日期”),我们完成了之前宣布的与托特纳姆收购第一有限公司(“托特纳姆”)的业务合并(“反向资本重组”)。在反向资本重组结束时,Clene Inc.收购了已发行和已发行的Clene Nanomedicine,Inc.(“Clene Nanomedicine”)普通股的100%,以换取向Clene Nanomedicine普通股股东发行的54,339,012股Clene Inc.普通股,面值0.0001美元(“普通股”),其中2,716,958股将发行并托管,以履行任何赔偿义务。在反向资本重组完成六个月的周年纪念日之后,托管股票被不受限制地释放。
于反向资本重组结束时,Clene Nanomedicine普通股的每股购股权被注销,其交换持有人获得0.1320份新发行的普通股期权,相当于反向资本重组交换比率的95%。此外,我们向购股权持有人发放(I)2020年计划项下370,101股限制性股票奖励的权利,以补充上文讨论的Clene Nanomedine普通股股东以托管方式持有的5%收盘价股份,以及(Ii)向期权持有人发放1,136,961股限制性股票奖励的权利,以补充将于实现里程碑时或有向某些Clene Nanomedine股东发放的盈利付款。有关里程碑的详细信息,请参阅“赚取股份”。
在实施反向资本重组和2020年管道发行(讨论如下)后,立即有59,526,171股普通股已发行和流通。
赚得股
关于反向资本重组,Clene Nanomedicine的某些普通股股东有权获得盈利付款(“Clene Nanomedicine或有盈利”),托特纳姆的前高级管理人员和董事以及Norwich Investment Limited(统称为“初始股东”)有权根据实现下文讨论的里程碑获得盈利付款(“初始股东或有盈利”,两者统称为“或有盈利”)。或有收益已在综合资产负债表中归类为负债,并于
82
目录表
反向资本重组的日期,随后在每个报告日期重新计量为公允价值。或有收益的公允价值变动已记录在截至2021年12月31日和2020年12月31日的综合业务表和综合损失表中。
烟斗产品
截止日期前,我们于2020年12月28日与多家投资者签订了认购协议(“2020 PIPE”)。根据认购协议,我们以每股10.00美元的价格发行了2,239,500股普通股,净收益为2,220万美元。2020年管道的目的是为一般公司费用提供资金。此外,2020年PIPE发行的投资者还获得了认股权证,可以购买相当于2020年PIPE股票数量的一半(1/2)的股份,总计1,119,750股普通股,行使价为每股0.01美元(“PIPE认股权证”),持有期为180天。
2021年5月24日,我们与不同的投资者签订了2021年管道的认购协议。根据认购协议,我们以每股9.63美元的价格发行了960,540股普通股,净收益约为930万美元。2021年管道的关闭基本上与完成与Avenue Venture Opportunities Fund,L.P.(“Avenue”)的贷款协议同时进行,并以此为条件。2021年管道的目的是为马里兰州制造能力的扩大提供资金,并为一般公司费用提供资金。
在2021年7月1日至2021年12月20日期间,不同投资者以每股0.01美元的行权价行使了1,119,750股普通股的管状认股权证。管道权证是在截止日期之前发行的,持有期为180天,于2021年6月28日到期。我们收到了11,198美元的现金收益。
财务概述
我们的经营业绩、财务状况以及财务业绩的期间可比性主要受以下因素影响:
研发费用
新候选药物的发现和开发需要在很长一段时间内投入大量资源,我们战略的核心部分是继续在这一领域进行持续投资。由于这一承诺,我们的候选药物流水线一直在推进和扩大,目前正在调查两种临床阶段的候选药物。
从历史上看,我们几乎所有的研发费用都与CNM-AU8有关®,我们的主要资产。我们的研究和开发费用受我们现有产品线的时间和进展以及新药物计划开始的时间和数量的影响。处于临床开发后期阶段的候选药物通常比处于临床开发早期阶段的候选药物具有更高的开发成本,这主要是由于较大临床试验的每个患者的临床试验地点费用、开设和监测临床地点的成本、CRO活动和制造费用。我们预计,由于开发我们的候选药物的临床试验费用增加,我们的研究和开发费用将大幅增加。
研究和开发成本在发生时计入运营费用。研发成本包括工资和人事支出,包括从事研发职能的员工的工资和相关福利和股票薪酬支出;支持我们临床试验的临床试验用品和材料;支付给CRO、主要研究人员和临床试验地点的费用;与临床前活动相关的成本;咨询成本;以及分配的管理费用,包括租金、设备、水电费、折旧、保险和设施维护成本。我们将不可退还的商品和服务预付款计入,这些预付款最初将作为资产用于未来的研发活动,然后在收到货物或提供服务时作为费用使用,而不是在付款时使用。
我们的临床试验应计过程寻求核算与进行临床试验相关的CRO、顾问合同和临床场地协议下的义务所产生的费用。这些合同的财务条款需要进行谈判,不同的合同会有所不同,可能会导致支付流量与根据此类合同向我们提供材料或服务的期限不匹配。我们通过将适当费用与服务和努力支出的期间相匹配,在合并财务报表中反映适当的试验费用。如果向CRO预付款,付款将被记录为预付资产,将在履行合同服务的一段时间内支出。
83
目录表
一般和行政费用
一般和行政费用主要包括工资和人事费用,包括薪金和相关福利以及股票薪酬费用;法律、会计、税务和信息技术服务的专业费用;董事和高级管理人员保险费;业务发展活动费用;水电费和设施费用;差旅费;租金;咨询费和其他行政费用。
我们预计,未来我们的一般和行政费用将增加,以支持我们药物开发活动的增加,以及我们在获得监管部门对我们候选药物快速推进的临床试验的批准之前建立我们的商业能力。这些增长可能包括增加员工人数,增加股票薪酬支出,扩大基础设施,包括在监管部门批准之前进行的某些销售和营销活动,以及增加保险费用。我们还预计,与上市公司相关的法律、合规、会计以及投资者和公关费用将会增加。
其他收入(费用),净额
其他收入(支出)净额主要包括(I)本公司(A)优先股权证负债、(B)普通股认股权证负债和(C)或有收益的公允价值变动;(Ii)因应付票据公允价值变动而产生的利息支出;(Iii)应付可转换票据和应付票据清偿的损益;(Iv)终止租约的收益;以及(V)澳大利亚研发信贷,如下所述。
我们还收到了非政府实体发放的赠款,这些赠款要求我们遵守赠款附带的条件。赠款收入在发生相关符合资格的费用期间确认,前提是提供赠款的条件已得到满足。我们从澳大利亚政府以现金补贴的形式获得税收优惠,用于与我们的澳大利亚子公司进行的临床试验活动相关的研究和开发活动,这些活动在符合某些条件时被确认为其他收入。
经营成果的构成部分
截至2021年12月31日和2020年12月31日止年度比较
截至2021年12月31日及2020年12月31日止年度的经营业绩如下:
|
|
截至十二月三十一日止的年度, |
|
|
变化 |
|
||||||||||
(单位:千) |
|
2021 |
|
|
2020 |
|
|
美元 |
|
|
% |
|
||||
产品收入 |
|
$ |
570 |
|
|
$ |
176 |
|
|
$ |
394 |
|
|
|
224 |
% |
专利权使用费收入 |
|
|
153 |
|
|
|
30 |
|
|
|
123 |
|
|
|
410 |
% |
总收入 |
|
|
723 |
|
|
|
206 |
|
|
|
517 |
|
|
|
251 |
% |
运营费用: |
|
|
|
|
|
|
|
|
|
|
|
|
||||
收入成本 |
|
|
289 |
|
|
|
65 |
|
|
|
224 |
|
|
|
345 |
% |
研发 |
|
|
28,416 |
|
|
|
15,204 |
|
|
|
13,212 |
|
|
|
87 |
% |
一般和行政 |
|
|
21,996 |
|
|
|
5,151 |
|
|
|
16,845 |
|
|
|
327 |
% |
总运营费用 |
|
|
50,701 |
|
|
|
20,420 |
|
|
|
30,281 |
|
|
|
148 |
% |
运营亏损 |
|
|
(49,978 |
) |
|
|
(20,214 |
) |
|
|
(29,764 |
) |
|
|
147 |
% |
其他收入(费用)合计,净额 |
|
|
39,810 |
|
|
|
1,343 |
|
|
|
38,467 |
|
|
|
2,864 |
% |
所得税前净亏损 |
|
|
(10,168 |
) |
|
|
(18,871 |
) |
|
|
8,703 |
|
|
|
(46 |
)% |
所得税费用 |
|
|
428 |
|
|
|
(406 |
) |
|
|
834 |
|
|
|
(205 |
)% |
净亏损 |
|
$ |
(9,740 |
) |
|
$ |
(19,277 |
) |
|
$ |
9,537 |
|
|
|
(49 |
)% |
收入
在截至2021年12月31日和2020年12月31日的年度里,我们与4Life签订了KHC46和锌元素补充剂的供应协议,在补充剂部门分别产生了60万美元和20万美元的产品收入,这两种膳食补充剂(矿物质)是我们在这两个时期开始供应的。于截至2021年12月31日及2020年12月31日止年度,根据与4Life签订的有关出售KHC46的独家许可协议及附带许可使用费的许可协议,我们的许可使用费收入总额分别为20万美元及30,000美元。有关供应和许可协议的更多详细信息,请参阅我们合并财务报表的附注20。
在这段时间里,我们还通过销售rMetx?znAg免疫增强产品获得了最低限度的产品收入。
84
目录表
收入成本
截至2021年12月31日和2020年12月31日的年度,收入成本分别为30万美元和10万美元,与销售KHC46、锌因子和rMetx膳食补充剂的生产和分销成本有关。
研发费用
截至2021年12月31日和2020年12月31日的年度研究和开发费用如下:
|
|
截至十二月三十一日止的年度, |
|
|
变化 |
|
||||||||||
(单位:千) |
|
2021 |
|
|
2020 |
|
|
美元 |
|
|
% |
|
||||
CNM-AU8 |
|
$ |
11,659 |
|
|
$ |
5,921 |
|
|
$ |
5,738 |
|
|
|
97 |
% |
CNM-ZnAg |
|
|
970 |
|
|
|
1,176 |
|
|
|
(206 |
) |
|
|
(18 |
)% |
未分配 |
|
|
3,542 |
|
|
|
2,471 |
|
|
|
1,071 |
|
|
|
43 |
% |
人员 |
|
|
7,414 |
|
|
|
5,156 |
|
|
|
2,258 |
|
|
|
44 |
% |
基于股票的薪酬 |
|
|
4,831 |
|
|
|
480 |
|
|
|
4,351 |
|
|
|
906 |
% |
总研发 |
|
$ |
28,416 |
|
|
$ |
15,204 |
|
|
$ |
13,212 |
|
|
|
87 |
% |
我们的大部分研发费用与我们的主要候选药物CNM-Au8的开发有关®,包括正在进行的临床试验。与CNM-AU8相关的研发费用增加® 这主要是由于临床开发过程的进展,包括参加Repair-PD、Repair-MS、Visionary-MS和RESPECT-ALS临床试验的人数增加,以及我们参与Healey ALS平台试验的日历付款。未分配研发费用的增加主要是由于与我们在马里兰州埃尔克顿的新租赁设施相关的租金费用增加,以及来自某些赠款的里程碑资金减少;部分被制造和材料费用的减少所抵消。人员和股票薪酬费用的增加是由于我们增加了员工人数。
一般和行政费用
2021年和2020年12月31日终了年度的一般和行政费用如下:
|
|
截至十二月三十一日止的年度, |
|
|
变化 |
|
||||||||||
(单位:千) |
|
2021 |
|
|
2020 |
|
|
美元 |
|
|
% |
|
||||
董事和高级管理人员ʼ保险 |
|
$ |
3,719 |
|
|
$ |
160 |
|
|
$ |
3,559 |
|
|
|
2,224 |
% |
法律 |
|
|
1,518 |
|
|
|
275 |
|
|
|
1,243 |
|
|
|
452 |
% |
财务与会计 |
|
|
3,183 |
|
|
|
1,889 |
|
|
|
1,294 |
|
|
|
69 |
% |
公共关系和投资者关系 |
|
|
887 |
|
|
|
— |
|
|
|
887 |
|
|
|
100 |
% |
人员 |
|
|
3,530 |
|
|
|
1,466 |
|
|
|
2,064 |
|
|
|
141 |
% |
基于股票的薪酬 |
|
|
7,553 |
|
|
|
281 |
|
|
|
7,272 |
|
|
|
2,588 |
% |
其他 |
|
|
1,606 |
|
|
|
1,080 |
|
|
|
526 |
|
|
|
49 |
% |
一般和行政合计 |
|
$ |
21,996 |
|
|
$ |
5,151 |
|
|
$ |
16,845 |
|
|
|
327 |
% |
一般和行政费用增加1,680万美元或327.0%,主要是由于(I)上市公司董事和高级管理人员保险增加,(Ii)上市公司律师费增加,(Iii)我们美国证券交易委员会合规职能产生的财务和会计费用增加,两份S-1表格注册声明的备案费用,改进我们的流程和内部控制的费用,以及各种金融供应商、机构、投资银行家和顾问的费用,(Iv)与我们的公共和投资者关系努力有关的费用增加,(V)信息技术服务费用增加。(Vi)在我们的候选药物快速推进的临床试验获得监管部门批准之前,增加商业前活动的费用,以及(Vii)由于我们增加了员工人数,增加了人员成本和基于股票的补偿费用。
其他收入(费用),净额
2021年和2020年12月31日终了年度的其他收入(支出)净额包括:
85
目录表
税收
美国
我们在美国特拉华州注册成立,在截至2021年12月31日和2020年12月31日的年度内,按21%的税率缴纳美国联邦法定企业所得税。我们还需要缴纳犹他州和马里兰州的州所得税,在截至2021年12月31日和2020年12月31日的财年,税率分别为4.95%和8.25%。截至2021年12月31日和2020年12月31日,由于我们的三年累计亏损状况以及围绕我们在可预见的未来产生税前收入的能力的不确定性,我们对我们的递延净资产计入了全额估值准备金。
澳大利亚
我们的全资附属公司Clene Australia Pty Ltd(“Clene Australia”)于2018年3月5日在澳大利亚成立,于截至2021年12月31日及2020年12月31日止年度分别按25%及27.5%的税率缴纳企业所得税。截至2021年12月31日和2020年12月31日的年度,克莱恩澳大利亚的所得税支出总额分别为40万美元和40万美元。在截至2021年12月31日和2020年12月31日的年度内,我们分别记录了150万美元和320万美元的其他收入,用于分别退还2021年和2020纳税年度与Clene Australia相关的研发抵免。
荷兰
我们的全资子公司CLENE荷兰公司于2021年4月21日在荷兰成立,将按15%的税率缴纳公司所得税,最高可达245,000欧元的应税收入,超过245,000欧元的应纳税所得额将按25%的税率缴纳公司所得税。在截至2021年12月31日的一年中,克莱恩荷兰公司没有应税收入,也没有所得税拨备。
流动性与资本资源
资金来源
自成立以来,我们的运营出现了重大亏损和负现金流。我们预计未来会出现更多亏损,以资助我们的运营和进行产品研发。我们认识到需要筹集额外资本来全面实施我们的业务计划。我们业务计划的长期延续有赖于从我们的产品中产生足够的收入来抵消开支和资本支出。如果我们不能产生足够的收入并无法获得资金,我们将被迫推迟、减少或取消部分或全部研发计划、产品组合扩展、商业化努力或资本支出,这可能会对我们的业务前景、满足长期流动性需求的能力产生不利影响,或者我们可能无法继续运营。
86
目录表
自我们成立以来,我们将几乎所有的资源都投入到我们候选药物的开发上。我们主要通过以下来源为我们的业务提供资金:
我们还获得了对Healey ALS平台试验的间接资金支持,该试验由马萨诸塞州综合医院管理,正在进行CNM-Au8的平台试验®与其他药物相比,如果我们以合理的市场价格进行类似设计的临床试验,成本要低得多。
流动性
截至2021年12月31日及2020年12月31日止年度,本公司的营运亏损分别为5,000万美元及2,020万美元,截至2021年12月31日及2020年12月31日止年度的净亏损分别为970万美元及1,930万美元。截至2021年12月31日,我们的累计赤字为1.633亿美元。截至2021年12月31日和2020年12月31日,我们的现金和限制性现金总额分别为5,030万美元和5,930万美元,截至2021年和2020年12月31日的年度内,我们在运营活动中使用的现金净额分别为3,460万美元和1,890万美元。
自成立以来,我们的运营出现了重大亏损和负现金流。到目前为止,我们还没有产生大量的收入,除非我们成功完成开发并获得监管部门对我们候选药物的批准,否则我们预计不会产生大量的收入。我们预计我们的费用将大幅增加,并在未来导致额外的亏损,以资助我们的运营,特别是当我们推进临床阶段候选药物的开发,继续研究和开发我们的临床前候选药物,并启动这些和其他未来候选药物的更多临床试验并寻求监管机构批准的时候。我们预计,如果我们的候选药物获得监管部门的批准,随着我们准备开始商业化,与法规遵从性以及销售和营销人员有关的费用将大幅增加。
随附的综合财务报表的编制假设我们将继续作为一家持续经营的企业,考虑在正常业务过程中实现资产和偿还负债。我们的长期运营需要获得额外的资本来为我们的运营提供资金。作为我们正在进行的业务计划的一部分,我们将继续寻求通过股权融资筹集更多资本,并可能寻求债务融资或其他资本来源,我们可能会尝试与第三方合作开发我们的候选药物并将其商业化。我们可能无法以可接受的条件获得资本,或者根本无法获得资本。任何融资条款都可能对我们股东的持股或权利产生不利影响。根据我们当前业务计划的结果,我们可能需要实施成本节约措施,包括可能推迟或减少研发计划和商业化努力,最早将于2022年第三季度开始。目前,在没有额外资本的情况下,我们相信我们有足够的资源为我们持续运营到2023年第二季度提供资金。
短期材料现金需求
至少在接下来的12个月里,我们的主要资本需求是为我们的运营提供资金,包括研发、人员、监管和其他与开发我们的主要候选药物CNM-Au8相关的临床试验成本®;以及在我们的候选药物获得监管批准之前支持我们的药物开发和商业前活动的一般和行政成本。
对资金的坚定承诺包括分别在融资和经营租赁义务项下支付约10万美元和90万美元;支付总计200万美元的应付票据利息;以及根据各种协议承诺与我们的制造设施建设相关的资本支出总计60万美元。我们预计主要通过手头现金来满足我们的短期流动性需求。其他资金来源,如果我们需要的话,包括股权融资、债务融资或其他资本来源。
87
目录表
我们在正常业务过程中与CRO签订了临床试验协议,并与供应商签订了临床前研究及其他服务和产品用于运营目的的协议,这些协议可由我们随时取消,但须支付我们在有约束力的采购订单下的剩余义务,在某些情况下,还需支付象征性的提前终止费。这些承诺被认为并不重要。
长期物资现金需求
在接下来的12个月里,我们的主要资本需求是为我们的运营提供资金,包括与开发我们的主要候选药物CNM-AU8®相关的研发、人事、监管和其他临床试验成本;以及在我们的候选药物获得监管部门批准之前支持我们的药物开发和商业前活动的一般和行政成本。我们可以酌情决定,可能会花费额外的资金来启动新的临床试验。未来12个月以后的已知债务包括融资和经营租赁债务项下的付款分别为10万美元和690万美元;应付票据的利息和本金偿还为2400万美元。
资金的使用
截至2021年12月31日和2020年12月31日的年度,我们的现金流如下:
|
|
截至十二月三十一日止的年度, |
|
|||||
(单位:千) |
|
2021 |
|
|
2020 |
|
||
用于经营活动的现金净额 |
|
$ |
(34,624 |
) |
|
$ |
(18,929 |
) |
用于投资活动的现金净额 |
|
|
(1,332 |
) |
|
|
(387 |
) |
融资活动提供的现金净额 |
|
|
27,112 |
|
|
|
69,534 |
|
外汇汇率变动对现金的影响 |
|
|
(85 |
) |
|
|
269 |
|
现金净增(减) |
|
$ |
(8,929 |
) |
|
$ |
50,487 |
|
我们在所有报告期间的现金主要用于资助我们的研发、监管和其他临床试验成本,以及一般公司支出。
经营活动
经营活动中使用的现金净额是指与除投资和融资活动以外的所有活动有关的现金收入和支出。营业现金流是通过调整我们的非现金项目的净亏损和我们的营业资产和负债的净变化而得出的。在截至2021年12月31日的一年中,用于经营活动的现金净额为3460万美元,这是由于经非现金项目调整后净亏损970万美元(2590万美元)以及营业资产和负债净变化100万美元造成的。重要的非现金项目包括我们的(I)与Avenue认股权证相关的普通股认股权证负债的公允价值变化(100万美元),以及(Ii)Clene Nanomedine和初始股东从反向资本重组中获得的或有收益分别为3400万美元和360万美元。该等工具的公允价值变动主要是由于上文“其他收入(开支)”一节所述本公司股价下跌所致。其他重要的非现金项目包括:(A)1,240万美元的股票薪酬支出,这是由于我们增加了员工人数;(B)与实验室和办公设备以及租赁改进有关的折旧支出100万美元;以及(C)与免除购买力平价贷款有关的应付票据清偿收益(60万美元)。我们业务资产和负债的净变化主要是由于以下原因:(A)应付账款和应计负债分别增加130万美元和90万美元,这两种情况下都是由于供应商开具发票和付款的时间,以及(B)由于供应商开具发票和付款的时间以及接收用于研究和开发的金属的时间安排,预付费用和其他流动资产增加了70万美元, 澳大利亚研发应收信贷的减少部分抵消了这一影响。
在截至2020年12月31日的一年中,用于经营活动的现金净额为1,890万美元,这是由于经非现金项目调整后净亏损1,930万美元,总计370万美元,以及营业资产和负债净变化(330万美元)。非现金项目主要包括:(1)100万美元的折旧支出,(2)80万美元的股票补偿支出,(3)1,460万美元优先股权证负债的公允价值变化,(4)Clene Nanomedine或有收益的公允价值变化(1,270万美元),(5)初始股东或有收益的公允价值变化(150万美元),(6)应付可转换票据清偿损失50万美元,及(Vii)应付票据利息增加及债务贴现增加分别为70万元及20万元。我们营业资产和负债的净变化主要是由于以下原因:(A)库存增加20万美元;(B)预付费用和其他流动资产增加280万美元,这是由于对CRO和其他供应商的预付款增加以及澳大利亚研发信贷的增加;(C)应付账款减少30万美元;(D)与Clene Australia相关的应付所得税增加20万美元;(E)由于供应商开具发票和付款的时间安排,应计负债减少30万美元;(F)应付账款减少
88
目录表
对关联方增加10万美元;(G)递延所得税增加30万美元;(H)关联方递延收入增加10万美元;(I)经营租赁债务减少10万美元。
投资活动
在截至2021年12月31日和2020年12月31日的年度内,用于投资活动的现金净额分别为130万美元和40万美元,分别包括购买财产和设备。
融资活动
在截至2021年12月31日的年度内,融资活动提供的现金净额为2,710万美元,主要包括:(I)发行应付票据所得收益2,000万美元,由支付应付票据发售成本50万美元所抵销;(Ii)2021年发行应付票据所得款项930万美元;(Iii)支付与反向资本重组有关的递延发售成本190万美元;(Iv)行使股票期权所得收益40万美元;以及(Ii)支付融资租赁债务20万美元。
在截至2020年12月31日的年度内,融资活动提供的现金净额为6,950万美元,主要包括:(1)发行D系列优先股的收益3,510万美元,(2)反向资本重组和2020年管道收益3,180万美元,被相关递延发行成本400万美元抵销,(3)发行应付可转换票据收益610万美元,(4)发行应付票据收益70万美元,(5)行使股票期权收益10万美元。和(6)支付融资租赁债务20万美元。
马里兰州贷款
2019年2月,我们与马里兰州主要部门住房和社区发展部签订了一项贷款协议(2019年MD贷款)。该协议规定提供50万美元的定期贷款。2019年MD贷款下的未偿还金额按8.0%的年利率计入单利。根据2019年MD贷款,我们同意了积极和消极的契约,我们将一直遵守这些契约,直到到期。这些条款包括提供有关我们公司和业务的信息;限制我们除证券条款以外的普通股或优先股、期权和认股权证的报废、回购或赎回能力;以及我们支付现金或财产红利的能力限制。没有与2019年MD贷款相关的金融契约。2019年MD贷款的违约事件包括到期不付款、破产事件和不遵守契约。我们没有违反任何肯定的公约。未偿还的全部余额将于2034年2月22日到期。2019年MD贷款建立在发行时确定的119,907股普通股(基于反向资本重组前的863,110股C系列优先股)的基础上建立的“幻影股份”。2019年MD贷款规定,还款金额将以本金和应计利息余额或幻影股份价值中较大者为准。我们决定该票据应按公允价值入账。我们在每个报告期结束时记录债务的公允价值。为了对票据进行估值,我们考虑了即将到期的简单利息支出的金额和影子股票的价值。2019年MD贷款的公允价值是根据在纳斯达克上市的CLNN股票的收盘价确定的。
在截至2021年12月31日和2020年12月31日的年度内,分别确认了50万美元的收入和50万美元的支出。本金和应计利息的公允价值分别为60万美元和110万美元,分别计入截至2021年和2020年12月31日的长期应付票据。
塞西尔县贷款
2019年4月,我们与根据马里兰州法律成立的非股份公司Advance Cecil Inc.签订了一项贷款协议(“2019 Cecil贷款”),在执行2019年Cecil贷款时,向美国国税局申请501(C)(3)身份。该协议规定提供10万美元的定期贷款。2019年塞西尔贷款下的未偿还金额按8.0%的年利率计入单利。根据2019年塞西尔贷款,我们同意了平权契约,我们将一直遵守这些契约,直到到期。这些契约包括提供有关我们公司和运营的信息。没有与2019年塞西尔贷款相关的金融契约。根据2019年塞西尔贷款的违约事件包括未能在到期时付款、破产事件和未能遵守契约。我们没有违反任何肯定的公约。未偿还的全部余额将于2034年4月30日到期。2019年塞西尔贷款建立在23,981股普通股(基于反向资本重组前的172,622股C系列优先股)的基础上,在发行时确定。2019年塞西尔贷款规定,偿还金额将是本金和应计利息余额或影子股票价值中的较大者。我们决定该票据应按公允价值入账。我们在每个报告期结束时记录债务的公允价值。为了对票据进行估值,我们考虑了即将到期的简单利息支出的金额和影子股票的价值。2019年塞西尔贷款的公允价值是根据在纳斯达克上市的CLNN股票的收盘价确定的。
89
目录表
在截至2021年12月31日和2020年12月31日的年度内,分别确认了10万美元的收入和10万美元的支出。公允价值10万美元的本金和应计利息分别计入截至2021年12月31日和2020年12月31日的长期应付票据。
大道贷款
2021年5月,我们与Avenue签订了一项贷款协议(2021大道贷款)。该协议规定提供最高3,000万美元的42个月定期贷款。第一批为2,000万美元,其中1,500万美元是在结束时提供的,500万美元是在2021年9月提供的(“第一批”)。我们产生了60万美元的发行成本,其中46,951美元立即支出。剩余的1,000万美元未融资部分(“第2批”)可应我们的要求在2022年12月31日之前提供。第二批的资金取决于:(A)我们通过马里兰州激励计划和/或其他马里兰州计划获得了500万美元的资金;(B)我们在主要终点上取得了统计上显著的结果,或者如果任何研究的总体结果保证进入后续的临床疗效研究,关于以下至少两项临床试验:(I)救援-ALS或Healey ALS平台试验;(Ii)REPAIR-PD;或(Iii)REPAIR-MS(“绩效里程碑1”);(C)我们在2021年5月2日至2022年12月31日期间出售和发行我们的股权证券(包括私募或后续发行)至少收到3,000万美元的净收益;以及(D)我们与Avenue的共同协议。
贷款的年利率为浮动利率,相当于(I)(A)《华尔街日报》不时刊登的最优惠利率或(B)3.25%加(Ii)6.60%的总和。前12个月的付款仅限利息,如果我们达到业绩里程碑1,我们可以将付款延长至(I)12个月(“首次仅限利息期限延长”),以及(Ii)如果(A)我们实现了首次仅限利息期限延长,以及(B)已从第2批中提取,则可延长至最多36个月。2021年8月16日,我们与Avenue相互确认,已实现业绩里程碑1和首次仅限利息期限延长。这笔贷款将在利息期末至2024年12月1日42个月期限届满期间以等额本金的方式摊销。在到期日,除了剩余的未偿还本金和应计利息外,还应支付相当于资金贷款4.25%的额外付款,即90万美元。最后一笔付款被记录为债务溢价,并使用有效利息法在合同期限内摊销。根据ASC 815,最终付款拨备与贷款承办方有关,不会被分流。
根据该协议,吾等向Avenue授予认股权证,以购买115,851股普通股(“Avenue认股权证”),行使价相等于(I)8.63美元(相等于于贷款协议执行前最后一个交易日最后一个交易日结束时厘定的每股五天成交量加权平均价(“VWAP”))或(Ii)现金投资者在3月31日前的下一轮真正股权融资中为我们的普通股支付的最低每股价格,2022年(“下一轮价格”)。于第二批融资后,大道认股权证将自动调整,以包括额外估计145,740股普通股,相当于第二批本金金额的5%,除以(I)每股五(5)天VWAP;于第二批发行日期前最后一个交易日收市时厘定的较低者;或(Ii)下一轮价格。我们根据ASC 815在2021大道贷款开始时计入了第2批认股权证,公允价值和可发行股份将在每个报告期重新计量。在贷款未清偿期间,大道银行也有权自行决定,但没有义务,从协议的第一年到第三年的任何时间。, 将最多500万美元的未偿还贷款本金转换为普通股(“转换特征”),每股价格相当于认股权证规定的股票购买价格的120%。兑换特征须受(I)紧接兑换前七个连续交易日的普通股收市价大于或等于兑换价格及(Ii)与任何该等兑换相关而发行的普通股不超过紧接该等兑换生效日期前二十二个连续交易日普通股总交易量的20%所规限。
根据2021大道的贷款,我们同意了积极和消极的契约,在没有提前还款的情况下,我们在到期时仍将遵守这些契约。这些条款包括提供有关我们公司和业务的信息;限制我们按照证券条款以外的其他方式报废、回购或赎回普通股、期权和认股权证的能力;以及限制我们支付现金或财产红利的能力。与贷款协议相关的财务契约包括维持至少500万美元的最低不受限制的现金和现金等价物;如果我们(I)实现业绩里程碑1,以及(Ii)通过出售和发行我们的股权证券(包括任何管道或后续发行)获得至少3,000万美元的净收益,我们将不再受财务契约的约束。我们没有违反公约。该协议规定了此类贷款的惯常违约事件,包括但不限于不付款、违约、发生重大不利变化或违约、破产和破产。2021大道的贷款以我们除知识产权以外的几乎所有资产为抵押,包括我们的股本和我们子公司的股本,Avenue被授予持续的担保权益。发放贷款的净收益最初分配给认股权证,数额等于其公允价值150万美元,其余部分分配给贷款。已发生融资成本的分配为50万美元,连同认股权证的公允价值和最后付款,分别记为债务折价和债务溢价,并按实际利息法在合同期限内摊销。截至2021年12月31日止年度内, 我们记录的利息支出为140万美元。
90
目录表
关键会计政策和估算
我们对我们的财务状况和经营结果的讨论和分析是以我们的综合财务报表为基础的,这些报表是根据美国公认会计原则编制的。在编制这些财务报表时,我们需要做出影响资产、负债、收入、成本和费用报告金额的估计、假设和判断。我们不断评估我们的估计和判断,我们的实际结果可能与这些估计不同。我们根据过往经验、已知趋势及事件、合约里程碑及其他被认为在当时情况下属合理的因素作出估计,其结果构成对资产及负债的账面价值作出判断的基础,而该等资产及负债的账面价值并非由其他来源轻易可见。
我们认为以下估计是关键的,因为它们涉及重大的估计不确定性,并且已经或合理地可能对我们的财务状况和运营结果产生重大影响。有关其他重要会计政策的说明,请参阅我们的合并财务报表附注2。
或有收益负债
关于反向资本重组,某些股东有权根据某些里程碑的成就获得或有收益付款。根据ASC 815,衍生工具和套期保值根据美国会计准则(“ASC 815”),我们将或有收益归类为综合资产负债表中的负债,该等负债最初于反向资本重组当日按公允价值计量。我们在每个报告日期重新计量负债,并将公允价值变动作为其他收入(费用)、净额和全面亏损的组成部分记录在综合经营报表中。我们使用蒙特卡罗估值模型来估计或有收益的公允价值。不可观测的输入包括预期股价波动率、无风险利率和预期期限。此外,对于一个里程碑,我们估计了新冠肺炎在反向资本重组结束后12个月内完成临床试验并获得临床疗效的显著结果的可能性,这需要重大判断。
截至2021年和2020年12月31日,预期股价波动率分别为105.00和85.00%;无风险利率分别为1.10和0.40个百分点;预期期限分别为4.00年和5.00年。截至2021年12月31日,里程碑3尚未实现,也不是估值模型中的输入,截至2020年12月31日,实现里程碑3的概率在5.80%至11.70%之间。
于截至二零二一年及二零二零年十二月三十一日止年度,Clene Nanomedicine或有盈利的公平值分别录得3,400万美元及1,270万美元;初始股东或有盈利分别录得360万美元及150万美元。
可转换票据
根据2021大道的贷款,未偿还本金中的500万美元受转换功能的约束。根据ASU 2020-06,债务-具有转换和其他期权的债务(分主题470-20)和衍生工具和对冲--实体自有股权的合同(分主题815-40):实体自有股权的可转换票据和合同的会计,我们将这部分归类为综合资产负债表中的可转换票据,并没有从主合同中分离出转换特征。因此,我们将可转换票据作为按其摊销成本计量的单一负债进行会计处理。截至2021年12月31日,可转换票据的价格为460万美元。
普通股认股权证责任
根据2021大道贷款的第1部分,我们向大道授予了大道认股权证。根据ASC 815,我们也确认了根据第二批的潜在提取而发行的第二批权证。我们将权证归类为综合资产负债表中的负债,该等资产负债表在2021 Avenue贷款开始时最初按公允价值计量。我们在每个报告日期重新计量负债,并将公允价值变动作为其他收入(费用)净额的组成部分记录在合并经营报表和全面亏损中。我们使用Black-Scholes期权定价模型估计Avenue认股权证的公允价值,该模型的概率权重与第2批的潜在吸引力有关,这需要重大判断。不可观测的输入包括预期股价波动率、无风险利率、预期期限和提取第2批的概率。
截至2021年12月31日和2021年5月21日,当大道权证发行时,预期股价波动率分别为105.00和90.00%;无风险利率分别为1.20%和0.80%;提取2021大道贷款第二批的概率分别为50.00%和50.00%。截至2021年12月31日,预期期限为3.89至4.39年,截至2021年5月21日,预期期限为5.00年。
91
目录表
在截至2021年12月31日的年度内,我们录得普通股认股权证负债的公允价值变动为100万美元。
所得税
我们采用两步法来确定应确认的税收优惠金额,以此来计入合并财务报表中确认的所得税的不确定性。首先,必须对税收状况进行评估,以确定税务机关在外部审查后维持这种状况的可能性。如果税务状况被认为更有可能持续,则对税务状况进行评估,以确定在合并财务报表中确认的利益金额。可确认的受益金额是在最终和解时实现可能性大于50%的最大金额。此外,我们评估我们的递延税项资产将从未来的应纳税所得额中收回的可能性,如果我们基于现有证据的权重认为所有或部分递延税项资产更有可能无法变现,则通过计入所得税费用建立估值拨备。透过估计预期未来应课税溢利及考虑审慎及可行的税务筹划策略,评估收回递延税项资产的潜力。对这些因素的估计需要重要的判断。根据我们对这些因素的评估,由于从这些项目实现收益的不确定性,我们没有记录净营业亏损或研发税收抵免或其他递延税项资产的所得税优惠。
基于股票的薪酬
我们使用公允价值为基础的方法来核算基于股票的薪酬安排,以计算与所有基于股票的支付相关的成本,包括股票期权和股票奖励。公允价值是在受让人被要求提供服务以换取期权奖励和基于服务的股票奖励的期间内确认的,这段期间被称为必要的服务期(通常是归属期间),按直线计算。对于有市场条件的股票奖励,公允价值以预期里程碑实现日期为派生服务期(通常为归属期间)为基础,按直线原则确认。对于有业绩条件的股票奖励,这些奖励的授予日公允价值是适用授予日的市场价格,当条件可能得到满足时,将确认补偿费用。由于相关服务期已在前一段时间内完成,一旦条件有可能得到满足,我们将确认累计调整。我们选择在没收发生时对其进行核算,而不是估计预期的没收。
我们使用布莱克-斯科尔斯期权定价模型来估计股票期权的公允价值。不可观测的输入包括预期价格波动率、无风险利率、预期股息收益率和预期期限。于截至2021年12月31日止年度内,预期股价波动介乎87.40%至91.51%之间,于截至2020年12月31日止年度内,预期股价波幅介乎75.00%至119.30%之间。截至2021年12月31日止年度的无风险利率介乎0.72%至1.34%,而截至2020年12月31日止年度的无风险利率介乎0.39%至0.53%。在截至2021年12月31日和2020年12月31日的年度内,预期期限为6.00年。
我们使用蒙特卡罗估值模型来估计限制性股票奖励的公允价值,以模拟特定股价里程碑的实现。不可观测的输入包括预期股价波动率、无风险利率和预期期限。截至2020年12月31日,预期股价波动率为85.00%,无风险利率为0.40%,预期期限为5.00年。在截至2021年12月31日的年度内,并无授予限制性股票奖励。
第7A项。关于市场风险的定量和定性披露
作为一家较小的报告公司,我们不需要提供本项目所要求的信息。
92
目录表
第八项。财务报表和补充数据
合并财务报表索引
独立注册会计师事务所报告(PCAOB ID: |
|
F-1 |
独立注册会计师事务所报告(PCAOB ID: |
|
F-2 |
合并资产负债表 |
|
F-3 |
合并经营报表和全面亏损 |
|
F-4 |
合并股东权益报表(亏损) |
|
F-5 |
合并现金流量表 |
|
F-6 |
合并财务报表附注 |
|
F-8 |
93
目录表
独立注册会计师事务所报告
致克莱恩公司的股东和董事会。
对财务报表的几点看法
本公司已审核所附Clene Inc.及其附属公司(“本公司”)于2021年12月31日的综合资产负债表、截至2021年12月31日止年度的相关综合经营报表及全面亏损、股东权益及现金流量,以及相关附注(统称为“财务报表”)。我们认为,财务报表在所有重要方面都公平地反映了公司截至2021年12月31日的财务状况,以及截至2021年12月31日的年度的经营结果和现金流量,符合美国公认的会计原则。
意见基础
这些财务报表由公司管理层负责。我们的责任是根据我们的审计对公司的财务报表发表意见。我们是一家在美国上市公司会计监督委员会(PCAOB)注册的公共会计师事务所,根据美国联邦证券法以及美国证券交易委员会和PCAOB的适用规则和法规,我们必须与公司保持独立。
我们是按照PCAOB的标准进行审计的。这些标准要求我们计划和执行审计,以获得关于财务报表是否没有重大错报的合理保证,无论是由于错误还是舞弊。本公司并无被要求对其财务报告的内部控制进行审计,我们也没有受聘进行审计。作为我们审计的一部分,我们被要求了解财务报告的内部控制,但不是为了对公司财务报告内部控制的有效性发表意见。因此,我们不表达这样的意见。
我们的审计包括执行评估财务报表重大错报风险的程序,无论是由于错误还是欺诈,以及执行应对这些风险的程序。这些程序包括在测试的基础上审查与财务报表中的数额和披露有关的证据。我们的审计还包括评价管理层使用的会计原则和作出的重大估计,以及评价财务报表的整体列报。我们相信,我们的审计为我们的观点提供了合理的基础。
/s/
March 11, 2022
自2021年以来,我们一直担任公司的审计师。
F-1
目录表
独立注册会计师事务所报告
致Clene Inc.董事会和股东。
对财务报表的几点看法
本公司已审核Clene Inc.及其附属公司(“贵公司”)于2020年12月31日的综合资产负债表,以及截至2020年12月31日止年度的相关综合营运及全面损益表、可赎回可转换优先股及股东权益(亏损)及现金流量表,包括相关附注(统称“综合财务报表”)。我们认为,综合财务报表在所有重要方面都公平地反映了本公司截至2020年12月31日的财务状况,以及截至2020年12月31日的年度的经营结果和现金流量,符合美国公认的会计原则。
意见基础
这些合并财务报表由公司管理层负责。我们的责任是根据我们的审计对公司的综合财务报表发表意见。我们是一家在美国上市公司会计监督委员会(PCAOB)注册的公共会计师事务所,根据美国联邦证券法以及美国证券交易委员会和PCAOB的适用规则和法规,我们必须与公司保持独立。
我们是按照PCAOB的标准对这些合并财务报表进行审计的。这些准则要求我们计划和执行审计,以获得关于合并财务报表是否没有重大错报的合理保证,无论是由于错误还是舞弊。
我们的审计包括执行评估合并财务报表重大错报风险的程序,无论是由于错误还是欺诈,以及执行应对这些风险的程序。这些程序包括在测试的基础上审查关于合并财务报表中的金额和披露的证据。我们的审计还包括评价管理层使用的会计原则和作出的重大估计,以及评价合并财务报表的整体列报。我们相信,我们的审计为我们的观点提供了合理的基础。
物质的侧重点
正如综合财务报表附注1所述,该公司将需要额外的融资或合作协议来为未来的运营提供资金。附注1还说明了管理层对事件和情况的评价以及减轻这一问题的计划。
/s/
March 26, 2021
我们于2019年至2021年担任本公司的审计师。
F-2
目录表
Clene Inc.
合并资产负债表
(单位为千,不包括每股和每股金额)
|
|
十二月三十一日, |
|
|||||
|
|
2021 |
|
|
2020 |
|
||
资产 |
|
|
|
|
|
|
||
流动资产: |
|
|
|
|
|
|
||
现金 |
|
$ |
|
|
$ |
|
||
应收账款 |
|
|
|
|
|
|
||
库存 |
|
|
|
|
|
|
||
预付费用和其他流动资产 |
|
|
|
|
|
|
||
流动资产总额 |
|
|
|
|
|
|
||
受限现金 |
|
|
|
|
|
|
||
使用权资产 |
|
|
|
|
|
|
||
财产和设备,净值 |
|
|
|
|
|
|
||
总资产 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
负债和股东权益 |
|
|
|
|
|
|
||
流动负债: |
|
|
|
|
|
|
||
应付帐款 |
|
$ |
|
|
$ |
|
||
应计负债 |
|
|
|
|
|
|
||
应付所得税 |
|
|
|
|
|
|
||
关联方递延收入 |
|
|
|
|
|
|
||
经营租赁债务,本期部分 |
|
|
|
|
|
|
||
融资租赁义务,本期部分 |
|
|
|
|
|
|
||
Clene Nanomedicine应急收益,当前部分 |
|
|
|
|
|
|
||
流动负债总额 |
|
|
|
|
|
|
||
经营性租赁债务,扣除当期部分 |
|
|
|
|
|
|
||
融资租赁债务,扣除当期部分 |
|
|
|
|
|
|
||
应付票据 |
|
|
|
|
|
|
||
可转换应付票据 |
|
|
|
|
|
|
||
递延所得税 |
|
|
|
|
|
|
||
普通股认股权证责任 |
|
|
|
|
|
|
||
Clene Nanomedics或有收益,扣除当前份额 |
|
|
|
|
|
|
||
初始股东或有收益 |
|
|
|
|
|
|
||
总负债 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
股东权益: |
|
|
|
|
|
|
||
普通股,$ |
|
|
|
|
|
|
||
额外实收资本 |
|
|
|
|
|
|
||
累计赤字 |
|
|
( |
) |
|
|
( |
) |
累计其他综合收益 |
|
|
|
|
|
|
||
股东权益总额 |
|
|
|
|
|
|
||
总负债和股东权益 |
|
$ |
|
|
$ |
|
||
见合并财务报表附注。
F-3
目录表
Clene Inc.
合并经营报表和全面亏损
(单位为千,不包括每股和每股金额)
|
|
截至十二月三十一日止的年度, |
|
|||||
|
|
2021 |
|
|
2020 |
|
||
收入: |
|
|
|
|
|
|
||
产品收入 |
|
$ |
|
|
$ |
|
||
专利权使用费收入 |
|
|
|
|
|
|
||
总收入 |
|
|
|
|
|
|
||
运营费用: |
|
|
|
|
|
|
||
收入成本 |
|
|
|
|
|
|
||
研发 |
|
|
|
|
|
|
||
一般和行政 |
|
|
|
|
|
|
||
总运营费用 |
|
|
|
|
|
|
||
运营亏损 |
|
|
( |
) |
|
|
( |
) |
其他收入(费用),净额: |
|
|
|
|
|
|
||
利息支出 |
|
|
( |
) |
|
|
( |
) |
应付票据的清偿收益 |
|
|
|
|
|
|
||
可转换票据清偿损失应付票据 |
|
|
|
|
|
( |
) |
|
租约终止时的收益 |
|
|
|
|
|
|
||
优先股权证负债的公允价值变动 |
|
|
|
|
|
( |
) |
|
普通股认股权证负债的公允价值变动 |
|
|
|
|
|
|
||
衍生负债的公允价值变动 |
|
|
|
|
|
|
||
Clene纳米医疗或有收益的公允价值变动 |
|
|
|
|
|
|
||
初始股东或有收益的公允价值变动 |
|
|
|
|
|
|
||
澳大利亚研发信贷 |
|
|
|
|
|
|
||
其他收入(费用),净额 |
|
|
( |
) |
|
|
|
|
其他收入(费用)合计,净额 |
|
|
|
|
|
|
||
所得税前净亏损 |
|
|
( |
) |
|
|
( |
) |
所得税优惠(费用) |
|
|
|
|
|
( |
) |
|
净亏损 |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
||
其他全面收益(亏损): |
|
|
|
|
|
|
||
外币折算调整 |
|
|
( |
) |
|
|
|
|
其他全面收益(亏损)合计 |
|
|
( |
) |
|
|
|
|
综合损失 |
|
$ |
( |
) |
|
$ |
( |
) |
|
|
|
|
|
|
|
||
每股净亏损--基本亏损和摊薄亏损(附注19) |
|
$ |
( |
) |
|
$ |
( |
) |
用于计算基本和摊薄净亏损的加权平均普通股 |
|
|
|
|
|
|
||
见合并财务报表附注。
F-4
目录表
Clene Inc.
合并股东权益报表(亏损)
(单位为千,不包括份额)
|
|
可赎回 |
|
|
|
普通股 |
|
|
其他内容 |
|
|
累计 |
|
|
累计 |
|
|
总计 |
|
||||||||||||||
|
|
股票 |
|
|
金额 |
|
|
|
股票 |
|
|
金额 |
|
|
资本 |
|
|
赤字 |
|
|
收入 |
|
|
(赤字) |
|
||||||||
2019年12月31日的余额(1) |
|
|
|
|
$ |
|
|
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|
$ |
( |
) |
||||||
发行D系列优先股,扣除发行成本(1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
可转换本票清偿后发行D系列优先股(1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
股票期权的行使(1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
反向资本重组时可赎回可转换优先股的转换(1) |
|
|
( |
) |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
转换可赎回可转换优先股时优先股认股权证债务的消灭 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
反向资本重组和私募发行普通股 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
反向资本重组提供成本 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
||||
发行普通股作为发行费用的支付 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Clene Nanomedic应急收益在反向资本重组中得到认可 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
||||||
反向资本重组确认的初始股东或有收益 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
||||
基于股票的薪酬费用 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
外币折算调整 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
净亏损 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
||||
2020年12月31日的余额 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|||||||
定向增发时发行普通股 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
股票期权的行使 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
认股权证的行使 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
保险人选择权的行使 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
基于股票的薪酬费用 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
在归属限制性股票奖励时发行普通股 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
外币折算调整 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
||||
净亏损 |
|
|
— |
|
|
|
|
|
|
|
— |
|
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
||||
2021年12月31日的余额 |
|
|
|
|
$ |
|
|
|
|
|
|
$ |
|
|
$ |
|
|
$ |
( |
) |
|
$ |
|
|
$ |
|
|||||||
见合并财务报表附注。
F-5
目录表
Clene Inc.
合并现金流量表
(单位:千)
|
|
截至十二月三十一日止的年度, |
|
|||||
|
|
2021 |
|
|
2020 |
|
||
经营活动的现金流: |
|
|
|
|
|
|
||
净亏损 |
|
$ |
( |
) |
|
$ |
( |
) |
对净亏损与经营活动中使用的现金净额进行的调整: |
|
|
|
|
|
|
||
折旧 |
|
|
|
|
|
|
||
非现金租赁费用 |
|
|
|
|
|
|
||
优先股权证负债的公允价值变动 |
|
|
|
|
|
|
||
普通股认股权证负债的公允价值变动 |
|
|
( |
) |
|
|
|
|
Clene纳米医疗或有收益的公允价值变动 |
|
|
( |
) |
|
|
( |
) |
初始股东或有收益的公允价值变动 |
|
|
( |
) |
|
|
( |
) |
基于股票的薪酬费用 |
|
|
|
|
|
|
||
衍生工具公允价值变动 |
|
|
|
|
|
( |
) |
|
应付票据的清偿收益 |
|
|
( |
) |
|
|
|
|
可转换应付票据清偿损失 |
|
|
|
|
|
|
||
租约终止时的收益 |
|
|
|
|
|
( |
) |
|
债务贴现的增加 |
|
|
|
|
|
|
||
应付票据公允价值变动 |
|
|
( |
) |
|
|
|
|
经营性资产和负债变动情况: |
|
|
|
|
|
|
||
应收账款 |
|
|
( |
) |
|
|
( |
) |
库存 |
|
|
|
|
|
( |
) |
|
预付费用和其他流动资产 |
|
|
( |
) |
|
|
( |
) |
应付帐款 |
|
|
|
|
|
( |
) |
|
应计负债 |
|
|
|
|
|
( |
) |
|
应付所得税 |
|
|
( |
) |
|
|
|
|
应付关联方 |
|
|
|
|
|
( |
) |
|
关联方递延收入 |
|
|
|
|
|
|
||
递延所得税 |
|
|
( |
) |
|
|
|
|
经营租赁义务 |
|
|
( |
) |
|
|
( |
) |
用于经营活动的现金净额 |
|
|
( |
) |
|
|
( |
) |
投资活动产生的现金流: |
|
|
|
|
|
|
||
购置财产和设备 |
|
|
( |
) |
|
|
( |
) |
用于投资活动的现金净额 |
|
|
( |
) |
|
|
( |
) |
融资活动的现金流: |
|
|
|
|
|
|
||
行使股票期权所得收益 |
|
|
|
|
|
|
||
行使认股权证所得收益 |
|
|
|
|
|
|
||
支付融资租赁债务 |
|
|
( |
) |
|
|
( |
) |
发行应付票据所得款项 |
|
|
|
|
|
|
||
债务发行成本的支付 |
|
|
( |
) |
|
|
|
|
应付票据的付款 |
|
|
( |
) |
|
|
|
|
私募所得收益 |
|
|
|
|
|
|
||
支付递延发售费用 |
|
|
( |
) |
|
|
( |
) |
反向资本重组和私募的收益 |
|
|
|
|
|
|
||
发行D系列优先股所得款项,扣除发行成本 |
|
|
|
|
|
|
||
发行可转换应付票据所得款项 |
|
|
|
|
|
|
||
融资活动提供的现金净额 |
|
|
|
|
|
|
||
外汇汇率变动对现金和限制性现金的影响 |
|
|
( |
) |
|
|
|
|
现金和限制性现金净增(减)额 |
|
|
( |
) |
|
|
|
|
现金和限制性现金--年初 |
|
|
|
|
|
|
||
现金和限制性现金--年终 |
|
$ |
|
|
$ |
|
||
|
|
|
|
|
|
|
||
对合并资产负债表中的现金和限制性现金进行核对 |
|
|
|
|
|
|
||
现金 |
|
|
|
|
|
|
||
受限现金 |
|
|
|
|
|
|
||
现金和限制性现金 |
|
$ |
|
|
$ |
|
||
见合并财务报表附注。
F-6
目录表
Clene Inc.
合并现金流量表(续)
(单位:千)
|
|
截至十二月三十一日止的年度, |
|
|||||
|
|
2021 |
|
|
2020 |
|
||
补充披露非现金投资和融资活动: |
|
|
|
|
|
|
||
因取得使用权资产、租赁改进和租赁奖励而产生的租赁负债 |
|
$ |
|
|
$ |
|
||
发行应付票据时记录的普通股认股权证负债 |
|
$ |
|
|
$ |
|
||
通过终止租赁而解决的租赁债务 |
|
$ |
|
|
$ |
|
||
发行与可转换票据有关的衍生工具 |
|
$ |
|
|
$ |
|
||
可转换本票清偿后发行D系列优先股 |
|
$ |
|
|
$ |
|
||
与可转换本票的终绝有关的衍生法律责任的终绝 |
|
$ |
|
|
$ |
|
||
应付帐款中的递延交易成本 |
|
$ |
|
|
$ |
|
||
应计负债中的递延交易成本 |
|
$ |
|
|
$ |
|
||
将可赎回可转换优先股转换为普通股 |
|
$ |
|
|
$ |
|
||
与转换可赎回可转换优先股有关的优先股权证法律责任的终绝 |
|
$ |
|
|
$ |
|
||
发行普通股作为相关发行成本的支付 |
|
$ |
|
|
$ |
|
||
Clene Nanomedic应急收益与反向资本重组有关的公认收益 |
|
$ |
|
|
$ |
|
||
与反向资本重组相关的初始股东或有盈利确认 |
|
$ |
|
|
$ |
|
||
补充披露: |
|
|
|
|
|
|
||
为利息支出支付的现金 |
|
$ |
|
|
$ |
|
||
见合并财务报表附注。
F-7
目录表
Clene Inc.
合并财务报表附注
1.业务性质
Clene Inc.(前身为切尔西全球公司)(“公司”、“我们”、“我们”或类似的参考文献)是一家临床阶段的制药公司,致力于发现、开发和商业化新的表面清洁的纳米技术疗法。我们开发了一个电晶体化学药物开发平台,可以生产浓缩、稳定、高活性、表面清洁的纳米晶体悬浮液。我们目前有多种药物资产正在开发中,用于神经学、传染病和肿瘤学。我们目前的努力集中于解决两个领域尚未得到满足的高度医疗需求:第一,与包括肌萎缩侧索硬化症(ALS)、多发性硬化症(MS)和帕金森病(PD)在内的中枢神经系统疾病有关的需求;第二,与新冠肺炎相关的需求,这是一种高度传染性的病毒性呼吸道疾病,会严重,有时甚至致命。我们的专利电晶体化学制造平台进一步使我们能够开发极低浓度的膳食补充剂,以促进广大人群的健康和福祉。这些膳食补充剂可以有很大的不同,包括不同组成、形状和大小的纳米晶体以及具有不同金属成分的离子溶液。膳食补充剂通过我们的全资子公司dOrbary,Inc.(“dOrbary”)或通过关联方4Life Research LLC(“4Life”)的独家许可证(见注20)进行营销和分销。
随附的综合财务报表包括Clene Inc.及其全资子公司Clene Nanomedicine,Inc.(“Clene Nanomedicine”)(一家在特拉华州注册成立的子公司)、Clene Australia Pty Ltd(“Clene Australia”)(一家在澳大利亚注册成立的子公司)以及在特拉华州注册成立的一家子公司dOrbary(一家在特拉华州注册成立的子公司)在注销所有公司间账户和交易后的账目。全资子公司克莱恩荷兰公司成立于2021年4月21日,到目前为止还没有财务状况或业务。
流动性
我们因经营……而蒙受损失$
自成立以来,我们的运营出现了重大亏损和负现金流。到目前为止,我们还没有产生大量的收入,除非我们成功完成开发并获得监管部门对我们候选药物的批准,否则我们预计不会产生大量的收入。我们预计我们的费用将大幅增加,并在未来导致额外的亏损,以资助我们的运营,特别是当我们推进临床阶段候选药物的开发,继续研究和开发我们的临床前候选药物,并启动这些和其他未来候选药物的更多临床试验并寻求监管机构批准的时候。我们预计,如果我们的候选药物获得监管部门的批准,随着我们准备开始商业化,与法规遵从性以及销售和营销人员有关的费用将大幅增加。
随附的综合财务报表的编制假设我们将继续作为一家持续经营的企业,考虑在正常业务过程中实现资产和偿还负债。我们的长期运营需要获得额外的资本来为我们的运营提供资金。作为我们正在进行的业务计划的一部分,我们将继续寻求通过股权融资筹集更多资本,并可能寻求债务融资或其他资本来源,我们可能会尝试与第三方合作开发我们的候选药物并将其商业化。我们可能无法以可接受的条件获得资本,或者根本无法获得资本。任何融资条款都可能对我们股东的持股或权利产生不利影响。根据我们当前业务计划的结果,我们可能需要实施成本节约措施,包括可能推迟或减少研发计划和商业化努力,最早将于2022年第三季度开始。目前,在没有额外资本的情况下,我们相信我们有足够的资源为我们持续运营到2023年第二季度提供资金。
新冠肺炎大流行的影响
新冠肺炎大流行始于2019年12月,目前已在全球范围内蔓延,已导致许多国家政府采取措施减缓疫情的蔓延。疫情的爆发和政府采取的应对措施对企业和商业产生了直接和间接的重大影响,因为工人短缺,供应链中断,设施和生产暂停。大流行的未来进展及其对我们的业务和业务的影响仍然不确定。新冠肺炎大流行可能会影响我们启动和完成临床前研究和临床试验的能力,推迟未来临床试验的启动,扰乱监管活动,或对我们的业务和运营产生其他不利影响。特别是,我们和我们的合同研究组织(CRO)面临着影响我们发起和
F-8
目录表
完成临床前研究,造成生产中断,并在临床试验场地启动和临床试验登记方面造成延误,导致正在进行的临床试验早日结束。这场大流行已经对金融市场造成了重大破坏,并可能继续造成这种破坏,这可能会影响我们筹集更多资金支持我们业务的能力。此外,这场大流行严重影响了世界各地的经济,并可能对我们的业务和运营造成不利影响。
我们正在监测新冠肺炎疫情对我们的业务和财务报表的潜在影响。虽然新冠肺炎疫情导致了各种研究限制,并导致我们的某些临床试验暂停和提前结束,但这些影响是暂时的,到目前为止,我们还没有因为疫情而经历重大业务中断或资产账面价值减值损失,我们也不知道有任何具体的相关事件或情况需要我们修订这些合并财务报表中反映的估计。新冠肺炎疫情将在多大程度上直接或间接影响我们的业务、运营结果、现金流和财务状况,包括计划及未来的临床试验和研发成本,将取决于高度不确定的未来发展,包括可能出现的有关新冠肺炎的新信息、采取的遏制或治疗措施以及相关影响的持续时间和强度。
注册声明
2021年2月16日,我们提交了S-1表格(档案号为333-253173)进行注册
2021年7月22日,我们提交了S-1表格(档案号为333-258098)进行注册
2.主要会计政策摘要
陈述的基础
本公司已根据美国公认会计原则(“GAAP”)编制随附的综合财务报表。管理层认为,合并财务报表反映了公允财务报表列报所需的所有正常和经常性调整。上期应收账款余额已重新分类,以符合本年度的列报方式。
预算的使用
按照公认会计原则编制合并财务报表要求管理层作出估计和假设,以影响报告的资产、负债、或有资产和负债的披露以及报告的费用金额。我们的估计是基于历史经验和我们认为合理的各种其他假设。实际结果可能与这些估计或假设不同。估计会根据情况、事实和经验的变化而定期审查,估计的任何变化将在未来期间随着其发展而记录下来。
F-9
目录表
风险和不确定性
我们开发的候选产品在商业销售之前需要获得监管机构的批准。不能保证我们目前和未来的候选产品将获得必要的批准或在商业上取得成功。如果我们被拒绝批准或批准被推迟,将对我们的业务和我们的合并财务报表产生实质性的不利影响。
我们会受到某些风险和不确定性的影响,并相信以下任何方面的变化都可能对未来的财务状况或经营结果产生重大不利影响:获得额外融资的能力;监管部门对候选产品的批准和市场接受程度以及对产品候选人的补偿;我们所依赖的第三方CRO和制造商的表现;对我们知识产权的保护;基于知识产权、专利、产品、监管或其他因素对我们的诉讼或索赔;以及我们吸引和留住支持我们增长所需的员工的能力。
信用风险的集中度
可能使我们面临严重集中信贷风险的金融工具主要是现金。我们的现金主要存放在金融机构。存款金额有时可能会超过联邦保险的限额。我们没有经历过现金存款的任何损失,我们不认为我们受到与商业银行关系相关的正常信用风险以外的异常信用风险的影响。
现金和现金等价物
我们将购买时原始到期日为三个月或更短的所有短期投资视为现金等价物。截至2021年12月31日和2020年,我们没有现金等价物。
受限现金
当现金在我们的一般经营活动中无法提取或使用时,我们将其归类为受限现金。根据限制的性质,限制现金和投资在合并资产负债表上被分类为流动和非流动。我们的受限现金余额包括与我们的公司信用卡相关的合同受限存款。截至2021年12月31日和2020年12月31日,我们限制了$
应收帐款
应收账款按发票价值减去销售退货准备和可疑账款的估计准备列报。我们根据12个月销售往绩平均值上的历史退货百分比来估算销售退货准备。我们持续监控客户付款,并为客户无力支付所需款项而造成的估计损失保留准备金。在估计坏账准备时,我们会考虑一些因素,例如历史经验、应收账款余额的年龄、与地理相关的风险以及可能影响客户支付能力的经济状况。在可能损害特定客户履行其财务义务的能力的情况下,特定拨备将被计入应付金额,从而将确认的应收账款净额减少至合理地认为是可收回的金额。应收账款在被认为无法收回时予以核销。以前核销的应收账款在收到时被记录下来。从历史上看,没有销售退货,没有核销的应收账款,也没有减少应收账款余额的可疑账款拨备。
库存
存货在先进先出的基础上按历史成本列报。我们的库存包括$
债务
当发行债务及衍生工具须分流(例如分流转换期权)或发行另一独立金融工具(例如认股权证)时,所产生的成本及费用会按收益分配比例分配至已发行(或分流)的工具。当部分成本及费用与其后按公允价值计量的分支衍生工具或独立金融工具有关时,该等已分配成本立即计入开支。与债务相关的债务贴现、债务溢价和债务发行成本被记录为扣除债务本金价值,并使用有效利息法在债务合同期限内摊销利息支出。
F-10
目录表
递延发售成本
我们利用某些法律、专业会计。以及与正在进行的股权融资直接相关的其他第三方费用,包括反向资本重组和2020年管道,作为推迟发行成本,直到此类融资完成。在股权融资完成后,这些成本计入股东权益(亏损),作为发行所产生的收益的减少。如果放弃任何正在进行的股权融资,递延发售成本将立即在综合经营报表中计入营业费用和全面亏损。
截至2021年12月31日止年度内,我们做到了
租契
在合同开始时,我们确定合同是否符合租赁的定义。我们确定合同是否传达了在一段时间内控制已确定资产的使用的权利。我们在整个使用期内评估我们是否同时拥有以下两项:(I)从使用确定的资产中获得几乎所有经济利益的权利,以及(Ii)指示使用确定的资产的权利。如果合同条款发生变化,将重新评估这一决定。租赁根据租赁协议的条款和已确认资产的某些特征被归类为经营性或融资性租赁。使用权资产及租赁负债于租赁开始日按未来租赁付款的现值减去收到的任何租赁奖励确认。于租赁开始日,租赁中隐含的贴现率用于贴现租赁负债(如可随时确定)。如果不容易确定或租约不包含隐含利率,我们的递增借款利率被用作贴现率。
我们的政策是不在综合资产负债表中记录原始期限为12个月或以下的租赁。我们以直线法在综合经营报表及全面亏损报表中确认该等短期租赁的租赁费用。
某些租赁协议可能要求我们支付额外的税费、保险费、维护费和其他费用,这些费用通常被称为非租赁部分。这些可变非租赁部分被视为可变租赁付款,并在产生这些付款的债务期间确认。可变租赁组成部分和可变非租赁组成部分不作为使用权资产和负债的一部分进行计量。只有当租赁组成部分及其相关的非租赁组成部分是固定的时,它们才会作为单一租赁组成部分入账,并被确认为使用权资产和负债的一部分。合同总对价分配给合并的固定租赁和非租赁部分。这一政策选择一致适用于租赁协议下的所有资产类别。
租约可能包含条款,可由我们选择续订。当合理地确定延长租赁的选择权将被行使或不在我们的选择权范围内时,将在选择期内支付的款项被确认为使用权租赁资产和租赁负债的一部分。我们通过考虑基于合同、资产、市场和实体的因素来确定是否达到合理确定的门槛。在综合经营及综合损益表中,按直线法于租赁期内确认的经营租赁费用及融资租赁使用权资产摊销计入物业及设备并已折旧,计入与租赁资产主要用途相符的研发或一般及行政费用。融资租赁负债的增值计入利息支出。
财产和设备
财产和设备按成本减去累计折旧列报。财产和设备包括实验室和办公室设备以及租赁装修。折旧是在资产的估计经济使用年限内使用直线方法计算的,这些使用年限是
我们将获取或开发供内部使用的计算机软件的成本资本化,包括软件开发阶段发生的开发成本和获取获取和转换旧数据的软件的成本。我们还利用成本来修改、升级或增强现有的内部使用软件,从而产生额外的功能。摊销是使用
F-11
目录表
直线估计资产的经济使用年限的方法。我们承担与内部使用软件相关的成本,包括初步项目阶段发生的成本、培训成本、数据转换成本和维护成本。
长期资产减值准备
可转换票据
根据ASU 2020-06,债务-具有转换和其他期权的债务(分主题470-20)和衍生工具和对冲--实体自有股权的合同(分主题815-40):实体自有股权的可转换票据和合同的会计,当我们发行带有转换功能的票据时,我们会评估转换功能是独立的还是嵌入的。如果嵌入了转换功能,我们不会将转换功能与不需要作为衍生品入账的可转换票据的主合同分开,或者不会导致大量溢价作为实收资本入账。因此,我们将可转换票据视为按其摊销成本计量的单一负债,并将可转换优先股视为以其历史成本衡量的单一权益工具,只要没有其他特征需要区分和确认为衍生品。
如果转换特征是独立的,或者是嵌入的,并且满足要进行分支的要求,则我们将转换特征作为ASC 815的派生项来考虑。衍生工具和套期保值(“ASC 815”)。吾等于开始时按公允价值记录衍生工具,其后于每个报告期及紧接衍生工具终止前按公允价值重新计量,并于综合经营报表及全面亏损中记录任何变动。
有认股权证的债项
根据ASC 470-20,具有转换和其他选项的债务,当我们发行带有权证的债务时,我们将权证视为债务折价,记录为债务的抵销负债,并在基础债务的寿命内摊销余额在综合经营报表和全面亏损中作为利息支出。如认股权证不按美国会计准则第480条作为衍生工具或负债处理,则对抵销负债的抵销在综合资产负债表中记为额外实收资本。区分负债与股权(“ASC 480”)。否则,对抵销负债的抵销将在综合资产负债表中记为认股权证负债,并须于每个资产负债表日按公允价值重新计量,公允价值的任何变动均在综合经营报表及全面亏损中确认。如果债务提前偿还,相关债务贴现将立即在综合经营报表和全面亏损中确认为利息支出。
或有收益负债
关于反向资本重组,某些股东有权在我们实现某些里程碑时获得额外的普通股股份(“或有盈利”)(见附注3和12)。根据美国会计准则委员会815,或有收益不计入我们自己的股票,因此在反向资本重组日作为负债入账,随后在每个报告日重新计量,公允价值变动在综合经营报表和全面亏损中作为其他收入(费用)净额的组成部分记录。
普通股认股权证
我们根据对认股权证条款的评估和适用的权威指引,将普通股股权证归类为权益类工具或负债类工具。评估考虑认股权证是否为ASC 480所指的独立金融工具,是否符合ASC 480所指的负债定义,以及认股权证是否符合ASC 815所指的所有股权分类要求,包括认股权证是否与我们的普通股挂钩,以及其他股权分类条件。这种评估需要使用专业判断,在权证发行时进行,对于责任分类权证,在权证尚未结清的情况下,自随后的每个季度结束日起进行。
F-12
目录表
收入确认
在ASC 606下,与客户签订合同的收入(“ASC 606”),实体于其客户取得对承诺货品或服务的控制权时确认收入,金额反映该实体预期以该等货品或服务换取的对价。为了确定实体确定属于ASC 606范围内的安排的收入确认,该实体执行以下五个步骤:(I)确定与客户的合同;(Ii)确定合同中的履约义务;(Iii)确定交易价格,包括可变对价(如果有的话);(Iv)将交易价格分配给合同中的履约义务;以及(V)当实体履行履约义务时(或作为履行义务时)确认收入。只有当我们可能会收取我们有权获得的对价,以换取我们转移给客户的商品或服务时,我们才会将五步模型应用于合同。
一旦合同在合同开始时被确定在ASC 606的范围内,我们就审查合同,以确定我们必须交付的履行义务,以及哪些履行义务是不同的。我们确认在履行履行义务或履行履行义务时分配给该履行义务的交易价格的金额为收入。我们通常通过向客户提供膳食补充剂来履行我们的履约义务。对于商业交易,在收到付款时应付款,对于在线零售,应收取预付款。在截至2021年12月31日和2020年12月31日的年度内,我们的收入包括膳食补充剂和特许权使用费的销售。
我们记录的递延收入为$
赠款资金
我们可以提交申请,接受政府和非政府实体的赠款资助。收到的赠款资金不含任何条件或持续的履约义务,在收到时予以确认。有条件或义务的赠款资金被确认为条件或义务已履行。我们已作出会计政策选择,将该等无条件拨款,例如澳大利亚研究及发展信贷,作为其他收入记入综合经营报表及全面亏损。有条件或有义务的赠款的收入在发生相关合格费用的期间确认,前提是提供赠款的条件已得到满足。我们确认澳大利亚研究和发展信贷的金额等于每个时期发生的符合条件的费用乘以适用的报销百分比。在截至2021年12月31日和2020年12月31日的年度内,我们认识到$
任何在履行该等条件或义务前收到的款项,如预期该等条件或义务将于未来12个月内满足,则于综合资产负债表中记入应计负债。截至2021年12月31日和2020年,我们记录了$
在有条件资助中确认的赠款资金被列为综合运营报表中研发费用的减少和全面亏损,因为条件与我们的研发工作有关,而且我们与组织之间的安排不是我们持续、主要或中央业务的一部分。在截至2021年12月31日和2020年12月31日的年度内,我们记录了$
金融工具的公允价值
根据公认会计原则,某些资产和负债按公允价值列账。公允价值被定义为在计量日市场参与者之间的有序交易中为资产或负债在本金或最有利的市场上转让负债而收取或支付的价格(退出价格)。用于计量公允价值的估值技术必须最大限度地利用可观察到的投入,最大限度地减少使用不可观察到的投入。按公允价值列账的金融资产和负债应在公允价值层次的下列三个级别之一进行分类和披露:
1级-基于在测量日期活跃市场上相同资产或负债的报价的投入。
2级-除一级市场报价外的其他可观察的投入,如活跃市场中类似资产和负债的报价;非活跃市场中相同或类似资产和负债的报价;或可观察到或可被可观察到的市场数据证实的其他投入。
F-13
目录表
3级-作为管理层对市场参与者在计量日期为资产或负债定价时使用的最佳估计的投入。这些投入在市场上是看不到的,对该工具的估值很重要。
我们每季度审查适用资产和负债的公允价值层次分类。估值投入的可观测性的变化可能导致某些金融资产或负债的重新分类。影响公允价值层次结构所有级别的重新分类在发生重新分类的季度初报告为调入或调出第1、2或3级类别。
外币折算和交易
我们的功能货币是美元。克莱恩澳大利亚确定其功能货币为澳元,我们的荷兰子公司确定其功能货币为欧元。我们使用美元作为合并财务报表的报告货币。我们非以美元为基础的功能货币业务的结果按期间的平均汇率换算为美元。我们的资产和负债按截至资产负债表日的当前汇率换算,股东权益按历史汇率换算。
将外币子公司的合并财务报表换算成美元所产生的调整不计入净亏损的确定,并在股东权益的单独组成部分中累积。这些外币折算损益目前是其他全面损失的唯一组成部分。
我们还因购买外币而产生外汇交易损益。汇兑交易损益计入合并经营表的其他收入(费用)和发生的全面损失。
综合损失
综合损失包括净损失以及除与股东的交易和经济事件以外的交易和经济事件导致的股东权益(赤字)的其他变化。列报任何期间的其他全面收益(亏损)的唯一要素是将克雷恩澳大利亚公司的澳元余额换算成美元进行合并。
普通股股东应占每股净亏损
普通股股东应占每股基本净亏损使用我们的加权平均已发行普通股计算。普通股股东应占每股摊薄净收益(亏损)采用我们的加权平均已发行普通股计算,其中包括按库存股方法确定的证券的稀释效应,但按IF转换法计算的应付可转换票据的稀释效应除外,即使嵌入的转换期权是现金外的。在我们报告普通股股东应占净亏损的期间,普通股股东应占稀释每股净亏损与普通股股东应占基本每股净亏损相同,因为如果稀释性普通股的影响是反摊薄的,则不假设已发行稀释性普通股。
段信息
我们已确定我们的首席执行官是首席运营决策者(“CODM”)。经营部门被确定为企业的组成部分,CODM在作出关于资源分配的决定和评估业绩时,可以获得关于这些部门的单独的离散财务信息,以供评估。我们查看我们的运营并管理我们的业务
所得税
我们采用资产负债法对所得税进行会计处理,该方法要求就已在合并财务报表或我们的纳税申报表中确认的事件的预期未来税务后果确认递延税项资产和负债。递延税项资产及负债乃根据财务报表与资产及负债的税基之间的差额,采用预期差额将拨回的年度的现行税率厘定。递延税项资产和负债的变动计入所得税准备。我们评估我们的递延税项资产将从未来应纳税所得额中收回的可能性,并根据现有证据的权重,在我们认为全部或部分递延税项资产更有可能无法变现的情况下,通过计入所得税费用来建立估值拨备。透过估计预期未来应课税溢利及考虑审慎及可行的税务筹划策略,评估收回递延税项资产的潜力。
F-14
目录表
我们采用两步法来确定应确认的税收优惠金额,以此来计入合并财务报表中确认的所得税的不确定性。首先,必须对税收状况进行评估,以确定税务机关在外部审查后维持这种状况的可能性。如果税务状况被认为更有可能持续,则对税务状况进行评估,以确定在合并财务报表中确认的利益金额。可确认的受益金额是在最终和解时实现可能性大于50%的最大金额。所得税拨备包括被认为适当的任何由此产生的税收准备金或未确认的税收优惠的影响,以及相关的净利息和罚款。
基于股票的薪酬
我们使用公允价值为基础的方法来核算基于股票的薪酬安排,以计算与所有基于股票的支付相关的成本,包括股票期权和股票奖励。基于股票的补偿费用根据受赠人所做工作的分类记入研究和开发费用以及一般和行政费用。
公允价值是在受让人被要求提供服务以换取期权奖励和基于服务的股票奖励的期间内确认的,这段期间被称为必要的服务期(通常是归属期间),按直线计算。对于有市场条件的股票奖励,公允价值以预期里程碑实现日期为派生服务期(通常为归属期间)为基础,按直线原则确认。对于有业绩条件的股票奖励,这些奖励的授予日公允价值是适用授予日的市场价格,当条件可能得到满足时,将确认补偿费用。由于相关服务期已在前一段时间内完成,一旦条件有可能得到满足,我们将确认累计调整。
基于股票的薪酬费用按公允价值确认。我们选择在没收发生时对其进行核算,而不是估计预期的没收。
在反向资本重组结束后,我们将根据纳斯达克股票市场有限责任公司(“纳斯达克”)在授予日报告的普通股收盘价来确定基于股票的奖励的每股普通股的公允价值。股票奖励的公允价值在市场条件下使用蒙特卡罗估值模型来确定。
研究与开发
研究和开发成本在发生时计入费用。我们将在收到货物或提供服务时,将在未来研发活动中使用的货物和服务的预付款作为费用进行核算,但不能退还。研究和开发费用包括发现和开发我们的候选产品所产生的成本。研发成本包括但不限于工资和人员支出,包括基于股票的补偿、临床试验用品、临床试验服务费、咨询成本和分配的管理费用,包括租金、设备和水电费。
临床试验应计
我们的临床试验应计过程计入了与CRO、顾问合同和临床现场协议下与进行临床试验相关的义务所产生的费用。临床试验费用在发生时计入研究和开发费用。这些合同的财务条款需要进行谈判,不同的合同会有所不同,可能会导致支付流量与根据此类合同向我们提供材料或服务的期限不匹配。我们通过将适当的费用与服务和努力支出的期间相匹配,在合并财务报表中反映适当的临床试验费用。如果向CRO预付款,付款将被记录为预付资产,在合同服务执行期间摊销为研发费用。除了传递成本外,我们通常在以下四个不同类别的临床试验中产生成本:
CRO初创企业-这些费用包括临床试验的初始设置,通常在合同签署后的几个月内发生,并包括在可识别的启动期内按比例支出的费用,以及在不存在启动期时按比例支出的费用。启动阶段的活动包括研究启动、现场招聘、监管申请、调查人员会议、筛选、准备、研究前访问和培训。
CRO网站和研究管理-这些成本包括医疗和安全监测、患者管理和数据管理。这些费用通常是以每个患者为基础计算的,并在患者登记之日开始的治疗期内按比例计价。
F-15
目录表
CRO关闭和报告-这些成本包括分析获得的数据和报告结果,这发生在患者停止治疗和收集的信息数据库被锁定之后。这些费用在任何关闭和报告期内发生的费用中计入。
第三方合同-这些费用包括第三方为非CRO提供的各种支持服务收取的费用,并包括实验室费用、数据质量审查费用以及调查产品监测和库存控制费用等项目。这些物品在与受雇第三方供应商的任何可识别的服务期内按比例计价。
CRO合同一般包括通行费,包括但不限于监管费用、调查员费用、差旅费用和其他杂项费用,包括运输和印刷费。我们通过适用人员和外部服务提供商关于试验或已完成服务的进度或完成状态的报告和讨论来确定应计估计数。我们根据我们当时所知的事实和情况在合并财务报表中估计截至每个报告日期的应计费用。
最近采用的会计公告
2020年8月,FASB发布了ASU 2020-06,债务--可转换债务和其他期权(分专题470-20)和衍生工具和套期保值--实体自有权益的合同(分专题815-40):实体自有权益的可转换工具和合同的会计通过取消某些可转换工具的分离模式,简化某些金融工具的会计处理。根据ASU 2020-06的修订,嵌入的转换功能不再与具有转换功能的可转换工具的宿主合同分开,这些转换功能不需要作为衍生品入账,或者不会导致大量溢价作为实缴资本入账。因此,可转换债务工具将被计入按其摊余成本计量的单一负债,可转换优先股将被计入按其历史成本计量的单一股本工具,只要没有其他特征需要分开并确认为衍生品。新标准还对可转换债务和独立工具引入了额外的披露,这些工具与实体自己的股本挂钩并以其结算。ASU 2020-06修订了稀释后每股收益指引,包括对所有可转换工具使用IF转换方法的要求。对于规模较小的报告公司,新指南在2023年12月15日之后开始的财年有效,应在全面或修改的追溯基础上应用,允许提前采用,但不得早于2020年12月15日之后开始的财年,包括这些财年的过渡期。2021年1月1日,我们提前采用了ASU 2020-06。采用这一指导方针并未对我们的合并财务报表产生实质性影响。
2019年12月,FASB发布了ASU 2019-12,所得税(话题740)修订了现行关于所得税会计的指导意见。这一会计准则旨在通过消除所得税会计一般原则的某些例外情况来简化所得税会计,并通过澄清和修改现有指导方针来改进公认会计准则在所得税会计其他领域的一致适用。新的指导方针适用于我们的财政年度,以及我们财政年度内的过渡期,从2020年12月15日之后开始。采用这一指导方针并未对我们的合并财务报表产生实质性影响。
2018年8月,FASB发布了ASU 2018-15,无形资产-商誉和其他-内部使用软件(子主题350-40):客户对作为服务合同的云计算安排中发生的实施成本的核算。新的指导意见规定推迟云计算安排的实施费用,并在云服务安排期间支出这些费用。新的指导方针对我们2020年12月15日之后开始的财年有效。采用这一指导方针并未对我们的合并财务报表产生实质性影响。
近期尚未采用的会计公告
2016年6月,FASB发布了ASU 2016-13,金融工具.信用损失(主题326):金融工具信用损失的测量。除其他事项外,本ASU中的修正案要求根据历史经验、当前状况以及合理和可支持的预测来计量在报告日期持有的金融资产的所有预期信贷损失。金融机构和其他组织现在将使用前瞻性信息来更好地告知他们的信贷损失估计。作为一家规模较小的报告公司,该指导意见在2022年12月15日之后开始的财年有效。我们目前正在评估新指南由于较小报告公司实施截止日期延长而产生的预期影响。
3.托特纳姆热刺和克伦纳米医疗的反向资本重组
于2020年12月30日(“截止日期”),我们的前身切尔西全球公司完成了先前宣布的业务合并(称为“反向资本重组”),根据特拉华州一家公司Clene Nanomedine,Tottenham,切尔西全球公司(“pubco”)于2020年9月1日签署的合并协议(“合并协议”)。
F-16
目录表
和托特纳姆的全资子公司,创新全球公司(“合并子”),特拉华州的公司和Pubco的全资子公司,以及作为股东代表的特拉华州有限责任公司Fortis Advisors LLC。在下文讨论的重新合并之前,托特纳姆作为空白支票公司在英属维尔京群岛注册成立,目的是与一个或多个企业或实体进行合并、换股、资产收购、股票购买、资本重组、重组或其他类似的业务合并。在反向资本重组之前,Clene Nanomedicine普通股的股票没有公开市场。
反向资本重组分两步进行:(I)Tottenham通过与Pubco合并并并入Pubco而重新注册到特拉华州(“再注册合并”);及(Ii)在重新合并合并后,Merge Sub立即与Clene Nanomedine合并并并入Clene Nanomedicine,导致Clene Nanomedicine成为pubco的全资子公司(“收购”)。截止日期,pubco将其名称从切尔西全球公司更名为Clene Inc.,并将其普通股上市,面值为$
反向资本重组完成后,在紧接重新合并生效时间之前发行并发行的每股托特纳姆普通股,总额为
在截止日期,当时发行和发行的每一股Clene Nanomedicine普通股被注销,其交换持有人收到
Clene Nanomedicine普通股的所有已发行股票期权,总计
我们收到的总收益是$
关于2018年8月托特纳姆的首次公开募股,托特纳姆向Chardan Capital Markets,LLC(以下简称Chardan)发出了购买
另外,关于反向资本重组,Clene Nanomedicine于2020年7月与LifeSci Capital LLC(“LifeSci”)签订了一项书面协议,LifeSci受聘担任Clene Nanomedicine的财务顾问,以确定和征求特殊目的收购公司,以便与Clene Nanomedicine及其股东进行合并或类似交易。根据这项协议,Clene Nanomedicine同意,如果它完成与托特纳姆的合并,
F-17
目录表
生活科学将会得到考虑
在实施反向资本重组后,立即出现了
在托特纳姆首次公开募股期间,托特纳姆产生了递延承销商费用,这些费用应在反向资本重组完成后从信托账户中持有的金额中支付给Chardan。在反向资本重组结束时,我们支付了$
根据公认会计原则,这笔交易被视为“反向资本重组”。在这种会计方法下,托特纳姆被视为财务报告中的“被收购”公司。这一决定主要基于以下事实:在反向资本重组后,Clene Nanomedicine的股东拥有本公司的多数投票权,Clene Nanomedine包括本公司所有正在进行的业务,Clene Nanomedine包括本公司管理机构的多数,Clene Nanomedine的高级管理人员包括本公司的所有高级管理人员。因此,为了会计目的,这笔交易被视为等同于Clene Nanomedicine为托特纳姆的净资产发行股票,并伴随着资本重组。反向资本重组前历史期间的股份和每股普通股净亏损已使用反向资本重组中确定的汇率追溯重报。托特纳姆的净资产按历史成本入账,没有商誉或其他无形资产入账。反向资本重组之前的手术是Clene Nanomedine的手术。
赚得股
Clene Nanomedicine的某些股东有权获得以下收益股票(“Clene Nanomedine或有收益”):(I)
初始股东可能有权获得如下收益股份(“初始股东或有收益”):(I)
或有收益在综合资产负债表中被归类为负债,在反向资本重组当日最初按公允价值计量,随后在每个报告日按公允价值重新计量(见附注16)。截至2021年12月30日,我们没有达到里程碑3和
F-18
目录表
4.预付费用和其他流动资产
截至的预付费用和其他流动资产2021年12月31日和2020年12月31日的情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
澳大利亚研发信用应收账款 |
|
$ |
|
|
$ |
|
||
CRO预付款 |
|
|
|
|
|
|
||
用于研究和开发的金属 |
|
|
|
|
|
|
||
董事及高级职员保险 |
|
|
|
|
|
|
||
其他 |
|
|
|
|
|
|
||
预付费用总额 |
|
$ |
|
|
$ |
|
||
5.财产和设备
财产和设备,净额,截至2021年12月31日和2020年12月31日的情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
实验室设备 |
|
$ |
|
|
$ |
|
||
家具和固定装置 |
|
|
|
|
|
|
||
租赁权改进 |
|
|
|
|
|
|
||
在建工程 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
减去累计折旧 |
|
|
( |
) |
|
|
( |
) |
财产和设备合计(净额) |
|
$ |
|
|
$ |
|
||
折旧费用合计$
6.应计负债
截至的应计负债2021年12月31日和2020年12月31日的情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
应计专业费用 |
|
$ |
|
|
$ |
|
||
应计薪酬和福利 |
|
|
|
|
|
|
||
应计CRO费用 |
|
|
|
|
|
|
||
递延赠款基金 |
|
|
|
|
|
|
||
应计费用报销 |
|
|
|
|
|
|
||
应计交易成本 |
|
|
|
|
|
|
||
其他 |
|
|
|
|
|
|
||
应计负债总额 |
|
$ |
|
|
$ |
|
||
7.租契
我们根据不可取消的运营和融资租赁租赁实验室和办公空间以及某些实验室设备。我们使用权租赁资产的账面价值主要集中在我们的房地产租赁上,而租赁协议的数量主要集中在设备租赁上。
经营租约
2020年4月,我们终止了办公空间的运营租约,并移除了剩余的使用权资产#美元。
2021年9月,我们开始了实验室空间的运营租赁,并记录了#美元的使用权资产。
F-19
目录表
由于租赁激励是根据我们控制范围内的事件支付的,并被视为合理地肯定会发生,因此我们将租赁激励记录为租赁开始时使用权资产和租赁负债的减少。截至2021年12月31日,我们发生了$
综合资产负债表上的使用权资产与经营租赁有关。截至2021年12月31日,我们的经营租赁债务的加权平均贴现率为
融资租赁
在融资租赁债务项下记录的资产,包括截至2021年12月31日和2020年12月31日的情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
实验室设备 |
|
$ |
|
|
$ |
|
||
家具和固定装置 |
|
|
|
|
|
|
||
Oracle Work in Process |
|
|
|
|
|
|
||
总计 |
|
|
|
|
|
|
||
减去累计折旧 |
|
|
( |
) |
|
|
( |
) |
网络 |
|
$ |
|
|
$ |
|
||
截至2021年12月31日,我们的融资租赁债务的加权平均利率为
租约成熟度分析
我们的融资和经营租赁的到期日分析2021年12月31日的情况如下:
(单位:千) |
|
金融 |
|
|
运营中 |
|
||
2022 |
|
$ |
|
|
$ |
|
||
2023 |
|
|
|
|
|
|
||
2024 |
|
|
|
|
|
|
||
2025 |
|
|
|
|
|
|
||
2026 |
|
|
|
|
|
|
||
此后 |
|
|
|
|
|
|
||
未贴现现金流合计 |
|
|
|
|
|
|
||
减去代表利息/贴现的金额 |
|
|
|
|
|
( |
) |
|
未来租赁付款的现值 |
|
|
|
|
|
|
||
未来租赁激励措施减少 |
|
|
|
|
|
( |
) |
|
减少租赁义务,本期部分 |
|
|
( |
) |
|
|
( |
) |
租赁义务,长期部分 |
|
$ |
|
|
$ |
|
||
我们预计,在正常业务过程中,现有租约将续期或由类似的租约取代。
F-20
目录表
租赁成本的构成
财务和经营租赁费用的构成部分截至2021年12月31日和2020年12月31日的年度如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
融资租赁成本: |
|
|
|
|
|
|
||
摊销 |
|
$ |
|
|
$ |
|
||
租赁负债利息 |
|
|
|
|
|
|
||
经营租赁成本 |
|
|
|
|
|
|
||
短期租赁成本 |
|
|
|
|
|
|
||
可变租赁成本 |
|
|
|
|
|
|
||
总租赁成本 |
|
$ |
|
|
$ |
|
||
补充现金流信息
(单位:千) |
|
2021 |
|
|
2020 |
|
||
来自经营租赁的经营现金流 |
|
$ |
( |
) |
|
$ |
( |
) |
融资租赁的营运现金流 |
|
$ |
( |
) |
|
$ |
( |
) |
融资租赁产生的现金流 |
|
$ |
( |
) |
|
$ |
( |
) |
8.应付票据
我们的长期债务,扣除原始发行贴现和未摊销债务发行成本,如2021年12月31日和2020年12月31日的情况如下:
(单位:千,利率数据除外) |
|
利率,利率 |
|
|
2021 |
|
|
2020 |
|
|||
应付票据: |
|
|
|
|
|
|
|
|
|
|||
马里兰州住房和社区发展部 |
|
|
% |
|
$ |
|
|
$ |
|
|||
高级塞西尔公司 |
|
|
% |
|
|
|
|
|
|
|||
工资保障计划 |
|
|
% |
|
|
— |
|
|
|
|
||
大道创业机会基金,L.P. |
|
|
% |
|
|
|
|
|
— |
|
||
其他 |
|
|
% |
|
|
— |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
减少未摊销债务发行成本和原始发行折扣 |
|
|
|
|
|
( |
) |
|
|
— |
|
|
扣除未摊销债务贴现和发行成本后的应付可转换票据减少(见附注11) |
|
|
|
|
|
( |
) |
|
|
— |
|
|
应付票据总额 |
|
|
|
|
$ |
|
|
$ |
|
|||
马里兰州贷款
2019年2月,我们与马里兰州主要部门住房和社区发展部签订了一项贷款协议(2019年MD贷款)。该协议规定定期贷款为$
的收入$
F-21
目录表
塞西尔县贷款
2019年4月,我们与根据马里兰州法律成立的非股份公司Advance Cecil Inc.签订了一项贷款协议(“2019 Cecil贷款”),在执行2019年Cecil贷款时,向美国国税局申请501(C)(3)身份。该协议规定定期贷款为$
的收入$
购买力平价贷款
2020年5月,我们签订了一份应付票据,金额为$
大道贷款
2021年5月,我们与Avenue签订了2021大道贷款。该协议规定提供最高可达42个月的定期贷款$
根据协议,我们向The Avenue授予了购买
F-22
目录表
已记账对于根据ASC 815于2021大道贷款开始时的第2批认股权证,公允价值及可发行股份将于每个报告期重新计量(见附注10)。Avenue也有权酌情决定,但没有义务,在贷款未偿还期间,从协议的第一年到第三年的任何时候,将最高可达$
根据2021大道的贷款,我们同意了积极和消极的契约,在没有提前还款的情况下,我们在到期时仍将遵守这些契约。这些条款包括提供有关我们公司和业务的信息;限制我们按照证券条款以外的其他方式报废、回购或赎回普通股、期权和认股权证的能力;以及限制我们支付现金或财产红利的能力。
以下
(单位:千) |
|
截至2021年12月31日 |
|
|
2022 |
|
$ |
|
|
2023 |
|
|
|
|
2024 |
|
|
|
|
2025 |
|
|
|
|
2026 |
|
|
|
|
此后 |
|
|
|
|
未来本金付款小计 |
|
|
|
|
与发行日期相关的减去未摊销债务折价权证公允价值 |
|
|
( |
) |
总计 |
|
$ |
|
|
9.优先股权证责任
在反向资本重组之前,2013年,我们发行了A系列优先股权证和10年期认股权证,以购买我们最优先股的单位,相当于
在反向资本重组之前,我们将优先股权证归类为综合资产负债表上的负债,因为权证是独立的金融工具,可能需要我们在行使时转移资产。优先股权证负债最初按公允价值入账,其后在综合经营及全面亏损报表中按公允价值重新计量为其他收入(支出)净额的一部分(见附注16)。在反向资本重组结束时,所有已发行的Clene Nanomedic优先股转换为普通股,优先股权证转换为认股权证,以购买普通股(见附注10,脚注4)。在转换时,我们评估了优先股权证负债的特征,并确定它们符合分类为永久股本的条件。因此,我们在反向资本重组结束时将优先股权证负债重新计量为公允价值,并将其重新分类为额外实收资本,并确认了$
F-23
目录表
10.普通股认股权证
自.起2021年12月31日,购买普通股的已发行认股权证如下:
可行使的日期 |
|
数量 |
|
|
|
|
行权价格 |
|
|
可行使的权力 |
|
分类 |
|
期满 |
||
2020年12月 |
|
|
|
|
(1) |
|
$ |
|
|
|
|
|||||
2020年12月 |
|
|
|
|
(2) |
|
$ |
|
|
|
|
|||||
2020年12月 |
|
|
|
|
(3) |
|
$ |
|
|
|
|
|||||
May 2021 |
|
|
|
|
(4)(5) |
|
$ |
|
|
|
|
|||||
总计 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
截至2020年12月31日,购买普通股股份的已发行认股权证如下:
可行使的日期 |
|
数量 |
|
|
|
|
行权价格 |
|
|
可行使的权力 |
|
分类 |
|
期满 |
||
2021年6月 |
|
|
|
|
(6) |
|
$ |
|
|
|
|
|||||
2020年12月 |
|
|
|
|
(1) |
|
$ |
|
|
|
|
|||||
2020年12月 |
|
|
|
|
(2) |
|
$ |
|
|
|
|
|||||
2020年12月 |
|
|
|
|
(3) |
|
$ |
|
|
|
|
|||||
总计 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
11.可转换票据
2020年可转换票据
我们于2020年2月至7月发行了可转换本票(“2020可转换票据”),本金总额$
F-24
目录表
导数仪器的使用$
于2020年8月,与本公司发行及出售D系列优先股有关,2020年可换股票据项下的未偿还本金及应计利息合共$
2020年12月,在完成反向资本重组(见附注3)后,所有已发行的D系列优先股均转换为普通股。我们将2020年可转换票据的转换计入债务清偿,并确认了$
我们确认了利息支出$
可转换应付票据
2021年5月,关于2021 Avenue贷款,我们向Avenue发布了转换功能(见附注8)。转换功能取决于与我们的股票价格和交易量相关的某些转换标准。转换功能不符合单独核算的要求,不作为衍生工具入账。截至2021年12月31日,转换后可能发行的普通股数量为
我们把它归为$
12.衍生工具
2020年可转换债券的赎回特点
2020年可换股票据的赎回功能包含嵌入式功能,为贷款人提供多种结算选择,包括(I)于票据转换时获得固定数目的吾等股份的权利,或(Ii)于完成集资交易、控制权变更或违约时收取现金或可变数目股份的权利。赎回功能符合作为衍生工具进行分类和核算的要求。2020年衍生工具按公允价值计入$
或有收益股
或有收益股份符合作为衍生工具单独核算的要求。在完成反向资本重组后,我们记录了(I)Clene Nanomedine或有收益的公允价值$
截至2021年12月31日和2020年12月31日,Clene Nanomedine应急收益的公允价值为$
截至2021年12月31日和2020年12月31日,初始股东或有收益的公允价值为$
F-25
目录表
截至2021年12月31日,我们没有达到里程碑3和
大道搜查令
根据2021 Avenue贷款的第1批发行的Avenue认股权证和根据第2批的潜在提款(见附注8)可发行的认股权证符合作为衍生工具单独核算的要求。在发行大道认股权证时,我们根据其公允价值将普通股认股权证负债确认为债务折扣。$
13.承付款和或有事项
我们在正常业务过程中与CRO签订了临床试验协议,并与供应商签订了临床前研究及其他服务和产品用于运营目的的协议,这些协议可由我们随时取消,但须支付我们在有约束力的采购订单下的剩余义务,在某些情况下,还需支付象征性的提前终止费。这些承诺被认为并不重要。
有时,我们可能会在正常的业务活动过程中产生某些或有法律责任。如果将来有可能发生支出,并且这些支出可以合理估计,我们就应为此类事项承担责任。我们不知道目前有任何悬而未决的法律问题或索赔。
截至2021年12月31日,我们根据各种协议承诺的资本支出总额为$
14.所得税
我们没有为截至2021年12月31日和2020年12月31日的年度发生的净营业亏损、研发税收抵免或其他递延税项资产记录所得税优惠,这是由于从这些项目实现收益的不确定性。
年度所得税前收入(亏损)的组成部分截至2021年12月31日和2020年12月31日的年度情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
美国 |
|
$ |
( |
) |
|
$ |
( |
) |
外国 |
|
|
( |
) |
|
|
|
|
扣除所得税准备前的亏损 |
|
$ |
( |
) |
|
$ |
( |
) |
企业所得税支出(福利)截至2021年12月31日和2020年12月31日的年度情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
当期税费(福利): |
|
|
|
|
|
|
||
联邦制 |
|
$ |
— |
|
|
$ |
|
|
状态 |
|
|
— |
|
|
|
|
|
外国 |
|
|
(146 |
) |
|
|
|
|
当期税费(收益)合计 |
|
|
(146 |
) |
|
|
|
|
|
|
|
|
|
|
|
||
递延税费(福利): |
|
|
|
|
|
|
||
联邦制 |
|
|
— |
|
|
|
|
|
状态 |
|
|
— |
|
|
|
|
|
外国 |
|
|
( |
) |
|
|
|
|
递延税费(福利)合计 |
|
|
( |
) |
|
|
|
|
所得税支出(福利)合计 |
|
$ |
( |
) |
|
$ |
|
|
F-26
目录表
对按美国联邦法定税率计算的所得税进行核对
(单位:千) |
|
2021 |
|
|
2020 |
|
||
按联邦法定税率缴纳所得税费用(福利) |
|
$ |
( |
) |
|
$ |
( |
) |
州所得税(扣除联邦福利后的净额) |
|
|
( |
) |
|
|
( |
) |
普通股认股权证负债的公允价值变动 |
|
|
( |
) |
|
|
|
|
或有收益的公允价值变动 |
|
|
( |
) |
|
|
( |
) |
研发税收抵免 |
|
|
( |
) |
|
|
( |
) |
股票薪酬 |
|
|
( |
) |
|
|
|
|
外币利差 |
|
|
( |
) |
|
|
|
|
其他 |
|
|
|
|
|
|
||
更改估值免税额 |
|
|
|
|
|
|
||
所得税支出(福利) |
|
$ |
( |
) |
|
$ |
|
|
(单位:千) |
|
2021 |
|
|
2020 |
|
||
递延税项资产(负债): |
|
|
|
|
|
|
||
净营业亏损结转 |
|
$ |
|
|
$ |
|
||
折旧及摊销 |
|
|
|
|
|
|
||
研发学分 |
|
|
|
|
|
|
||
租赁责任 |
|
|
|
|
|
|
||
使用权资产 |
|
|
( |
) |
|
|
( |
) |
应计利息 |
|
|
|
|
|
|
||
非限制性股票期权和限制性股票奖励 |
|
|
|
|
|
|
||
应计补偿 |
|
|
|
|
|
|
||
其他 |
|
|
|
|
|
( |
) |
|
递延税项资产(负债)总额 |
|
|
|
|
|
|
||
减去:估值免税额 |
|
|
( |
) |
|
|
( |
) |
递延税项净资产(负债) |
|
$ |
|
|
$ |
( |
) |
|
在评估递延税项资产的变现能力时,我们会考虑部分或全部递延税项资产是否更有可能不会变现。递延税项资产的最终变现取决于在这些临时差额可扣除期间产生的未来应纳税所得额。在作出评估时,我们会考虑递延税项负债的预定冲销、预计未来应课税收入、结转机会及税务筹划策略。我们认为,我们很可能不会意识到这些可扣除差额的好处,并对它们应用了全额估值免税额。
我们的联邦和州净营业亏损(“NOL”)约为$
根据1986年《国内税法》第382条的规定,我们所有权的重大变化可能会导致未来几年可以利用的NOL结转和研发信用额度受到限制。无论产生结转和研发抵免的纳税年度是否已根据法规关闭,结转和研究与开发抵免都应在其使用的年度接受审查。免税额仅限于已使用的金额。因此,我们可能会受到以前的NOL和抵免的审查,这些NOL和抵免是由于利用此类税收属性而产生的。
截至2021年12月31日和2020年12月31日,我们没有记录任何未确认的税收优惠金额。我们在所得税支出中确认与所得税相关的利息和罚金。我们在综合资产负债表上没有应计利息和罚金,也没有在截至2021年12月31日和2020年12月31日的年度的综合经营表和全面亏损中确认利息和罚金。
F-27
目录表
我们在美国、澳大利亚、荷兰和各个州的司法管辖区都要纳税。由于未使用的净营业亏损和研发抵免的结转,我们从2014年到现在的纳税申报单受到美国和州当局的审查。目前没有悬而未决的考试。
15.福利计划
401(K)计划
我们的401(K)计划是根据《国税法》第401(K)节的延期工资安排。根据401(K)计划,参与计划的美国员工可以推迟支付部分税前收入,最高可达美国国税局的年度缴费限额。我们配得上
2020年股票计划
2020年12月,关于反向资本重组,董事会批准了2020年股票计划,并保留了
2020年股票计划由董事会管理。
截至2021年12月31日,董事会批准
2014年股票计划
在反向资本重组结束后,2014年股票计划由董事会管理。根据2014股票计划授予的股票期权在授予日期十年后到期。授予员工、高级管理人员、董事和顾问的股票期权和限制性股票奖励通常在四年内授予。
作为反向资本重组的结果,
基于股票的薪酬费用
截至2021年12月31日和2020年12月31日止年度,在研究和开发费用以及一般和行政费用中记录的股票薪酬支出如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
一般和行政 |
|
$ |
|
|
$ |
|
||
研发 |
|
|
|
|
|
|
||
基于股票的薪酬总额 |
|
$ |
|
|
$ |
|
||
F-28
目录表
股票期权
截至2021年12月31日的年度未偿还股票期权及相关活动如下:
(以千为单位,不包括股票、每股和期限数据) |
|
数量 |
|
|
加权 |
|
|
加权 |
|
|
固有的 |
|
||||
未偿还-2020年12月31日 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
授与 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
已锻炼 |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|||
没收 |
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|||
未偿还-2021年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
既得和可行使--2021年12月31日 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
既得、可行使和预期的 |
|
|
|
|
$ |
|
|
|
|
|
$ |
|
||||
与股票期权相关的股票薪酬费用合计$
在反向资本重组之前,股票期权的行权价格是基于Clene Nanomedicine董事会在授予日确定的Clene Nanomedic普通股的公平市场价值,并得到管理层的投入。Clene Nanomedicine的董事会通过考虑多个客观和主观因素来确定公允价值,这些因素包括第三方409a估值报告、可比公司的估值、可赎回可转换优先股的销售、向非关联第三方出售普通股、经营和财务业绩、我们普通股的流动性不足,以及总体和行业特定的经济前景。
在反向资本重组之后,股票期权使用布莱克-斯科尔斯期权定价模型进行估值。由于我们普通股的交易历史有限,预期波动率是根据我们行业内几家不相关的可比上市公司在相当于股票期权授予的预期期限的期间内的平均历史股票波动率得出的。股票期权合同期限内的无风险利率以授予日生效的美国国债收益率曲线为基础。预期股息假设为零,因为我们从未支付过股息,也没有这样做的计划。预期期限代表股票期权预期未偿还的期间。对于被认为是在正常过程中的股票期权,我们使用简化的方法来确定预期期限,该方法认为该期限是股票期权的归属时间和合同期限的平均值。对于其他股票期权授予,我们使用关于员工行使和授予后雇佣终止行为的历史数据来估计预期期限,同时也考虑到授予的合同期限。
在截至2021年12月31日的年度内,用于计算已授予股票期权公允价值的假设如下:
|
|
2021 |
|
2020 |
预期股价波动 |
|
|
||
无风险利率 |
|
|
||
预期股息收益率 |
|
|
||
期权的预期期限 |
|
|
截至2021年12月31日止年度内已授出之购股权之加权平均授出日公允价值为$
限制性股票奖
F-29
目录表
未予行使的限制性股票奖励权利及相关活动截至2021年12月31日的年度情况如下:
|
|
数量 |
|
|
加权平均授予日期公允价值 |
|
||
截至2020年12月31日的未归属余额 |
|
|
|
|
$ |
|
||
归属时转换为普通股 |
|
|
( |
) |
|
|
|
|
没收 |
|
|
( |
) |
|
|
|
|
截至2021年12月31日的未归属余额 |
|
|
|
|
$ |
|
||
与限制性股票奖励权利相关的基于股票的薪酬支出总额$
我们使用蒙特卡罗估值模型来估计股票奖励的公允价值,以模拟某些股票价格里程碑的实现。不可观测的输入包括预期股价波动率、无风险利率和预期期限。截至2020年12月31日,预期股价波动为
16.公允价值
现金按公允价值计提。金融工具,包括应收账款、应付账款和应计费用按成本列账,考虑到其短期性质,成本接近公允价值。2019年MD贷款、2019年塞西尔贷款、与2021大道贷款相关的衍生品工具以及与或有收益相关的衍生品工具按公允价值列账。2021大道的贷款、相关的应付可转换票据和转换功能按摊销成本列账,由于我们的信用风险和市场利率,该成本接近公允价值。
F-30
目录表
按公允价值经常性计量的负债
截至2021年12月31日,按公允价值经常性计量的负债的公允价值等级如下:
|
|
2021 |
|
|||||||||||||
|
|
1级 |
|
|
2级 |
|
|
3级 |
|
|
总计 |
|
||||
应付票据 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
普通股认股权证责任 |
|
|
|
|
|
|
|
|
|
|
$ |
|
||||
Clene Nanomedics应急收益 |
|
|
|
|
|
|
|
|
|
|
$ |
|
||||
初始股东或有收益 |
|
|
|
|
|
|
|
|
|
|
$ |
|
||||
截至2020年12月31日,按公允价值经常性计量的负债的公允价值等级如下:
|
|
2020 |
|
|||||||||||||
|
|
1级 |
|
|
2级 |
|
|
3级 |
|
|
总计 |
|
||||
应付票据 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||
Clene Nanomedics应急收益 |
|
|
|
|
|
|
|
|
|
|
$ |
|
||||
初始股东或有收益 |
|
|
|
|
|
|
|
|
|
|
$ |
|
||||
在截至2021年12月31日的一年中,1级、2级或3级之间没有任何转移。于截至2020年12月31日止年度,应付票据由第3级转至第1级,这是因为在进行反向资本重组后,应付票据的公允价值乃根据纳斯达克报告的普通股价格厘定。
应付票据和可转换应付票据的估值
应付票据及可转换票据的账面价值包括若干按摊销成本列账的票据,以及若干于截至2021年及2020年12月31日的综合资产负债表内按公允价值经常性重计量的票据。为了评估票据的价值,我们考虑了即将到期的简单利息支出金额和我们普通股的价值。
截至2021年12月31日和2020年12月31日,2019年MD贷款和2019年塞西尔贷款的公允价值是根据我们普通股的收盘价确定的$
截至2021年12月31日,2021大道贷款的摊销成本为$
转换功能的评估
2021大道贷款的应付可转换票据的转换特征是按摊销成本计入的,不符合单独核算的要求,也不作为衍生工具入账。截至2021年12月31日,转换功能的估计公允价值为$
|
|
2021 |
|
|
预期股价波动 |
|
|
% |
|
无风险利率 |
|
|
% |
|
预期股息收益率 |
|
|
% |
|
预期期限 |
|
|
||
优先股购买权证的估值
我们的优先股权证负债包含无法观察到的信息,这些信息反映了我们自己的假设。因此,优先股权证负债在经常性基础上使用不可观察的投入按公允价值计量。在2020年12月30日优先股权证债务解除之前,优先股权证债务是使用Black-Scholes期权定价模型进行估值的。
Clene Nanomedicine董事会通过考虑多个客观和主观因素来确定优先股的公允价值,这些因素包括第三方估值、可比公司的估值、可赎回可转换优先股的销售、向无关第三方出售普通股、经营和财务业绩、我们的股本缺乏流动性,以及总体和行业特定的经济前景。我们根据可比同行估计了优先股的波动性。
F-31
目录表
公司的历史波动性。认股权证合约期内的无风险利率以估值日生效的美国国债收益率曲线为基础。我们没有宣布任何未来股息的计划。优先股权证负债的公允价值的确定可能会根据我们优先股价值的变化和上文所述的其他假设在未来期间发生变化。本公司将公允价值变动计入综合经营报表中优先股权证负债支出项目的公允价值变动及全面亏损。
在反向资本重组结束时(见附注3),所有已发行的Clene Nanomedine优先股转换为普通股,Clene Nanomedine优先股权证转换为购买普通股的认股权证。因此,优先股权证债务已于2020年12月30日与Clene Nanomedicine优先股转换有关(见附注9)。
普通股认股权证负债的估值
根据2021大道贷款的第1批,我们发布了大道认股权证以购买
普通股认股权证负债的估计公允价值是使用Black-Scholes期权定价模型确定的。负债的账面金额可能会大幅波动,实际金额可能与负债的估计价值存在重大差异。截至2020年12月31日,普通股认股权证债务尚未清偿。截至2021年12月31日,布莱克-斯科尔斯期权定价模型的不可观测输入如下:
|
|
2021 |
|
|
预期股价波动 |
|
|
% |
|
无风险利率 |
|
|
% |
|
预期股息收益率 |
|
|
% |
|
预期期限 |
|
|
||
或有收益的估值
在完成反向资本重组后,截至2020年12月31日,
或有收益的估计公允价值是使用蒙特卡罗估值模型来确定的,以便模拟收益期间我们的股票价格的未来路径。负债的账面价值可能会大幅波动,实际支付的金额可能与负债的估计价值存在重大差异。截至2021年12月31日和2020年12月31日,蒙特卡洛估值模型的不可观测投入如下:
|
|
2021 |
|
|
2020 |
|
||
预期股价波动 |
|
|
% |
|
|
% |
||
无风险利率 |
|
|
% |
|
|
% |
||
预期股息收益率 |
|
|
0.00 |
% |
|
|
% |
|
预期期限 |
|
|
|
|
||||
F-32
目录表
截至2021年12月31日和2020年12月31日的年度,我们财务负债的公允价值变动如下:
(单位:千) |
|
备注 |
|
|
衍生工具 |
|
|
择优 |
|
|
普通股认股权证 |
|
|
克伦纳米医学 |
|
|
首字母 |
|
||||||
余额-2019年12月31日 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||||
发行可转换本票 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
票据的初始公允价值 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
公允价值变动 |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
||
与转换可赎回可转换优先股有关的优先股权证法律责任的终绝 |
|
|
|
|
|
|
|
|
( |
) |
|
|
|
|
|
|
|
|
|
|||||
与2020年可换股票据清偿有关的衍生法律责任的清偿(附注12) |
|
|
|
|
|
( |
) |
|
|
|
|
|
( |
) |
|
|
|
|
|
|
||||
余额-2020年12月31日 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||||
票据的初始公允价值 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
公允价值变动 |
|
|
( |
) |
|
|
|
|
|
|
|
|
( |
) |
|
|
( |
) |
|
|
( |
) |
||
余额-2021年12月31日 |
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
|
$ |
|
||||||
17.可赎回可转换优先股
在反向资本重组之前,我们向不同的投资者发行了A、B、C和D系列优先股。优先股可根据持有者的选择权以转换价格转换为Clene Nanomedicine普通股。我们评估了优先股,并得出结论,它不符合被归类为负债的标准。然而,我们决定优先股应该被归类为临时股本,因为我们可能需要以现金赎回已发行的优先股。我们得出的结论是,赎回事件不太可能发生,因此,优先股的价值没有根据其赎回金额进行调整。
随着反向资本重组的结束,优先股被转换为
18.普通股
截至2021年12月31日和2020年12月31日,经修订和重述的公司注册证书授权我们发行
我们的普通股股东有权每股一票,并有权获得任何股东大会的通知。普通股持有人的投票权、分红和清算权受各类股票持有人优先权利的约束,并受优先股持有人的权利、权力、优先权和特权的限制。在所有已宣布的优先股股息支付或拨备支付给优先股持有人之前,不得对普通股进行分配。普通股不能根据持有人的选择进行赎回。
在完成反向资本重组后,总未偿还
在完成反向资本重组之前,我们于2020年12月与多家投资者订立认购协议,出售及发行
F-33
目录表
2021年5月,我们与2021年管道的各个投资者签订了认购协议,以出售和发行
2021年7月,查尔丹行使查尔丹单位购买选择权
截至2021年12月31日和2020年12月31日,我们发行和发行的普通股为
19.普通股股东每股净亏损
计算截至2021年12月31日和2020年12月31日的年度普通股股东应占每股基本和摊薄净收益(亏损)如下:
(以千为单位,不包括每股和每股数据) |
|
2021 |
|
|
2020 |
|
||
分子: |
|
|
|
|
|
|
||
普通股股东应占净亏损 |
|
$ |
( |
) |
|
$ |
( |
) |
分母: |
|
|
|
|
|
|
||
加权平均流通股 |
|
|
|
|
|
|
||
普通股股东应占每股基本亏损和稀释后每股净亏损 |
|
$ |
( |
) |
|
$ |
( |
) |
在计算截至2021年12月31日和2020年12月31日的年度普通股股东应占每股摊薄净亏损时,不包括下列潜在稀释性证券股份,因为包括这些股份将是反稀释的,或者此类股份的发行取决于某些条件的满足,而这些条件在期末尚未满足,或者它们不在资金范围之内:
|
|
2021 |
|
|
2020 |
|
||
可转换认股权证(见附注11) |
|
|
|
|
|
|
||
普通股认股权证(见附注10) |
|
|
|
|
|
|
||
购买普通股的期权 |
|
|
|
|
|
|
||
未归属的限制性股票奖励 |
|
|
|
|
|
|
||
购买普通股的单位购买选择权(见附注1) |
|
|
|
|
|
|
||
赚取股份(见附注3及12) |
|
|
|
|
|
|
||
总计 |
|
|
|
|
|
|
||
20.关联方交易
许可和供应协议
2018年8月,我们与4Life签订了一项供应协议,同时4Life投资于我们的C系列优先股和认股权证。根据供应协议,我们授予4Life使用我们的某些知识产权开发膳食补充剂的独家许可。独家许可的期限为自供应协议下的产品销售开始之日起数年,如果到2023年1月1日仍未开始销售,则视为开始日期,并可选择续订额外的五年期限。我们向4Life提供非医药产品进行开发,4Life支付
于截至二零二一年十二月三十一日及二零二零年十二月三十一日止年度内,我们根据供应协议销售产品合共$
F-34
目录表
21.地理位置和细分市场信息
地理信息
截至2021年12月31日和2020年12月31日,由财产和设备组成的按地点净额的长期资产如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
美国 |
|
$ |
|
|
$ |
|
||
澳大利亚 |
|
|
|
|
|
|
||
财产和设备合计(净额) |
|
$ |
|
|
$ |
|
||
段信息
我们的运营部门利润衡量标准是运营部门亏损,计算方法为收入减去收入成本、研发成本以及一般和行政费用。
(单位:千) |
|
2021 |
|
|
2020 |
|
||
毒品: |
|
|
|
|
|
|
||
来自外部客户的收入 |
|
$ |
|
|
$ |
|
||
折旧费用 |
|
|
( |
) |
|
|
( |
) |
股票补偿费用 |
|
|
( |
) |
|
|
( |
) |
运营亏损 |
|
|
( |
) |
|
|
( |
) |
补充剂: |
|
|
|
|
|
|
||
来自外部客户的收入 |
|
$ |
|
|
$ |
|
||
折旧费用 |
|
|
( |
) |
|
|
( |
) |
股票补偿费用 |
|
|
|
|
|
|
||
营业收入(亏损) |
|
|
|
|
|
|
||
综合: |
|
|
|
|
|
|
||
来自外部客户的收入 |
|
$ |
|
|
$ |
|
||
折旧费用 |
|
|
( |
) |
|
|
( |
) |
股票补偿费用 |
|
|
( |
) |
|
|
( |
) |
运营亏损 |
|
|
( |
) |
|
|
( |
) |
对应报告部门的运营亏损总额与综合所得税前净亏损的核对截至2021年12月31日和2020年12月31日的年度情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
运营中的部门损失 |
|
$ |
( |
) |
|
$ |
( |
) |
其他收入(费用)合计,净额 |
|
|
|
|
|
|
||
所得税前净亏损 |
|
$ |
( |
) |
|
$ |
( |
) |
部门资产不包括公司资产,如现金、限制性现金和公司设施。截至按可报告部门分列的总资产2021年12月31日和2020年12月31日的情况如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
总资产: |
|
|
|
|
|
|
||
毒品 |
|
$ |
|
|
$ |
|
||
补充剂 |
|
|
|
|
|
|
||
公司 |
|
|
|
|
|
|
||
整合 |
|
$ |
|
|
$ |
|
||
F-35
目录表
对长期资产的补充截至2021年12月31日和2020年12月31日的年度如下:
(单位:千) |
|
2021 |
|
|
2020 |
|
||
毒品 |
|
$ |
|
|
$ |
|
||
补充剂 |
|
|
|
|
|
|
||
公司 |
|
|
|
|
|
|
||
整合 |
|
$ |
|
|
$ |
|
||
22.后续事件
2022年2月11日,我们对Avenue贷款进行了修改,延长了我们提取美元的能力
F-36
目录表
项目9。会计与财务信息披露的变更与分歧
没有。
第9A项。控制和程序
信息披露控制和程序的评估
在包括我们的首席执行官和首席财务官在内的管理层的监督和参与下,我们对截至2021年12月31日的披露控制和程序的有效性进行了评估,该术语在《交易法》规则13a-15(E)和15d-15(E)中定义。作为这项评估的结果,我们的首席执行官和首席财务官得出结论,截至2021年12月31日,由于下文所述的财务报告内部控制存在重大弱点,我们的披露控制和程序并不有效。尽管发现了重大弱点,但管理层,包括我们的首席执行官和首席财务官,认为本年度报告中包括的综合财务报表在所有重要方面都公平地反映了我们截至和根据美国公认会计原则列报的期间的财务状况、经营结果和现金流量。
披露控制和程序旨在确保在我们根据交易所法案提交或提交的报告中需要披露的信息在美国证券交易委员会规则和表格中指定的时间段内被记录、处理、汇总和报告,并且这些信息被积累并在适当时传达给我们的管理层,包括我们的首席执行官和首席财务官,以便及时做出关于所需披露的决定。
管理层财务报告内部控制年度报告
管理层负责按照《交易法》第13a-15(F)和15d-15(F)条的规定,建立和维持对财务报告的充分内部控制。管理层根据特雷德韦委员会赞助组织委员会发布的《内部控制-综合框架(2013)》中确立的标准,评估了我们对财务报告的内部控制的有效性。作为这项评估的结果,管理层得出结论,截至2021年12月31日,由于下文所述的财务报告内部控制存在重大弱点,我们对财务报告的内部控制并不有效。作为一家新兴的成长型公司,我们不需要在本年报中包括由我们的独立注册会计师事务所出具的财务报告内部控制的认证报告。
财务报告内部控制存在的重大缺陷
在对截至2021年和2020年12月31日的财务报表进行审计时,我们的管理层发现了财务报告内部控制中的重大弱点。重大缺陷是指财务报告的内部控制存在缺陷或缺陷的组合,使得我们的年度或中期财务报表的重大错报有合理的可能性无法及时防止或发现。发现的重大弱点与我们没有设计或维持与我们的财务报告要求相称的有效控制环境有关。我们控制环境中的这一缺陷导致了与我们财务报告内部控制活动以及信息和通信有关的以下其他重大缺陷:
上述控制缺陷中的每一个都可能导致一个或多个账户余额或披露的错报,从而导致年度或中期合并财务报表的重大错报,而这些错报是无法预防或发现的。因此,我们的管理层已经确定,上述每一项控制缺陷都构成重大弱点。
94
目录表
物质劣势补救
管理层继续积极参与并致力于采取必要步骤,以补救构成上述重大弱点的控制缺陷。2021年期间,我们对我们的控制环境进行了以下改进:
我们继续加强公司对流程级别控制和结构的监督,以确保适当分配权力、责任和问责,以弥补我们的重大弱点。我们相信,我们的补救计划将足以补救已发现的重大弱点,并加强我们对财务报告的内部控制。随着我们继续评估并努力改进我们对财务报告的内部控制,管理层可能会确定有必要采取额外措施来解决控制缺陷或对补救计划的修改。
财务报告内部控制的变化
除以下项描述的更改外--物质弱点补救“如上所述,在截至2021年12月31日的季度内,我们对财务报告的内部控制没有发生变化,这些变化是根据《交易法》规则13a-15和15d-15的(B)段要求的管理层评估而确定的,这些变化对我们的财务报告内部控制产生了重大影响,或有合理的可能性对其产生重大影响。
项目9B。其他信息
没有。
项目9C。关于妨碍检查的外国司法管辖区的披露
不适用。
95
目录表
第三部分
第10项。董事、高管与公司治理
按项目要求的信息包括在我们关于2022年股东年会的最终委托书中,并以引用的方式并入本文。最终委托书将在与本年度报告相关的财政年度结束后120天内提交给美国证券交易委员会。
项目11。高管薪酬
按项目要求的信息包括在我们关于2022年股东年会的最终委托书中,并以引用的方式并入本文。最终委托书将在与本年度报告相关的财政年度结束后120天内提交给美国证券交易委员会。
项目12。某些实益拥有人的担保所有权以及管理层和相关股东的事项
按项目要求的信息包括在我们关于2022年股东年会的最终委托书中,并以引用的方式并入本文。最终委托书将在与本年度报告相关的财政年度结束后120天内提交给美国证券交易委员会。
第13项。某些关系和相关交易,以及董事的独立性
按项目要求的信息包括在我们关于2022年股东年会的最终委托书中,并以引用的方式并入本文。最终委托书将在与本年度报告相关的财政年度结束后120天内提交给美国证券交易委员会。
项目14。首席会计师费用及服务
按项目要求的信息包括在我们关于2022年股东年会的最终委托书中,并以引用的方式并入本文。最终委托书将在与本年度报告相关的财政年度结束后120天内提交给美国证券交易委员会。
96
目录表
第四部分
项目15。展示和财务报表明细表
独立注册会计师事务所报告
合并资产负债表
合并经营报表和全面亏损
可赎回可转换优先股和股东权益合并报表(亏损)
合并现金流量表
合并财务报表附注
所有附表都被省略,因为合并财务报表或附注中包含了所需资料,或因为不需要这些资料。
见下文(B)部分所列的证物。
展品 |
|
展品说明 |
2.1 |
|
合并协议,日期为2020年9月1日(通过参考切尔西全球公司于2020年9月10日提交的S-4表格的委托书/征求同意书/招股说明书附件A-1并入)。 |
3.1 |
|
Clene Inc.的第三次修订和重新注册证书(通过引用注册人于2021年7月16日提交的当前8-K表格报告的附件3.1并入)。 |
3.2 |
|
Clene Inc.的章程(通过参考注册人于2021年1月5日提交的表格8-K的当前报告的附件3.2并入)。 |
4.1* |
|
注册人的证券描述。 |
4.2 |
|
认股权证协议,日期为2018年8月1日,由大陆股票转让信托公司和注册人签署(通过引用附件4.1并入托特纳姆于2018年8月7日提交的当前8-K表格报告中)。 |
4.3 |
|
托塔授权证样本(通过引用托特纳姆于2018年7月5日提交的S-1表格注册声明的附件4.3并入)。 |
10.1# |
|
Clene Inc.董事会薪酬计划(通过引用附件10.1并入注册人于2021年4月22日提交的当前8-K表格报告中)。 |
10.2# |
|
2020年股权激励计划(通过引用附件10.4并入注册人于2021年1月5日提交的当前8-K表格报告中)。 |
10.3# |
|
注册人与其董事及行政人员之间的赔偿协议格式(由 参考附件10.18切尔西全球公司于2020年12月15日提交的S-4表格注册声明)。 |
10.4# |
|
行政人员聘用协议表格(参照注册人于2022年2月2日提交的当前8-K表格报告的附件10.3)。 |
10.5 |
|
注册权协议表格(通过引用切尔西全球公司于2020年12月15日提交的S-4表格注册声明的附件10.10并入)。 |
10.6 |
|
认购协议表格(引用切尔西全球公司于2020年12月15日提交的S-4表格注册声明的附件10.12)。 |
10.7 |
|
认购协议表格(通过引用附件10.4并入注册人于2021年5月24日提交的当前8-K表格报告中)。 |
10.8## |
|
Clene Nanomedicine,Inc.和4Life Research,LLC之间的许可协议,2018年8月31日生效(通过引用切尔西全球公司于2020年12月15日提交的S-4表格注册声明的附件10.14合并)。 |
10.9 |
|
Clene Nanomedicine,Inc.和4Life Research,LLC之间的独家供应协议,日期为2018年8月31日(通过引用切尔西全球公司于2020年12月15日提交的S-4表格注册声明的附件10.15而并入)。 |
10.10 |
|
Clene Nanomedicine,Inc.和General Hospital Corporation于2019年9月27日签署的临床研究支持协议(通过引用切尔西全球公司于2020年12月15日提交的S-4表格注册声明的附件10.17而并入)。 |
97
目录表
10.11 |
|
贷款和担保协议,日期为2021年5月21日,由Clene Inc.、Clene Nanomedicine,Inc.和Avenue Venture Opportunities Fund,L.P.(通过引用注册人于2021年5月24日提交的当前8-K表格报告的附件10.1并入)。 |
10.12## |
|
贷款和担保协议的第一修正案,日期为2021年6月30日,由Clene Inc.,Clene Nanomedicine,Inc.和Avenue Venture Opportunities Fund,L.P.(通过引用注册人于2021年8月9日提交的Form 10-Q季度报告的附件10.3合并而成)。 |
10.13 |
|
Clene Inc.、Clene Nanomedicine,Inc.和Avenue Venture Opportunities Fund,L.P.之间的贷款和担保协议补编,日期为2021年5月21日(通过引用注册人于2021年5月24日提交的当前8-K表格报告的附件10.2并入)。 |
10.14* |
|
《2022年2月11日Clene Inc.、Clene Nanomedicine Inc.和Avenue Venture Opportunities Fund,L.P.之间的贷款和担保协议补充修正案》。 |
10.15 |
|
购买Clene Inc.股票的Avenue Venture Opportunities Fund,L.P.认股权证的表格(注册人于2021年5月24日提交的当前8-K表格中的附件10.3已并入)。 |
10.16## |
|
Clene Nanomedicine,Inc.和100 Chesapeake Blvd LLC之间的租赁协议,日期为2021年8月10日。(在登记人于2021年8月11日提交的当前8-K表格报告中通过引用附件10.1并入)。 |
10.17## |
|
Clene Nanomedicine,Inc.和High Chesapeake Flex One,LLC之间的租赁协议,日期为2021年8月10日。(在登记人于2021年8月11日提交的当前8-K表格报告中通过引用附件10.2并入)。 |
21.1* |
|
注册人的子公司。 |
23.1* |
|
普华永道会计师事务所同意。 |
23.2* |
|
德勤律师事务所同意。 |
31.1* |
|
根据修订后的1934年《证券交易法》颁布的规则13a-14(A)和规则15d-14(A)颁发的首席执行官证书。 |
31.2* |
|
根据经修订的1934年《证券交易法》颁布的规则13a-14(A)和规则15d-14(A)对首席财务官进行认证。 |
32.1** |
|
根据2002年《萨班斯-奥克斯利法案》第906条通过的《美国法典》第18编第1350条规定的首席执行官证书。 |
32.2** |
|
根据2002年《萨班斯-奥克斯利法案》第906节通过的《美国法典》第18编第1350条对首席财务官的证明。 |
101.1 |
|
内联XBRL实例文档。 |
101.2 |
|
内联XBRL分类扩展架构文档。 |
101.3 |
|
内联XBRL分类扩展计算链接库文档。 |
101.4 |
|
内联XBRL分类扩展定义Linkbase文档。 |
101.5 |
|
内联XBRL分类扩展标签Linkbase文档。 |
101.6 |
|
内联XBRL分类扩展演示文稿Linkbase文档。 |
104 |
|
封面交互数据文件(格式为内联XBRL,包含在附件101中)。 |
* |
现提交本局。 |
** |
随信提供。 |
# |
管理合同或补偿计划或协议。 |
## |
根据S-K条例第601(A)(5)项,本展品的附表和类似附件已被省略。我们同意根据要求向美国证券交易委员会补充提供此类遗漏材料的副本。 |
|
本展品的某些部分已根据S-K条例第601(B)(10)(Iv)项进行了编辑。我们同意根据要求向美国证券交易委员会补充提供未经编辑的副本。 |
项目16.表格10-K SU主干道
没有。
98
目录表
签名
根据1934年《证券交易法》第13或15(D)节的要求,注册人已正式授权下列签署人代表其签署本报告。
|
Clene Inc. |
|
|
|
|
日期:2022年3月11日 |
由以下人员提供: |
罗伯特·埃瑟林顿 |
|
|
罗伯特·埃瑟林顿 |
|
|
总裁兼首席执行官兼董事 |
根据1934年《证券交易法》的要求,本报告已由以下人员以登记人的身份在指定日期签署。
签名 |
|
标题 |
|
日期 |
|
|
|
|
|
罗伯特·埃瑟林顿 |
|
总裁兼首席执行官兼董事 |
|
March 11, 2022 |
罗伯特·埃瑟林顿 |
|
(首席行政主任) |
|
|
|
|
|
|
|
/s/Morgan R.Brown |
|
首席财务官 |
|
March 11, 2022 |
摩根·R·布朗 |
|
(首席财务会计官) |
|
|
|
|
|
|
|
/s/David J.Matlin |
|
董事会主席 |
|
March 11, 2022 |
大卫·J·马特林 |
|
|
|
|
|
|
|
|
|
/s/Jonathon T.Gay |
|
董事 |
|
March 11, 2022 |
乔纳森·T·盖伊 |
|
|
|
|
|
|
|
|
|
/s/沙洛姆·雅各博维茨 |
|
董事 |
|
March 11, 2022 |
沙洛姆·雅各博维茨 |
|
|
|
|
|
|
|
|
|
/瓦莱丽·V·麦克劳克林 |
|
董事 |
|
March 11, 2022 |
瓦莱丽·V·麦克劳克林 |
|
|
|
|
|
|
|
|
|
/s/艾莉森·H·莫斯卡 |
|
董事 |
|
March 11, 2022 |
艾莉森·H·莫斯卡 |
|
|
|
|
|
|
|
|
|
约翰·亨利·史蒂文斯 |
|
董事 |
|
March 11, 2022 |
约翰·亨利·史蒂文斯 |
|
|
|
|
|
|
|
|
|
/s/Chidozie Ugwumba |
|
董事 |
|
March 11, 2022 |
Chidozie Ugwumba |
|
|
|
|
|
|
|
|
|
里德·尼尔·威尔科克斯 |
|
董事 |
|
March 11, 2022 |
里德·尼尔·威尔科克斯 |
|
|
|
|
99