
根据2021年1月26日以保密方式提交给美国证券交易委员会(Securities And Exchange Commission)的文件
本注册声明草案尚未向美国证券交易委员会公开提交,本声明中的所有信息均严格 保密。
注册编号333-
美国
证券交易委员会
华盛顿特区,20549
表格S-1
注册声明
在……下面
1933年证券法
递归制药公司
(注册人的确切名称 如其章程所规定)
| 特拉华州 (注册成立或组织的州或其他司法管辖区) |
2836 (主要 标准行业 分类代码编号) |
46-4099738 (国际税务局雇主识别号码) |
格兰德河南街41号
盐湖城,UT 84101
(385) 269-0203
克里斯托弗·吉布森
首席执行官
递归 制药公司
格兰德河南街41号
盐湖城,UT 84101
(385) 269-0203
复制到:
| 帕特里克·J·舒尔特斯 菲利普·H·厄廷格 金珍娜(Jeana S.Kim) 威尔逊·桑西尼·古德里奇和罗萨蒂 专业公司 第五大道701号, 5100套房 华盛顿州西雅图,邮编:98104 (206) 883-2500 |
路易莎·丹尼尔斯 首席法务官 内森·哈特菲尔德 副总法律顾问 递归 制药公司 格兰德河南街41号 盐湖城,UT 84101 (385) 269-0203 |
艾伦·F·德南伯格 斯蒂芬·萨蒙 Davis Polk&Wardwell LLP 1600 El Camino Real 加利福尼亚州门洛帕克 94025 |
建议向公众销售的大概开始日期:在本注册声明生效日期之后,在切实可行的范围内尽快开始。
如果根据1933年《证券法》(Securities Act)第415条规定,本表格中登记的任何证券将以延迟或连续方式发售,请勾选以下复选框。☐
如果根据证券法第462(B)条的规定,提交此表格是为了为发行注册额外的 证券,请选中以下框,并列出同一发行的较早生效注册声明的证券法注册声明编号。☐
如果此表格是根据证券法下的规则462(C)提交的生效后修订, 请选中以下框,并列出同一产品的较早生效注册声明的证券法注册声明编号。☐
如果此表格是根据证券法下的规则462(D)提交的生效后修订,请选中下面的复选框,并列出同一产品的较早生效注册表的证券法注册表编号 。☐
用复选标记表示注册人是大型加速申报公司、加速申报公司、 非加速申报公司、较小的报告公司或新兴成长型公司。请参阅交易法规则12b-2中的大型加速文件服务器、加速文件服务器、较小报告公司的定义 公司和新兴成长型公司
| 大型加速滤波器 | ☐ | 加速文件管理器 | ☐ | |||
| 非加速文件服务器 | 规模较小的报告公司 | ☐ | ||||
| 新兴成长型公司 | ||||||
如果是新兴成长型公司,请用复选标记表示注册人是否已选择不使用延长的过渡期 来遵守根据证券法第7(A)(2)(B)节提供的任何新的或修订的财务会计准则。☐
注册费的计算
|
| ||||
| 普通股面值0.00001美元 |
$ | $ | ||
|
| ||||
|
| ||||
注册人特此修改本注册声明的生效日期,以将其生效日期延后至注册人 提交进一步修订,明确规定本注册声明此后将根据修订后的1933年证券法第8(A)条生效,或直至注册声明 在证监会根据上述第8(A)条决定的日期生效。
解释性注释
根据《修复美国地面运输法》的适用条款,我们将省略截至2018年12月31日及截至2018年12月31日的年度的综合财务报表,以及截至2019年9月30日及2020年9月30日的9个月的未经审计财务报表,因为它们涉及我们认为在计划发行时不需要包括在 招股说明书中的历史时期。我们打算在 向投资者分发初步招股说明书之前,修改注册说明书,将S-X法规要求的所有财务信息包括在修订之日。
这份初步招股说明书中的信息不完整,可能会被更改。在提交给美国证券交易委员会的注册声明生效之前,这些 证券不得出售。本初步招股说明书不是出售要约,也不寻求在任何不允许要约或出售的司法管辖区购买这些证券的要约 。
主题 完成,日期为2021年
初步 招股说明书
股票

普通股
这是Recursion PharmPharmticals,Inc.首次 公开发行普通股。我们正在发行我们的普通股。首次公开募股(IPO) 价格预计在每股$1到$1之间。
在这次发行之前,我们的普通股还没有公开市场。我们打算申请将我们的普通股在纳斯达克全球精选市场(Nasdaq Global Select Market)挂牌上市,交易代码为?RXRX。
根据联邦证券法的定义,我们是一家新兴的成长型公司,因此,我们选择遵守某些降低的报告要求。
| 每股 | 总计 | |||||||
| 首次公开发行(IPO)价格 |
$ | $ | ||||||
| 承保折扣和佣金(1) |
$ | $ | ||||||
| 递归制药公司扣除费用前的收益 |
$ | $ | ||||||
| (1) | 有关向承保人支付的赔偿的说明,请参阅承保。 |
我们已授予承销商为期30天的选择权,最多可额外购买 股普通股。
投资我们的 普通股风险很高。见第22页开始的风险因素。
美国证券交易委员会(Securities and Exchange Commission)或任何其他州证券委员会都没有批准或不批准这些证券,也没有就本招股说明书的准确性或充分性作出判断。任何相反的陈述都是刑事犯罪。
承销商预计将于2021年 左右通过存托信托公司的账簿记账设施将股票在纽约支付时交付给购买者。
| 高盛有限责任公司 | 摩根大通 |
| 美国银行证券 | SVB Leerink | Allen&Company LLC |
KeyBanc资本市场
招股说明书日期:2021年

我们是一家生物技术公司
扩展更像一家科技公司
|
56M+
人体实验 以我们自己的方式进行的细胞 实验室
|
几乎 7PB
接近7PB,其中一个 最大的专有生物和 化学数据集 | |
|
13B+
推断出的关系是 人类基因,化合物 更多地使用我们的生物地图
|
35
内部合计 已开发的程序 | |
|
4
临床分期方案
|
200+
回归者联合在一起 一项任务..。 |

破译生物学,从根本上改善生活
我们的一封信
联合创始人兼首席执行官
我们的联合创始人兼首席执行官的一封信
尊敬的投资者,
我们的任务是破译生物学,从根本上改善生活 。它是故意大胆的、扩张性的和有影响力的。我们正在利用千载难逢近 多个科学技术领域的指数级进步同时汇聚,这将使本世纪成为生物学的世纪。
这封信的目的是与您分享一些重要的想法和原则,这些想法和原则可能很难表达,但我认为这些想法和原则对实现我们的使命至关重要。当您考虑作为股东加入我们的使命时,您应该知道我们现在是一家什么样的公司,并打算在未来成为一家公司 。
生物学是复杂的
生物学极其复杂,高度网络化。作为一个物种,到目前为止,我们对这个问题的了解只有一小部分, 尽管数百万令人难以置信的科学家奉献了毕生精力来揭开这个问题的真相。此外,生物学的许多内容可能过于复杂,任何人都无法理解。揭开生物学的复杂性是一条更好的药物之路。
尽管面临挑战,但现代生物制药工业在过去30年中取得了巨大成就:抗病毒化合物将艾滋病毒/艾滋病从死刑转变为慢性病,并治愈了100多万丙型肝炎患者;越来越有针对性的化疗药物和新一代令人兴奋的免疫疗法帮助数百万癌症患者获得缓解,看到孩子的婚礼,或与家人多吃几顿感恩节大餐;抗体疗法,如针对肿瘤坏死因子(TNF)的抗体疗法,已帮助数百万癌症患者获得缓解,看到孩子的婚礼,或与家人多吃几顿感恩节大餐;抗体疗法,如针对肿瘤坏死因子(TNF)的抗体疗法,已帮助数百万癌症患者获得缓解,看到孩子的婚礼,或与家人多吃几顿感恩节大餐。a这些疫苗极大地改善了数以百万计的患者的生活质量;今天,世界见证了以创纪录的时间开发的新冠肺炎疫苗的推出。这些例子只是数百种令人难以置信的新药中的一小部分,这要归功于基础研究和应用研究,感谢热情献身于科学的研究人员,以及继续激励我们的患者。
尽管取得了这些进展,世界各地的科学家也做出了令人难以置信的工作,但一个令人不快的事实仍然存在:90%以上进入临床试验的药物在上市前就失败了。即使在今天,数以千计的疾病影响着数亿人,却没有有效的治疗方法。有意义地加快步伐,扩大规模,降低成本,为需要的患者提供有效的新药,这是人类面临的最大挑战之一,也是最大的机遇。
利用技术实现规模和复杂性是我们发现意想不到的东西的方式
生物系统可能很复杂,但也不是根本无法解决的。在过去五年中,我们见证了多个技术领域中使用的工具集的指数级进步,包括:i)通过CRISPR基因组编辑和合成生物学等工具加强对生物学的控制;ii)快速发展的机器人技术,使包括生物实验在内的复杂任务能够以前所未有的规模实现可靠自动化;iii)新的计算技术利用新的神经网络架构,能够对超大型、复杂和不完整的数据集进行迭代分析和推理;以及iv) 得益于云解决方案,高性能计算的弹性不断增强。这些基本领域的快速进步和改进同时汇聚在一起,为新药的发现和开发创造了一场革命的环境。
2
我们提高药物发现规模和效率的方法的核心原则是自动化 并整合湿实验室以创建大量的生物学实验数据集,而在干实验室中我们利用机器学习(ML)来解开数据集中的复杂模式。任何静态数据集都不可能对解决疾病生物学问题做出有意义的贡献;秘诀在于迭代方法,在这种方法中,对先前数据的学习通知新数据的生成,而该方法的秘诀是在内部生成我们自己的数据。我们的 数据集适合机器学习,每周增长约80TB,因此算法的改进速度比应用于静态数据集的速度要快得多。
此外,我们的方法使我们能够避免人类偏见,这往往是药物发现过程的主要威胁。作为人类,我们能够解释的数据的大小和规模是有限的,我们很容易看到适合我们的数据,并证明我们的假设是正确的。虽然今天我们的ML过程缺乏精明的毒品猎人的所有直觉,但算法并不关心假设。
我们的人和文化是我们的根基
在Recursion的早期,我最低估的不是生物学或筹款,而是招聘优秀人才并让他们 轻松解决众多不同技术领域的难题所面临的挑战。多亏了难以置信的导师、出色的联合创始人,以及一些出色的早期招聘,创造一个环境多样性、包容性、好奇心、学习、正直和大胆的理念很早就印在了我们身上。从早期开始,我们就在员工身上投入了大量资金,因为没有他们,再多的基础设施或代码也无法让我们完成使命。 经过七年多的时间,我们现在有了一个蓬勃发展的社区,数据科学家、软件工程师和自动化工程师与他们在生物、化学和临床开发领域的同事打成一片,我们一起致力于解决令人难以置信的难题 ,我们的使命让我们团结在一起。
我们可以从其他行业学到什么
在过去的二十年里,我们都目睹了技术在一个又一个行业中的扩散。由于一种新的方法,拥有悠久而杰出历史的老牌和根深蒂固的公司几乎被遗忘了。
通过将可靠的数据来源 与系统、流程和算法方法相结合,电子书商与传统零售业展开了较量,邮寄视频服务成为娱乐业最强大的力量之一 ,一家小型电动汽车制造商领先汽车业其他公司十年之久。在每一种情况下,该公司都垄断了一小块利基市场,然后利用数据和技术智慧实现了比大多数人认为的更快的增长 。此外,随着他们大规模整合新的数据集,网络效应站稳脚跟,他们方法的力量呈指数级加速。当他们的竞争对手意识到并对正在发生的事情做出反应时,他们处于明显的劣势 。
同样,我们从小规模开始,专注于悄悄地构建地球上最大、增长最快的生物图像数据集之一,以及在一系列罕见疾病的背景下探索它的系统、过程和算法。这一初步的方法导致了候选药物的渠道比年龄和规模相似的传统生物制药公司要广泛得多。
就在去年,我们已经开始利用我们学到的所有知识,开始大规模创建额外的 数据集,并开始专注于构建它们之间以及它们之间的集成和关系的系统、流程和算法。随着网络效应的深入人心,我们方法的威力将呈指数级增长。我们不会止步于 发现;我们将利用新技术和我们围绕数据集创造良性学习循环的精神,打造下一代、集成和垂直的生物制药公司。
3
许多人认为,过去20年在其他行业看到的颠覆性变化不会发生在生物制药领域 ;这个领域太复杂了,监管也太严格了。这是最后几个经历这些变化的行业之一,这当然不足为奇,但它也不能幸免。事实上,该行业以前也经历过这样的技术颠覆周期;在20世纪80年代,新的数据和技术让我们能够剖析分子途径,在20世纪90年代末和21世纪初,随着生物制品开始蓬勃发展,我们又经历了一次。这种循环以前就发生过,而且风险很高: 很少有其他行业的公司市值超过1000亿美元,更少的行业的产品在开发过程中90%的时间是失败的,没有一个行业具有同样的影响潜力。 循环将再次发生。
人类细胞生物学的递归图预测了数十亿种关系
我们已经建立了一张人类细胞生物学地图,它使我们能够预测生物学和化学的各种元素之间的关系和相互作用,并以一定的规模和速度进行预测。此外,我们一直专注于控制我们自己的垂直方向;我们的预测可以在我们自己的实验室里得到实验验证,通过我们自己的里的动物模型进行翻译,并由我们自己的团队通过临床进行开发。
在接下来的几十年里,我们将继续在物理世界和数字世界的交汇处建设,不仅在药物发现方面,而且在临床开发和制造方面,以及在治疗方式和适应症方面,创建数据生成、分析和迭代的良性 周期。这种方法产生了递归信条:
构建地图
遵循 地图
为病人服务
这八个字既是我们导航的指南针,也是作为投资者的您,是我们战略的精髓升华。
我们的开拓进取精神和失败者心态依然存在
从我们最早的时候起,我们的故事就不太可能发生。我们是一家由两名研究生和一名教授创办的公司,总部设在犹他州盐湖城。像许多早期的科技公司一样,我们最初的资金来源是信用卡上的现金预付款、储蓄以及信任我们的朋友和家人。我们从圣地亚哥一家废弃的实验室购买了二手设备,把它装进一辆搬家的面包车里,然后连夜开着车回到我们的衣橱实验室开始吧。
我们卑微而不太可能的开端是我们今天所建立的基础 。我们是失败者,也有这种感觉。现在我们是这个领域的领导者,但我们将保持饥饿和专注。我们每天都会以失败者的身份运作,让那些低估我们的人大吃一惊。
我们在数据和演示问题方面处于领先地位
今天, 我们的方法原则与2013年开始时基本保持不变。在短短七年多的时间里,我们建造或展示了:
| • | 地球上最大的专有生物数据集之一。 |
| • | 这是所有科技药物研发公司中最大、最广、最深的管道之一。 |
4
| • | 与拜耳建立变革性的合作伙伴关系,我们寻求在未来五年内发现10多种治疗纤维化的新疗法 。 |
| • | 一支由200多名推荐人组成的令人难以置信的团队,拥有世界级的才华、专业知识和领导力,以及令人难以置信的 关怀、学习、交付和诚实勇敢行事的文化一次递归。 |
我们是一家生物技术公司 规模更像一家技术公司,我们才刚刚起步。
一份加入我们的邀请和我们对你们的承诺
你可以投资许多公司,谢天谢地,许多伟大的技术专家正在将注意力转向对人类至关重要的推进任务。 未来是光明的。
在接下来的几页中,你会读到很多关于我们团队建立的公司的信息。我们纳入了广泛的 事实和数字,因为在Recursion,我们总是以数据和可证明的数据领先。您将了解到我们构建的地图是如何展示药物发现和开发产业化的有意义的领先指标的。我们希望 无论您是技术投资者、医疗保健投资者还是多面手投资者,您都能找到我们故事中的元素,让您对我们雄心勃勃的使命和过去七年来的进步感到兴奋。
但我们也希望您考虑我们正在努力建立的公司类型,以及我们将如何努力为数百万人带来有意义的影响;我们永远不会对我们建立的管道、我们建立的地图或取得的中等成功感到自满。我们会大打出手。
毫无疑问,道路上会有许多颠簸,也会有失败;生物和化学是硬的。在像发现和开发新药这样复杂和昂贵的过程中,在实现工业化的战争中,我们不可避免地会输掉战斗,但我们将永远牢记这一使命。如果您加入我们的行列,请期待同时经历我们的挫折和成功,并知道我们 从两者中都学到了东西,也许最重要的是从我们的失败中学到了东西。
最后,要知道,我们的雄心并不局限于药物的发现,因为我们已经向自己证明了我们制作人类细胞生物学地图的能力,因此,如果我们不绘制生物学的其他元素地图,那将是愚蠢的。归根结底,没有一地图,但很多,我们是一家能够建造它们并 巩固它们的公司,有朝一日我们的信条将远远超出生物制药:
建造地图集
跟着地图集走
为人类服务
我们对您的承诺是,我们敬业的团队将大胆而紧迫地工作,以实现我们的使命。我们希望通过这些页面中的文字 传递递归精神,当您投资于我们时,您正在投资于这个团队和我们的使命能够实现的影响,就像我们面前的金融机会一样。通过合作,我们可以破译生物学,从根本上改善生活。
谢谢,
克里斯·吉布森(Chris Gibson)博士。
5
目录
| 页面 | ||||
| 招股说明书摘要 |
1 | |||
| 风险因素 |
22 | |||
| 关于前瞻性陈述的特别说明 |
92 | |||
| 市场、行业和其他数据 |
95 | |||
| 收益的使用 |
96 | |||
| 股利政策 |
98 | |||
| 大写 |
99 | |||
| 稀释 |
101 | |||
| 选定的合并财务数据 |
104 | |||
| 管理层对财务状况和经营成果的讨论与分析 |
106 | |||
| 业务 |
125 | |||
| 管理 |
245 | |||
| 高管薪酬 |
256 | |||
| 某些关系和关联方交易 |
273 | |||
| 主要股东 |
277 | |||
| 股本说明 |
280 | |||
| 符合未来出售条件的股票 |
287 | |||
| 针对非美国普通股持有者的重要美国联邦所得税考虑因素 |
290 | |||
| 包销 |
295 | |||
| 法律事项 |
301 | |||
| 专家 |
301 | |||
| 在那里您可以找到更多信息 |
301 | |||
| 财务报表索引 |
F-1 | |||
到2021年 (本招股说明书发布之日后第25天)(含该日),所有交易这些证券的交易商,无论是否参与本次发售,都可能被要求递交招股说明书。这是交易商在担任承销商和未售出的配售或认购时, 交付招股说明书的义务之外的义务。
我们和 承销商均未授权任何人向您提供除本招股说明书或由我们或代表我们编写的任何免费书面招股说明书中包含的信息或陈述以外的任何信息或陈述,或我们已向您推荐的任何其他信息或陈述。我们和 承销商对他人可能向您提供的任何其他信息的可靠性不承担任何责任,也不能提供任何保证。我们和承销商不会在任何不允许 要约或出售的司法管辖区出售这些证券。您应假设本招股说明书中的信息仅在本招股说明书封面上的日期是准确的。自该日期以来,我们的业务、财务状况、运营结果和前景可能已发生变化 。
对于美国以外的投资者:我们没有,承销商也没有采取任何措施, 允许在除美国以外的任何司法管辖区(除美国外)为此目的而采取行动的任何司法管辖区内发行或拥有或分发本招股说明书。在美国以外拥有本招股说明书的人必须 告知自己,并遵守与发行普通股和在美国境外分发本招股说明书有关的任何限制。
i
招股说明书
摘要
招股说明书摘要
本摘要重点介绍了本招股说明书其他部分包含的精选信息,并以本招股说明书其他部分包含的更详细的信息和合并财务报表 完整地加以限定。此摘要并不包含您在投资我们的普通股之前应考虑的所有信息。在做出投资决定之前,您应仔细阅读整个招股说明书,包括 《风险因素》、《管理层对财务状况和运营结果的讨论和分析》一节下的信息,以及本招股说明书中其他地方包括的我们的合并财务报表和相关说明 。除非上下文另有要求,否则本招股说明书中提到的递归制药公司、递归公司、公司、我们、我们的 和我们的公司都是指递归制药公司。
概述
我们是一家临床阶段的生物技术公司,通过整合跨越生物、化学、自动化、数据 科学和工程的技术创新来解码生物学,从而从根本上改善患者的生活并实现药物研发的产业化。我们使命的核心是Recursion操作系统或Recursion OS,它结合了一个高级基础架构层,以生成我们 认为是世界上最大、增长最快的专有生物和化学数据集之一,以及Recursion Map,这是一套定制软件、算法和机器学习工具,我们使用它来探索不受人类偏见限制的基础生物学 ,导航到新的生物学见解,并快速加速程序。湿法实验室生物学与硅片我们闭环系统中的工具加快了我们的药物 发现过程,并使我们有别于行业内的其他公司。同样,我们由生命科学家以及计算和技术专家组成的平衡团队创造了一种环境,让经验数据、严谨的统计数据和创造性思维应用于每一项决策 。到目前为止,我们已经利用我们的Recursion OS创造了三个价值驱动力:i)35个内部开发的计划,专注于未得到满足的重大需求领域,其中几个项目的年销售额超过10亿美元;ii)与领先的生物制药公司建立战略合作伙伴关系;iii)诱导实验室,这是一个增长引擎,旨在探索Recursion OS在治疗学内外的新扩展 。自2019年以来,我们的渠道规模翻了一番,我们预计未来将继续加快项目增加的步伐。因此,我们是一家规模更像 技术公司的生物技术公司。
1

我们相信,我们的方法已经证明,我们的方法实现了药物发现的产业化,拓宽了潜在治疗起点的漏斗,在研究周期早期发现相对便宜的失败,并在降低成本的同时加快了高潜力候选药物的临床交付。2020年年中,我们开始从暴力搜索方法过渡,在这种方法中,我们体检我们图书馆中的每一种疾病模型和候选药物组合都使用我们的自动化湿实验室基础设施,以更高效、更强大的推理搜索方法。在这一新范式下,我们独立地描述数千种疾病模型和数十万候选药物,然后推断出数百亿种生物和化学关系。硅片,确定最有希望的候选对象进行进一步验证的优先顺序. 雄心勃勃的探索,使用我们目前的吞吐量和暴力搜索,可能需要大约1,000 年才能执行,现在可以推断几个月后。这一转变标志着我们在实现创始愿景方面取得了初步进展,该愿景融合了海量生物和化学 数据集和现代机器学习(ML)算法,以超越物理世界所能研究或探索的速度和规模推动新疗法的无偏见发现。
2
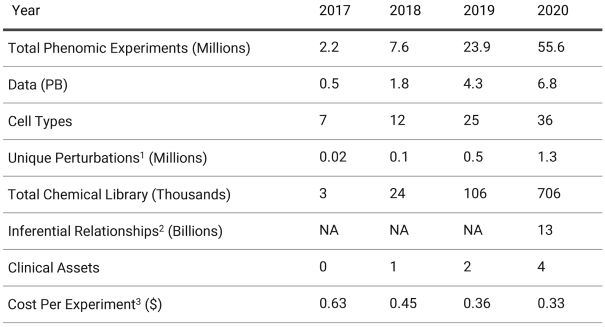
年份2017 2018 20192020总表型实验(百万)2.2 7.6 23.9 55.6数据(PB)0.5 1.8 4.3 6.8细胞类型7 12 25 36 独特扰动1(百万)0.02 0.1 0.5 1.3总化学库(千)3 24 106 706推断关系2(十亿)NA 13临床资产0 1 2 4每个实验的成本3($)0.63 0.45 0.36 0.33
| (1) | 独特的扰动是指物理探索的基因、可溶性因子、细胞和/或化合物组合的数量 。 |
| (2) | 推理关系指的是使用我们的 递归映射预测到的唯一扰动的数量。 |
| (3) | 每个实验的成本是指执行一个表观实验的平均调整后的直接成本(定义为 每次扰动一口井),包括消耗品成本、化合物成本和人工成本。 |
在其理想状态下,药物发现漏斗 的形状将类似于字母T.T,其中可能的治疗方法的广泛范围可以立即缩小到完美的候选药物,这将快速地通过该过程的后续步骤,而不会造成任何自然损耗。我们的目标 是利用技术将典型的药物发现漏斗重塑为理想状态,方法是扩大潜在治疗起点的漏斗,通过在研究周期早期识别失败(其成本相对较低)来快速缩小漏斗,并加快高潜力候选药物的开发。在当今的药物研发模式中,晚期临床失败是成本的主要驱动因素。降低代价高昂的后期失败率,并加快从HIT到临床候选的时间表,将创建更可持续的研发模式。
3

我们相信,我们在重塑传统药物发现漏斗方面取得了以下进展:
| 1. | 拓宽治疗起点的漏斗。我们灵活且可扩展的基础设施,以及我们使用 我们的基于推理的用于预测疾病模型和候选治疗方案之间数百亿关系的递归图,拓宽了发现漏斗的瓶颈,超出了假设和人的偏见的目标。 |
| 2. | 在研究周期的早期识别成本相对较低的故障,以快速缩小漏斗的范围 。递归地图结合了大量的生物和化学数据集以及计算工具,使我们能够:i)选择更具可译性的治疗起点;ii)预测选定的吸收、 分布、新陈代谢、排泄和毒理或ADMET,以及候选药物的潜在风险,从而快速确定下游成功可能性更高的计划的优先顺序。值得注意的是,这一策略不仅会增加早期的自然流失率,而且我们预计还会降低药物开发的总体成本。 |
| 3. | 加速将高潜力候选药物推向临床。递归地图 包含一套数字化学工具,可实现高效的化学空间探索,包括3D虚拟筛选以及提高稳定性和实用性的翻译工具体内学习。 |
我们利用不断发展的递归操作系统探索许多疾病计划,深度足以量化 与传统药物发现范式相比,计划在时间、成本和预期成功可能性方面的阶段性改进。这些指标是领先的指标,使用我们的方法,我们可以将药物发现产业化。我们相信未来的 次迭代
4
递归操作系统将带来更大的改进。最终,我们希望将总的美元加权失败降至最低,同时最大化临床成功的可能性。
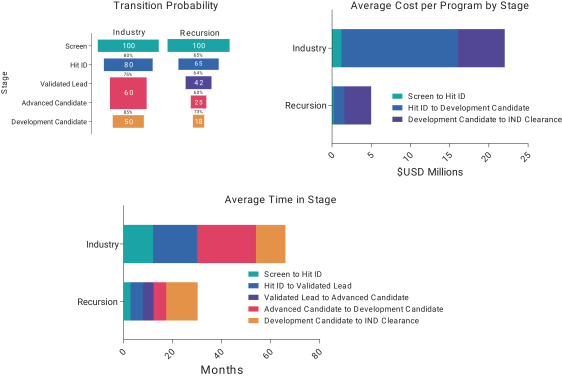
递归操作系统
Recursion OS是一个集成的多层系统,用于生成、分析生物和化学数据集并从中得出见解。它由 三个部分组成:
| • | 基础设施层:由高度可扩展的使能硬件和软件组成的同步网络,用于设计和执行各种生物实验,并随后存储我们不断增长的数据集。 |
| • | 递归数据宇宙:截至2020年12月31日,我们的递归数据宇宙 包含了大约7 PB的高度相关的生物和化学数据,涉及多种不同的数据模式。递归数据宇宙的大小 自2018年来增长了三倍多,并且持续加速增长 。就背景而言,我们的数据集需要的存储容量已经超过人类历史上所有高清长篇电影的总和。 |
| • | 递归贴图:一套内部软件 工具、算法和机器学习方法,旨在将递归数据世界中的数据处理和转换为我们的研发团队可操作的见解。 |
用于生成我们专有数据集的湿实验室生物学和硅片我们 闭环系统中的工具使我们在科技药物研发领域脱颖而出。该领域的许多公司:i)利用不同、嘈杂且往往无法复制的第三方数据集,这些数据集不太适合ML,或者ii)构建工具 n将工具作为服务提供给其他公司,这可能会随着时间的推移限制它们的优势和影响。更重要的是,我们重复的湿实验室验证和硅片预测会产生飞轮效应,其中
5
数据生成和学习加速并排进一步加强我们的药物发现平台。 新兴竞争对手和资源雄厚的大型现有企业可能会采取类似的策略,但作为先行者,我们有两个优势:i)任何资源都无法压缩观察自然发生的生物过程所需的时间,以及 ii)不断增长的递归数据宇宙会产生复杂的网络效应,这可能会使缩小竞争差距变得困难。
虽然递归数据宇宙由各种专有数据集组成,但核心数据集基于数十亿张人类 细胞的标记图像,这些图像是使用我们自己潮湿的实验室中生成的各种生物工具,在数百万次独特的扰动中生成的。我们在开发此数据集方面的专业知识是我们构建其他互补的、可扩展的 生物和化学数据集的基础。
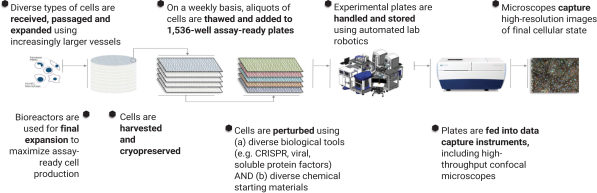
我们的人民和文化
我们在科技的交汇点和前沿开展业务。与传统生物技术公司不同,我们由200多名Recursionauts组成的快速增长的团队在生命科学家(约40%的员工)和计算和技术专家(约35%的员工)之间实现了平衡,创造了一个将经验数据、严谨的统计数据和 创造性思维应用于我们解决的问题的环境。当我们团结在一个共同的使命中时,破译生物学,从根本上改善生活,我们最大的优势在于我们的差异:专业知识、性别、种族、学科、 经验和视角。刻意建设和培育这种文化对于实现我们大胆的目标至关重要。
我们的价值驱动因素
到目前为止,我们已经使用Recursion OS构建了三个价值驱动因素:i)35个内部开发的计划,专注于 重大未得到满足的需求领域,其中几个项目的市场机会年销售额超过10亿美元;ii)与领先的生物制药公司建立战略合作伙伴关系;以及iii)诱导实验室,这是一个增长引擎,旨在 探索Recursion OS在治疗学内外的新扩展。
6
我们的管道
Recursion的每一个程序都是我们的Recursion OS的产品。虽然我们有35个计划正在筹备中,但我们重点介绍了十个值得注意的计划 ,考虑到它们各自的市场机会以及它们为每一代递归操作系统提供的验证,这些计划是关键的短期价值驱动因素。

| (1) | EU5被定义为法国、德国、意大利、西班牙和英国。除非另有说明,否则所有数字均为流行数字。 |
| (2) | 全球流行。 |
| (3) | 所有NF2驱动的脑膜瘤每年US-EU5发病率。 |
| (4) | 遗传性和散发性症状人群。 |
| (5) | 美国每年的发病率为730,000例--欧盟5国。最初的临床研究将集中在总人口中反复感染率较高的亚群 。 |
| (6) | 我们的计划有可能解决神经炎症中的一些适应症,包括在美国总计至少600万名患者的多种神经退行性疾病。我们打算在未来选择这些适应症的一个子集。 |
| (7) | 每年的US-EU5发病率。 |
| (8) | 我们的计划有可能解决一些由以下因素驱动的适应症MyC做些改动。目前,我们 尚未最终确定特定指示的目标产品配置文件。 |
暴力搜索程序
我们的八个值得注意的项目是使用我们的暴力搜索方法确定的。这些计划中有四个是现有已知化学 实体(KCE)的新用途,我们已将其推进到临床开发,并获得了密钥启用许可证。这些项目中的另外四个是新的化学实体,或称NCE,已经被发现并在内部进行了改进。
| • | REC-4881用于治疗FAP。REC-4881是一种口服生物利用剂,非ATP-竞争性MEK1和MEK2的变构小分子抑制剂正在开发,用于缩小家族性腺瘤性息肉病(FAP)患者和躯体疾病患者的肿瘤体积装甲运兵车-突变肿瘤。REC-4881似乎耐受性良好,与预期用途一致,并且在人类中具有肠道定位的PK谱,这对FAP和潜在的其他胃肠道肿瘤非常有利。我们希望将第一位患者纳入第二阶段, 双盲、随机、安慰剂对照试验。 |
| • | REC-3599用于治疗GM2神经节苷脂沉积症。REC-3599是一种口服生物利用、选择性、有效的蛋白激酶C(PKC)和糖原合成酶激酶3β(GSK3?)抑制剂,正在开发用于治疗GM2神经节苷脂沉积症。该分子对致病生物标记物gm2和脂褐素水平有很强的挽救作用。 |
7
| 来自具有多种不同突变的患者的细胞六角形或HEXB,分别称为泰-萨克斯病或桑德霍夫病。应FDA的要求,我们目前正在应FDA的要求,在GM2的HEXB突变动物模型中产生额外的药效学数据,预计将在2018年招募第一名患者参加开放标签的第二阶段试验。 |
| • | REC-2282用于治疗NF2。REC-2282是一种CNS穿透性口服生物利用型小分子组蛋白去乙酰化酶或HDAC抑制剂,正在开发用于治疗NF2这种分子似乎耐受性良好,包括多年服药的患者,并有可能降低心脏毒性,使其有别于其他HDAC抑制剂 。与已批准的HDAC抑制剂相比,REC-2282既是中枢神经系统渗透性的,又是口服生物利用度的。我们希望招募第一名患者参加 第二阶段的双盲、随机、安慰剂对照研究。 |
| • | REC-994用于CCM的治疗。REC-994是一种口服生物可用超氧化物清除剂小分子,正在开发用于治疗脑海绵状畸形(CCM)。在我们在健康志愿者中进行的第一阶段单次递增剂量(SAD)和多次递增剂量(MAD)试验中,REC-994证明了对慢性剂量的耐受性和适宜性。CCM是最大的罕见疾病机会之一,在美国和EU5约有36万名有症状的患者,没有批准的治疗方法。我们希望在 中招募第一名患者参加2期、双盲、安慰剂对照、安全性、耐受性和探索性疗效研究。 |
| • | 治疗艰难梭菌结肠炎的先导分子。我们已经鉴定出三种具有潜在口服活性、肠道偏向的 铅NCE(rEC-163964、rEC-164014和rEC-164067)。艰难梭菌毒素抑制剂,我们已经证明它是葡萄糖转移酶的抑制剂。这些分子具有预防疾病复发的潜力,可用于高危患者的二级预防治疗。艰难梭菌感染是抗生素相关性腹泻的主要原因,也是发病率和死亡率的主要原因。我们目前正在完成探索性的非临床安全性研究,以便能够潜在地选择开发候选药物。 |
| • | 治疗神经炎的铅分子。我们已经确定了三种潜在的铅 NCE(REC-648455、REC-648597和REC-648677)第一位患者,口服生物利用、安全、中枢神经系统渗透的小分子小胶质细胞激活调节剂。小胶质细胞活化和神经炎症是阿尔茨海默病和帕金森氏病等神经退行性疾病以及多发性硬化症等中枢神经系统炎症性疾病的特征。小胶质细胞激活的小分子调节剂有可能减少中枢神经系统退行性疾病和炎症性疾病中与促炎过程相关的神经元死亡。该项目处于领先优化阶段。 |
| • | 治疗巴顿病的铅分子。我们已经确定了三种主要的NCE (REC-648190、REC-259618和REC-648647),它们具有口服生物利用度、CNS穿透性、多种亚型巴顿病的疾病改善疗法的潜力。巴顿病是一种常染色体隐性遗传的神经退行性疾病,由14个基因中的一个突变引起。CLN 个基因。虽然罕见,但这些疾病共同代表了最常见的儿童神经退行性疾病,并显示出重大的未得到满足的需求。该项目目前处于领先优化阶段。 |
| • | 治疗CMT2A的铅分子。我们已经确定了四个铅分子(rec-64810、rec-648458、rec-1262和rec-150357)第一位患者,口服生物利用型疾病修饰分子,可减缓或逆转2A型线粒体疾病或CMT2A型线粒体疾病的进展。CMT2A 是一种罕见的常染色体显性遗传性周围神经退行性疾病,由CMT2A基因突变引起Mfn2导致小腿和手部进行性肌肉萎缩的基因。有 |
8
| 未批准用于CMT2A的疾病修饰疗法。该项目目前处于领先优化阶段。 |
推理搜索程序
我们的两个值得注意的项目是 从2020年中开始使用我们的新推理搜索方法确定的。其中一个计划是对现有KCE的新使用,而另一个计划是内部发现和高级的NCE 。
| • | 用于治疗免疫检查点抵抗的REC-64151 在……里面 STK11-突变型NSCLC.我们已经确定了临床阶段口服生物利用小分子的一种新的潜在用途,以恢复和提高肿瘤中含有肿瘤抑制基因突变的肿瘤对免疫检查点抑制剂的敏感性。STK11。大约有3万例STK11-突变型转移性非小细胞肺癌(NSCLC),在美国和EU5一年内,这些突变已被证明预示着不良预后和对免疫检查点抑制剂(ICI),特别是抗PD-(L)1疗法的耐药性。目前还没有被批准的治疗方法被开发出来特异性地调节肿瘤的反应 STK11-突变癌症。该计划目前正处于剂量优化阶段。 |
| • | MYC抑制分子治疗实体和血液性恶性肿瘤 . 我们已经使用我们的推理搜索方法确定了多个热门系列,这些系列随后在抑制MYC下游的转录活性方面显示出浓度依赖的活性 。MYC转录靶基因的表达增加在肿瘤学中普遍存在,高达50%的癌症存在MYC的改变。具有抑制MYC依赖活性的新型小分子可以改善对多种肿瘤的治疗,特别是那些含有直接涉及MYC激活的基因突变的肿瘤。目前还没有批准的分子专门针对myc 。此程序当前在点击率领先相位。 |
9
除了上面突出显示的值得注意的计划外,我们还在积极探索另外25个 计划,这些计划可能被证明是我们未来增长的驱动力。使用我们的推理搜索方法,自2020年7月以来,我们已经发现并验证了其中16个程序。展望未来,我们预计我们渠道中的绝大多数新成员 将使用我们的推论搜索方法发现。

我们的合作伙伴关系
我们并不是唯一肩负着将药物发现产业化和改善患者生活的人。使用我们的Recursion OS,我们将继续与拥有资源和经验的领先生物制药公司合作,帮助我们广泛探索不同的疾病领域(例如,纤维化、神经科学、肿瘤学、免疫学和炎症),并快速识别 一流的或同类中最好的治疗候选人。
2020年8月,我们宣布与拜耳在纤维化领域建立多年战略合作伙伴关系。根据合作关系,双方同意在五年内启动10多个发现项目,以确定针对包括肺、肝和心脏在内的多个器官系统的破坏性和复杂性纤维性疾病的新疗法。拜耳从其专有库中贡献了大约500,000种 化合物,并将在整个合作伙伴关系中提供深厚的科学专业知识。
虽然到目前为止,我们的合作伙伴关系主要集中在小分子研究上,但未来的合作伙伴关系可能会扩展到大分子和新的治疗方式,包括基因疗法和细胞疗法。
10
我们的价值创造战略
我们是一家生物技术公司,规模更像一家科技公司。我们业务战略的中短期要素与我们的三个关键 价值驱动因素保持一致。我们打算:
| • | 开发当前的资产管道,同时实现超线性管道增长。 |
| • | 执行战略合作伙伴关系,最大限度地发挥我们平台的潜在价值. |
| • | 通过归纳实验室探索递归地图带来的新扩展和商机. |
如果我们成功地追求药物发现的产业化,我们可能有机会通过以下方式在生物制药行业中开创价值分配的先河 :i)在发现和开发过程中更早地与项目合作,(Ii)解决那些原本被认为对传统药物开发来说太小或无利可图的疾病领域, 太小或无利可图,以及iii)在创新上竞争和 快速推向市场在主要治疗领域,确保 领导地位。我们相信,这些努力的成功可能会对患者的生活和整个生物制药行业产生持久的、积极的和变革性的影响。
与我们的业务相关的风险
我们的业务 存在许多风险和不确定性,您在投资我们公司之前应该考虑这些风险和不确定性。这些风险在本招股说明书中题为风险因素的一节中有更详细的描述。这些风险包括但不限于以下 :
| • | 我们是一家临床阶段的生物技术公司,运营历史有限。 |
| • | 自成立以来,我们已遭受重大运营亏损,并预计在可预见的未来,我们将继续亏损 。 |
| • | 即使我们完成了这项服务,我们的使命也是广泛而昂贵的,我们将需要筹集大量的 额外资金。 |
| • | 我们没有获准商业销售的产品,也没有从产品销售中获得任何收入。 |
| • | 我们或我们当前和未来的合作伙伴可能永远不会成功开发药品并将其商业化,这将 对我们的运营结果和我们继续业务运营的能力产生负面影响。 |
| • | 由于多种因素,我们的季度和年度运营业绩在未来可能会大幅波动,其中许多 都不在我们的控制范围之内,可能很难预测。 |
| • | 我们的药物发现方法是独一无二的,可能不会带来成功的药物产品。 |
| • | 我们的候选药物处于临床前或临床开发阶段,这是一个漫长而昂贵的过程,结果不确定,而且有可能出现实质性的延误。 |
| • | 虽然我们打算探索其他治疗机会,但除了我们目前正在开发的候选药物外,由于多种原因,我们可能无法确定可用于临床开发的可行新药候选药物。如果我们不能发现更多可行的潜在候选药物,我们的业务可能会受到实质性的损害。 |
| • | 如果计算机系统故障、网络攻击或我们的 网络安全或第三方、供应商或服务提供商的网络安全存在缺陷,我们的业务和运营将受到影响。 |
11
| • | 如果我们不能为我们的平台开发新的解决方案和增强功能,以跟上技术 的发展步伐,我们的业务和运营结果将受到损害。 |
| • | 我们平台中的缺陷或中断可能会降低我们的价值和前景。 |
| • | 传染病的流行、流行或爆发,如新冠肺炎或 其他不可抗力事件,可能会对我们的业务和财务业绩产生重大不利影响,并可能中断我们候选药物的开发。 |
| • | 如果我们不能充分管理和改进我们的技术硬件基础设施,我们可能会遇到错误、延迟和 其他性能问题。 |
| • | 我们的内部设施以及外部服务提供商和供应商的物理和数字基础设施均面临与监管和运营风险相关的风险。 |
| • | 我们可能寻求在候选药物的临床开发或商业化方面建立更多合作, 如果我们不能以商业合理的条款建立这些合作关系,或者根本无法建立合作关系,我们可能不得不改变我们的开发和商业化计划。 |
| • | 如果我们无法充分保护和执行我们的知识产权和专有技术,或无法获得并 保持对我们的技术和产品的专利保护,或者如果获得的专利保护范围不够广泛,我们的竞争对手可能会开发和商业化与我们类似或相同的技术和产品,我们成功将我们的技术和产品商业化的能力可能会受到损害。 |
| • | 如果我们不能保护我们的商业秘密和专有技术的机密性, 我们的业务和竞争地位可能会受到损害。 |
| • | 如果我们未能履行我们与第三方合作或从第三方获得知识产权许可的协议中的义务,或者我们与我们的合作者或许可人的业务关系受到中断,我们可能会失去对我们的业务非常重要的权利。 |
企业信息
我们于2013年11月在特拉华州成立,名为Recursion PharmPharmticals,LLC,是一家 有限责任公司。2016年9月,我们改名为特拉华州的一家公司,随后更名为递归制药公司。我们的主要执行办公室 位于德克萨斯州盐湖城格兰德街41号,邮编84101。我们的电话号码是(385)269-0203。我们的网站地址是www.recursion.com。网站上包含的信息未通过 参考并入本招股说明书,因此不应视为本招股说明书的一部分。
我们将Recursion徽标和其他标志用作 美国和其他国家/地区的商标。本招股说明书包含对我们的商标和服务标志以及属于其他实体的商标和服务标志的引用。仅为方便起见,本招股说明书中提及的商标和商号(包括徽标、 插图和其他视觉展示)可能不带TM符号出现,但此类引用并不意味着我们不会在适用法律下最大程度地主张我们的权利或适用许可人对这些商标和商号的权利。我们不打算使用或展示其他实体的商号、商标或服务标志,以暗示我们与任何其他实体存在关系,或由任何其他实体背书或赞助。
12
成为一家新兴成长型公司的意义
我们是一家新兴的成长型公司,正如修订后的2012年Jumpstart Our Business Startups Act或JOBS Act所定义的那样。我们将保持 新兴成长型公司,直到出现以下最早的情况:i)本财年的最后一天,我们的年收入超过10.7亿美元;ii)我们有资格成为大型加速申报公司的日期,非关联公司持有至少7亿美元的股权证券;iii)我们在前三年期间发行了超过10亿美元的不可转换债务证券 ;以及iv)本财年的最后一天。 我们将一直是一个新兴的成长型公司。 我们的年收入超过10.7亿美元的财年的最后一天;ii)我们有资格成为大型加速申报机构的日期,非关联公司持有至少7亿美元的股权证券;iii)我们在前三年期间发行了超过10亿美元的不可转换债务证券 。
新兴成长型公司可能会利用免除某些报告要求和其他一般适用于 上市公司的负担的优势。这些规定包括:
| • | 仅提供两年的审计财务报表和两年的精选财务数据; |
| • | 豁免遵守2002年《萨班斯-奥克斯利法案》(Sarbanes-Oxley Act)第404条或《萨班斯-奥克斯利法案》(Sarbanes-Oxley Act)的审计师认证要求; |
| • | 减少定期报告、委托书和注册声明中有关高管薪酬安排的披露;以及 |
| • | 免除对高管薪酬或黄金降落伞安排进行不具约束力的咨询投票的要求。 |
由于这一状况,我们利用了本招股说明书中降低的报告要求 ,并可能选择在未来提交给美国证券交易委员会的文件中利用其他降低的报告要求。特别是,在这份招股说明书中,我们只提供了两年的 经审计的财务报表,没有包括如果我们不是一家新兴成长型公司所需的所有高管薪酬相关信息。
此外,《就业法案》规定,新兴成长型公司可以利用较长的过渡期遵守新的或修订的 会计准则,推迟这些会计准则的采用,直到它们适用于私营公司。我们已选择利用这一豁免来遵守新的或修订的会计准则,因此,我们将不会 与其他非新兴成长型公司或那些选择不使用延长过渡期的上市公司同时遵守相同的新的或修订的会计准则,这可能会使我们的 财务报表更难与此类其他上市公司进行比较。我们可以利用这些报告豁免,直到我们不再有资格成为新兴成长型公司,或者在采用某些新的或修订的会计准则方面,直到我们不可撤销地选择不使用延长的过渡期。因此,我们的财务报表可能无法与截至上市公司生效日期 遵守新的或修订的会计准则的公司进行比较。
13
供品
| 我们提供的普通股 |
股份。 |
| 购买额外股份的选择权 |
我们已授予承销商为期30天的选择权,最多可购买我们普通股的额外股份。 |
| 普通股将在本次发行后紧随其后发行 |
股票(如果承销商行使其 全额购买额外股票的选择权,则为股票)。 |
| 收益的使用 |
我们估计,本次发行的净收益约为100万美元,如果 承销商全面行使其购买额外普通股的选择权,假设首次公开募股(IPO)价格为每股$,这是本招股说明书首页价格区间的中点,并扣除估计的承销折扣和佣金以及我们应支付的估计发售费用,则本次发行的净收益约为100万美元。 |
| 我们目前打算使用此次发行的净收益,以及我们现有的现金和现金等价物,如下所示:用于资助研发活动,包括但不限于我们平台的运营、药物发现和研究计划,以及我们正在进行的计划的持续开发,包括设计和进行临床前研究和临床试验,以及为支持我们的流水线的基础设施提供资金; 用于偿还债务;剩余金额用于营运资金、其他一般公司用途和战略投资,包括通过上岗实验室。但是,我们目前没有任何投资协议或承诺 。有关详细信息,请参阅标题为“收益的使用”的部分。 |
| 风险因素 |
有关在决定投资我们普通股之前应仔细考虑的因素的讨论,请参阅标题为?风险因素?的一节。 |
| 建议的纳斯达克交易代码 |
?RXRX? |
14
本次发行后我们普通股的流通股数量以截至2020年12月31日的流通股为基础 ,不包括:
| • | 截至2020年12月31日,在行使已发行期权时可发行的普通股 ,加权平均行权价为每股$; |
| • | 可在行使2020年12月31日之后授予的期权时发行的普通股 ,加权平均行权价为每股$; |
| • | 自2020年12月31日起行使认股权证可发行的普通股 ; |
| • | 截至2020年12月31日,根据我们修订的2016股权激励计划为未来发行预留的普通股 ,哪些股票将被添加到我们的2021年股权激励计划或2021计划为未来发行预留的股票中; |
| • | 根据我们的2021计划为未来发行预留的普通股 ,该计划将在本次发行中生效,以及根据本计划为未来发行预留的普通股数量的任何自动增加;以及 |
| • | 根据我们的2021年员工购股计划(或2021年ESPP)为未来发行预留的普通股 股票,该计划将与本次发行相关生效,以及根据本计划为未来 发行预留的普通股数量的任何自动增加。 |
除非另有说明,本招股说明书假定或实施以下事项:
| • | 未行使未到期期权; |
| • | 承销商在本次发行中未行使向我们购买额外普通股的选择权; |
| • | 将我们截至2020年12月31日的所有可转换优先股的流通股自动转换为紧接本次发售完成之前我们普通股的总和;以及 |
| • | 我们修订和重述的公司证书的备案和有效性,以及我们修订和重述的章程的通过,每一项都将在紧接本次发售完成之前发生。 |
15
汇总合并财务数据
下表列出了我们所指时期的汇总综合财务数据。我们从本招股说明书其他部分包括的经审计的合并财务报表中获取了截至2019年12月31日和2020年12月31日的 运营数据的合并报表,以及截至2020年12月31日的合并资产负债表数据。我们的历史 结果不一定代表未来任何时期的预期结果。您应阅读以下汇总合并财务数据,以及选定的 合并财务数据、管理层对财务状况和运营结果的讨论和分析、合并财务报表和我们的合并财务报表以及本招股说明书其他部分包含的相关注释中包含的更详细的信息。
| 截至十二月三十一日止的年度, | ||||||||
| 2019 | 2020 | |||||||
| (以千为单位,共享和按次共享数据除外) | ||||||||
| 综合运营报表数据: |
||||||||
| 收入: |
||||||||
| 赠款收入 |
$ | 608 | $ | |||||
| 营业收入 |
1,711 | |||||||
|
|
|
|
|
|||||
| 总收入 |
2,319 | |||||||
| 运营费用: |
||||||||
| 研发费用 |
45,809 | |||||||
| 一般事务和行政事务 |
18,951 | |||||||
|
|
|
|
|
|||||
| 总运营费用 |
64,760 | |||||||
|
|
|
|
|
|||||
| 运营亏损 |
(62,441 | ) | ||||||
| 其他收入,净额 |
562 | |||||||
|
|
|
|
|
|||||
| 净亏损和综合亏损 |
$ | (61,879 | ) | $ | ||||
|
|
|
|
|
|||||
| 每股基本和稀释后净亏损(1) |
$ | (4.30 | ) | $ | ||||
|
|
|
|
|
|||||
| 基本普通股和稀释普通股的加权平均份额 |
14,380,177 | |||||||
|
|
|
|
|
|||||
| 预计每股基本和摊薄净亏损 (未经审计)(2) |
$ | (0.96 | ) | $ | ||||
|
|
|
|
|
|||||
| 预计加权平均-用于计算预计每股净亏损、基本亏损和 摊薄(未经审计)的流通股 |
64,746,144 | |||||||
|
|
|
|
|
|||||
| (1) | 有关基本和稀释后每股净亏损的计算详情,请参阅本招股说明书末尾的综合财务报表附注11。 |
| (2) | 计算未经审核备考基本及摊薄每股净亏损,以使所有 可转换优先股已发行股份自动转换为与合资格首次公开发行有关的普通股,采用转换后的方法,犹如转换已于所述期间期初或 发行日期(如较后)发生。 |
16
| 截至2020年12月31日 | ||||||||||||
| 实际 | 形式上的(1) | 形式上作为 调整后的(2)(3) |
||||||||||
| (未经审计) (单位:千) |
||||||||||||
| 合并资产负债表数据: |
||||||||||||
| 现金和现金等价物 |
$ | $ | $ | |||||||||
| 营运资金(4) |
||||||||||||
| 总资产 |
||||||||||||
| 总负债 |
||||||||||||
| 可转换优先股 |
||||||||||||
| 股东赤字总额 |
||||||||||||
| (1) | 预计资产负债表数据使我们的可转换 优先股的所有流通股自动转换为我们普通股的总和,这将在本次发售完成之前发生,从而产生我们的普通股的总流通股 。 |
| (2) | 上述资产负债表数据表中的备考调整栏适用于i)上文脚注(1)所述的备考调整 和ii)本次发行中普通股的发行和出售,其首次公开发行价格为每股 $,这是本招股说明书封面所列价格区间的中点,扣除承销折扣和 佣金以及本公司应支付的预计发售费用后。 |
| (3) | 假设本招股说明书封面所列价格区间的中点,即每股首次公开募股价格( $)每增加或减少1.00美元,我们的现金和现金等价物、营运资金、总资产和股东赤字的调整金额为预计(Br)形式将增加或减少(视情况而定)100万美元,假设 本招股说明书封面所列我们提供的股票数量:在扣除估计的承保折扣和佣金以及估计应支付的发售费用后,本公司的预期承销折扣和佣金保持不变。同样,我们以假设的首次公开募股价格发行的股票数量每增加或减少100万股,我们的现金和现金等价物、营运资金、总资产和 股东赤字将增加或减少(视情况而定)100万美元。上述调整后的备考信息仅供参考,并将取决于实际的首次公开发行价格和定价时确定的本次发行的其他条款。 |
| (4) | 营运资本的定义是流动资产减去流动负债。有关我们流动资产和流动负债的详细信息,请参阅 本招股说明书中其他地方的财务报表。 |
17
词汇表
本招股说明书中使用的关键术语摘要
生物工具。科学家可以用来扰乱生物状态的方法和物理试剂,尤其是用来模拟疾病。递归数据领域中的例子包括:CRISPR介导的基因编辑、可溶性因子(例如蛋白质、代谢物和毒素)、活病毒等。
蛮力搜索。通过直接实验发现潜在的治疗剂以评估大量试剂/干扰组合的过程(例如,针对10种细胞疾病模型高通量筛选100万个小分子,需要10,000,000个实验)。请参阅推理搜索的定义以进行对比。
化学实体,已知的和新的(KCE,NCE)。评估已在人类临床前和/或临床试验中研究过(已知化学实体)或以前未在人类临床试验中研究过(新化学实体)的候选治疗剂的药物发现计划的类别 。已知的化学实体计划评估候选的 治疗剂,用于与其原始研究不同的应用,并可能提供更快的治疗途径。新的化学实体通常代表着知识产权保护的更大机遇,例如合成 物质专利。
化学工具。该套化学治疗剂,包括现有的已知化学实体 和化学起点用于暴力或推理搜索的新化学实体程序;存储、合成和分析这些小分子及其衍生物的基础设施;以及使这些小分子向临床候选方向发展的技术诀窍和软件,包括数字化学和预测ADMET。
数字化学。使用计算方法来解决药物发现中的化学问题。它包括使用 方法,如大规模结构搜索、蛋白质目标模拟、小分子属性计算和基于机器学习的预测来做出决策。
药物发现漏斗。将大量潜在的治疗药物按顺序过滤至少数候选药物的过程,这些候选药物对临床有益的可能性越来越大,并且对患者具有可接受的安全性和耐受性。它包括治疗进展的各个顺序阶段,包括早期和晚期发现、临床前研究和临床开发。
无论是早发现还是晚发现。在推断(早期发现)或随后的正交实验验证(后期发现)的情况下,一旦潜在的治疗剂显示出早期实验成功或预测,药物 发现漏斗中的各个阶段就会启动。
功能读出。指的是一种实验读数,在这种情况下是一个复杂的生理终点(例如,细胞活力、神经元突起、线粒体呼吸等)。我们利用我们的组学和定制分析中测量的功能读数来验证潜在的治疗剂。
高维的。如果同时进行多个独立的数值测量,提供生物系统潜在活动和状态的大体上整体视图,则数据集或数据源被认为是高维的。高维与低维形成对比,在低维中进行少量的数值 测量,提供对生物或化学活动和状态的高度受限的视图。
18
高通量筛选。在数以百万计的化学和生物扰动范围内进行药物发现实验的方法 。它是通过部署机器人、自动监控系统、液体处理设备和综合分析管道等工具来实现的。
高度相关。如果数据在独立实验、延长的持续时间(数月和数年)和不同的生物或化学工具(如CRISPR到可溶性因子到小分子)之间具有可重复性和可比性(通过应用 专有控制和参考策略),则数据集高度相关。
工业化。在药物发现方面,指的是通过标准化生物和化学实验系统和技术分析来实现超线性增长,以创建具有更高的临床成功可能性、更低的成本和更快的时间表的管道。
推论搜索。通过基于先前实验对未来结果(例如治疗和疾病扰动之间的关系)启用ML的预测来发现潜在的治疗扰动的过程。要进行的实验数量与治疗和疾病微扰库的大小之和成正比(例如,一百万个小分子对十个细胞疾病模型的大小为1,000,010)。请参阅暴力搜索的定义以了解对比度。
实验室,湿的和干的。为进行科学实验而建立的研究环境。在潮湿的实验室中,使用化学工具、生物工具和其他实验试剂进行物理测试。在干燥的实验室里,我们可以做出推论。在硅胶中,通过计算程序、模型或模拟(例如,预测性ADMET)。
大分子。指的是由大量小构件组成的天然聚合物(例如,RNA、蛋白质和抗体疗法以及某些天然产品)。
行动机制。治疗剂(如小分子)通过 发挥其有益作用的特定生物相互作用。目标假设试图在发现之初选择一种机制,而无偏见的方法可能能够发现新的、意想不到的机制。
元数据。有关实验技术执行的数据,而不是实验本身的结果, 例如物理条件和试剂批次。跟踪元数据对于生成高度相关的数据和正确解释高通量筛查至关重要。
经济学。各种数据捕获和分析方法,从而可以分析具有普遍或非常广泛的 覆盖范围(例如,整个基因组)的生物信号。组学包括:表观组学(细胞形态学)、转录组学(RNA水平)、蛋白质组学(蛋白质表达模式)和InVivology(复杂动物行为的数字化)。鉴于表现学在 递归中的核心作用,正交经济学是指正交的或独立于表现学的组学数据。
微扰。应用生物或化学工具改变生物系统的状态,如培养中的细胞 类型,例如模拟和产生生物状态。
拍字节。数据量:1015字节、1,000 TB或1,000,000 GB。相当于大约5000亿页标准打字文本或1.25亿张显微镜图像。
临床前。临床开发前药物发现漏斗中的一个阶段。对于KCE计划,具有 人PK/PD和安全配置文件的计划支持In-License,我们正在为其申请许可证。对于NCE计划,执行毒理学和疗效研究以追求所需 适应症的IND的计划。
19
预测性广告。ADMET,或吸收、分布、代谢、排泄和毒性,是一套旨在了解药物责任的评估的缩写,特别是关注对整个系统、器官和生物体的影响。预测性ADMET是一种计算干燥实验室方法,用于检测 并避免与此类负债相关的风险。
递归数据宇宙。我们收集了高度相关的、 专有的高维生物和化学数据集,递归地图在这些数据集上运行。
递归 基础结构。我们由高度可扩展的使能硬件和使能软件组成的同步网络来设计、执行、聚合和存储我们的海量生物和化学数据集。
递归映射。我们的软件工具和算法使用我们的数据获得洞察力比在实验室测试一切更有效 以便为我们的研发团队提供可操作的洞察力。
递归操作系统,或递归 操作系统。我们集成的、多方面的系统,用于生成、分析和从海量生物和化学数据集中获得洞察力。它由基础设施层、递归数据世界和递归地图组成,它们共同支持我们的药物发现产业化。
小分子。与 大分子不同的是,治疗剂不包含重复构建块的聚合物:分子质量通常在900道尔顿以下。大多数批准的药物都属于这一类。
超线性增长。以随时间增长的速度增长(例如,每年翻一番,指数增长)。在 药物发现中,它是一个产业化的目标。这与线性增长形成对比,线性增长具有恒定的增长率(例如,计划总数每年增加2倍)。
不偏不倚。数据和分析的集合,减少对与给定疾病适应症或生物学问题相关的生物学的预期先验理解的数量,例如追求新的治疗方法。不偏不倚与有偏见形成鲜明对比,在这两种情况下,人类的解释和预期推动了收集的数据和执行的分析。
验证。一种过程,通过该过程,确认发现在与感兴趣的特定疾病适应症高度相关的次要和附加的、 独立的实验方法中具有有效的潜力(参见组学,特别是正交学)。
20
风险因素
危险因素
投资我们的普通股有很高的风险。在决定是否投资于 我们的普通股之前,您应仔细考虑以下描述的风险以及本招股说明书中的其他 信息,包括我们的合并财务报表和相关说明,以及管理层对财务状况和运营结果的讨论和分析。下列任何事件或发展的发生都可能损害我们的业务、财务状况、经营业绩和增长前景。在这种情况下,我们普通股的市场价格可能会下跌, 您可能会损失全部或部分投资。我们目前不知道或我们目前认为无关紧要的额外风险和不确定性也可能损害我们的业务运营。
与我们的财务状况和额外资本需求相关的风险
我们是一家临床阶段的生物技术公司,运营历史有限。
我们是一家临床阶段的生物技术公司,运营历史有限。生物制药产品开发是一项投机性很强的工作 ,涉及很大程度的风险。自2013年11月成立以来,我们几乎所有的努力和财政资源都集中在开发我们的药物发现平台和首批候选药物上。我们没有批准用于商业销售的产品 ,因此从未从药品销售中获得任何收入,我们预计在可预见的未来也不会从药品销售中获得任何收入。我们尚未获得任何候选药物上市的监管批准 也不能保证我们将来会获得监管部门的批准来营销和销售药物产品。
自成立以来,我们 已遭受重大运营亏损,并预计在可预见的未来还将继续亏损。
我们 自成立以来每年都出现净亏损。截至2019年12月31日和2020年12月31日的年度,我们的净亏损分别为6190万美元和100万美元。截至2020年12月31日,我们的累计赤字为100万美元。我们几乎所有的运营亏损都源于 与研发工作(包括临床研究)相关的成本,以及与我们运营相关的一般和行政成本。我们预计,随着我们继续 投资于研发工作以及现有和未来候选药物的临床试验的开始和继续,我们的运营费用将大幅增加。此外,如果我们获得任何候选药物的上市批准,我们将产生大量销售、 营销和外包制造费用。一旦我们成为一家上市公司,我们将产生与上市公司运营相关的额外成本。因此,我们预计在可预见的未来,运营亏损将继续大幅增加。 我们之前的亏损,加上预期的未来亏损,已经并将继续对我们的股东赤字和营运资本产生不利影响。由于与开发医药产品和新技术相关的众多风险和不确定性 ,我们无法预测未来亏损的程度或何时实现盈利(如果有的话)。即使我们确实实现盈利,我们也可能无法维持或提高我们的 季度或年度盈利能力。
即使我们完成了这项服务,我们的使命也是广泛而昂贵的,我们将需要筹集大量额外资金 。如果我们无法在需要时筹集资金,我们将被迫推迟、减少或取消至少部分产品开发计划、业务开发计划、战略投资或潜在的 商业化努力。
我们有雄心勃勃的计划来破译生物学,并向需要的患者提供新药。我们的任务范围广泛,实现成本高昂,未来还需要更多资金。此外,
22
医药产品的开发是资本密集型的。我们有4个临床阶段计划和31个处于临床前发展不同阶段的额外计划。我们预计我们的 费用将因我们正在进行的活动而增加,特别是当我们继续研发、启动临床试验,并可能为我们的候选药物寻求市场批准,并向我们的管道中添加 我们认为将会加速增加的额外计划。此外,根据潜在监管审批的状态,或者如果我们获得任何当前或未来候选药物的上市审批,我们可能会产生与产品销售、营销、制造和分销相关的巨额费用 。如果我们选择为候选药物寻求更多适应症和/或地域,或者以比我们目前预期更快的速度扩展 ,我们可能还需要更快地筹集额外资金。此外,在此次发行结束后,我们预计将产生与上市公司运营相关的额外成本。因此,我们将需要在 与我们持续运营相关的方面获得大量额外资金。如果我们无法在需要时或在有吸引力的条件下筹集资金,我们将被迫推迟、减少或取消某些研发计划或未来潜在的商业化努力 。
我们预计,此次发行的净收益,加上我们现有的现金和现金等价物、可供我们使用的借款以及截至招股说明书日期的 短期投资,将足以支付我们至少未来 个月的运营费用和资本支出。我们未来的资本需求将视乎多项因素而定,并可能因此而大幅增加,这些因素包括:
| • | 任何业务中断对我们的运营的影响,包括我们 计划的临床试验参与者的时间安排和登记,或新冠肺炎大流行或类似的公共卫生危机或其他不可抗力事件导致的对我们的制造商、供应商或其他供应商的运营的影响; |
| • | 我们当前和未来的临床试验以及其他临床前研究的范围、进展、结果和成本。 我们的计划; |
| • | 我们追求的未来候选药物的数量和他们的开发需求; |
| • | 对我们的候选药物进行监管审查的成本、时间和结果; |
| • | 我们在有利条件下建立和维持合作的能力(如果有的话); |
| • | 我们可能与第三方达成的任何合作的成功; |
| • | 我们收购或投资业务、产品和技术的程度,包括为候选药物签订许可或 合作安排; |
| • | 准备、提交和起诉专利申请、维护、保护和执行我们的知识产权以及为与知识产权相关的索赔辩护的成本; |
| • | 随着我们扩大业务运营和研发活动,我们的员工数量增长和相关成本增加; 和 |
| • | 作为一家上市公司的运营成本。 |
确定潜在候选药物并进行临床前开发测试和临床试验是一个耗时、昂贵且不确定的过程,需要数年时间才能完成,而且我们可能永远无法生成获得上市批准和实现产品销售所需的必要数据或结果。此外,我们的候选药物如果获得批准,可能不会在商业上取得成功。我们 预计,我们的商业收入(如果有的话)将来自销售我们预计多年内无法投入商业销售的产品(如果有的话)。因此,我们将需要继续依靠额外融资来实现 我们的业务目标。
23
任何额外的筹款努力都可能使我们的管理层从日常工作这可能会对我们开发和商业化我们的候选药物和技术的能力产生不利影响,我们不能保证此类资金将以我们可以接受的条款 提供,或者根本不能。
在此之前,如果我们能够产生可观的收入,我们预计将通过私募和公开股权发行、债务融资、战略合作、战略联盟和许可安排相结合的方式来满足我们的现金需求 。我们没有任何承诺的外部资金来源。整体和最近由于新冠肺炎疫情造成的金融市场中断可能会增加股权和债务融资的难度,并可能对我们满足筹款需求的能力产生实质性的不利影响。我们不能 保证未来的融资金额充足或条款可接受(如果有的话)。此外,任何融资条款可能会对我们股东的持股或权利产生不利影响,我们额外发行 证券(无论是股权还是债务)或此类发行的可能性,可能会导致我们股票的市场价格下跌。如果我们通过出售普通股或可转换或 可兑换为普通股的证券来筹集额外资本,您的所有权权益将被稀释,这些证券的条款可能包括清算或其他对您作为普通股股东的权利产生重大不利影响的优惠。 债务的产生将导致固定支付义务的增加,我们可能需要同意某些限制性契约,例如对我们产生额外债务的能力的限制,对我们获取、出售或许可知识产权的能力的限制,以及可能对我们的资本支出、宣布股息的能力产生不利影响的其他经营限制。 我们可能需要同意某些限制性条款,例如限制我们产生额外债务的能力,限制我们获取、出售或许可知识产权的能力,以及其他可能对我们的资本支出和宣布股息的能力产生不利影响的经营限制, 或者以其他方式开展我们的业务。我们还可能被要求通过与合作者的安排 或以其他方式提前寻求资金,并可能被要求放弃对我们的某些技术或候选药物、未来收入流或研究项目的权利,或以其他方式同意对我们不利的 条款。如果我们不能及时获得资金,我们可能会被要求大幅缩减、推迟或停止我们的一个或多个研发计划或任何候选药物的商业化,或者 无法根据需要扩大我们的业务或以其他方式利用我们的商机,这可能会对我们的业务、财务状况和运营结果产生重大影响。
我们没有批准商业销售的产品,也没有从产品销售中获得任何收入。
我们盈利的能力取决于我们是否有能力创造足够的收入来抵消我们的开支。到目前为止,除了有限的拨款收入、武田制药有限公司的里程碑付款和拜耳的技术访问费外,我们还没有从我们的候选药物或技术中获得任何收入,我们预计近期内不会从产品销售中获得任何收入 。除非我们使我们的候选药物通过临床试验,获得市场批准,并开始销售我们的一个或多个候选药物,或者以其他方式获得大量许可或其他付款,否则我们预计不会产生可观的收入。我们创造收入的能力取决于多个因素,包括但不限于,我们有能力:
| • | 圆满完成临床前研究; |
| • | 获得美国食品药物管理局(FDA)批准的研究新药(IND)申请,使我们能够 开始临床试验; |
| • | 成功招募受试者并完成临床试验; |
| • | 获得相关监管部门的监管批准; |
| • | 启动并成功完成为我们的候选药物获得美国和国外市场批准所需的所有安全性和其他研究 ; |
24
| • | 建立商业制造能力或与第三方制造商安排临床供应和 商业制造; |
| • | 获得并维护我们候选药物的专利和商业秘密保护或法规排他性; |
| • | 如果获得批准,无论是单独还是与他人合作,都可以启动我们候选药物的商业销售; |
| • | 在患者、医学界和第三方付款人批准的情况下,获得并保持对候选药物的接受; |
| • | 有效地与其他疗法竞争; |
| • | 获得并维持医疗保险和适当的报销; |
| • | 保护和执行我们的知识产权,抵御知识产权索赔; |
| • | 采取临时预防措施,帮助将新冠肺炎大流行或其他不可抗力事件对我们业务的影响降至最低。 |
| • | 在批准后,保持候选药物的持续可接受的安全性概况。 |
如果我们不能及时或根本实现这些因素中的一个或多个,我们可能会遇到重大延误或无法成功 将我们的候选药物商业化,这将严重损害我们的业务。如果我们的候选药物得不到监管部门的批准,我们可能无法继续运营。
我们或我们当前和未来的合作伙伴可能永远不会成功开发药品并将其商业化,这将对我们的运营结果 和我们继续业务运营的能力产生负面影响。
我们可能不会成功地生产出可以商业化的候选药物。要在我们的候选药物上取得成功,我们或我们当前或未来的合作者必须开发并最终将一个或多个产生可观收入的药物产品商业化。我们目前主要从我们的 协作关系中获得收入,并预计在我们或我们的合作者的药物开发和商业化努力取得成功(如果有的话)之前,我们的大部分收入将继续从这些关系中获得。
要在药物开发方面取得成功,需要我们或我们当前或未来的合作伙伴在一系列具有挑战性的活动中发挥作用, 包括完成候选药物的临床前测试和临床试验,获得这些候选药物的监管批准,以及制造、营销和销售我们或他们可能获得监管批准的任何产品。我们 和我们目前的药物发现合作者只处于这些活动的初步阶段。我们和他们可能永远不会在这些活动中取得成功,即使我们成功了,我们也可能永远不会产生足以实现 盈利的收入,或者即使我们的合作者成功了,我们也可能无法从他们那里获得足以让我们实现盈利的期权费用、里程碑付款或版税。由于我们的数据解决方案市场竞争激烈 ,以及与生物制药产品开发相关的众多风险和不确定性,我们无法准确预测我们何时或是否能够实现或维持盈利。
即使我们实现盈利,我们也可能无法维持或提高季度或年度盈利能力。我们未能成为并 保持盈利,最终将降低我们公司的价值,并可能削弱我们筹集资金、扩大业务、维持研发努力、开发候选药物管道、进行合作、 甚至继续运营的能力。我们公司的价值下降也可能导致您的全部或部分投资损失。
25
由于多种因素,我们的季度和年度运营业绩在未来可能会大幅波动, 其中许多因素不在我们的控制范围之内,可能很难预测。
我们未来的亏损数额是不确定的,我们的季度和 年度经营业绩可能会大幅波动,或者可能会低于投资者或证券分析师的预期,每一种情况都可能导致我们的股价波动或下跌。我们的季度和年度运营业绩可能 波动的原因包括以下几个方面:
| • | 继续保持、发展和整合技术进步的成本; |
| • | 我们候选药物或竞争候选药物的临床试验的时间、质量、法规遵从性和成功或失败,或我们行业竞争格局中的任何其他变化,包括我们的竞争对手或合作伙伴之间的整合; |
| • | 我们成功招募和留住临床试验受试者、地点和员工的能力,以及因此类努力中的困难而造成的任何延误; |
| • | 我们为候选药物获得上市批准的能力,以及我们 可能获得的任何此类批准的时间和范围; |
| • | 与我们的候选药物相关的研究和开发活动的时间、成本和投资水平, 可能会不时变化; |
| • | 生产我们的候选药物的时间、复杂性和成本,这可能会因生产数量和我们与制造商的协议条款而有所不同; |
| • | 我们有能力吸引、聘用和留住合格的人员,包括高度专业化的科学家、临床医生和 工程师; |
| • | 我们将会或可能发生的用于开发更多候选药物的支出; |
| • | 如果我们的候选药物获得批准,对它们的需求水平可能会有很大差异; |
| • | 关于我们的候选药物(如果获得批准)以及与我们候选药物竞争的现有 和潜在未来疗法的风险/收益概况、成本和报销政策; |
| • | 不断变化和动荡的美国和全球经济环境,包括新冠肺炎大流行和恐怖主义造成的环境;以及 |
| • | 未来的会计声明或我们会计政策的变化。 |
这些因素和其他因素的累积影响可能会导致我们季度和年度运营业绩的大幅波动和不可预测性。 因此,将我们的运营业绩与一期一期基础可能没有意义。这种变化性和不可预测性也可能导致我们无法 满足行业或金融分析师或投资者对任何时期的预期。如果我们的收入或经营业绩低于分析师或投资者的预期,或低于我们可能向市场提供的任何预测,或者如果我们 向市场提供的预测低于分析师或投资者的预期,我们普通股的价格可能会大幅下跌。即使我们满足了我们可能 提供的任何先前公开声明的指导,也可能出现这样的股价下跌。
如果我们从事未来的收购或战略合作,这可能会增加我们的资本要求,稀释我们的股东权益, 导致我们产生债务或承担或有负债,并使我们面临其他风险。
我们未来可能会进行各种收购和战略 合作,包括通过许可或收购互补产品、知识产权、技术或业务。任何收购或战略合作伙伴关系都可能带来许多风险,包括:
| • | 运营费用和现金需求增加; |
26
| • | 承担债务或或有负债; |
| • | 发行我们的股权证券,这将导致我们的股东股权被稀释; |
| • | 吸收被收购公司的运营、知识产权、产品和候选药物,包括 与整合新人员相关的困难; |
| • | 将我们管理层的注意力从寻求此类收购或战略合作伙伴关系的现有产品计划和计划上转移; |
| • | 关键员工的保留、关键人员的流失以及我们维护关键业务关系能力的不确定性 ; |
| • | 与此类交易的另一方相关的风险和不确定性,包括该方及其现有产品或候选药物的前景和监管批准;以及 |
| • | 我们无法从获得的知识产权、技术和/或产品中获得足够的收入来实现我们的 目标,甚至无法抵消相关的交易和维护成本。 |
此外,如果我们进行此类交易, 我们可能会发行稀释证券、承担或产生债务、产生巨额一次性费用以及收购可能导致重大未来摊销费用的无形资产。
与候选药物的发现和开发相关的风险
我们的 药物发现方法是独一无二的,可能不会带来成功的药物产品。
我们对细胞进行成像,并使用细胞形态学来了解 患病细胞对药物的反应以及它什么时候看起来正常。生物学是复杂的。如果研究细胞的形状、结构、形状和大小被证明不是更好地了解疾病的准确方法,或者不能带来 洞察力、可行的候选药物或我们预期的产品,那么我们的药物发现平台可能没有用处,或者可能不会产生成功的药物产品,或者我们可能不得不转向新的商业模式,其中任何一个都可能对我们的 声誉和运营结果产生不利影响。
我们的候选药物处于临床前或临床开发阶段,这是一个漫长而昂贵的过程,结果不确定,可能会出现实质性的延误。我们不能保证我们的候选药物将在临床试验中获得成功或获得监管部门的批准,这些批准是它们可以 商业化之前所必需的。
我们的候选药物处于临床前或临床开发阶段,这是一个漫长而昂贵的过程,结果不确定,而且有可能出现实质性的延误。我们尚未证明我们有能力完成临床开发、获得监管部门的批准、制造商业规模的产品、或安排第三方代表我们这样做, 或开展成功商业化所需的销售和营销活动。我们目前有四个临床阶段的候选药物,专注于罕见的单基因疾病,没有已知的既定监管先例。我们预计将向FDA提交第二阶段研究的IND 申请,并开始对所有四种候选药物进行此类研究。我们可能无法在预期的时间表内为任何其他候选药物 提交此类IND或IND(如果有的话),任何此类延迟都可能影响任何其他产品开发时间表。例如,我们可能会在临床前和临床研究中遇到生产延迟的情况。此外,我们不能确定 提交IND是否会导致FDA允许进一步的临床试验开始,或者一旦开始,不会出现需要我们暂停或终止临床试验的问题。这些临床试验中的每一项都要在 最终确定后才能开始
27
基于与FDA和其他监管机构的讨论进行的试验设计。我们从FDA或其他监管机构收到的任何指导意见都可能发生变化。这些监管机构 可能随时改变立场,包括他们对我们的试验设计的可接受性或所选临床终点或人群的立场,这可能要求我们完成额外的临床试验或施加比我们目前预期更严格的 批准条件。成功完成临床试验是为每个候选药物向FDA提交新药申请(NDA)和向欧洲药品管理局(EMA)或药品和医疗保健产品监管机构(MHRA)提交营销授权申请(MAA),从而最终批准每个候选药物并进行商业营销的先决条件。我们不知道我们未来的任何临床试验是否会按时开始,或者是否会如期完成(如果有的话)。
如果要求我们对候选药物进行超出我们目前预期的额外临床试验或其他 测试,如果我们无法成功完成候选药物的临床试验或其他测试,如果这些试验或测试的结果不呈阳性或仅为轻度阳性,或者如果存在安全问题,我们可能会:
| • | 延迟获得我们候选药物的上市批准; |
| • | 根本没有取得上市许可; |
| • | 获得对适应症或患者群体的批准,这些适应症或患者群体不像预期或期望的那样广泛,或者实施标签 限制、警告或风险缓解要求; |
| • | 接受上市后测试要求;或 |
| • | 产品经批准上市后下架的。 |
临床开发是一个漫长而昂贵的过程,结果不确定。
我们无法预测我们的候选药物何时或是否会在人体上证明是有效和安全的,或者是否会获得监管部门的批准。要获得监管部门对任何候选药物销售的市场批准,我们必须完成临床前研究,然后进行广泛的临床试验,以证明我们的候选药物在人体上的安全性和有效性。我们可以 直接从我们的药物发现平台中的细胞模型加速到患者身上,而无需通过动物试验验证结果,或者在我们进行第一阶段临床试验的同时在动物试验中验证它们。这种方法可能会给我们的成功带来额外的风险,因为我们的某些候选药物在人体试验之前没有在动物身上进行过试验。临床测试费用昂贵,难以设计和实施,可能需要数年时间才能完成,而且结果还不确定。一个或多个临床试验的失败可能发生在测试的任何阶段。临床前开发试验和早期临床试验的结果可能不能预测后续临床试验的成功,临床试验的中期结果也不一定能预测最终结果。此外,临床前和临床数据往往容易受到不同解释和分析的影响,许多公司认为他们的候选药物 在临床前研究和临床试验中表现令人满意,但仍然未能获得候选药物的上市批准或对批准的产品进行足够的付款人报销。我们的临床前研究和未来的临床试验可能不会成功。
我们可能会不时发布临床试验的临时顶线或初步数据 。临床试验的中期数据面临这样的风险,即随着参与者登记的继续和更多数据的获得,一个或多个临床结果可能会发生实质性变化。初步或最重要的数据也要接受审计和核实程序,这可能会导致最终数据与我们之前公布的初步数据大不相同。因此,在最终数据可用之前,应谨慎查看中期数据和 初步数据。初步或中期数据与最终数据之间的不利差异可能会严重损害我们的业务前景。
28
我们在完成候选药物的 开发和商业化过程中可能会产生额外成本或遇到延迟,或者最终无法完成。
我们可能会在完成临床前研究和启动或 完成临床试验方面遇到延误,并且在我们可能进行的任何未来临床试验期间或作为结果,我们可能会遇到许多不可预见的事件,这些事件可能会推迟或阻止我们获得上市批准或使我们的候选药物商业化 ,包括:
| • | 监管机构或机构审查委员会或伦理委员会不得授权我们或我们的调查人员 开始临床试验或在预期试验地点进行临床试验; |
| • | 我们可能会在与预期试验地点和 预期合同研究组织(CRO)就可接受的条款达成协议方面遇到延误或无法达成协议,其条款可能需要进行广泛的谈判,并且在不同的CRO和试验地点之间可能会有很大差异; |
| • | 我们候选药物的临床试验可能会产生否定或不确定的结果,我们可能决定或监管机构可能要求我们进行额外的临床前研究或临床试验,或者我们可能决定放弃产品开发计划; |
| • | 我们候选药物的临床试验所需的参与者人数可能比我们预期的多,这些临床试验的登记人数 可能比我们预期的慢,或者参与者可能退出这些临床试验或无法以高于我们预期的速度返回进行治疗后随访; |
| • | 我们的第三方承包商可能不遵守法规要求或未能及时履行其对我们的合同义务 ,或者根本不遵守,或者可能偏离临床试验方案或退出试验,这可能需要我们增加新的临床试验地点或研究人员; |
| • | 我们可能会选择,或监管机构、IRBs或伦理委员会可能会要求我们或我们的研究人员因各种原因暂停或终止 临床研究,包括不符合监管要求或发现参与者暴露在不可接受的健康风险中; |
| • | 我们候选药物的临床试验成本可能比我们预期的要高; |
| • | 我们候选药物的供应或质量或进行我们候选药物临床试验所需的其他材料可能不足或不充分 ; |
| • | 延迟生产我们的候选药物;以及 |
| • | 我们的候选药物可能具有不良副作用或其他意外特征,导致我们或我们的调查人员、 监管机构、IRBs或伦理委员会暂停或终止试验,或者报告可能来自对其他疗法的临床前或临床测试,这些测试提高了我们候选药物的安全性、有效性或其他担忧。 |
如果临床试验被我们、进行此类试验的机构的IRBs或伦理委员会、用于此类试验的数据安全监控委员会、FDA或其他监管机构暂停或终止,我们可能会遇到延迟。监管当局可能会因多种因素 而强制暂停、终止或临床暂停临床试验,例如未按照监管要求或我们的临床规程进行临床试验、FDA或其他监管机构对临床试验操作或试验地点进行检查、无法预见的 安全问题或不良副作用、未能证明使用产品有益处、政府法规或行政措施的变化,或者缺乏足够的资金来继续临床试验。许多可能导致或导致延迟开工或完工的因素
29
临床试验也可能最终导致我们的候选药物被拒绝获得监管部门的批准。此外,FDA可能不同意我们的临床试验设计和我们对临床试验数据的解释 ,或者即使在审查和评论了我们的临床试验设计之后,也可能更改审批要求。
如果我们在测试或监管审批方面遇到延误,我们的产品开发成本也会增加。我们不知道我们未来的任何临床试验是否会按计划开始,或者我们当前或未来的临床试验是否需要重组或是否会如期完成(如果有的话)。重大的临床前研究或临床试验延迟,包括新冠肺炎疫情 导致的延迟,也可能缩短我们拥有候选药物商业化独家权利或允许我们的竞争对手先于我们将产品推向市场的任何时间, 会削弱我们成功将候选药物商业化的能力,并可能损害我们的业务和运营结果。我们临床前或未来临床开发计划的任何延误都可能严重损害我们的业务、财务状况和前景 。
如果我们在临床试验的患者登记过程中遇到延迟或困难,我们收到必要的监管批准可能会被推迟或阻止 。
如果我们无法根据FDA或美国以外的类似监管机构的要求, 找到并招募足够数量的合格参与者参加这些试验,我们可能无法启动或继续针对当前或未来候选药物的临床试验。我们招收合格参与者的能力可能有限,或者可能导致 招生速度比我们预期的要慢。此外,竞争对手可能会启动或正在进行候选药物的临床试验,这些候选药物与我们当前或未来的候选药物具有相同的适应症,而原本有资格参加我们的临床试验的参与者可能会转而报名参加我们的竞争对手的临床试验。此外,我们招募参与者的能力可能会因新冠肺炎大流行的演变而延迟,目前我们不知道这种延迟的程度和范围。
除了竞争性试验环境外,我们计划的临床试验的资格标准 将进一步限制可用的研究参与者,因为我们将要求参与者具有特定的特征,例如与我们的候选药物相关的罕见疾病,这也可能使注册具有挑战性。此外,寻找潜在参与者的 过程可能成本高昂。我们也可能无法确定、招募和招募足够数量的参与者来完成我们的临床研究,原因包括被研究药物 候选药物的已知风险和益处、竞争疗法和临床试验的可用性和有效性、潜在参与者的临床试验地点的邻近和可用性以及医生的推荐做法。如果人们出于任何原因不愿意 参加我们的研究,招募参与者、进行研究以及获得监管部门对潜在产品的批准的时间可能会推迟。
临床试验登记可能受到其他因素的影响,包括:
| • | 被调查的疾病的严重程度; |
| • | 有关临床试验的资格准则为何; |
| • | 适当的基因组筛选测试的可用性; |
| • | 接受研究的候选药物的感知风险和益处; |
| • | 为及时招募临床试验提供便利的努力; |
| • | 医生的转诊做法; |
| • | 在试验期间和试验后充分监测参与者的能力; |
| • | 潜在参与者的临床试验地点的近似性和可用性; |
30
| • | 我们可能无法控制的因素,例如当前或潜在的流行病可能会限制 参与者、主要研究人员、研究人员或临床站点的可用性,例如新冠肺炎的爆发; |
| • | 医生的转介做法; |
| • | 有能力在试验期间和试验后充分监测参与者; |
| • | 有能力招聘具有适当能力和经验的临床试验研究人员; |
| • | 我们维护参与者知情同意和隐私的能力;以及 |
| • | 登记的参与者无法完成临床试验的风险。 |
我们计划中的临床试验或我们未来潜在合作者的临床试验可能会揭示我们的临床前或非临床 研究中未见的重大不良事件,并可能导致安全状况,这可能会阻碍监管部门批准或市场接受我们的任何候选药物。
在 获得任何产品商业销售的监管批准之前,我们必须通过漫长、复杂且昂贵的临床前研究和临床试验证明,我们的候选药物在每个目标适应症中都是安全有效的 。临床测试费用昂贵,可能需要数年时间才能完成,而且其结果本身也不确定。在临床试验过程中,任何时候都可能发生失败。我们候选药物的临床前研究和早期临床试验的结果可能无法预测后期临床试验的结果。此外,临床试验的初步成功可能并不代表这些试验完成后所取得的结果。由于候选药物在临床试验中失败,通常有极高的流失率 。尽管在非临床研究和初步临床试验中取得了进展,但临床试验后期阶段的候选药物也可能无法显示出所需的安全性和有效性。生物制药行业的许多公司由于缺乏疗效或不可接受的安全性问题,在高级临床试验中遭受了重大挫折,尽管在 早期试验中取得了令人振奋的结果。大多数开始临床试验的候选药物从未作为产品获得批准,不能保证我们当前或未来的任何临床试验最终会成功或支持我们任何候选药物的进一步临床开发 。
我们可能会结合一种或多种疾病疗法来开发未来的候选药物。将我们的候选药物与其他疾病疗法结合使用所产生的不确定性 可能会使在未来的临床试验中准确预测副作用变得困难。
就像许多治疗罕见疾病和其他疾病的方法一样,使用我们的候选药物已经产生了副作用,而且很可能会有副作用 。如果在我们当前或未来的候选药物中观察到重大不良事件或其他副作用,我们可能难以招募临床试验参与者,他们可能会退出我们的 试验,或者我们可能被要求完全放弃一个或多个候选药物的试验或开发工作。我们、FDA或其他适用的监管机构或IRB可以出于各种原因 随时暂停或终止候选药物的临床试验,包括认为此类试验中的受试者面临不可接受的健康风险或不良副作用。生物技术行业开发的一些潜在疗法最初在早期试验中显示出治疗前景,但后来发现它们会产生副作用,阻碍它们的进一步发展。即使副作用并不妨碍该产品获得或保持上市批准,但由于与其他疗法相比,该产品的耐受性,不良副作用 可能会抑制市场对该产品的接受。这些发展中的任何一个都可能对我们的业务、财务状况和前景造成实质性的损害。
31
我们未来可能会在美国以外的地方为我们的候选药物进行临床试验,FDA和 类似的外国监管机构可能不会接受此类试验的数据。
我们未来可能会选择在美国以外的地方(包括澳大利亚、欧洲、亚洲或其他外国司法管辖区)进行额外的临床试验。FDA接受在美国境外进行的临床试验的试验数据可能会受到某些条件的限制。如果来自美国境外进行的临床试验的数据 打算作为在美国上市批准的唯一依据,FDA通常不会仅根据外国数据批准申请,除非i)数据 适用于美国人口和美国医疗实践;Ii)试验由具有公认能力的临床研究人员进行,iii)数据可被认为是有效的,无需FDA进行现场检查 ,或者,如果FDA认为有必要进行现场检查,FDA可以通过现场检查或其他适当方式验证数据。此外,还必须满足FDA的临床试验要求,包括足够大的试验总体规模和统计能力。许多外国监管机构也有类似的审批要求。此外,此类外国审判将受进行 审判的外国司法管辖区适用的当地法律管辖。不能保证FDA或任何类似的外国监管机构会接受在美国或适用司法管辖区以外进行的试验数据。如果FDA或任何类似的外国监管机构不接受此类数据,将导致需要额外的试验,这将是昂贵和耗时的,并会延误我们业务计划的各个方面,并可能导致我们的候选药物无法在适用司法管辖区获得商业化的批准或许可 。
随着英国于2020年1月31日脱离欧盟,并于2020年12月31日结束过渡期,欧盟和英国达成了一项贸易与合作协议,该协议规范了未来关系的某些方面,包括确保 某些商品和服务的零关税贸易。由于英国有关药品的质量、安全性和有效性、临床试验、营销授权、商业销售和分销的监管框架源自欧盟指令和法规,英国脱欧将对英国未来适用于产品和候选药物审批的监管制度产生重大影响。从长远来看,英国可能会制定自己的立法,与欧盟的立法有所不同。
我们 候选药物的目标患者人群的发病率和流行率尚未准确确定。如果我们候选药物的市场机会比我们估计的要小,或者如果我们获得的任何批准是基于对患者群体的更狭隘的定义,我们的收入和 实现盈利的能力将受到不利影响,可能会造成实质性影响。
即使我们的候选药物获准商业化销售,我们候选药物的总潜在市场最终也将取决于最终标签中包含的诊断标准(如果我们的候选药物获得这些适应症的批准、医学界和 患者的接受程度、产品定价和报销)。我们候选药物的目标患者数量可能会低于预期,患者可能无法以其他方式接受我们的产品治疗,或者新患者可能变得越来越难以识别或接触,所有这些都会对我们的运营结果和业务产生不利影响。我们确定更多候选药物的努力可能不会成功。由于我们的资源和获得资金的渠道有限,我们必须优先开发某些候选药物,这可能被证明是错误的选择,并可能对我们的业务产生不利影响。
32
虽然我们打算探索其他治疗机会,但除了我们目前正在开发的候选药物外,由于多种原因,我们可能无法确定可用于临床开发的可行新药候选药物。如果我们不能发现更多的潜在候选药物,我们的业务可能会受到实质性的损害。
继续开发我们现有的和计划中的候选药物以获得更多适应症,并确定新的候选药物和疾病靶点的研究计划需要大量的技术、财政和人力资源,无论它们最终是否成功。例如,根据我们与拜耳股份公司的研究协作和选项协议或拜耳协议,我们 与拜耳股份公司或拜耳合作开发各种与纤维化相关的项目。不能保证我们会使用这种方法找到潜在的靶点,不能保证任何这样的靶点都是容易处理的,也不能保证这样的临床验证会成功 。我们的研究计划最初可能在确定潜在适应症和/或候选药物方面显示出希望,但由于多种原因未能产生临床开发结果,包括:
| • | 使用的研究方法可能不能成功识别潜在的适应症和/或候选药物,包括 ,这是因为我们的数据库中显示的患者样本有限,以及基于来自特定细胞环境(可能不适用于其他更相关的细胞环境)的洞察力进行推断的有效性; |
| • | 在进一步研究后,潜在的候选药物可能被证明具有有害的副作用或其他特征, 表明它们不太可能是有效的产品;或 |
| • | 为我们的候选药物确定额外的治疗机会或通过内部研究计划开发合适的潜在候选药物可能需要比我们所拥有的更多的人力和财力,从而限制了我们开发、多样化和扩展产品组合的能力。 |
由于我们的财力和人力资源有限,我们将不得不优先考虑和专注于某些研究项目、候选药物和靶向 适应症,而放弃其他项目。因此,我们可能会放弃或推迟寻求与其他候选药物或后来证明具有更大商业潜力或更大成功可能性的其他适应症的机会。我们的资源 分配决策可能导致我们无法利用可行的商业产品或有利可图的市场机会。
因此, 不能保证我们将能够通过内部研究计划为我们的候选药物确定额外的治疗机会或开发合适的潜在候选药物,这可能会对我们未来的增长和前景产生实质性的不利影响 。我们可能会将我们的努力和资源集中在潜在的候选药物或其他最终被证明是不成功的潜在项目上。
如果我们无法获得或延迟获得候选药物所需的监管批准,我们将无法将候选药物商业化,或者 将推迟商业化,我们的创收能力将受到严重影响。
我们的候选药物以及与其开发和商业化相关的活动,包括其设计、测试、制造、安全性、有效性、记录保存、标签、储存、审批、广告、促销、销售、分销、进口和 出口,均受美国FDA和其他监管机构以及其他国家类似机构的全面监管。在我们可以将任何候选药物商业化之前,我们必须获得上市批准。 目前,我们所有的候选药物都在开发中,我们尚未从任何司法管辖区的监管机构获得将任何候选药物上市的批准。我们的候选药物,包括我们可能寻求开发的任何候选药物 都有可能
33
未来,将永远不会获得监管部门的批准。我们在向监管机构提交和支持申请方面的经验有限,预计将依靠CRO和/或监管 顾问来协助我们完成这一过程。要获得监管部门的批准,需要针对每个治疗适应症向各个监管机构提交广泛的临床前和临床数据和支持信息,以确定 候选药物的安全性和有效性。要获得监管部门的批准,还需要向相关监管机构提交有关产品制造过程的信息,并由相关监管机构检查制造设施。我们的 候选药物可能无效,可能只是中等有效,或者可能被证明具有不良或意外的副作用、毒性或其他特征,这些可能会阻止我们获得上市批准,或者阻止或限制商业使用 。此外,监管部门可能会发现我们的制造工艺或设备或第三方合同制造商的制造工艺或设备有问题。在制造我们的候选药物时,我们也可能面临比预期更大的困难。
无论是在美国还是在国外,获得监管批准的过程都是昂贵的,而且往往需要很多年的时间。如果FDA或类似的外国监管机构要求我们进行额外的临床前或临床试验,如果获得批准,可能会被推迟。这种延迟的长度根据各种因素而有很大不同,包括所涉及的候选药物的类型、复杂性和新颖性。开发期内市场审批政策的更改、附加法规或法规的更改,或对每个提交的NDA、 510(K)、上市前审批申请或PMA或同等申请类型的监管审查的更改,都可能导致申请审批或拒绝的延迟。FDA和其他国家的类似机构在审批过程中拥有相当大的自由裁量权,可以拒绝接受任何申请,也可以决定我们的数据不足以获得批准,需要进行额外的临床前、临床或其他研究。我们的候选药物可能会因多种原因而延迟获得或无法获得监管批准,包括以下原因:
| • | FDA或类似的外国监管机构可能不同意我们临床试验的设计或实施; |
| • | 我们可能无法在我们的临床研究中招募足够数量的患者; |
| • | 我们可能无法向FDA或类似的外国监管机构证明候选药物对于其建议的适应症是安全有效的,或者相关的伴随诊断适合识别合适的患者群体; |
| • | 临床试验结果可能达不到美国食品药品监督管理局(FDA)或国外可比监管机构批准的统计显著性水平; |
| • | 我们可能无法证明候选药物的临床和其他益处大于其安全风险; |
| • | FDA或类似的外国监管机构可能不同意我们对临床前研究或临床试验数据的解释。 |
| • | 从我们候选药物的临床试验中收集的数据可能不足以或质量不足以支持提交保密协议或其他提交或获得美国或其他地方的监管批准; |
| • | FDA或类似的外国监管机构可能发现与我们签订临床和商业供应合同的第三方制造商的制造 工艺或设施存在缺陷或未获批准;以及 |
| • | FDA或类似的外国监管机构的批准政策或法规可能会发生重大变化, 以至于我们的临床或生产数据不足以获得批准。 |
即使我们获得批准,监管部门 也可能批准我们的任何候选药物,其适应症比我们要求的更少或更有限,从而缩小商业范围。
34
候选药物的潜力。此外,监管部门可能会根据昂贵的上市后临床试验的表现给予批准,或者可能会批准带有 标签的候选药物,该标签不包括候选药物成功商业化所必需或需要的标签声明。上述任何一种情况都可能对我们候选药物的商业前景造成实质性损害。
如果我们在获得批准方面遇到延误,或者如果我们未能获得候选药物的批准,我们候选药物的商业前景可能会受到损害 ,我们的创收能力将受到严重损害。
在我们的 药物研发合作中,我们的资源和现金投资可能永远不会实现回报。
我们为从事药物发现和 开发的合作者或与他们一起开展药物发现活动。这些合作者包括商业化前的生物技术公司和大型制药公司。当我们与这些合作者一起从事药物发现时,我们通常会提供我们的平台和平台专家的好处 ,他们识别对一个或多个指定目标具有活性的分子。考虑到这一点,我们已收到股权投资、预付费用和/或获得期权费用、现金里程碑 在实现指定开发、药品发现目标的监管、商业销售里程碑和潜在专利费方面的付款。
我们可能永远不会从我们在药物发现合作中的资源和现金投资中获得更长期的回报。临床药物开发 涉及一个漫长而昂贵的过程,结果不确定。我们的药物发现合作者在完成或最终无法完成任何 候选药物的开发和商业化时,可能会产生额外成本或遇到延迟。此外,我们从药物发现合作中实现回报的能力受到以下风险的影响:
| • | 药物发现合作者在决定 他们将应用于我们的合作的努力和资源的数量和时间方面有很大的自由裁量权,并且可能无法按预期履行其义务; |
| • | 药物发现合作者不得对我们 有权获得期权费用、里程碑付款或版税的任何候选药物进行开发或商业化,或者可以根据临床试验或其他研究的结果、合作者战略重点的变化或 可用资金或外部因素(如收购),选择不继续或续签开发或商业化计划; |
| • | 药物发现合作者可能会推迟我们有权获得里程碑付款的临床试验; |
| • | 我们可能无法获取或可能被限制披露有关我们的合作者正在开发或商业化的候选药物 的某些信息,因此,向我们的股东告知此类合作的里程碑付款或特许权使用费的状况以及实现该等合作的可能性的能力可能有限; |
| • | 药物发现合作者可以独立开发或与第三方开发与任何候选药物直接或 间接竞争的产品,以及我们有权获得里程碑式付款或版税的产品,并且合作者可能认为竞争产品更有可能成功开发,或者可以根据更具经济吸引力的条款 进行商业化; |
| • | 在与我们的药物发现合作中发现的候选药物可能会被我们的合作者视为与 他们自己的候选药物或产品竞争,这可能会导致我们的 |
35
| 合作者停止为任何此类候选药物的商业化投入资源; |
| • | 现有的药物发现合作者和潜在的未来药物发现合作者可能开始将我们视为更广泛的 竞争对手,特别是当我们推进内部药物发现计划时,因此可能不愿意继续与我们现有的合作或与我们进行新的合作; |
| • | 药物发现合作者可能无法遵守有关候选药物或产品的开发、 生产、分销或营销的适用法规要求,这可能会影响我们获得里程碑付款的能力; |
| • | 与药物发现合作者的分歧,包括在知识产权或专利权、 合同解释或首选的开发过程方面的分歧,可能会导致我们有资格获得里程碑付款的候选药物的研究、开发或商业化的延迟或终止,或者可能导致 诉讼或仲裁; |
| • | 药物发现合作者可能无法正确获取、维护、强制执行、捍卫或保护我们的知识产权或 专有权利,或可能以某种方式使用我们的专有信息,从而可能导致纠纷或法律诉讼,从而危及我们或他们的知识产权或专有权利或使我们和他们面临 潜在的诉讼; |
| • | 药物发现合作者可能侵犯、挪用或以其他方式侵犯第三方的知识产权或所有权 ,这可能使我们面临诉讼和潜在的责任;以及 |
| • | 在我们收到协作的任何重要价值之前,可能会终止药物发现协作。 |
我们的药物发现合作可能不会导致候选药物的开发或商业化,从而导致我们及时收到选择费、里程碑付款、特许权使用费或其他付款,或者根本不会收到选择费、里程碑付款、特许权使用费或其他付款。例如,我们可能过度依赖我们的合作伙伴为我们许可的分子提供信息。 我们许可的分子可能没有得到很好的保护,因为曾经保护它们的合成物质专利已经过期。此外,我们可能难以获得有效药物成分(API)的质量和数量 ,或者无法确保分子的稳定性,所有这些都是进行临床试验或将候选药物推向市场所必需的。对于那些我们试图改变用途以用于其他 指示的分子,我们的合作伙伴可能没有足够的数据、质量较差的数据或能够帮助我们解释数据,任何这些都可能导致我们的合作失败。
如果我们参与的任何药物发现合作未能成功开发药物产品并将其商业化,从而导致 向我们支付期权费用、里程碑付款、版税或其他付款,我们在此类药物发现合作中投入的资源可能得不到回报。此外,即使药物发现合作最初导致 实现里程碑,从而向我们付款,它也可能不会继续这样做。
我们面临着激烈的竞争,这可能会导致其他人 比我们更早或更成功地发现、开发或商业化产品。
生物制药及相关行业新产品的开发和商业化竞争激烈。还有其他公司专注于技术驱动的药物发现,以识别和开发NCE和KCE。其中一些具有竞争力的公司基于与我们的方法相同或相似的 科学方法,而其他公司则基于完全不同的方法。这些公司包括大型制药公司的部门。
36
和各种规模的生物技术公司。我们目前的候选药物面临竞争,未来我们可能寻求 开发或商业化的任何候选药物都将面临来自世界各地主要制药公司、专业制药公司和生物技术公司的竞争。潜在竞争对手还包括学术机构、政府机构和其他进行研究、寻求专利保护并为研究、开发、制造和商业化建立协作安排的公共和私人研究组织。
我们成功开发和商业化的任何候选药物都将与目前批准的疗法和未来可能 从制药、生物技术和其他相关行业寻求新疗法的部门提供的新疗法展开竞争。影响我们与其他疗法有效竞争能力的关键产品功能包括我们产品的有效性、安全性和便利性。我们相信,我们业务的主要竞争因素包括计算和预测的准确性、整合实验和计算能力 的能力、成功将研究项目转化为临床开发的能力、筹集资金的能力以及平台、管道和业务的可扩展性。
与我们相比,我们的许多竞争对手或未来可能竞争的公司在研发、制造、临床前测试、进行临床试验、获得监管批准和营销批准产品方面拥有更多的财务资源和专业知识 。制药、生物技术和诊断行业的合并和收购可能会导致更多的资源集中在我们数量较少的竞争对手中。规模较小或处于早期阶段的公司也可能成为重要的竞争对手,特别是通过与大公司和 成熟公司的协作安排。这些竞争对手还在招聘和留住合格的科学和管理人员、建立临床试验场地和临床试验患者注册,以及获得补充或必要于我们计划的 技术方面与我们展开竞争。此外,我们无法预测我们目前的竞争优势和我们的软件工具是否会保持不变,并在未来适当地演变为进入壁垒。如果 没有,其他公司可能会更直接或更有效地与我们竞争。
如果我们的 竞争对手开发和商业化比我们或我们的合作者可能开发的任何产品更安全、更有效、副作用更少或更少、更方便或更便宜的产品,我们的商业机会可能会减少或消失。我们的竞争对手还可能 比我们更快地获得FDA或其他监管机构对其产品的批准,这可能会导致我们的竞争对手在我们或我们的合作者能够进入市场之前建立强大的市场地位。 如果获得批准,影响我们所有候选药物成功的关键竞争因素可能是它们的疗效、安全性、便利性、价格、仿制药竞争水平以及政府和 其他第三方付款人是否可以报销。
由于我们正在开发多个计划和候选药物,并且正在追求各种目标适应症 和治疗方式,因此我们可能会将有限的资源用于追求特定的候选药物,而无法利用可能更有利可图或 成功可能性更大的开发机会或候选药物。
我们目前专注于候选药物的开发,而不考虑治疗方式或特定的目标适应症。 由于我们的财力和人力资源有限,我们可能会放弃或推迟追求具有潜在目标适应症或候选药物的机会,这些机会后来被证明比我们当前和计划中的开发计划和候选药物具有更大的商业潜力。 我们的资源分配决策可能会导致我们无法充分利用可行的资源。
37
商业产品或有利可图的市场机会。我们在当前和未来研发项目以及其他特定适应症的未来候选药物上的支出可能不会 产生任何商业上可行的未来候选药物。
我们和我们的合作者可能无法在我们或他们宣布的时间范围内实现预计的发现和开发里程碑以及其他 预期的关键事件,这可能会对我们的业务产生不利影响,并可能导致我们的股价下跌。
我们预计,我们将不时就某些里程碑和关键事件的预期时间发表公开声明,例如我们内部药物发现计划中的临床前和临床研究的 开始和完成,以及我们合作下的进展和里程碑。我们的合作者(如拜耳)还发表了关于 对与我们合作的项目开发的期望的公开声明,并可能在未来就他们与我们合作的目标和期望发表更多声明。这些活动的实际时间可能会因多种因素而大不相同,例如我们或我们当前和未来的合作者的药物发现和开发计划的延迟或失败,我们和我们当前和未来的合作者投入的时间、精力和资源的数量,以及药物开发过程中固有的 许多不确定因素。因此,不能保证我们或我们当前和未来的合作者计划会在我们或他们宣布或预期的时间范围内推进或完成。如果我们 或任何合作者未能按计划实现其中一个或多个里程碑或其他关键事件,我们的业务可能会受到重大不利影响,我们的普通股价格可能会下跌。
与我们的平台和数据相关的风险
我们的业务和运营 将受到计算机系统故障、网络攻击或我们或第三方网络安全缺陷的影响。
我们 越来越依赖信息技术系统、基础设施和数据来运营我们的业务。在正常业务过程中,我们收集、存储和传输机密信息(包括但不限于知识产权、专有业务信息、个人信息和其他机密信息)。我们必须以安全的方式这样做,以保持这些信息的机密性和完整性,这一点至关重要。我们还将我们运营的 要素外包给第三方,因此我们管理着许多第三方供应商以及其他承包商和顾问,他们可以访问我们的机密信息。
鉴于我们有限的运营历史,我们仍在实施内部安全和业务连续性措施,并 发展我们的信息技术基础设施。我们的内部计算机系统以及我们所依赖的当前和未来第三方的计算机系统可能会出现故障,容易受到计算机病毒和未经授权的访问的破坏。我们的信息技术 和其他内部基础架构系统,包括公司防火墙、服务器、我们所在的数据中心设施、实验室设备、租用线路和互联网连接,都面临着服务中断、系统故障、自然灾害、恐怖主义、战争、电信和电气故障,以及我们的员工、承包商、顾问、业务合作伙伴和/或其他第三方或网络的疏忽或故意行为造成的安全破坏的风险 拒绝服务攻击、社会工程和其他手段影响服务可靠性并威胁信息的机密性、完整性和可用性), 其中每一种都可能危及我们的系统基础设施,或导致我们的数据或代表我们处理或维护的数据或其他资产丢失、破坏、更改、泄露或传播,或损坏或未经授权访问我们的数据或数据。 任何一种情况都可能导致我们的数据或代表我们处理或维护的数据或其他 资产丢失、破坏、更改、泄露或传播。
38
如果发生此类事件并导致我们的运营中断,可能会对我们的开发计划和业务运营造成重大 中断,并可能对我们造成财务、法律、业务和声誉方面的损害。例如,我们的主要优势之一是我们专有的技术信息和生物 和化学数据。我们的数据丢失、腐败、不可用或损坏将干扰和破坏我们从我们的平台获得的洞察力,这可能导致在基于有缺陷的前提的洞察力上浪费资源。此外,来自已完成或未来临床试验的临床试验数据的丢失或损坏或其他损坏可能会导致我们的监管审批工作延迟,并显著增加我们恢复或复制数据的成本。 同样,我们依赖第三方生产我们的候选药物或任何未来候选药物并进行临床试验,与其系统和操作相关的类似事件也可能对我们的 业务产生重大不利影响,并导致监管机构采取行动。安全漏洞或破坏的风险,特别是通过网络攻击或网络入侵(包括计算机黑客、外国政府和网络恐怖分子)的风险普遍增加,因为来自世界各地的未遂攻击和入侵的数量、强度和复杂性都有所增加。经验丰富的网络攻击者(包括从事工业间谍活动的外国对手)擅长适应现有的安全技术,并开发新的方法来访问组织的敏感业务数据,这可能会导致包括商业机密在内的专有信息丢失。我们可能无法预见所有类型的安全威胁 , 我们可能无法针对所有这些安全威胁采取有效的预防措施。例如,第三方过去和将来可能会非法盗版我们的软件,并在 上公开提供该软件点对点文件共享网络或其他。网络罪犯使用的技术经常变化,可能要到启动时才能被识别,而且可能来自广泛的来源,包括外部服务提供商、有组织犯罪分支机构、恐怖组织或敌对的外国政府或机构等外部组织。此外,为了应对持续的新冠肺炎疫情,我们的大部分员工目前都在远程工作。这可能会增加我们的网络安全风险,造成数据可访问性问题,并使我们更容易受到通信中断的影响 。
任何安全漏洞或其他事件导致个人信息(包括有关临床试验对象、承包商、董事或员工的个人信息、我们的知识产权、专有业务信息或其他机密或专有信息)的丢失、损坏或未经授权访问、使用、更改或披露或 传播,都可能直接损害我们的声誉,使竞争对手能够更有效地与我们竞争,迫使我们遵守联邦和/或州违反通知法和外国等效法律,我们将受到强制性纠正措施的 和其他方面的约束。这可能会导致重大的法律和财务风险以及声誉损害,这可能会对我们的业务产生 不利影响。与安全事件相关的通知和后续行动可能会影响我们的声誉,我们可能会在 与这些措施相关或与任何实际或疑似安全违规相关的情况下招致包括法律和补救费用在内的巨额成本。我们预计在检测和预防安全事件以及以其他方式实施我们的内部安全和 业务连续性措施时会产生巨额成本,而实际的、潜在的或预期的攻击可能会导致我们的成本增加,包括部署更多人员和保护技术、培训员工以及聘请第三方专家和 顾问的成本。我们可能会面临增加的成本,并发现在发生实际或感觉到的安全漏洞时,有必要或适当地花费大量资源。
与重大安全漏洞或中断相关的成本可能是重大的,我们的保险单可能不足以赔偿我们因存储或处理对我们的业务运营或商业发展重要的信息的系统或第三方系统中的任何此类中断、故障或安全漏洞而产生的潜在损失。此外,我们未来可能无法按经济合理的条款购买此类 保险,或者
39
一点也没有。此外,我们的保险可能不会覆盖针对我们的所有索赔,在任何情况下都可能有很高的免赔额,而且无论胜诉与否,为诉讼辩护都可能代价高昂,并分散 管理层的注意力。此外,如果我们的第三方供应商、其他承包商和顾问的信息技术系统受到中断或安全漏洞的影响,我们可能没有足够的追索权来对抗此类第三方 ,我们可能不得不花费大量资源来减轻此类事件的影响,并制定和实施保护措施以防止未来发生此类事件。
如果我们不能为我们的平台开发跟上技术发展步伐的新解决方案和增强功能,我们的业务和 运营结果将受到损害。
我们增加收入的能力在很大程度上取决于我们增强和改进我们平台的能力。 我们平台的任何增强能否成功取决于几个因素,包括生成额外的生物和化学数据、硬件解决方案的创新、计算存储和处理能力的增加以及 更高级算法的开发。我们开发的任何新增强功能可能不会以及时或经济高效的方式引入,可能包含错误、漏洞或错误,或者可能无法实现产生可观收入所需的功能。 如果我们不能成功开发新创新、增强现有平台或以其他方式获得市场认可,我们的声誉、业务、运营结果和财务状况都将受到损害。我们的成功还取决于我们 识别重要和新兴使用案例并快速开发新的有效创新来解决这些使用案例的能力。
我们已经进行了投资,并且 预计将继续投资于研发工作,以进一步增强我们的平台。此类投资可能会影响我们的经营业绩,如果这些投资的回报低于我们的预期或发展速度慢于我们的预期,我们的 收入和经营业绩可能会受到影响。
我们已经并将继续投资于研发工作,以进一步 增强我们的平台。这些投资可能涉及大量时间、风险和不确定因素,包括与这些投资相关的费用可能会影响我们的利润率和运营业绩,以及此类投资可能无法 产生足够的收入来抵消承担的债务和与这些新投资相关的费用的风险。随着技术和产品的发展,软件行业变化很快,这可能会降低我们的解决方案 的效率。我们相信,我们必须继续在我们的平台上投入大量的时间和资源,以保持和提高我们的竞争地位。如果我们没有实现这些投资的预期收益,如果延迟实现这些收益 ,我们的业务、运营结果和前景可能会受到重大不利影响。
我们 平台中的缺陷或中断可能会降低我们的价值和前景。
我们的平台依赖于 我们的软件、硬件、数据库以及相关工具和功能的持续、有效和可靠的运行,以及我们数据的完整性。我们的专有软件工具、硬件和数据集本身就很复杂,可能包含缺陷或错误。错误可能源于我们的专有软件和硬件工具与我们的数据或第三方系统和数据的接口 ,而这些系统和数据不是我们开发的。首次引入新软件或硬件或实施现有软件或硬件的新版本或 增强功能时,出错风险尤其显著。我们经常发现我们的软件和硬件存在缺陷,未来可能会在现有的软件和硬件中检测到新的错误。我们的软件、硬件或数据集的任何错误、缺陷、 中断或其他性能问题都可能损害我们收集推动药物发现的宝贵见解的能力。此外,我们的平台可能会产生覆盖范围不足的不完整数据集 ,这可能会对我们发现新药候选药物的能力造成实质性的不利影响。这样的发现取决于
40
我们数据的完整性和完整性。任何此类事件的发生都可能导致我们平台和数据的价值缩水,并对我们的业务、运营业绩和前景产生重大不利影响。
我们依赖基于云的基础设施的第三方提供商来托管我们的平台。 这些第三方提供商的任何运营中断、容量限制或干扰我们的使用都可能对我们的业务、财务状况和运营结果产生不利影响。
我们将与我们的托管平台相关的几乎所有技术基础设施外包给第三方托管服务,如Google Cloud 和Amazon Web Services(简称AWS)。我们无法控制这些第三方中的任何一方,虽然我们试图通过最大限度地减少对任何第三方或其运营的依赖来降低风险,但我们不能保证此类第三方提供商不会 经历系统中断、停机或延迟或性能下降。我们需要能够随时访问我们的计算平台,而不会中断或降低性能。我们的托管平台依赖于 通过维护第三方托管服务托管的虚拟云基础架构的配置、架构、功能和互连规范,以及保护存储在这些虚拟数据中心中的信息(由第三方互联网服务提供商传输)来保护第三方托管服务托管的虚拟云基础架构。我们已经经历过,并预计在未来,由于各种 因素,包括基础设施更改、人为或软件错误、网站托管中断和容量限制,我们可能会再次遇到服务和可用性方面的中断、延迟和中断。对我们第三方托管服务容量的任何限制都可能对我们的业务、财务状况、 和运营结果产生不利影响。此外,任何可能由网络攻击、自然灾害、火灾、洪水、严重风暴、地震、断电、电信故障、恐怖或其他攻击引起的影响我们第三方托管服务基础设施的事件, 而我们无法控制的其他破坏性事件可能会对我们的基于云的解决方案产生负面影响。影响我们基于云的解决方案的长期服务中断可能会损害我们的声誉或损害我们的业务 。我们还可能因使用替代设备或采取其他行动来准备或应对损害我们使用的第三方托管服务的事件而招致巨额费用。
如果我们与第三方托管服务的服务协议终止,或者出现服务中断、我们使用的服务 或功能取消、互联网服务提供商连接中断或此类设施损坏的情况,我们可能会遇到访问我们平台的中断,以及在安排或 创建新设施和服务和/或重新架构我们的托管软件解决方案以部署到其他云基础设施服务提供商时的重大延迟和额外费用,这可能会对我们的业务产生不利影响, 财务状况
如果我们的安全措施遭到破坏或以其他方式获得对我们其他数据的未经授权访问,我们的 数据可能被视为不安全,我们可能会承担重大责任。
我们使用一套专有工具来生成、分析、 并从我们的数据中获得新的见解。因此,由于第三方行为、员工或承包商的错误、渎职或其他原因导致的对我们数据的未经授权的访问或安全漏洞可能导致信息丢失或损坏,或 其他信息损害、索赔和诉讼、赔偿义务、我们的声誉损害以及其他责任。我们的合作者和与我们合作的其他第三方可能也会遭遇我们所依赖的类似数据安全漏洞。 因为用于获取未经授权访问或破坏系统的技术经常变化,通常在针对目标启动之前无法识别,因此我们和我们的合作伙伴可能无法预料到这些技术 或实施足够的预防措施。此外,如果我们的员工或承包商未能遵守惯例
41
我们已经在内部药物发现团队和与外部人员(包括我们的合作者)合作的团队之间建立了防火墙,或者如果我们采用的维护防火墙故障的技术解决方案 出现故障,我们的合作者可能会对我们为其知识产权保密的能力失去信心,我们可能难以吸引新的合作者,我们可能会违反我们的合作者的合同索赔 ,因此我们可能会遭受声誉和其他损害。任何或所有这些问题都可能导致声誉损害或使我们面临第三方诉讼或其他诉讼或责任,这可能会 对我们的经营业绩产生不利影响。我们的保险可能不足以覆盖与此类事件相关的损失,而且在任何情况下,此类保险可能不会涵盖我们为应对和 补救安全漏洞而可能招致的所有类型的成本、费用和损失。有关更多信息,请参阅?我们的业务和运营的风险因素?如果发生计算机系统故障、网络攻击或我们或第三方的网络安全缺陷,我们的业务和运营将受到影响。
我们的解决方案使用第三方开源软件,任何不遵守一个或多个此类开源软件许可证条款的行为都可能 对我们的业务产生不利影响,使我们受到诉讼,或产生潜在的责任。
我们的解决方案包括由第三方 在任何一个或多个开源许可证(包括Apache 2.0许可证、MIT、BSD变体和其他许可证)下授权的软件,我们希望在未来继续将开源软件纳入我们的解决方案中。此外,我们不能确保我们 已有效监控我们对开源软件的使用,或验证了此类软件的质量或来源,也不能确保我们遵守适用的开源许可证的条款或我们当前的政策和程序。已有 针对在其产品和服务中使用开源软件的公司提出索赔,声称使用此类开源软件侵犯了索赔人的知识产权。因此,我们可能会受到 第三方的诉讼,声称我们认为获得许可的开源软件侵犯了这些第三方的知识产权。此外,如果分发此类开源软件的作者或其他第三方 声称我们未遵守其中一个或多个许可证的条件,我们可能被要求针对此类指控招致巨额法律费用,并可能遭受重大损害,并需要遵守 这些解决方案的繁琐条件或限制,这可能会扰乱这些解决方案的分发和销售。诉讼可能会让我们付出高昂的辩护费用,对我们的业务、财务状况和 运营结果产生负面影响,或者需要我们投入额外的研发资源来更改我们的解决方案。此外,这些第三方开源提供商可能会经历服务中断、数据丢失、隐私泄露、网络攻击, 以及与其提供的应用程序和服务相关的其他 事件,这些事件可能会降低这些服务的效用,并可能因此损害我们的业务。
使用开源软件可能会带来比使用第三方商业软件更大的风险,因为开源许可方通常不会就侵权索赔或代码质量提供 担保或其他合同保护,包括在开源软件可能更容易受到影响的安全漏洞方面。此外,某些开源许可证 要求免费向公众提供与此类开源软件交互的软件程序的源代码,并且对此类开源软件的任何修改或衍生作品继续按照与开源软件许可证相同的 条款进行许可。我们所受的各种开源许可证的条款尚未由相关司法管辖区的法院解释,而且此类许可证的解释方式可能会对我们营销或提供软件和数据的能力施加意想不到的条件或限制 。根据某些开放源码许可的条款,如果我们以某种方式将我们的专有软件与开放源码软件相结合,我们可能被要求发布我们专有软件的源代码,并使 我们的专有软件在开放源码许可下可用。如果我们的专有软件的某些部分被确定受开放源代码许可证的约束,我们可以
42
需要公开发布我们的源代码的受影响部分,重新设计我们的全部或部分解决方案,或者以其他方式限制我们解决方案的许可 ,每一项都可能降低或消除我们解决方案的价值。披露我们的专有源代码可以让我们的竞争对手以更少的开发工作量和时间创建类似的产品,最终可能会 导致销售损失。此外,任何此类重新设计或其他补救措施都可能需要大量额外的研发资源,而我们可能无法成功 完成任何此类重新设计或其他补救措施。任何这些事件都可能对我们造成责任并损害我们的声誉,这可能会对我们的收入、业务、 经营业绩、财务状况和我们股票的市场价格产生实质性的不利影响。
与我们的运营/商业化相关的风险
我们的保险单很贵,而且只能保护我们免受一些商业风险的影响,这让我们承担了大量未投保的责任。
我们没有为我们的业务可能遇到的所有类别的风险投保,而且保险范围变得越来越昂贵。以 为例,我们只能为我们的数据损失购买保险,这将部分补偿我们的损失。我们不知道我们将来是否能够保持现有保险的承保水平,而且我们将来获得的任何责任 保险覆盖范围可能不足以补偿我们可能遭受的任何费用或损失。如果我们或我们的合作者可能开发的任何候选药物获得市场批准,我们打算购买包括商业产品销售在内的 保险,但我们可能无法以商业合理的条款或足够的金额获得此类保险。我们的保单目前维持的承保范围或承保范围限制 可能不够充分。如果我们的损失超出了我们的保险范围,我们的财务状况将受到不利影响。我们任何候选药物的临床试验或监管审批都可能被暂停,这可能会对我们的 运营和业务结果产生不利影响,包括阻止或限制我们或我们的合作伙伴可能确定的任何候选药物的开发和商业化。此外,作为上市公司运营将使我们获得董事和高级管理人员责任保险的成本更高 。如果我们没有足够的董事和高级管理人员责任保险,我们可能更难吸引和留住合格的人员加入我们的 董事会。
流行病、流行病或传染性疾病(如新冠肺炎)的爆发可能会对我们的业务和财务业绩产生实质性的不利影响 ,并可能中断我们候选药物的开发。
大流行或类似疫情等公共卫生危机 可能会对我们的业务造成不利影响。2020年初,一种名为SARS-CoV-2导致新冠肺炎的冠状病毒已经蔓延到全球大多数国家和美国所有50个州,包括犹他州,特别是盐湖城,我们的主要办公室和实验室就位于盐湖城。冠状病毒大流行正在演变,到目前为止已经导致实施了各种应对措施,包括政府强制实施的隔离、旅行限制和其他公共卫生安全措施。冠状病毒对我们的运营或我们第三方合作伙伴(包括我们的临床前研究或临床试验运营)的影响程度 将取决于未来的发展,这些发展高度不确定,无法 有信心地预测,包括爆发的持续时间、将出现的有关冠状病毒感染严重程度的新信息,以及遏制冠状病毒或治疗其影响的行动等。新冠肺炎在全球的持续传播,或者新冠肺炎新变种的演变,更具传染性、产生更严重的影响或对治疗或疫苗具有抵抗力,可能会 对我们在美国的临床前或临床试验运营产生不利影响,包括我们招募和留住试验参与者以及主要研究人员和现场工作人员的能力,作为医疗保健提供者,他们可能
43
如果地理位置发生疫情,则增加对新冠肺炎的接触。例如,与其他生物制药公司类似,我们可能会在启动临床前和临床研究、方案偏差、登记临床试验或临床试验中给患者配药以及激活新的试验点方面遇到 延迟。新冠肺炎或任何 变体也可能影响位于受影响地区的第三方CRO的员工,我们依赖这些CRO进行临床试验。此外,由于与我们寻求在我们的试验中登记和治疗的患者的疾病相关的医疗并发症,我们的Lead和其他候选药物所针对的患者群体可能特别容易受到新冠肺炎或任何变体的影响,这可能会使我们 更难确定能够登记参加我们当前和未来临床试验的个人,并可能影响那些登记的人完成任何此类试验的能力。新冠肺炎或任何变体对 注册或我们药物试验的执行产生的任何负面影响都可能导致代价高昂的延迟,这可能会对我们获得监管部门批准并将我们的候选药物商业化的能力产生不利影响,增加我们的运营费用,并对我们的财务业绩产生重大 不利影响。
此外,是否及时登记参加计划中的临床试验取决于临床试验地点,而这些地点 可能会受到全球健康问题(如流行病)的不利影响。我们计划在目前受冠状病毒影响的地区对我们的候选药物进行临床试验。冠状病毒爆发的一些因素(br}将推迟或以其他方式对我们候选药物的临床试验以及我们的业务产生不利影响)包括:
| • | 可能将医疗资源从临床试验的实施转移到关注大流行问题, 包括作为我们临床试验研究人员的医生、作为我们临床试验地点的医院以及支持我们进行预期临床试验的医院工作人员的关注; |
| • | 对可能中断关键试验和业务活动的旅行限制,例如临床试验地点的启动和 监测、员工、承包商或患者前往临床试验地点的国内和国际旅行,包括政府实施的任何旅行限制或隔离,这些限制或隔离将影响患者、员工或 承包商前往我们的临床试验地点或获得签证或入境许可的能力或意愿面对面与潜在合作伙伴的会议和其他互动, 其中任何一项都可能延迟或对我们的预期临床试验的进行或进度产生不利影响; |
| • | 对我国第三方制造商经营的潜在负面影响; |
| • | 全球运输中断影响临床试验材料的运输,如组织样本、研究药物产品和对照药物以及我们研究中使用的其他供应;以及 |
| • | 潜在的工作场所、实验室和办公室关闭以及对员工在家工作的依赖增加而导致的业务中断 、正在进行的实验室实验和操作中断或延迟、人员短缺、差旅限制或公共交通中断,任何这些都可能对我们的业务运营产生不利影响,或推迟与当地监管机构、道德委员会和其他重要机构和承包商进行必要的 互动。 |
我们已采取临时 预防措施,旨在帮助将冠状病毒对员工的风险降至最低,包括暂时允许某些员工远程工作、暂停员工在全球范围内的所有非必要旅行 以及不鼓励员工参加行业活动和与工作相关的面对面会议,这可能会对我们的业务产生负面影响。我们目前无法预测 企业和政府机构(如美国证券交易委员会(Securities And Exchange Commission)、美国证券交易委员会(SEC)或美国食品和药物管理局(FDA))计划或潜在关闭或中断的范围和严重程度。
44
冠状病毒引起的这些因素和其他因素可能会在已经感染冠状病毒的国家恶化,或者可能继续传播到其他国家。上述任何因素,以及与任何此类不可预见的中断相关的其他因素,都可能对我们的业务以及我们的运营结果和财务状况产生重大不利影响 。此外,围绕这些和相关问题的不确定性可能会对美国和其他经济体的经济造成不利影响,这可能会影响我们筹集开发候选药物并将其商业化所需资金的能力。
如果我们不能充分管理和改进我们的技术硬件基础设施,我们可能会遇到错误、延迟和 其他性能问题。
我们的硬件 基础设施支持的数据和软件工具的复杂性显著增加。此外,我们需要适当地管理和改进我们的技术硬件基础设施,以支持硬件和软件参数的变化以及我们工具的发展。我们已经并可能在未来经历我们的软件工具或硬件基础设施的中断、停机、故障和其他性能问题。这些类型的问题可能由多种因素引起,包括基础设施更改、人为因素、 机械或软件错误、病毒、安全攻击和欺诈。在某些情况下,我们可能无法在可接受的时间内或根本无法确定这些问题的一个或多个原因。如果我们不能准确预测和识别我们的基础设施要求和故障,包括采购较新的基础设施,我们的团队可能会遇到性能问题,这可能会导致我们的研发计划延迟,这可能会对我们的业务、财务状况、运营结果和前景产生不利影响。
即使我们开发的任何候选药物获得市场批准,它们也可能无法获得医生、患者、医疗保健付款人和医学界其他人对商业成功所必需的 程度的市场接受度。
我们候选药物的商业成功将取决于他们被医生、患者、第三方付款人和医学界其他人 接受的市场程度。即使我们可能开发的任何候选药物获得市场批准,它们也可能无法获得医生、患者、医疗保健付款人和医学界其他人的足够市场接受。如果我们开发的任何候选药物获准用于商业销售,其市场接受度将取决于许多因素,包括:
| • | 这些候选药物的有效性和安全性,在关键的临床试验中得到证明,并发表在同行评审的 期刊上; |
| • | 与替代治疗(包括任何类似的非专利治疗)相比的潜在优势和感知优势; |
| • | 能够以有竞争力的价格出售这些产品; |
| • | 能够提供适当的患者访问计划,例如自付 帮助; |
| • | 与替代疗法相比,给药和给药的方便性和简便性; |
| • | 候选药物获得FDA或类似监管机构批准的临床适应症; |
| • | FDA或其他类似外国监管机构的产品标签或产品插入要求,包括 产品批准标签中包含的任何限制、禁忌或警告; |
| • | 对产品分销方式的限制; |
| • | 竞争产品投放市场的时机; |
45
| • | 有关该等产品或竞争产品及治疗方法的宣传; |
| • | 营销和分销支持的实力; |
| • | 有利的第三方承保范围和充足的报销;以及 |
| • | 任何副作用或不良事件的流行率和严重程度。 |
医疗产品的销售还取决于医生开这种疗法的意愿,这很可能是基于 这些医生确定产品是安全的、治疗有效的和具有成本效益的。此外,将产品纳入或排除在不同医师团体制定的治疗指南中以及有影响力的 医师的观点可能会影响其他医师开出治疗处方的意愿。我们无法预测医生、医生组织、医院、其他医疗保健提供者、政府机构或私人保险公司是否会确定 与竞争疗法相比,我们可能开发的任何产品都是安全的、治疗有效的和经济实惠的。如果我们开发的任何候选药物没有达到足够的接受度,我们可能不会产生显著的产品 收入,也可能无法盈利。
如果在未来,我们无法建立销售和营销能力,或无法与第三方 达成协议来销售和营销我们可能开发的任何候选药物,如果这些候选药物获得批准,我们可能无法成功将其商业化。
我们没有销售或营销基础设施,在医药产品的销售、营销或分销方面几乎没有经验。要使我们保留销售和营销职责的任何已批准产品取得商业成功,我们必须开发一个销售和营销组织、销售和营销软件解决方案,或者将这些功能外包给第三方 。将来,如果我们的候选药物获得批准,我们可能会选择建立一个集中的销售、营销和商业支持基础设施来营销和销售我们的候选药物。我们还可以选择与第三方建立合作或战略 合作伙伴关系,以参与特定候选药物、适应症或地理区域(包括美国以外的区域)的商业化活动,尽管不能保证我们能够 达成这些安排,即使我们的意图是这样做。
建立我们自己的商业能力以及与第三方达成执行这些服务的安排都存在风险。例如,招聘和培训销售人员或报销专家既昂贵又耗时,可能会推迟任何产品的发布。如果我们招聘销售人员并建立营销和其他商业化能力的候选药物的商业发布 因任何原因而延迟或没有发生,我们将过早或不必要地产生这些 商业化费用。这可能代价高昂,如果我们不能留住或重新定位商业化人员,我们的投资将会损失。
可能会阻碍我们将任何经批准的产品自行商业化的因素包括:
| • | 无法招聘和留住足够数量的有效销售、营销、报销、客户服务、医疗事务和其他支持人员; |
| • | 销售人员或软件工具无法接触医生或说服足够数量的医生开出任何未来批准的产品; |
| • | 报销专业人员无法协商付款方获取处方、报销和其他 承兑的安排; |
| • | 无法以足够的价位为产品定价,以确保足够和有吸引力的盈利水平; |
46
| • | 分销渠道受限或封闭,难以将我们的产品分销给部分患者 ; |
| • | 缺乏销售人员提供的补充产品,这可能使我们相对于拥有更广泛产品线的公司处于竞争劣势 ;以及 |
| • | 与创建独立的商业化组织相关的不可预见的成本和费用。 |
如果我们与第三方达成协议来执行销售、营销、商业支持和分销服务,我们的 产品收入或产品收入的盈利能力可能会低于我们在内部开发的任何产品的营销和销售。此外,我们可能无法成功地与第三方达成将我们的候选药物商业化 的安排,或者可能无法以对我们或他们有利的条款这样做。我们可能无法控制此类第三方,其中任何一方可能无法投入必要的资源和注意力有效地销售和营销我们的产品 ,或者我们可能因不遵守有关处方药产品销售和推广的监管要求和限制(包括那些限制标签外促销的要求和限制)而面临法律和监管风险。如果我们不能成功地建立商业化能力,无论是我们自己还是与第三方合作,如果获得批准,我们将无法成功地将我们的候选药物 商业化。
随着我们药物开发渠道的增加和成熟,我们的 设施和第三方对临床和商业供应的需求增加可能会影响我们的运营能力。我们将需要增加我们整个供应链的产能。此外,我们依赖许多服务提供商,包括那些提供制造或测试服务的服务提供商,所有这些服务提供商在运营中都存在可能对我们的运营产生不利影响的固有风险。
我们目前并将继续 利用第三方制造原材料、组件、零部件和消耗品,并执行质量测试,包括为我们的自动化机器人平台提供此类材料。如果技术支持的药物 发现领域继续扩大,我们可能会遇到对这些材料和服务的日益激烈的竞争。对第三方制造或测试设施的需求增长速度可能快于其现有产能,这可能会破坏我们 找到和保留能够生产足够数量的候选药物所需的此类原材料、组件、部件和消耗品的第三方供应商和制造商以及维护我们的自动化机器人平台的能力。 服务提供商和供应商的使用可能会使我们面临风险,包括但不限于:
| • | 以 方式或在对我们造成代价或损害的时间终止或不续签与第三方的供应和服务协议; |
| • | 这些供应商和服务提供商的运营中断是由与我们的业务或 运营无关的条件造成的,包括供应商或服务提供商破产或不可抗力事件,如新冠肺炎疫情;以及 |
| • | 监管机构对第三方设施的检查可能会产生负面结果,并导致延迟 或终止他们满足我们要求的能力。 |
我们的自动化机器人平台面临的其他风险包括依赖第三方设备和仪器供应商以及消耗品和试剂供应商。第三方供应商未能满足我们的需求可能会对我们继续运营我们的药物发现平台并产生新的 洞察力以获得成功候选药物的能力产生不利影响。
47
我们面临与我们内部设施和外部服务提供商的物理和数字基础设施相关的监管和运营风险。 我们的内部设施和外部服务提供商的设施都存在与此相关的监管和运营风险。
我们在犹他州盐湖城的设施没有经过任何监管机构的审查或预先批准,也没有经过任何联邦监管机构(如FDA)的检查。FDA的检查可能会破坏我们生成数据和开发候选药物的能力 。我们的实验室设施旨在将设备的高度自动化与多个数字系统集成在一起,以提高研究工作的效率。我们尝试实现相对于行业标准的研究操作的高水平数字化 。虽然这旨在提高运营效率,但由于内部或 外部因素(包括但不限于设计问题、系统兼容性或潜在的网络安全漏洞),可能会带来额外的设备故障风险,甚至整个系统故障或停机。这可能会导致潜在候选药物识别的延迟或我们设施的关闭。我们数据生成能力的任何中断都可能导致将新的候选药物推入我们的流水线、推进现有计划或增强我们平台的功能(包括扩展我们的数据)的延迟 如果发生这种情况,可能会对我们的业务、财务状况、运营结果和前景产生重大的不利影响。
未来,我们可能会在我们的设施中生产用于临床前和临床使用的药物物质或产品,而我们之前的生产经验有限。
如果我们在未来决定生产 种药物或产品,我们将没有在我们的设施中生产用于临床前和临床使用的经验。我们可能会延迟实施设施的全面运营状态,导致临床前或 临床供应延迟,或者需要依赖第三方服务提供商,从而导致计划外费用。
随着我们扩大开发和商业产能 ,我们可能会在盐湖城区域内建立制造能力,或者扩展到其他地点或地理位置,这可能会导致监管延迟或成本高昂。如果我们不能选择正确的地点,以高效的方式完成 建设,招聘适当的人员,并总体上有效地管理我们的增长,我们的研究药物的开发和生产可能会延迟或减少。 如果我们制造流程的更改导致工厂基础设施发生所需的更改,则可能需要额外投资。
我们目前的业务位于犹他州和加利福尼亚州;我们或我们所依赖的第三方可能会受到自然灾害的不利影响,我们的业务连续性和灾难恢复计划可能无法充分保护我们免受严重灾难的影响。
我们目前的业务位于犹他州盐湖城和加利福尼亚州米尔皮塔斯。任何计划外事件,如洪水、火灾、爆炸、地震、 极端天气条件、医疗流行病,包括当前新冠肺炎全球传播的任何潜在影响、电力短缺、电信故障或其他自然或人为事故或事件,导致我们无法充分利用我们的设施,或我们第三方合同制造商的制造设施,都可能对我们的业务运营能力产生实质性和不利影响,并对我们的财务和运营状况产生重大负面影响。无法使用这些设施可能会导致成本增加、我们候选药物的开发延迟或 我们的业务运营中断。新冠肺炎疫情等自然灾害或流行病可能会进一步扰乱我们的运营,并对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。例如,我们为非必要办公室人员制定了临时在家工作政策,这可能会对我们业务计划和运营的执行 产生负面影响,特别是因为我们依赖于在湿实验室中验证某些药物发现生物学。此外,我们潮湿的实验室里有机器人用来
48
生成我们构建递归数据宇宙的数据集,这是我们进行候选药物发现的关键手段。如果发生自然灾害、停电或其他事件, 使我们无法使用GPU群集所在的全部或大部分总部或数据中心,或损坏关键基础设施或我们的机器人(如我们的研究设施或我们 第三方合同制造商的制造设施),或者以其他方式中断运营,我们可能很难(在某些情况下甚至不可能)在相当长的一段时间内继续我们的业务。我们现有的灾难恢复和业务连续性计划 可能不足以应对严重灾难或类似事件。此外,我们没有与化学相关的系统的灾难恢复和业务连续性计划。由于我们的灾难恢复和业务连续性计划的性质有限,我们可能会产生巨额费用,这可能会对我们的业务产生实质性的不利影响。作为我们风险管理政策的一部分,我们将保险范围维持在我们认为适合我们业务的水平 。然而,一旦这些设施发生意外或事故,我们不能向投资者保证保险金额足以弥补任何损害和损失。如果我们的设施或我们第三方合同制造商的制造 设施因事故或事件或任何其他原因而无法运行,即使是在很短的时间内,我们的任何或所有研发项目都可能受到损害。任何业务中断 都可能对我们的业务、财务状况、运营结果和前景产生重大不利影响。
此外,我们在犹他州盐湖城的设施位于繁华的市中心。虽然我们相信我们已经采取了必要的步骤来确保我们的运营对周围地区是安全的,但如果我们在我们的设施中进行 危险物质研究,包括使用易燃化学品和材料,可能会给公众带来风险。到目前为止,我们没有收到任何与我们的行动有关的公众投诉。我们还不时在盐湖城的设施中举办公共活动。我们已经制定了协议来保护我们的设施以及其中的机密信息和资产;但是,很难保护我们设施的某些部分,我们机密信息的安全性和 专有信息可能会受到损害。尽管我们已经采取了这些措施,但周围的社区可能仍然认为我们的设施不安全,这可能会对我们的声誉和运营产生实质性的不利影响。
不利的全球经济状况可能会对我们的业务、财务状况或经营业绩产生不利影响。
我们的经营业绩可能会受到全球经济和全球金融市场总体状况的不利影响。例如,在 2008年,全球金融危机导致资本和信贷市场极度波动和中断,而当前的新冠肺炎疫情在美国和 国际市场造成了极大的波动和不确定性。严重或长期的经济低迷可能会给我们的业务带来各种风险,包括对我们候选药物的需求减弱,以及在需要时以可接受的条件筹集额外资金的能力受损(如果有的话)。经济疲软或下滑也可能给我们的供应商带来压力,或者可能导致供应中断。上述任何一项都可能损害我们的业务,我们无法预见当前的经济环境和金融 市场状况可能对我们的业务产生不利影响的所有方式。
当前和未来针对我们的诉讼可能在我们的正常业务过程中发生, 辩护可能代价高昂且耗时。
我们会定期收到在正常业务过程中出现的索赔,例如 我们的合作者或供应商提出的与商业纠纷相关的索赔,我们现任或前任员工提出的雇佣索赔,或第三方因未能充分保护其个人数据而提出的索赔。第三方 未来可能主张对我们的业务重要的技术的知识产权,并要求退还版税或要求我们许可
49
他们的技术。诉讼可能会导致巨额成本,并可能分散管理层的注意力和资源,这可能会严重损害我们的业务、整体财务状况和 经营业绩。保险可能不包括此类索赔,可能不足以支付一项或多项此类索赔,并且可能不会继续以我们可以接受的条款提供保险。向我们提出未投保或保险不足的索赔可能导致 意外成本和管理分心,对我们的业务、财务状况和运营结果产生负面影响。
如果我们不遵守 环境、健康和安全或其他法律法规,我们可能会受到罚款或处罚,或者产生成本,这可能会对我们的业务成功产生实质性的不利影响。
我们受到许多环境、健康和安全以及其他法律法规的约束,包括管理实验室程序以及危险材料和废物的处理、使用、储存、处理和处置的法律法规。我们的行动涉及使用危险和易燃材料,包括化学品、生物和放射性材料。我们的业务还会产生 危险废物产品。我们通常与第三方签订合同,处理这些材料和废物。我们无法消除这些材料造成污染或伤害的风险。如果因使用危险材料而造成污染或伤害,我们可能要对由此造成的任何损害负责,并且任何责任都可能超出我们的资源范围。我们还可能招致与民事或刑事罚款和处罚相关的巨额费用。
尽管我们维持工人补偿保险,以支付因使用危险材料而导致员工受伤而可能产生的成本和开支,但该保险可能不足以承担潜在责任。我们不为可能因我们 储存或处置生物、危险或放射性材料而对我们提出的环境责任或有毒侵权索赔提供保险。
我们利用净营业亏损结转和某些其他税收 属性的能力可能有限。
根据修订后的1986年《国税法》(Internal Revenue Code Of 1986)第382条或该法规,如果一家公司经历了所有权变更(通常定义为在三年期间股权所有权按价值变化超过50%),我们使用变更前净营业亏损结转和某些变更前 税收属性抵销变更后收入的能力可能受到每年的限制。(注:根据《税法》修订本),如果一家公司发生所有权变更(通常定义为在三年内其股权所有权按价值变化超过50%),我们使用变更前净营业亏损结转和某些变更前 税属性来抵消变更后收入的能力可能受到年度限制。这一年度限制可能导致在使用前结转的部分净营业亏损到期。如果不使用,结转的 将于2036年开始过期。我们过去可能经历过此类所有权变更,未来可能会因为此次发行或随后的股票所有权变更而经历所有权变更,其中一些变更不在我们的控制范围内;但是,我们尚未确定是否发生了所有权变更。截至2020年12月31日,我们有大约 万美元的联邦净营业亏损结转,我们利用这些净营业亏损结转的能力可能会受到颁布的法律或上文所述的所有权变更 的限制,这可能会导致我们的纳税义务增加。
如果我们对关键会计政策的估计或判断被证明是不正确的,或者财务报告标准或解释发生变化,我们的运营结果可能会受到不利影响。
按照美国公认会计原则或美国公认会计原则编制财务报表时,管理层需要做出估计和假设,以影响合并财务报表和附注中报告的金额 。我们的估计基于历史经验、已知趋势和事件,以及我们认为在这种情况下合理的各种其他因素,如 所述
50
管理层对财务状况和运营结果的讨论和分析涉及关键会计政策和估算的使用。这些估算的结果构成了对资产和负债账面价值做出判断的基础,而这些资产和负债的账面价值从其他来源看不是很明显。编制合并财务报表时使用的重要假设和估计包括基于股票的薪酬和对我们在早期生物技术公司的股权投资的估值。 如果我们的假设发生变化或实际情况与我们的假设不同,我们的运营结果可能会受到不利影响,这可能会导致我们的运营结果低于证券分析师和投资者的预期,从而导致我们普通股的交易价格下降。
此外,我们还定期监控我们对适用财务报告标准的遵守情况,并审查 与我们相关的新声明和草案。由于新准则、现有准则的变化及其解释的变化,我们可能需要更改我们的会计政策,改变我们的运营政策,并实施新的或增强现有的 系统,以便它们反映新的或修订的财务报告准则,或者我们可能需要重新陈述我们发布的财务报表。对现有标准的此类更改或对其解释的更改可能会对我们的声誉、业务、财务状况和利润产生不利影响。
与我们对第三方的依赖相关的风险
我们预计将依赖第三方进行我们的临床试验以及我们的研究和临床前测试的某些方面,而这些第三方可能无法令人满意地执行 ,包括无法在截止日期前完成此类试验、研究或测试。
我们目前依赖并预计 将继续依赖第三方(如临床研究组织、临床数据管理组织、医疗机构和临床研究人员)进行某些方面的研究、临床前测试和临床试验。 这些第三方中的任何一方都可能终止与我们的合约或无法履行其合同义务。如果我们与这些第三方的任何关系终止,我们可能无法以商业上合理的条款与备选 第三方达成安排,或者根本无法达成安排。如果我们需要达成替代安排,就会延误产品开发活动。
我们对这些第三方的研发活动的依赖减少了对这些活动的控制,但并不能减轻我们的 责任。例如,我们仍有责任确保我们各自的临床试验都按照试验的一般研究计划和方案以及适用的法律、法规和科学标准进行,并且我们对第三方的依赖不会减轻我们的监管责任。此外,FDA和类似的外国监管机构要求在进行、记录和报告临床试验结果时遵守良好的临床实践或GCP指南 ,以确保数据和报告的结果可信、可重复性和准确性,并保护试验参与者的权利、完整性和机密性。 监管机构通过定期检查试验发起人、主要研究人员和试验地点来执行GCP合规性。如果我们或这些第三方中的任何一方未能遵守适用的GCP规定,在我们的临床试验中生成的部分或全部临床 数据可能被认为是不可靠的,FDA或类似的外国监管机构可能会要求我们进行额外的非临床或临床试验,或者在批准我们的 上市申请之前招募更多的患者。我们不能确定,在检查之后,这些监管机构是否会确定我们的临床试验是否符合GCP规定。在进行临床试验期间任何违反法律法规的行为 , 我们可能会受到无标题的警告信或执法行动的影响,这些行动可能包括民事处罚,最高可达(包括刑事起诉)。我们还需要注册正在进行的临床试验,并在一定的时间范围内将 完成的临床试验结果发布到政府资助的数据库中。不这样做可能会导致罚款、负面宣传以及民事和刑事制裁。
51
如果这些第三方未成功履行其合同职责、未能在预期期限内完成或 根据法规要求或我们声明的方案进行临床试验,我们将无法或可能延迟获得我们可能开发的任何候选药物的上市批准,并且我们将无法或可能延迟我们的药物成功商业化的努力。(br}如果这些第三方不能成功履行其合同职责、未能在预期期限内完成或 根据我们规定的协议进行临床试验,我们将无法获得或可能延迟获得我们可能开发的任何候选药物的上市批准,也将无法或可能延迟我们的药物成功商业化。我们未能或这些第三方未能遵守适用的法规要求或我们声明的协议也可能使我们受到执法行动的影响。
我们与第三方签约生产我们的候选药物,用于临床前开发和临床测试,并希望继续这样做以实现 商业化。这种对第三方的依赖增加了我们无法以可接受的成本获得足够数量的候选药物或产品或此类数量的风险,这可能会延迟、阻止或损害我们的开发或 商业化努力。
我们目前不拥有或运营任何制造设施或人员,尽管我们正在 获得一个设施,以建立临床前动物研究和早期人类临床试验的生产能力。如果我们的候选药物获得上市批准,我们将依赖于并将继续依赖第三方生产我们的许多候选药物进行临床前开发和临床测试,以及我们产品的商业生产(如果我们的候选药物获得了上市批准),并且我们将继续依赖第三方生产我们的候选药物进行 临床前开发和临床测试,以及我们的产品的商业生产。这种对第三方的依赖增加了我们无法以可接受的成本或质量获得足够 数量的候选药物或产品或此类数量的风险,这可能会推迟、阻止或损害我们的开发或商业化努力。
我们的合同制造商用来生产我们的候选药物的设施必须由FDA根据批准前检查进行检查,这些检查将在我们向FDA提交营销申请后进行。在近期到中期或可能的长期内,我们不控制并将完全依赖我们的合同制造商 在生产我们的候选药物时遵守当前的良好制造规范指南或cGMP。如果我们的合同制造商不能成功 生产出符合我们的规格和FDA或其他机构严格监管要求的材料,他们将无法通过监管检查和/或保持其制造设施的监管合规性。此外,我们无法控制我们的合同制造商保持足够的质量控制、质量保证和合格人员的能力。如果FDA或类似的外国监管机构发现这些设施存在缺陷或未批准这些设施来生产我们的候选药物,或者如果它发现缺陷或在未来撤回任何此类批准,我们可能需要寻找替代生产设施,这将严重影响我们 开发、获得监管机构批准或营销我们的候选药物的能力(如果获得批准)。此外,我们或我们的第三方制造商未能遵守适用的法规可能会导致对我们实施制裁, 包括临床封存、罚款、禁令、民事处罚、延迟、暂停或撤回批准、吊销执照、扣押或召回候选药物或产品(如果获得批准)、操作限制和刑事起诉, 其中任何 都可能对我们的业务和候选药物的供应产生重大不利影响。我们的第三方制造商可能会受到第三方诉讼,这可能会扰乱我们的供应链,导致责任并损害我们的 业务,包括需要提高与未来候选药物商业化相关的价格。
我们可能无法 与第三方制造商达成任何协议,也无法以可接受的条款这样做。即使我们能够与第三方制造商达成协议,依赖第三方制造商也会带来额外的风险,包括:
| • | 依赖第三方进行监管合规和质量保证; |
| • | 第三方可能违反制造协议; |
| • | 可能盗用我们的专有信息,包括我们的商业秘密和专有技术;以及 |
52
| • | 第三方可能在代价高昂或给我们带来不便的时间终止或不续订协议。 |
我们的候选药物和我们可能开发的任何产品都可能与其他候选药物和批准的产品竞争生产设施或产能。在cGMP法规下运营的制造商数量有限,而且可能有能力为我们制造产品。
我们现有或未来制造商的任何业绩失误都可能延误临床开发或市场批准。如果我们当前的 合同制造商不能按约定执行,我们可能需要更换这些制造商。我们在确定和鉴定任何此类替代产品时可能会产生额外的成本和延迟。
我们目前和预期的未来对其他候选药物或产品生产的依赖可能会对我们未来的利润 利润率以及我们在及时和具有竞争力的基础上获得上市批准的任何产品进行商业化的能力产生不利影响。
我们还希望依赖 其他第三方为我们的临床试验储存和分发药品供应。我们的分销商的任何业绩失误都可能推迟我们可能开发的任何候选药物的临床开发或市场审批,或者 我们的药品商业化,造成额外损失,并剥夺我们潜在的产品收入。
我们在候选药物中使用的某些设备和活性药物成分的供应所依赖的第三方是我们唯一的供应来源,失去这些供应商中的任何一个都可能严重损害我们的业务。
我们在候选药物中使用的某些专用设备和活性药物成分(或原料药)是从单一来源 供应商提供给我们的。我们能否成功开发我们的候选药物,并最终提供足够数量的商业产品以满足市场需求,在一定程度上取决于我们是否有能力根据法规要求获得这些 产品的设备和原料药,并获得足够数量的临床测试和商业化产品。如果我们现有的任何此类设备或原料药供应商因任何原因停止运营,我们目前没有安排在 中提供多余或第二来源的任何此类设备或原料药。我们也无法预测不断变化的全球经济状况或潜在的全球健康问题(如新冠肺炎大流行)将如何影响我们的第三方供应商和制造商。此类事件对我们的第三方供应商和制造商的任何负面影响也可能对我们的 运营结果或财务状况产生不利影响。
对于我们所有的候选药物,我们打算在向FDA和/或MAA提交NDA和/或MAA之前,确定并确认其他供应商和制造商 提供此类设备或原料药的资格。但是,我们不确定我们的单一来源供应商是否能够满足我们对其产品的需求,这要么是因为我们与这些供应商的 协议的性质,要么是因为我们与这些供应商的有限经验,或者是因为我们作为客户对这些供应商的相对重要性。根据过去的 业绩,我们可能很难评估他们未来是否有能力及时满足我们的需求。虽然我们的供应商过去通常会及时满足我们对他们产品的需求,但他们未来可能会将我们的需求从属于他们的其他客户。
如果需要,为我们的候选药物中使用的某些设备和原料药建立额外或替换供应商可能不会很快完成 。如果我们能够找到替代供应商,该替代供应商将需要合格,并可能需要额外的监管检查或批准,这可能会导致进一步的延误。在我们努力保持充足的同时
53
我们候选药物中使用的原料药的库存、组件或材料供应的任何中断或延迟,或者我们无法以可接受的 价格从替代来源获得此类原料药,都可能阻碍、延迟、限制或阻碍我们的开发努力,这可能会损害我们的业务、运营结果、财务状况和前景。
我们可能寻求在候选药物的临床开发或商业化方面建立更多合作,如果我们不能以商业合理的条款 建立合作关系,或者根本无法建立合作关系,我们可能不得不改变我们的开发和商业化计划。
我们的产品开发 计划和候选药物的潜在商业化将需要大量额外的现金来支付费用。对于我们的一些候选药物,我们可能会决定与其他制药和生物技术公司合作 开发这些候选药物并将其商业化。在短期内,我们公司的价值将在一定程度上取决于我们创建的协作的数量和质量。
潜在的合作者可能会根据他们对我们的财务、法规或知识产权状况的评估来拒绝合作。我们 是否就协作达成最终协议将取决于我们对协作者的资源和专业知识的评估、提议协作的条款和条件以及提议的协作者对许多因素的 评估。这些因素可能包括临床试验的设计或结果、FDA或美国境外类似监管机构批准的可能性、候选药物的潜在市场、制造和向患者交付此类候选药物的成本和复杂性、竞争产品的潜力、我们对技术所有权的不确定性,如果在不考虑挑战的是非曲直以及行业和市场条件的情况下 对此类所有权提出挑战,则可能存在这种不确定性。合作者还可以考虑替代候选药物或类似适应症的技术,以供 合作,以及这样的合作是否比我们与我们合作的合作对我们的候选药物更具吸引力。我们可能建立的任何其他合作或其他安排的条款可能对我们不利。
与第三方的协作关系可能会导致我们花费大量资源,并在无法保证 财务回报的情况下招致巨大的业务风险。管理我们与协作者的关系需要:
| • | 我们的管理团队付出了大量的时间和精力; |
| • | 协调我们的营销和研发计划与合作伙伴的营销和研发重点 ;以及 |
| • | 有效地将我们的资源分配给多个项目。 |
如果我们不能在未来以对我们有利的条款建立或维持这样的战略合作关系,我们的研发努力和 创收潜力可能会受到限制。
根据协作协议,我们还可能受到限制,不能与潜在的协作者就 某些条款签订未来协议。协作的谈判和记录既复杂又耗时。此外,最近大型制药公司之间的大量业务合并导致未来潜在合作伙伴的数量减少 。
我们可能无法及时、按可接受的条款或完全按 协商更多协作。如果我们无法做到这一点,我们可能不得不削减我们正在寻求合作的候选药物的开发,减少或推迟其开发计划或我们的一个或多个
54
其他开发计划,推迟其潜在商业化或缩小任何销售或营销活动的范围,或增加我们的支出并自费进行开发或 商业化活动。如果我们选择增加自己的支出来资助开发或商业化活动,我们可能需要获得额外的资金,而这些资金可能无法按可接受的条款 或根本无法获得。如果我们没有足够的资金,我们可能无法进一步开发我们的候选药物,或者将它们推向市场并产生产品收入。即使我们成功地建立了新的合作关系,这些关系也可能永远不会 导致候选药物的成功开发或商业化或产生销售收入。我们合作安排的成功将在很大程度上取决于我们的合作者的努力和活动。协作者通常 在确定将应用于这些协作的工作和资源方面有很大的自由裁量权。在我们达成协作安排的范围内,相关产品的收入可能会低于我们直接 营销和销售产品的情况。这样的合作者还可以考虑替代候选药物或类似适应症的技术,以供合作,以及对于任何未来的候选药物,这样的合作是否会比与我们合作的合作更具吸引力。合作安排各方之间在临床开发或商业化问题上的分歧可能会导致适用候选药物的开发过程或商业化进程的延误,在某些情况下, 合作安排的终止。如果双方都没有最终决策权,这些分歧可能很难解决。与制药或生物技术公司或其他第三方的合作通常会被另一方终止或终止。任何此类终止或到期都将对我们的财务造成不利影响,并可能损害我们的商业声誉。如果我们与任何协作者卷入 仲裁或诉讼,将耗费时间,转移运营管理资源,损害我们的声誉,影响我们签订未来协作协议的能力,并可能导致我们向协作者支付巨额款项以解决任何纠纷。
与我们的知识产权有关的风险
如果我们不能充分保护和执行我们的知识产权和专有技术,或者不能获得并保持对我们的技术和产品的专利保护,或者如果获得的专利保护范围不够广泛,我们的竞争对手可能会开发和商业化与我们相似或相同的技术和产品,我们成功将我们的 技术和产品商业化的能力可能会受到损害。
我们的商业成功在一定程度上将取决于我们是否有能力为我们的候选药物获得、维护、保护和执行 我们在美国和其他国家的专利和知识产权,以及我们的核心技术,包括我们的表观平台、临床前和临床资产、物质组成、使用方法和 配方专利和相关技术。我们寻求保护我们的专有和知识产权地位,其中包括在美国和海外提交与我们的专有技术、发明和改进相关的专利申请,这些专利技术、发明和改进对我们的业务发展和实施非常重要。但是,专利过程昂贵、耗时且复杂,我们可能无法在所有司法管辖区或根本无法以合理成本及时申请我们技术和产品的某些方面的专利,而且我们获得的任何潜在专利覆盖范围可能不足以阻止实质性竞争。此外,我们还依靠商业秘密、技术诀窍和持续的技术创新来发展和保持我们的专有和知识产权地位。对于我们的某些项目,包括我们的候选产品rec-3599、治疗艰难梭菌结肠炎的领导分子(rec-163964、rec-164014和rec-164067)、治疗神经炎的领导分子(rec-648455、rec-648597和rec-648677)、治疗巴顿病的领导分子(rec-648190、rec-259618和rec-648677),我们没有任何已颁发的专利,包括我们的候选产品rec-3599、我们用于治疗艰难梭菌结肠炎的领导分子(rec-163964、rec-164014和rec-164067)、我们用于治疗巴顿病的领导分子(rec-648190、rec-259618和rec-648677)。和REC-150357),REC-64151用于治疗
55
STK11免疫检查点抗性和MYC抑制分子用于治疗实体和血液恶性肿瘤我们不能保证我们当前或未来的任何专利申请都将获得专利授权,或者任何专利授权将为我们提供任何竞争优势。
生物技术和制药公司的专利地位通常高度不确定,涉及复杂的法律和事实问题,近年来一直是许多诉讼的主题。
我们将候选药物成功商业化所需的专利保护程度在某些情况下可能无法获得或受到严格限制, 可能无法充分保护我们的权利或使我们无法获得或保持任何竞争优势。我们不能保证我们的任何未决专利申请将会发布,或者我们任何成熟为已发布 专利的未决专利申请将包括范围足以保护我们的候选药物免受竞争的权利要求。此外,外国法律可能不会像美国法律那样保护我们的权利,许多公司在美国境外建立和执行其专有权利时遇到了重大挑战。此外,专利的寿命是有限的。在美国,专利的自然失效时间通常是其第一个有效的非临时申请日之后的二十年 。可以有多种延期;然而,专利的有效期及其提供的保护是有限的。考虑到新药候选药物的开发、测试和监管审查所需的时间,保护这些候选药物的专利可能会在这些候选药物商业化之前或之后不久到期。因此,我们拥有的专利组合以及我们未来可能 许可的任何专利组合可能无法为我们提供充分和持续的专利保护,不足以阻止其他公司将与我们的候选药物相似或相同的产品商业化,包括此类产品的仿制版本。
其他方已开发出可能与我们的技术相关或具有竞争力的技术,这些方可能已提交或可能提交专利 申请,或者可能已收到或可能收到专利,要求的发明可能与我们自己的专利中要求的发明重叠或冲突。科学文献中发现的发布往往落后于实际发现,美国和其他司法管辖区的专利申请通常在提交后18个月才会发布,或者在某些情况下根本不会发布。因此,我们无法确定我们或我们的许可人是否最先提出了我们拥有或许可的专利或未决专利申请中声明的 发明,或者我们或我们的许可人是最先为此类发明申请专利保护的。因此,我们的专利权的颁发、范围、有效性、可执行性和 商业价值不能有任何确定的预测。
此外,专利起诉过程昂贵、耗时且复杂,我们可能无法以合理成本或及时提交、起诉、维护、强制执行或许可所有必要或理想的专利申请。此外,对于涵盖我们候选药物的大部分未决专利申请 ,起诉尚未开始。专利诉讼是一个漫长的过程,在此期间,最初由美国专利商标局(USPTO)提交审查的权利要求的范围可能会在发布时 大幅缩小(如果有的话)。我们也有可能无法及时识别我们的研发成果中的可申请专利的方面,从而无法获得专利保护。此外,在某些情况下,我们 无权控制专利申请的准备、提交和起诉,或维护专利,包括我们从第三方许可的技术。我们还可能需要许可方和协作者的合作,以 强制执行任何许可的专利权,而此类合作可能不会提供。因此,这些专利和申请可能不会以符合我们业务最佳利益的方式起诉和强制执行。
我们目前拥有多项美国临时专利申请。美国临时专利申请没有资格成为已颁发的专利,直到, 除其他事项外,我们提交了
56
在提交一项或多项相关临时专利申请后12个月内提出非临时专利申请。对于此类美国 临时专利申请,如果我们不及时提交任何非临时专利申请,我们可能会失去与我们的临时专利申请相关的优先日期以及对我们 临时专利申请中披露的发明的任何专利保护。此外,如果我们确实及时提交了与我们的临时专利申请相关的非临时专利申请,我们无法预测任何此类专利申请是否会导致 项专利的颁发,或者此类颁发的专利是否会为我们提供任何竞争优势。
即使我们获得了我们期望能够保持这种竞争优势的专利保护,第三方也可能会对其有效性、可执行性或范围提出质疑,这可能会导致此类专利被缩小、失效或无法强制执行。专利的颁发不像 对其发明性、范围、有效性或可执行性那样具有决定性,我们拥有和许可的专利可能会在美国和国外的法院或专利局受到挑战。例如,我们可能需要第三方将现有技术提交给 美国专利商标局,挑战我们其中一项专利中要求保护的发明的优先权,这种提交也可以在专利颁发之前提交,从而排除我们任何未决专利申请的批准。此外,在提交专利申请之前无意中 向公众披露我们的发明已经并可能在未来阻止我们在某些司法管辖区获得专利保护。我们可能会卷入异议、派生、 复审、各方间审查、授予后审查或干扰程序,挑战我们的专利权或我们从其获得此类权利许可的其他人的专利权。此类诉讼可能导致我们的专利被撤销或 修改,使其不再涵盖我们的技术或候选药物。
竞争对手可能会声称他们发明了 在我们之前颁发的专利或专利申请中声称的发明,或者可能在我们之前提交专利申请。竞争对手可能还会声称我们侵犯了他们的专利,因此,如果我们的专利发布,我们将无法实践 根据我们的专利所声称的技术。竞争对手也可以通过向专利审查员证明发明不是原创的、不是新颖的或显而易见的,来挑战我们的专利(如果颁发的话)。在诉讼中,竞争对手可能会声称,如果我们的专利(如果 颁发)出于多种原因无效。如果法院同意,我们将失去对这些受到质疑的专利的权利。
此外,在 未来,我们的前员工或顾问可能会因为他们代表我们所做的工作而主张对我们的专利或专利申请拥有所有权。虽然我们通常要求我们的所有员工、 顾问和顾问以及能够访问我们专有技术、信息或技术的任何其他第三方将其发明的类似权利转让或授予我们,但我们不能确定 我们已经与所有可能对我们的知识产权做出贡献的各方签署了此类协议,也不能确定我们与这些各方达成的协议在面临潜在挑战时是否会得到维护,或者我们不会 违反这些协议,因此我们可能没有足够的补救措施。失去全部或部分独家经营权,可能会让其他人与我们竞争,损害我们的业务。
在任何此类提交或程序中做出不利裁决可能会导致失去排他性或运营自由,或导致专利主张全部或部分缩小、无效或无法执行,这可能会限制我们阻止他人在不向我们付款的情况下使用类似或相同的技术和产品或将其商业化的能力,或者可能会限制 针对我们的技术和候选药物的专利保护期限。这样的挑战也可能导致我们无法在不侵犯第三方专利权的情况下制造或商业化我们的候选药物。此外,如果我们的专利和专利申请提供的保护的广度或强度 受到威胁,可能会阻止公司与我们合作,对当前或未来的候选药物进行许可、开发或商业化。
即使它们没有受到挑战,我们拥有的专利组合和我们未来可能许可的任何专利组合也可能不会为我们提供任何有意义的保护,也不会阻止竞争对手设计
57
围绕我们的专利主张,通过以非侵权方式开发类似或替代技术或产品来规避我们拥有或许可的专利 。例如,第三方可能开发一种具有竞争力的产品,该产品提供与我们的一个或多个候选药物相似的益处,但其成分不同,超出了我们的专利保护范围。如果我们持有或申请的针对候选药物的专利和专利申请提供的专利 保护不够广泛,不足以阻碍此类竞争,我们成功将候选药物商业化的能力可能会受到负面 影响,从而损害我们的业务。
获得和维持专利保护有赖于遵守政府专利机构提出的各种程序、文件提交、费用 支付和其他要求,如果不符合这些要求,我们的专利保护可能会减少或取消。
美国专利商标局和各种外国政府专利机构要求在专利申请和起诉过程中遵守一些程序、文件、费用支付和其他类似的 条款。此外,在专利和/或专利申请的有效期内,通常必须向美国专利商标局和 外国专利代理机构支付定期维护费、续期费、年金费和各种与专利和/或专利申请有关的其他政府费用。虽然在许多情况下,非故意失误可以通过支付滞纳金或根据适用规则通过其他方式来补救,但在 中也存在不遵守规定可能导致专利或专利申请被放弃或失效,从而导致相关司法管辖区部分或全部专利权丧失的情况。 可能导致专利或专利申请被放弃或失效的不遵守规定的事件包括但不限于:未能在规定的期限内对官方行动做出回应、不支付费用。 不遵守规定的事件包括但不限于:未在规定的期限内对官方行为做出回应、不支付费用。 可能导致放弃或完全丧失专利或专利申请的不符合规定的事件包括但不限于未能在规定的期限内对官方行动做出回应、不支付费用如果我们未能保留涵盖我们产品或程序的专利和专利申请,我们可能无法阻止 竞争对手销售与我们的候选药物相同或相似的产品,这将对我们的业务产生重大不利影响。
如果我们 无法保护我们的商业秘密和专有技术的机密性,我们的业务和竞争地位可能会受到损害。
除了专利提供的保护外,我们还依靠非专利的商业秘密保护、非专利的技术诀窍和持续的技术创新来发展和保持我们的竞争地位。关于我们的数据和小分子资料库的总体管理,我们认为商业秘密和技术诀窍是我们的主要知识产权。我们寻求通过与合作者、科学顾问、 员工和顾问签订保密协议,以及与我们的顾问和员工签订发明分配协议,来保护我们的专有技术和工艺。然而,尽管普遍存在保密协议和其他合同限制,我们可能无法阻止这些协议的各方未经授权披露或使用我们认为是机密的信息、我们的技术诀窍或其他商业秘密。监控未经授权的使用和 泄露是困难的,我们不知道我们为保护我们的专有技术而采取的步骤是否有效。如果作为这些协议当事人的任何合作者、科学顾问、员工和顾问 违反或违反任何这些协议的条款,我们可能没有足够的补救措施来弥补任何此类违反或违规行为,我们可能会因此丢失我们的商业机密。例如,如果我们的一名员工公开泄露了我们认为是机密的信息或商业秘密,我们将来可能无法对其进行保护。即使在有补救措施的情况下,强制要求当事人非法披露或挪用我们的商业秘密,就像专利诉讼一样,也是昂贵和耗时的,结果也是不可预测的。此外,美国以外的法院有时也不太愿意保护商业秘密。
否则,我们的商业秘密可能会被我们的竞争对手知道或独立发现。竞争对手可以购买我们的候选药物,并 尝试复制部分或全部
58
我们从我们的开发工作中获得的竞争优势,故意侵犯我们的知识产权,围绕我们受保护的技术进行设计,或者开发他们自己的具有竞争力的 不在我们知识产权范围内的技术。如果我们的任何商业秘密是由竞争对手或其他第三方合法获取或独立开发的,我们将无权阻止他们或 他们向其传达信息的人使用该技术或信息与我们竞争。
第三方可能会提起法律诉讼,指控我们 侵犯、挪用或以其他方式侵犯他们的知识产权或专有权利,其结果将是不确定的,并可能对我们业务的成功产生重大不利影响。
我们的商业成功取决于我们和我们的合作者在不侵犯、挪用或以其他方式侵犯第三方知识产权或专有权利的情况下开发、制造、营销和销售我们的候选药物并使用我们的专有技术的能力。生物技术和制药行业的特点是涉及专利和其他知识产权的诉讼广泛而频繁。例如,我们从获得许可的供应商处获得CRISPR-Cas9基因编辑技术的再许可,该技术提供了我们的药物发现流程所依赖的关键工具,但 第三方之间关于此类技术的所有权和许可权的争议仍在持续,我们并不是其中一方。CRISPR-Cas9基因编辑是一个专利申请非常活跃的领域。2018年11月, 据报道,全球211个专利家族和1835个专利家族成员在标题、摘要或权利要求中引用了CRISPR或CA。与CRISPR和CA相关的大量专利申请使我们很难全面评估可能涵盖CRISPR-CAS9的相关专利和未决申请的范围 。未来可能会有第三方专利或具有权利要求的未决专利申请,涵盖我们对CRISPR-CAS9的使用。我们可能需要访问 中的此类专利才能继续使用CRISPR-Cas9,但我们不能确定此类专利是否可按商业合理的条款进行许可。我们未来可能会参与或威胁与我们的候选药物和技术有关的知识产权方面的对抗性诉讼或诉讼 ,包括向美国专利商标局提起的干扰诉讼。我们的竞争对手或其他第三方可能会对我们提出侵权索赔。, 声称我们的 产品或技术受其专利保护。鉴于我们技术领域的专利数量庞大且不断增加,我们不能确定我们没有侵犯现有专利,或者我们不会侵犯未来可能授予的专利 。许多公司已经提交并将继续提交与人工智能和深度学习、技术辅助药物发现、CRISPR、高通量筛选以及所有这些领域的组合相关的专利申请。这些专利申请中,有些已经被批准或发布,另一些可能在未来发布。由于这些领域竞争激烈,制药和生物技术公司对此兴趣浓厚,因此未来可能会 提交更多专利申请和授予更多专利,以及预计未来会有更多研发项目。如果专利持有人认为我们的产品或候选药物侵犯了其专利, 即使我们的技术已获得专利保护,专利持有人也可以起诉我们。此外,我们可能会面临非执业实体的专利侵权索赔,这些实体没有相关的产品收入 ,因此我们拥有的专利组合和我们未来可能许可的任何专利组合可能不会对这些实体产生威慑作用。如果针对我们、我们的合作者或我们的第三方服务提供商提出任何此类索赔或诉讼,我们的 开发、制造、营销、销售和其他商业化活动也可能受到类似的不利影响。即使我们认为第三方知识产权索赔没有法律依据,也不能保证法院会在侵权、有效性、可执行性等问题上裁定 对我们有利, 或优先权。有管辖权的法院可以裁定针对我们主张的第三方专利是有效的、可强制执行的和被侵犯的,这可能会对我们开发、制造、营销、销售和商业化我们的任何候选药物或技术的能力造成实质性和不利的 影响。为了在联邦法院成功挑战任何此类美国专利的有效性,我们需要克服 有效性的推定。因为这个负担很重,需要我们提出清楚和
59
关于任何此类美国专利主张无效的令人信服的证据,不能保证有管辖权的法院会宣布任何此类美国专利的主张无效。
如果我们被发现侵犯了第三方的专利或其他知识产权,我们可能需要从该第三方 获得许可证,才能继续开发和营销我们的候选药物和技术。我们可以选择获得许可,即使在没有提起诉讼或发现侵权的情况下也是如此。在任何一种情况下,我们都可能无法以商业上合理的条款或根本无法获得任何所需的许可证。即使我们能够获得这样的许可,它也可以以非独家条款授予,从而使我们的竞争对手和其他第三方能够访问向我们许可的相同 技术,这可能需要我们支付大量许可、版税和其他费用。如果没有这样的许可证,我们可能会被迫(包括法院命令)停止开发和商业化侵权技术或候选药物 。此外,如果我们被发现故意侵犯此类第三方专利或其他知识产权,我们可能会被判承担金钱损害赔偿责任,包括三倍损害赔偿和律师费。如果发现 侵权,可能会阻止我们将候选药物商业化,或者迫使我们停止部分业务运营,这可能会对我们的业务造成实质性损害。如果我们在外国专利诉讼中败诉,声称我们侵犯了 竞争对手的专利,我们可能会被阻止在一个或多个外国销售我们的产品,这将对我们的业务产生实质性的不利影响。
如果我们或我们的员工错误使用或披露竞争对手的所谓商业秘密,或 违反了与竞争对手的竞业禁止或竞标协议,或声称拥有我们视为自己的知识产权,我们可能会受到损害。
我们未来可能会受到指控,称我们或我们的员工无意中或以其他方式使用或泄露了所谓的商业机密 或前雇主或竞争对手的其他专有信息。尽管我们尽力确保我们的员工和顾问在为我们工作时不使用他人的知识产权、专有信息、技术诀窍或商业秘密,但我们未来可能会被指控导致员工违反其竞业禁止协议或 竞标协议的条款,或者我们或这些个人无意或以其他方式使用或披露了前雇主或竞争对手所谓的商业秘密或其他专有信息。 可能有必要提起诉讼以进行辩护。 为了辩护,我们或这些个人可能会被指控使用或披露前雇主或竞争对手的所谓商业秘密或其他专有信息。 为了辩护,我们可能需要提起诉讼。 我们或这些个人可能会无意中或以其他方式使用或披露前雇主或竞争对手的所谓商业秘密或其他专有信息。 即使我们成功地对这些索赔进行了辩护,诉讼也可能导致巨额成本,并可能分散管理层的注意力。如果我们对这些索赔的辩护失败,除了要求我们支付金钱损害赔偿外,法院还可以禁止我们使用对我们的候选药物至关重要的技术或功能,前提是这些技术或功能被发现包含或源自前雇主的商业秘密 或其他专有信息。如果不能整合这些技术或功能,将对我们的业务产生实质性的不利影响,并可能阻碍我们成功地将候选药物商业化。此外,我们可能会因此类索赔而失去宝贵的知识产权或人员。此外,任何此类诉讼或其威胁都可能对我们雇用员工或与独立销售代表签订合同的能力产生不利影响 。关键人员或他们的工作成果的流失可能会阻碍或阻碍我们将候选药物商业化的能力。, 这将对我们的业务、经营业绩和财务状况产生不利影响。
此外,虽然我们的政策是要求可能参与知识产权构思或开发 的员工和承包商执行将此类知识产权转让给我们的协议,但我们可能无法与实际上构思或开发我们视为自己的知识产权的每一方执行此类协议。 知识产权转让可能不是自动执行的,或者转让协议可能被违反,我们可能被迫向第三方提出索赔,或为他们可能对我们提出的索赔进行抗辩,以确定我们 视为我们的知识产权的所有权。此类索赔可能会对我们的业务、运营结果和财务状况产生不利影响。
60
我们可能会卷入保护或强制执行我们的专利和其他知识产权的诉讼中,这可能是昂贵、耗时且不成功的 。
竞争对手和其他第三方可能侵犯、挪用或以其他方式侵犯我们的专利和其他知识产权。 为了打击侵权或未经授权的使用,我们可能会被要求提出侵权索赔。但是,法院可能不同意我们的指控,并可能以我们的专利不涵盖为由,拒绝阻止对方使用有争议的技术 。此外,这些第三方可以反诉我们侵犯了他们的知识产权,或者我们向他们主张的专利是无效的或不可强制执行的。在美国的专利诉讼中,被告反诉和各方间对主张的专利的有效性、可执行性或范围提出质疑的审查是司空见惯的。此外,第三方可以对 我们提起法律诉讼,对我们的知识产权提出此类挑战。任何此类诉讼的结果通常都是不可预测的。质疑有效性的理由可能是据称未能满足多项法定要求中的任何一项,包括 缺乏新颖性、明显或无法启用。如果与专利起诉有关的人员向美国专利商标局隐瞒相关信息或在起诉期间做出误导性陈述,专利可能无法强制执行 。有可能存在我们和专利审查员在起诉期间没有意识到的先前技术,这可能会使任何可能颁发的专利无效。此外,也有可能存在我们知道但不相信与我们未来的专利相关的现有技术(如果它们发布),但这可能会导致我们的专利无效。
任何诉讼程序的不利结果都可能使我们的一项或多项专利面临被宣布无效或被狭义解释的风险。如果被告 在法律上认定我们的某一候选药物专利无效或不可强制执行,我们将失去该候选药物或技术的至少部分甚至全部专利保护。竞争对手 产品也可能在我们的专利覆盖范围可能不存在或同样强大的其他国家/地区销售。
知识产权诉讼可能导致我们 花费大量资源,并分散我们人员的正常职责。
与 知识产权索赔相关的诉讼或其他法律程序,无论是否有价值,都是不可预测的,通常代价高昂且耗时,很可能会将大量资源从我们的核心业务中分流出来,包括分散我们的技术和管理人员 的正常职责。此外,由于与知识产权诉讼相关的大量信息披露要求,我们的一些机密信息有可能在此类诉讼期间因披露而泄露 。此外,听证会、动议或其他临时程序或事态发展的结果可能会公开公布,如果证券分析师或投资者认为这些结果是负面的,可能会对我们普通股的价格产生重大不利影响。此类诉讼或诉讼可能大幅增加我们的运营亏损,并减少可用于开发活动或任何未来销售、营销或分销活动的资源。
我们可能没有足够的财政或其他资源来适当地进行这类诉讼或法律程序。我们的一些 竞争对手可能比我们更有效地承担此类诉讼或诉讼的费用,因为他们拥有更多的财力和更成熟、更发达的知识产权组合。因此,尽管我们 做出了努力,但我们可能无法阻止第三方侵犯或挪用我们的知识产权或成功挑战我们的知识产权。专利诉讼或 其他诉讼的发起和继续带来的不确定性可能会对我们在市场上的竞争能力产生重大不利影响。
61
我们可能无法在世界各地有效地起诉和执行我们的知识产权。
在世界所有国家申请、起诉和保护我们候选药物的专利将是昂贵得令人望而却步的。对可专利性的 要求在某些国家可能有所不同,特别是在发展中国家。此外,我们保护和执行知识产权的能力可能会受到国外知识产权法律意外变化的不利影响 。专利保护最终必须在一个逐个国家/地区这是一个昂贵且耗时的过程,且结果不确定 。因此,我们可以选择不在某些国家寻求专利保护,我们在这些国家也不会享受到专利保护的好处。此外,一些国家的专利法,包括一些具有重大商业利益的司法管辖区 ,对知识产权的保护程度不及美国法律,特别是在涉及现有药物的软件技术和治疗方法方面。许多 公司在保护和捍卫某些外国司法管辖区的知识产权方面遇到了严重问题。一些国家,特别是发展中国家的法律制度不支持专利和其他知识产权的执行。这可能会使我们很难阻止侵犯我们的专利(如果获得)或挪用我们的其他知识产权。例如,许多外国国家都有 强制许可法,根据该法律,专利所有者必须向第三方授予许可和/或限制专利对第三方(包括政府机构或政府承包商)的可执行性。因此,我们可能无法 阻止第三方在美国以外的所有国家实施我们的发明,而在这些国家,专利可能提供有限的好处,甚至没有任何好处。此外,如果专利被侵犯或我们或我们的许可人被迫向第三方授予许可,我们和我们的许可人在这些 外国的补救措施可能有限,这可能会大幅降低这些专利的价值,并可能限制我们的潜在收入机会。
竞争对手可以在我们未获得专利保护的司法管辖区使用我们的技术来开发自己的产品,而且,如果我们执行专利以阻止侵权活动的能力不足,竞争对手可能会 将其他侵权产品出口到我们拥有专利保护的地区。这些产品可能会与我们的候选药物竞争,而我们的专利或其他 知识产权可能无法有效或不足以阻止它们竞争。在外国司法管辖区强制执行我们的专利权的诉讼,无论是否成功,都可能导致巨额成本,并将我们的努力和资源从我们业务的其他方面转移 。此外,虽然我们打算为候选药物在主要市场保护我们的知识产权,但我们不能确保我们能够在我们希望销售候选药物的所有司法管辖区启动或保持类似的努力, 或获得类似的专利范围。因此,我们在这些国家保护知识产权的努力可能不足以从我们拥有或许可的知识产权中获得显著的商业优势。
如果我们没有获得我们 可能开发的任何候选药物的专利期延长和数据独占权,我们的业务可能会受到实质性损害。
根据FDA对我们可能开发的任何候选药物 的上市批准的时间、期限和细节,我们的一项或多项美国专利可能有资格根据1984年的药品价格竞争和专利期限恢复行动或Hatch-Waxman 修正案获得有限的专利期延长。Hatch-Waxman修正案允许专利展期最长为五年,作为对FDA监管审查过程中失去的专利期的补偿。专利期延长不能超过自产品批准之日起 总共14年的专利有效期;只能延长一项专利,并且只能延长涉及批准的药物、使用方法或制造方法的权利要求。但是,我们可能无法获得 延期,例如因为在测试期间未进行尽职调查
62
阶段或监管审查过程中,未在适用期限内申请、未在相关专利到期前申请或未能满足适用要求。 此外,适用期限或提供的专利保护范围可能比我们要求的要短。如果我们无法获得专利期延长或任何此类延长的期限比我们要求的短,我们的竞争对手可能会在我们的专利到期后获得竞争产品的 批准,我们的业务、财务状况、运营结果和前景可能会受到实质性损害。
我们可能需要从第三方获得某些知识产权许可,这些许可可能无法获得,也可能无法按商业合理的条款 获得。
第三方可能持有对我们的 产品开发非常重要或必要的知识产权,包括专利权。我们可能需要使用第三方的专利或专有技术将我们的产品商业化,在这种情况下,我们将被要求以商业合理的条款从这些第三方获得许可,否则我们的业务可能会受到损害,可能会受到严重损害。例如,当我们探索重新调整合作伙伴或其他第三方拥有的分子的用途时,我们获得了使用这些分子的权利 供我们使用。如果我们不能获得许可,或者不能以商业合理的条款或足够的广度获得许可,以涵盖第三方知识产权的预期使用,我们的业务可能会受到实质性的损害 ,或者我们可能会卷入纠纷。
如果我们未能履行我们与第三方合作或从第三方获得知识产权许可的协议中的义务,或者我们与我们的合作者或许可人的业务关系受到中断,我们可能会失去对我们的业务非常重要的权利。
我们许可对我们的业务非常重要的某些知识产权,将来我们可能会签订其他协议,为我们 提供有价值的知识产权或技术的许可。我们预计我们未来的许可协议将把各种开发、勤奋、商业化和其他义务强加给我们,以维持许可。尽管我们做出了 努力,但未来的许可方可能会得出结论,认为我们严重违反了此类许可协议下的义务,并寻求终止许可协议,从而取消或限制我们开发和商业化这些许可协议涵盖的产品和 技术的能力。如果这些许可证内的产品终止,或者根据其许可的基础专利权不能提供预期的排他性,竞争对手或其他第三方将有权寻求监管部门的批准并将与我们相同的产品推向市场,我们可能会被要求停止某些候选药物的开发和商业化。上述任何一项都可能对我们的竞争地位、业务、财务状况、经营结果和前景产生重大不利影响。
此外,受许可协议约束的知识产权可能会 产生争议,包括:
| • | 许可协议授予的权利范围和其他与解释有关的问题; |
| • | 我们的技术和工艺在多大程度上侵犯了不受许可协议约束的许可方的知识产权; |
| • | 我们合作开发关系下的专利和其他权利的再许可; |
| • | 我们在许可协议下的尽职义务,以及哪些活动满足这些尽职义务; |
| • | 由我们的许可人和我们以及我们的合作伙伴共同创造或使用知识产权而产生的发明和专有技术的发明和所有权;以及 |
| • | 专利技术发明的优先权。 |
63
我们向第三方许可知识产权或技术所依据的协议可能非常复杂,此类协议中的某些条款可能会受到多种解释的影响。可能出现的任何合同解释分歧的解决可能会缩小我们认为的相关 知识产权或技术的权利范围,或增加我们认为是相关协议下的财务或其他义务,其中任何一项都可能对我们的业务、财务状况、运营结果、 和前景产生实质性的不利影响。此外,如果围绕我们许可的知识产权的纠纷阻碍或削弱我们以商业上可接受的条款维持许可安排的能力,我们可能无法成功开发和商业化 受影响的候选药物,这可能会对我们的业务、财务状况、运营结果和前景产生重大不利影响。
我们的协作协议(如拜耳协议)可能会出现这些和类似的问题。我们与拜耳的合作是我们的 重要合作之一,不能保证此合作在当前期限过后会以优惠条款或根本不存在,也不能保证双方在合作生效期间的任何时间都将根据协议运营 而不存在争议。例如,可能的纠纷可能涉及知识产权的所有权或控制权、由合作产生的许可协议谈判、排他性义务、尽职调查和付款义务。
我们的一些知识产权是通过政府资助的计划发现的,因此可能受到联邦法规的约束,如进行权、某些报告要求以及对美国公司的偏好,遵守这些法规可能会限制我们的专有权和我们与非美国制造商签订合同的能力。
我们的知识产权可能会受到一个或多个第三方的权利保留。例如,我们许可的某些知识产权是通过使用美国政府资金产生的,因此受到某些联邦法规的约束。因此,根据1980年的《贝赫-多尔法案》或《贝赫-多尔法案》,美国政府 可能对我们当前或未来的流程及相关产品和服务中体现的知识产权拥有某些权利。美国政府的这些权利包括将发明用于任何政府目的的非排他性、不可转让、不可撤销的全球许可。此外,在某些有限的情况下,如果美国政府确定(1)没有采取足够的步骤将发明商业化并实现政府资助的技术的实际应用,(2)政府必须采取行动以满足公共卫生或安全需要,则美国政府有权要求许可方将上述任何发明的独家、部分独占或非独家许可授予第三方。 如果美国政府确定(1)没有采取足够的步骤将发明商业化并实现政府资助的技术的实际应用,则有权要求许可方向第三方授予这些发明的独家、部分独家或非独家许可。(3)政府必须采取行动以满足联邦法规对公共使用的 要求,否则(4)我们无法满足联邦法规的要求(也称为入场权)。如果我们或我们的许可人未向政府披露发明或未在规定的期限内提交知识产权注册申请,美国政府也有权 取得这些发明的所有权。这些权利可能允许政府 向第三方披露我们的机密信息。此外, 我们对此类发明的权利可能会受到在美国制造包含此类发明的产品的某些要求的约束。在 政府资助的计划下产生的知识产权也受某些报告要求的约束,遵守这些要求可能需要我们花费大量资源。如果我们未来拥有或许可的任何知识产权也是通过使用美国政府资金而产生的,那么贝赫-多尔法案的条款也可能同样适用。政府对此类权利的任何行使都可能对我们的竞争地位、业务、经营结果和财务状况产生实质性的不利影响 。
64
美国和其他司法管辖区专利法的修改可能会降低专利的整体价值 ,并可能影响我们专利权的有效性、范围或可执行性,从而削弱我们保护候选药物的能力。
正如其他生物制药公司的情况一样,我们的成功在很大程度上依赖于知识产权,特别是专利。在生物制药行业获得和实施专利涉及技术和法律复杂性 ,因此成本高、耗时长,而且本质上是不确定的。我们的专利权、其相关成本以及此类专利权的执行或保护可能会受到专利法、专利案例法或USPTO规则和法规的发展或不确定性的影响。专利法或专利法解释的更改可能会增加围绕专利申请的起诉以及执行或保护我们已颁发的专利的不确定性和成本 。例如,2013年3月,根据《莱希-史密斯美国发明法》(Leahy-Smith America Invents Act)或《美国发明法》(America Inents Act),美国从最初的发明转变为 ?最先提交的文件专利制度。在一个?最先提交的文件系统, 假设满足可专利性的其他要求,第一个提交专利申请的发明人通常将有权获得一项发明的专利,无论其他发明人是否在此之前已经发明了该发明。在2013年3月之后向美国专利商标局提交专利申请的第三方 ,因此在我们之前可以获得涵盖我们的发明的专利,即使我们在发明由该第三方制造之前就已经制造了该发明。这将要求我们 了解从发明到专利申请的时间。由于美国和大多数其他国家/地区的专利申请在提交后或发布前的一段时间内是保密的,因此我们不能确定 我们或我们的许可人是第一个提交与我们的技术或候选药物相关的专利申请或发明我们或我们的许可人的专利或专利申请中要求的任何发明的公司。美国发明法 还包括对美国专利法的其他一些重大修改,包括影响专利申请起诉方式的条款,允许第三方提交现有技术,以及建立包括授权后审查在内的新的授权后审查制度 。各方间审查和派生程序。由于USPTO程序中的证据标准低于美国联邦法院宣布专利权利要求无效所需的证据标准 ,第三方可能会在USPTO程序中提供足以让USPTO认定权利要求无效的证据,即使同样的证据如果首先在地区法院诉讼中提交,也不足以使权利要求无效。 因此,第三方可能会尝试使用USPTO程序来使我们的专利权利要求无效,如果发生以下情况,则不会使我们的专利权利要求无效。 在以下情况下,第三方可能会尝试使用USPTO程序来使我们的专利权利要求无效,如果我们的专利权利要求不会被无效,那么第三方可能会尝试使用USPTO程序来使我们的专利权利要求无效这些变化的影响目前尚不清楚 因为美国专利商标局继续颁布与《美国发明法》相关的新法规和程序,以及专利法的许多实质性修改,包括?最先提交的文件这些条款在2013年3月才生效。此外,法院尚未处理这些条款中的许多条款,该法案和本申请中讨论的关于 特定专利的新法规的适用性尚未确定,需要进行审查。然而,《美国发明法》及其实施可能会增加围绕我们专利申请的起诉以及我们已授权专利的实施或保护的不确定性和成本。
近年来,美国最高法院对几个专利案件做出了裁决, 要么在某些情况下缩小了专利保护的范围,要么在某些情况下削弱了专利所有者的权利。此外,最近有人提议对美国和其他国家/地区的专利法进行更多修改,如果被采纳,可能会影响我们为我们的专有技术获得专利保护的能力或我们执行专有技术权利的能力。根据美国国会、美国 法院、USPTO和其他国家相关立法机构未来的行动,管理专利的法律和法规可能会以不可预测的方式发生变化,从而削弱我们获得新专利或 强制执行我们未来可能获得的任何专利的能力。
65
知识产权不一定能解决所有潜在威胁。
我们的知识产权提供的未来保护程度是不确定的,因为知识产权是有限制的,可能 无法充分保护我们的业务或使我们无法保持竞争优势。例如:
| • | 其他人可能能够制造与我们的候选药物相似的产品,或者使用类似的技术,但这些产品不在我们许可或可能拥有的专利权利要求的 范围内; |
| • | 其他公司可能能够以侵犯我们专利但不可检测的方式复制或利用类似技术, 或在我们无法获得或执行专利权的司法管辖区复制或使用类似技术; |
| • | 我们或我们的许可人或合作者可能不是第一个做出我们现在或将来许可或拥有的已发布专利或 未决专利申请所涵盖的发明的人; |
| • | 我们或我们的许可人或合作者可能不是第一个提交专利申请的人,这些专利申请涵盖我们或他们的某些发明; |
| • | 其他公司可以独立开发类似或替代技术或复制我们的任何技术,而不会 侵犯我们拥有或许可的知识产权; |
| • | 我们目前或将来的未决专利申请(无论是拥有的还是许可的)可能不会导致颁发 项专利; |
| • | 我们拥有权利的已颁发专利可能被认定为无效或不可强制执行,包括由于 我们的竞争对手或其他第三方的法律挑战; |
| • | 我们的竞争对手或其他第三方可能会在我们没有专利权的国家进行研发活动,然后利用从这些活动中学到的信息来开发有竞争力的产品,在我们的主要商业市场销售; |
| • | 我们可能不会开发其他可申请专利的专有技术; |
| • | 他人的专利可能会损害我们的业务;以及 |
| • | 我们可能会选择不申请专利以保护某些商业秘密或专有技术,然后第三方可能会提交涵盖此类知识产权的专利。 |
如果发生上述任何事件,都可能对我们的业务、财务状况、运营结果和前景产生实质性的不利影响。
如果我们的商标和商号没有得到充分保护,那么我们可能无法在感兴趣的市场上建立知名度,我们的业务 可能会受到不利影响。
我们的注册或未注册商标或商号可能被质疑、侵犯、规避或宣布为通用商标,或被认定为侵犯其他商标。我们可能无法保护我们对这些商标和商号的权利,我们需要在我们感兴趣的市场中的潜在合作者或客户中建立知名度。在 次,竞争对手可能采用与我们类似的商号或商标,从而阻碍我们建立品牌标识的能力,并可能导致市场混乱。此外,其他商标或商标的所有者可能会提出潜在的商号或商标侵权索赔 ,这些商标或商标包含我们的注册或未注册商标或商号的变体。从长远来看,如果我们无法根据我们的商标和商号建立名称认知度, 那么我们可能无法有效竞争,我们的业务可能会受到不利影响。我们可能会将我们的商标和商号授权给第三方,例如分销商。尽管这些许可协议可能会为如何使用我们的 商标和商号提供指导原则,但违反这些协议或
66
被许可人滥用我们的商标和商号可能会危及我们的权利或削弱与我们的商标和商号相关的商誉。我们执行或保护与商标、商号、商业秘密、专有技术、域名、版权或其他知识产权相关的专有权的努力可能无效,可能导致巨额成本和 资源转移,并可能对我们的业务、财务状况、运营结果和前景产生不利影响。
我们向 第三方所有者授予专利权。如果这些所有者没有正确或成功地获得、维护或强制执行这些许可所依据的专利,我们的竞争地位和业务前景可能会受到损害。
我们是许可协议的一方,这些协议赋予我们对我们业务所需或有用的第三方知识产权的权利。例如, 我们已从第三方获得了涵盖多个临床候选药物的专利权许可,并从某些其他方获得了用于我们药物发现工作的技术许可(隐含或明确的)。我们未来可能会与第三方知识产权签订 其他许可协议。
我们的成功在一定程度上将取决于我们的许可方 获取、维护和执行我们许可产品的专利保护的能力。我们的许可方可能无法成功起诉我们许可的专利申请。即使就这些专利申请颁发专利,我们的许可人也可能无法 维护这些专利,可能决定不对侵犯这些专利的其他公司提起诉讼,或者可能不会像我们那样积极地提起诉讼。如果不保护我们许可的知识产权, 其他公司可能会提供基本相同的产品供销售,这可能会对我们的竞争业务地位产生不利影响,并损害我们的业务前景。
我们目前对某些候选药物的专有地位取决于我们拥有或授权的专利申请,这些专利申请涵盖了此类候选药物的 成分、制造相关方法、配方和/或使用方法,这可能无法充分防止竞争对手或其他第三方将同一候选药物用于相同或不同的用途。
物质组合物专利保护通常被认为是药品所需要的,因为它提供的保护不涉及任何特定的使用、制造或配方方法。对于我们从协作合作伙伴那里获得许可的某些分子,我们不能依赖Compostion of Matter专利保护,因为这些专利的期限已经过期或即将过期。
使用方法专利保护特定方法产品的使用, 配方专利涵盖提供治疗药物的配方。虽然我们在开发过程中的适当时间提交了涉及我们程序使用方法的申请,但我们不能确定 这些申请在未来发布的任何专利中是否会涵盖竞争用途中所有与商业相关的分子应用。这些类型的专利并不阻止竞争对手或其他第三方为专利方法范围以外的指示开发、营销或商业化类似或相同的产品 ,或开发专利配方范围以外的不同配方。此外,在使用方法专利方面,即使竞争对手或其他第三方 没有针对我们可能获得专利的目标适应症或用途积极宣传他们的产品,医生也可能建议患者在标签外使用这些产品,或者患者自己 这样做 。尽管非标签使用可能会侵犯或助长对使用方法专利的侵权,但这种做法很常见,此类侵权很难防止或执行。 因此,我们可能无法阻止第三方在美国或国外实施我们的发明。此外,一些与商业相关的司法管辖区不允许专利涵盖使用其他已知分子的新方法。
67
与政府监管相关的风险
即使我们的任何候选药物获得了监管部门的批准,我们也将受到持续的监管义务和持续的监管审查的约束,这 可能会导致巨大的额外费用。此外,如果我们的候选药物获得批准,可能会受到上市后研究要求、营销和标签限制,如果在批准后发现意外的安全性问题,甚至可能会召回或退出市场 。此外,如果我们不遵守监管要求,我们可能会受到惩罚或采取其他执法行动。
考虑到我们的新药发现方法,FDA可能不会批准从我们的平台派生的任何候选药物,并可能选择检查我们用于生成数据的 自动化机器人平台。但是,如果FDA或类似的外国监管机构批准我们的任何候选药物,该产品的生产工艺、标签、包装、分销、不良事件报告、 储存、广告、促销和记录将受到广泛和持续的监管要求的约束。这些要求包括提交安全性和其他上市后信息和报告、建立 注册和上市,以及我们在批准后进行的任何临床试验继续遵守cGMP和GCP。我们为候选药物获得的任何监管批准也可能受到批准的 指明的产品上市用途或批准条件的限制,或者包含可能代价高昂的上市后研究的要求,以及监控产品安全性和有效性的要求。以后发现产品存在 以前未知的问题,包括未预料到的严重程度或频率的不良事件,或我们的第三方制造商或制造流程,或未能遵守监管要求,可能会导致 其他问题:
| • | 限制产品的销售或制造,将产品从市场上召回,或自愿或 强制召回产品; |
| • | 临床试验有效 |
| • | 罚款、警告信或者其他监管执法行为; |
| • | FDA拒绝批准我们提交的待决申请或已批准申请的补充申请; |
| • | 扣押、扣留产品,或者拒绝允许产品进出口的; |
| • | 禁制令或施加民事或刑事处罚。 |
FDA的政策可能会发生变化,可能会颁布额外的政府法规,以阻止、限制或推迟对我们的候选药物的监管审批。如果我们缓慢或无法适应现有要求的变化或新要求或政策的采用,或者如果我们无法保持合规性,我们可能会失去我们可能获得的 任何营销批准,这将对我们的业务、前景和实现或维持盈利的能力产生不利影响。
我们可能会为 某些候选药物申请孤儿药物指定,并且我们可能不会成功或可能无法保持与孤儿药物指定相关的好处,包括潜在的市场排他性。
作为我们商业战略的一部分,我们可能会为我们的某些候选药物寻求孤儿药物指定,但我们可能不会成功。包括美国和欧洲在内的一些司法管辖区的监管当局可能会将患者人数相对较少的药物指定为孤儿药物。根据《孤儿药品法》,如果一种药物是孤儿药物,FDA可以将其指定为孤儿药物
68
旨在治疗罕见疾病或疾病,通常定义为在美国每年患者人数少于200,000人,或在美国患者人数为200,000人或更多,且无法合理预期在美国的销售将收回开发药物的成本。在美国,孤儿药物指定使一方有权获得财政 奖励,例如获得临床试验费用赠款资助的机会、税收优惠和用户费用减免。
同样,在欧洲,欧盟委员会根据EMA孤儿药物产品委员会的建议,授予孤儿药物 称号,以促进用于诊断、预防或治疗欧洲每10,000人中不超过5人的危及生命或慢性衰弱疾病的药物的开发,并且没有授权 令人满意的诊断、预防或治疗方法(否则产品将对受影响的人产生重大好处)。此外,对于用于诊断、预防或治疗 危及生命、严重虚弱或严重和慢性疾病的药物,以及在没有激励措施的情况下,该药物在欧洲的销售不太可能足以证明开发该药物的必要投资是不合理的,将被授予名称。在欧洲,孤儿药物指定使一方有权获得经济奖励,如降低费用或免除费用。
通常,如果具有孤儿药物 名称的药物随后获得了其具有该名称的适应症的首次上市批准,则该药物有权享有一段市场独占期,这将阻止FDA或EMA在该时间段内批准同一药物和适应症的另一次上市 申请,但在有限情况下除外。适用期限在美国为七年,在欧洲为十年。如果一种 药物不再符合孤儿药物指定标准,或者如果该药物具有足够的利润从而不再具有市场独占性,则可以将欧洲独占期缩短至六年。
即使我们获得了一种药物的孤儿药物排他性,这种排他性也可能不能有效地保护该药物免受竞争,因为不同的药物可以 被批准用于相同的条件。即使在孤儿药物获得批准后,如果FDA得出结论认为后一种药物在临床上更安全、更有效或对患者护理有重大贡献,则FDA随后可以针对相同的情况批准不同的药物。此外,如果指定的孤儿药物被批准用于的用途比其获得孤儿指定的适应症更广泛,则可能不会获得孤儿药物独家经营权。 此外,如果FDA后来确定指定请求存在重大缺陷,或者如果制造商无法确保足够的药物数量来满足患有罕见疾病或疾病的患者的需求,或者如果确定具有相同分子活性部分的另一种药物更安全、更安全,则可能会失去孤儿药物在美国的独家营销权。孤儿药物指定 既不会缩短药物的开发时间或监管审查时间,也不会在监管审查或审批过程中给药物带来任何优势。虽然我们可能会为我们的候选药物申请孤儿药物称号,但我们可能永远不会获得这样的 称号。即使我们真的收到了这样的称号,也不能保证我们会享受到这些称号的好处。
在一个司法管辖区获得并保持 我们候选药物的监管批准,并不意味着我们将在其他司法管辖区成功获得我们候选药物的监管批准。
我们也可以在其他国家提交营销申请。美国以外司法管辖区的监管机构有 批准候选药物的要求,我们在这些司法管辖区上市前必须遵守这些要求。例如,到目前为止,我们的试验患者人数较少,而一些国际监管机构提交的申请可能需要较大的患者人数。 获得外国监管机构的批准和遵守外国监管要求可能会给我们带来重大延误、困难和成本,并可能推迟或阻止引入
69
我们的产品在某些国家/地区。如果我们未能遵守国际市场的监管要求和/或获得相应的上市批准,我们的目标市场将会减少 ,我们充分发挥候选药物市场潜力的能力将受到损害。
在一个司法管辖区获得并保持对我们 候选药物的监管批准并不能保证我们能够在任何其他司法管辖区获得或维持监管批准,而在一个司法管辖区未能或延迟获得监管批准可能会对其他司法管辖区的监管审批流程产生负面影响 。例如,即使FDA批准候选药物上市,外国司法管辖区的可比监管机构也必须批准候选药物在这些国家的制造、营销和推广。审批程序因司法管辖区而异,可能涉及与美国不同或大于美国的要求和行政审查期,包括额外的非临床研究或 临床试验,因为在一个司法管辖区进行的临床试验可能不会被其他司法管辖区的监管机构接受。简而言之,外国监管审批过程涉及与FDA审批相关的所有风险。在美国以外的许多 司法管辖区,候选药物必须先获得报销批准,然后才能在该司法管辖区获准销售。在某些情况下,我们可能打算对我们的产品收取的价格也需要 批准。
管理我们未来可能拥有的任何国际业务的法律法规可能会阻止我们在美国以外开发、制造和销售某些产品,并要求我们制定和实施代价高昂的合规计划。
如果我们将我们的业务扩展到美国以外的地区,我们必须投入额外的资源来遵守我们计划在其中开展业务的每个司法管辖区的众多法律法规。《反海外腐败法》(Foreign Corrupt Practices Act,简称FCPA)禁止任何美国个人或企业直接或间接向任何外国官员、政党或候选人支付、提供、授权支付或提供任何有价值的东西,目的是影响外国实体的任何行为或决定,以便 帮助个人或企业获得或保留业务。《反海外腐败法》还要求证券在美国上市的公司遵守某些会计条款,这些条款要求公司保存准确和公平地反映公司(包括国际子公司)所有交易的账簿和 记录,并为国际业务设计和维护充分的内部会计控制系统。
遵守《反海外腐败法》既昂贵又困难,特别是在腐败是公认问题的国家。此外,《反海外腐败法》 给制药业带来了特殊的挑战,因为在许多国家,医院是由政府运营的,医生和其他医院员工被认为是外国官员。与临床试验和其他工作相关的向医院支付的某些款项被认为是向政府官员支付的不当款项,并已导致FCPA执法行动。
各种法律、法规和行政命令还限制在美国境外使用和传播,或与某些非美国国民共享出于国家安全目的而保密的信息,以及某些产品和与这些产品相关的技术数据。如果我们将业务扩展到美国以外的地区, 将需要我们投入额外的资源来遵守这些法律,而这些法律可能会阻止我们在美国以外开发、制造或销售某些产品和候选药物,这可能会限制我们的增长潜力并增加我们的开发成本。
不遵守有关国际商业惯例的法律可能导致重大的 民事和刑事处罚以及暂停或禁止政府合同。美国证券交易委员会(Securities and Exchange Commission,简称SEC)也可能暂停或禁止发行人因违反FCPA的会计规定而在美国交易所交易证券。
70
我们受到美国和外国的某些反腐败、反洗钱、出口管制、制裁和 其他贸易法律法规的约束。我们可能会因违规行为而面临严重后果。
除其他事项外,美国和外国的反腐败、 反洗钱、出口管制、制裁和其他贸易法律法规统称为贸易法,禁止公司及其员工、代理、临床研究组织、法律顾问、会计师、 顾问、承包商和其他合作伙伴授权、承诺、提供、提供、招揽或直接或间接接受公共或私营部门收款人的腐败或不当付款或任何其他有价值的东西 。违反贸易法可能导致巨额刑事罚款和民事处罚、监禁、丧失贸易特权、取消资格、重新评估税收、违反合同和欺诈诉讼、声誉损害和其他 后果。我们与政府机构或政府附属医院、大学和其他组织的官员和员工有直接或间接的互动。我们还预计我们在美国以外的活动将会及时增加。我们计划聘请第三方进行临床试验和/或获得必要的许可、许可证、专利注册和其他监管批准,即使我们没有明确授权或事先了解此类活动,我们也可能被要求对我们的人员、代理或合作伙伴的腐败或其他非法活动负责。
我们可能会为我们的一个或多个其他候选药物寻求优先 评审指定,但我们可能不会收到此类指定,即使我们获得了此类指定,此类指定也可能不会带来更快的监管审查或审批过程。
如果FDA确定候选药物提供了治疗严重疾病的方法,并且如果获得批准,该产品将在安全性或有效性方面有显著的改善 ,FDA可以指定该候选药物进行优先审查。优先审查指定意味着FDA审查申请的目标是六个月,而不是标准的十个 个月的审查期。我们可能会要求优先审查我们的候选药物。FDA在是否授予候选药物优先审查地位方面拥有广泛的自由裁量权,因此,即使我们认为特定候选药物有资格获得此类 指定或地位,FDA也可能决定不授予该资格。此外,与传统的FDA程序相比,优先审查指定不一定会加快监管审查或批准过程,也不一定会在批准方面带来任何优势 。接受FDA的优先审查并不能保证在六个月的审查周期内获得批准,或者根本不能保证批准。
FDA的突破性治疗指定和快速通道指定,即使授予我们的任何候选药物,也可能不会带来更快的开发、 监管审查或审批过程,而且每个指定都不会增加我们的候选药物在美国获得上市批准的可能性。
我们可能会为我们的一些候选药物寻求突破性的治疗指定。突破性疗法被定义为一种旨在单独或与一种或多种其他药物联合治疗严重或危及生命的疾病或状况的药物,初步临床证据表明,该药物可能在一个或多个 临床重要终点显示出比现有疗法有实质性改善的效果,例如在临床开发早期观察到的实质性治疗效果。对于被指定为突破性疗法的药物,FDA和试验赞助商之间的互动和沟通 可以帮助确定最有效的临床开发路径,同时最大限度地减少处于无效控制方案中的患者数量。被FDA指定为突破性疗法的药物也可能有资格获得优先审查和 加速审批。指定为突破性疗法是FDA的自由裁量权。因此,即使我们相信我们的候选药物之一符合被指定为突破性疗法的标准,FDA也可能不同意,而是决定不进行此类指定。在……里面
71
在任何情况下,与根据FDA常规程序考虑批准的疗法相比,收到候选药物的突破性治疗指定可能不会带来更快的开发过程、审查或批准 也不能保证FDA最终批准。此外,即使我们的一个或多个候选药物有资格成为突破性疗法,FDA稍后也可能决定这些候选药物不再符合 资格条件,或者决定FDA审查或批准的时间不会缩短。
我们可能会为我们的一些候选药物寻求快速通道认证 。如果一种药物用于治疗严重或危及生命的疾病,并且该药物显示出解决该疾病未得到满足的医疗需求的潜力,则药物赞助商可以申请快速通道认证 。FDA拥有广泛的自由裁量权来决定是否授予该称号,因此,即使我们认为某个特定的候选药物有资格获得该称号,我们也不能向您保证FDA会决定授予该称号。即使我们确实获得了 快速通道认证,与传统的FDA程序相比,我们可能不会体验到更快的开发流程、审查或批准。如果FDA认为我们临床开发项目的数据 不再支持快速通道指定,它可能会撤销该指定。快速通道指定本身并不能保证符合FDA优先审查程序的资格。
FDA、EMA和其他监管机构可能会对我们候选药物的开发和商业化实施额外的法规或限制,这些变化可能很难预测。
FDA、EMA和其他国家的监管机构都表示有兴趣进一步监管小分子药品。 美国联邦和州一级的机构以及美国国会委员会和其他政府或管理机构也表示有兴趣进一步监管小分子制药 行业。这样的行动可能会推迟或阻止我们的部分或全部候选药物商业化。其他人进行的产品临床试验的不利发展可能会导致FDA或其他监督机构更改对我们任何候选药物的 审批要求。这些监管审查机构和委员会及其发布的新要求或指南可能会延长监管审查流程,要求我们进行额外的研究或试验,增加我们的开发成本,导致监管立场和解释的变化,推迟或阻止我们候选药物的批准和商业化,或者导致重大的批准后限制或限制。在我们推进我们的候选药物 时,我们将被要求咨询这些监管机构,并遵守适用的要求和指南。如果我们不能做到这一点,我们可能会被要求推迟或停止这种候选药物的开发。这些额外的 流程可能会导致审核和审批流程比我们预期的更长。由于监管审批流程增加或延长或对我们候选药物开发的进一步限制而导致的延误可能代价高昂,并可能对我们及时完成临床试验和将我们当前和未来的候选药物商业化(如果有的话)的能力产生负面影响。
医疗保健立法改革措施可能会对我们的业务和运营结果产生实质性的不利影响。
美国和许多外国司法管辖区已经颁布或提议了影响医疗保健系统的立法和监管改革,这些改革可能会阻止或 推迟我们当前或未来候选药物或任何未来候选药物的上市审批,限制或监管审批后活动,并影响我们以盈利方式销售获得上市批准的产品的能力。 法规的更改或对现有法规的解释可能会影响我们未来的业务,例如,要求:i)更改我们的制造安排,ii)添加或修改产品标签, iii)召回或停产我们的产品,或iv)额外的记录保存要求。如果实施任何此类改变,都可能对政府的运作产生不利影响。
72
我们的业务。在美国,已经并将继续有许多立法举措来控制医疗成本。例如,2010年3月通过了《平价医疗法案》(Affordable Care Act,简称ACA),该法案极大地改变了政府和私营保险公司为医疗保健融资的方式,并对美国制药业产生了重大影响。除其他事项外,ACA使生物制品受到较低成本生物仿制药的潜在竞争,解决了一种新的方法,即对吸入、输液、滴注、植入或注射的药物计算制造商在医疗补助药物回扣计划下所欠的回扣,提高医疗补助药物回扣计划下制造商所欠的最低医疗补助回扣,并将回扣计划扩大到登记在医疗补助管理的护理组织中的个人,建立对某些品牌的制造商的年费和税收。其中制造商必须同意提供70%(根据2018年两党预算法增加,自2019年起生效)销售点在承保间隔期内,向符合条件的受益人提供适用品牌药品的协商价格折扣,作为制造商的 门诊药品在联邦医疗保险D部分承保的条件。此后,ACA风险调整计划付款参数每年都会更新。
美国国会议员已表示有意通过立法或通过行政命令,从根本上改变或废除ACA的部分内容。 尽管国会迄今尚未通过废除立法,但TCJA废除了ACA对某些未能 维持一年全部或部分时间合格医疗保险(通常称为个人强制医保)的个人基于税收的分担责任付款。2018年12月14日,德克萨斯州的一家联邦地区法院裁定了这名个人。由于作为TCJA的一部分被废除,ACA的其余条款也是无效的,2019年12月18日,美国第五巡回上诉法院裁定,个人授权是违宪的,并将此案发回下级法院重新考虑其早先对ACA全文的无效。美国最高法院于2020年3月2日批准了移审令,并于2020年11月10日听取了该案的口头辩论,预计该案将在2021年的某个时候做出裁决。在等待审查期间,ACA仍然有效,但目前尚不清楚最新裁决将对ACA的地位产生什么影响。有关ACA的诉讼和立法 可能会继续,结果不可预测和不确定。我们将继续评估ACA及其可能的废除和取代对我们业务的影响。
此外,2017年1月20日签署了一项行政命令,指示根据ACA拥有权力和责任的联邦机构 放弃、推迟、授予豁免或推迟实施ACA的任何条款,这些条款会给各州带来财政负担,或者给个人、医疗保健提供者、医疗保险公司或 药品或医疗器械制造商带来成本、费用、税收、罚款或监管负担。2017年10月13日,签署了一项行政命令,终止了根据ACA向保险公司报销的费用分担补贴。特朗普政府得出结论,ACA要求向保险公司支付的成本分担 削减(CSR)没有收到国会的必要拨款,并宣布将立即停止这些支付,直到这些拨款到位。企业社会责任付款的损失预计将增加ACA下合格健康计划出具的某些保单的保费。几个州的总检察长提起诉讼,要求阻止政府终止补贴,但他们提出的 限制令请求于2017年10月25日被加州的一名联邦法官拒绝。成本份额削减付款的损失预计将增加ACA下合格健康计划签发的某些保单的保费。此外,2018年6月14日,美国联邦巡回上诉法院(U.S.Court of Appeals for the Federal Circuit)裁定,联邦政府无需向第三方付款人支付超过120亿美元的ACA风险走廊付款,他们认为这些付款是欠他们的。这种报销差距对第三方付款人、ACA市场、提供商以及我们潜在业务的影响尚不清楚。
73
此外,2018年1月22日,一项关于2018财年拨款的持续决议获得批准,该决议推迟了ACA规定的某些费用的实施,包括对某些高成本雇主赞助的保险计划征收所谓的凯迪拉克税,根据市场份额向 某些医疗保险提供商征收年费,以及对非豁免医疗器械征收医疗器械消费税;然而,2019年12月20日,进一步综合拨款法案(H.R. 1865)被无法确定未来是否会开征类似的税种。2018年两党预算法也修订了ACA,自2019年1月1日起生效,增加了销售点参与Medicare Part D并缩小大多数Medicare药物计划的承保差距(通常称为甜甜圈漏洞)的制药制造商所欠的折扣。CMS发布了一项最终规则,允许对某些符合ACA资格的健康计划和ACA风险调整计划下的医疗保险发行商进行进一步的收款和付款,以回应联邦地区法院关于CMS用于确定此风险调整的方法的诉讼结果。此外,CMS最近发布了一项最终规则,即从2020年开始,在为个人和小团体市场的保险公司设定基准方面, 将给予各州更大的灵活性,这可能会放宽ACA对通过此类市场销售的计划所要求的基本健康福利 。自ACA颁布以来,美国还提出并通过了其他立法修改。2011年8月,“2011年预算控制法案”(Budget Control Act Of 2011)等法案为国会制定了削减开支的措施。 赤字削减联合特别委员会负责建议2013至2021年至少1.2万亿美元的赤字削减目标,但该委员会无法达到所需目标,从而触发立法自动 削减多个政府项目。这包括每个财年向提供者支付的医疗保险总额减少2%,由于后续的立法修订,除非采取额外的 国会行动,否则这些费用将一直有效到2029年。2012年的《美国纳税人救济法》(American纳税人救济法)减少了向多家医疗服务提供者(包括医院、影像中心和治疗中心)支付的医疗保险费用,并将政府向提供者追回多付款项的诉讼时效期限 从三年延长至五年。
在特殊药品定价实践方面, 美国的立法和执法兴趣与日俱增。具体地说,美国国会最近进行了几次调查,并提出了联邦和州立法,这些立法旨在提高药品定价的透明度, 降低联邦医疗保险(Medicare)下处方药的成本,审查定价与制造商患者计划之间的关系,以及改革政府计划的药品报销方法。在联邦一级,特朗普政府2019年和2020财年的预算包含进一步的药品价格控制措施,这些措施可能会在预算过程或其他未来立法中颁布,例如,包括允许联邦医疗保险D部分计划 谈判联邦医疗保险B部分下某些药物的价格的措施,允许一些州根据医疗补助谈判药品价格,以及取消低收入患者仿制药的成本分担。此外,特朗普政府还发布了一份降低药品价格和降低药品自付成本的蓝图,其中包含增加制造商竞争、提高某些联邦医疗计划的谈判力、激励 制造商降低其产品标价以及降低消费者支付的候选药品的自付成本的额外建议。 特朗普政府发布了一份蓝图,以降低药品价格和药品自付成本,其中包括增加制造商竞争、提高某些联邦医疗计划的谈判力、激励制造商降低产品标价以及降低消费者支付的候选药品的自付成本。美国卫生与公众服务部(HHS)已经开始就其中一些措施征求反馈意见,同时,正在根据其现有权限立即实施其他措施。例如,2019年5月,CMS发布了一项最终规则,允许Medicare Advantage计划从2020年1月1日起选择对B部分药物使用阶梯疗法,这是一种事先的 授权。这一最终规则将CMS的政策变更编入法典,从1月1日起生效。, 2019年。此外,2020年9月发布了一项行政命令,指示卫生与公众服务部部长继续实施两种新的支付模式,根据这两种支付模式,联邦医疗保险将测试分别在B部分和D部分涵盖的某些包括的药品和生物制品支付不超过最惠国价格是否会减轻
74
与高昂的药费相关的不良临床结果和增加的医疗保险支出。如果实施,最惠国价格通常将反映在经济合作与发展组织(Organization for Economic Co-operation and Development,简称OECD)经济可比成员国销售的药品的最低价格。 经过某些调整后,最惠国价格将反映在经济上可比的经济合作与发展组织成员国销售的药品的最低价格。国会还继续对处方药行业的定价做法进行 调查。虽然几项拟议的改革措施将需要国会通过立法才能生效,但国会已表示,它将继续寻求新的立法和/或监管措施,以解决处方药成本问题。在州一级,立法机构越来越多地通过立法,各州正在实施旨在控制用于治疗和患者的支出的法规。自掏腰包药品的成本。实施影响药品定价和/或供应的成本控制措施或其他医疗改革,可能会影响我们创造 收入、实现或维持盈利能力,或将我们未来可能获得监管部门批准的产品商业化的能力。
此外,2018年5月30日,《审判权法案》签署成为法律。除其他事项外,该法律还为某些患者提供了一个联邦框架,让他们可以访问某些已完成第一阶段临床试验且 正在接受调查以获得FDA批准的研究用新药候选药物。在某些情况下,符合条件的患者可以在不参加临床试验和根据FDA扩大准入计划获得FDA许可的情况下寻求治疗。根据《试用权利法案》,制药商没有义务 将其候选药物提供给符合条件的患者。
在州 层面,各个州越来越积极地通过立法和实施旨在控制药品和生物制品定价的法规,包括价格或患者报销限制、折扣、对某些产品准入和营销成本披露的限制 以及透明度措施,在某些情况下,旨在鼓励从其他国家进口和批量采购。此外,地区医疗当局和个别医院 越来越多地使用招标程序来确定哪些药品和供应商将包括在其处方药和其他医疗保健计划中。这些措施一旦获得批准,可能会降低对我们产品的最终需求 ,或者给我们的产品定价带来压力。
我们预计未来将采取额外的州和联邦医疗改革措施,其中任何一项都可能限制联邦和州政府为医疗产品和服务支付的金额,这可能会导致对我们当前或未来候选药物的需求减少或额外的定价压力。
我们的收入前景可能会受到美国和海外医疗支出和政策变化的影响。
我们在高度监管的行业中运营,与医疗保健可用性、医疗保健产品和服务的交付或支付方式相关的新法律、法规或司法裁决,或对现有法律、法规或 决定的新解释,可能会对我们的业务、运营和财务状况产生负面影响。
外国、联邦和州政府已经并可能继续提出立法和监管建议,旨在扩大医疗保健的可获得性,并控制或降低医疗保健成本。我们无法预测未来可能采取的举措,包括废除、取代或对ACA进行重大修订。 政府、保险公司、管理医疗组织和医疗服务的其他付款人继续努力控制或降低医疗成本和/或实施价格控制可能会产生不利影响:
| • | 如果我们获得监管部门的批准,对我们当前或未来候选药物的需求; |
75
| • | 我们有能力为我们的产品设定一个我们认为是公平的价格; |
| • | 我们获得产品承保和报销批准的能力; |
| • | 我们创造收入、实现或保持盈利的能力; |
| • | 我们须缴交的税项水平;及 |
| • | 资金的可获得性。 |
任何减少联邦医疗保险或其他政府计划的报销都可能导致私人付款人支付的类似减少,这可能会 对我们的运营结果和未来的盈利能力产生不利影响。
我们与医疗保健提供者、其他客户和第三方付款人的关系 将受到适用的反回扣、欺诈和滥用以及其他医疗法律法规的约束,这可能使我们面临刑事制裁、民事处罚、被排除在政府医疗保健计划之外、合同损害、声誉损害以及利润和未来收入减少。
虽然我们目前没有任何产品上市,但一旦我们开始将候选药物商业化 ,我们将受到联邦政府以及我们开展业务的州和外国政府的额外医疗法律法规要求和执法的约束。医疗保健提供者、 医生和第三方付款人在我们获得市场批准的任何候选药物的推荐和处方中扮演主要角色。我们未来与第三方付款人和客户的安排可能会使我们面临广泛适用的欺诈和滥用以及其他医疗法律法规,这些法律法规可能会限制我们营销、销售和分销我们获得上市批准的候选药物的业务或财务安排和关系。 适用的联邦和州医疗法律法规的限制包括:
| • | 除其他事项外,联邦反回扣法规禁止任何人在知情的情况下故意索取、提供、 直接或间接以现金或实物形式收取或提供报酬,以诱使或奖励个人推荐或购买、订购或推荐任何商品或服务,而这些商品或服务可根据联邦和州医疗保健计划(如Medicare和Medicaid)支付。个人或实体不需要实际了解法规或违反法规的具体意图即可实施违规; |
| • | 联邦民事和刑事虚假索赔和民事罚款法律,包括联邦虚假索赔法案,或 FCA,对故意或导致向联邦政府提交虚假、欺诈性或虚假陈述以避免、减少或隐瞒向联邦政府支付资金义务的个人或实体实施刑事和民事处罚,包括通过民事举报人或Qui-tam诉讼。 FCA或 FCA对故意向联邦政府提交或导致向联邦政府提交虚假或欺诈性付款索赔的个人或实体实施刑事和民事处罚,包括通过民事举报人或Qui-tam诉讼来避免、减少或隐瞒向联邦政府支付资金的义务。此外,政府可以断言,包括因违反联邦《反回扣条例》而产生的物品和服务的索赔,就《虚假索赔法》而言,构成欺诈索赔的虚假索赔; |
| • | 1996年的联邦医疗保险携带和责任法案,或HIPAA,对 执行诈骗任何医疗福利计划的计划,或故意伪造、隐瞒或掩盖与医疗福利、项目或服务的交付或付款有关的重大事实或作出任何重大虚假陈述,施加刑事和民事责任 与联邦反回扣法令类似,个人或实体不需要实际了解该法令或具体意图来违反该法令,以 |
76
| • | 联邦医生支付透明度条款,有时被称为《平价医疗法案》(Affordable Care Act)中的阳光法案,要求根据联邦医疗保险(Medicare)、医疗补助(Medicaid)或儿童健康保险计划(Children‘s Health Insurance Program)可报销的药品、设备、生物制品和医疗用品的制造商向卫生与公众服务部(Department Of Health And Human Services)报告与向执业医生(目前定义为包括医生、牙医、视光师、足科医生和脊医)和教学医院转移价值有关的信息从2022年1月1日起,这些报告义务将扩大到包括向某些非医生提供者(如医生助理和执业护士)进行的价值转移; |
| • | HIPAA经2009年《促进经济和临床健康的健康信息技术法案》及其实施条例修订,规定某些覆盖的实体医疗保健提供者、健康计划和医疗信息交换所及其业务伙伴在保护个人可识别健康信息的隐私、安全和传输方面承担义务,这些服务涉及使用或披露个人可识别的健康信息,包括强制性合同条款;以及 |
| • | 类似的州法律法规(如州反回扣和虚假索赔法)可能适用于销售或营销 涉及由非政府第三方付款人(包括私营保险公司)报销的医疗项目或服务的安排和索赔。一些州法律要求制药公司遵守制药行业的自愿合规指南和联邦政府颁布的相关合规指南,此外还要求制药商报告与支付给医生和其他医疗保健提供者或营销支出有关的信息。此外,在某些情况下,许多管理健康信息隐私和安全的州法律在很大程度上各不相同,而且往往不会被HIPAA抢先一步,因此 使合规工作复杂化。 |
努力确保我们未来与第三方的业务安排符合适用的医疗法律和法规,可能会涉及大量成本,并可能需要我们采取或实施其他政策或措施。我们可能面临私人当事人的索赔和诉讼,以及政府当局的索赔、调查和其他 诉讼,涉及我们的业务行为不符合当前或未来涉及适用欺诈和滥用、隐私或数据保护或其他医疗保健法律和法规的当前或未来法规、法规或案例法的指控,法院或政府当局可能会得出结论认为我们没有遵守它们,或者我们可能认为有必要或适当地解决任何此类索赔或其他诉讼。对于任何此类索赔、诉讼或和解,我们可能面临重大民事、刑事和行政处罚、损害赔偿、罚款、其他损害赔偿、监禁、被排除在政府资助的医疗保健计划(如Medicare和Medicaid)之外,以及削减或重组我们的业务。如果我们预期与之开展业务的任何医生或其他提供者或实体被发现不符合适用法律,他们可能会受到刑事、民事或行政制裁,包括被排除在政府资助的医疗保健计划之外。
遵守全球隐私和数据安全要求 可能会给我们带来额外的成本和责任,或者抑制我们在全球收集和处理数据的能力,如果不遵守这些要求,我们可能会受到巨额罚款和处罚,这可能会对我们的业务、财务状况或运营结果产生 实质性的不利影响。
全球信息收集、使用、 保护、共享、传输和其他处理的监管框架正在迅速演变,在可预见的未来可能仍不确定。在全球范围内,我们运营的几乎每个司法管辖区都建立了自己的司法管辖区
77
我们必须遵守的数据安全和隐私框架。例如,收集、使用、披露、转移或以其他方式处理有关欧盟内个人的个人数据,包括个人健康数据和员工数据,受2018年5月在欧洲经济区(EEA)所有成员国生效的欧盟一般数据保护条例(GDPR)的约束。GDPR范围广泛,对处理个人数据的公司提出了许多要求,包括与处理健康和其他敏感数据、征得与个人数据相关的个人同意、 向个人提供有关数据处理活动的信息、实施保障措施以保护个人数据的安全和机密性、提供数据泄露通知,以及在使用第三方处理器时采取某些措施等方面的要求。GDPR通过将个人数据的定义扩大到包括编码数据,并要求更改知情同意做法以及针对临床试验受试者和研究人员的更详细的通知,来告知我们关于在欧洲经济区进行的任何临床试验的义务。此外,GDPR对向欧盟以外的国家(包括美国)转移个人数据实施了严格的规则,因此加强了审查 此类规则应适用于将个人数据从位于欧洲经济区的任何临床试验地点转移到美国。GDPR还允许数据保护当局要求销毁不当收集或使用的个人信息和/或对违反GDPR的行为处以巨额罚款,罚款金额最高可达全球收入的4%或2000万欧元,以金额较大者为准, 并授予对数据主体和消费者协会提起私人诉讼的权利 ,以向监管当局提出投诉,寻求司法补救,并就违反GDPR造成的损害获得赔偿。此外,GDPR还规定,欧盟成员国可以制定自己的 进一步的法律法规,限制个人数据的处理,包括基因数据、生物特征数据或健康数据。
鉴于 其义务的广度和深度,遵守GDPR的要求既严格又耗时,需要大量资源并对我们的技术、系统和实践以及处理或传输在欧盟收集的个人数据的任何第三方合作者、服务提供商、承包商或顾问的技术、系统和实践进行评估。
此外,英国从2020年1月31日起退出欧盟,过渡期截止于2020年12月31日。英国脱欧和英国的持续发展给英国的数据保护监管带来了不确定性,并可能导致我们在英国的业务以及我们对位于英国的个人数据的处理应用新的数据隐私和保护法律和标准。英国已经实施了实质性实施GDPR的立法,欧盟委员会和英国政府于2020年12月24日宣布了一项欧盟-英国贸易与合作协议, 规定欧盟和英国之间的个人数据暂时自由流动,但英国退出欧盟将如何影响英国数据保护法或法规的发展方式,以及英国信息专员将如何监管和执行进出英国的数据传输,仍有待观察。
在美国,与隐私和数据安全相关的各种法律法规可能适用于我们的活动。州和联邦两级也在考虑新的法律,加州等州立法机构已经通过并颁布了隐私法。例如,2020年1月1日生效的《加州消费者隐私法》(CCPA)为加州消费者创造了个人隐私权,并增加了处理某些个人数据的实体的隐私和安全义务。除其他事项外,CCPA要求覆盖的公司向加州消费者提供新的 披露,并为这些消费者提供新的能力,以选择退出某些个人信息的销售,访问并要求删除他们的个人信息,以及接收有关他们的个人 信息如何使用的详细信息。CCPA
78
已多次修改,加利福尼亚州总检察长的附加规定于2020年8月14日生效。然而,CCPA及其解释的各个方面仍然不清楚 。CCPA的影响是重大的,可能需要我们修改我们的数据处理做法和政策,并产生大量的成本和费用来努力遵守。不遵守CCPA可能导致 总检察长采取执法行动并损害我们的声誉。CCPA规定了对违规行为的民事处罚,以及对数据泄露的私人诉权,预计这将增加数据泄露诉讼。此外,在2020年11月的选举中,加州选民通过了一项由隐私权倡导者发起的旨在增强和扩大CCPA的投票倡议,该倡议名为加州隐私权法案(California Privacy Rights Act,简称CPRA)。从2022年1月1日开始,CPRA对在加州开展业务的公司的 消费者数据施加了额外的义务,预计将于2022年7月1日或之前实施法规,并从2023年7月1日开始执行。CPRA对CCPA进行了重大修改, 包括扩大消费者对某些敏感个人信息的权利,这可能会导致进一步的不确定性,并要求我们为遵守规定而产生额外的成本和费用,因为我们可能需要 修改或扩大我们现有的做法。CPRA还创建了一个新的国家机构,该机构将被授予实施和执行CCPA和CPRA的权力。许多州提议或颁布的新立法对收集、存储、使用、保留、披露、转移和以其他方式处理机密、敏感和个人信息的公司施加或有可能施加额外义务。, 并将继续在全国范围内塑造数据隐私环境。 州法律变化迅速,国会正在讨论一项新的联邦数据保护和隐私法,如果颁布,我们将受到该法的约束。此外,所有50个州都有法律,包括有义务向受影响的个人、州官员和其他人提供 计算机数据库安全漏洞的通知,这些数据库包含个人信息。
无数的国际和美国隐私和数据泄露法律并不一致,在发生大范围数据泄露的情况下遵守法律是困难的,而且可能代价高昂。此外,各州一直在频繁修改现有法律,要求 注意不断变化的监管要求。除了政府监管外,隐私倡导者和行业团体已经并可能在未来不时提出自我监管标准。这些标准和其他行业标准可能在法律上或 合同上适用于我们,或者我们也可以选择遵守这些标准。我们预计将继续有关于数据隐私和安全的新的拟议法律法规,我们还无法确定这些未来的法律、法规和标准可能会对我们的业务产生什么影响。 由于GDPR、CCPA、CPRA以及其他与隐私和数据保护相关的法律、法规和其他义务施加了新的且相对繁重的义务,并且这些义务和其他义务的解释和应用存在很大的不确定性 ,我们在满足他们的要求、建立额外的合规机制以及对我们的政策和做法进行必要的更改方面可能会面临挑战,因此可能会产生巨大的成本和开支。
我们通过隐私政策、网站上提供的信息和新闻声明公开声明我们使用和披露个人 信息。尽管我们努力遵守我们的公开声明和文件,但我们有时可能无法遵守或被指控未能遵守。如果发现此类政策或声明具有欺骗性、不公平或与我们的实际做法不符,我们 可能会受到潜在的政府或法律行动的影响。此外,可能会不时有人担心我们的 技术是否会损害我们客户和其他人的隐私。虽然我们相信我们在所有重要方面都遵守与隐私和数据保护相关的行业标准、适用法律和行业行为准则,但不能保证 我们不会受到违反适用法律或行为准则的索赔,不能保证我们能够成功抗辩此类索赔,也不能保证我们不会在违规事件 中受到巨额罚款和处罚。 我们不能保证我们不会受到违反适用法律或行为准则的索赔,也不能保证我们不会在违规事件 中受到巨额罚款和处罚。此外,如果引入了多个州级法律,但标准不一致或相互冲突,并且没有联邦法律可以先发制人,那么遵守这些法律可能会很困难 ,我们可能会受到
79
违规情况下的罚款和处罚。此外,监管部门针对数据安全事件和侵犯隐私行为的执法行动和调查也在持续增加。
此外,如果与我们合作的第三方(如供应商或服务提供商)违反了适用的法律或法规或我们的政策,则此类违规行为也可能使我们的数据面临风险,进而可能对我们的业务产生不利影响。我们或我们的服务提供商未能或被认为未能遵守我们适用的有关隐私或数据保护的政策或通知、我们对第三方的合同或其他义务,或我们与隐私或数据保护有关的任何其他法律义务,都可能导致政府调查或执行 行动、诉讼、索赔和其他诉讼,并可能导致巨额罚款、处罚和其他责任。此外,针对任何索赔、诉讼、监管程序或其他程序进行辩护可能成本高昂、耗时,而且可能需要大量的财力和人力资源。因此,即使我们成功地抵御了可能对我们提起的任何此类诉讼或诉讼,我们的业务也可能受到损害,我们可能遭受 声誉和其他损害。
我们的员工、独立承包商、顾问和供应商可能从事不当行为或其他不当活动, 包括不遵守监管标准和要求以及内幕交易法,这可能会给我们带来重大责任并损害我们的声誉。
我们面临员工、独立承包商、顾问和供应商欺诈或其他不当行为的风险。这些合作伙伴的不当行为 可能包括故意不遵守FDA法规或可比外国监管机构的类似法规、向FDA或可比外国监管机构提供准确信息、遵守制造 标准、遵守联邦和州医疗欺诈和滥用法律法规以及可比外国监管机构制定和执行的类似法律法规、准确报告财务信息或数据,或 向我们披露未经授权的活动。员工不当行为还可能涉及不当使用在临床试验过程中获得的信息,这可能导致监管制裁和严重损害我们的声誉。这可能 包括违反HIPAA、其他美国联邦和州法律,以及非美国司法管辖区的要求,包括欧盟数据保护指令。我们还面临与员工或与我们有关联的其他人的任何内幕交易违规行为相关的风险 。并非总是能够识别和阻止员工的不当行为,我们采取的检测和防止此类行为的预防措施可能无法有效控制 未知或无法管理的风险或损失,或保护我们免受因未能遵守此类法律、标准、法规、指导方针或行为准则而引起的政府调查或其他行动或诉讼。此外, 我们的员工可能会不时因雇佣问题对我们提起诉讼,包括伤害、歧视、工资和工时纠纷、性骚扰、敌对工作环境或其他雇佣问题。如果对我们采取任何此类行动 , 如果我们没有成功地为自己辩护或维护我们的权利,这些行为可能会对我们的业务和运营结果产生重大影响,包括施加巨额罚款或其他 制裁。
与员工事务和管理增长相关的风险
我们未来的成功取决于我们留住关键高管和经验丰富的科学家的能力,以及吸引、留住和激励合格人才的能力。
我们高度依赖首席执行官Christopher Gibson、首席运营官兼总裁Tina Marriott Larson、首席财务官Michael Secora、首席企业发展官Shafique Virani和首席医疗官Ramona Doyle以及其他人员的研发、临床和业务发展专业知识
80
我们的管理、科技和临床团队的主要成员。虽然我们已经与我们的高管签订了聘书协议,但他们中的每一位都可以 随时终止与我们的雇佣关系,或者在未来无法履行我们需要的服务。我们不为我们的任何高管或其他员工提供关键人员保险。此外,我们依赖我们的员工 帮助操作和维修我们的机器人,以及顾问和顾问,包括科学和临床顾问,以帮助我们制定研发和商业化战略。我们的顾问和顾问可能受雇于我们以外的 雇主,并可能根据与其他实体签订的咨询或咨询合同作出承诺,这可能会限制他们对我们的可用性。如果我们无法继续吸引和留住高素质人才,我们实施 增长战略的能力将受到限制。
招聘和留住合格的科研、临床、制造以及销售和营销人员也将是我们成功的关键。失去高管或其他关键员工的服务,包括因病暂时失去服务,可能会阻碍我们研发和商业化目标的实现,并严重 损害我们成功实施业务战略的能力。此外,更换高管和关键员工可能很困难,而且可能需要较长的时间,因为我们行业中拥有成功开发、获得监管部门批准并将产品商业化所需的技能和经验的人员数量有限。从这个有限的人才库招聘的竞争非常激烈,考虑到众多制药和生物技术公司之间对类似人员的竞争,我们可能无法以可接受的条件招聘、培训、留住或激励这些关键 人员。我们还面临着从大学和研究机构招聘科学和临床人员的竞争 。未能在临床试验中取得成功,可能会使招募和留住合格的科学人员变得更具挑战性。
我们在盐湖城(我们的总部所在地)的存在 可能会限制我们招聘人才的能力。我们未来可能要招聘的一些员工将居住在旧金山、纽约、圣地亚哥或波士顿大都市区,他们可能不想 搬迁到盐湖城。与我们竞争合格人才的许多其他制药公司比我们拥有更多的财政和其他资源,不同的风险状况,以及更长的行业历史。它们还可以 提供更多样化的机会和更好的职业晋升机会。对于高素质的应聘者来说,这些特点中的一些可能比我们提供的更具吸引力。如果我们不能继续吸引和留住高素质的 人才,我们发现和开发候选药物的速度和成功率以及我们的业务将受到限制。
我们的员工、主要意见领袖、 或KOL、CRO和顾问可能从事不当行为或其他不当活动,包括不遵守监管标准和要求以及内幕交易。
我们面临员工、KOL、CRO和顾问可能从事欺诈行为或其他非法活动的风险。这些 方的不当行为可能包括故意、鲁莽和/或疏忽的行为或向我们披露违反FDA和其他监管机构规定的未经授权的活动,包括要求向这些机构报告真实、完整和准确信息的法律;美国和国外的医疗欺诈和滥用法律法规;或要求准确报告财务信息或数据的法律。特别是,医疗保健行业的销售、营销、 和业务安排受到旨在防止欺诈、不当行为、回扣、自我交易和其他滥用行为的广泛法律法规的约束。这些法律法规可能会限制或禁止广泛的定价、折扣、营销和促销、销售佣金、客户奖励计划和其他业务安排。受这些法律约束的活动还涉及不当使用在临床试验过程中获得的信息,或在我们的临床前研究或临床试验中创建虚假数据,这可能会导致监管制裁,并对
81
我们的声誉。我们打算在本次发售完成之前采用适用于我们所有员工的行为准则,但并非总是能够识别和阻止员工和其他第三方的不当行为 ,我们为发现和防止此类行为而采取的预防措施可能无法有效控制未知或无法控制的风险或损失,或保护我们免受因未能遵守这些法律或法规而引起的政府调查或其他行动或 诉讼。此外,我们还面临这样的风险,即有人可能会指控此类欺诈或其他不当行为,即使没有发生。如果对我们提起任何此类诉讼,而 我们未能成功为自己辩护或维护权利,这些诉讼可能会对我们的业务产生重大影响,包括施加民事、刑事和行政处罚、损害赔偿、罚款、可能 被排除在联邦医疗保险、医疗补助和其他联邦医疗保健计划之外、合同损害、声誉损害、利润和未来收益减少以及我们的业务缩减,任何这些都可能对我们运营业务的能力和我们的运营结果产生不利影响。
我们预计将扩展我们的开发和监管能力,并可能实施 销售、营销和分销能力,因此,我们在管理增长方面可能会遇到困难,这可能会扰乱我们的运营。
截至2021年1月14日,我们有209名全职员工。我们预计我们的员工数量和业务范围将大幅增长,特别是作为一家上市公司,在产品开发、监管事务以及如果我们的候选药物获得上市批准、销售、营销和分销的情况下,更是如此。为了管理我们预期的 未来增长,我们必须继续实施和完善我们的管理、运营和财务系统,扩大我们的设施,并继续招聘和培训更多合格的人员。由于我们的财力有限,而且我们的管理团队在管理一家具有如此预期增长的公司方面的经验也有限,我们可能无法有效地管理我们业务的扩张或招聘和培训更多合格的人员。我们 业务的扩展可能会导致巨额成本,并可能转移我们的管理和业务开发资源。任何无法管理增长的情况都可能推迟我们业务计划的执行或扰乱我们的运营。
我们可能会收购更多业务或产品、结成战略联盟或与第三方建立合资企业,我们认为这些合资企业将补充或扩大我们现有的业务。如果我们收购市场或技术前景看好的企业,如果我们不能成功地将它们与我们现有的运营和公司文化整合在一起,我们可能无法实现收购这些企业的好处。 我们在开发、制造和营销因战略联盟或收购而产生的任何新产品时可能会遇到许多困难,这些新产品会延迟或阻碍我们实现预期收益或增强我们的业务 。我们不能向您保证,在任何此类收购之后,我们将实现预期的协同效应,以证明这笔交易是合理的。
产品责任 针对我们的诉讼可能导致我们承担重大责任,并可能限制我们可能开发的任何候选药物的商业化。
我们在人体临床试验中面临与候选药物测试相关的固有产品责任风险,如果我们将我们可能开发的任何药物商业化销售,我们将面临更大的 风险。如果我们不能成功地为自己辩护,声称我们的候选药物或药物造成了伤害,我们可能会招致重大责任。无论是非曲直或最终 结果如何,责任索赔可能会导致:
| • | 对我们可能开发的任何候选药物或疗法的需求减少; |
| • | 损害我们的声誉和媒体的严重负面关注; |
| • | 临床试验参与者退出; |
82
| • | 相关诉讼的辩护费用较高; |
| • | 对试验参与者或患者给予巨额金钱奖励; |
| • | 收入损失;以及 |
| • | 无法将我们的候选药物商业化。 |
虽然我们维持产品责任保险,包括我们赞助的临床试验的承保范围,但它可能不足以覆盖我们可能产生的所有 责任。我们预计,随着我们开始更多的临床试验,如果我们成功地将任何候选药物商业化,我们将需要增加我们的保险覆盖范围。保险覆盖市场越来越昂贵,随着我们临床项目规模的扩大,保险覆盖成本将会增加。我们可能无法以合理的费用或足够的金额维持保险范围,以应付可能出现的任何责任。
与我们的普通股和本次发行相关的风险
我们是《就业法案》中定义的新兴成长型公司,将能够利用降低适用于新兴成长型公司的披露要求,这可能会降低我们的普通股对投资者的吸引力,并 对我们普通股的市场价格产生不利影响。
我们是一家新兴的成长型公司,正如2012年的Jumpstart Our Business Startups Act或JOBS Act所定义的那样。我们将一直是一家新兴的成长型公司,直到以下较早的一天:i)本财年总收入达到或超过10.7亿美元的最后一天;ii)本次发行完成五周年后的下一财年的最后一天 ;iii)我们在过去三年中发行了超过10亿美元的不可转换债券的日期;或iv)根据美国证券交易委员会(Securities And Exchange Commission)的规则,我们被视为大型加速申报机构的日期 ,这意味着截至前一年6月30日,非关联公司持有的我们普通股的市值超过7亿美元。对于 ,只要我们仍然是新兴成长型公司,我们就被允许并打算依赖于适用于其他非新兴成长型公司的上市公司的某些披露要求的豁免。这些豁免包括:
| • | 未被要求遵守2002年萨班斯-奥克斯利法案第404条或第404条的审计师认证要求; |
| • | 未被要求遵守上市公司会计监督委员会(br}可能采纳的关于强制轮换审计公司的任何要求或提供有关审计和财务报表的额外信息的审计师报告的补充; |
| • | 除了任何要求的未经审计的中期财务报表外,仅提供两年的已审计财务报表 ,并相应减少管理层对财务状况和运营结果披露的讨论和分析; |
| • | 减少有关高管薪酬的披露义务;以及 |
| • | 免除就高管薪酬和股东批准之前未批准的任何金降落伞支付进行不具约束力的咨询投票的要求 。在这份招股说明书中,我们没有包括所有与高管薪酬相关的信息,如果我们不是一家新兴的成长型公司,这些信息就会被要求提供。 |
我们可能会选择利用部分(但不是全部)可用的豁免。我们利用了此 招股说明书中减轻的报告负担。特别是,我们只提供了两年的审计财务报表,没有包括所有的高管薪酬。
83
如果我们不是一家新兴成长型公司,则需要提供的信息。我们无法预测,如果我们依赖这些豁免,投资者是否会发现我们的普通股吸引力下降。 如果一些投资者因此发现我们的普通股吸引力下降,我们的普通股交易市场可能会变得不那么活跃,我们的股价可能会更加波动。
此外,《就业法案》规定,新兴成长型公司可以利用延长的过渡期来遵守新的或修订的 会计准则。这使得新兴成长型公司可以推迟采用某些会计准则,直到这些准则适用于私营公司。在我们仍是一家新兴成长型公司期间,我们已选择将延长的过渡期用于新的或 修订的会计准则;但是,我们可能会提前采用某些新的或修订的会计准则。
尽管我们仍在评估《就业法案》,但我们目前打算利用部分(但不是全部)降低的监管和报告要求 ,只要我们符合新兴成长型公司的资格就可以使用这些要求。?我们已选择利用这一豁免,因此,我们不受 其他非新兴成长型公司的上市公司相同的新会计准则或修订后的会计准则的约束。因此,美国公认会计原则规则或其解释的变化、采用新的指导方针或应用现有指导方针来改变我们的业务 可能会对我们的财务状况和运营结果产生重大影响。此外,只要我们有资格成为新兴成长型公司,我们的独立注册会计师事务所就不需要提供关于我们对财务报告的内部控制的有效性的证明报告,这可能会增加我们在财务报告内部控制中的重大弱点或重大缺陷未被发现的风险。 同样,只要我们有资格成为新兴成长型公司,我们就可以选择不向您提供某些信息,包括某些财务信息和关于我们高管薪酬的某些信息, 。 同样,只要我们有资格成为新兴成长型公司,我们就可以选择不向您提供某些信息,包括某些财务信息和有关我们高管薪酬的某些信息, 这可能会增加我们财务报告内部控制中的重大弱点或重大缺陷未被发现的风险。 这可能会增加投资者和证券分析师评估我们公司的难度。我们无法预测投资者是否会发现我们的普通股吸引力下降 ,因为我们可能依赖这些豁免。如果一些投资者因此发现我们的普通股吸引力下降,我们的普通股交易市场可能会变得不那么活跃,我们的股价可能会更加波动,可能会下跌。
我们普通股的价格可能会波动很大,这可能会导致我们普通股的购买者在此次 发售中蒙受重大损失。
我们的股票价格可能会波动。一般的股票市场,特别是生物技术公司的市场都经历了极端的波动,这种波动往往与特定公司的经营业绩无关。由于这种波动,你可能无法以或高于首次公开募股(IPO)的价格出售普通股。我们普通股的市场价格可能受到许多因素的影响,包括:
| • | 有竞争力的产品或技术的成功; |
| • | 我们候选药物或我们竞争对手的临床试验结果; |
| • | 美国和其他国家的法规或法律发展; |
| • | 与专利申请、已颁发的专利或者其他专有权利有关的开发或者争议; |
| • | 关键人员的招聘或者离职; |
| • | 与我们的任何候选药物或临床开发计划相关的费用水平; |
| • | 我们努力发现、开发、获取或许可额外 候选药物或产品的结果; |
84
| • | 证券分析师对财务业绩、发展时间表或建议的估计的实际或预期变化 ; |
| • | 我们的财务业绩或那些被认为与我们相似的公司的财务业绩变化; |
| • | 改变医疗保健支付制度的结构; |
| • | 制药和生物技术行业的市场状况; |
| • | 一般经济、工业和市场状况;以及 |
| • | 本风险因素一节中描述的其他因素。 |
在公开市场上出售我们的大量普通股可能会导致我们的股票价格下跌。
如果我们的现有股东在本招股说明书中讨论的锁定和其他法律限制失效后,在公开市场上出售或表示有意出售大量普通股,我们普通股的市场价格可能会下跌。根据截至2020年12月31日已发行普通股的数量(在转换基础上),本次发行完成后,我们将拥有总计 股普通股,包括非既得性限制性普通股,并假设不行使承销商购买额外股份的选择权。在这些股票中,截至本招股说明书的日期, 约有我们普通股的股份,加上在行使承销商购买额外股份选择权时出售的任何股份,将在本次发行后立即在公开市场上自由流通,不受限制, 假设当前股东不购买本次发行的股票。但是,承销商的代表可自行 决定是否允许我们的高级管理人员、董事和其他受这些禁售协议约束的股东在禁售协议期满前出售股份。
与本次发行相关的锁定协议将自本 招股说明书发布之日起180天到期。锁定协议到期后,根据截至2020年12月31日已发行的已转换普通股的数量,至多 股普通股将有资格在公开 市场上出售,其中%的普通股由董事、高管和其他附属公司持有,并将受到1933年证券法(修订本)或证券法第144条的某些限制。
本次 发售完成后,根据我们的股权激励计划,在各种归属时间表、锁定协议以及证券法第144条和第701条的规定允许的范围内,根据我们的股权激励计划,受未偿还期权约束或预留供未来发行的普通股股票将 有资格在公开市场出售。如果这些 额外的普通股被出售,或者如果人们认为它们将在公开市场上出售,我们普通股的市场价格可能会下降。
本次发行后,持有约 股我们普通股的持有者将有权根据证券法获得与其股票登记相关的权利,但须遵守上述锁定协议。根据证券法注册这些股票将导致这些股票在证券法下不受限制地自由交易,但关联公司购买的股票除外。这些股东的任何证券出售都可能对我们普通股的 市场产生重大不利影响。
我们的普通股可能不会形成活跃的交易市场,您可能无法以或高于 首次公开募股(IPO)的价格转售您的股票。
在这次发行之前,我们的普通股还没有公开市场。虽然我们的普通股已获准在纳斯达克股票市场上市,但活跃的交易市场
85
此次发行后,我们的股票可能永远不会发展或持续。我们普通股的首次公开募股价格将通过我们与 承销商之间的谈判确定。这一首次公开募股的价格可能不能代表本次发行后我们普通股的市场价格。如果我们的普通股没有活跃的交易市场,投资者可能无法以首次公开募股(IPO)价格或高于首次公开募股(IPO)价格或在他们想要出售的时间出售普通股 。
本次发行后,我们的高管、董事、主要股东和 他们的关联公司将继续对我们公司实施重大控制,这将限制您影响公司事务的能力,并可能延迟或阻止公司控制权的变更。
在本次发售完成后,不考虑他们在本次发售中购买的任何普通股,我们的高管、董事、主要股东及其关联公司现有的 持有量将相当于我们已发行普通股的总实益所有权,约占我们已发行普通股的 %,假设我们没有行使在此次发售中收购额外普通股的选择权 ,并假设我们发行了本招股说明书封面所列的普通股数量。因此,如果这些股东一起行动,他们将能够影响我们的管理和事务,并控制提交给我们股东审批的 事项的结果,包括选举董事以及出售、合并、合并或出售我们全部或几乎所有资产。这些股东以远低于本次发行普通股价格的 收购普通股,这些股东可能拥有与本次发行投资者不同的普通股权益,这些股东的投票权 集中可能会对我们普通股的价格产生不利影响。此外,这种所有权集中可能通过以下方式对我们普通股的市场价格产生不利影响:
| • | 延迟、推迟或阻止我们控制权的变更; |
| • | 妨碍涉及我们的合并、合并、收购或其他业务合并;或 |
| • | 阻止潜在收购者提出收购要约或以其他方式试图控制我们。 |
有关我们的高管、董事、主要股东及其附属公司对我们已发行普通股的所有权的更多信息,请参见本招股说明书中的主要股东。
如果您在此次发行中购买我们的普通股,您的股票的账面价值将立即大幅稀释 。
您在此次发行中购买的普通股的有形净账面价值将立即大幅稀释。 您购买的普通股的账面净值将立即大幅稀释。假设首次公开募股(IPO)价格为每股$1,也就是本招股说明书封面上规定的价格区间的中点 ,此次发行普通股的购买者将立即经历普通股有形账面净值每股$s的稀释。此外,在本次发行中购买普通股的投资者将贡献 股东自成立以来投资总额的%,但只拥有已发行普通股的%。过去,我们发行期权和其他证券来收购 普通股,价格远远低于首次公开募股(IPO)价格。在这些已发行证券最终被行使的情况下,在此次发行中购买普通股的投资者将遭受进一步稀释。有关在此次发行中向新投资者进行稀释的更详细说明,请参阅 n稀释。
86
我们在如何使用此次发行的收益方面拥有广泛的自由裁量权,可能无法有效地使用这些收益, 这可能会影响我们的运营结果,并导致我们的股价下跌。
我们将有相当大的自由裁量权来应用此次发行的净收益 。我们打算利用此次发行的净收益为我们的药物发现平台提供资金,寻求战略合作,并通过临床开发努力推进候选药物的研发。我们还打算 利用此次发行所得资金扩大我们的基础设施和设施,以支持我们的开发努力,为新的和正在进行的研究活动和新药候选药物提供资金,并用于营运资本和其他一般企业用途,其中 可能包括招聘额外人员的资金、资本支出和上市公司的运营成本。投资者将依赖管理层的判断,对我们使用此次发行的净收益余额的具体意图只有有限的信息 。我们可以将净收益用于不会为我们的股东带来显著回报或任何回报的目的。此外,在使用之前,我们可能会将此次发行的净收益 以不产生收入或贬值的方式进行投资。
由于我们预计在可预见的将来不会对我们的 股本支付任何现金股息,因此资本增值(如果有的话)将是您唯一的收益来源。
我们从未为我们的股本申报或支付过现金 股息。我们目前打算保留我们未来的所有收益(如果有的话),为我们业务的增长和发展提供资金。此外,任何现有或未来债务协议的条款可能会阻止我们支付 股息。因此,在可预见的未来,我们普通股的资本增值(如果有的话)将是您唯一的收益来源。
我们将因作为上市公司运营而增加成本 ,我们的管理层将需要投入大量时间在新的合规计划上。
作为一家上市公司,特别是在我们不再是一家新兴的成长型公司之后,我们将招致大量的法律、会计和 其他费用,这些费用是我们作为私人公司没有招致的。此外,2002年的“萨班斯-奥克斯利法案”(Sarbanes-Oxley Act)以及随后由证券交易委员会(Securities And Exchange Commission)和纳斯达克证券市场(Nasdaq Stock Market)实施的规则对上市公司提出了各种要求,包括建立和维持有效的披露、财务控制和公司治理做法。我们的管理层和其他人员将需要投入大量时间来实施这些合规性计划 。此外,这些规则和法规将增加我们的法律和财务合规成本,并将使一些活动更加耗时和昂贵。例如,我们预计这些规章制度可能会增加 我们获得董事和高级管理人员责任保险的难度和成本。
根据第404条,我们将被要求 提交我们管理层关于财务报告内部控制的报告,包括由我们的独立注册会计师事务所出具的财务报告内部控制的证明报告。然而,虽然我们仍然是一家新兴的成长型公司,但我们不会被要求包括由我们的独立注册会计师事务所出具的财务报告内部控制的证明报告。为了在 规定的期限内达到第404条的合规性,我们将参与记录和评估我们对财务报告的内部控制的过程,这既成本高昂,又具有挑战性。在这方面,我们将需要继续投入内部资源,可能需要 聘请外部顾问并采用详细的工作计划,以评估和记录财务报告内部控制的充分性,继续采取适当步骤改进控制流程,通过测试验证控制是否按照文件规定运行,并实施持续的报告和改进财务报告内部控制流程。尽管我们做出了努力,但我们和我们的独立注册会计师事务所都存在风险,即我们或我们的独立注册会计师事务所都不能 在
87
根据第404条的要求,我们对财务报告的内部控制有效的规定时限。这可能会导致金融市场的不良反应,因为 对我们财务报表的可靠性失去了信心。此外,如果我们不能继续满足这些要求,我们可能无法继续在纳斯达克股票市场上市。
我们修订和重述的公司注册证书以及修订和重述的法律和特拉华州法律中的条款可能会阻止、推迟或阻止 我们公司控制权的变更或我们管理层的变更,从而压低我们普通股的市场价格。
我们修订和 重述的公司注册证书以及修订和重述的章程将在本次发行结束后生效,其中包含的条款可能会阻止、推迟或阻止 本公司股东可能认为有利的本公司控制权变更或管理层变更,从而压低本公司普通股的市场价格。除其他事项外,这些条文包括:
| • | 建立分类董事会,不是所有董事会成员都是一次选举产生的; |
| • | 只允许董事会确定董事会人数和填补董事会空缺; |
| • | 授权发行空白支票优先股,我们的董事会可以用这些优先股来实施股东权利计划 (也称为毒丸计划); |
| • | 取消我们的股东召开股东特别会议的能力; |
| • | 禁止股东在书面同意下采取行动,这要求所有股东行动必须在我们的 股东会议上采取; |
| • | 禁止累积投票; |
| • | 授权本公司董事会修改公司章程; |
| • | 确定提名进入董事会或提出股东可在年度股东大会上采取行动的事项的事先通知要求;以及 |
| • | 需要股东的绝对多数票才能修改上述一些条款。 |
此外,特拉华州一般公司法(DGCL)第203条禁止特拉华州上市公司 与有利害关系的股东(通常是与其关联公司一起拥有或在过去三年内拥有我们15%有表决权股票的人)在 成为利益股东的交易日期后三年内与该股东进行企业合并,除非该企业合并以规定的方式获得批准。
我们修订和重述的公司注册证书、修订和重述的公司章程或特拉华州法律中任何具有延迟或阻止控制权变更效果的条款 都可能限制我们的股东从他们的 股票获得溢价的机会,还可能影响一些投资者愿意为我们的普通股支付的价格。
我们修订和重申的章程规定, 将在本次发售结束后生效,规定特拉华州衡平法院和美利坚合众国联邦地区法院将是我们和我们股东之间几乎所有纠纷的独家论坛,这可能会限制我们的股东获得有利的司法论坛来处理与我们或我们的董事、高级管理人员或员工的纠纷。(br} =
我们修订和重述的附则将在本次发售结束后生效,规定特拉华州衡平法院 或者,如果衡平法院没有
88
位于特拉华州的另一个州法院或特拉华州地区的联邦地区法院是以下案件的独家审判庭,但该法院 认定存在不受该法院管辖的不可缺少的一方,且不可缺少的一方在裁决后10天内不同意该法院的属人管辖权的任何索赔除外,该法院被授予 该法院以外的法院或法院的独家管辖权,或者该法院没有标的物管辖权:
| • | 代表我们提起的任何派生诉讼或法律程序; |
| • | 主张违反受托责任的诉讼; |
| • | 根据DGCL、我们修订和重述的公司证书或我们修订和重述的章程对我们提出索赔的任何诉讼;以及 |
| • | 任何主张受内政原则管辖的针对我们的索赔的行为。 |
本条款不适用于为执行《交易法》规定的义务或责任而提起的诉讼,也不适用于美国联邦 法院拥有专属管辖权的任何其他索赔。我们修订和重述的章程进一步规定,美利坚合众国联邦地区法院将是解决根据《证券法》提出诉因的任何投诉的独家论坛。
这些排他性论坛条款可能会限制股东在司法论坛上提出其认为有利于与我们或我们的董事、高级管理人员或其他员工发生纠纷的索赔的能力,这可能会阻碍针对我们以及我们的董事、高级管理人员和其他员工的诉讼。购买或以其他方式获得我们任何 证券的任何权益的任何个人或实体应被视为已知悉并同意这些规定。法院是否会执行这些条款还存在不确定性,其他公司章程文件中类似选择的法院条款的可执行性在法律程序中受到了挑战。法院可能会发现这些类型的条款不适用或不可执行,如果法院发现我们修订和重述的附则 中的任何一项排他性论坛条款在诉讼中不适用或不可执行,我们可能会产生与在其他司法管辖区解决纠纷相关的额外费用,这可能会严重损害我们的业务。
如果证券分析师不发表关于我们业务的研究或报告,或者如果他们发表对我们股票的负面评价,我们股票的价格可能会 下跌。
我们普通股的交易市场将在一定程度上依赖于行业或金融分析师发布的关于我们或我们业务的研究和报告 。我们可能永远不会获得行业或金融分析师的研究报道。如果没有或很少有分析师开始对我们进行报道,我们股票的交易价格可能会下跌。即使我们确实获得了分析师的报道,如果一个或 个跟踪我们业务的分析师下调了他们对我们股票的评估,我们的股票价格也可能会下跌。如果其中一位或多位分析师停止跟踪我们的股票,我们的股票可能会在市场上失去可见性,进而 可能会导致我们的股价下跌。
我们可能会受到证券诉讼的影响,这是昂贵的,可能会转移管理层的注意力。
我们普通股的市场价格可能会波动。股票市场,特别是纳斯达克股票市场和生物技术公司, 经历了极端的价格和成交量波动,这些波动往往与这些公司的经营业绩无关或不成比例。在过去,经历过股票市场价格波动的公司 都会受到证券集体诉讼的影响。我们未来可能会成为这类诉讼的目标。针对我们的证券诉讼可能导致巨额成本,并将我们管理层的注意力从其他业务上转移 ,这可能会严重损害我们的业务。
89
我们的实际运营结果可能与我们提供的任何指导意见大不相同。
我们可能会不时在季度收益电话会议、季度收益发布或其他方面提供有关我们未来业绩的指导 ,这代表了我们管理层截至发布日期的估计。该指导将包括前瞻性陈述,将基于我们管理层准备的预测。我们的注册会计师 、任何其他独立专家或外部机构都不会编制或审查这些预测。因此,该等人士不会就该等预测发表任何意见或作出任何其他形式的保证。
预测基于多个假设和估计,虽然这些假设和估计是以数字细节表示的,但本质上会受到重大的 业务、经济和竞争不确定性和意外事件的影响,其中许多是我们无法控制的,基于对未来业务决策的特定假设,其中一些将发生变化。我们 发布指引的主要原因是为我们的管理层提供一个基础,让他们与分析师和投资者讨论我们的业务前景。对于任何此类第三方发布的任何预测或报告,我们不承担任何责任。
指导必须是投机性的,可以预期,我们提供的任何指导所依据的部分或全部假设将 不会实现或将与实际结果大不相同。因此,我们的指导只是对管理层认为截至发布之日可实现的情况的估计。实际结果可能与我们的指导不同,变化可能 是实质性的。
作为上市公司的结果,我们将有义务制定并保持对财务报告的适当和有效的内部控制 。如果不能保持这些内部控制的充分性,可能会对投资者对我们公司的信心产生不利影响,从而影响我们普通股的价值。
我们的首席财务官不是上市公司的首席财务官,我们的首席执行官也不是上市公司的首席执行官。这两家公司都没有通过首次公开募股(IPO)参与私人公司向上市公司的转型。根据《萨班斯-奥克斯利法案》(Sarbanes-Oxley Act)第404条,我们将被要求 从我们成为上市公司后向美国证券交易委员会第二次提交Form 10-K年度报告开始,提交我们管理层关于财务报告内部控制的报告。此 评估需要包括披露我们管理层在财务报告内部控制中发现的任何重大弱点。然而,我们的独立注册会计师事务所在我们不再是一家新兴成长型公司之后,将不再需要证明我们财务报告的内部控制 的有效性,直到我们被要求提交给SEC的第一份年度报告。在我们被要求获得审计师 认证的时候,如果我们有重大弱点,我们将从我们的独立注册会计师事务所收到关于我们财务报告内部控制的负面意见。
为了在规定的期限内达到第404条的要求,我们将着手记录和评估我们对财务报告的内部控制 ,这既昂贵又具有挑战性。在这方面,我们需要继续投入内部资源,包括聘请更多的财务和会计人员,可能聘请外部顾问 ,并采用详细的工作计划来评估和记录财务报告内部控制的充分性,继续采取适当步骤改进控制程序,通过测试验证控制是否按文档所述发挥作用,以及 实施持续的报告和改进财务报告内部控制的过程。在评估我们的内部控制时,如果我们发现财务报告的内部控制存在一个或多个重大缺陷, 我们将无法断言
90
我们对财务报告的内部控制是有效的。我们不能向您保证,未来我们对财务报告的内部控制不会存在重大缺陷或重大缺陷。 任何未能对财务报告进行内部控制的行为都会严重抑制我们准确报告财务状况或经营结果的能力。如果我们不能确定我们对财务报告的内部控制 是有效的,或者如果我们的独立注册会计师事务所确定我们对财务报告的内部控制存在重大缺陷或重大缺陷,我们可能会对我们的财务报告的准确性和完整性失去信心 ,我们普通股的市场价格可能会下跌,我们可能会受到纳斯达克股票市场、SEC或其他监管机构的制裁或调查 。未能弥补我们在财务报告内部控制方面的任何重大缺陷,或未能实施或维护上市公司要求的其他有效控制系统,也可能会限制我们未来进入资本市场的机会 。
91
关于前瞻性陈述的特别说明
本招股说明书包含前瞻性陈述,这些陈述基于我们管理层的信念和假设,以及我们管理层目前可获得的信息。前瞻性陈述主要包含在招股说明书摘要、风险因素、管理层对财务状况和经营结果的讨论和分析、行业概述和经营业绩的讨论和分析、行业概述和经营业绩等部分。除本招股说明书中包含的历史事实陈述外,其他所有陈述,包括有关本招股说明书中包含的未来经营业绩和财务状况、业务战略、发展计划、计划中的临床前研究和临床试验、临床试验的未来结果、预期研发成本、监管战略、时间和可能性的陈述。在某些情况下,您可以通过以下术语来识别前瞻性陈述,例如:可能、将会、应该、?将、?会、 ?预期、?计划、?预期、?可能、?意图、?目标、?项目、?沉思、?相信、?估计、?预测、?潜在、?或继续?或这些术语或其他类似表达的否定。本招股说明书中包含的前瞻性陈述包括但不限于以下陈述:
| • | 我们研发计划的启动、时间、进度、结果和成本,以及我们当前和未来的临床前和临床研究 ,包括有关研究或试验和相关准备工作的设计、启动和完成的时间以及相关准备工作的声明,试验结果将在多长时间内可用,以及我们的研究和开发计划; |
| • | 我们的临床试验证明候选药物的安全性和有效性以及其他积极结果的能力; |
| • | 我们的第三方战略合作伙伴继续与我们的开发候选药物和研究药物相关的研发活动的能力和意愿 ; |
| • | 未来与第三方就我们的研究药物和任何 其他批准产品商业化达成的协议; |
| • | 监管申请和批准的时间、范围和可能性,包括调查性新药 申请的时间和美国食品和药物管理局(FDA)对我们目前的候选药物和任何其他未来候选药物的最终批准,包括我们保持任何此类批准的能力; |
| • | 外国监管机构提交和批准的时间、范围或可能性,包括我们保持此类 批准的能力; |
| • | 我们候选药物的市场机会的大小,包括我们对患有我们目标疾病的患者数量的估计; |
| • | 我们识别临床开发可行的新药候选药物的能力,以及我们期望通过推理或其他方式识别这些候选药物的加速速度; |
| • | 我们的预期是,将为我们带来最大价值的资产是那些我们将在未来使用我们的数据集和工具确定的资产 ; |
| • | 我们有能力开发和推进我们当前的候选药物和计划,并成功完成临床 研究; |
| • | 相对于传统的药物发现模式,我们能够减少时间或成本或增加研发成功的可能性; |
| • | 我们在基础设施、数据集、生物学和技术工具以及药物发现平台方面的改进能力和改进速度,或从此类改进中实现收益的能力; |
92
| • | 我们的期望与我们的生物蜂巢-1超级计算机的性能和好处有关。 |
| • | 我们在药物发现合作中实现资源和现金投资回报的能力; |
| • | 我们能够像一家科技公司一样进行扩展,每年向我们的管道中添加比以前更多的计划; |
| • | 我们在竞争激烈的市场中成功竞争的能力; |
| • | 我们的制造、商业化、营销能力和战略; |
| • | 我们与候选药物商业化相关的计划(如果获得批准),包括重点地理区域和销售 战略; |
| • | 我们对我们候选药物的批准和与其他药物联合使用的期望; |
| • | 我们目前的候选药物和我们 可能开发的其他候选药物的市场接受度和临床实用性的速度和程度; |
| • | 我们的竞争地位和已有或可能获得的竞争性疗法的成功; |
| • | 我们对我们将在临床试验中登记的患者数量和登记时间的估计; |
| • | 我们候选药物的有益特征、安全性、有效性和治疗效果; |
| • | 我们与候选药物进一步开发相关的计划,包括我们可能寻求的其他适应症; |
| • | 美国、欧洲和其他司法管辖区的现有法规和法规动态; |
| • | 我们充分保护和执行我们的知识产权和专有技术的能力,包括我们能够为我们目前的候选药物和我们可能开发的其他候选药物建立和维护的知识产权保护范围、获得专利保护、现有专利条款的延长(如果可用)、 第三方持有的知识产权的有效性、保护我们的商业秘密,以及我们不侵犯、挪用或以其他方式侵犯任何第三方知识产权的能力; |
| • | 当前或未来任何知识产权诉讼的影响,以及我们对 侵犯、挪用或其他侵犯任何第三方知识产权的索赔进行辩护的能力; |
| • | 我们有能力跟上新科技发展的步伐; |
| • | 我们能够利用我们所依赖的第三方开源软件和基于云的基础设施; |
| • | 我们的保单是否足够及其承保范围; |
| • | 大流行、流行病或传染病爆发(如新冠肺炎)或自然灾害的潜在影响,以及此类爆发或自然灾害对我们的业务和财务业绩的影响; |
| • | 我们维护技术运营基础设施以避免错误、延迟或网络安全漏洞的能力; |
93
| • | 我们继续依赖第三方对我们的候选药物进行额外的临床试验,并 生产用于临床前研究和临床试验的候选药物; |
| • | 我们有能力获得开发、生产或商业化我们的候选药物所必需或需要的任何合作、许可或其他安排,并就这些合作、许可或其他安排进行谈判; |
| • | 如果获得批准,我们目前的候选药物和我们可能开发的其他候选药物的定价和报销; |
| • | 我们对费用、未来收入、资本需求和额外融资需求的估计; |
| • | 我们的财务业绩; |
| • | 我们估计现有现金和现金等价物将足以为我们未来的运营费用和资本支出需求提供资金的期间; |
| • | 我们有能力筹集大量额外资金; |
| • | 当前和未来法律法规的影响,以及我们遵守我们现在或可能遵守的所有法规的能力; |
| • | 需要增聘人员,以及我们吸引和留住这些人员的能力; |
| • | 任何当前或未来诉讼的影响,这些诉讼可能在正常业务过程中发生,且辩护成本较高(br}); |
| • | 我们对根据《就业法案》获得新兴成长型公司资格的期限的期望; |
| • | 我们对现有资源的预期使用和此次发行的净收益;以及 |
| • | 其他风险和不确定性,包括标题“风险因素”下列出的风险和不确定性。 |
这些前瞻性陈述主要基于我们目前对我们的业务、我们经营的行业以及我们认为可能会影响我们的业务、财务状况、运营结果和前景的财务趋势的预期和预测,这些前瞻性陈述不能保证未来的业绩或发展。这些前瞻性陈述 仅说明截至本招股说明书发布之日的情况,并受本招股说明书的风险因素一节和其他部分所述的一系列风险、不确定性和假设的影响。由于前瞻性陈述固有地受到风险和不确定性的影响,其中一些风险和不确定性是无法预测或量化的,因此您不应依赖这些前瞻性陈述作为对未来事件的预测。我们的前瞻性 陈述中反映的事件和情况可能无法实现或发生,实际结果可能与前瞻性陈述中预测的结果大不相同。除非适用法律另有要求,否则在分发本招股说明书之前,无论是由于任何新信息、未来事件或其他原因,我们都不打算公开更新或修改本文中包含的任何前瞻性 陈述。
在 此外,我们认为的声明和类似的声明反映了我们对相关主题的信念和意见。这些陈述基于截至本招股说明书发布之日向我们提供的信息,虽然我们认为 此类信息构成此类陈述的合理基础,但此类信息可能是有限或不完整的,我们的陈述不应被解读为表明我们已对所有潜在的 可用的相关信息进行了详尽的调查或审查。这些陈述本质上是不确定的,提醒您不要过度依赖这些陈述。
94
市场、行业和其他数据
本招股说明书包含有关我们的行业、我们的业务和候选药物市场的估计、预测和其他信息, 包括这些市场的估计规模和某些医疗条件的发生率的数据。我们从内部估计和研究以及学术和行业研究、出版物、调查以及包括政府机构在内的第三方进行的研究中获得了本招股说明书中列出的行业、市场和类似数据。在某些情况下,我们并未明确提及此数据的来源。基于估计、 预测、预测、市场研究或类似方法的信息本质上会受到不确定因素的影响,实际事件或情况可能与本信息中假设的事件和情况大不相同。虽然我们相信 我们使用的第三方数据是可靠的,但我们没有单独验证此数据。任何行业预测都基于各种专业人士的数据(包括第三方数据)、模型和经验,并基于各种 假设,所有这些假设都可能在不另行通知的情况下发生变化。此外,虽然我们相信我们的内部研究是可靠的,但此类研究尚未得到任何第三方的证实。虽然我们不知道本文中提供的关于市场数据的任何错误陈述 ,但行业预测和预测涉及风险和不确定性,可能会根据各种因素(包括标题中讨论的风险因素)而发生变化。
95
收益的使用
我们估计,在本次发行中出售我们普通股的净收益约为 百万美元,或者,如果承销商行使其全额购买额外 股票的选择权,那么根据假设的首次公开募股(IPO)价格每股$(这是本招股说明书封面上价格区间的中点),以及扣除承销折扣和佣金以及我们预计应支付的发售费用后,我们将获得约 美元的净收益。
假设本招股说明书封面所列的我们发行的股票数量保持不变,在扣除预计承销的 折扣和佣金以及预计应支付的发售费用后, 假设首次公开募股(IPO)每股价格每增加或减少1.00美元,我们从本次发行中获得的净收益将增加或减少约 百万美元。同样,假设假设首次公开募股价格保持不变,在扣除估计承销折扣和 佣金以及估计应支付的发售费用后,我们发行的股票数量每增加或减少100万股,我们从此次发行中获得的净收益将增加或减少(视情况而定) 。
此次发行的主要目的是获得额外资本以支持我们的 运营,为我们的普通股建立一个公开市场,并为我们未来进入公共资本市场提供便利。
我们目前打算 使用此次发行的净收益,以及我们现有的现金和现金等价物,如下所示:
| • | 大约100万至 百万美元用于资助研究和开发活动,包括但不限于我们平台的运营、药物发现和研究计划,以及我们正在进行的计划的持续开发,包括设计和进行临床前研究和临床试验,以及为支持我们的流水线的基础设施提供资金; |
| • | 约100万美元用于偿还债务; 和 |
| • | 剩余资金用于营运资金、其他一般企业用途和战略投资,包括 通过上岗实验室进行的投资。然而,我们目前还没有关于任何投资的协议或承诺。 |
根据我们目前的 运营计划,我们相信,此次发行的净收益,加上我们现有的现金和现金等价物、可供我们使用的借款以及截至本招股说明书之日的短期投资,将足以支付我们至少未来几个月的 运营费用和资本支出。我们基于可能被证明是错误的假设做出了这一估计,我们可能会比预期更早耗尽可用的资本资源 。此次发行的预期净收益,加上我们的现金和现金等价物,可能不足以让我们通过监管部门的批准推进我们的候选药物,我们可能需要筹集额外的资金 来完成我们候选药物的开发、临床试验和商业化。
根据我们目前的计划和业务条件,我们对此次发行净收益的预期用途 代表了我们的意图。我们无法确切预测本次发售完成后将收到的净收益的所有特定用途,或我们实际将 用于上述用途的金额,我们可能需要额外资金才能完全实现上述指定用途。我们相信,通过获得许可证或收购或投资于互补的业务、产品,可能会不时地有机会扩大我们目前的业务。
96
或技术。虽然我们目前没有就任何特定的许可证内、收购或投资达成协议、承诺或谅解,但我们可能会将部分净收益用于这些目的,但要遵守适用的监管限制。因此,我们的管理层将在使用此次发行的净收益方面拥有广泛的自由裁量权。
我们实际支出的金额和时间可能因众多因素而有很大差异,包括我们的研究和 开发进度、临床前研究的时间和成功、我们未来可能开始的临床研究、患者参加临床试验的时间、监管提交和不断变化的监管要求的时间、我们可能与第三方达成的任何 合作安排或我们获得的战略机遇,以及任何不可预见的现金需求。
在使用之前,我们打算将此次发行的净收益投资于美国政府的短期和中期有息债务、投资级 票据、存单或直接或担保债务,但须遵守适用的监管限制。我们无法预测投资的收益是否会产生有利的回报。
97
股利政策
我们从未宣布或支付过我们的股本的任何现金股息。我们目前打算保留任何未来收益,在可预见的未来不会支付任何 股息。未来宣布现金股息的任何决定将由我们的董事会酌情决定,并受适用法律的约束,这将取决于许多因素,包括我们的财务状况、 经营结果、资本要求、合同限制、一般业务条件以及董事会可能认为相关的其他因素,包括我们当前和未来债务工具的限制、我们未来的 收益、资本要求、财务状况、前景和适用的特拉华州法律(该法律规定股息只能从盈余或当前净利润中支付)。
98
大写
下表列出了截至2020年12月31日我们的现金和现金等价物及资本化情况:
| • | 在实际基础上; |
| • | 在形式基础上,实现i)在紧接本次发售完成之前将我们的可转换优先股的所有流通股自动转换为普通股的总和,以及ii)我们修订和重述的公司证书在紧接本次发售完成之前的备案和生效 ;以及 |
| • | 按经调整的备考基准计算,以反映i)上述备考调整及ii)吾等以假设首次公开发行(IPO)价格(即本招股说明书封面所载价格区间的中点)发行及 本次发售的普通股,扣除吾等估计承销的 折扣及佣金及吾等应支付的估计发售费用后,于本次发售中发行及 出售普通股。 |
以下列出的调整后信息的备考信息仅供参考,并将取决于实际的首次公开募股(IPO)价格和定价时确定的本次发行的其他条款。您应将此信息与我们的财务报表和本招股说明书中其他地方出现的相关注释,以及标题为《精选财务数据》和《管理层对财务状况和运营结果的讨论和分析》的章节一并阅读。
| 截至2020年12月31日 | ||||||||||||
| 实际 | 形式上的 | 形式上的调整后的(1) | ||||||||||
| (未经审计) (单位:千) |
||||||||||||
| 现金和现金等价物 |
$ | $ | $ | |||||||||
|
|
|
|
|
|
|
|||||||
| 可转换优先股,每股面值0.00001美元; 授权股份,已发行和已发行股份,实际;无授权、已发行或已发行股份, 形式和调整后的形式 |
||||||||||||
| 股东赤字: |
||||||||||||
| 优先股,每股面值0.00001美元; 股已授权、已发行和已发行股份,实际 股已授权、已发行和已发行股份, 形式和调整后的形式 |
||||||||||||
| 普通股,每股面值0.00001美元; 股授权股份,已发行股份和 实际流通股; 股授权股,已发行和流通股,预计数;授权股份, 股已发行和流通股,调整后预计数 |
||||||||||||
| 额外实收资本 |
||||||||||||
| 累计赤字 |
||||||||||||
|
|
|
|
|
|
|
|||||||
| 股东赤字总额 |
||||||||||||
|
|
|
|
|
|
|
|||||||
| 总市值 |
$ | $ | $ | |||||||||
|
|
|
|
|
|
|
|||||||
| (1) | 假设本招股说明书封面所列价格区间的中点--每股首次公开募股(IPO)价格每增加或减少1.00美元(即本招股说明书封面所列价格区间的中点),我们的预计现金和现金等价物、额外实收资本、股东赤字总额和总资本将视情况增加或减少约 百万美元,前提是本招股说明书首页所载我们提供的普通股数量保持不变。以及 扣除我们预计应支付的承销折扣和佣金以及预计发行费用后。同样,假设假定的首次公开募股(IPO)价格每股 $保持不变,我们提供的普通股数量每增加或减少100万股,我们的预计现金和现金等价物、额外实收资本、股东亏损总额和总资本将增加或减少约 百万美元,并扣除估计的承销折扣和佣金以及我们应支付的估计发售费用。 |
99
如果全部行使承销商购买额外股份的选择权,我们预计截至2020年12月31日调整后的现金和现金等价物、额外实收资本、股东赤字总额和总资本将分别为 百万美元、百万美元、 百万美元和百万美元。
上表中调整的已发行和已发行普通股、预计和预计普通股数量是基于截至2020年12月31日我们普通股的已发行和已发行普通股数量,不包括:
| • | 截至2020年12月31日,在行使已发行期权时可发行的普通股 ,加权平均行权价为每股$; |
| • | 在行使2020年12月31日之后授予的期权时可发行的普通股 ,加权平均行权价为每股$; |
| • | 截至2020年12月31日,在行使已发行认股权证时可发行的普通股 ; |
| • | 根据我们的2016年计划,截至2020年12月31日,未来发行的普通股 ,这些股票将被添加到我们的2021年计划下为未来发行保留的股份中; |
| • | 根据我们的2021计划为未来发行预留的普通股 ,该计划将在本次发行中生效,以及根据本计划为未来发行预留的普通股数量的任何自动增加;以及 |
| • | 根据我们的2021年ESPP为未来发行保留的普通股 ,该计划将与本次发行相关生效,以及根据本计划为未来发行保留的普通股数量的任何自动增加。 |
100
稀释
在此次发行中购买我们普通股的投资者将在形式上立即大幅稀释,即其普通股的调整后有形账面净值 。预计摊薄为调整后的有形账面净值,代表我们普通股的首次公开募股(IPO)价格与紧随发售后的我们普通股的调整后每股有形账面净值的预计值之间的差额 。
截至2020年12月31日,我们的历史有形账面净赤字为 百万美元,或普通股每股亏损$1。我们的 历史有形账面净值(赤字)是我们的总有形资产减去我们的总负债和可转换优先股的金额,这不包括在我们的股东赤字中。每股历史有形账面净值 (赤字)代表历史有形账面净值(赤字)除以截至2020年12月31日我们普通股的流通股数量。
截至2020年12月31日,我们的预计有形账面净值为 百万美元,或每股普通股1美元。预计 有形账面净值代表我们的有形资产总额减去负债总额。预计每股有形账面净值指的是预计有形账面净值除以截至2020年12月31日的已发行股票总数,在此之前,我们的可转换优先股截至2020年12月31日的所有流通股自动转换为紧接本次发售完成之前的普通股总数 ,就像此类转换发生在2020年12月31日一样。
在进一步实施我们以假设的首次公开募股(IPO)价格每股$出售本次发行中的 普通股股票后,这是本招股说明书封面上列出的价格区间的中点,扣除估计的承销折扣和佣金以及我们估计应支付的发售费用后,截至2020年12月31日,我们的预计调整有形账面净值约为 百万美元。对我们的现有股东来说,这意味着预计每股有形账面净值立即增加约$,对于购买本次发行普通股的投资者来说,预计每股有形账面净值立即稀释约$。 这意味着我们的现有股东的预计每股有形账面净值立即增加约$,对购买本次发行普通股的投资者来说,预计每股有形账面净值立即稀释约$。
下表说明了对新投资者的每股摊薄(不影响承销商购买额外股票的 选择权的任何行使):
| 假设每股首次公开发行(IPO)价格 |
$ | |||||||
| 截至2020年12月31日的每股有形账面净值(亏损) |
$ | |||||||
| 截至2020年12月31日每股有形账面净值预计增长 |
||||||||
|
|
|
|||||||
| 截至2020年12月31日的预计每股有形账面净值 |
||||||||
| 可归因于购买本次发行普通股股票的投资者的预计每股有形账面净值增加 |
||||||||
|
|
|
|||||||
| 预计调整后每股有形账面净值 |
||||||||
|
|
|
|||||||
| 对参与本次发行的投资者每股摊薄 |
$ | |||||||
|
|
|
|
|
假设首次公开募股(IPO)价格为每股 $,即本招股说明书封面所述价格区间的中点,每增加或减少1.00美元,将根据适用情况增加或减少调整后每股有形账面净值的预计 形式
101
假设本 招股说明书封面所列的我们发行的股票数量保持不变,扣除我们估计的承销折扣和佣金以及我们预计应支付的发售费用后,本次发行将减少约$/股,并向购买本次发行中普通股的投资者摊薄约$/股。同样,假设假设首次公开募股(IPO)价格不变,在扣除估计承销折扣和佣金以及估计应支付的发售费用后,我们每增加100万股股票发行量,将 本次发行后调整后每股有形账面净值的备考金额增加约$,并将向购买本次发行普通股的投资者的每股摊薄减少约$ 。假设假设首次公开发行(IPO)价格不变,在扣除预计承销折扣和 佣金以及预计应支付的发售费用后,我们发售的股票数量每减少100万股,预计本次发售后调整后的有形 每股账面净值将减少约$,并使购买本次 发售普通股的投资者的每股摊薄增加约$。
如果承销商行使选择权,以每股 $的假定首次公开发行价格(即本招股说明书封面所列价格区间的中点)全额购买本次发行的额外普通股,并假设本招股说明书首页所列的我们发行的股票数量保持不变,并扣除我们预计的承销折扣和佣金以及我们预计应支付的发售费用后,本次发行后的预计调整后每股有形账面净值约为每股$,对购买本次发行普通股的投资者的每股摊薄将约为每股$。 本次发行后调整后的每股有形账面净值约为每股$,对购买本次发行普通股的投资者的每股摊薄将约为每股$。
下表 在上述调整后的备考基础上汇总了截至2020年12月31日,现有股东和投资者在扣除估计的首次公开发行(IPO)价格之前向我们购买的普通股数量、已支付或将支付的总对价以及已支付或将支付的加权平均每股价格(假设首次公开募股(IPO)价格为每股$), 是本招股说明书封面上列出的价格区间的中点。
| 购买的股份 | 总对价 | 加权的- 平均值 单价 分享 |
||||||||||||||||||
| (美元金额以千为单位,每股除外 金额) |
数 | 百分比 | 金额 | 百分比 | ||||||||||||||||
| 本次发行前的现有股东 |
% | $ | % | $ | ||||||||||||||||
| 在此次发行中购买股票的投资者 |
$ | |||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
| 总计 |
100% | $ | 100% | |||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
上表假设没有行使承销商购买本次发行额外股份的选择权 。如果承销商全面行使购买额外股份的选择权, 现有股东持有的普通股数量将减少至本次发行后已发行普通股总数的%,而购买此次发行普通股 的投资者持有的普通股数量将增加至本次发行后已发行普通股总数的%。
假定首次公开募股(IPO)价格为每股 美元,即本招股说明书封面所列价格区间的中点,每增加或减少1.00美元,投资者在此次发行中购买股票所支付的总对价将根据需要增加或减少约100万美元,前提是我们设定的股票发行数量
102
本招股说明书首页第四页的内容保持不变。同样,假设首次公开募股价格不变,我们发行的股票数量每增加或减少100万股,投资者购买本次发行股票所支付的总对价将增加或减少约100万美元(视 适用情况而定)。
前述表格和计算(不包括历史有形账面净值计算) 基于我们截至2020年12月31日的已发行普通股股份,不包括:
| • | 截至2020年12月31日,在行使已发行期权时可发行的普通股 ,加权平均行权价为每股$; |
| • | 在行使2020年12月31日之后授予的期权时可发行的普通股 ,加权平均行权价为每股$; |
| • | 截至2020年12月31日,在行使已发行认股权证时可发行的普通股 ; |
| • | 截至2020年12月31日,我们2016年计划未来发行的普通股,这些股票将被添加到我们的2021年计划下为未来发行保留的股份中; |
| • | 根据我们的2021计划为未来发行预留的普通股 ,该计划将与本次发行以及根据本计划为未来发行预留的普通股数量的任何自动增加相关而生效;以及 |
| • | 根据我们的2021年ESPP为未来发行预留的普通股 ,该计划将与本次发行以及根据本计划为未来发行预留的普通股数量的任何自动增加相关而生效。 |
只要根据我们的股权福利计划行使任何未偿还期权或发行新的期权,或我们在未来额外发行 可转换为或可行使或可交换为我们股本股份的普通股或其他证券,在此次发售中购买普通股的投资者将进一步稀释。
103
选定的合并财务数据
下表汇总了我们选定的各期间和截至指定日期的财务数据。我们选择了截至2019年12月31日和2020年12月31日的 运营数据报表,以及截至2019年12月31日和2020年12月31日的资产负债表数据,这些数据来自本招股说明书中其他地方的经审计财务报表。您应阅读以下 精选财务数据,以及我们的财务报表和本招股说明书中其他地方的相关注释,以及标题为管理层对财务状况和运营结果的讨论和分析 一节中的信息。
| 截至十二月三十一日止的年度, | ||||||||
| 2019 | 2020 | |||||||
| (以千为单位,不包括共享和每股数据) | ||||||||
| 综合运营报表数据: |
||||||||
| 收入: |
||||||||
| 赠款收入 |
$ | 608 | $ | |||||
| 营业收入 |
1,711 | |||||||
|
|
|
|
|
|||||
| 总收入 |
2,319 | |||||||
| 运营费用: |
||||||||
| 研发费用 |
45,809 | |||||||
| 一般事务和行政事务 |
18,951 | |||||||
|
|
|
|
|
|||||
| 总运营费用 |
64,760 | |||||||
| 运营亏损 |
(62,441 | ) | ||||||
|
|
|
|
|
|||||
| 其他收入,净额 |
562 | |||||||
|
|
|
|
|
|||||
| 净亏损和综合亏损 |
$ | (61,879 | ) | $ | ||||
|
|
|
|
|
|||||
| 每股基本和稀释后净亏损(1) |
$ | (4.30 | ) | $ | ||||
|
|
|
|
|
|||||
| 基本普通股和稀释普通股的加权平均份额 |
14,380,177 | |||||||
|
|
|
|
|
|||||
| 预计每股基本和摊薄净亏损 (未经审计)(2) |
$ | (0.96 | ) | $ | ||||
|
|
|
|
|
|||||
| 预计加权平均-用于计算预计每股净亏损、基本亏损和 摊薄(未经审计)的流通股 |
64,746,144 | |||||||
|
|
|
|
|
|||||
| (1) | 有关基本和稀释后每股净亏损的计算详情,请参阅本招股说明书末尾的综合财务报表附注11。 |
| (2) | 计算未经审核备考基本及摊薄每股净亏损,以使所有 可转换优先股已发行股份自动转换为与合资格首次公开发行有关的普通股,采用转换后的方法,犹如转换已于所述期间期初或 发行日期(如较后)发生。 |
| 截止到十二月三十一号, | ||||||||
| 2019 | 2020 | |||||||
| (单位:千) | ||||||||
| 合并资产负债表数据: |
||||||||
| 现金和现金等价物 |
$ | 69,883 | ||||||
|
|
|
|
|
|||||
| 营运资金(1) |
69,714 | |||||||
|
|
|
|
|
|||||
| 总资产 |
101,431 | |||||||
|
|
|
|
|
|||||
| 可转换优先股 |
201,109 | |||||||
|
|
|
|
|
|||||
| 股东赤字总额 |
(124,265 | ) | ||||||
|
|
|
|
|
|||||
| (1) | 营运资本的定义是流动资产减去流动负债。 |
104
管理层的讨论和
财务状况分析
和运营结果
管理人员对财务状况和经营结果进行讨论和分析
您应阅读以下关于我们的财务状况和运营结果的讨论和分析,以及本招股说明书末尾的选定综合财务数据部分以及我们的综合财务报表和相关注释。本讨论和分析中包含的一些信息或本招股说明书中其他部分阐述的信息,包括有关我们业务和相关融资的计划和战略的信息,包括涉及风险和不确定性的前瞻性陈述。由于许多因素的影响,包括 本招股说明书风险因素部分阐述的那些因素,我们的实际结果可能与以下讨论和 分析中包含的前瞻性陈述中描述或暗示的结果大不相同。
概述
我们是一家临床阶段的生物技术公司,通过整合跨越生物、化学、自动化、数据科学和工程的技术创新来解码生物学,从而从根本上改善患者的生活并实现药物研发的产业化。我们的核心使命 是Recursion操作系统,它结合了先进的基础架构层,以生成我们认为是世界上最大、增长最快的专有生物和化学数据集之一,以及Recursion Map,这是一套 自定义软件、算法和机器学习工具,我们使用它来探索不受人类偏见限制的基础生物学,导航到新的生物学见解,并快速加速程序。在我们的闭环系统中,湿实验室生物学和硅胶 工具的结合加快了我们的药物发现过程,并使我们有别于行业内的其他公司。同样,我们由生命科学家以及计算和技术专家组成的平衡团队创造了一种环境,让 经验数据、严谨的统计数据和创造性思维应用于每一项决策。到目前为止,我们利用我们的Recursion操作系统创造了三个价值驱动力:i)35个内部开发的计划,专注于 个重要的未得到满足的需求领域,其中几个的市场机会年销售额超过10亿美元;ii)与领先的生物制药公司建立战略合作伙伴关系;以及iii)诱导实验室,这是一个增长引擎,旨在 探索Recursion操作系统在治疗学内外的新扩展。自2019年以来,我们的渠道规模翻了一番,我们预计未来将继续加快项目增加的步伐。因此,我们是一家 生物技术公司,规模更像一家科技公司。
整合跨越生物、化学、自动化、数据、科学和工程的技术创新,以实现治疗学发现的产业化 这要求我们筹集大量资金,并采取平衡短期风险和长期价值创造的长期资本分配方法。在我们35个项目的 流水线中,我们有四个候选药物,我们预计它们将在明年进入临床试验。截至2020年12月31日,我们已经组建了一支由200多名员工组成的卓越团队。我们大约40%的全职员工是生物和化学员工,35%的全职员工是数据科学和软件工程员工。
从成立到2020年12月31日,我们从投资者那里筹集了大约4.492亿美元的股权融资,此外,我们还从与拜耳的战略合作伙伴关系中获得了3000万美元的预付款。我们将筹集的资金用于平台研究运营、药物研发、临床开发、数字和 其他基础设施、创建我们的知识产权组合以及行政支持等方面的运营和投资活动。我们没有任何获准商业销售的产品,也没有从产品销售中获得任何收入。截至2020年12月31日,我们拥有现金和现金等价物 百万美元。
自 成立以来,我们出现了严重的运营亏损。截至2019年12月31日和2020年12月31日的年度,我们的净亏损分别为6190万美元和100万美元 。自.起
106
2020年12月31日,我们的累计赤字为100万美元。在可预见的未来,我们预计将继续产生巨额费用和运营亏损。此外,我们预计与我们正在进行的活动相关的费用将大幅增加,因为我们:
| • | 继续我们的平台研究、药物发现和临床开发工作; |
| • | 继续投资于我们平台研究能力的规模和范围,以确定新的生物学和 疗法; |
| • | 继续投资扩展我们整个平台的医疗功能,包括大分子和RNA 疗法; |
| • | 投资或收购实现我们平台目标的公司或知识产权; |
| • | 加快对机制的投资,通过上岗实验室显著扩大我们的潜在市场总量; |
| • | 利用我们的平台识别和验证其他候选治疗方案、技术和商机; |
| • | 为我们的候选产品启动额外的临床前研究或临床或其他试验,包括根据我们的 合作协议; |
| • | 继续或扩大我们的候选产品的临床试验范围; |
| • | 在生物学的不同领域进行广泛的候选治疗项目的上面和下面的开发活动 ; |
| • | 与合同研究组织(CRO)和合同制造组织(CMO)就我们的临床前研究和临床试验 建立协议; |
| • | 改变或增加内部制造能力或能力; |
| • | 更换或增加其他供应商; |
| • | 寻求监管部门对我们的候选治疗方案的批准; |
| • | 为我们的候选治疗寻求市场批准和报销; |
| • | 建立销售、营销和分销基础设施,将我们可能获得 市场批准的任何产品商业化; |
| • | 收购或许可其他候选治疗方法和技术; |
| • | 根据任何许可协议进行里程碑或其他付款; |
| • | 维护、保护、捍卫、执行和扩大我们的知识产权组合; |
| • | 为我们的质量控制、质量保证、法律、合规和其他团队增加额外的基础设施,以支持我们的 运营,同时我们将候选治疗药物推向商业化; |
| • | 增加额外的基础设施,以支持我们作为上市公司的运营以及我们的产品开发和未来的商业化努力,包括扩展公司网站; |
| • | 吸引和留住世界级人才,包括竞争领域的人才;以及 |
| • | 遇到上述任一项的任何延迟或遇到问题。 |
除非我们成功完成临床开发并获得监管部门对我们候选药物的 批准,否则我们不会从销售候选药物中获得收入。如果我们能够获得监管机构对我们的任何候选治疗方案的批准,我们可能会招致
107
与开发我们的商业化能力以单独或与他人合作支持产品销售、营销和分销活动相关的巨额商业化费用 。此外,此次发行结束后,我们预计将产生与上市公司运营相关的额外成本,包括重大的法律、会计、投资者关系以及其他我们作为私营公司没有发生的费用。
因此,我们将需要大量的额外资金来支持我们的持续运营和实施我们的增长战略。 在我们能够从药品销售中获得可观的收入之前,我们预计将通过公共或私募股权发行和债务融资、政府融资安排、 合作以及营销、分销和许可安排相结合的方式为我们的运营提供资金。我们可能无法筹集更多资金或以优惠条件达成这样的其他安排,或者根本不能。如果我们不能筹集资金或达成如下安排, 在需要的时候,我们可能不得不大幅推迟、缩减或停止一个或多个候选产品的开发和商业化,或者推迟 潜在的许可证内或收购。
由于与药品开发相关的众多风险和不确定性 ,我们无法预测增加费用的时间或金额,也无法预测我们何时或是否能够实现或保持盈利。即使我们能够从销售产品中获得收入,我们也可能 无法盈利。如果我们无法实现盈利或无法持续盈利,那么我们可能无法继续按计划运营,并可能被迫减少运营。
战略协议
下面列出了可能对我们的运营结果产生影响的战略性 协议:
拜耳
2020年8月,我们与拜耳股份公司(Bayer AG)签订了为期五年的研究协作和选项协议-拜耳协议(Bayer Agreement) ,根据该协议,我们和拜耳可以启动十多个与肺、肝和心脏等多个器官系统纤维化相关的研究项目。作为拜耳协议的一部分,我们在2020年9月收到了3000万美元的预付技术访问费。在每个研究项目下,我们将与拜耳合作,确定潜在的开发候选者。如果拜耳向潜在候选者行使许可选择权,我们将获得选择权行使费、 可能获得的超过1亿美元的开发和商业里程碑,以及每个此类许可的分级版税。
REC-2282:俄亥俄州创新基金会授权
2018年12月,我们与俄亥俄州立创新基金会(OSIF)签订了独家许可协议,根据该协议,我们获得了由OSIF控制并与泛组蛋白去乙酰化酶抑制剂OSU-HDAC42或REC-2282相关的某些权利的许可证,以便在全球范围内开发、制造、使用、销售、发售和进口含有OSU-HDAC42的产品。Osif还向我们分配了某些资产,与被称为AR-42的药物成分有关。作为 许可证的对价,我们在2018年12月向Osif支付了200万美元的预付款,并有义务向Osif支付总计高达2000万美元的某些里程碑,以及授权产品净销售额的个位数中位数版税 。此外,我们还欠二期临床试验前任何非特许权使用费再许可费用的25%或启动二期临床试验后此类再许可费用的15%,前提是里程碑付款可抵免这些再许可费用。截至本招股说明书发布之日,我们尚未向OSIF支付任何里程碑或特许权使用费。
108
REC-3599:Chromaderm许可协议
2019年12月,我们与Chromaderm,Inc.或Chromaderm签订了一项许可协议,根据该协议,我们获得了Chromaderm控制的非特效性制剂Ruboxistaurin(蛋白激酶C抑制剂)的 独家许可,用于治疗、预防和/或诊断皮肤色素沉着状况或疾病以外的所有用途 。根据协议,我们在2019年12月向Chromaderm支付了125万美元的预付款。对于获得许可的 产品,我们有义务向Chromaderm支付某些开发和审批里程碑,第一个适应症的总金额高达3550万美元,如果追求多个适应症,我们有义务支付高达5250万美元的费用,某些商业里程碑的总金额高达4900万美元。最后,我们将根据REC-3599的净销售额向 较低的两位数分级版税支付Chromaderm中期个位数的版税。截至本招股说明书发布之日,我们尚未向Chromaderm支付任何里程碑或特许权使用费。
REC-4881:武田许可协议
2020年5月,我们与武田制药有限公司或武田公司签订了许可协议或武田In-License,根据该协议,我们获得了武田临床阶段化合物TAK-733的某些权利的独家许可(即使是武田及其附属公司)。非ATP-竞争性MEK1和MEK2的变构抑制剂。我们必须在 每个国家(A)美国、(B)至少以下三个欧洲国家/地区(英国、法国、德国、意大利和西班牙)以及(C)日本,使用商业上合理的努力开发和商业化至少一种授权产品。(A)美国、(B)至少三个欧洲国家/地区:英国、法国、德国、意大利和西班牙,以及(C)日本。协议签署后,我们于2020年5月向武田支付了150万美元的预付款。根据武田许可,我们有义务在特定开发和监管里程碑事件完成后向武田里程碑支付总计3950万美元。此外, 我们有义务向武田付款中低档个位数版税,基于我们、我们的附属公司或分被许可方对含有许可化合物的产品的净销售额, 可按指定的降幅计算。截至本招股说明书发布之日,我们尚未向武田支付任何里程碑或特许权使用费。
有关这些战略协议的更多 信息,请参阅业务战略协议。
经营成果的组成部分
收入
到目前为止,我们的业务收入来自 两个来源:i)赠款收入和ii)运营收入。
奖助金收入:我们在根据相关补助协议赚取 收入的期间确认补助收入,该期间是根据补助协议产生相应的可报销费用的期间。赠款收入来自国家卫生研究院和比尔和梅林达·盖茨基金会授予的赠款。
营业收入V运营收入主要来自由战略联盟(如我们与拜耳的战略合作伙伴关系)衍生的资助研究 和开发协议。随着某些里程碑的实现,我们有权获得不同的考虑。收入确认的时间与现金收入的时间并不直接 相关。
109
研究与开发
研发费用占我们运营费用的很大一部分。我们确认研发费用为 已发生的费用。研发费用包括进行研发活动所产生的成本,包括:
| • | 开发和运营我们平台的成本; |
| • | 导致开发候选者的发现努力; |
| • | 我们项目的临床开发成本; |
| • | 与发现和临床开发工作相关的成本,包括研究材料和外部 研究; |
| • | 与生产用于临床前试验和临床试验的药物物质和药品相关的材料和供应成本; |
| • | 与人员有关的费用,包括从事研发职能的员工的工资、福利、奖金和股票报酬; |
| • | 与营运数码基础设施有关的成本;以及 |
| • | 设施、折旧和摊销、保险以及因研发活动而产生的其他直接费用和分摊费用。 |
我们根据适用合同中指定的 活动完成情况确认与第三方合同服务相关的费用。在终止与第三方的合同时,我们的财务义务仅限于到目前为止发生或承诺的费用。根据合同安排在未来的研究和产品开发活动中使用或提供的任何商品或服务的任何预付款都被归类为预付费用,直到该等商品或服务被提供为止。
一般事务和行政事务
我们按已发生的费用支付一般费用和 管理费用。一般和行政费用主要包括高管、财务、人力资源、法律和其他公司行政职能人员的工资、福利、股票薪酬和外包劳动力。 一般和行政费用还包括与公司和专利事务有关的法律费用,会计、审计、税务和行政咨询服务的专业费用,保险 成本,设施和折旧费用。
我们预计,随着我们增加研发活动,以及与我们最初的候选药物REC-4881、REC-3599、REC-2282和REC-994的潜在商业化相关的活动,未来我们的一般和管理费用将增加,以支持 人员的研发和总体运营。我们还预计与上市公司运营相关的费用会增加 ,包括与遵守交易所上市和证券以及交易委员会(SEC)要求相关的会计、审计、法律、监管和税务相关服务的成本、董事和高级管理人员保险成本,以及投资者和公关成本。
其他收入,净额
其他收入,净额主要包括我们的现金和现金等价物赚取的利息,根据我们的贷款协议产生的利息支出,与注销未摊销债务发行成本有关的债务清偿损失,以及支付最后付款费用。
110
经营成果
截至2019年12月31日和2020年12月31日止年度比较
下表汇总了我们在所示时期的运营结果:
| 年终 十二月三十一日, |
变化 | |||||||||||||||
| 2019 | 2020 | $ | % | |||||||||||||
| (除百分比外,以千为单位) | ||||||||||||||||
| 收入 |
||||||||||||||||
| 赠款收入 |
$ | 608 | ||||||||||||||
| 营业收入 |
1,711 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 总收入 |
2,319 | |||||||||||||||
| 运营费用 |
||||||||||||||||
| 研发费用 |
45,809 | |||||||||||||||
| 一般事务和行政事务 |
18,951 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 总运营费用 |
64,760 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 运营亏损 |
(62,441 | ) | ||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 其他收入,净额 |
562 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 净亏损和综合亏损 |
$ | (61,879 | ) | |||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
收入
下表汇总了截至2019年12月31日和2020年12月31日的年度确认收入的组成部分。
| 截止的年数 十二月三十一日, |
变化 | |||||||||||||||
| 2019 | 2020 | $ | % | |||||||||||||
| (除百分比外,以千为单位) | ||||||||||||||||
| 收入 |
||||||||||||||||
| 赠款收入 |
$ | 608 | ||||||||||||||
| 营业收入 |
1,711 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 总收入 |
$ | 2,319 | ||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
与截至2019年12月31日的230万美元相比,截至2020年12月31日的财年收入增加了 美元,增幅为3%。 截至2019年12月31日的财年,收入为230万美元。 收入的增长是由于。
111
研究与开发
下表汇总了截至2019年12月31日和2020年12月31日的年度研发费用构成。
| 年终 十二月三十一日, |
变化 | |||||||||||||||
| 2019 | 2020 | $ | % | |||||||||||||
| (除百分比外,以千为单位) | ||||||||||||||||
| 研发费用 |
||||||||||||||||
| 站台 |
$ | 19,617 | ||||||||||||||
| 发现 |
15,423 | |||||||||||||||
| 临床 |
8,221 | |||||||||||||||
| 基于股票的薪酬 |
947 | |||||||||||||||
| 其他 |
1,601 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 项目总费用 |
$ | 45,809 | ||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
研发的重要组成部分包括以下费用类别:Platform,主要是指与通过HIT鉴定进行筛选相关的费用;Discovery,主要是指通过开发候选人进行HIT鉴定的费用;以及临床,主要是指与开发 候选人及以上相关的费用。
在截至2020年12月31日的财年,研发费用增加了 美元,达到100万美元,而截至2019年12月31日的财年,研发费用为4580万美元。研发费用的增加是由于 。
一般和行政费用
下表汇总了截至2019年12月31日和2020年12月31日的年度的一般和行政费用构成。
| 年终 十二月三十一日, |
变化 | |||||||||||||||
| 2019 | 2020 | $ | % | |||||||||||||
| (除百分比外,以千为单位) | ||||||||||||||||
| 一般和行政合计 |
$ | 18,951 | ||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
截至2020年12月31日的年度,一般和行政费用增加 美元至100万美元,而截至2019年12月31日的年度为1,900万美元。一般和行政费用的增加是由于 。
其他收入,净额
下表汇总了截至2019年12月31日和2020年12月31日的年度的其他收入净额构成。
| 年终 十二月三十一日, |
变化 | |||||||||||||||
| 2019 | 2020 | $ | % | |||||||||||||
| (除百分比外,以千为单位) | ||||||||||||||||
| 利息收入 |
$ | 1,741 | ||||||||||||||
| 利息支出 |
(635 | ) | ||||||||||||||
| 债务清偿损失 |
(555 | ) | ||||||||||||||
| 权证公允价值重新计量收益 |
11 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
| 其他收入,净额 |
$ | 562 | ||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
112
其他收入, 截至2020年12月31日的年度净增$,或%,至 百万美元,而截至2019年12月31日的年度为110万美元。其他收入中的 净额应为。
流动性与资本资源
流动资金来源
我们还没有将任何产品商业化,我们预计在几年内不会从任何候选产品的销售中获得收入。截至2019年12月31日,现金和 现金等价物总额为6990万美元,截至2020年12月31日,现金和现金等价物总额为100万美元。我们将购买期限在90天或以下的所有高流动性 投资视为现金等价物。
我们已经发生了运营亏损,并经历了 个负运营现金流,我们预计至少在可预见的未来,我们将继续亏损。截至2019年12月31日的年度,我们的净亏损总额为6,190万美元,截至2020年12月31日的年度,净亏损总额为 百万美元。截至2019年12月31日和2020年12月31日,我们的累计赤字分别为1.266亿美元和1.266亿美元。
到 为止,我们主要通过私募优先股来为我们的运营融资。截至2019年12月31日,我们从销售A系列优先股中获得了2,130万美元的毛收入,从销售B系列优先股中获得了6,000万美元,从C系列优先股中获得了1.221亿美元。
在2020年9月和10月,我们 从D系列优先股的销售中获得了超过2.459亿美元的毛收入,以及我们与拜耳的战略合作伙伴关系预付款3,000万美元。
中型股信贷和担保协议
2019年9月,我们与Midcap Financial Trust或MidCap签订了信用和安全协议,我们将其称为我们的信用协议。信贷协议包括:i)本金总额为1,190万美元的初步定期贷款;及ii)第二批定期贷款,若提取,则未偿还本金总额最高为2,690万美元。第二批资金将根据某些 药物开发里程碑的实现情况提供。我们需要在2019年9月至2021年9月期间只支付利息,此后每月支付36笔本金,30万美元外加利息,从2021年10月开始,一直持续到2021年9月的 到期日。当达到某些筹款相关的里程碑时,仅限利息的期限将再延长12个月。未偿还本金的利息按浮动年利率计算,等于 伦敦银行同业拆借利率加5.75%。
这笔债务是以我们所有的资产作担保的。信用协议包括标准肯定和限制性 契诺和标准违约事件,包括付款违约、在任何适用的治疗期之后违反契诺、Midcap担保权益或抵押品价值的完善或优先权出现重大损害,以及我们的业务、运营或条件发生重大不利变化。一旦发生违约事件并在任何适用的救济期之后,MidCap可宣布所有立即到期和应付的未偿债务,并 采取信贷协议中规定的其他行动。截至2020年12月31日,我们遵守了信贷协议下的所有债务契约。2019年,我们支付了大约30万美元与发起信贷协议 相关的费用。该等费用已递延并记作直接从应付贷款账面价值扣除,并于信贷协议余下期限内摊销为利息开支。
113
现金流
下表列出了以下每个期间现金和现金等价物的主要来源和用途:
| 年终 十二月三十一日, |
||||||||
| 2019 | 2020 | |||||||
| (单位:千) | ||||||||
| 用于经营活动的现金 |
$ | (57,042 | ) | |||||
| 用于投资活动的现金 |
(3,910 | ) | ||||||
| 融资活动提供的现金 |
120,410 | |||||||
|
|
|
|
|
|||||
| 现金及现金等价物净增加情况 |
$ | 59,458 | ||||||
|
|
|
|
|
|||||
经营活动
截至2020年12月31日的一年中,运营活动中使用的净现金为100万美元。经营活动中使用的现金是由于使用与我们的运营相关的资金,导致净亏损 百万美元,经 百万美元的非现金费用以及 百万美元的营业资产和负债变动调整。非现金项目包括基于股票的薪酬支出 百万美元和折旧及摊销百万美元, 由租赁激励债务摊销百万美元抵消。资产和负债的净变化主要是由于其他 资产增加了100万美元,但被应付账款减少 百万美元以及应计费用、递延收入和其他流动负债减少 百万美元所抵消。
截至2019年12月31日的年度,经营活动中使用的净现金为 5700万美元。运营活动中使用的现金是由于与运营相关的资金使用,导致净亏损6190万美元,经 440万美元的非现金费用以及40万美元的运营资产和负债变化调整后。非现金项目包括140万美元的基于股票的薪酬支出 和350万美元的折旧和摊销,但被50万美元的租赁激励债务摊销所抵消。资产和负债的净变化主要是由于其他资产增加了60万美元,但被应付账款减少30万美元以及应计费用、递延收入和其他流动负债增加10万美元所抵消。
投资活动
截至2020年12月31日的一年中,用于投资 活动的现金净额为100万美元。投资活动中使用的现金用于购买 。
截至2019年12月31日的年度,用于投资活动的现金净额为390万美元,用于购买物业和设备,其中350万美元用于购买实验室设备,40万美元用于办公设备、 固定装置和租赁改进。
融资活动
截至2020年12月31日的一年中,融资活动中使用的净现金为100万美元。融资活动中使用的现金主要由出售优先股所得的百万美元(减去发行成本)构成。
截至2019年12月31日的年度,融资活动提供的现金净额为1.204亿美元,其中主要由出售优先股所得的1.199亿美元减去
114
发行成本和长期债务收益,扣除1160万美元的发行成本。融资活动提供的现金流被1,120万美元的长期债务偿还所抵消。
未来的资金需求
自 成立以来,我们出现了严重的运营亏损。截至2019年12月31日和2020年12月31日的年度,我们的净亏损分别为6190万美元和100万美元 。截至2020年12月31日,我们的累计赤字为100万美元。考虑到我们广泛而雄心勃勃的使命,我们预计在可预见的未来,我们将继续 招致巨额费用和运营亏损。此外,我们预计与我们正在进行的活动相关的费用将大幅增加,因为我们:
| • | 继续我们的平台研究、药物发现和临床开发工作; |
| • | 继续投资于我们平台研究能力的规模和范围,以确定新的生物学和 疗法; |
| • | 继续投资扩展我们整个平台的医疗功能,包括大分子和RNA 疗法; |
| • | 投资或收购实现我们平台目标的公司或知识产权; |
| • | 加快对机制的投资,通过上岗实验室显著扩大我们的潜在市场总量; |
| • | 利用我们的平台识别和验证其他候选药物、技术和商机; |
| • | 为我们的候选药物启动额外的临床前研究或临床或其他试验,包括根据我们的 合作协议; |
| • | 继续或扩大我们候选药物的临床试验范围; |
| • | 在我们不同生物学领域的候选药物流水线上开展以上和下面的开发活动; |
| • | 与CRO和CMO就我们的临床前研究和临床试验建立协议; |
| • | 改变或增加内部制造能力或能力; |
| • | 更换或增加其他供应商; |
| • | 为我们的候选药物寻求监管批准; |
| • | 为我们的候选药物寻求上市批准和报销; |
| • | 建立销售、营销和分销基础设施,将我们可能获得 市场批准的任何产品商业化; |
| • | 获取或许可其他候选药物和技术; |
| • | 根据任何许可协议进行里程碑或其他付款; |
| • | 维护、保护、捍卫、执行和扩大我们的知识产权组合; |
| • | 为我们的质量控制、质量保证、法律、合规和其他部门增加额外的基础设施,以支持我们的 运营,使我们的候选药物走向商业化; |
| • | 增加额外的基础设施,以支持我们作为上市公司的运营以及我们的产品开发和未来的商业化努力,包括扩展公司网站; |
115
| • | 吸引和留住世界级人才,包括竞争领域的人才;以及 |
| • | 遇到上述任一项的任何延迟或遇到问题。 |
我们相信,此次发行的预期净收益,加上我们现有的现金和现金等价物、可供我们使用的借款以及截至本招股说明书日期的 短期投资,将足以支付我们至少在未来 个月的运营费用和资本支出。我们基于可能被证明是错误的假设做出了这一估计,我们可能会比我们 预期的更快耗尽可用的资本资源。
在我们成功完成重要的药物开发里程碑(无论是我们自己还是与第三方合作)之前,我们预计不会从外部许可交易、开发里程碑或版税中获得可观的收入,我们预计这将需要数年时间。为了将我们的候选药物 商业化,我们或我们的合作伙伴需要完成临床开发并遵守全面的法规要求。我们面临着许多与生物技术行业内其他同等规模的公司类似的风险和不确定性,例如临床试验结果的不确定性、额外资金的不确定性以及运营亏损的历史。
我们 还面临与早期企业相关的许多其他风险,包括日益激烈的竞争、有限的运营历史、开发和完善我们的发现平台和开发运营的需要、获得足够的资金以完成开发活动、聘用管理层和其他关键人员、扩展我们的实验室流程以最大限度地提高生产能力、避免污染和其他导致平台停机的原因,以及将跨职能运营 整合到我们的团队中 。我们开发计划的成功完成以及最终盈利运营的实现取决于未来的事件,其中包括我们获得融资、吸引、留住和激励 合格人员、高效管理供应链、经济高效地扩大和维护实验室运营以适应增长、保护我们的知识产权和执行战略合作伙伴关系的能力。尽管我们相信我们将 能够成功缓解这些风险,但不能保证我们能够做到这一点,也不能保证我们将永远盈利。
由于 与开发临床项目和其他早期候选产品相关的众多风险和不确定性,以及我们可能在多大程度上与第三方合作开发我们的候选产品 ,我们无法估计与完成候选产品研发相关的增加资本支出和运营费用的时间和金额。我们未来的资本需求 将取决于许多因素,包括:
| • | 任何业务中断对我们的运营的影响,包括患者参加我们计划的 临床试验的时间和登记的影响,或者对我们的制造商、供应商或其他供应商因新冠肺炎大流行或类似的公共卫生危机而造成的影响; |
| • | 我们目前和未来的临床试验以及我们项目的额外临床前研究的范围、进度、结果和成本; |
| • | 我们追求的未来候选药物的数量和他们的开发需求; |
| • | 对我们的候选药物进行监管审查的成本、时间和结果; |
| • | 我们在有利条件下建立和维持合作的能力(如果有的话); |
| • | 我们可能与第三方达成的任何合作的成功; |
| • | 我们收购或投资业务、产品和技术的程度,包括为候选药物签订许可或 合作安排; |
116
| • | 准备、提交和起诉专利申请,维护、保护和执行我们的 知识产权,以及为与知识产权相关的索赔辩护的成本; |
| • | 随着我们扩大业务运营和研发活动,我们的员工数量增长和相关成本增加; 和 |
| • | 作为一家上市公司的运营成本。 |
开发药品(包括进行临床前研究和临床试验)是一个耗时、昂贵且不确定的过程,需要数年时间才能完成 ,我们可能永远无法生成获得任何候选产品上市批准所需的必要数据或结果,或从销售任何我们可能获得上市批准的候选产品中获得收入 。此外,我们的候选药物如果获得批准,可能不会在商业上取得成功。我们的商业收入(如果有的话)将来自药品销售,我们预计这些药品将在很多年内(如果有的话)无法投入商业使用。 因此,我们需要获得大量额外资金来实现我们的业务目标。
按可接受的条款,我们可能无法获得足够的额外资金 ,或者根本无法获得。我们目前没有任何承诺的外部资金来源。如果我们通过出售股权或可转换债务证券筹集额外资本,您的所有权权益可能会被稀释, 这些证券的条款可能包括清算或其他优惠以及反稀释保护,这可能会对您作为普通股股东的权利产生不利影响。额外的债务或优先股融资(如果可用)可能涉及 协议,其中包括限制性契约,这些契约可能会限制我们采取特定行动的能力,例如招致债务、进行资本支出或宣布股息,这可能会对我们开展业务的能力产生不利影响,并且 可能需要发行认股权证,这可能会进一步稀释您的所有权权益。
如果我们通过 合作、战略联盟或与第三方的许可安排筹集额外资金,我们可能不得不放弃对我们的技术、未来收入流、研究计划或候选产品的宝贵权利,或者以可能对我们不利的条款授予许可证。如果我们无法在需要时通过股权或债务融资或合作、战略联盟或与第三方的许可安排筹集更多资金,我们可能会被要求推迟、限制、减少和/或 终止我们的产品开发计划或任何未来的商业化努力,或授予开发和营销我们原本希望自己开发和营销的候选产品的权利。
表外安排
在提交报告期间,我们没有,目前也没有任何表外安排,正如美国证券交易委员会(Securities and Exchange Commission,简称SEC)的规则和法规中所定义的 。
117
合同义务和承诺
下表汇总了我们在2020年12月31日的合同义务,以及这些义务预计将对我们未来的 流动性和现金流产生的影响:
| 按期到期付款 | ||||||||||||||||||||
| 总计 | 较少 大于1 年 |
1至3 年份 |
3至5 年份 |
更多 多于5 年份 |
||||||||||||||||
| (单位:千) | ||||||||||||||||||||
| 经营租赁承诺(1) |
$ | $ | $ | $ | $ | |||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
| 发展义务(2) |
||||||||||||||||||||
| 债务和利息 |
||||||||||||||||||||
| 购买义务 |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
| 总计 |
$ | $ | $ | $ | $ | |||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
| (1) | 表示我们在犹他州盐湖城的两个办公地点根据租约应支付的最低金额。 |
| (2) | 表示根据我们与第三方的现有研究和许可协议应支付的许可证维护费总额 。 |
我们还与其他第三方签订了一定的战略合作伙伴关系以及研究和许可协议,为我们提供研究服务,目标是识别和开发候选产品,直到对第三方的所有付款义务到期。我们有权在合理的通知期内终止这些协议。有关这些战略协议的更多 信息,请参阅业务战略协议。
我们在正常业务过程中与CRO和CMO签订服务协议 ,用于临床试验、临床前研究研究和测试、制造以及用于运营目的的其他服务和产品。这些合同不包含任何最低采购承诺。某些协议 规定了终止权,但需支付终止费或清盘费用。根据此类协议,我们有合同义务向供应商支付某些款项,主要用于补偿他们在 取消之前发生的无法收回的费用。这类债务的确切金额取决于终止的时间和相关协议的确切条款,无法合理估计。截至2020年12月31日,我们预计不会取消这些 协议,因此,协议下的金额包含在上面的合同义务表中。
在2020年间,我们签订了 购买超级计算机、附件和部件的承诺,预计价格约为1860万美元。
关键会计政策和估计的使用
我们管理层对财务状况和运营结果的讨论和分析基于我们的财务 报表,该报表是根据美国公认会计原则(GAAP)编制的。编制我们的合并财务报表和相关披露要求我们作出估计和 假设,这些估计和假设会影响我们财务报表中报告的资产和负债、成本和费用以及或有资产和负债的披露。我们的估计基于历史经验、已知趋势和事件、 以及我们认为在这种情况下合理的各种其他因素,这些因素的结果构成了对资产和负债的账面价值作出判断的基础,而这些资产和负债的账面价值从其他来源看起来并不明显。我们 会持续评估我们的估计和假设。在不同的假设或条件下,我们的实际结果可能与这些估计不同。
118
新冠肺炎疫情将在多大程度上直接或 间接影响我们的业务、运营结果和财务状况,包括费用、临床试验和研发成本,将取决于高度不确定的未来发展,包括可能出现的关于新冠肺炎的新 信息,遏制或治疗新冠肺炎的行动,以及对当地、地区、国家和 国际市场的经济影响。
虽然我们的重要会计政策在本招股说明书末尾的综合财务报表附注 中有更详细的描述,但我们认为以下会计政策对我们编制综合财务报表时使用的判断和估计最为关键。
收入确认
我们已从 我们的战略联盟中获得收入。我们与战略合作伙伴的联盟可能包含多种元素,包括研究和其他许可、获得开发和商业化权利的选项、研发服务、 开发和制造临床前和临床材料的义务,以及获得其他研发服务和临床前和临床材料的选项。此类安排可能规定向我们支付各种类型的款项,包括预付 费用、研发服务资金以及临床前和临床材料、技术、开发、监管和商业里程碑付款、许可费、期权行使费以及产品销售的特许权使用费和分红付款。 此类付款通常与收入确认的时间不相称,因此会导致收入确认的延迟。
应计研究和开发费用
作为编制财务报表过程的一部分,我们需要估计 我们根据与供应商、临床研究组织和顾问的合同以及临床现场协议所承担的与进行临床试验相关的费用。这些合同的财务条款以协商为准, 这些条款因合同而异,可能导致付款条款与此类合同提供材料或服务的期限不匹配。我们的目标是在我们的财务报表中反映适当的费用 ,将这些费用与提供服务和付出努力的时间相匹配。我们根据费用各方面的时间安排对这些费用进行会计处理,并考虑到与适用人员和外部服务提供商就临床试验进展或完成的服务进行的 讨论,从而确定应计估计数。在临床试验过程中,如果实际结果与 估计值不同,我们会调整临床费用确认。我们根据当时已知的事实和情况,对截至每个资产负债表日期的应计费用进行估计。我们的临床试验收益取决于合同研究 组织和其他第三方供应商的及时和准确报告。虽然我们预计估计不会与实际发生的金额有实质性差异,但我们对所执行服务的状态和时间相对于所执行服务的实际状态和时间的理解可能会有所不同,并可能导致报告的金额在任何特定时期过高或过低。
基于股票的薪酬
我们根据授予日 员工、董事和非员工的公允价值来衡量授予员工、董事和非员工的股票期权和其他基于股票的奖励,并确认这些奖励在必要的服务期或相应奖励的授权期内的薪酬支出。随着 没收的发生,我们认识到没收对基于股票的薪酬费用的影响。我们将费用确认的直线方法应用于所有仅具有基于服务的授予条件的奖励。
119
我们使用Black-Scholes 期权定价模型估算授予日每个股票期权的公允价值,该模型使用普通股的公允价值和我们对普通股波动性的假设、我们股票期权的预期期限、接近我们股票期权预期期限的一段时间的无风险利率以及我们的预期股息率作为输入。
普通股公允价值的确定
由于我们的普通股到目前为止还没有公开市场,我们普通股的估计公允价值已由我们的 董事会或薪酬委员会在考虑到我们最近可获得的第三方普通股估值和董事会对额外客观 和主观因素的评估后确定,截至每次期权授予日期,这些估计公允价值已由管理层提供意见。 董事会认为这些客观因素和主观因素从最近一次估值之日起到授予之日可能发生了变化。从历史上看,我们的股权工具的这些独立第三方估值是 与确定的价值拐点同时进行的。
这些第三方评估是根据《美国注册会计师协会会计与估值指南》中概述的指导 进行的。作为补偿或实践辅助发行的私人持股股权证券的估值。本练习辅助工具确定了在每个估值日期确定普通股公允价值时跨系列股本类别分配企业价值的各种 可用方法。
用于确定我们普通股的估计公允价值的假设基于许多客观和主观因素,并结合 管理层判断,包括:
| • | 影响制药和生物技术行业的外部市场状况以及行业内的趋势; |
| • | 我们的发展阶段和经营战略; |
| • | 我们的可赎回可转换优先股相对于我们普通股的权利、优先权和特权 ; |
| • | 我们出售可赎回可转换优先股的价格; |
| • | 我们的财务状况和经营业绩,包括我们的可用资本资源水平; |
| • | 我们研发工作的进展情况; |
| • | 影响可比上市公司的股票市场状况;以及 |
| • | 美国整体市场状况以及我们普通股缺乏可销售性。 |
根据实践援助,概率加权预期回报方法(PWERM)和期权定价方法(OPM)是根据我们的发展阶段和其他相关因素确定普通股公允价值的最合适的方法。
我们的估值 是使用OPM方法进行的。选择的方法是基于可获得性和信息质量来制定方法的假设。
OPM?OPM将普通股和优先股视为公司总股本价值的看涨期权,行使价格基于公司证券在不同持有者之间的分配发生变化的价值 门槛。根据这种方法,普通股只有在可供分配给股东的资金超过发生流动性事件(如战略出售或合并)时清算优先股的价值时才有价值。普通股被建模为看涨期权
120
以预先确定的行使价对标的权益价值的期权。在该模型中,行权价格是基于与总股本价值的比较,而不是像 常规期权的情况那样,与每股股票价格进行比较。因此,普通股被认为是一种看涨期权,其行使价格等于优先股清算后紧随其后的剩余价值 ,对企业拥有索取权。OPM使用Black-Scholes期权定价模型为看涨期权定价。该模型将证券的公允价值定义为公司当前公允价值的函数,并使用了一些假设,如潜在流动性事件的预期 时机和股权证券的估计波动率。我们在2020年的估值中使用了OPM方法。
这些估值所依据的 假设代表管理层的最佳估计,其中涉及固有的不确定性和管理层判断的应用。因此,如果我们使用显著不同的假设或 估计,我们普通股的公允价值和我们基于股票的薪酬支出可能会有很大的不同。
一旦我们普通股的公开交易市场因本次发行的结束而建立,我们的董事会将不再需要根据我们授予的股票期权和其他此类奖励的会计核算来估计我们普通股的公允价值,因为我们普通股的公允价值将基于我们普通股的报价市场价格来确定。
下表按授予日期汇总了我们在2019至2020年间授予的普通股期权,以及截至授予日期我们普通股每股的估计公允 价值:
| 授予日期 |
股份数量 视选项而定 赠款 |
每股行权 期权价格(1) |
普通股公允价值 上的每股股票 期权授予日期(2) |
|||||||||
| 2019年1月1日-2019年6月30日 |
519,000 | $ | 3.33 | $ | 3.33 | |||||||
| 2019年7月1日-2019年12月31日 |
1,256,000 | 3.33 | 3.33 | |||||||||
| 2020年1月1日-2020年6月30日 |
5,270,589 | 3.33 | 3.33 | |||||||||
| 2020年7月1日-2020年12月31日 |
3,613,458 | 3.71 | 3.71 | |||||||||
| (1) | 经董事会批准,我们根据最近独立的 第三方估值授予了行使价格等于普通股公允价值的期权。我们的估值截至2020年9月1日、2020年2月12日和2019年2月12日。 |
| (2) | 上表中普通股的公允价值代表我们的董事会 根据我们最新的当时和独立的第三方估值,考虑到各种客观和主观因素后确定的我们普通股的公允价值。我们在2020年9月1日、2020年2月12日和2019年2月12日进行了回溯性评估。 |
新冠肺炎大流行的影响
2020年3月,世界卫生组织宣布新型冠状病毒病或新冠肺炎的爆发为大流行。新冠肺炎疫情正在演变,迄今已导致实施各种应对措施,包括政府强制实施的隔离、旅行限制和其他公共卫生安全措施 。新冠肺炎在全球各个行业造成了市场波动和不确定性,因此,我们预计我们的运营也可能受到影响。我们正在密切关注 新冠肺炎疫情对我们业务方方面面的影响。新冠肺炎最终对我们的运营和财务状况的影响程度将取决于未来的事态发展,这些事态发展具有很高的不确定性,无法有把握地预测,例如疫情的持续时间、可能出现的有关新冠肺炎严重程度的新信息,或者遏制新冠肺炎或处理其影响的行动的有效性 等等。此外,重现
121
根据感染率最高的地区,新冠肺炎病例或其他浪潮可能会造成其他广泛或更严重的影响。
我们的资产账面价值并未因此次疫情而出现任何重大减值损失,我们也不知道有任何 具体的相关事件或情况需要我们修改我们在经审计的合并财务报表中反映的估计。
新兴成长型 公司
2012年4月,“2012年创业法案”(Jumpstart Our Business Startups Act Of 2012)或“就业法案”(JOBS Act)颁布。JOBS法案第107节规定,新兴成长型公司、创业板或EGC可以利用修订后的1933年证券法或证券法第7(A)(2)(B)节规定的延长过渡期,以遵守新的或修订的 会计准则。因此,企业管治委员会可延迟采纳某些会计准则,直至该等准则适用于私营公司为止。在我们仍是一家新兴成长型公司期间,我们已选择将延长的过渡期用于新的或修订的会计准则 ;但是,我们可能会提前采用某些新的或修订的会计准则。
我们将 一直是一家新兴成长型公司,直到出现以下最早的情况:i)本财年的最后一天,我们的年收入超过10.7亿美元;ii)我们有资格成为大型加速申报机构的日期,非关联公司持有至少700亿美元的股权证券;iii)我们在前三年期间发行了超过10亿美元的不可转换债券 证券;以及iv)本财年的最后一天
我们也是一家较小的报告公司,这意味着我们由 非附属公司持有的股票的市值加上此次发行给我们带来的拟议毛收入总额不到7.0亿美元,我们在最近结束的财年的年收入不到1.00亿美元。如果i)非关联公司持有的我们股票的市值低于2.5亿美元或 ii)在最近结束的财年中我们的年收入不到1.00亿美元,并且非关联公司持有的我们股票的市值低于7.00亿美元,则我们可能在此次发行后继续成为一家规模较小的报告公司。如果我们 在我们不再是一家新兴成长型公司时是一家较小的报告公司,我们可能会继续依赖较小的报告公司可以获得的某些披露要求的豁免。具体地说,作为一家规模较小的报告公司 ,我们可能会选择在Form 10-K年报中仅显示最近两个会计年度的经审计财务报表,并且与新兴成长型公司类似,较小的报告公司 减少了有关高管薪酬的披露义务。
近期发布和采纳的会计公告
本招股说明书末尾的合并财务报表的 附注2中披露了最近发布的可能影响我们的财务状况和经营结果的会计声明的说明。
关于市场风险的定量和定性披露
利率风险
我们面临与根据我们与Midcap的信贷协议发行的可变利率票据的利率变化相关的市场风险 ;未偿还本金的利息按浮动年利率等于LIBOR利率加5.75%,LIBOR 下限为2%计算。
122
适用于我们可变利率票据的利率可能会上升,从而增加利息支出。我们不会购买或持有任何衍生工具来防范利率变化的影响 。截至2019年12月31日和2020年12月31日,根据我们与MidCap的信贷协议发行的债务的未偿还余额分别为1190万美元和 百万美元。
我们的现金和现金等价物 主要包括高流动性的货币市场基金投资和手头现金,原始到期日为90天或更短。我们的现金和现金等价物的公允价值不会受到利率 上升或下降的重大影响,这主要是由于这些工具的短期性质。
123
业务
生意场
概述
我们是一家临床阶段的生物技术公司 通过整合跨越生物、化学、自动化、数据科学和工程的技术创新来解码生物学,从而从根本上改善患者的生活并实现药物研发的产业化。我们使命的核心是Recursion 操作系统或Recursion OS,它结合了一个高级基础架构层,以生成我们认为是世界上最大、增长最快的专有生物和化学数据集之一,以及Recursion Map,这是一套 自定义软件、算法和机器学习工具,我们使用它来探索不受人类偏见限制的基础生物学,导航到新的生物学见解,并快速加速程序。 湿实验室生物学和硅片我们闭环系统中的工具加速了我们的药物发现过程,并使我们有别于行业内的其他公司。同样,我们平衡的LIFE团队 科学家(约40%的员工)和计算和技术专家(约35%的员工)创造了将经验数据、严谨的统计数据和创造性思维应用于每项决策的环境。到目前为止,我们已经利用我们的Recursion操作系统创造了三个价值驱动因素:i)35个内部开发的项目流水线,专注于重要的未得到满足的需求领域,其中几个项目的市场机会年销售额超过10亿美元;ii)与领先的生物制药公司建立战略合作伙伴关系;以及iii)归纳实验室,这是一个增长引擎,旨在探索Recursion操作系统在治疗学内外的新扩展。 自2019年以来,我们的流水线规模翻了一番,我们预计因此,我们是一家生物技术公司,规模更像一家科技公司。

图1.药物发现产业化的递归操作系统(OS)Recursion OS是一个集成的、多方面的系统,用于生成、分析和从海量生物和化学数据集中获得洞察力,以实现药物发现的工业化。它由支持硬件和软件的基础架构层、存放我们多样化且可扩展的数据集的递归数据领域,以及专有的发现、设计和开发工具套件Recursion Map组成。
125
我们相信,我们的方法已经证明,我们的方法实现了药物发现的产业化,拓宽了 潜在治疗起点的漏斗,在研究周期的早期发现了相对便宜的失败,并在降低成本的同时加快了高潜力候选药物的临床交付。2020年年中,我们开始从暴力搜索方法过渡,在这种方法中,我们体检我们图书馆中的每一种疾病模型和候选药物组合都使用我们的自动化湿实验室基础设施,以更高效、更强大的推理搜索方法。在这一新范式下,我们独立地描述数千种疾病模型和数十万候选药物,然后推断出数百亿种生物和化学关系。硅片,确定最有希望的候选对象进行进一步验证的优先顺序. 雄心勃勃的探索,使用我们目前的吞吐量和暴力搜索,可能需要大约1,000 年才能执行,现在可以推断几个月后。这一转变标志着我们在实现创始愿景方面取得了初步进展,它将海量生物和化学 数据集与现代机器学习(ML)算法融合在一起,以超越物理世界所能研究或探索的速度和规模,推动新疗法的无偏见发现。

年份2017 2018 20192020总表型实验(百万)2.2 7.6 23.9 55.6数据(PB)0.5 1.8 4.3 6.8细胞类型7 12 25 36 独特扰动1(百万)0.02 0.1 0.5 1.3总化学库(千)3 24 106 706推断关系2(十亿)NA 13临床资产0 1 2 4每个实验的成本3($)0.63 0.45 0.36 0.33
表1.我们历史上多轴增长的规模和加速我们是一家规模更像 技术公司的生物技术公司,我们的投入(湿式实验室使用的细胞类型)的超线性增长和产出(数据和临床资产)的快速增长证明了这一点。1独特的 扰动是指物理探索的基因、可溶性因子、细胞和/或化合物组合的数量。2推理关系指的是使用我们的递归映射预测的唯一 扰动的数量。3每个实验的成本是指执行一个表观实验的平均调整后的直接成本(定义为每次扰动一口井 ),包括消耗品成本、化合物成本和人工成本。
我们已经使用Recursion OS生成了一个包含35个内部开发程序的管道 。我们的计划针对的是横跨多个治疗领域的疾病:i)病因明确,ii)存在高度未得到满足的需求,没有批准的治疗方法,或者现有治疗模式存在重大缺陷。我们的几个计划针对的是年销售额超过10亿美元的市场机会超过10亿美元的适应症,我们正在准备四个流水线计划,以便在 进入第二阶段临床试验。
126
我们的八个值得注意的程序是使用我们的暴力搜索方法发现的:
| • | REC-4881用于治疗家族性腺瘤性息肉病,或FAP,预计将于 |
| • | REC-3599用于治疗GM2神经节苷脂沉积症,或GM2预期的第二阶段 开始于 |
| • | REC-2282用于治疗2型神经纤维瘤病或NF2预期阶段 2启动 |
| • | REC-994用于治疗脑海绵状畸形或CCM,预计将于#年启动 第二阶段 |
| • | 治疗糖尿病的铅分子艰难梭菌结肠炎潜伏期 |
| • | 治疗神经炎的先导分子新发现 |
| • | 治疗巴顿病的先导分子新发现 |
| • | 治疗Charcot-Marie-Tooth 2A型疾病(或CMT2A)的铅分子晚发现 |
紧随其后的是使用我们的推理搜索方法发现并迅速推进的两个值得注意的程序:
| • | REC-64151治疗人免疫关卡抵抗的实验研究STK11-突变型 非小细胞肺癌临床前 |
| • | MYC抑制分子治疗实体和血液系统恶性肿瘤的新发现 |
除了上述重点项目外,我们还在积极探索另外25个项目,这些项目可能会成为我们未来增长的 驱动力。使用我们新的推理搜索方法,自2020年7月以来,我们已经发现并启动了其中16个项目的验证。展望未来,我们预计我们渠道中的绝大多数新成员将使用我们的推理搜索方法 发现。

图2.我们的Recursion OS的强大功能,如活跃研发计划的广度所证明 我们已经开发了一个由35个内部开发的程序组成的流水线
127
跨越多个治疗领域,既包括现有化合物的新用途,也包括正在积极研究和开发的新化学实体或NCE。(1)我们的计划有可能解决神经炎症的一些适应症,包括在美国总计至少600万名患者的多种神经退行性疾病。我们打算在未来推出这些适应症的精选子集 。(2)美国每年的发病率为730,000例--欧盟5国。最初的临床研究将集中在总人群中复发率较高的亚群 。(3)每年美国-EU5发病率(4)全球流行(5)所有人每年的US-EU5发病率 NF2致病脑膜瘤(6)遗传性和散发性症状人群
在 其理想状态下,药物发现漏斗的形状将类似字母“T”,其中可能的治疗方法的广泛范围可以立即缩小到完美的候选药物,这将快速地完成 过程的后续步骤,而不会造成自然减员。我们的目标是利用技术将典型的药物发现漏斗重塑到其理想状态,方法是扩大潜在治疗起点的漏斗,通过在研究周期早期发现相对便宜的失败来迅速缩小漏斗,并加速开发高潜力候选药物。晚期临床失败是当今制药研发模式中成本的主要驱动因素。 降低代价高昂的后期失败率,加快从HIT到临床候选药物的时间表,将创造一种更可持续的研发模式。

图3.重塑药物发现漏斗。Recursion OS正在将传统的 制药管道重塑为更理想的漏斗。输入到该平台的大量生物和化学数据被快速分拣并输入到诊所的加速转换路径中。
128
我们相信,我们在重塑传统药物发现漏斗方面取得了以下进展:
| • | 拓宽治疗起点的漏斗。我们灵活且可扩展的基础设施 以及我们使用基于推理的用于预测疾病模型和候选治疗方案之间数百亿关系的递归图拓宽了发现漏斗的瓶颈,超出了假设和人类偏见的目标 。 |
| • | 在研究周期的早期识别成本相对较低的故障,以快速缩小漏斗的范围。递归地图结合了大量的生物和化学数据集以及计算工具,使我们能够:i)选择更高可翻译的治疗起点;ii)预测选定的吸收、 分布、代谢、排泄和毒理或ADMET,或ADMET,以快速确定候选药物的风险,并迅速优先考虑下游成功的可能性更高的计划。值得注意的是,这一策略不仅会增加早期的自然流失率,而且我们预计还会降低药物开发的总体成本。 |
| • | 加速将高潜力候选药物推向临床。递归地图 包含一套数字化学工具,可实现高效的化学空间探索,包括3D虚拟筛选以及提高稳定性和实用性的翻译工具体内学习。 |
我们利用不断发展的递归操作系统来探索许多疾病计划,其深度足以量化 与传统药物发现范式相比,计划在时间、成本和预期成功可能性方面的进步。这些指标是领先的指标,使用我们的方法,我们可以将药物发现产业化。我们相信,Recursion OS的未来 迭代将实现更大的改进。最终,我们希望将总的美元加权失败降至最低,同时最大化临床成功的可能性。

图4.我们药物发现漏斗的轨迹反映了最理想的药物发现漏斗 与行业平均水平相比,我们i)在早期确定了低可行性计划
129
研究周期,更快地缩小漏斗;ii)由于我们的方法,每个项目花费更少;iii)更快地将项目从项目开始推进到临床。显示的数据是自2017年末以来我们所有计划的平均值 1.
随着时间的推移,我们相信在上面强调的任何或所有方面持续和改进的 成功将提高整体研发效率,使我们能够解决使用传统药物发现方法可能无法在商业上可行的较小患者群体。 此外,我们相信我们的公正方法可能会导致新的目标,并使我们能够在竞争激烈的疾病领域超越其他人,因为在这些领域,多方通常同时追求有限数量的类似目标假设。这些 优势极大地扩展了我们技术的总潜在市场。
递归操作系统
Recursion OS是一个集成的多层系统,用于生成、分析生物和化学数据集并从中获得洞察力。它由 三个部分组成:
| • | 基础架构层:由高度可扩展的使能硬件和软件组成的同步网络,用于设计和执行各种生物实验,并随后存储我们不断增长的数据集。 |
| • | 递归数据宇宙: 截至2020年12月31日,我们的递归数据宇宙 包含了大约7 PB的高度相关的生物和化学数据,涉及多种不同的数据模式。递归数据宇宙的大小 自2018年来增长了三倍多,并且持续加速增长 。就背景而言,我们的数据集需要的存储容量已经超过人类历史上所有高清长篇电影的总和。 |
| 1 | 所有行业数据均改编自Paul等人。“自然”杂志回顾药物发现. (2010) 9, 203–214. |
130
| • | 递归映射:一套内部软件 工具、算法和机器学习方法,旨在将递归数据世界中的数据处理和转换为我们的研发团队可操作的见解。 |

图5.用于药物发现产业化的递归操作系统(扩展)Recursion OS是一个集成的、多方面的系统,用于生成、分析和从海量生物和化学数据集中获得洞察力,从而实现药物发现的工业化。它由支持硬件和软件的基础架构层、存放我们多样化且可扩展的数据集的递归数据领域,以及我们专有的发现、设计和开发工具套件Recursion Map组成。
用于生成我们专有数据集的湿实验室生物学和硅片我们 闭环系统中的工具使我们在科技药物研发领域脱颖而出。该领域的许多公司:i)利用不同的、嘈杂且通常不可复制的第三方数据集,这些数据集不太适合ML,或者ii)构建工具作为 为其他公司的服务,这可能会限制它们随着时间的推移带来的好处和影响。更重要的是,我们重复的湿实验室验证和硅片预测会产生飞轮效应,从而加速数据 的生成和学习并排进一步加强我们的药物发现平台。虽然新兴竞争对手和资源雄厚的大型现任者可能会 采取类似的战略,但我们作为先行者有两个优势:i)再多的资源也无法压缩所需的时间
131
观察自然发生的生物过程,ii)不断增长的递归数据世界产生复杂的网络效应,可能使缩小竞争差距变得困难。
基础设施层
递归操作系统的基础层是一个高度同步的硬件和软件网络,用于设计、执行、聚合和存储大约7 PB的快速增长的生物和化学数据。我们基于过去几年创造的尖端技术构建了我们 基础设施的核心要素,并继续在每个组件中采用新的技术进步。
我们的基础架构层的八个组件包括:
| • | 生物工具。我们利用最新的生物学工具,如CRISPR基因编辑, 构建人类疾病模型并探索大规模生物学。例如,我们创建了一种算法来定制设计一个排列的全基因组CRISPR文库,用于在多种人类细胞类型中单独敲除每个基因。 |
| • | 化学工具。我们对基础设施进行了投资,为候选药物存储了数百万个化学起始点,并在我们的设施中快速选择任何分子或分子组合进行实验。此外,我们正在对基础设施进行大量投资,以在内部大规模合成和分析新的化学实体。我们已经探索了其他方法,如抗体、蛋白质和基于RNA的疗法,并可以在未来迅速扩展我们的能力以支持这些领域。 |
| • | 细胞培养。我们已经投资了最先进的用于培养、存储和利用大量不同人类细胞类型和患者来源细胞系的设施和设备,用于发现和 验证实验。这包括使用最初为细胞治疗行业首创的生物反应器,将数十种原代人类细胞培养到数十亿细胞的规模,然后将它们储存在我们的生物库 设施中。 |
| • | 实验室机器人。我们创建了高度可扩展的自动化实验室机器人工作流程, 使我们能够每周进行多达150万次实验,每年最多50周,在任何给定时间都只有一个小团队监督我们的流程。每个实验的每一步都经过监控和测量,从而创建了一个全面的 层元数据,这对于我们的递归地图中的解释和分析至关重要。 |
| • | 数据捕获。我们利用最先进的从我们的实验中捕获高维、多模式生物和化学数据的硬件。这包括用于生成人体细胞图像的高通量显微镜, 用于收集RNA转录数据的测序系统,以及来自自定义动物研究笼中嵌入的摄像机的连续视频馈送。 |
| • | 技术堆栈。我们创建了高度可扩展的高级计算资源,使 我们能够在公共云和私有云环境中移动、存储、处理和保护PB级的数据资产。这个堆栈的一个基石是我们的最先进的ML超级计算机,BioHave-1,于2020年12月购买,我们相信它将是任何一家生物制药公司在药物发现应用方面全资拥有的最强大的计算机之一,在全球最先进的超级计算机中排名第66位。2 |
| • | 实验设计。我们构建了一套支持软件工具,使我们的科学家 能够每周设计越来越多的实验,同时考虑到实时的现场试剂供应、一致的控制策略和设计标准,使每周的数据能够随时间关联。 |
| • | 实验实施与质量控制。我们在一套支持 的软件工具上投入了大量资金,以协调每周多达150万个实验的执行,同时监控质量以保持高效的数据流。异常将自动标记给团队以供解决。 |
| 2 | NVIDIA(供应商)提供的TOP500超级计算机排行榜预估。 |
132
递归数据宇宙
递归数据宇宙是我们专有的高度相关的高维生物和化学数据集,涵盖多种 不同的数据模式。截至2020年12月31日,递归数据宇宙包含大约7PB的高度相关的生物和化学数据。
递归数据世界的核心是我们专有的、基于图像的数据集,我们认为它是世界上最大、最全面的数据集之一。每个映像都是我们的底层基础架构层的产品,底层基础架构层由以下自动化工作流程生成:
| • | 使用我们的细胞培养基础设施,我们培养了数十种人类细胞类型的数十亿个细胞,并将它们冷冻保存在我们的生物库设施中 。 |
| • | 使用我们的实验设计软件,我们每周可以设计多达150万个实验,同时保持 个关键设计和控制约束。 |
| • | 根据需要,我们解冻等份细胞,并将它们添加到1536孔的试板中。 |
| • | 使用不同的生物学工具,我们在这些细胞中模拟人类疾病,例如,使用CRISPR基因编辑来敲除人类基因或添加致病的可溶性蛋白因子。 |
| • | 同时,我们可以从化学工具中分析数十万个化学起点,以便能够对 药理相互作用进行建模。 |
| • | 所有实验板都由我们的自动化实验室机器人基础设施处理、存储和维护,然后再将其送入我们的高通量显微镜,该显微镜可捕捉细胞的高分辨率图像。 |
| • | 我们的实验执行和质量控制软件实时监控数据质量,仅将经过验证的数据移入 递归数据领域。 |

图6.用于生成基于图像的大规模数据集的自动化工作流。递归数据宇宙中的核心数据集基于我们自己的潮湿实验室中生成的数十亿张人类细胞的标记图像,这些图像跨越数百万种独特的扰动(即基因敲除、可溶性蛋白因子添加、药物添加或其组合)。
截至2020年12月,此过程每周最多可在 150万次实验中生成多达900万张图像,或大约80 TB的数据。重要的是,在实验过程中生成的元数据由自动和手动QC系统记录,以确保数据在添加到递归数据 领域之前是干净和可关联的。
133
图像是递归数据宇宙的基础数据集,原因有两个。首先,图像是二比四每美元的数据密度比转录组或蛋白质组学等其他高维数据集高出数量级,我们也利用了这两种数据集,但规模较小。其次,可以说,在过去十年中,神经网络在计算机视觉和图像处理领域取得了最大的进步。我们利用这些进步为 药物发现创建了我们的基于图像的专有算法,我们认为这些算法比使用其他类型的生物数据开发的算法要先进得多。
递归数据领域内的其他数据集 包括:
| • | 整形外科。大规模转录组和蛋白质组数据集的组合,用于验证在我们的表型平台上识别的化合物的活性,并进一步阐明候选药物可能的作用机制。 |
| • | 阿德梅特·阿萨德。大量吸收、分配、新陈代谢、排泄和毒理学 数据,使我们能够识别和预测经常导致计划终止的早期责任。 |
| • | 在活体组学中. 自定义 动物研究笼中嵌入的摄像头提供的传感器数据和连续视频馈送。使用这些数据,我们可以收集更多动物行为的整体测量结果,并创建体内疾病状态。 |
| • | 定制一次性评估。不同的自定义 分析集,用于特定于程序的验证。 |
我们计划继续利用我们的专业知识和基础设施投资来加快上述数据集的生成,并向递归数据领域添加补充的新数据资产 随着时间的推移。
递归映射
递归地图是一套快速发展的内部软件应用程序,旨在处理递归数据世界中的数据,并将其 转换为可操作的见解,供我们的研发团队加速执行程序。这些工具涵盖广泛的用途,包括:
| • | 数据处理。我们的工具可大规模管理和监控我们的数据流向适当的 公共和私有云,通过我们内部专有的卷积神经网络将我们的图像转换为数学表示,并根据用户的要求执行 参数化的标准和自定义分析。 |
| • | 生物和化学活动评估。我们的工具允许我们评估 疾病模型的健壮性,并使用蛮力搜索方法测量潜在疗法的活性。 |
| • | Program Insight。我们的工具将经过处理的数据转化为可操作的洞察力,使我们能够 推断生物和化学扰动之间的数百亿种关系,并预测潜在的安全隐患。 |
| • | 程序加速。我们的数字化学工具为我们的化学家提供有价值的 信息,因为他们可以将治疗起点优化为可行的候选药物,包括进行以下操作的工具硅片基于3D虚拟屏幕和密集的结构活动关系,成功扩展到内部和商业图书馆 。这些工具还包括增强功能的应用程序体内研究设计与实施。 |
现代ML工具,通过构建递归地图,学习识别高维、多因素数据中的复杂模式,而不需要人工监督。 许多递归地图都是由这些工具构建的,它们可以学习识别高维、多因素数据中的复杂模式,而不需要人为的监督。我们的ML工具旨在从基础生物学数据集中提取对人类解释来说过于复杂的见解,最大限度地减少人类偏见,并识别传统药物
134
发现方法可能会失败。我们的分析结果不一而足,有完全新奇的,也有挑战教条的。
当前和未来的递归地图工具套件增强了我们在药物发现过程的每个步骤中的决策,并可以越来越多地预测 后续步骤的可能结果。重要的是,这些硅片预测在我们自己的潮湿实验室中得到了验证。这在递归地图中创造了一个相辅相成的学习循环。经过实验验证的预测( 这是一个积极的信号)正在迅速推进,并加强了我们的学习。没有通过实验验证的预测是一个负面信号,它会生成有价值的数据来测试我们的理解,并且可以用来重新训练或重新加权算法,以 改进未来的预测。这种迭代的预测和验证过程是复杂数据集上成功的最大似然估计的关键要素。
我们的人民和 文化
我们在科技的交汇点和前沿开展业务。与传统生物技术公司不同,我们快速增长的200多名Recursionauts团队在化学家和生物学家等生命科学家(约40%的员工)和数据科学家和软件工程师等计算和技术专家(约35%的员工)之间进行了平衡,创造了一个将经验数据、统计严谨性和创造性思维应用于我们解决的问题的环境。当我们团结在一个共同的使命中时,破译生物学,从根本上改善生活,我们最大的优势在于我们的差异:专业知识、性别、种族、学科、经验和视角。刻意建设和培育这种文化对于实现我们大胆的目标至关重要。
我们的价值驱动因素
到目前为止,我们已使用Recursion OS构建了三个价值驱动因素:i)35个内部开发的计划管道,专注于重大未得到满足的需求领域,其中几个计划的年销售额超过10亿美元;ii)与领先的生物制药公司建立战略 合作伙伴关系;iii)诱导实验室,这是一个增长引擎,旨在探索Recursion OS在治疗学内外的新扩展。
135
我们的管道
Recursion的每一个程序都是我们的Recursion OS的产品。虽然我们有35个计划正在筹备中,但我们重点介绍了十个值得注意的 计划,考虑到它们各自的市场机会以及它们为每一代递归操作系统提供的验证,这些计划是关键的短期价值驱动因素。

图7.更广泛的递归流水线中值得注意的程序。鉴于其市场机遇和所提供的验证,值得注意的计划是我们近期的关键 价值驱动因素。我们的四个主导计划预计将在2021年招募患者参加第二阶段临床试验,同时临床前计划正在取得进展。(1)EU5被定义为法国、德国、意大利、西班牙和英国。除非另有说明,否则所有数字均为流行率。(2)全球流行 。(3)所有NF2驱动的脑膜瘤每年US-EU5发病率。(4)遗传性和散发性症状人群。(5)美国每年的发病率为730,000例--欧盟5国。最初的临床研究将集中在总人群中反复感染率较高的部分。 (6)我们的计划有可能解决神经炎症的一些适应症,包括在美国总计至少600万名患者的多种神经退行性疾病。我们 打算在未来选择这些适应症的子集。(7)每年的US-EU5发病率。(8)我们的计划有可能解决由以下因素驱动的 多个适应症MyC做些改动。目前,我们尚未最终确定特定适应症的目标产品配置文件。
暴力-强制 搜索程序
我们的八个值得注意的项目是使用我们的暴力搜索方法确定的。这些计划中有四个是 现有已知化学实体(KCE)的新用途,我们已将其推进到临床开发,并获得了密钥启用许可证。这些项目中的另外四个是新的化学实体,或称NCE,已经被发现并在内部进行了改进。
| • | REC-4881治疗FAP。REC-4881是一种口服生物利用剂,非ATP-竞争性正在开发MEK1和MEK2的变构小分子抑制剂 以缩小家族性腺瘤性息肉病(FAP)患者和躯体疾病患者的肿瘤体积装甲运兵车-突变肿瘤。REC-4881似乎耐受性良好,与预期用途一致,并且在人类中具有肠道定位的PK特征,这对FAP和潜在的其他胃肠道肿瘤非常有利。我们希望让 第一位患者参加第二阶段的双盲、随机、安慰剂对照试验。 |
136
| • | 用于治疗GM2的REC-3599 神经节苷脂沉积症。REC-3599是一种口服生物利用度高、选择性强的蛋白激酶C(PKC)小分子抑制剂,GSK3-b正在被开发用于治疗GM2神经节苷脂沉积症,或GM2。该分子已显示出强大的挽救致病生物标记物gm2和脂褐素水平的能力,这些细胞来自具有多种不同基因突变的患者。六角形或HEXB, 分别称为泰-萨克斯病或桑德霍夫病。我们目前正在 在一个动物模型中生成额外的药效学数据HEXB-突变的GM2应FDA的要求,预计将在 招募第一名患者参加开放标签第二阶段试验。 |
| • | 用于治疗NF2的REC-2282。REC-2282是一种经中枢神经系统渗透的口服生物利用型小分子HDAC抑制剂,正在开发中,用于治疗NF2驱动的脑膜瘤和神经纤维瘤病2型,或NF2。该分子具有良好的耐受性,包括服用多年的患者,并且潜在地降低了心脏毒性,这将使其有别于其他组蛋白去乙酰化酶(HDAC)抑制剂 。与已批准的HDAC抑制剂相比,REC-2282既是中枢神经系统渗透性的,又是口服生物利用度的。我们希望将第一位患者纳入第二阶段, 双盲、随机、安慰剂对照研究。 |
| • | 治疗慢性萎缩性胃炎的REC-994。REC-994是一种口服生物利用型、超氧化物、清除剂小分子,正在开发用于治疗脑海绵状畸形(CCM)。在我们在健康志愿者中进行的第一阶段单次递增剂量(SAD)和多次递增剂量(MAD)试验中,REC-994显示出极好的耐受性和对慢性剂量的适合性。CCM是最大的罕见疾病机会之一, 在美国和EU5约有36万名有症状的患者,没有批准的治疗方法。我们希望在 中招募第一名患者参加2期、双盲、安慰剂对照、安全性、耐受性和探索性疗效研究。 |
| • | 治疗艰难梭菌结肠炎的铅分子。我们已经确定了三种具有口服活性、肠道偏向的小分子铅NCE(REC-163964、REC-164014和REC-164067)。艰难梭菌毒素抑制剂,我们已经证明它是葡萄糖转移酶的抑制剂。这些分子具有预防疾病复发的潜力,可用于高危患者的二级预防治疗。艰难梭菌感染是抗生素相关性腹泻的主要原因,也是发病率和死亡率的主要原因。我们目前正在完成探索性的非临床安全性研究,以便能够选择开发候选药物。 |
| • | 治疗神经炎的铅分子。我们已经确定了三个 主要NCE(REC-648455、REC-648597和REC-648677),它们有可能成为第一位患者,口服生物利用、安全、中枢神经系统渗透的小分子小胶质细胞激活调节剂。小胶质细胞活化和神经炎症是阿尔茨海默病和帕金森病等神经退行性疾病以及多发性硬化症等中枢神经系统炎症性疾病的特征。小胶质细胞激活的小分子调节剂有可能减少中枢神经系统退行性疾病和炎症性疾病中与促炎过程相关的神经元死亡。该项目处于领先优化阶段。 |
| • | 治疗巴顿病的铅分子。我们已经确定了三种主要的NCE(REC-648190、REC-259618和REC-648647),它们具有口服生物利用度、CNS穿透性和疾病改善疗法的潜力,可用于多种亚型的巴顿病。巴顿病是一种常染色体隐性遗传的神经退行性疾病,由14个基因中的一个突变引起。CLN 个基因。虽然罕见,但这些疾病共同代表了最常见的儿童神经退行性疾病,并显示出重大的未得到满足的需求。该项目目前处于领先优化阶段。 |
137
| • | 治疗CMT2A的铅分子。我们已经确定了四个铅 分子(rec-64810、rec-648458、rec-1262和rec-150357)第一位患者,口服生物利用型疾病修饰分子,可减缓或逆转2A型线粒体疾病或CMT2A型线粒体疾病的进展。CMT2A 是一种罕见的常染色体显性遗传性周围神经退行性疾病,由CMT2A基因突变引起Mfn2导致小腿和手部进行性肌肉萎缩的基因。目前还没有批准的CMT2A疾病修饰疗法。此 项目当前处于主导优化阶段。 |
推理搜索程序
我们的两个值得注意的项目是从2020年年中开始使用我们的推理搜索方法确定的。这些 计划中的一个是现有KCE的新用途,另一个是内部发现的高级NCE。
| • | 用于治疗免疫检查点抵抗的REC-64151 在 STK11-突变体NSCLC中。我们已经确定了一种临床阶段口服生物利用型小分子的新用途,用于恢复和提高携带肿瘤抑制基因突变的肿瘤患者对免疫检查点抑制剂的敏感性。STK11。大约有3万例STK11突变型转移性非小细胞肺癌(NSCLC)在美国和EU5每年都会发生,这些突变已被证明预示着不良预后和对免疫检查点抑制剂(ICI),特别是抗PD-(L)1疗法的耐药性 。目前还没有被批准的治疗方法被开发出来专门调节肿瘤的反应。STK11突变的癌症。此 计划目前处于剂量优化阶段。 |
| • | MYC抑制分子治疗实体和血液性恶性肿瘤 。我们已经用我们的推理搜索方法确定了多个热门序列,这些序列随后在抑制myc下游的转录活性方面显示出浓度依赖性的活性。 在肿瘤学中,myc转录靶基因的表达增加,高达50%的癌症存在改变。MyC。具有抑制MYC依赖活性的新型小分子可以改善对多种肿瘤的治疗,特别是那些含有与MYC激活直接相关的基因突变的肿瘤。目前还没有被批准的针对MYC的分子。此程序当前在点击率领先相位。 |
除了上面强调的值得注意的项目 之外,我们还发现了另外25种化合物,它们可能被证明是我们未来增长的驱动力。使用我们的推理搜索方法,自2020年7月以来,我们已经发现并验证了其中16个程序。展望未来,我们 预计我们渠道中的绝大多数新成员将使用我们的推论搜索方法来发现。
138

图8.我们庞大而多样的附加研究计划。正在积极开发的其他项目涵盖了许多治疗领域,从癌症到炎症再到罕见的遗传疾病。所有这些程序都是使用我们的递归操作系统发现和开发的。
我们的合作伙伴关系
我们并不是唯一一个致力于将药物研发产业化并改善患者生活的公司。使用我们的Recursion OS,我们已经并将继续与领先的生物制药公司合作,这些公司拥有资源和经验来帮助我们广泛探索不同的疾病 领域(例如,纤维化、神经科学、肿瘤学、免疫学和炎症),并快速识别一流的和同类中最好的治疗候选人。
2020年8月,我们与拜耳股份公司(Bayer AG)在纤维化领域建立了多年的战略合作伙伴关系 。根据这项合作,双方同意在五年内启动10多个发现项目,以确定针对包括肺、肝和心脏在内的多个器官系统的破坏性和复杂性纤维性疾病的新疗法。拜耳从其专有库贡献了大约50万种化合物,并将在整个合作过程中贡献深厚的科学专业知识。
虽然到目前为止,我们的合作伙伴关系主要集中在小分子研究上,但未来的合作伙伴关系可能会扩展到大分子和新的治疗方式,包括基因疗法和细胞疗法。
139
我们的价值创造战略
我们是一家生物技术公司,规模更像一家科技公司。我们业务战略的中短期要素与我们的三个关键价值驱动因素保持一致 。我们打算:
开发当前的资产管道,同时实现超线性管道增长。
| • | 通过开发和潜在的法规提交,快速推进我们著名的产品。 |
| • | 超线性地扩展和推进我们的管道。 |
| • | 通过治疗性和机械性多样化以及选择资产合作伙伴关系来降低投资组合风险。 |
| • | 证明我们在发现和开发的每个阶段的时间和成本都低于行业平均水平。 |
| • | 证明我们临床项目的技术成功水平高于行业平均水平。 |
| • | 继续发展递归数据世界并改进递归地图,因为我们相信,将推动 递归和社会最大价值的资产是那些仍将到来的资产。 |
执行战略合作伙伴关系,最大限度地发挥我们 平台的潜在价值。
| • | 与行业领先的公司建立合作伙伴关系,涉及广泛的治疗领域或其他治疗 方式,例如大分子或RNA疗法,我们可以利用我们的工具和合作伙伴的专业知识和资源快速推进计划。 |
| • | 履行我们与拜耳在纤维化领域的战略合作伙伴关系。 |
通过归纳实验室探索递归地图带来的新扩展和商机。
| • | 通过探索切线业务(例如,其他治疗方式、诊断、金融、农业和兽医),最大限度地提高基础设施、工具和人员方面现有和计划投资的价值 。 |
如果我们成功地追求药物发现的产业化,我们可能有机会通过以下方式率先在生物制药行业内分配价值:i)在发现和开发过程中更早地与项目合作,同时获得更多价值;ii)解决原本被认为对传统药物开发来说太小或无利可图的高度未得到满足的疾病领域,以及iii)在创新和快速推向市场在重大治疗领域,处于领导地位。我们相信,这些努力的成功可能会给患者的生活和整个生物制药行业带来持久的、积极的和变革性的影响。
140
数字生物学的机遇
药物发现的过去和现在
传统的 药物发现和开发过程的特点是存在巨大的财务风险,开发项目的长期资本支出不断增加,而这些项目往往无法作为市场产品到达患者手中。从历史上看,将药物发现项目从早期发现转变为批准的治疗方法需要 十年以上的时间,每个批准的药物的平均资本化研发成本约为20亿美元。这样的生产效率达到顶峰的行业 从发现到商业化的成功率为8%到14%,导致该行业的内部收益率迅速下降,从2010年的10%下降到2019年的2%。3-7

图9.生物制药行业历史研发指标 发现和开发新药成本的主要驱动因素是临床失败。在启动的药物发现计划中,只有不到4%的药物获得了批准的治疗方法,导致每推出一种新药的风险调整成本在18亿至26亿美元之间。3-7
这些发人深省的指标表明需要更高效的药物发现过程。 传统药物发现依赖于科学界的基础研究发现,以寻找与疾病相关的途径和目标。从历史上看,生物学的复杂性迫使该行业依赖于复杂疾病关键驱动因素的简化论假设,这可能会造成一种羊群心态,因为多方追逐有限数量的治疗目标,并因正常的人类偏见(例如,确认偏差和沉没成本谬误)而加剧。使这一问题更加突出的是,当前药物发现活动的顺序性质导致了很长的时间线来消除此类假说的科学风险和代价高昂的晚期临床失败。
| (3) | 阿拉克里塔咨询公司。药物成功的概率。(2018年) |
| (4) | 德勤。十年过去了:衡量医药创新的回报(2019年) |
| (5) | DiMasi等人。制药行业的创新:研发成本的新估算。《卫生经济学杂志》。 47:20-33(2016) |
| (6) | Paul等人的研究成果。如何提高研发生产率:制药业面临的重大挑战。自然评论药物 发现。9:203-214(2010) |
| (7) | Martin等人。尽管业界做出了努力,临床试验周期时间仍在继续增加。《自然评论》药物发现。 16:157(2017) |
141
与此同时,技术创新(如ML)实现了效率和规模,改变了许多行业。然而,生物制药行业除了在非常狭窄的领域外,接受这种创新的速度一直很慢。其结果是,尽管积累了几十年的知识,药物发现可能会变得几乎是手工制作的,为创新制造了一个重大的(尽管是无意的)障碍。我们正在通过建造一种新型的药物发现引擎来填补这一创新空白,重新设计端到端 使用在过去十年中实现的技术进步从头开始的流程。
我们全新的药物发现方法
突破性技术创新的出现创造了设想在 规模上发现疗法的新方法的机会。我们正在率先整合这些跨越生物、化学、自动化、数据科学和工程的技术创新,以实现药物发现和开发的完全现代化。将高含量显微技术的进步与阵列CRISPR基因组编辑技术相结合,我们可以严格地生成海量、高维的生物和化学数据集,以探测多个人类细胞条件下基因组规模的生物学背景,从而产生 递归数据宇宙。同时,在技术行业的推动下,计算速度的指数级提高和数据存储成本的降低,再加上用于理解复杂数据的ML工具,使我们能够高效地利用这些海量数据集,并且不受假定假设的约束,对因果人类生物学进行公正的查询。我们相信,这将使我们能够获得科学研究人员以前无法获得的新的生物学见解,并在项目开始时降低 翻译风险。例如,给定任何感兴趣的基因,我们的平台都会显示它与递归数据宇宙中包括的所有基因和分子的关系,极大地扩展了可测量生物学的范围,并将新颖、基础科学和治疗发现结合到一个步骤中。
递归:一家规模更像科技公司的生物技术公司
科技公司生产可靠的软件,自动化并改进手动和定制流程,以更低的单位成本为客户带来价值。 将ML引入这些应用程序使机器能够从数据中学习并执行超出人类能力的复杂任务。
传统的药物发现方法通常始于特定的适应症和人类衍生的靶点假设。随后建立定制的化验,并生成数据,以确定针对提议的靶点的候选治疗方法。相比之下,我们 经验性地生成包含广泛适应症的大型数据集,数据涉及数十万种生物和化学扰动。我们将这些数据与我们递归地图中的 高级计算工具专有套件相结合,以启动和推进新的治疗方案。ML算法的进步与通过持续数据生成不断增长的知识体系相辅相成,形成了新见解的飞轮 ,提高了我们流水线的效率和产出。
142
最大的生物和化学数据集之一大约为7 PB,每周增加多达150万个实验数据 和作为递归地图中的一套软件应用程序,我们能够很好地自动化和加速基础科学和药物发现任务,使科学 团队能够快速、迭代地评估候选治疗方案。总体而言,这些进步可能会重新定义研发效率,因为技术已经颠覆了许多其他行业,我们相信它们将带来未来的计划增长,因为它们 在科技公司的背景下带来了未来的收入增长。

图10.我们的集成方法创建了一个迭代学习的闭环、良性循环。我们专有的数据生成、递归数据世界和高级计算工具递归地图的 组合,使我们能够生成新的见解来启动或加速治疗计划。我们反复使用此方法以 在我们的系统内创建学习的良性循环,并在发现和开发的每个阶段推进计划。
通过将递归操作系统应用于药物发现,递归希望将药物发现从连续的反复试验变成了一个搜索问题。
递归操作系统
Recursion OS是一个集成的多层系统,用于生成、分析生物和化学数据集并从中得出见解。它由三部分组成:
| • | 基础架构层:由高度可扩展的硬件和软件组成的同步网络,用于设计和执行各种生物实验,并随后存储我们不断增长的数据集。 |
| • | 递归数据宇宙:截至2020年12月31日,约有7 PB高度相关的生物和化学数据涵盖了表现学、正交学、英活组学和定制生物化验数据。 |
| • | 递归映射:一套内部软件工具、算法和机器学习方法 旨在将递归数据世界中的数据处理和转换为我们的研发团队可操作的见解。 |
143
| • | 递归数据宇宙。约7PB的高度相关 累积的生物和化学数据,涵盖表现学、正交学、InVivology和定制的生物分析数据。 |
用于生成我们专有数据集的湿实验室生物学组合和硅片我们闭环系统中的工具使我们在科技驱动的药物发现领域脱颖而出。此 领域的许多公司可能:i)利用不同的、嘈杂且通常不可复制的第三方数据集,这些数据集不太适合ML;或者ii)将工具构建为他人的服务,这可能会随着时间的推移限制它们的优势和影响。更重要的是,我们 重复的湿实验室验证和硅片预测创造了飞轮效应,数据生成和学习同时加速,进一步加强了我们的药物发现平台。虽然新兴竞争对手和资源雄厚的大型 现有公司可能会采取类似的战略,但我们作为先行者有两个优势:i)任何资源都无法压缩观察自然发生的生物过程所需的时间;ii)不断增长的递归数据 宇宙会产生复杂的网络效应,这可能会使缩小竞争差距变得困难。

图11.药物发现的递归操作系统(扩展)Recursion OS是一个集成的、 多方面的系统,用于生成、分析和从海量生物和化学数据集中获得洞察力,从而实现药物发现的产业化。它由支持硬件和软件的基础架构层组成,即递归数据 领域,它容纳了我们多样化且可扩展的
144
数据集和递归映射,这是我们专有的发现、设计和开发工具套件。
基础设施层

图12.基础架构层在我们的海量递归数据 领域中生成专有数据。基础架构层是Recursion OS运行的主干,由多种高度先进的使能硬件(深灰色)和软件系统(浅灰色)协同工作。
Recursion OS的基础层是一个高度同步的硬件和软件网络,用于设计、执行、聚合和 存储大约7 PB的快速增长的生物和化学数据。该层的离散组件包括以下组件:
生物 工具
我们特意设计了我们的平台,使用相同的基于图像的端点和核心技术堆栈对跨越多个治疗领域的广泛生物学进行建模,包括肿瘤学、免疫学、神经科学、心血管、新陈代谢和传染病。我们的模块化设计使我们能够系统地将搜索空间扩展到新的探索领域,同时将定制化验开发的需求降至最低。在我们流程的后续步骤中,我们的模块化设计和一致的协议使我们能够分析和比较结果数据横穿这些模块揭示了人类生物学和易于处理的治疗起点之间的相互联系。
遗传学模块。我们已经开发了我们专有的 协议,使用CRISPR基因编辑,以阵列和高通量格式模拟人类基因组中每个基因的基因缺陷。我们已经重复了这些CRISPR试剂的设计,有关详细信息,请参阅递归映射中的FreshCuts, 创建了我们专有的全基因组阵列引导RNA文库,称为N-检测就绪全基因组人类阵列库,或称独角鲸。我们继续构建这些工具的新 扩展,以扩展我们的遗传工具箱,包括函数增益和新的CRISPR基因编辑应用。总而言之,这些工具使我们能够 广泛询问人类遗传学,范围从孟德尔遗传病到针对肿瘤抑制生物的精确疗法。
可溶性因子模块。我们使用可溶性因子(如细胞因子和趋化因子)开发了我们的专利方案, 在广泛的免疫相关疾病基础上。使用这些方法,我们可以很容易地在同一实验中组合多种可溶性因子来模拟更复杂的疾病生物学,例如与巨噬细胞极化状态或细胞因子风暴相关的鸡尾酒。我们的免疫调节工具使我们能够询问具有挑战性和知之甚少的领域,如神经免疫学、炎症体生物学和免疫肿瘤学。
传染病模块。我们使用多种生物病原体开发了我们的专有协议,这些病原体导致了广泛的传染病 。例如,我们使用不同的
145
由艰难梭菌细菌对疾病进行建模,并随后为我们的晚期临床前研究确定了铅分子艰难梭菌结肠炎计划。在2020年上半年,我们使用了现场直播SARS-CoV-2病毒建立疾病模型,设置 端到端根据筛选方案,在不到4周的时间内测试1,670种美国食品和药物管理局批准的化合物和参考化合物对新冠肺炎的疗效。我们经常使用与先天免疫反应有关的药物(例如,脂多糖、环二核苷酸等)。以生成与传染病研究相关的其他模型。此 模块使我们能够广泛探索传染病生物学,并确定针对病原体和宿主定向靶点的治疗方法。
纤维化模块。我们正在与拜耳合作开发我们的专利模型和协议,以研究纤维化 疾病,包括细胞共培养系统。我们的新兴工具使我们能够解决这一复杂的疾病领域,在这里,传统的、基于目标的方法已被证明具有挑战性。
复杂的多细胞疾病工具。我们正在开发和扩大使用先进的共培养模式来探索多因素疾病,在这些疾病中,细胞间的串扰是疾病状态的关键驱动因素。这些方法在免疫学中特别相关,适应性免疫细胞(即T细胞、B细胞)和先天免疫细胞(即单核细胞、巨噬细胞)之间的调节对于理解全面的免疫反应至关重要。
患者派生的工具。我们正在积极开发新技术,以提高我们 验证和翻译早期发现的可译性和速度。我们正在积极寻找患者细胞(迄今为止,来自60多种疾病的300多个单独的细胞系),将它们重新编程为诱导多能干细胞(IPSCs),并将产生的细胞系存入银行,以便我们可以将这些细胞快速分化为多种组织特异性状态,以便在需要时进行下游验证。我们计划在未来 18个月内将这些努力的规模扩大一个数量级或更多。
我们继续构建更多的生物学工具和模块,以进一步扩展我们的搜索空间,同时维护一个通用的、基于图像的端点,以降低复杂性、提高灵活性,并确保我们不断增长的数据世界的相关性。随着时间的推移,我们计划引入更多的变量,如可变成像时间点、3D模型和组织特异性 有机物,它们使我们的屏幕更加接近人类系统生物学。
化学工具
我们的内部化学工具包括物理化合物收集,最先进的复合式储存和搬运基础设施,以及高精度的分析设备。我们经验丰富的化学家团队使用这种设备和声誉良好的CRO网络来快速推进发现工作,并提供差异化的候选药物。
已知化学实体 库。我们战略的一个组成部分是确定现有的临床前和临床小分子的新用途,但不是上市的小分子。这些化合物通常都有现有的数据包,我们可以利用它们 快速启动新的临床研究,加快患者的进程,同时增加计划回报。由于《孤儿药物法案》(Orphan Drug Act)为罕见病项目提供了额外的行业激励和保护,这些分子对于罕见病适应症特别有吸引力,否则这些项目可能会面临太多障碍,无法获得商业利益。此外,这些分子通常具有众所周知的作用机制,或称MOA, 使用我们递归图中的工具,我们可以用来发现未知化合物的MOA或启动新的NCE发现工作。
为此,我们 管理了世界上最全面的KCE库之一,目前包含6000多种化合物,涉及大约2500种独特的机制。我们积极
146
在公开论坛或文件中披露的新分子添加到这个库中,合成商业上没有的分子。我们的医药合作伙伴也可能向该文库贡献 化合物,进一步扩大其规模和化学多样性。
NCE起点库。此外,我们还可以从商业、半专有和专有来源获得70多万个小分子起点,并使用此库为小分子发现活动确定新的化学起点。 我们的NCE库中约有200,000个此类化合物,由我们的药物化学家管理,设计用于高度可药物的化学特性,同时避免不良的化学特性,如较差的溶解性和渗透性。 虽然此库的构建目的是最大限度地提高化学多样性,我们已确保包含多个复合岩芯的多个类似物,以帮助识别早期命中的紧急结构活动关系,并使命中快速扩展 为现成的类似物。根据我们与拜耳的战略合作伙伴关系,我们获得了额外的500,000个小分子起点,并将这些组合文库用作我们纤维化合作的起始底物。
使用我们的基础性暴力方法,在所有疾病模型中筛选越来越大的化学库将需要 平台吞吐量的指数增长。随着我们过渡到基于推理的发现方法,我们可以在多个蜂窝环境中加载和分析更大的复合库,而只需增加 带宽,这是递归操作系统的一个重要优势。因此,我们计划在未来几年通过内部投资和合作,以及在感应实验室内探索自动化微合成系统的新计划 ,大幅增加我们NCE图书馆的规模和多样性。我们相信,我们有潜力达到或超过拥有大约140万至400万种化合物的大型制药公司的规模。

图13.我们的内部化学库高度多样化。这是我们的小分子NCE库中大约200,000种化合物的结构多样性的可视化,其中
147
使用t分布随机邻域嵌入基于描述符对化合物进行聚类,显示了化合物的均匀分布和多样性。这种多样性增加了我们在广泛的生物学领域捕捉到有用的生化相互作用的可能性。
海量 复合存储&处理。我们在复杂的化合物管理基础设施方面进行了投资,允许在管子和板中对超过一百万种化合物进行环境控制(温度和湿度)存储。环境控制对于维持我们的化学库的长期稳定性至关重要,并且内部质量控制程序已经到位,以便随着时间的推移监控 库。该存储系统还可以快速扩展,以适应未来的增长。我们的系统可以从我们现有的复合库存中快速创建专门构建的定制库。此外,自动化移液系统已就位 以持续地将这些化合物等分并稀释成各种构型进行实验。所有关键事件和实验室数据都在我们的实验室信息管理软件中进行跟踪,该软件与实验设计和 日程安排软件集成在一起,为我们的实验提供准确、无缝的信息跟踪。
药物化学/CMC 外包。我们由经验丰富的药物化学家组成的内部团队执行所有药物设计活动,但将药物合成和选择ADMET分析外包给 个信誉卓著的CRO网络,我们与这些CRO建立了良好的关系。外部CRO提供了易于扩展和特定于项目的资源灵活性,可获得不同的化学专业知识,并可在我们迭代SAR时快速周转。截至2021年1月,我们有超过50名全职相当于全职员工(FTE)的多家供应商致力于扩展KCE库并在不同阶段推进6个计划,并制定了在2021年第一季度再增加65名全职FTE的计划。随着项目进入更高级的临床前阶段,大规模合成是更重要的任务,我们的药物化学家与我们的CRO和内部CMC小组更加紧密地合作,为临床前、IND支持和临床供应制定详细的材料计划。
148
分析和生物分析化学。我们已经建立了一个分析实验室,配备了最先进的液相色谱-质谱联用设备。我们的实验室进行分析工作, 评估化合物纯度和鉴定以进行质量控制,生物分析工作测量血浆和组织样本中的化合物水平体内ADME和疗效研究,以及血浆蛋白结合和渗透性研究。 此外,该团队还开展生物标记物识别和验证活动,以支持临床前和临床转化工作。

图14.我们可扩展的自动化复合存储和处理系统实现了灵活性和 速度。我们的系统使我们能够安全可靠地将100多万种化合物储存在板或管中,并快速创建专门定制的库。该系统是我们的基础架构层中众多高度自动化的 组件之一,并与实验设计和日程安排软件集成,以最大限度地减少错误。
149
细胞培养
我们 已经建立了最先进的细胞培养设施可持续生产高质量的哺乳动物细胞,如静脉、肾脏、肺、肝、皮肤和血细胞亚群,这些细胞可进入我们平台上运行的每个实验并进行后续验证。我们利用一个工具箱体外培养在降低成本的同时实现规模化生产的细胞培养技术。这包括 逐步使用25厘米大小的小烧瓶2 生长表面积,到大型一次性生物反应器,375,000厘米2 生长 表面积,这使我们能够产生100亿个正常的人体细胞,这足以每批生产多达5,000,536个孔板。我们正在积极参与前沿创新,如微载体悬浮培养系统,以进一步扩大我们的 工作。

原生细胞缩写。细胞系简称br。IPSC来源的细胞类型正常人皮肤成纤维细胞NHDF腺癌人肺泡基底细胞A549 IPSC来源的心肌细胞肾脏原代近端小管上皮细胞R-PTEC人心肌细胞系AC16 iPSC来源的神经元人骨髓间充质干细胞hMSC自发永生化视网膜色素上皮细胞HepaRG肺腺癌CALU-3骨骼肌内皮细胞HUVEC人原发性胰腺癌BXPC3正常人表皮角质形成细胞Nhek神经母细胞瘤细胞系SH-SY5Y巨噬细胞(来自Apheresis,白细胞)巨噬细胞单核细胞系THP-1外周血单个核细胞PBMC人骨肉瘤上皮细胞U2OS成人视网膜色素上皮细胞RPE-Ad乳腺/乳腺;来源于转移点AU565人肝细胞癌HuH7小气道上皮细胞SAEC正常人支气管上皮细胞NHBE正常 人肺成纤维细胞NHLF纯化单核细胞(来自Apheresis、Leukopacs)单核细胞(Apheresis,Leukopacs)单核细胞
表2.我们平台上的多种细胞类型 使我们能够广泛地询问生物学。到目前为止,我们的高通量发现系统已经安装了30多种人类细胞类型,包括原代细胞、细胞系和来自ipscs的细胞。
150
我们通过实施在科技药物研发公司中不常见的设施设计和控制系统,在我们的细胞培养设施中保持了良好的质量和一致性记录。这些设计和控制包括严格的过程验证和文档、人员培训和资格认证计划,以及例行的质量监控。我们的质量体系是这样设计的,我们定期监控我们的表现,以识别和实施适当的预防性和持续改进措施。

图15.我们利用细胞治疗行业首创的生物反应器技术,为我们的大型内部实验培养大量细胞。
实验室机器人
我们组装并同步了机器人组件,如液体分配器、洗碗机和孵化站,使我们能够高效地 每周执行多达150万个实验,而在任何给定时间只有一个小团队监督该过程。这些机器人系统在设计上是模块化的,并且可以轻松配置,使我们能够创建复杂多变的工作流程。这种灵活性对于使用我们的各种生物工具(例如,遗传和可溶性因子)和化学库进行大规模和高质量的实验至关重要。
151
我们通过使用多个系统来确保我们的实验室生成一致、准确和精确的数据: 防止细胞污染的设施控制;确保一致性的严格分析验证和仪器鉴定;以及自动捕获数据和跟踪所有关键实验规格的例行质量监控。我们的 质量体系的设计使我们能够定期监控我们的绩效,以确定并实施适当的预防性和持续改进措施。

图16.我们的高通量自动化平台看起来更像是一个复杂的制造设施,而不是生物研发实验室 。我们的平台每周可执行多达150万次高质量的实验,以支持下游分析。
152
我们的实验室每年运行大约50周。自2017年以来,我们的吞吐量每年至少翻一番,我们预计2021年我们的吞吐量将至少再翻一番,同时达到我们的质量基准。我们已经实现了这一级别的卓越运营,通过将最先进的技术和采用精益生产原则。

图17.我们的高维表观组学分析的实验吞吐量随着时间的推移有了显著的增长。我们的表型组学分析能力在整个2021年都在增长,在经历了新冠肺炎诱导的,2020年初全面关闭办公室 。
数据捕获
递归数据宇宙 包含大约7PB的高度相关的生物和化学数据,跨越多种不同的经济形态。我们已经投资了最先进的用于大规模捕获这些数据的设备和流程,以确保将最高质量的数据送入递归数据世界。
153
高通量显微镜。递归数据领域的核心是 我们基于图像的数据集。截至2020年12月,我们的实验室安装了13台ImageExpress显微镜。这些显微镜几乎连续运行,每小时通过六个成像通道捕获超过91,000张荧光显微镜图像 。如果检测到质量问题,将自动触发警报,使我们的团队能够快速重塑我们的实验条件,以获得更高质量的数据。在成像后,我们的数字数据管道会立即将这些图像上传到 云中,并在几秒钟内对其进行处理。每周,我们的管道都会捕获、上传和处理高达80TB的成像数据,以添加到递归数据宇宙中。

图18.我们的大型高通量显微镜安装。13台高通量 自动化显微镜由多个机械臂提供服务,以实现我们的表观实验近乎连续的成像。这种成像过程不仅提高了成像速度,而且减少了人为干预和误差。
高通量测序。2020年,我们购买了第一个测序系统,并将其集成到我们的实验室中。这台 设备使我们能够在内部捕获完整的转录组测量结果。随着时间的推移,我们打算增加对高通量测序的投资,并集成更大规模的生产系统,以将另一个快速增长的互补数据流 添加到递归数据领域。
154
在Vivo数据收集中。我们使用我们专有的CAGE硬件和 连续的高分辨率视频系统来大规模收集InVivics数据。截至2020年12月,我们已有7个机笼系统投入运行,并积极调查了总共343个可能体内受试者正在接受我们候选药物的药代动力学、疗效、 和安全性研究。这些数据在10分钟内被上传到云中,在那里它被集成到我们的递归数据宇宙中。

图19.我们专有的、可扩展的智能住宅系统体内研究自动收集并 连续分析所有笼子中的视频和传感器数据。
其他数据收集系统。除了 表现学、正交学和InVivology之外,我们在验证我们的发现计划时,还不断地从定制的分析中获取实验数据。示例数据捕获基础设施包括用于生物分析、流式细胞术、 和电细胞-基质阻抗测试的多路复用读数。生成此数据后,它将包含在递归知识库中,这是我们的数据仓库系统,它将一次性实验分析与递归数据世界的其余部分连接起来。
技术堆栈
递归操作系统构建在高度可扩展和灵活的核心技术堆栈之上。我们采用了全新的混合云战略,根据环境和我们的需求充分利用公共云和私有云基础设施的优势:
| • | 公共云。对于生产工作负载和 应用程序,公共云是我们的默认选择。公共云计算提供商提供的规模、计算和存储弹性以及规模经济使我们能够经济高效地执行我们的战略。 |
| • | 私有云。私有云或边缘计算用于集成我们的实验室数据流, 包括将数据上传到公共云。 |
| • | 私有云中的BioHave-1和高性能计算 。2020年12月,我们进行了一项重大投资,以扩大我们的计算能力,购买了一台名为BioHave-1的世界级超级计算机。320个GPU和200个峰值AI 千万亿次浮点运算, 生物蜂巢-1是 |
155
| 截至2021年1月,预计在全球最强大的超级计算机500强排行榜上排名第66位。这一新的计算能力将使我们能够更快、更高效地迭代新的神经网络 架构,加快我们的深度学习模型,并增强我们不断增长的ML专家队伍。在我们的现有群集上运行需要一周的深度学习项目在新群集上只需要不到一天的时间。 |

图20.我们相信BioHave-1是最强大的超级计算机之一 完全致力于单一公司的药物研发。这幅图显示了生物蜂巢1号在安装时的样子,预计将于2021年初安装。超级计算机进一步 扩展了我们快速改进ML模型的能力。
启用软件工具
除了我们的基础设施,我们还构建了一套工具,使我们的科学家能够准确地设计、执行和验证每周150多万个不同的实验的质量,包括现象分析、正交分析和ADMET分析。我们的工具考虑了实时的现场试剂供应,实现了一致的控制策略和设计标准,使每个 周的数据能够随时间变化而相互关联。此外,这些工具会自动标记未达到质量要求或在过程中的某个点停滞的实验或过程,并通知相应的Recursionaut,为他们提供手动干预所需的工具 。
实验设计工具
大锅。CROCRON是我们专有的实验室信息管理系统,用于跟踪试剂库存,并 便于从我们的库、生物试剂和细胞类型/系中快速灵活地选择化合物。大锅与我们的实验室设备和操作无缝集成,因此可以在实验设计期间查看实时库存并计算 。
实验快乐。实验喜悦是一个自定义软件应用程序 开发,使生物学家和化学家能够创建大型和复杂的实验设计(例如,数百万
156
扰动条件),轻松使用内部验证的构造,在最大化信号和相关性的同时将实验伪影和噪声降至最低。实验快乐自动 对海量平板布局的扰动进行随机化,包括适当的控制,创建试剂挑选列表,并自动执行基本质量保证,更好地确保在单个系统中管理实验元数据。

图21。实验愉悦使我们的生物学家能够设计大规模的实验,同时遵守我们复杂的 专有布局规则。实验快乐是我们的内部实验设计工具,用于快速创建具有高度灵活性的大型实验集,同时整合我们在大约十年的迭代改进过程中学到的实验 布局的专有规则。图形界面便于实验板布局规范。
新鲜剪裁。FreshCuts是我们的专有算法,用于设计CRISPR基因编辑引导RNA,以实现最大的敲除效率。该算法 基于我们的内部基因敲除效率测序数据,这些数据是从我们的核心表型组学平台中使用的我们自己的主要细胞类型生成的。使用FreshCuts,我们创建了一个专有的、全基因组排列的CRISPR基因编辑库--独角鲸, 与供应商指南设计相比,它在基因敲除效率方面有了明显的改进。

识别高效CRISPR指南的期望专用性比供应商型号改进95%2.7x 80%2.2x
表3.FreshCuts超过 最先进的供应商库设计算法。在每个特定阈值下,FreshCuts都能够 成功地设计出更多有效的指南。
实验执行和质量控制工具
实验执行指挥中心。实验执行指挥中心(EECC)是我们开发的一套工具和仪表板 可自动连续执行
157
监控我们的研究人员设计的实验方案。EECC自动比较来自实验设计和执行动作的元数据,以确认正确执行。此外,EECC 允许用户通过各种执行状态监控实验进度,并为仪表板提供关于我们可靠的实验执行的明确指标。该系统是我们负责大规模执行我们的表观组学平台的团队的中流砥柱 。
图像资源管理器。Image Explorer是一个自定义的Web应用程序,使 我们的科学家能够查看来自我们的表观组学平台的显微图像并与之交互,包括:分离特定的污渍、过滤实验中的图像至具有特定生物或化学扰动的图像,以及查看与每个图像和实验条件相关的 元数据。图像资源管理器是质量控制和实验调试的关键工具。

图22。图像资源管理器允许生物学家清晰地查看图像,以识别潜在缺陷并确保数据质量 。Image Explorer使我们的科学家和实验室技术人员能够查看和浏览我们的图像以及元数据和任何由此产生的质量控制指标。
肖像师。ICOTOGISTER是我们的专有工具,用于捕获图像级别的质量控制指标,并在图像从我们的平台流式传输到云时识别 系统错误。这些测量包括关于通道强度的汇总统计、图像焦点的量化、细胞计数和关于图像捕获的元数据。图标绘制器将 与其他检查图像趋势的工具(如PlateWatch和实验执行命令中心的组件)集成在一起。
158
PlateWatch。PlateWatch是用于检测板级质量问题的自定义应用程序 。由于我们的实验条件在微滴定板上的排列特性,这些实验有时会受到混杂的板内空间效应的影响,例如放射状图案。虽然我们的实验室控制和 机器人工作单元减少了与生物实验自然相关的噪音和变异,但PlateWatch会标记任何异常,以便可以解决问题,并在需要时从递归数据世界中删除。

图23。PlateWatch使我们的团队能够识别潜在的违规行为,并确保 高质量数据进入递归数据领域。PlateWatch自动生成板块级别的指标和数字,以协助我们的技术人员为 所有表观组学实验提供质量控制,快速识别可能存在问题的板块,并确保高质量的数据进入递归数据世界。在这种情况下,一组车牌不由于板对各种参数的影响而通过QC 被自动标记以供进一步审查。
159
递归数据宇宙

图24。位于递归映射核心的递归数据宇宙。递归地图的核心资产是递归数据宇宙,它包含多种复合在一起的数据类型,整体上提供了比 更好的洞察力各部分的总和。
160
递归数据宇宙由大约7PB的高度相关的生物和化学数据组成,包括:表型组学、正交学、ADMET分析、英活组学和定制的生物分析数据。随着我们推进药物发现和开发计划,这些不同的数据模式具有很强的互补性。物候学数据提供了广泛的生物和化学数据的基础层,而其他数据集则提供了更多的翻译洞察力。自2018年以来,递归数据宇宙的规模增长了三倍多,而且还在继续加速增长。

图25递归数据宇宙中的各种数据集具有很强的互补性。递归 数据宇宙由跨越多个数据模态的互补数据集组成。虽然可以经济高效且规模化地生成表观组学数据,但其他数据集(如转录组、蛋白质组学和InVivology)提供了越来越多的洞察力,因为 我们将程序从早期发现转化为开发。
161
表型组学
在 ,递归数据宇宙的核心是由我们的自动化表型组学平台生成的专有细胞图像数据集。虽然我们的表型组学平台的输入可能会因我们使用的生物和化学工具而有所不同,但读数 保持不变:荧光显微镜图像捕捉细胞形态(一种细胞表型)的复合变化。我们使用我们的单一、专有染色方案来捕捉几乎所有 现象实验中细胞形态的这些变化。该方案包括六种亚细胞染料,在六个不同的通道中成像,经过优化,可以捕获几乎所有可以在实验室条件下培养和干扰的人类细胞类型中的各种生物。因此,我们可以捕捉到一系列令人感兴趣的生物和药理学现象的影响,包括小分子引起的表型变化,遗传增益-以及功能丧失,毒素、分泌因子、细胞因子或上述任何组合。

图26。我们的荧光染色方案可对多个大型细胞结构进行成像,以捕获对细胞状态的整体评估 。我们使用荧光染料对一组常见的细胞亚结构进行染色,然后用荧光显微镜成像捕捉到这些亚结构。结合递归地图中的工具,这种复杂而丰富的 生物数据模式可用于解决一系列科学问题。上图是6个通道的合成图。接下来是HUVEC细胞的6个单独的通道人造彩色图像:蓝色的细胞核、绿色的内质网、红色的肌动蛋白、青色的核仁、品红的线粒体和黄色的高尔基体。通道内容重叠的部分原因是荧光染料之间没有完全的光谱分离。
细胞形态是对细胞状态的一种整体测量,它将细胞生物学底层的变化(包括基因表达、蛋白质生产和修饰以及细胞信号)整合到一个强大的读数中。图像的每美元数据密度也比专注于这些更接近的读数的其他组学数据集高2到4个数量级,使我们 能够生成更多的每美元数据,为我们的药物发现工作提供信息。事实上,自2017年以来,我们的表现学平台的容量每年大约翻一番,目前通过150万次实验,每周向递归数据宇宙生成多达900万张图像或80TB的新数据。我们预计2021年这一产能将再翻一番。
162
最后,我们的表现学方法建立在过去五年技术行业推动的强大计算机视觉和ML方法 最近的爆炸性发展基础上。可以对现代ML工具进行培训,以识别图像的最显著特征,而无需依赖任何预先选择的、特定于疾病的主题 专业知识,即使这些特征是人眼无法察觉的。使用这些工具,我们可以捕捉由致病干扰或治疗引起的聚合细胞反应,并以公正的方式量化这些变化, 将我们从人类偏见中解放出来。相比之下,传统的药物发现依赖于假定的靶点假设和定制的生物信号分析,它们只能捕捉限制生物探索范围的狭隘的、预先确定的生物学。

图27。ML算法可以检测人眼无法分辨的细胞表型。我们图像中的大多数形态差异太微妙,肉眼无法察觉;然而,像我们在递归映射中部署的ML算法可以很容易地区分它们。此处显示的这些图像的习得嵌入之间的相似 热图显示了高度相似的细胞变化的明显分离。
整形外科
表型组学提供了成本效益高、信息丰富、功能齐全的生物学数据,非常适合广泛的生物学探索;然而,转录组学和蛋白质组学等其他数据模式可能具有很强的互补性。这两种方法都会产生补充数据,这些数据可用于:1)解开化合物的活性作用机理和/或2)更精确地 测量(和确认)化合物的功能活性和功效。虽然使用这些方法测量生物分子的成本比表型组学高出几个数量级,但这些数据可以为先进的项目提供高度的信息。此外,如果我们能够以经济高效和规模化的方式生成这些数据,我们可能能够显著减少在每个生物分子基础上开发特定分析所需的时间。总而言之,我们将这些可供选择的模态称为正交学,即作为递归数据宇宙的一部分的正交组学级别数据集的生成和集成。
按比例转译。我们已经开发出一种内部实验室流程,能够从我们的任何生物模块中提取样本, 分析2万多个基因。我们通常每周对数百个样本运行这一过程,截至2021年1月,我们已经收集了1920个不同个体 扰动的完整转录组数据。从扩展表观组学中吸取教训,我们正在积极增加产量并降低样本成本,以将这种方法扩展到数量级。
大规模蛋白质组学。2021年1月,我们与一家蛋白质组学供应商签订了一项为期一年的协议,以测量数千种蛋白质水平的变化 为了加快我们的功能验证和机械去卷积工作,我们需要对数千个样本进行分析。同时,我们正在共同开发 定制蛋白质组学面板,以实现翻译后修饰的测量,以及规模化和更具成本效益的多重蛋白质组学面板。在迄今为止的小型先导性蛋白质组学研究中,我们利用大约166个蛋白质分析器, 证明了由此产生的蛋白质组分
163
通过识别受我们平台确定的致病干扰和治疗化合物影响的途径和特定蛋白,可以帮助通知和指导程序验证。

图28。蛋白质组学功能增加了丰富的功能数据,这是对我们的表现学数据集的补充 。小分子JAK1/2抑制剂挽救干扰素诱导的人原代细胞复杂蛋白质组学特征的实验研究g。整合蛋白质组学等其他模式增加了递归数据宇宙中可用数据的多样性.
其他规模经济学。规模化代谢组学和脂质组学的探索和开发是我们的路线图,作为正交验证的额外 中通量机制。
阿德梅特·阿萨德
虽然我们的表型组学平台历史上一直被用来识别化合物疗效的信号,但我们正在积极探索使用我们基于图像的 读数来在药物发现过程的早期预测有希望的化合物的适配风险。穷体内药代动力学,包括不想要的副作用,是晚期药物计划失败的主要驱动因素。
为了训练预测ADMET模型,我们的团队建立了涵盖各种复合风险的大型ADMET数据集,包括CYP抑制,它 可以指示药物-药物相互作用的并发症风险和HERG风险,这可能表明心律失常的风险增加。此外,我们发展了一种心肌细胞球体搏动试验,作为一种体外培养心脏毒性的替代物 。所有这样的admet数据,使用我们内部的复合库生成,都驻留在递归数据宇宙中。重要的是,与通常仅为单程序使用创建的传统ADMET数据不同,我们的ADMET数据是在高度受控和标准化的分析条件下生成的,以实现高保真预测模型。
如后续章节所述, 此admet数据已与表观和化合物结构数据相结合,以创建早期预测模型,在投入时间和资源之前筛选出潜在责任可能性较高的候选药物。
在活体组学中
活体内研究是 在完整、复杂的生物系统中评估化合物有效性和安全性的重要工具。与药物发现和开发过程中的其他步骤类似,常规体内研究充满了人类偏见,而且局限于它们测量的终点。使用我们的在体数据收集基础设施,我们可以使用 收集单个动物的行为和生理状态的更全面的测量结果
164
持续的视频馈送和我们专有的动物笼子,在它们的家中监视动物。通过自动化数据收集过程,我们可以在几天、几周甚至几个月内不间断地收集动物 行为和生理的数据,从而在整个研究过程中对动物的健康状态进行更准确和全面的评估。这些数据随后可以用来创建更抽象的动物行为表示 ,从而使我们能够快速地对新的动物模型进行表型分析和识别体内可能与评估复合疗效和潜在风险更相关的疾病特征。
定制一次性评估
除了上述大型数据集之外,我们的团队在开发程序特定验证所需的自定义分析方面经验丰富, 规模较小。这些检测涵盖了不同的生物分子,包括核酸、蛋白质和脂质,从而完全覆盖了不同的治疗领域。这些定制化验的典型例子包括:
| • | 用于测量蛋白质变化的高含量蛋白质易位读取器和多路读取器 |
| • | QPCR或基于珠子的技术来测量记录变化的面板 |
| • | 质谱法测量更具挑战性的生物分子(例如,低丰度蛋白质、脂质和代谢物) |
| • | 电池-衬底阻抗传感、活细胞成像和其他功能读数 |
| • | 流式细胞术检测不同细胞亚群 |
生成此数据后,它将包含在递归知识库中,这是我们的数据仓库系统,将 一次性实验分析与递归数据世界的其余部分连接起来。
165
递归映射
递归地图是一套快速发展的内部软件应用程序,旨在将递归数据世界 中的数据处理并转换为可操作的见解,供我们的研发团队加速执行程序。

图29。递归映射。递归地图是海量生物和化学 数据集(或称递归数据世界)和一套专有数据生成、发现和开发工具的组合,可将数据转换为可操作的洞察力。我们专有的数据生成和软件工具的结合为数据驱动的决策提供了 基础。
数据处理工具
要理解、探索和关联递归数据宇宙中的新数据或现有数据,我们必须对数据进行规范化、转换和分析。我们在 这一层中的工具管理将我们的数据大规模地传输到适当的公共云和私有云,通过我们内部专有的卷积神经网络将我们的图像转换为数学表示,以及根据用户的要求对我们的数据执行的标准和自定义分析。异常情况会被标记给团队,以便快速解决。
电影公司。Moving Pictures是我们的专有应用程序,可安全高效地搬家从我们的表现学平台到云环境的海量图像 数据,这是我们数据处理管道中非常重要且非常关键的一步。每周约150万次实验中,此数据传输量可能接近80 TB。Moving Pictures与我们的硬件和其他软件系统紧密集成,具有高度的容错性。
166
管道工程. 管道工程是我们专有的内部系统,用于处理 和协调在我们的表观组学平台上,每周生成数百万张图像,进行各种图像级别的处理活动。使用Pipeworks,我们可以应用复杂的计算机视觉算法从高维 图像中提取信号,然后运行在大型显微镜图像库上训练的深层卷积神经网络,从这些图像创建高维抽象特征表示。

图30。Pipeworks过程将原始图像转换为允许跨图像 比较的功能列表。显微镜图像通过一个深度的卷积网络,其结构与上面的类似,由Pipeworks组织。网络根据我们的表观组学数据进行训练,以便将每个图像逐层转换为代表图像中细胞生物学的128个特征的列表。由此产生的功能为下游分析提供了动力。
分析平台。我们的分析平台负责使用Pipeworks创建的特征表示 、来自设计工具的实验元数据和我们的科学团队成员定义的分析参数来执行定义的任务。这些任务可能包括执行生物和化学活动评估、准备数据以在我们的 基于推理的屏幕中使用,以及评估我们的特征表示的质量。数据科学家通常会将更多的分析添加到系统中,然后科学家就可以选择这些分析。分析平台强大、可重复性和高度灵活性,使 我们能够快速加入不同的疾病模型和实验类型。
生物和化学活性评估
我们的活动评估工具使我们能够评估不同疾病模型表型的稳健性,并随后测量这些疾病模型中潜在的 治疗剂的活性。这些工具在设计上与目标无关,从整体上探索细胞生物学,能够同时探索多种疾病模型和潜在的治疗方法,而不需要对核心平台进行重大更改 。
167
PhenoDetect。PhenoDetect是我们的专有应用程序,用于确认 统计意义通过引入一种或多种生物扰动,在我们的平台上产生疾病表型。这一步对于将给定的生物扰动(例如CRISPR基因敲除)映射到其在细胞形态上的高维和可重现的变化是至关重要的。这些表型是下游分析的主要输入,包括预测的基因-基因和基因-分子关系。
HitFinder。HitFinder是我们的软件工具,用于评估高维疾病模型中候选治疗药物(小分子或大分子)的活性 。这一过程在几个重要方面不同于传统的药物发现方法。首先,传统的生化分析方法测量的是化合物相对于单个假想目标 的活性,而HitFinder测量的是化合物拯救由致病生物扰动引起的疾病表型的能力。这种与目标无关的评估可防止我们在此过程中注入人为偏见。 其次,虽然传统的分析是低维或单变量的测量,但HitFinder在高维环境中评估化合物活动,增加了我们观察到的活动不太可能由于 随机机会而发生的可能性。最后,HitFinder能够快速评估大型和多样化的化学库的活动,其规模超过了大多数传统方法。
药物活性报告表。药物活性报告表(DART)是我们的专有软件工具,用于汇总和可视化化合物活性数据。重要的是,在DART中,研究人员可以比较一种化合物:i)挽救那些由用于模拟感兴趣疾病的生物扰动具体诱导的形态变化的能力;ii)由化合物引起的任何新的形态变化,这是潜在的脱靶或有害的靶上效应的早期测量。使用DART, 研究人员可以快速识别和优先选择那些被认为具有最大的有效性和安全性的分子。

图31。DART使我们的生物学家能够快速确定对疾病表型影响最大的化合物,同时将其他影响降至最低。我们的经验性命中识别屏幕的结果显示在DART中,这是我们的用户界面,允许药物发现团队快速探索和了解结果,并将重点放在 认为是最有希望测试的化合物上。
168
计划洞察
我们的Program Insight工具将经过处理的数据转化为可操作的见解。这些见解分为两大类:i)深入了解潜在的生物学和早期治疗起点,或者从哪里开始?ii)深入了解感兴趣的特定化学底物,或者深入了解哪些和如何进行?我们挖掘生物和化学数据的递归数据宇宙来预测 治疗活性和行为,这可能会催生新的NCE程序或已知化学实体程序的新用途。复合智能工具使我们能够根据与我们数据集中其他高维地标的 相似性度量以及包含图像和化学结构的预测模型来推断复合的作用机制和潜在的ADMET负债。
PhenoMap。PhenoMap是一个庞大的生物和化学扰动表型关系数据库,它允许我们根据表型相似性 推断任意两个扰动(或扰动组)之间的关系硅片。到目前为止,我们能够推断出超过130亿个关系,这些关系完全是由ML工具生成的,没有任何 人类偏见,使我们能够理解疾病的基础机制,以及如何操纵这些机制来改善人类健康。例如,我们可以查询CRISPR工程敲除的任何 两个基因在我们的全基因组阵列CRISPR屏幕上产生的相似性(或不相似性),揭示了科学文献中从未描述过的已知和新的药物靶点。我们可以查询我们图书馆中的任何小分子和所有基因敲除之间的相似性, 揭示化合物的作用机制,最重要的是,推断这些分子对高价值药物靶点的活性。我们能够探测我们库中的任何扰动(跨越基因组和大约10万个小分子)之间的关系,从而改变了药物发现的迭代方式反复试验处理为计算驱动的搜索 问题。

图32。PhenoMap允许我们的团队查看多个推断的比较并排以快速识别基因和化合物之间的关系。我们的PhenoMap工具使我们能够在 中快速探索推断的生物和化学关系,以便i)运行目标发现,ii)预测活动命中,iii)优化表观相似性和iv)去卷积作用机制。
169
在未来,我们的目标是包括来自全数字药物发现流水线堆栈的越来越多的见解:关于我们物理库中化合物的物理化学和结构信息,以及关于尚未在我们的平台上测试的可合成化合物的预测、admet化验读数和预测,甚至最终。在 活体中读数和预测。
复合智能。我们的复合智能(CI)工具可产生对特定候选治疗方案的深入和早期洞察,帮助我们在投入宝贵的时间和资源之前提拔那些具有良好特性的人,并淘汰那些失败的可能性较高的人。使用CI的一个应用,我们可以通过将化合物的表型与i)来自我们的全基因组阵列CRISPR实验的表型(询问小分子抑制诱导的表型是否模仿我们文库中的任何基因敲除)或ii)我们再利用文库中注释良好的化合物所诱导的表型来阐明NCE化合物的作用机制(br}通过将化合物的表型与我们的全基因组阵列CRISPR实验中的表型进行比较(查询小分子抑制诱导的表型是否与我们的文库中的任何基因敲除相似)来阐明NCE化合物的作用机制。在CI中使用不同的应用程序,我们可以使用不断增长的ADMET数据集和计算模型来预测候选治疗方案的特定ADME和 毒理学终点。预测ADMET性能低的化合物是先进的。具有高预测ADMET性能的化合物可被丢弃或标记以供后续研究。
程序加速
一旦真知灼见浮出水面,我们的 研究人员就可以使用一套数字化学和翻译工具来优化化合物并加快发现和开发计划。
170
复合阿特拉斯。Component Atlas是我们专有且可商业化的数字化学工具的集合,使我们的科学家能够使用来自Enamine和无锡等供应商的大型枚举化学库,从有希望的治疗起点扩展到更多样化的化学底物。 Component Atlas中的一个模块Scaffold Shopper可以将我们平台识别的候选化合物与超过120亿种化合物进行比较现成合成和现成的基于我们的3D化学功能和基于形状的相似性,我们可以在几分钟内以较低的计算费用获得分子。此外,我们还 构建了软件,使我们的化学家能够围绕可复制和经过验证的HIT分子快速组装密集的微库,以加快SAR的建立,而不需要定制合成。

图33。脚手架购物者使我们的化学家能够快速识别阅读到合成和现成的命中扩展的复合体。比较基于在几分钟内生成的3D 化学功能和基于形状的相似性,并且计算费用较低。
171
分子消防管。分子消防软管过滤化合物Atlas中广泛的搜索结果 ,以便我们的药物化学家能够快速确定感兴趣的分子的优先顺序。化学家可以使用一系列分子属性和基于2D和3D的 相似性评分来动态筛选搜索结果,以便更好地识别从我们的化学品供应商订购的合适化合物集以进行合成。

图34。分子消防软管增加了多种特性的过滤功能,可快速识别要合成的理想化合物 。分子消防软管提供对我们大规模化学扩展结果的动态分析和过滤,使我们的药物化学家能够快速识别下一组化合物,以便在我们的平台上订购和测试 。
InVivology Research Suite
InVivology研究套件是我们专有的软件工具集合,使科学家能够监控和分析正在进行和已完成的行为和生理数据体内研究。可以近乎实时地查看单个动物的研究数据或跨 个研究小组汇总的研究数据,从而更好地确保最终研究数据是可重现和可解释的。持续监测允许研究人员以类似的方式标记动物处理、给药或复合负债可能产生的意外影响,并根据需要修改或终止研究。在研究结束时,将自动生成图表和数据表,以帮助评估研究结果和设计 后续行动体内研究。
172
更重要的是,连续的视频馈送和我们专有的动物笼子使我们能够在几天、几周甚至几个月内不间断地收集动物行为和生理的数据。然后,我们的InVivology Research Suite中的ML工具可以用来创建更抽象的动物行为表示,使我们能够快速地对新的动物模型进行表型 和识别体内可能与评估潜在化合物安全性和有效性属性更相关的疾病特征。

图35。InVivology Research Suite使我们的团队能够跟踪和分析正在进行的动物研究中的大量数据 。研究套件使我们的体内科学家们通过近乎实时的视频馈送和数据生成来监测单个受试者,并审查研究水平数据。
机构知识
知识 存储。Knowledge Store是一个数据仓库系统,包括递归数据宇宙、由我们的研究科学家生成的电子实验室笔记本,以及由我们的数据和ML科学家发布到我们内部知识库的技术分析 。知识库是集中式的,可供授权的Recursionauts访问,有助于保存机构知识、进一步的集体学习,并为新的发现和开发工具生成想法。
从递归地图洞察力到计划推进的桥梁
递归地图中的工具将实验结果转化为可操作的见解,我们的研发团队可以利用这些见解在药物发现和开发过程的每个阶段加速 计划。虽然没有标准的药物发现计划,但我们推理搜索方法下的大多数计划如下所示:
| • | 我们使用递归图识别早期治疗起点或新的生物靶点。 |
| • | 我们在与疾病相关的背景下经验性地验证化合物。 |
173
| • | 我们预测了具有活性的化合物的作用机制。 |
| • | 我们将化合物优化为可行的候选药物。 |
| • | 我们选择并推动候选药物进入临床开发。 |
第一步:确定早期治疗起点和新的生物靶点。使用递归贴图, 我们 可以筛选并随后推断数千种不同的生物扰动之间的关系,包括CRISPR基因敲除、可溶性因子、病毒、细菌毒素和数十万种小分子扰动在硅胶中,基于每个扰动的高维表型的相似性(下图中的红色阴影)或不同(下图中的蓝色阴影)。利用这些推断的关系,我们既可以阐明新的药物靶点,也可以阐明早期的治疗化合物,以启动新的药物发现计划。
为了识别新的程序起点, 递归映射能够准确地预测跨越生物学不同领域的关系是至关重要的。为了确认我们预测的准确性,我们已经演示了我们的方法概括了众所周知的生物学途径。在下面的示例 中,我们使用CRISPR基因编辑工具敲除了典型生物学途径中的基因。此外,我们还分析了这些相同途径的已知激动剂或拮抗剂的小分子。将这些 扰动引起的表型相互比较,我们观察到i)每个扰动产生一个独特的表型,但ii)表型形成的簇概括了人们熟知的生物途径,包括涉及以下方面的基因:
| • | Bcl-2信号转导 |
| • | NF-KB信令 |
| • | RAS信令 |
| • | JAK/STAT信令 |
| • | 转化生长因子β信号转导 |
174
这些发现不仅验证了我们预测的准确性,还表明我们可以使用我们的 推理搜索方法来识别新药靶点或早期治疗起点,从而为新药发现计划提供种子。

图36。基因和小分子之间的推断关系重建了已知的生物学。图中显示了我们的递归映射生成的100多亿个推断关系中的一小部分 。深浅的红色反映了表型相似性的增加程度。深浅的蓝色反映了表型相反程度的增加。 递归图中突出显示的部分揭示了经过充分研究的生物路径上的预期关系。
步骤2:在与疾病相关的背景下经验性地验证 化合物。基于其选择了感兴趣的化合物推断活动,然后我们物理上在与疾病相关的背景中筛选候选化合物以确认我们的预测。
为了确定晋级候选人的优先顺序,我们的平台能够准确测量 化合物的活性是至关重要的。为了确认我们测量的准确性,我们已经证明我们的模型正确地重新发现了已知在人类疾病中活跃的化合物,也被称为阳性对照。到目前为止,我们已经执行了200多项研究, 再次确认了众所周知的阳性对照的活性。这些实验涵盖:
| • | 小分子和抗体之前已经被研究和记录在科学文献中,目前正在进行临床试验,和/或上市治疗。 |
| • | 几十种不同的疾病和相关的生物途径。 |
| • | 我们用三种不同的技术来模拟疾病,包括可溶性因子、CRISPR和BacMam基因功能增益。 |
175
下表汇总了我们在我们的平台上重新发现的来自整个行业 的数百种成熟的临床和开发药物的子集。

CRISPR功能丧失疾病模型基因疾病或途径药物#类*药物化合物*BMPR2肺动脉高压1SRC 萨拉卡替尼LEMD3 Buschke-Ollendorff综合征4Alk5GW788388,EW-7197,LY21557299,SD-208NF1新纤维瘤病15MEK RO5126766,PD 184352,MEK162,pimasertib,GDC0388,EW-7197,LY21557299,SD-208NF1新纤维瘤病15MEK RO5126766,PD 184352,MEK162,pimasertib,GDC0.AKTI-1/2+2XL388,AZD2014,WYE-125132,CC-223,AZD8055+1SOCS3途径生物学13 JAK Solcitinib,tofacitinib,Ruxolitini,Baritinib,TPCA-1+8TSC2结节性硬化症18mTor Everolimus,Temsirolimus,pp242,CC-223,OSI-027+13VHL von Hippel-Lindau综合征1HIF-2+/-PT2385可溶性因子病模型SF病或途径药物#类药物**干扰素+/-多种炎症性疾病2 4 2 5INF+/-(A)PI3K ikk JAK anifroab(A),sivalimumab(A)vs-5584,gdc-0980,Pilaralisib,PF-4989216 Ar托法替尼,Pefitinib,AZD1480+11 IL-12多发性炎症性疾病1 5 IL-1b(A)ikk Canakinumab IKK-1,ACHP,LY2409881,AZD-3264,TPCA-1 IL-4多发性炎症性疾病1 5 IL-4(A)JAK AMG317(A)Ruxolitinib,Tofacitinib,TG 101209,TG 101348,NVP-BSK805Cerdaratinib,tofacitinib,Solcitinib,CYT387+12TGF2-2纤维化疾病和癌症1 6TGFb(A)alk5 fsolimumab(A)SD208,SB 525334,GW 788388,Repsox,SB 431542+1TNF+/-多种自身免疫性疾病3 5TNFa(A)ikk Adalimumab(A)Infliximab (A),Golimumab(A), BMS 345541血管生成因子/肿瘤23 VEGFR(1a)Bevacizumab(A)、索拉非尼、苏尼替尼、波纳替尼、Axitinib+18Bacmam功能获得性疾病模型基因疾病或途径药物#药物化合物BRAF 1 1 1 ERK抑制剂BRAF(A)MEK抑制剂Ulixtertinib Drapfenib MEK162(S)BRAF 1 1 ERK抑制剂BRAF(A)MEK抑制剂Ulixtertinib Drapfenib MEK162(S)BRAF 1 1 ERK抑制剂BRAF(A)MEK抑制剂Ulixtertinib Drapfenib MEK162
176
表4. 递归映射 准确恢复已知阳性 控件的活动。这张表格总结了大约200种在临床试验中显示出活性的化合物,我们的平台已经使用我们的蛮力方法准确地恢复了这些化合物。
第三步:预测行动机制。在实证验证了我们的预测后,我们的药物化学家致力于进一步 了解化合物的作用机制,这是表型药物发现的传统阿喀琉斯之踵。我们的KCE库包含数千种具有良好注释的作用机制的化合物。这些 化合物的表型,以及我们使用CRISPR基因编辑工具剔除的数千个基因,都包含在我们的递归图谱中。利用这些信息,我们的化学家可以将我们验证的化合物的表型与这些 个高维地理标志进行比较,并评估其相似程度。
为了准确地预测化合物的机理,递归映射(Recursion Map)能够基于表型关系准确地捕捉小分子的机理相似性是至关重要的。我们已经证明,虽然所有的化合物都会在细胞中产生独特的形态变化,但具有相似作用机制的化合物彼此之间的表型相似性程度更高。在下面的例子中,我们使用我们的表型组学平台测试了大量具有已知作用机制的化合物。当我们根据表型相似性绘制得到的 表型图时,我们观察到i)它们是高度多样化的,但ii)基于机械相似性形成了数百个簇。
177
这些结果表明,给定一个具有未知机制的感兴趣的化合物,我们可能能够 将其与我们的注释良好的化合物的KCE库进行比较,并对其机制进行去卷积。

图37。具有相同机制的化合物聚集在一起,表现为典型的。UMAP图,其中每个点代表 个不同的化合物。表型相似的化合物更紧密地位于一起,并概括了机理上的相似之处(如标签所示)。
第四步:将经过验证的化合物优化为可行的候选药物。虽然一种化合物在我们的筛查中可能是有效的, 大多数早期治疗起点的效力都很低,而且药物性能也不理想,必须先进行优化,然后才能进入体内以及最终的人体研究。在铅优化过程中,我们的化学家依靠我们的 表观组学平台重复测量化合物结构变化导致的化合物效力变化。
因为这个过程可能会持续几个月,所以我们的平台分析在一段时间内高度稳定是至关重要的。为了测试这一点,我们确保我们的测试可以在间隔数周甚至数月的实验中重现化合物活性的特定测量,例如化合物的EC50(产生半最大反应的药物浓度 )或最大效应(最大反应)。
178
在下面的示例中,我们对HIF2运行了四个单独的实验a已知的抑制剂对我们的VHL三个月的疾病模型。所有四个运行的剂量-反应曲线显示高度重叠,包括高度相似的EC50和最大效应。我们从这项研究中计算出的最小显著性比,这是一种常见的行业指标,体外培养随着时间的推移,化验的重复性为1.076,行业基准高度稳健5。这些结果证明了我们分析的稳定性,以及在我们进行程序的过程中将我们的表观平台作为SAR的基础的能力。

图38。化合物活性在实验运行中是可重现的。针对我们的疾病模型, 同一工具化合物多次运行的剂量反应曲线VHL 功能丧失表现出很高的一致性,计算出的工具化合物最小 显著性比为1.076。
步骤5:选择并推进候选药物进入临床试验。在将早期治疗起点优化为可行的候选药物后,我们选择那些化学性质最好的化合物作为开发和最终临床候选药物。我们已经建立了内部能力,通过启用IND的研究、监管审批流程以及人类临床研究来推动临床 候选人。总体而言,我们的开发团队成员参与了100多项临床研究,包括 最近在2019年完成了我们的第一个SAD研究,并在2020年完成了MAD研究。此外,我们在监管、CMC和临床运营方面与外部顾问团队密切合作,以确保执行成功。
我们的人民和文化
我们在多个尖端科学技术领域的交汇点 开展业务,创造了一个将经验数据、严谨的统计数据和创造性思维应用于决策的环境。我们多元化的Recursionauts团队现在由200多名全职员工组成,我们的增长心态、使命驱动的承诺和包容的文化将我们团结在一起。我们的跨学科员工队伍分布在生物学、药物搜索和化学领域(约占员工总数的40%),此外还有软件工程、自动化工程和数据科学方面的专家。
| 5 | 首页--期刊主要分类--期刊细介绍--期刊题录与文摘--期刊详细文摘内容最小显著性比是评估分析变异性的一种统计方法。2013 11月1日[更新2017年11月20日]。见:Markossian S,Sittampalam GS,Grossman A,等编辑。化验指南手册[网际网路]。贝塞斯达(医学):礼来公司和国家先进翻译科学中心;2004年。 |
179
(约占我们员工的35%)。我们的项目团队可以随时随地跨职能工作。我们的Value?One Recursion强化了这一重要的、公司优先的、 功能第二的心态,这对于最大限度地提高基础架构层的效率和Recursion OS的整体效率至关重要。
鉴于Recursion OS的发展速度,再加上公司的发展轨迹,学习和教学环境对我们的成功至关重要。我们的人员系统、流程和仪式都是专门为强化这些行为而设计的。例如,我们的绩效和发展系统围绕三个问题来评估绩效,这些问题 与我们的价值观相关:i)交付了什么,ii)学到了什么,iii)对他人有什么影响?另一个文化维度是整个基础架构层和递归操作系统的关键推动因素,那就是我们愿意大胆和 雄心勃勃,这体现在我们的价值观中:用诚信大胆行动。长期以来,在这一价值观的基础上,我们采取了一种大胆押注的方式,追求我们的使命,加快进步;我们倾向于变革,这将定期推动我们。
我们的文化
文化是我们的性格和个性; 它是我们的价值观、传统、信仰、行为和态度的总和。我们有意寻找非凡的人才,并创造了一个环境,让我们的推荐人能够尽其所能。我们深思熟虑的方法对我们 未来的成功至关重要,因为我们的使命是大胆的,并将总部设在盐湖城打造一家具有行业定义的公司。我们的文化是由一群令人难以置信的多样化、忠诚、雄心勃勃、目标驱动和才华横溢的人所定义的,他们 带着好奇心、谦逊、善良和尊重来到谈判桌前。人员、制度和公司礼仪强化了让我们的文化活起来的行为。归根结底,我们最大的优势在于我们的差异:专业知识、性别、种族、 学科、经验和视角。
我们的价值观。价值观是定义我们文化的核心行为。我们的 价值观对我们来说极其重要,因为它们是我们如何实现使命的最简单定义。

图39。我们的五大价值支柱。我们的价值观是定义我们文化的核心行为。
180
我们关心.我们关心我们的候选药物、我们的复习者、他们的家人、彼此、我们生活和工作的社区,我们深深地关心我们要服务的患者和他们的亲人。我们也关心我们的工作;我们以业主的心态运作。我们如此关心 ,为了让彼此和公司变得更好,我们愿意做和说困难的事情。我们关怀的一个例子是,我们为所有Recursionauts及其家人支付100%的健康保险费,并提供大量的精神健康福利, 相信每个人都应该有公平的医疗保健机会,这样他们才能健康,进而为我们的使命服务。
我们 了解。从不同的专业知识和观点中学习,并从失败中学习,是我们如何取得进步的重要组成部分。我们寻求创建跨职能团队,以便我们能够教授和 了解我们解决问题的各种方法。我们希望每个人都能以公司的增长速度学习。我们从来不是一成不变的,也不应该是一成不变的。我们为期刊俱乐部提供的时间和 甚至是101系列讲座就体现了这一价值,我们一些最聪明、最有成就的Recursionauts定期向新员工(或任何想要提升技能的员工)讲授各自领域的入门课程。
我们送货。我们对交货的期望值过高,对此我们毫无歉意。我们有潜力从根本上改善数百万人的生活,我们不希望他们中的任何人等待的时间超过必要的一天。我们的生存迫在眉睫。对中国人民的深切关怀是他们实现这些期望的动力。这一 价值在本文档以及我们自2013年11月成立以来所构建的所有内容中都得到了体现。
我们以诚信勇敢行事 。没有一家公司没有胆量就能改变世界或重塑一个行业。大胆的一部分是创造一种文化,在这种文化中,如果失败能带来学习和成长,我们就会接受它。我们非常大胆,而不是 庆祝如果我们放松抱负,我们可能会取得的更温和的成功。然而,大胆必须是平衡的;不是通过胆怯,而是通过诚实行事,即使在没有人注意的情况下也要做正确的事情。我们以 数据为先导,长期优化关系,在我们所做的每一件事中都以最高级别的完整性为目标。这一价值的最佳例子是我们任务的广度,我们针对它所取得的进展,以及我们拥有的数据来支持这一进展和我们的主张。我们高度诚信的另一个强有力的例子来自于我们去年更新了新的招聘股本指导方针。我们没有在 前进的基础上采取行动,而是回顾和完整了每一位新员工拨款低于新指导方针的Recursionaut。
我们是一个递归。我们本着公司第一、功能第二的经营理念。我们做对任务最有利的 ,无论是对我们自己还是对我们的职能团队来说都是最好的结果。我们的成功来自于作为一个跨学科团队的合作。领导和员工始终愿意 放弃权力、控制权或责任,转而支持另一个人,这意味着任务可以向前推进,这就是这种价值的例证。
181
我们文化的其他主要驱动力。以犹他州为基地对我们的文化产生了积极的影响,将忠诚、坚韧、善良和尊重与对我们雄心壮志的不懈追求结合在一起,所有这些都不在传统的回音室之外。这一强大的组合为我们的价值观提供了持久的承诺,并加速了我们的 使命。在我们最新的员工敬业度调查中,我们实现了83%的敬业度,比我们使用的技术、科学和研究基准高出10多分。敬业度类似于激励,是行业标准指数得分, 研究表明,敬业度是业绩和业务结果的驱动因素。作为一家公司,我们的目标是75%-85%的高但平衡的敬业度分数,这样我们就可以对组织的健康状况充满信心,同时 承认在我们以坚持不懈的步伐移动和变化的过程中存在一定程度的摩擦。参与度超过85%的过度索引可能会以为业务中的其他利益相关者(如我们的合作伙伴、股东或我们 目标服务的患者)提供服务为代价。

图40。我们的员工敬业度调查得分超过行业基准。6
为了利用我们多样性的力量,我们强调建设公平包容的文化和环境。从入职到 培训,再到全体员工会议,我们投资于技能建设,并利用讲故事来培养包容的工作场所,这可以成为我们许多不同之处的共享家园。我们强调要让自己保持清醒, 受过教育,并能与周围的人产生共鸣。在我们进行的2020年的一项调查中,91%的Recursionauts同意我们培育了一个高度诚信的环境,83%的人认为他们可以表达相反的观点,但仍然受到尊重,远远高于 许多类似情况的公司的基准。招聘、晋升和薪酬公平对我们很重要,我们在流程、培训和分析方面进行投资,以最大限度地提高公平结果,从而使差异基于每位员工为企业带来的价值 。
最后,我们文化中最独特的凝聚力是我们的使命。我们通过首席执行官为每位新 员工举办的Vision Talks(所有当前的Recursionauts都会被邀请参加)、我们对我们设施了解的患者的照片、知名科学家、患者、患者权益倡导者和其他利益相关方的邀请讲座等方式将其带入生活。我们是专业人士的混合体,他们在自己的职业生涯中选择了一条有意义的职业道路,有的更早,有的更晚。2020年只会增强我们对目标的集体渴望,它突显了医疗保健在我们的生活和经济中的重要性,以及对新方法必要性的深刻认识。这为我们和我们未来的回归者提供了动力。
我们的人民
截至2021年1月14日,我们雇佣了209名员工,并且正在快速增长。我们的团队受过高等教育,经验丰富,超过25%的团队拥有 个高级技术学位(例如医学博士或博士学位)。以及作为核心团队成员为53种上市药物和77种药物做出贡献的集体经验
| 6 | 我们的基准来自截至2019年12月31日的12个月内来自可比公司的20,000多份调查回复 。 |
182
临床分期分子。我们的团队也高度交叉职能,数据科学家和工程师(约占我们员工的35%)与生物学家和化学家(约占我们员工的40%)一样多。我们的大部分员工都在盐湖城市中心的总部工作。我们还有一个体内我们位于加利福尼亚州米尔皮塔斯的vivarium的科学团队以及一些远程员工,特别是 数据科学、ML和计算化学领域的员工。该团队在各个领域都有不同的经验。同类中最好的生命科学、技术、 和商业领域的全球公司和机构。
截至2021年1月14日,超过30%的员工被我们的使命、科学、技术、 和文化所吸引,搬到犹他州加入我们。盐湖城本身已经吸引了许多新的回归者,因为它的负担能力、娱乐设施、生活质量和日益成熟的多样性。我们采用了创造性的方法来发现和招募一些最聪明的人才 ,包括基于发布我们的第一个公共数据集RxRx1的ML竞赛,该竞赛是我们与首屈一指的人工智能会议NeurIPS联合主办的。特别是,我们成功地吸引了旧金山湾区的人才,那里拥有 丰富的科技和生物技术人才库。
我们坚定地致力于建立一个多元化的组织。大量研究得出结论,多样化团队的表现优于同质团队。今天,我们的劳动力大约有40%是女性,我们继续努力在各个层面上改善性别和种族多样性。我们的价值观和流程旨在实现我们的多样性、公平性和 包容的抱负,为实现我们的使命服务。例如,我们专注于将非二进制和BIPOC(黑人、土著或有色人种)个人和女性纳入所有新员工的面试人员小组和候选人名单 。作为犹他州妇女技术委员会(Women Tech Council Of Utah)三次获得TSatter奖的获奖者,我们的进展在当地得到了注意。

图41。递归公司按级别划分的女性代表人数远远超过平均公司渠道,在公司渠道中,较高级别的女性代表人数较少。7
最后,尽管取得了惊人的增长,我们 不仅有意从外部来源发展我们的人才,而且还通过提升和调动我们的内部团队来培养我们的人才。递归操作系统的固有复杂性和发展导致了机构知识的价值被重视,这些知识随着递归时间的推移而来 。作为一名Recursionaut的价值主张的一部分是,你的职业生涯将会发展。值得注意的是,我们20%的高管团队是内部流动的产物,他们是以个人身份加入的
| 7 | 改编自2020年麦肯锡女性职场精益报告。 |
183
贡献者,并成长为公司的执行人员。2020年,我们有38名员工进入了新的角色,承担了更多的责任。
管道
我们已经使用Recursion OS生成了包含35个内部开发程序的 管道。我们的计划针对的是横跨多个治疗领域的疾病:i)病因明确,ii)存在高度未得到满足的需求,没有批准的治疗方法,或者现有治疗模式存在重大缺陷。我们的几个计划针对的是年销售额超过10亿美元的市场机会超过10亿美元的适应症,我们正在准备四个流水线计划,以便进入第二阶段临床 试验。
我们的大多数后期项目都是使用暴力搜索方法创建的,我们使用自动化湿实验室基础设施对库中的每种疾病模型和候选药物组合进行物理测试。2020年年中,我们开始向更高效、更强大的推论搜索方法过渡。在这一新范式下,我们独立地描述数千种疾病模型和数十万候选药物,然后推断出数百亿种生物和化学关系。硅片,为后续验证确定最有希望的候选对象的优先顺序.我们的大多数新兴早期发现阶段计划 都是使用推理搜索工具创建的,展望未来,我们预计此方法将为我们的渠道带来绝大多数新成员。

图42。Recursion OS的强大体现在活跃的研发计划 的广度上。35个项目,涵盖多个治疗领域,包括现有化合物和正在积极研发的NCEs的新用途。(1)我们的 计划有可能解决神经炎症中的一些适应症,包括在美国总计至少600万名患者的多种神经退行性疾病。我们打算在未来选择这些适应症的一个子集。(2)美国每年的发病率为730,000例--欧盟5国。最初的临床研究将集中在总人群中反复感染率较高的部分。 (3)每年美国-EU5发病率(4)全球流行(5)所有人每年的US-EU5发病率 NF2致病脑膜瘤(6)遗传性和散发性症状人群。
184
值得注意的计划
我们认为十个值得注意的计划是关键的短期价值驱动因素。
我们的八个值得注意的程序是使用我们的暴力搜索方法发现的:
| • | REC-4881用于治疗家族性腺瘤性息肉病,或FAP,预计将于#年启动 第二阶段 |
| • | REC-3599用于治疗GM2神经节苷脂沉积症,或GM2预期的第二阶段 开始于 |
| • | REC-2282用于治疗2型神经纤维瘤病或NF2预期阶段 2启动 |
| • | REC-994用于治疗脑海绵状畸形或CCM,预计将于#年启动 第二阶段 |
| • | 治疗糖尿病的铅分子艰难梭菌结肠炎潜伏期 |
| • | 治疗神经炎的先导分子新发现 |
| • | 治疗巴顿病的先导分子新发现 |
| • | 治疗Charcot-Marie Tooth 2a型疾病(或CMT2A)的铅分子晚发现 |
紧随其后的是使用我们的推理搜索方法发现并迅速发展的两个值得注意的程序:
| • | REC-64151治疗STK11突变型非小细胞肺癌免疫关卡耐药的临床前研究 |
| • | MYC抑制分子治疗实体和血液系统恶性肿瘤的新发现 |

图43。值得注意的项目在我们的流水线中。鉴于其市场机遇和所提供的验证,值得注意的计划是 我们的关键短期价值驱动因素。我们的四个主导计划准备在2021年招募患者参加第二阶段临床试验,同时临床前计划正在快速进展。(1)EU5被定义为法国、德国、意大利、西班牙和英国。全
185
除非另有说明,否则数字为流行数字。(2)全球流行。(3)所有NF2驱动的脑膜瘤的年US-EU5 发病率。(4)遗传性和散发性症状人群。(5)美国每年的发病率为730,000例--欧盟5国。最初的临床研究将集中在总人群中反复感染率较高的人群。(6)我们的计划有可能解决神经炎症中的一些适应症, 包括美国总计至少600万名患者的多种神经退行性疾病。我们打算在未来选择这些适应症的一个子集。(7)每年的US-EU5发病率。(8)我们的计划有可能解决一些由以下因素驱动的适应症MyC做些改动。目前,我们尚未最终确定特定适应症的目标产品配置文件。
REC-4881:家族性腺瘤性息肉病

摘要
REC-4881是一种口服生物利用度, 非ATP-竞争性MEK1和MEK2的变构小分子抑制剂正在开发以缩小FAP患者和躯体疾病患者的肿瘤体积装甲运兵车-突变的 肿瘤。REC-4881已经被很好地耐受,与预期用途一致,并且在人类中具有肠道定位的PK-Profile,这对FAP非常有利,并且装甲运兵车胃肠道肿瘤。我们希望让第一位患者参加第二阶段的双盲、随机、安慰剂对照试验。
疾病概述
FAP是一种罕见的肿瘤综合征,在美国和欧洲5国约有50,000名患者未获批准治疗。FAP是由肿瘤抑制基因的常染色体显性失活突变引起的装甲运兵车,编码Wnt 信号通路的负调控因子。FAP患者一生中会发展为结肠、直肠、直肠袋、胃和十二指肠的息肉和腺瘤。这些生长有很高的恶变风险,并可能导致结肠、胃、十二指肠和直肠组织的浸润性癌症。对FAP患者的标准护理是在青少年后期进行结肠切除术。如果没有手术干预,受影响的患者将在成年早期发展为结直肠癌。结肠切除术后,患者每6-12个月接受一次内窥镜检查,以监测病情进展。
尽管进行了外科治疗,但由于术后十二指肠和硬纤维瘤的风险持续存在,对FAP有效的药物治疗的需求仍然很高。这些肿瘤发生在大多数患者中,手术切除这些肿瘤可能会导致很高的发病率。非甾体抗炎药,如舒林酸或塞来昔布,有时被用来治疗这些肿瘤,但疗效有限,对癌前病变没有影响。虽然手术治疗和监测改善了FAP患者的预后,但硬纤维瘤仍然是FAP患者结肠切除术后死亡的主要原因。
产品概念
我们的REC-4881候选药物是口服生物利用度,非ATP-竞争性与非甾体抗炎药塞来昔布相比,MEK1和MEK2的变构小分子抑制剂(IC50分别为2-3 nM和3-5 nM)在息肉和发育不良腺瘤中显示出有效的减少作用。近似值FAP小鼠模型。在千禧制药公司之前进行的第一阶段研究中,51名实体肿瘤患者接受了REC-4881的治疗,没有表现出与这一类别相关的典型眼部毒性。REC-4881表现出极低的肝脏代谢,其主要途径为
186
消除是通过胆汁排泄,这可能使其优先暴露在十二指肠和下消化道的肿瘤部位,减少全身暴露和 毒性。我们于2020年5月从武田制药获得了REC-4881的全球许可。我们计划在FAP中寻求REC-4881的孤儿药物名称,并装甲运兵车由肿瘤驱动。
临床前
REC-4881用于FAP的新用途是通过我们的暴力搜索方法发现的,该方法利用了FAP疾病基因的敲除装甲运兵车在人类细胞中。我们用肿瘤细胞系和球体验证了我们的发现,这些细胞系和球体是从人类上皮性肿瘤细胞中培养出来的。装甲运兵车。在这些模型中,REC-4881抑制了球体的生长和组织,在肿瘤细胞系中,REC-4881在含有装甲运兵车突变。

图44。平台式救援装甲运兵车型号为REC-4881。REC-4881挽救了击倒的影响装甲运兵车在人类细胞中使用我们的表型组学分析。
随后,我们在FAP的疾病相关临床前模型中评估了REC-4881。窝藏截断的小鼠 APC,或APC最小,每天口服多剂量的阿司匹林REC-4881或塞来昔布治疗8周。用塞来昔布治疗的小鼠比用赋形剂治疗的小鼠息肉少约30%,而用1毫克/千克或3毫克/千克REC-4881治疗的小鼠比用赋形剂治疗的小鼠息肉少约50%。服用10毫克/千克REC-4881(测试的最高剂量)的小鼠,显示出大约70%的息肉总数减少。

图45。REC-4881减少胃肠道息肉数量APC最小 小白鼠 FAP模型。口服指示剂量的REC-4881、塞来昔布或赋形剂对照组8周后进行胃肠道息肉计数。
187
开始给药时的息肉计数反映了研究开始时(15周大)处死的动物。P 0.001:所有REC4881治疗组与车辆对照组相比 。
在FAP中,由基因突变引起的息肉装甲运兵车可能通过积累额外的 突变而进展为高级别腺瘤,最终发展为恶性肿瘤。为了评价REC-4881对良性息肉和晚期腺瘤的活性,对REC-4881处理的小鼠胃肠组织进行了组织学评价,并将息肉分为良性和高度腺瘤。虽然塞来昔布减少了模型中良性息肉的生长,但保留下来的息肉中有很大一部分是发育不良的。相比之下,使用REC-4881治疗不仅可以明显减少良性息肉,而且也癌前高级别腺瘤,这一发现具有潜在的翻译意义。

图46。FAP的疾病进展始于FAP基因的突变装甲运兵车。良性疾病的进展 装甲运兵车-突变息肉到高级别腺瘤,最终发生恶性肿瘤,是随着额外基因改变的积累而发生的8.

图47。REC-4881可降低 中的高级别腺瘤APC最小 FAP的小鼠模型。高级别腺瘤与息肉总数的定量:基于A组的盲法组织学回顾
| 8 | 改编自http://syscol-project.eu/about-syscol/ |
188
病理学家。虽然塞来昔布可以减少良性息肉,但剩下的大部分病变都是高度恶性的腺瘤。相比之下,REC-4881可同时减少息肉和高级别腺瘤。
REC-4881是一款 非ATP-竞争性以及MEK1和MEK2的特异性变构小分子抑制剂。研究表明,在腺瘤上皮细胞和肿瘤间质细胞(包括成纤维细胞和血管内皮细胞)中,丝裂原活化蛋白激酶信号(MEK)和细胞外信号调节激酶(ERK)信号被激活。此外,导致丝裂原激活的蛋白激酶信号或MAPK改变的基因组事件,如激活克拉斯,是FAP中常见的促进腺瘤生长的躯体事件。因此,用REC-4881抑制FAP腺瘤中异常的MAPK信号有可能通过作用于驱动肿瘤生长的核心通路来减慢或减缓肿瘤的生长。
临床
我们计划在年内启动FAP的2期临床试验。
千禧制药以前 使用REC-4881(当时称为TAK-733)进行包括人体暴露在内的临床研究。第一阶段研究共纳入51名患者,该研究 显示REC-4881的毒性可控,达到最大耐受剂量(MTD),即在28天治疗周期的第1至21天服用16毫克。最常见的不良反应是皮炎、痤疮样皮疹(53%)、乏力(36%)和腹泻(31%),与其他MEK抑制剂一致。在前8个剂量组(0.2-8.4毫克)中接受REC-4881治疗的患者没有观察到剂量限制性毒性或DLT。4名患者分别接受了12 mg(n=1)、16 mg(n=1)和22 mg(n=2)剂量的3级痤疮皮炎DLT治疗。重要的是,REC-4881显示出比这类批准药物更好的眼部安全性。我们在FAP中的临床前数据支持第二阶段的低剂量队列,剂量范围在前一阶段(0.2-8.4毫克)中未经历DLT的 。
我们计划启动一项2期、随机、双盲、安慰剂对照研究,以 评估REC-4881在典型FAP患者和患有体细胞APC突变的上、下消化道息肉病的非FAP患者中的有效性和安全性 。我们预计将在晚些时候启动第二阶段临床试验。
| • | 这项研究将在经典的FAP或具有体细胞APC突变的非FAP肿瘤患者中进行,这些患者在登记时年龄在18岁或以上。 |
| • | 患者将被随机分为两个有效组和一个安慰剂组,治疗24周,延长时间为24 周。 |
| • | 这项研究将评估接受REC-4881 与安慰剂治疗的患者的肿瘤反应终点。 |

189
图48。REC-4881的临床试验示意图。计划进行第二阶段临床试验,以评估REC-4881在患有经典型FAP和非FAP的上、下消化道息肉患者中的有效性和安全性。
主要竞争对手
在FAP的临床开发中有四种治疗方法,都集中在减少大肠息肉。
| • | Guselkumab是一种IL-23人类单克隆抗体(MAb),由扬森制药公司(Janssen PharmPharmticals)开发,处于第二阶段,假设可以减少细胞因子的产生、炎症和肿瘤息肉的发展。 |
| • | 不含二十碳五烯酸的脂肪酸是一种多不饱和脂肪酸,目前正由S.L.A.制药股份公司进行FAP的第三阶段开发。 Pharma AG Pharma AG。二十碳五烯酸自由脂肪酸被认为可以减少息肉的形成,因为它是花生四烯酸氧化的竞争性抑制剂。 |
| • | Eflornithine和Sulindac的组合正在由FAP癌症预防制药公司开发,在最近的3期研究中,使用该组合的疾病进展发生率并不比单独使用任何一种药物显著降低。 |
| • | 微囊化雷帕霉素,或称eRAPA,目前正处于FAP的2期开发阶段,并被假设通过抑制mTOR途径来减少肿瘤形成 。 |
与FAP中其他活跃的临床研究不同,我们的REC-4881计划将包括良性息肉和发育不良腺瘤的患者,临床前数据表明这两种类型的肿瘤都有预防生长的益处。
REC-3599:GM2神经节苷脂沉积症

摘要
REC-3599是一种口服生物利用度高、选择性强的蛋白激酶C(PKC)小分子抑制剂,目前正在开发用于治疗GM2的GSK3?Rec-3599已经显示出强大的挽救致病生物标记物GM2和脂褐素水平的能力,这些细胞来自于具有多种不同突变的患者 六角形或HEXB,分别称为泰-萨克斯病或桑德霍夫病。我们目前正在一种动物模型中产生额外的药效学数据。GM2应 FDA的要求,预计将在中国招募第一名患者参加开放标签第二阶段试验。
疾病概述
GM2是一种溶酶体储存性疾病,全世界有250多名患者受到影响。这种疾病是由两种基因中的任何一种突变引起的。六角形或HEXB编码溶酶体β-氨基己糖苷酶亚基的基因。GM2出现在婴儿期、儿童期或晚年,取决于遗传缺陷的程度,并按发病时期进行分类:婴儿期起病、青少年起病和晚发性泰-萨克斯病或桑德霍夫病。婴儿GM2患者在出生第一年就被诊断出来,并表现出迅速发展的神经功能下降,与神经元溶酶体功能障碍和GM2积聚相关,导致完全神经功能障碍和在生命的最初几年内过早死亡。 GM2患者在出生后的第一年就被诊断为神经功能减退,并伴有神经元溶酶体功能障碍和GM2积聚。最早观察到的一些迹象包括视网膜异常和出生后头六个月内夸大的惊吓反射。受影响的婴儿可能会达到一些
190
接近正常发育年龄的运动里程碑长达12个月左右;然而,他们最终会在18-24个月大时失去所有获得的运动技能,包括翻身、坐着、爬行和吞咽等基本技能,并且通常在4岁之前死于疾病。(br}在18-24个月大的时候,他们最终会失去所有获得的运动技能,包括翻身、坐着、爬行和吞咽的能力,通常会在4岁之前死于疾病。)没有批准的疾病修饰疗法 该疾病。对这些患者的标准护理是支持性干预,包括使用抗惊厥药物控制癫痫发作,通过鼻胃管辅助喂养,或经皮内窥镜胃造口术,最终是通气支持。 虽然疾病进展仍然很快,但支持性护理可以改善婴儿GM2患者的存活率。
产品概念
我们正在开发一种一流的小分子疗法作为单一疗法或联合基因疗法减缓GM2患者神经功能衰退的进展。REC-3599是一种口服生物利用型、中枢神经系统穿透的PKC?小分子抑制剂,对GSK3?具有额外的抑制活性。在临床前研究中,REC-3599显示在IC50s时,病人来源的成纤维细胞模型中神经节苷脂GM2的积聚和鞘磷脂相关的自体荧光明显减少,适合于人类服用含有GM2的婴儿。六角形和HEXB突变。REC-3599被认为在调节溶酶体的生物发生中具有双重作用,即通过抑制GSK3?,同时还通过抑制PKC?刺激细胞自噬。(2)REC-3599在调节溶酶体的生物发生中起着双重作用,即通过抑制GSK3?,同时通过抑制PKC??刺激细胞自噬。礼来公司之前研究了REC-3599(当时被称为Ruboxistaurin)治疗糖尿病视网膜病变,包括3期临床试验。该化合物已在2500多名成人受试者中使用,疗程长达两年。REC-3599在成人受试者中有很好的耐受性, 支持它在这种罕见和破坏性的婴儿神经系统疾病中的评估。我们目前正在执行相关的体内应FDA的要求进行药效学研究和幼年啮齿动物毒理学研究,以帮助进入儿科人群。2015年,礼来公司将ruboxistaurin的授权授权给Chromaderm;随后,我们在2019年12月向Chromaderm授予了ruboxistaurin的全球授权,用于所有系统用途,我们正在开发REC-3599。我们在2020年获得了GM2中REC-3599的儿科罕见病称号。我们计划在GM2中为REC-3599寻求孤儿药物编号 。
临床前
REC-3599用于GM2的新用途是通过我们的暴力搜索方法发现的,该方法利用了GM2疾病基因的敲除HEXB在人类细胞中。

图49。抢救HEXB型号为 REC-3599。REC-3599挽救了基因敲除的影响HEXB在人类细胞中使用我们的表型组学分析。
191
在Tay-Sachs和Sandhoff病中,β-己糖苷酶功能丧失导致GM2神经节苷脂和脂褐素在溶酶体中积聚。GM2患者成纤维细胞系暴露于REC-3599后,GM2神经节苷脂聚集体、总GM2水平和脂褐素相关的自体荧光降低到与明显健康的对照成纤维细胞系相当的水平。这些数据与REC-3599暴露后溶酶体功能的改善是一致的。
REC-3599最初被开发为PKC?的抑制剂;然而,该化合物对GSK3?也表现出较弱但显著的抑制活性。GSK3?是已知的溶酶体生物发生抑制剂,抑制GSK3?可通过激活受转录因子TFEB调控的溶酶体基因的转录而增加溶酶体的产量和功能。此外,抑制GSK3?可通过TFEB导致促进生存的自噬信号。 同时,结果支持PKC?作为细胞自噬的抑制剂的作用,细胞自噬是溶酶体介导的降解过程中的一个关键细胞过程,溶酶体储存疾病中溶酶体介导的降解受到损害。因此,REC-3599通过抑制GSK3?调节溶酶体的生物发生和通过抑制PKC?刺激细胞自噬的双重作用,可能是REC-3599在人类GM2细胞模型中独特活性的基础。

图50。当增加REC-3599处理时,患者细胞表现出疾病特异性活性降低。泰-萨克斯(Tay-Sachs)和桑德霍夫病(Sandhoff Disease)患者成纤维细胞表现出较高的GM2平均荧光(左图)、聚集数(中图)和自身荧光底物积聚(右图)。
临床
我们正计划在中国启动婴儿GM2的第二期临床试验。
礼来公司之前进行的临床研究包括大量人体接触REC-3599,以前被称为Ruboxistaurin。在美国、欧洲和亚洲进行的26项成人受试者研究已经确定了REC-3599的吸收、分布、代谢、排泄、药效学和耐受性。共有3521名患者被纳入初级安全性数据库(安慰剂:1408,REC-3599:2113),每日剂量分别为4、8、16、32和64毫克。其中,937名患者(安慰剂:401,REC-3599:536)是糖尿病视网膜病变安全数据库的一部分。REC-3599的安全性也在至少250名成人受试者中进行了评估,该数据库包括至少20项临床药理学研究和86名成年受试者的全面QT间期研究。在这些临床药理学研究中,健康受试者在两周内单剂量服用最高256毫克的REC-3599和每天多次服用最高128毫克的REC-3599,长期服用32毫克的REC-3599的患者耐受性良好。
礼来公司的NDA 22005中提供的安全信息支持REC3599在成人患者中的安全概况 。安全性结论总结如下:大多数不良反应都是轻微到中度的,并没有导致研究药物的中断;
192
REC-3599无论年龄、性别、种族和糖尿病类型都是相似的;与安慰剂相比,接受32毫克REC-3599治疗的患者至少有1起严重不良事件(SAE)的发生率更低;SAE的模式没有显示任何器官特异性或系统性毒性。对实验室测量、生命体征和眼科安全评估的分析显示,临床上没有明显的安全性问题。
在圆满完成体内药效学研究后 HEXB通过建立小鼠模型,我们期望启动一项开放标签的第二阶段研究,评估REC-3599每日给药对婴儿GM2患者的有效性、安全性和耐受性。我们预计将在以下时间启动 第二阶段临床试验。
| • | 这项研究将在确诊为婴儿GM2的婴儿患者中进行,患者将至少达到一个特定的发育里程碑。 |
| • | 这项研究将包括四个阶段:筛查、剂量递增、治疗和 随访。整个研究期预计为15个月。 |
| • | 我们将使用已建立并经过 验证的综合量表来跟踪发展里程碑、神经功能和生活质量的完成情况。 |

图51。REC-3599第二阶段临床试验示意图。计划进行第二阶段临床试验,以评估REC-3599在婴儿GM2患者中的有效性和安全性。
主要竞争对手
REC-3599计划的主要竞争对手包括两个治疗类别:基因疗法和小分子底物减少疗法。有两家公司正在开发基于AAV的基因疗法,通过基因传递恢复功能性的β-己糖苷酶:
| • | 泰莎基因疗法公司正在开发一种基于AAV的基因疗法TSHA-101。该计划目前处于第二阶段。 |
| • | SIO基因疗法也在开发一种基于AAV的基因疗法,AXO-AAV-GM1/GM2。该计划目前处于阶段1/2。 |
两家公司正在开发小分子底物减少疗法:
| • | 赛诺菲正在开发Venglustat作为一种口服生物利用型小分子,假设可以减少GM2和其他溶酶体储存疾病中的底物积累。该计划目前正处于针对晚发性GM2患者的第三阶段研究。 |
| • | IntraBio正在开发 N-乙酰-L-亮氨酸作为口服生物可利用的氨基酸酯。该计划目前处于第二阶段。 |
虽然通过基因疗法恢复基因功能为患有GM2等遗传性疾病的患者提供了巨大的潜在治疗益处,但其他破坏性的神经疾病也会导致这种情况。
193
脊髓肌萎缩等疾病表明,即使采用了有效的基因疗法,未得到满足的需求预计仍将居高不下。因此,我们预计,多种疾病调整疗法(包括基因疗法)联合使用,可能为患有严重神经疾病(如GM2)的患者提供最大益处的潜力。 联合使用 ,包括基因疗法,可能为患有严重神经疾病(如GM2)的患者提供最大的益处。
REC-2282:神经纤维瘤病2型

摘要
REC-2282是一种用于治疗NF2的小分子HDAC抑制剂。该分子耐受性良好,包括多年服药的患者,并有可能降低心脏毒性,使其有别于其他HDAC抑制剂。与已批准的HDAC抑制剂相比,REC-2282既是中枢神经系统渗透性的,又是口服生物利用度的。我们希望在 中招募第一名患者参加2期双盲、随机、安慰剂对照研究。
疾病概述
NF2是一种常染色体显性遗传性罕见肿瘤综合征,由 功能丧失NF2肿瘤抑制基因突变,该基因编码细胞信号调节蛋白Merlin。NF2的丢失会导致表征这种疾病的标志性肿瘤的生长:前庭神经鞘瘤,或VS,以及脑膜瘤。NF2所见的VS和脑膜瘤是神经肿瘤学中最常见的肿瘤类型之一。此外,NF2突变会导致自发性脑膜瘤、间皮瘤和其他肿瘤类型的亚群。总而言之,我们相信NF2由前庭驱动的神经鞘瘤和脑膜瘤每年发生在大约33,000名患者中。
NF2患者在十几岁或20岁出头时被诊断为听力损失,发病时通常为单侧听力损失,局灶性神经功能缺损,以及与颅内压升高相关的症状。虽然病程变化很大,但大多数患者都失聪了,许多人最终会因为进行性的神经衰退而需要轮椅辅助 。治疗的标准是手术或放射外科,病人一生可能需要多次手术。虽然手术或放疗可以有效地控制肿瘤的生长,但大多数外科手术都会根据肿瘤的位置导致与神经缺陷相关的发病率 。听力损失、面神经麻痹和中度面神经功能障碍也是常见的手术结果。辐射可以诱发恶性转化,而这反过来又会使手术变得更加复杂。此外,随着新肿瘤的生长,肿瘤可能会在手术后复发。与NF2相关的肿瘤和治疗相关的发病率可能导致比预期更早的死亡。如果不治疗,NF2-颅内压升高会导致肿瘤死亡。
产品 概念
我们正在开发一种一流的口服小分子药物抑制肿瘤生长的实验研究NF2家族性和散发性疾病患者的脑膜瘤。REC-2282是一种口服生物利用、穿透中枢神经系统的泛组蛋白脱乙酰化酶(HDAC)抑制剂,具有PI3K/AKT/mTOR途径调节活性。与市场上销售的HDAC抑制剂相比,REC-2282特别适合NF2患者,而且NF2-突变的中枢神经系统肿瘤,由于其口服生物利用度和中枢神经系统暴露。NF2疾病是由 基因突变引起的NF2该基因编码一个重要的细胞信号调节因子Merlin。Merlin的缺失导致多条汇聚在PI3K/AKT/上的信号通路被激活
194
mTOR等。人类临床药效学数据支持REC-2282在抑制多种异常信号通路活性方面的作用 NF2-有缺陷的肿瘤。HDAC抑制剂诱导癌细胞生长停滞、分化和凋亡。我们于2018年12月从俄亥俄州创新基金会获得了REC-2282的全球许可。美国和欧盟已经批准了NF2中REC-2282的孤儿药物名称。

图52。REC-2282在肿瘤发生中起重要作用,抑制肿瘤细胞的生长。REC-2282在NF2中的作用机理9.
临床前
REC-2282在NF2中的新用途 是用我们的暴力搜索方法发现的,它利用了疾病基因的敲除NF2在人类细胞中。

图53。抢救NF2型号为 REC-2282。REC-2282挽救了被击倒的影响NF2在人类细胞中使用我们的表型组学分析。
| 9 | 改编自彼得里和费尔南德斯-瓦莱。Merlin/NF2失活在肿瘤生物学中的作用癌基因2016 35(5):537-48 |
195
在我们使用我们的 平台发现REC-2282用于NF2的新用途后,我们进行了文献搜索,以更好地理解分子和验证疾病模型。当时,我们发现REC-2282已经被证明可以抑制体外培养在与AKT失活相关的剂量下,通过诱导细胞周期停滞和凋亡来促进前庭神经鞘瘤(VS)和脑膜瘤细胞的增殖。在临床前模型中,REC-2282抑制原代人VS和NF2缺陷的小鼠神经鞘瘤细胞,以及原代患者来源的脑膜瘤细胞和良性脑膜瘤细胞系,本-门-1。
在NF2动物模型中,REC-2282被抑制体内An的增长NF2-缺陷性小鼠前庭神经鞘瘤同种异体移植。此外,REC-2282被抑制体内在小鼠体内建立人类前庭神经鞘瘤异种移植模型,饲喂标准的啮齿动物饲料或配方为每天提供25 mg/kg REC-2282的饲料,持续45天。这些动物数据是我们平台研究结果的功能性和正交验证。

图54。REC-2282可预防前庭神经鞘瘤移植瘤的生长。REC-2282显著降低SCID-ICR小鼠VS异种移植瘤的平均大小。显示的错误条是95%CI。P=0.006。
临床
我们预计将在以下时间启动 第二阶段临床试验。
之前在 研究者发起的试验和由Arno Treateutics赞助的试验中进行的临床工作包括人类接触REC-2282(以前称为AR-42)。在美国,共有三项已完成的成人受试者 研究,研究对象为实体或血液系统恶性肿瘤患者。共有77名患者接受了REC-2282的治疗,剂量从20毫克到80毫克不等,每周三次,连续三周,然后停药一周,四周为一个周期。多名患者在60毫克剂量下使用该剂量方案治疗多年,40毫克剂量下记录的最长疗程为4.4年。大多数不良事件是一过性细胞减少,没有导致剂量减少或停止。恶性血液病和实体瘤患者的MTD分别为40 mg和60 mg。恶性血液病和实体瘤患者的REC-2282血浆暴露量一般随剂量增加而增加。没有一致的 血浆REC-2282迹象
196
血液病患者和实体肿瘤患者在19天的服药期内没有明显的PK差异。
在早期的第一阶段药效学研究中,REC-2282抑制了NF2患者切除的前庭神经鞘瘤中ERK、AKT和S6通路的异常激活 。
我们计划启动一项2期随机、双盲、安慰剂对照 研究,以评估REC-2282对患有潜在NF2疾病的进展性脑膜瘤患者和有记录的散发性脑膜瘤患者的疗效和安全性。NF2突变。特殊协议 评估(SPA)已提交给FDA,我们预计将在中启动第二阶段试验。
| • | 这项研究将在具有NF2突变的进展性脑膜瘤患者中进行,这些患者在筛查后的三个月内不适合接受手术 ,登记时至少18岁。 |
| • | 患者将接受最多13个周期的REC-2282治疗;每个周期为期4 周,治疗3周,停药1周。一旦参与者完成了13个周期,他们将被临床随访。如果有进展,则参与者可以选择 接收开放标签REC-2282,如果参与者在双盲期内收到REC-2282。我们计划在研究的 第二阶段部分的六个月内进行临时和无效性分析。 |
| • | 我们将根据目标皮损的客观应答率(ORR)来评估治疗反应。 |

图55。REC-2282的第二阶段临床试验示意图。计划中的第二阶段临床试验设计,观察进展性脑膜瘤和散发性脑膜瘤患者中的REC-2282,这些脑膜瘤有潜在的NF2疾病和有记录的散发性脑膜瘤NF2突变。
竞争对手
目前在临床开发目标方面有三个活跃的计划NF2-导致脑瘤。
| • | Brigatinib是武田制药公司批准的用于非小细胞肺癌的ALK抑制剂,目前正处于脑膜瘤、前庭神经鞘瘤和室管膜瘤的第二阶段。 |
| • | 克里佐替尼是一种ALK/ROS1抑制剂,目前正在研究者赞助的进行性前庭神经鞘瘤第二阶段研究中进行研究。 |
| • | 阿斯利康(AstraZeneca)的MEK抑制剂selumetinib正在进行第二阶段试验,用于NF2相关肿瘤。 |
从接受REC-2282治疗的患者切除的前庭神经鞘瘤显示,这些肿瘤中活跃的多个异常通路(包括ERK和AKT)的激活受到抑制。这些结果可能很难用ALK或MEK的单途径抑制剂来实现。
197
REC-994:脑海绵状血管畸形

摘要
REC-994是一种口服生物利用型、超氧化物、清除剂、小分子药物,正在开发中,用于治疗CCM。在我们指导和执行的健康志愿者的第一阶段SAD和MAD试验中,REC-994显示出极好的耐受性和长期给药的适合性。CCM是最大的罕见疾病机会之一 ,没有批准的治疗方法。我们希望在 中招募第一名患者参加2期、双盲、安慰剂对照、安全性、耐受性和探索性疗效研究。
疾病概述
CCM是一种神经血管疾病,在美国和欧盟5国约有36万名患者被诊断或出现症状。 只有不到30%的CCM患者出现症状,导致该病被严重低估。CCM及其标志性血管畸形是由涉及内皮功能的三个基因中的任何一个的遗传或体细胞突变引起的 :CCM1, CCM2,或CCM3. 大约20%的患者有常染色体显性遗传的家族性CCM。剩余人群中的散发性疾病是由同一基因中出现的体细胞突变引起的。 CCM表现为脊髓和脑的血管畸形,其特征是毛细血管腔异常增大,没有干预脑实质。患有CCM病变的患者极有可能出现癫痫发作、头痛、进行性神经功能缺损和潜在的致命性出血性中风。目前的非药物治疗包括显微手术切除和立体定向放射外科治疗。鉴于这些干预的侵入性和风险性,这些选项是为有明显症状和/或容易接触到的病变的患者子集保留的。再出血和治疗的其他负面后遗症进一步限制了这些干预措施的有效性 。目前还没有批准的药物治疗可以影响CCM病变的生长速度或出血倾向或以其他方式引起症状。CCM可能是一种严重的疾病,会导致进行性神经功能损害和出血性中风的高死亡风险。
产品概念
我们正在开发一种第一位患者,口服小分子疗法 旨在改善与CCM相关的神经症状,并潜在地减少新病变的积累。REC-994是一种口服生物可用小分子超氧化物清除剂,其药代动力学支持人体每日一次给药。从机制上讲,内皮超氧化物的减少可以改善该病的细胞发病机制。此外,REC-994 具有抗炎特性,有助于减少疾病相关的病理改变。临床前数据已经证明,对急性到亚急性疾病相关的血流动力学参数(如血管通透性和血管动力学)有好处。在CCM的啮齿动物遗传模型中,慢性给药在减少病变数量方面显示出长期的益处。在我们第一阶段研究中登记的健康人中,REC-994的耐受性很好,每天剂量高达800毫克,在测试的任何剂量下都没有严重的不良反应。我们执行的第一阶段研究的安全性结果支持在第二阶段研究中继续对REC-994进行评估 。我们于2016年2月从犹他州大学获得了REC-994的全球版权,并已获得美国和欧盟的孤儿药物称号。
临床前
REC-994在连铸机上的新用途 是用我们的暴力搜索方法发现的,它利用了疾病基因的敲除CCM2在人类细胞中。在二次正交试验中,
198
REC-994逆转了人内皮细胞-细胞连接完整性的缺陷,这是一种与人内皮细胞-细胞连接完整性缺失相关的功能表型CCM2.
REC-994随后在两种内皮特异性基因敲除小鼠模型中进行了测试,以确定两种最普遍的遗传原因。CCM1和CCM2。这些小鼠模型忠实地再现了人类疾病的中枢神经系统海绵状畸形。使用REC-994治疗的小鼠显示出与使用药物治疗的对照组相比,病灶数量减少了 。值得注意的是,这一地区24小时循环血浆中的REC-994水平体内实验结果与人体每天服用200毫克的剂量一致。

图56。REC-994可降低慢性CCM小鼠模型的病变严重程度 。用REC-994治疗的小鼠在统计上显示小型病变的数量显著减少,中型病变的数量有减少的趋势。
临床
我们在健康志愿者身上完成了第一阶段SAD和MAD研究,预计将在 启动第二阶段试验。
我们在健康的人类志愿者中进行了一项SAD研究,使用的是不含赋形剂的活性药物成分瓶装粉末剂型。结果表明,在单次和多次剂量后,全身暴露(Cmax和AUC)普遍与REC-994成比例增加。中位数Tmax和t1/2似乎与剂量无关。在这项研究中没有报告死亡或SAE,也没有TEAE导致受试者退出研究。这些数据支持了一项针对健康志愿者的疯狂研究。
MAD 研究旨在调查多剂量口服REC-994的安全性、耐受性和PK,以从 瓶装粉末从片剂剂型到片剂剂型,以及评估单次口服后食物对PK的影响。总体而言,多次口服REC-994
199
在健康男性和女性受试者中耐受性良好,在本研究中使用的各个剂量水平。TEAE、生命体征、心电图、脉搏血氧饱和度、体检结果或神经学检查结果似乎没有剂量相关趋势。

队列2:Rec-99450 mg(N=6)队列3:Rec-994200 mg(N=6)队列5:Rec-994400 mg(N=6)队列7:Rec-994800 mg(N=6)队列 6a:Rec-994800 mg(N=6)第1天Cmax(ng/mL)Tmax b(H)AUC 0-24(小时*ng/mL)C24(1861.0(34.2)23.70(44.9)626.7(16.8)1.00(1.00,2.00)4939.0(19.7)57.52(39.1)111.3(43.7)1.53(0.75,4.00)8596.6(37.3)110.85 (69.6)2686.7(35.4)1.5(0.75,23789.1(32.3)284.3(39.8)1775.0(31.9)1.03(0.75,4.00)NA 137.80(35.60)d10 Cmax(ng/mL)Tmax b(H)AUC0-24(h*ng/mL)C24(ng/mL)T1/2(H)128.2(16.3)0.750(0.50,1092.0(15.2)13.67(26.3) 7.266(17.6)699.2(24.9)1.500(0.5,2.07)5038.4(22.1)54.52(38.2)7.725(15.4)1138.0(41.4)2.000(0.75,9648.7(26.4)107.1(33.0)8.541(10.7)1979.5(55.2)1.500(1.00,8.00)17541.6(47.7)195.7(62.1)7.711(13.1)1979.5(55.2) 1.500(1.00,8.00)17541.6(47.7)195.7(62.1)7.711(13.1)
表5.血浆REC-994的汇总统计数据 总体MAD队列的药代动力学参数。

安慰剂(N=8)n(%)REC-99450 mg(N=6)n(%)REC-994200 mg(N=6)n(%)REC-994400 mg(N=6)n(%)REC-994800 mg(N=6)n(%)TEAE总数 至少有一次TEAE的受试者总数5 4(50.0)0 103(50.0)4 3(50.0)15 4(66.73(50.0)0 03(50.0)0 03(50.0)1(16.7)0与研究药物的关系不太可能 可能肯定3(37.5)1(12.5)0 0 0 1(16.7)0 2(33.3)0 2(33.3)1(16.7)0 0 01(16.7)2(33.3)0 1(16.7)0(33.3)0 1(16.7)0至少一个SAE由于 AE 0 0 0停止药物研究的受试者总数
表6.第一阶段多重递增剂量研究的不良事件摘要。AE=不良事件 ;MAD=多次上升剂量;SAE=严重不良事件;TEAE=治疗-紧急不良事件
我们计划启动一项REC-994治疗症状性CCM的探索性第2期 双盲安慰剂对照、安全性和耐受性研究。
| • | 这项研究将招募年龄在18岁以上、有MRI证实的解剖性CCM损害的有症状的CCM患者。 |
| • | 第二阶段研究的主要目标将是评估REC-994低剂量组和高剂量组在12个月内每日服用REC-994的安全性和耐受性,与安慰剂相比。 |
200
| 有症状的CCM患者。探索性次要终点将包括对患者报告结果的评估,以及已建立的神经体征和症状的复合量表。 |
| • | 目前,还没有CCM药物开发的开发或监管先例或途径。我们将在FDA的指导下进行 探索性第二阶段,为关键的试验设计提供信息。第二阶段将探索多种临床结果评估,包括我们与CCM患者倡导组织、血管瘤联盟和罗切斯特大学合作开发的CCM特定患者报告结果评估 。 |

图57。REC-994的第二阶段临床试验示意图。计划的第二阶段试验设计,评估REC-994在有症状的CCM患者中的有效性和安全性。
竞争对手
有两项由研究者发起的临床研究正在进行中,以研究CCM患者的市场疗法。
| • | 芝加哥大学的研究人员正在评估阿托伐他汀或立普妥在降低CCM患者出血率方面的疗效。 |
| • | 意大利马里奥·内格里药理研究所的研究人员正在评估批准的β受体阻滞剂心得安在减少皮损和临床事件方面的疗效。 |
据我们所知,REC-994计划是CCM临床试验中唯一由行业赞助的治疗计划。如果获得批准,REC-994将成为首个针对CCM的药物疾病修饰疗法,CCM是罕见疾病领域中最大的未得到满足的需求领域之一。
艰难梭状芽孢杆菌结肠炎

摘要
我们已经鉴定出三种主要的NCEs(REC-163964,REC-164014和REC-164067),它们具有潜在的口服活性,肠道偏向,小分子艰难梭菌毒素抑制剂,我们已经证明它们是葡萄糖基转移酶的抑制剂。 这些分子具有防止复发的潜力,并可用于高危患者的二级预防治疗。艰难梭菌感染是抗生素引起腹泻的主要原因,也是发病率和死亡率的主要原因。我们目前正在完成探索性、非临床、安全性研究,以便能够选择开发候选药物。
201
疾病概述
艰难梭菌诱导性腹泻是抗生素引起腹泻的主要原因,由结肠内正常菌群的破坏引起。这种细菌分泌的毒素A或TcdA和B或TcdB会导致相当大的发病率,包括严重腹泻、结肠炎、毒性巨结肠、脓毒症、住院时间延长,甚至可能死亡。每年有超过730,000名患者 在美国和5欧元被确诊。在接受标准治疗的患者中,疾病复发的比例为20%-30%。
产品概念
我们的目标是发现并开发首个安全有效、口服生物利用的小分子毒素抑制剂。艰难梭菌它可用于预防复发感染,并预防性用于高危患者,包括长期护理机构中有相关感染和住院史的免疫功能低下的老年患者。 该药可用于预防复发感染,并用于预防高危患者,包括长期护理机构中有相关感染和住院史的免疫功能低下的老年患者。我们正在为这个项目开发的分子是为肠道偏向药理学 设计的,目的是在减少全身暴露和潜在的全身影响的同时,针对胃肠道的解剖部位进行感染。此外,这些分子代表了一种新的机制,可以与目前批准的和 正在开发的新型抗菌药一起用于治疗这种疾病。与抗生素治疗不同的是,抗生素治疗可以消除肠道微生物区系,并进一步增强艰难梭菌如果受到感染,这种宿主导向的机制预计不会对肠道微生物群产生负面影响。我们的候选药物有可能提供预防复发的保护艰难梭菌预防感染,从而防止严重的发病率和死亡率。
临床前
我们设计并生产了三种NCE,包括REC-163964、REC-164014和REC-164067,这三种NCE是使用我们的暴力搜索方法发现的,这些细胞利用暴露在艰难梭菌毒素B。这些化合物在亚结构上是多样化的,并且具有使它们适合于预防性治疗的性质。所有这三种分子都在我们的平台上以及在正交功能验证分析中显示 纳摩尔效力,这些功能验证分析包括电池衬底阻抗传感,这是一种衡量屏障完整性的指标。我们在一项基于靶点的实验中发现,这三个分子都能抑制 葡萄糖基转移酶(IC50=1.2-10 nM),这表明抑制毒素诱导的宿主细胞中Rho-GTP酶的糖基化是最可能的作用模式。这些 分子的靶外活性可以忽略不计,口服后会产生较高的肠道/血浆比,药物间相互作用的可能性较低,并且无致突变性。这三种分子都能提高仓鼠模型的存活率。艰难梭菌感染。

202
图58。先导化合物挽救毒素B诱导的表型,并改善内皮细胞屏障的完整性。平台法(左图)和ECIS法(右图)中先导化合物的活性。左图:用毒素B或TcdB诱导HUVECs与受试化合物孵育的疾病表型。右图:人脐静脉内皮细胞与10 ng/mLTcdB孵育后,ECIS定量检测内皮细胞的跨内皮阻力。艰难梭菌在测试化合物存在的情况下。两者的数据均以均值±扫描电镜表示,N=>3 个独立实验。

图59。艰难梭菌使用铅化合物治疗的感染模型仓鼠比使用交通工具治疗的动物存活时间更长。试验化合物每日2次灌胃,连续5d,同时给予赋形剂组和万古霉素组(50 mg/kg,qd)。在未经处理和万古霉素处理的动物中n=5,在赋形剂和试验化合物处理的动物中 N=10。
临床
这三个主要候选者正在进入非GLP、非临床 安全性研究。具有最大安全边际的分子将被推进到支持IND的安全研究中。
神经炎

摘要
我们已经确定了三个主要NCE(REC-648455、REC-648597和REC-648677)第一位患者,口服生物利用、安全、中枢神经系统穿透性、小分子小胶质细胞激活调节剂。小胶质细胞激活和神经炎症是神经退行性疾病(如阿尔茨海默病和帕金森病)和中枢神经系统炎症性疾病(如多发性硬化症)的特征。小胶质细胞激活的小分子调节剂有可能减少神经退行性疾病和中枢神经系统炎症性疾病中与促炎过程相关的神经元死亡。该项目正处于领先优化阶段。
疾病概述
神经炎是许多中枢神经系统疾病的标志,包括神经退行性变。仅在美国,就有600多万人患有神经退行性疾病,随着人口老龄化,患病率预计还会增加。大多数神经退行性疾病缺乏安全有效的疾病修正疗法。小胶质细胞是中枢神经系统特有的一种细胞类型,当长期激活时,会释放促炎细胞因子,如肿瘤坏死因子(TNFa、IL-6、IL-1?、MCP-1,它们是神经元毒性和疾病进展的驱动力。
203
产品概念
我们的目标是确定口服生物有效性和安全性、中枢神经系统渗透的小分子小分子调节剂来激活小胶质细胞,它们可以抑制肿瘤坏死因子的活性和/或释放。a、IL-6等促炎细胞因子。与已知的抗炎分子相比,已知的抗炎分子通过NF-kB和JAK等成熟的途径发挥作用,并具有已知的相关免疫相关责任,我们为该计划开发的分子通过新的NF-kB和JAK非依赖机制发挥作用。我们认为,神经退行性疾病以及炎症性肠道疾病和皮肤病(特应性皮炎和牛皮癣)等外周免疫性炎症性疾病都存在治疗机会。
临床前
这三个分子,rec-648455,rec-648597和rec-648677,都是利用肿瘤坏死因子处理的人内皮细胞的强力搜索方法发现的。a 这些分子还能抑制肿瘤坏死因子a刺激HUVEC细胞分泌IL-6,诱导小鼠小胶质细胞表达IBA1。REC-648455、REC-648597和REC-648677在人脐静脉内皮细胞中的IC50值分别为95、75和230nM,在小胶质细胞中的IC50值分别为80、78和210nM。使用我们的蛋白质组学平台,我们发现REC-648455拯救了一种肿瘤坏死因子a-在HUVEC细胞中诱导高维细胞因子信号,包括抑制与神经炎症有关的关键细胞因子,如IL-1、CCL2(MCP-1)、CXCL5和CCL5。
这些 分子的作用机制似乎是独特的,与NF-kB和JAK无关,因为它们不抑制TNFa-诱导NF-kB核 易位和JAK活性。我们的递归图谱表明,这些分子的高维表型特征与一个新的靶点聚集在一起,这个新靶点在文献中没有与神经炎症相关,也没有在临床上被探索 。所有这三种分子都具有与良好的脑渗透相一致的特性,我们目前正在优化这一系列分子的代谢稳定性和清除特性。

204
图60。拯救肿瘤坏死因子 a-铅分子诱发模型。三种铅分子挽救肿瘤坏死因子对人体细胞的作用a使用我们的表型组学分析。

图61。铅分子拯救肿瘤坏死因子a-在人脐静脉内皮细胞和小鼠原代小胶质细胞中诱发功能效应。左图:HUVEC细胞与测试化合物、肿瘤坏死因子(TNF)孵育后a加入25 ng/mL的培养液,孵育平板,收集培养上清液,用均相时间分辨荧光法分析IL-6的含量。右图:小鼠小胶质细胞与受试化合物孵育后,加入LPS(100 mg/ml),孵育平板 ,细胞行Iba1染色,用IXM工作细胞成像。数据以平均值±标准差表示,N=10(HUVEC)和N=5(小胶质细胞)。

图62。REC-648455拯救了一名肿瘤坏死因子a-在人脐静脉内皮细胞中诱发高维蛋白质组学特征。在用1 ng/mL的TNF刺激HUVEC之前,先用化合物预处理 a。处理样品的上清液由NPLEx Biosciences收集和处理,使用微型化的nELISA技术。使用5个生物重复对每个条件进行测试。
巴顿病

205
摘要
我们已经确定了三种主要的NCEs,即REC-648190、REC-259618和REC-648647,它们具有口服生物利用度、中枢神经系统穿透性和疾病调节疗法的潜力,可用于治疗多种亚型的巴顿病。巴顿病是一种常染色体隐性遗传性神经退行性疾病,由14个基因中的一个突变引起。CLN基因。虽然罕见,但这些疾病共同代表了最常见的儿童神经退行性疾病,并显示出重大的未得到满足的需求。 项目目前处于销售线索优化阶段。
疾病概述
巴顿病,又称神经性蜡样脂褐素沉积症,是一种常染色体隐性遗传的神经退行性溶酶体储存障碍,由14个CLN基因中的一个基因突变引起。美国和欧盟5国的流行情况CLN2和CLN3据估计,这种疾病的形式大约有2000名患者。虽然罕见,但这些疾病共同代表了最常见的儿科神经退行性疾病。这种疾病会导致认知、知觉和运动协调功能受损,最终导致过早死亡。发病年龄因特定的突变而异,死亡的范围从儿童早期到成年早期。
产品概念
我们的目标是发现和开发一种口服生物利用型、中枢神经系统渗透性的疾病修饰疗法,用于治疗多种亚型的巴顿病,包括CLN2, CLN3,及CLN8。一种中枢神经系统穿透性、疾病改良性、小分子疗法将有可能改善这种神经退行性疾病的中枢和外周方面。由于缺乏已知的可用药靶点,且对潜在疾病生物学的了解较差,这表明发现新疗法的靶点不可知性方法可能是有用的。
临床前
我们已经从两个化学系列中鉴定出三个 先导分子,rec-648190,rec-259618和rec-648647,使用我们的暴力搜索方法,利用巴顿病基因的敲除。CLN8在人类血管内皮细胞中。此外,我们还在一项患者成纤维细胞功能试验中测试了这些分子,在该试验中,我们评估了溶酶体功能的生物标志物--ATP合成酶亚单位-c水平的减少。CLN2BATTEN患者来源的成纤维细胞。该项目正处于领先优化阶段,目标是提高药效以及口腔和脑暴露。

图63。多个铅分子拯救CLN8在患者成纤维细胞二次实验中建立模型并显示活性 。左图:三个铅分子拯救了被击倒的影响CLN8输入人类细胞使用我们的表型组学分析。右侧面板:CLN2用试验化合物处理BATTEN患者成纤维细胞,检测疾病相关溶酶体功能障碍的相关标志物ATP合成酶亚单位-c的积聚。数据以平均值±SEM表示,n=2。
206
Charcot-Marie-Tooth病,2A型

摘要
我们已经确定了多种铅分子,包括rec-64810、 rec-648458、rec-1262和rec-150357,它们有可能是 第一位患者,口服生物利用型疾病修饰分子,可减缓或逆转线粒体疾病CMT2A的进展。CMT2A是一种罕见的常染色体显性显性周围神经退行性疾病,由CMT2A基因突变引起Mfn2导致小腿和手部进行性肌肉萎缩的基因。目前还没有批准的CMT2A疾病修饰疗法。此项目目前处于销售线索优化阶段 。
疾病概述
CMT2A是一种罕见的常染色体显性遗传性周围神经疾病,由Mfn2基因突变引起,导致小腿和手的进行性肌肉萎缩。CMT2A是这种疾病最常见的轴突神经病变形式,据估计在美国和欧洲5国约有15,000名患者受到影响。Mfn2编码丝裂原蛋白-2(mitofusin-2),该蛋白在线粒体功能和运输中起关键作用。大多数患者在童年早期到晚期出现症状,并在一生中变得越来越依赖拐杖或轮椅。
产品概念
我们的目标是发现和开发第一种安全有效的口服生物可用小分子疾病修饰疗法,用于治疗CMT2A。我们 正在为这个项目开发的分子被设计成能够穿透周围神经系统,从而在受影响的组织上实现活动。这些分子的靶向机制新颖,但已有临床先例,支持CMT2A的靶向产物特征。
临床前
我们使用我们的蛮力搜索方法,利用人类视网膜色素上皮细胞中疾病基因Mfn2的敲除,从多个化学系列中鉴定出四个先导分子,Rec-64810,Rec-648458,Rec-1262和Rec-150357。这些分子中最有效的REC-64810被进一步鉴定,并被证明可以挽救CMT2A生物学的一个关键特征-线粒体断裂。REC-64810在啮齿类动物中具有良好的血神经屏障穿透特性,在坐骨神经和背根节中的高药物暴露证明了这一点。最后,REC-64810提高了IPSC来源的野生型和患者神经元中的三磷酸腺苷水平,这与线粒体功能的改善是一致的。我们的递归图显示, REC-64810和其他三个导联通过一种新的激酶机制起作用,这在以前并没有涉及到这种疾病。该项目目前正处于领先优化阶段。
207

图64。REC-64810挽救了MFN2疾病模型,并在二次 正交试验中显示活性。左面板:REC-64810拯救了击倒的效果Mfn2在人视网膜色素上皮细胞中。右图: REC-64810还挽救了衡量线粒体健康的关键指标--线粒体长度。

输注速率6小时血浆(NM)脑(NM)SN(NM)背根神经节(NM)0.25 mg/kg.h13.9+/-3.059+/-14430+/-1651692+/-7241 mg/kg.h112+/-72 262+/-531122+/-237 13141+/-2181
表7.REC-64810在外周神经中实现高暴露 。以两种输液速率给大鼠灌胃重组EC-64810,以达到稳态水平。6小时后测定指定组织中的暴露水平。

208
图65。REC-64810可增加健康受试者和CMT2A患者IPSC神经元的三磷酸腺苷产量。健康(顶板)和CMT2A(底板)患者IPSC来源的运动神经元样本培养5天,然后用REC-64810处理。测量了线粒体功能的关键指标ATP水平。数据代表两个独立实验的平均值,以百分比相对发光单位±SEM表示。
STK11突变型非小细胞肺癌的免疫检查点抗性

摘要
我们已经确定了一种临床阶段口服生物可用小分子的新用途,以恢复和提高肿瘤中携带肿瘤抑制基因突变的肿瘤对免疫检查点 抑制剂的敏感性。STK11。大约有3万例STK11在美国和EU5,每年都有突变的转移性非小细胞肺癌,这些突变已经被证明可以预测不良的预后和对ICI的耐药性,特别是抗PD(L)-1治疗。目前还没有被批准的治疗方法被开发出来专门调节肿瘤的反应 STK11突变的癌症。该计划目前正处于剂量优化阶段。
疾病概述
STK11是一种肿瘤抑制基因,参与多种细胞过程,包括细胞代谢、细胞凋亡、细胞极性和DNA损伤反应。基因突变STK11被广泛认为是抵抗免疫检查点封锁的驱动力,特别是在非小细胞肺癌患者中。高达30%的NSCLC病例和大约14%的转移性NSCLC病例 在STK11基因,以及STK11缺陷与浸润的细胞毒性CD8+T淋巴细胞密度降低有关,导致患者预后不良和预后不良。抗PD(L)-1心理治疗。据估计,只有7%的非小细胞肺癌患者从检查点抑制剂中受益,而且FDA还没有批准针对患有 的患者的治疗方法。STK11转移性非小细胞肺癌的突变。
产品概念
我们的目标是发现和开发新一代口服生物利用型小分子疗法,这种疗法可以逆转STK11缺乏 ,并使肿瘤对联合治疗和抗PD(L)1治疗变得敏感。STK11突变可减弱肿瘤对 的反应抗PD(L)-1。我们打算将这些疗法与抗PD-(L)1 和其他针对检查点难治性和单纯转移性非小细胞肺癌人群的靶向治疗。
临床前
REC-64151的新用途STK11突变型NSCLC 是使用我们的推理搜索 方法发现的。基于递归地图的推论,我们启动了动物研究,以评估rEC-64151与 的结合。抗PD-1抗体在一个专为用途而建26号货柜码头STK11肿瘤模型。该化合物显示 免疫检查点抵抗力有统计学意义的逆转。正在进行的药理学研究将使剂量优化成为可能,并收集更多的流式细胞仪数据以建立作用机制。 REC-64151是一种已知的化学物质,有临床先例,如果啮齿动物体内的剂量优化研究支持在人类暴露时的疗效,该分子可能处于有利地位,使 进入第一阶段研究。
209

图66。REC-64151抢救STK11型疾病模型。REC-64151产生了对高维平台的有力救援STK11HUVEC的KO表型从疾病状态恢复到健康细胞状态,EC50为244 nM。

图67。REC-64151逆转STK11缺陷的CT26肿瘤的免疫检查点抵抗。将CT26亲本细胞和CT26 STK11 KO细胞注射到小鼠的皮下,使其大小匹配,治疗15d(CT26STK11 KO)或21d(CT26),分别用赋形剂(黑色)、抗PD1(10 mg/kg/d)、REC-0064151(100 mg/kg/d,qd)或抗PD1+REC-64151(每种化合物的剂量相同)进行治疗。 抗PD1(10 mg/kg/d)、REC-0064151(100 mg/kg/d,qd)或抗PD1+REC-64151(每种化合物剂量相同)。肿瘤体积用平均值±扫描电镜表示。
小分子Myc抑制剂

210
摘要
我们已经使用我们的推理搜索方法确定了多个热门系列,这些系列随后在抑制MYC下游的转录活性方面显示出浓度依赖的活性。MYC转录靶基因的表达增加存在于肿瘤学中,高达50%的癌症存在MYC的改变。具有抑制MYC依赖活性的新型小分子可以改善对多种肿瘤的治疗,特别是那些含有与MYC激活直接相关的基因突变的肿瘤。目前还没有被批准的针对MYC的分子。此程序当前在点击率领先相位。
疾病概述
函数增益中的更改MyC已在超过50%的人类癌症中发现10,但药理上抑制这种蛋白质的努力受到了传统化合物结合袋中缺乏的蛋白质结构的阻碍。此外,在癌基因和相关通路的肿瘤抑制因子(如WNT-β-catenin)发生改变的肿瘤中,也观察到MYC 通路的激活。小分子在 肿瘤的情况下特别有效函数增益 MYC生物学可能对多发性实体肿瘤和血液系统恶性肿瘤广泛有效。
产品概念
我们的目标是发现 并开发新的口服生物可用小分子来抑制MyC治疗以MYC通路异常激活为特征的多种癌症的活性。使用推理搜索方法,我们已经从我们的化学库中识别出与MYC活性或蛋白质稳定性相关的多个不同的结构和机械类别,并扩展这些命中以生成多个独特的命中系列。
临床前
我们已经从多个化学序列中确定了几个靶向分子,包括REC-841、REC-136302、REC-163196、REC-120464、REC-145834和REC-162977,用我们的推理搜索方法预测了可能抑制MYC激活的分子。 靶向HSP90的分子被恢复为阳性对照,HSP90是已知调节MYC转录活性的靶向分子。 我们使用我们的推理搜索方法从多个化学系列中鉴定了几个靶向分子,包括REC-841、REC-136302、REC-163196、REC-120464、REC-145834和REC-162977。此外,泛素蛋白酶体系统中的已知分子REC-841被发现作为设计MYC特异性降解物分子的潜在起点。据预测,其他HIT分子将通过新的机制发挥作用。这些预测的命中结果在基于细胞的荧光素酶MYC报告试验中得到了验证。热门系列剧目前正在使用我们的数字化学工具进行扩展。
| 10 | 陈华,刘海清,G。以致癌Myc为靶点作为癌症治疗的策略。签名转账目标3, 5(2018年)。Https://doi.org/10.1038/s41392-018-0008-7 |
211

图68。从我们的平台推断的命中率在正交MYC转录报告 分析中得到验证。基于推理的HIT选择基于表型相似性比较恢复与MYC活性有关的已知和新分子MyCCRISPR基因敲除表型。新分子 和已知分子的表型组学图谱明显地聚在一起,尽管它们都显示出与 的相似性MyC击倒(左)。在一项正交的Myc荧光素酶实验中,表型组学推断的MYC HITS显示浓度依赖性地抑制Myc转录活性
其他计划
除了上面突出显示的值得注意的计划 之外,我们还有25个其他计划,我们相信这些计划将为我们带来未来的商机。自2020年7月以来,使用我们的推理搜索方法确定了其中14个程序,并对其进行了发现和验证。展望未来, 我们预计,我们渠道中的绝大多数新产品都将使用我们的推理方法来发现。
212

图69。我们庞大多样的附加研究项目。正在积极开发的其他项目涵盖了许多治疗领域,从癌症到炎症再到罕见的遗传疾病。所有这些程序都是使用我们的递归操作系统发现和开发的。
肺动脉高压

摘要
我们已经确定了REC-1886的新用途,REC-1886是一种已知的化学实体,具有临床先例,是一种潜在的第一位患者,用于治疗肺动脉高压(PAH)的口服疾病修正疗法。肺动脉高压是一种进展性疾病,其特征是肺动脉高压,死亡率和发病率都很高。基于我们对REC-1886的 理解,该项目有可能导致获得许可的临床阶段候选人或触发NCE项目。
疾病概述
肺动脉高压的特征是由于血管平滑肌细胞增殖、肥大和纤维化导致肺动脉内血管阻力和血压异常升高,从而导致心力衰竭和死亡。在美国和欧盟,大约有3.5万名PAH患者。PAH可以是散发性的(特发性),也可以是遗传性的(家族性)。80%的家族性PAH是由基因突变引起的 BMPR2吉恩。发病情况各不相同,但通常发生在30到40岁之间。早期症状包括呼吸急促和疲劳。未经治疗的中位生存期为2.8年。
213
产品概念
我们的目标是发现和开发一种安全的、口服生物利用型、小分子、疾病修饰疗法,可以逆转PAH的潜在生物学,提高存活率。PAH由多种批准的血管扩张剂治疗,这些药物提供症状缓解,但不改变潜在的病程。一种新的疾病修正疗法可以提高肺动脉高压患者的存活率,这对这些患者来说将是一个主要的治疗益处。
临床前
我们使用我们的暴力搜索方法和利用CRISPR敲除人内皮细胞中PAH基因BMPR2的方法,鉴定了REC-1886,一种口服生物利用的已知化学实体,具有临床先例。此外,REC-1886可挽救原代人肺动脉内皮细胞由细胞因子诱导的内皮细胞向间充质细胞的转化,这是肺动脉高压中肺血管平滑肌增殖和血管重塑的关键生物学驱动因素。

图70。REC-1886挽救了平台表型和次级功能 检测。左面板:REC-1886挽救了CRISPR介导的基因敲除BMPR2在我们的表型组学平台上的HUVEC。右侧面板:用细胞因子鸡尾酒处理人肺动脉内皮细胞,诱导相关的纤维化疾病状态和血管内皮生长因子的表达。a平滑肌肌动蛋白(SMA)是纤维化的关键平滑肌标志物,采用免疫荧光法进行定量。数据以平均值±SEM表示,n=3。
我们还评估了REC-1886在野百合碱大鼠肺动脉高压模型中的作用。在本研究中,REC-1886 15 mg/kg,2次,po,使右心室收缩压和右心室重量正常化,与肺血管疾病的改善相一致。Macitentan是一种内皮素受体拮抗剂,被批准用于PAH,它适度降低了右心室收缩压,但对右心室重量没有影响。
214

图71。REC-1886对野百合碱诱导的大鼠肺动脉高压模型有效。左面板:右心室收缩压。右面板:右心室重量与左心室加室间隔重量之和的比值RV/(LS+IVS)。雄性SD大鼠皮下注射野百合碱60 mg/kg复制PAH模型。给动物灌胃赋形剂、REC-1886或Macitentan(30 mg/kg,qd),共28天。在给药阶段结束时,将大鼠置于麻醉状态下进行血流动力学评估,然后取肺组织进行组织学测量。数据以平均值±SEM表示,每组n=10。*p
增敏剂治疗系统性硬化症

摘要
我们已经用我们的暴力手段确定了REC-4249作为一种铅分子第一位患者,口服活性抗衰老药,用于治疗一系列衰老疾病。衰老生物学与许多与年龄相关的慢性病有关。如果成功,这个项目有可能导致一个有执照的临床阶段候选人。
疾病概述
衰老是细胞不可逆转地停止分裂并进入永久生长停滞状态而不经历细胞死亡的过程。在组织中慢性分泌促纤维化/炎症信号的衰老细胞的积累与许多年龄相关的慢性疾病有关,包括系统性硬化症和骨关节炎。涉及细胞衰老的疾病,如肺纤维化、肺动脉高压、心功能不全、肾功能衰竭等,死亡率很高。这些致病细胞的药理消除有可能减缓或逆转疾病的进展,并已被证明可以延长啮齿动物模型的寿命。
产品概念
我们的目标是发现和开发一种安全的、口服生物利用的小分子衰老药物,用于治疗涉及细胞衰老的疾病。衰老疗法 有可能在涉及细胞衰老的多个适应症中发挥作用。最初的临床前模型将集中在致残性结缔组织疾病硬皮病上,但该计划的分子也可能在其他 适应症中发挥作用。目前针对涉及细胞衰老的疾病的治疗方法是针对症状缓解,并不能改变疾病进展。
215
临床前
我们已经确定了一种口服生物利用的已知分子,REC-4249,这是一种有临床先例的分子,使用我们的暴力搜索方法,利用内皮细胞衰老的模型。根据基于细胞的高维表型组学分析的活性和健康内皮细胞与衰老内皮细胞的差异活性,REC-4249被选为先导。REC-4249显著降低衰老小鼠肝组织中衰老生物标志物(P16)的水平。此外,在肾脏和肺组织中也检测到类似但没有统计学意义的趋势 。这个体内REC-4249的有效性和安全性正在临床前啮齿动物硬皮病模型中进行评估。

图72。REC-4249可降低老龄小鼠衰老标志物的表达。老龄小鼠(23月以上)分别给予赋形剂(黑色)、0.3 mg/kg/d REC-4249(青色)和1.0 mg/kg/d REC-4249(蓝色)处理4d,RT-qPCR检测P16RNA表达水平,归一化至18S表达水平。数据以平均值±扫描电镜表示,每组n=8。*p
我们的价值创造战略
我们的Recursion OS 为我们这样规模和成熟的公司提供了医疗行业内最大、最多样化的治疗管道之一。除了流水线的广度,我们致力于推动这些项目从早期发现到临床开发,并最终尽可能高效地惠及患者。然而,创建一条深度和成熟的治疗管道是资金和人员密集型的。因此,我们已经在内部和外部部署了资源,以创建 多管齐下、资本高效的价值创造战略,随着公司逐渐成熟,这将有助于促进更大程度的整合。
在近期和中期内,我们预计将继续建立和推进进入临床的内部项目管道,主要关注基因驱动的疾病(包括罕见疾病和基因定义的肿瘤学)和其他未得到满足的利基需求领域。在这些领域的工作给我们带来了许多好处,包括监管机构提供的特殊激励措施(通常可以缩短患者获得治疗所需的时间)、治疗方法通常具有显著的经济性、一段时间内可能的市场排他性、研发成本的税收抵免,以及与较大适应症相比可能以相对较低的成本进行的临床试验。
216
通过临床试验和商业化对早期发现的大型疾病指征进行起诉 对于我们在公司成长的现阶段完全独立开展可能成本过高,而且有可能分散我们对长期价值创造战略的注意力。因此,在近期和中期内,我们希望在炎症、神经变性、衰老、大型肿瘤学适应症、免疫肿瘤学和传染病等较大的疾病适应症方面寻求与大型制药或生物技术公司的合作伙伴关系。
我们的多管齐下、资本高效的价值创造战略旨在短期和中期推进商机,并朝着公司的长期愿景和生存能力迈进。通过领导其内部治疗流水线的临床起诉,我们在一系列适应症和监管方案上磨练了我们的执行专业知识。通过实现 我们企业级合作伙伴的目标,我们不仅获得了卓越的运营,还获得了在大型疑难疾病和新型治疗模式方面的经验。通过对我们企业级合作伙伴关系的收益进行再投资,我们将进一步 推进我们正在筹备中的计划,并继续扩大其广度和深度。此外,我们将建设更大的技术和生物能力,以推动整合和运营协同效应。在中期内,我们将完善我们的 商机,包括内部开发、子公司组建、合作伙伴关系和外部许可。
我们业务战略的中短期要素与我们的三个关键价值驱动因素保持一致。我们打算:
开发当前的资产管道,同时实现超线性管道增长。
| • | 通过开发和潜在的法规提交,快速推进我们著名的产品。 |
| • | 超线性地扩展和推进我们的管道。 |
| • | 通过治疗性和机械性多样化以及选择资产合作伙伴关系来降低投资组合风险。 |
| • | 证明我们在发现和开发的每个阶段的时间和成本都低于行业平均水平。 |
| • | 证明我们临床项目的技术成功水平高于行业平均水平。 |
| • | 继续发展递归数据世界并改进递归地图,因为我们相信,将推动 递归和社会最大价值的资产是那些仍将到来的资产。 |
执行战略合作伙伴关系,最大限度地发挥我们 平台的潜在价值。
| • | 与行业领先的公司建立合作伙伴关系,解决广泛的治疗领域或其他治疗方式(如大分子或RNA疗法),我们可以利用我们的工具和合作伙伴的专业知识和资源快速推进计划。 |
| • | 履行我们与拜耳在纤维化领域的战略合作伙伴关系。 |
通过归纳实验室探索递归地图带来的新扩展和商机。
| • | 通过探索切线 业务垂直领域(例如,其他治疗方式、诊断、金融、农业、兽医),最大限度地提高基础设施、工具和人员方面现有和计划投资的价值。 |
217
如果我们成功地追求药物发现的产业化,我们可能有机会开创 生物制药行业的价值如何分配以及在哪里分配的先河:i)在发现和开发过程中更早地与项目合作,ii)解决那些原本被认为对传统药物开发来说太小或无利可图的疾病领域, 这些领域被认为太小或无利可图,以及iii)在创新和开发过程中竞争快速推向市场在主要治疗领域,占据领导地位 。我们相信,这些努力的成功可能会给患者的生活和生物制药行业带来持久的、积极的和变革性的影响。
218
设施
总部。2018年,我们搬到了目前位于犹他州盐湖城市中心的总部。根据2028年5月到期的租约,我们 租赁了105,419平方英尺的办公、研究和实验室空间,并签订了额外的91,748平方英尺的办公、研究和实验室空间的租赁协议,该租约将在我们入驻后或2032年3月的较早10 年内到期。我们的现代化总部吸引了当地、国内和国际的人才,并设有传统和自动化药物研究实验室。

219
图75。我们的总部位于犹他州盐湖城市中心。我们在犹他州盐湖城总部的照片。我们是生物蜂巢的创始成员,该组织是犹他州生命科学中心的品牌推广活动。与州和地方政府合作,我们正在帮助当地生命科学公司迅速迁往以我们总部为中心的市中心集群。
研究 间歇性。根据一份2028年5月到期的租约,我们还在加利福尼亚州米尔皮塔斯租赁了一处24974平方英尺的房产,作为啮齿动物的隔间。我们使用该设施进行药物发现,以实现 药代动力学、药效学和探索性安全性研究。该设施配备了我们正在开发的专有的数字化笼子技术。

图76。我们先进的用于表演的体内研究。
企业社会责任
我们围绕企业社会责任的理念源自我们的使命:解码 生物学将从根本上改善生活。我们在从根本上改善生活方面采取了慷慨的立场,考虑到患者和 爱他们的人的生活(受我们创新的影响),我们员工及其家人的生活(受我们的福利、文化、学习和成长的机会以及公平薪酬的影响),以及重要的是我们工作的社区的生活,因为坚实的基础有助于我们建立长期的基础。从社区的角度来看,我们专注于与我们的价值观和优势一致的影响领域,这指导着我们的企业社会责任理念。 有鉴于此,我们积极参与或赞助以下重点领域内的关键社区努力:
| • | 技术和生物技术领域的多样性、公平性和包容性(例如,我们主办了广受欢迎的本地季度科技女性演讲者系列,并赞助了硅坡会议(br}会议的第一个多样性和包容性轨道)。 |
220
| • | 我们当地生命科学和技术生态系统的增长和可持续性(例如,我们是围绕犹他州生命科学行业的品牌推广活动BioHave的创始赞助商和 成员,并将我们以前的总部改用为推出Alight Labs,这是一个生物技术孵化器/加速器,重点是支持未被充分代表的创始人)。 |
| • | 推广可持续的环境实践(例如,我们选择目前的总部是为了最大限度地利用公共交通 ,并因成为全国最环保的自行车友好型初创企业之一而获奖)。 |
递归基础
递归基金会成立于2019年,作为一种工具,我们可以通过它来推动我们的慈善和慈善努力 时间。2020年底,我们的董事会承诺将我们1%的股权投入递归基金会,以帮助展示我们对社会责任的坚定承诺,并确保我们在这一领域的工作有一个可持续的未来。
海拔实验室
海拔实验室是递归基金会的第一项工作 。海拔实验室与犹他州大学合作,作为孵化器/加速器的混合模式成立,专注于在犹他州培养新一代生物技术创始人,包括特别强调 未被充分代表的创始人。海拔实验室于2020年秋季开始运营,已经收到了数十家当地、国内和国际初创企业的申请,并接纳了其中6家初创企业。我们寻求帮助这些公司 实现早期增长和筹资,同时为他们提供使用实验室和设备的机会,否则这些实验室和设备的价格将高得令人望而却步。我们的目标是让这些初创企业在犹他州永久成长,以创造更可持续的生命 科学生态系统。海拔实验室的早期使用者包括Y Combinator初创公司Knowledge Medicines、3Helix、NexEos Bio、Teiko(其创始人兼首席执行官是Counsyl的前首席执行官)等。

图77。海拔实验室孵化器已经在犹他州培育下一代创新型生命科学公司。我们和犹他州大学在犹他州大学研究园区的前总部共同创建了海拔实验室,以帮助犹他州建立一个可持续的生命科学公司生态系统 ,重点关注未被充分代表的创始人。
商业化
我们打算保留一些候选药物的重要开发和商业权,如果获得市场批准,我们可能会在美国和其他地区将我们的候选药物 单独商业化,或可能与合作伙伴一起商业化。我们目前没有销售、营销或商业产品分销能力。随着时间的推移,我们可能会为美国以及潜在的其他地区构建必要的基础设施和能力,尽管像我们所做的所有事情一样,我们会寻求利用技术来构建这些能力,使其效率大大高于 行业平均水平。建立这一基础设施和能力的决定将在我们的候选药物进一步进步后做出,并基于我们的
221
评估我们构建具有竞争优势的上述能力和基础设施的能力。临床数据、可寻址患者群体的规模、商业基础设施的规模、制造需求以及有关该行业如何积累价值的主要趋势都可能影响或改变我们的商业化计划。
制造业
我们利用并期望继续利用 合同开发和制造组织来生产药品和药品,以支持我们流水线内的资产。到目前为止,我们已经从第三方合同 制造商那里获得了我们候选药物的药物物质和药物产品。我们正在为我们的每一位候选药物开发供应链逐个项目基于我们的发展需要。
随着我们的发展,我们将继续重新评估生产能力,并可能建立内部制造。作为迈向内部制造的第一步,该公司正在确保在犹他州盐湖城建立一个设施,以建立临床前动物研究和早期人类临床试验的生产 能力。
知识产权
我们的知识产权重点是表型组学的产业化,这是一种新的组学数据类别,到目前为止我们已经应用了行业知识 继续构建和扩展各种其他尖端技术。此外,我们在工作过程中生成了算法、软件和统计见解。在新兴的科技药物发现领域,我们 寻求通过专利和商业秘密的结合来保护我们的创新,对于我们开发的每一项新技术或改进,我们都会考虑适当的知识产权保护过程。
我们的商业成功在一定程度上取决于我们是否有能力获得和维护对候选药物和我们未来的任何候选药物的专有保护 、新发现、产品开发技术和诀窍;在不侵犯、挪用或以其他方式侵犯他人专有权的情况下运营;以及防止他人侵犯、挪用或 以其他方式侵犯我们的专有权。我们的政策是通过提交或授权美国和外国专利以及与我们的专有技术、发明 和对我们业务的发展和实施非常重要的改进相关的专利申请等方法来保护我们的专有地位。我们还依靠商标、商业秘密、技术诀窍、持续的技术创新和许可机会的潜力来发展和保持我们的 专有地位。
我们相信开源科学的好处,相信开源数据共享为我们和整个社会带来价值。例如,我们已经发布了从我们的新冠肺炎平台得出的某些关键发现,条款旨在允许任何人使用这些数据,并希望这些数据将对抗击全球流行病有用 。我们还发布了一些世界上最大的开源生物数据集,RXRX系列,其条款允许广泛的学术和非商业用途。
专利
截至2021年1月,我们拥有42项已颁发的美国专利、34项未决的美国专利申请、24项未决的美国临时专利申请、2项未决的外国专利申请、6项未决的国际申请,我们独家许可了9项已颁发的美国专利、2项未决的美国专利
222
申请国外专利一百一十七件,国外专利申请十九件。这些专利分属全球79个不同司法管辖区的95个不同专利家族。
| • | 递归操作系统IP:我们的Recursion OS由多个专利所有系列涵盖,包括3项 美国专利、4项待决的美国临时申请、9项待决的美国非临时申请、5项待决的PCT申请和2项待决的外国专利申请。我们还奉行一项战略,在我们的整个流程中为较小的离散发明寻求专利保护 ,范围从实验设计、我们实验室内的操作、数据收集和分析(包括深度学习见解);我们与递归学习平台系统IP 相关的专利一般在2038年至2041年之间到期,不包括任何专利期调整或专利期延长。 |
| • | 在活体组学中:此外,通过收购Vium,我们获得了与InVivology相关的有效专利系列 ,其中包括39项已颁发的专利,涉及笼子设计、数据收集和数据分析,24项正在申请的美国非临时专利和1项正在申请的美国设计申请。我们与InVivology相关的专利一般在2035年至2040年之间到期,不包括任何专利期调整或专利期延长。 |
| • | 复合IP:我们的复合知识产权组合包括167项拥有和独家许可的专利 和申请,其中我们拥有20项美国临时专利申请、1项未决的国际申请,我们独家许可1项美国临时专利申请、9项美国专利、1项未决的美国专利申请、20项未决的外国专利申请和116项外国专利。我们的复合IP产品组合的进一步细分如下: |
| • | REC-2282:我们独家许可3项已颁发的美国专利、1项未决的美国专利申请、38项已颁发的外国专利,以及3项与OSIF的REC-2282相关的未决的外国专利申请。我们与REC-2282相关的许可专利一般在2027年至2036年之间到期,不包括任何专利期调整或专利期延长。 |
| • | REC-3599:我们拥有3项与我们的REC-3599候选产品相关的美国临时专利申请。 |
| • | REC-994:我们独家许可了2项美国专利、2项已颁发的外国专利和9项未决的外国专利申请,这些专利与我们的UURF候选REC-994产品相关。我们与REC-2282相关的许可专利一般在2035年至2036年之间到期,不包括任何专利期调整或专利期延长。 |
| • | REC-4881:我们独家授权武田REC-4881候选产品的3项美国专利、69项外国专利和5项未决的外国专利申请 。我们与REC-4881相关的许可专利一般在2027年至2032年之间到期,不包括任何专利期调整或专利期延长。 |
像我们这样的公司的专利地位通常是不确定的,涉及复杂的法律和事实问题。在美国和欧洲等国家,还没有出现关于生物技术领域专利中允许的权利要求范围的一致政策。其他国家的专利法和规则的变化,无论是通过立法、司法裁决或监管解释 ,都可能会削弱我们保护我们发明和执行我们知识产权的能力,更广泛地说,可能会影响我们知识产权的价值。特别是,我们是否有能力阻止第三方直接或间接地制造、使用、销售、提供销售、进口或以其他方式将我们的任何专利发明商业化,这在一定程度上取决于我们能否成功地获得、捍卫和实施涵盖我们的 技术、发明和改进的专利主张。对于许可的和公司所有的知识产权,我们不能确保我们的任何未决专利申请或我们未来提交的任何专利申请都将获得专利,也不能确保我们的任何现有专利或未来可能授予我们的任何专利在
223
保护我们的平台和候选药物以及用于制造它们的方法。此外,我们已颁发的专利以及未来可能颁发的专利可能不能保证我们有权 将我们的技术应用于我们平台候选药物的商业化。生物技术中的专利和其他知识产权领域是一个不断发展的领域,具有许多风险和不确定性,这可能会阻碍我们将候选药物和未来候选药物商业化,并实践我们的专有技术。
我们已颁发的专利以及 未来可能颁发的专利可能会受到挑战、缩小范围、规避或失效,这可能会限制我们阻止竞争对手营销相关平台或候选药物的能力,或者限制我们 对31个候选药物、未来候选药物和平台的专利保护期。此外,根据任何已颁发的专利授予的权利可能无法针对具有类似技术的竞争对手提供完整的保护或竞争优势。 此外,我们的竞争对手可能会独立开发类似的技术,其结果相似,但方法不同。出于这些原因,我们可能会在候选药物上展开竞争。此外,我们候选产品的开发、测试和监管审查所需的时间可能会缩短商业化后的有效专利保护时间。有关与我们的专有技术、发明、改进、平台和候选药物 相关的这一风险和其他风险,请参阅与我们的知识产权相关的风险因素和风险一节。
我们的商业成功在一定程度上还取决于不侵犯第三方的专有权。目前尚不确定颁发任何第三方专利是否会要求我们改变产品或流程的开发或商业战略,或者 是否需要获得许可或停止某些活动。我们违反任何许可协议或未能获得开发或商业化我们未来产品所需的专有权许可,可能会对我们产生不利影响。如果第三方 在美国准备和提交的专利申请也声称拥有我们拥有权利的技术,我们可能必须参与美国专利商标局的干扰或派生程序,以确定发明的优先权。有关更多 信息,请参阅与我们的知识产权相关的风险因素和风险。?
我们在美国的一些未决专利申请是临时专利申请。临时专利申请在我们提交一项或多项相关临时专利申请后的12 个月内提交非临时专利申请后,才有资格成为已获授权的专利。如果我们不及时提交任何非临时专利申请,我们可能会失去临时专利申请的优先权日期,以及临时专利申请中披露的发明的任何专利保护。虽然我们打算及时提交与我们的临时 专利申请相关的非临时专利申请,但我们无法预测任何此类专利申请是否会导致颁发为我们提供任何竞争优势的专利。
个别专利的期限取决于获得专利的国家的法律期限。在我们 提交的大多数国家/地区,专利期为自提交与该专利相关的非临时专利申请的最早日期起20年。然而,专利提供的实际保护在不同的情况下是不同的。逐个产品具体情况取决于许多因素,包括专利的类型、覆盖范围、与监管相关的延期的可用性、特定国家 的法律补救措施的可用性以及专利的有效性和可执行性,这些因素包括专利的类型、覆盖范围、与监管相关的延期的可用性、在特定国家的法律补救的可用性 以及专利的有效性和可执行性。在某些情况下,美国专利还可以获得专利期限调整(PTA),以补偿从美国专利商标局获得专利的延迟。在某些情况下,这样的专利协议可能会导致美国专利期从提交与美国专利相关的非临时专利申请的最早日期起延长20年以上。此外,在美国 ,涵盖FDA批准的药物的美国专利的期限也可能符合延长专利期限的资格,这允许恢复专利期限,以补偿在FDA监管审查过程中丢失的专利期 。
224
商标
截至2021年1月,我们的商标组合包括全球70多个注册商标或现行商标申请。此类投资组合 包括20个注册的外国商标、30个待处理的外国商标申请、11个注册的美国商标和9个待处理的美国商标申请,其中我们已在美国颁发了Recursion To和Recursion PharmPharmticals的商标。
商业秘密
除了我们的发明、候选药物和计划依赖专利保护之外,我们还依赖商业秘密、技术诀窍、保密协议和持续的技术创新来 发展和保持我们的竞争地位。例如,制造流程、专有化验、分析技术和流程的某些要素、通过临床经验获得的知识(如给药方法和患者的管理和管理方法)、计算生物算法以及相关流程和软件,均基于未公开 披露的未获专利的商业秘密和诀窍。尽管我们采取措施保护我们的专有信息和商业机密,包括通过与员工、顾问和顾问签订合同的方式,但这些协议可能会被违反,我们可能没有足够的补救措施来应对 任何违规行为。此外,第三方可以独立开发实质上同等的专有信息和技术,或以其他方式获取我们的商业秘密或披露我们的技术。因此,我们可能无法 切实保护我们的商业秘密。我们的政策是要求我们的员工、顾问、外部科学合作者、赞助研究人员和其他顾问在与我们开始雇佣或 咨询关系时执行保密协议。这些协议规定,在当事人与我方关系期间开发或向个人或实体披露的有关我方业务或财务的所有机密信息均应保密 ,除非在特定情况下,否则不得向第三方披露。就雇员而言,协议规定个人在受雇期间构思的所有发明, 与 有关或合理地能够或正在我们当前或计划中的业务或研发中使用的是我们的专有财产。此外,我们还采取其他适当的预防措施,例如物理和技术安全措施,以防止 我们的专有技术被第三方盗用。然而,这样的协议和政策可能会被违反,而我们可能没有足够的补救措施来弥补这类违规行为。有关与我们的 知识产权相关的风险的更多信息,请参阅与我们的知识产权相关的风险因素和风险。
政府监管
美国联邦、州和地方以及其他国家的政府当局对药品和生物产品的研究、 开发、测试、制造、质量控制、审批、标签、包装、储存、记录保存、促销、广告、分销、审批后的监控和报告、营销以及进出口等方面进行监管。 产品的研发、测试、制造、质量控制、审批、标签、包装、储存、记录保存、促销、广告、分销、审批后的监控和报告、营销以及药品和生物产品的进出口 。通常,在新药上市之前,必须获得大量证明其质量、安全性和有效性的数据,组织成每个监管机构特定的格式,提交审查并获得监管机构的批准。
美国药物开发
在美国,FDA根据“食品、药物和化妆品法案”(FDCA)对药品进行监管。药品还受其他联邦、州和地方法律法规的约束。获得监管批准并随后 符合适当的联邦、州、地方、
225
和国外的法律法规需要花费大量的时间和财力。在 产品开发流程、审批流程或上市后的任何时候,如果申请人不遵守适用的美国要求,可能会受到行政或司法制裁。这些制裁可能包括FDA拒绝批准待决申请、撤回批准、临床封存、无标题或警告函、产品召回或市场撤回、产品扣押、完全或部分暂停生产或分销、禁令、罚款、拒绝政府合同、恢复原状、 退货以及民事或刑事处罚等行为,这些制裁可能包括:FDA拒绝批准待决申请、撤销批准、临床封存、无标题或警告函、产品召回或市场撤回、产品扣押、全部或部分暂停生产或分销、禁令、罚款、拒绝政府合同、恢复原状、 退货以及民事或刑事处罚。任何机构或司法执法行动都可能对我们产生实质性的不利影响。
| • | 我们的候选药物被认为是小分子药物,必须通过新药申请( 或NDA)流程获得FDA的批准,然后才能在美国合法上市。这一过程通常包括以下内容:根据适用法规完成广泛的临床前研究,包括根据良好实验室操作规范(GLP)进行的研究; |
| • | 向FDA提交正在研究的新药或IND申请,该申请必须在人类 临床试验开始之前生效; |
| • | 在每项 试验开始之前,每个临床试验地点的独立机构审查委员会或IRB或伦理委员会批准; |
| • | 根据适用的IND法规、良好的临床实践或GCP要求以及其他与临床试验相关的法规进行充分和受控的人体临床试验,以确定针对每个建议适应症的研究产品的安全性和有效性的确凿证据; |
| • | 向FDA提交保密协议; |
| • | FDA在收到保密协议后60天内决定接受申请复审; |
| • | 令人满意地完成FDA对将生产药物的一个或多个制造设施的批准前检查,以评估符合cGMP要求的情况,以确保设施、方法和控制足以保持药物的特性、强度、质量和纯度; |
| • | FDA对产生支持NDA文件的数据的临床前研究和/或临床试验地点的潜在审计 ; |
| • | 在美国进行任何商业营销或销售该药物之前,FDA审查和批准NDA,包括考虑任何FDA顾问委员会的意见;以及 |
| • | 遵守任何审批后要求,包括实施风险评估和缓解策略(REMS)的潜在要求,以及进行审批后研究的潜在要求。 |
支持NDA 所需的数据是在两个不同的发展阶段生成的:临床前和临床。临床前和临床测试和审批过程需要大量的时间、精力和财力,我们不能确定是否会及时批准或根本不批准任何 当前和未来的候选药物。
临床前研究与工业
临床前开发阶段通常包括药物化学、配方和稳定性的实验室评估,以及支持后续临床试验的动物毒性评估研究。赞助商必须提交临床前研究的结果,连同
226
作为IND的一部分,向FDA提供生产信息、分析数据、任何可用的临床数据或文献以及建议的临床方案。IND是FDA授权给人类使用研究产品的请求,必须在人体临床试验开始前生效。
临床前研究 包括产品化学和配方的实验室评估,以及体外培养和动物研究,以评估不良事件的可能性,并在某些情况下建立治疗使用的理由。临床前 研究的实施受联邦法规和要求的约束,包括安全/毒理学研究的GLP法规。IND赞助商必须将临床前试验结果与生产信息、分析数据、任何 可用的临床数据或文献以及临床研究计划等一起提交给FDA,作为IND的一部分。提交IND后,可能会继续进行一些长期的临床前测试,例如生殖不良事件和致癌性的动物测试。IND在FDA收到后30天自动生效,除非在此之前FDA对一项或多项拟议的临床试验提出担忧或问题,并将试验搁置。在这种情况下,IND赞助商和FDA必须在临床试验开始之前解决任何悬而未决的问题。因此,提交IND可能不会导致FDA允许临床试验开始。
临床试验
临床开发阶段 涉及根据GCP 要求(包括要求所有研究对象就其参与任何临床试验提供知情同意书),在合格研究人员(通常是未受雇于试验赞助商或在试验赞助商控制下的医生)的监督下,向健康志愿者或患者使用研究产品。临床试验是在详细说明临床试验目标、给药程序、受试者选择和排除标准以及用于监测受试者安全性和评估疗效的参数的方案下进行的,这些方案包括: 临床试验目标、给药程序、受试者选择和排除标准以及用于监测受试者安全性和评估疗效的参数。每项协议以及对协议的任何后续修改都必须作为IND的 部分提交给FDA。此外,每项临床试验都必须由将进行临床试验的每个机构的IRB审查和批准,以确保参与临床试验的个人的风险降至最低 ,并且相对于预期的益处是合理的。IRB还必须批准必须提供给每个临床试验受试者或其法定代表人的知情同意书,并且必须监督临床试验直到完成。 还要求向公共注册机构报告正在进行的临床试验和已完成的临床试验结果。
希望在美国境外进行临床试验的赞助商 可以(但不需要)获得FDA的授权,根据IND进行临床试验。如果国外临床试验不是根据IND进行的,赞助商可以向FDA提交 临床试验的数据,以支持NDA。如果外国临床试验是根据《赫尔辛基宣言》(根据21 CFR 312.120(C)(4))中包含的伦理原则(包含1989年版的《宣言》)进行的,或者符合进行试验的外国监管机构的法律和法规,如欧洲药品管理局(EMA),以对人体提供更大的保护,且符合《全球药品采购协议》和《药品生产管理规范》的要求,则美国食品和药物管理局通常会接受不是根据IND进行的精心设计和实施的外国临床试验,该试验符合《赫尔辛基宣言》中包含的伦理原则(包括1989年版的《宣言》),或符合进行试验的外国监管机构的法律和法规,如欧洲药品管理局或欧洲药品管理局,以对人体提供更大的保护为准。而且国外的医学实践与美国是一致的。
在美国,临床试验通常分三个连续阶段进行, 称为第一阶段、第二阶段和第三阶段,可能会重叠。
| • | 第一阶段临床试验通常涉及少数健康志愿者或患病患者,他们最初使用单剂药物,然后使用多剂药物。(br}第一阶段临床试验通常涉及少量健康志愿者或患病患者,他们最初使用单剂药物,然后使用多剂药物。) |
227
| 候选人。这些临床试验的主要目的是评估药物的新陈代谢、药理作用、耐受性和安全性。 |
| • | 第二阶段临床试验涉及对受疾病影响的患者进行研究,以确定产生预期益处所需的剂量和给药时间表。同时,收集安全性和进一步的药代动力学和药效学信息,识别可能的不良反应和安全风险,并对疗效进行初步评估。 |
| • | 第三阶段临床试验通常涉及多个地点的大量患者,旨在提供必要的数据 ,以证明产品的预期用途有效性、使用安全性,并确定产品的总体收益/风险关系,并为产品审批提供充分的基础。这些试验可能包括 与安慰剂和/或其他对照治疗的比较。治疗的持续时间经常被延长,以模拟产品在营销过程中的实际使用。 |
批准后试验,有时被称为4期临床试验,是在最初的上市批准之后进行的。这些试验用于从预期治疗适应症患者的治疗中获得 其他经验。在某些情况下,FDA可能会强制执行4期临床试验,作为批准NDA的条件。
除其他信息外,详细说明临床试验结果的进展报告必须至少每年提交给FDA。赞助商还负责提交书面的IND安全报告,包括严重的和意想不到的可疑不良事件的报告,其他研究表明接触该药物对人类有重大风险的报告,来自动物或在 体外对人类受试者有重大风险的测试,以及与方案或研究人员手册中列出的测试相比,临床上严重疑似不良反应发生率的显著增加。
第一阶段、第二阶段和第三阶段临床试验可能不会在任何指定的时间内成功完成(如果有的话)。FDA或赞助商可以基于各种理由 随时暂停或终止临床试验,包括发现研究对象或患者面临不可接受的健康风险。同样,如果临床试验不是按照IRB的要求进行的,或者如果药物对患者造成了意外的严重伤害,IRB可以暂停或终止对其机构的临床试验的批准。 如果临床试验没有按照IRB的要求进行,则IRB可以暂停或终止对其机构的临床试验的批准。此外,一些临床试验由临床试验赞助商组织的 独立的合格专家小组监督,称为数据安全监测委员会或委员会。此组根据对试验中某些数据的访问权限 ,授权试验是否可以在指定检查点进行。
在临床试验的同时,公司通常会完成额外的动物安全性研究,还必须 开发有关药物化学和物理特性的额外信息,并根据cGMP要求最终确定商业批量生产产品的流程。由 制造工厂执行的制造流程必须能够持续生产我们的候选药物的高质量批次。此外,必须选择和测试适当的包装,并进行稳定性研究,以证明我们的候选药物 在标有标签的保质期内不会发生不可接受的变质。
保密协议审查流程
临床试验完成后,将对数据进行分析,以评估研究产品对于建议的 指示用途是否安全有效。临床前研究和临床试验的结果随后将作为NDA的一部分提交给FDA,以及建议的标签、化学和制造信息,以确保产品质量和其他相关数据。 简而言之,NDA是一项申请,要求批准该药物在美国销售一个或多个指定适应症,并且必须包含药物的安全性和有效性证明。
228
申请必须包括临床前研究和临床 试验的阴性和模棱两可的结果,以及阳性结果。数据可能来自公司赞助的临床试验,旨在测试产品使用的安全性和有效性,或者来自许多替代来源,包括研究人员发起的研究。要支持上市审批,提交的数据必须在质量和数量上足够,以确定研究产品的安全性和有效性,使FDA满意。在药物可以 在美国合法销售之前,必须获得FDA对NDA的批准。
根据修订后的处方药使用费法案(PDUFA),每个保密协议必须附有使用费 。FDA每年调整PDUFA用户费用。PDUFA还对每种上市的人类药物征收年度计划费。在某些情况下可以减免费用,包括免除小企业提交的第一个 申请的申请费。此外,被指定为孤儿药物的NDA不评估使用费,除非该产品还包括非孤儿适应症。
FDA在接受提交的所有NDA进行备案之前会对其进行审核,并且可能会要求提供更多信息,而不是接受NDA进行备案。 FDA必须在收到NDA后60天内做出是否接受NDA进行备案的决定。一旦提交的申请被接受,FDA就开始对NDA进行深入审查。根据FDA根据PDUFA达成的目标和政策 ,FDA有十个月的时间完成对新的分子实体NDA的初步审查并回应申请人,以及自指定进行优先审查的新的分子实体NDA的提交日期起计六个月。 自提交申请之日起,FDA有10个月的时间完成对新分子实体NDA的初步审查并对申请人做出回应。 指定用于优先审查的新分子实体NDA的提交日期起6个月。FDA并不总是满足其PDUFA标准和优先NDA的目标日期,而且FDA要求提供更多信息或澄清的请求往往会延长审查过程。
在批准NDA之前,FDA将对 新产品的生产设施进行审批前检查,以确定它们是否符合cGMP要求。除非FDA确定其制造工艺和设施符合cGMP要求,并足以确保产品在所要求的规格内持续生产,否则FDA不会批准该产品。FDA还可能审核临床试验的数据,以确保符合GCP要求。此外,FDA可能会将新药或药物产品的申请提交给咨询委员会(通常是由临床医生和其他专家组成的小组)审查、评估,并就是否应批准申请以及在什么 条件下(如果有)提出建议。FDA不受咨询委员会建议的约束,但它在做出批准决定时会考虑这些建议。FDA可能会重新分析临床试验数据,这可能会导致FDA和申请人在审查过程中进行广泛的 讨论。在FDA对NDA进行评估后,它将出具批准信或完整的回复信。批准函授权该药物的商业营销,并提供特定适应症的具体 处方信息。一封完整的回复信表明申请的审查周期已经结束,该申请将不会以目前的形式获得批准。一封完整的回复信通常描述 FDA确定的NDA中的所有具体缺陷。完整的回复信可能需要额外的临床数据、额外的关键3期临床试验和/或与 临床试验相关的其他重要且耗时的要求, 临床前研究和/或生产。如果发出了完整的回复信,申请人可以重新提交保密协议,解决信中确定的所有不足之处,或者撤回申请。即使提交了这样的 数据和信息,FDA也可能认定NDA不符合批准标准。从临床试验获得的数据并不总是决定性的,FDA对数据的解读可能与我们对相同数据的解读不同。
229
孤儿药物
根据《孤儿药品法》,FDA可以将用于治疗罕见疾病或疾病的药物或生物制品授予孤儿称号,这种疾病或疾病通常在美国影响不到200,000人,或者在美国影响超过200,000人,并且没有合理的预期在美国开发和提供治疗此类疾病或疾病的 产品的成本将从产品的销售中收回。(br}通常是指在美国影响不到200,000人或超过200,000人的疾病或疾病,并且没有合理的预期将从产品的销售中收回在美国开发和提供此类疾病或疾病的 产品的成本。
提交保密协议之前,必须申请孤儿药物名称 。在FDA批准孤儿药物指定后,FDA公开披露了治疗剂的身份及其潜在的孤儿用途。孤立药物指定不会在 中传递任何优势,也不会缩短监管审批流程的持续时间。
如果具有孤儿指定的产品随后获得fda对其具有此类指定的疾病或条件的第一次批准 ,则该产品有权获得孤儿药物独占权,这意味着fda在自批准之日起7 年内不得批准针对同一适应症销售同一药物的任何其他申请,除非在有限的情况下,例如通过更有效、更安全或对患者 护理或治疗做出重大贡献来表现出优于具有孤儿独占性的产品的临床优势。但是,竞争对手可能会获得针对同一适应症的不同产品或针对不同适应症的相同产品的批准,但这些产品可以在孤立适应症的标签外使用 。如果竞争对手在我们之前获得批准(根据FDA的定义 ),获得批准的是我们正在寻求批准的相同适应症,或者如果候选药物被确定包含在竞争对手的产品范围内(根据FDA的定义),则孤立药物独占性也可能在七年内阻止我们的产品获得批准。如果我们的一种指定为孤儿药物的产品获得了 比指定范围更广的适应症上市批准,则该产品可能无权获得孤儿药物独家经营权。欧盟的孤儿药物地位有类似的要求和好处,但不是完全相同的。
加快发展和审查计划
FDA有一个快速通道计划,旨在加快或促进审查符合特定标准的新药的过程。具体地说,如果新药旨在治疗严重或危及生命的疾病,并且临床前或临床数据表明有可能解决该疾病未得到满足的医疗需求,则有资格获得快速通道指定。快速通道指定既适用于该产品,也适用于该产品正在研究的特定适应症。 赞助商可以在获得NDA批准之前的任何时间请求FDA将该产品指定为快速通道状态,但最好不晚于NDA前与FDA的会议。
任何提交FDA上市的产品,包括快速通道计划,都可能符合FDA旨在加快开发和审查的其他类型计划的资格,例如优先审查和加速审批。任何治疗严重或危及生命的疾病的产品都有资格接受优先审查,如果获得批准,与现有疗法相比,它将在安全性和有效性方面提供显著改善 。
如果一种产品治疗了严重或危及生命的疾病,并且通常提供了比现有疗法更有意义的优势,那么它也有资格获得加速批准。此外,它还必须证明对合理可能预测临床益处的替代终点的影响,或对临床终点 的影响,该终点可以早于不可逆转的发病率或死亡率或IMM(合理地可能预测对IMM或其他临床益处的影响)进行测量。作为批准的一项条件,FDA可以要求获得加速批准的药物的赞助商在以下方面表现充分和良好-
230
受控的上市后临床试验。如果验证性上市后试验未能验证临床 益处或未显示足够的临床益处来证明与药物相关的风险是合理的,FDA可能会撤回药物审批或要求更改药物的标签适应症。如果FDA得出结论认为,被证明有效的药物只有在分销或使用受到限制的情况下才能安全使用,它可能会要求 它认为必要的上市后限制,以确保该产品的安全使用。
此外,如果一种药物单独或与一种或多种其他药物或生物制品联合用于治疗严重或危及生命的疾病,并且初步临床证据表明该产品可能在一个或多个临床重要终点显示出比目前批准的疗法有实质性改善,则该药物可能有资格被指定为 突破性疗法。突破性治疗指定的好处包括与快速通道指定相同的好处,以及FDA的密集指导,以确保有效的药物开发计划。快速通道指定、优先审查、加速批准和突破性治疗指定不会改变批准的标准,但可能会加快开发或批准过程。
审批后要求
新产品获得批准后,制造商和已批准的产品将继续受到FDA的监管,其中包括监控和记录要求、报告不良事件的要求以及遵守促销和 广告要求(其中包括限制推广用于未经批准的用途或患者群体的药物,称为非标签促销)、限制行业赞助的科学和教育活动 。虽然医生可能会开合法的药品用于标签外的用途,但制造商可能不会销售或推广这种用途。处方药宣传材料必须在首次使用时 提交给FDA。此外,如果药物有任何修改,包括适应症、标签或生产工艺或设施的更改,申请人可能需要提交并获得FDA对新的NDA或NDA补充剂的批准,这可能需要开发额外的数据或临床前研究和临床试验。
FDA还可以在批准上附加其他条件,包括对REMS的要求,以确保产品的安全使用。REMS可以包括用药指南、医生沟通计划或确保安全使用的要素,例如受限的 分发方法、患者登记表和其他风险最小化工具。批准或营销方面的任何这些限制都可能限制产品的商业推广、分销、处方或分发。产品审批可能会因不符合法规标准或在初始营销后出现问题而被撤回 。
如果没有遵守监管要求和标准,或者产品上市后出现问题,FDA可能会撤回批准。 如果后来发现产品存在以前未知的问题,包括未预料到的严重程度或频率的不良事件,或生产过程,或未能遵守法规要求,可能会导致修订批准的标签以添加新的安全信息;实施上市后研究或临床研究以评估新的安全风险,或根据REMS计划实施分销限制或其他限制。其他潜在的 后果包括:
| • | 限制产品的销售或制造,将产品完全撤出市场,或 产品召回; |
| • | 罚款、警告函或者暂停批准后的临床研究; |
| • | FDA拒绝批准待决申请或已批准申请的补充; |
| • | 暂停或者撤销产品批准; |
| • | 产品被扣押或扣留; |
231
| • | 拒绝允许产品进出口的; |
| • | 禁制令或施加民事或刑事处罚。 |
FDA对投放市场的产品的营销、标签、广告和促销进行严格监管。只能根据批准的适应症和批准的标签的规定推广药物。FDA和其他机构积极执行禁止推广标签外使用的法律和法规,被发现不当推广标签外使用的公司 可能会承担重大责任。
FDA对伴随性诊断的规定
一种治疗产品可能依赖于体外培养配对诊断,用于选择 对该疗法更有可能有效的患者。如果一个体外培养诊断对于治疗产品的安全和有效使用至关重要,如果制造商希望销售或分销此类诊断作为辅助诊断使用,则FDA将要求单独批准或批准诊断作为治疗产品的辅助诊断。根据FDA的指导,在药物临床试验中用于做出治疗决策的未经批准或未批准的配套诊断设备通常将被视为研究医疗设备,除非该设备已被批准或批准用于预期用途。如果用于做出关键的治疗决策,如患者选择,根据FDA的研究设备豁免(IDE)法规,诊断设备通常将被视为重大风险设备。诊断设备的赞助商将被要求遵守涉及研究诊断设备的临床研究的IDE规定。根据指南,如果一种诊断设备和一种药物要一起研究以支持它们各自的批准,如果试验同时满足IDE法规和IND法规的要求,这两种产品可以在 同一临床试验中进行研究。指南规定,根据临床试验方案、研究产品和涉及的受试者的详细情况,赞助商可以单独提交IDE(例如,如果药物已获得FDA批准并与其批准的标签一致使用),或同时提交IND和IDE。
寻求FDA对AN的批准/清除体外培养配套诊断需要售前 通知(也称为510(K)许可),或需要售前批准,或PMA,或该诊断的从头分类。伴随诊断的审查包括与FDA设备和放射健康中心协调审查。
510(K)审批流程
为获得510(K)许可,需向FDA提交上市前通知,证明建议的 装置实质上等同于先前批准的510(K)装置或1976年5月28日之前处于商业分销状态的装置,FDA尚未要求提交PMA申请。FDA的510(K) 审批过程可能需要3到12个月的时间,从申请提交到FDA提交之日起算,但如果FDA要求提供更多信息等原因,可能需要更长的时间。在某些情况下,FDA可能要求临床数据 支持实质上的等效性。在审查上市前通知提交时,FDA可能会要求提供更多信息,这可能会显著延长审查过程。尽管符合所有这些要求 ,但始终无法保证许可。
设备获得510(K)许可后,对设备进行的任何后续修改,如果 可能显著影响其安全性或有效性,或会对其预期用途造成重大改变,则需要新的510(K)许可或需要PMA。此外,FDA可能会对行业要求进行重大更改, 包括哪些设备有资格获得510(K)许可,这可能会对流程产生重大影响。
232
从头分类过程
如果一种新的医疗设备因为无法识别与其基本等效的谓词 设备而不符合510(K)上市前通知流程,则该设备自动被归类为III类。1997年的《食品和药物管理局现代化法案》(Food And Drug Administration Monization Act)为低到中等风险的医疗设备建立了一条不同的进入市场的途径 这些医疗设备由于缺少谓词设备而被自动归入III类,这一过程被称为评估自动III类指定的请求,或从头开始分类过程。此流程 允许其新型设备被自动归类为III类的制造商根据设备呈现低或中等风险来请求将其医疗设备降级为I类或II类,而不是 要求提交和批准PMA。如果制造商寻求重新分类为II类,则制造商必须包括一份特殊控制建议草案,该草案对于合理保证医疗器械的安全性和 有效性是必要的。如果FDA确定合法上市的适用于510(K)的谓词设备,或确定该设备不是低到中等风险并需要PMA,或者一般控制不足以控制风险且无法开发特殊控制,则FDA可能会拒绝重新分类申请。
获得FDA的营销授权、从头开始降低分类或批准医疗器械是昂贵且不确定的,可能需要数年时间,通常需要重要的科学和临床数据。
PMA工艺
PMA过程,包括临床和非临床数据的收集,以及提交给FDA并由FDA审查,可能需要几年或更长时间。申请人必须准备并向FDA提供设备的安全性和有效性的合理保证,包括有关设备及其组件的 有关设备设计、制造和标签等方面的信息。PMA申请需交纳申请费。此外,医疗器械的PMAS通常必须包括广泛的临床前和充分且控制良好的临床试验的结果 ,以确定该设备对于寻求FDA批准的每个适应症的安全性和有效性。特别是,对于诊断,申请人必须证明 该诊断产生了可重现的结果。作为PMA审查的一部分,FDA通常会检查制造商的设施是否符合质量体系法规(QSR),该法规规定了广泛的测试、控制、 文档以及其他质量保证和GMP要求。
其他美国监管事项
| • | 我们目前和未来与医疗保健提供者、第三方付款人、客户和其他人的安排可能会使我们面临广泛适用的欺诈和滥用以及其他医疗法律法规,这可能会限制我们研究、销售、营销和分销我们 获得市场批准的任何产品的业务或财务安排和关系。可能影响我们运营能力的适用的联邦、州和外国医疗保健法律和法规包括但不限于:联邦反回扣法规,规定任何人,包括处方药或医疗器械制造商(或代表其行事的一方),在知情和故意的情况下索取、接受、提供或支付任何旨在诱导或奖励转诊的报酬,包括购买、推荐、订购或处方特定药物,均属违法。 可根据联邦医疗保健支付这些报酬。 该法规规定,任何人,包括处方药或医疗器械制造商(或代表其行事的一方),明知并故意索取、接受、提供或支付任何旨在诱导或奖励转诊的报酬,包括购买、推荐、订购或处方特定药物,均属违法。此外,ACA(定义如下)规定,政府可以断言 包括因违反联邦反回扣法规而产生的物品或服务的索赔 根据民事虚假索赔法的目的构成虚假或欺诈性索赔; |
233
| • | 联邦虚假申报法,包括可由普通公民通过民事举报人或刑事诉讼强制执行的《民事虚假申报法》和民事罚款,禁止个人或实体在知情的情况下向联邦政府提出或导致向联邦政府提交虚假或欺诈性的付款索赔,或 通过虚假陈述来避免、减少或隐瞒向联邦政府支付资金的义务,和/或将其排除在联邦医疗保健计划之外和/或对参与的各方进行处罚。 该法案可由普通公民通过民事诉讼强制执行。 民事虚假索赔法案禁止个人或实体在知情的情况下向联邦政府提出或导致向联邦政府提出虚假或欺诈性的付款要求,和/或将其排除在联邦医疗保健计划之外和/或对参与方施加惩罚。 |
| • | 1996年的联邦健康保险携带和责任法案,或HIPAA,除其他事项外,禁止执行 或试图执行诈骗任何医疗福利计划的计划,或作出与医疗保健事项有关的虚假陈述; |
| • | 经《健康信息技术促进经济和临床健康法案》修订的HIPAA及其实施条例还对医疗保险计划、医疗信息交换所、某些医疗保健提供者及其各自的业务伙伴等覆盖实体施加义务,包括强制性合同条款, 保护个人可识别健康信息的隐私、安全和传输; |
| • | 联邦医生支付阳光法案要求根据Medicare、Medicaid或Children‘s Health Insurance Program支付费用的承保药品、设备、生物制品和医疗用品的适用制造商每年向医疗保险和医疗补助服务中心(CMS)报告有关向医生和教学医院支付某些款项和其他价值转移的信息,以及关于医生及其直系亲属持有的所有权和投资利益的信息;以及 |
| • | 类似的州和外国法律法规,例如可能适用于 销售或营销安排以及涉及由非政府第三方付款人(包括私营保险公司)报销的医疗项目或服务的索赔的州反回扣和虚假索赔法律,州法律要求生物技术公司 遵守生物技术行业的自愿合规指南和联邦政府颁布的相关合规指南;州和地方法律要求药品制造商报告与 向医生和其他医疗保健提供者或营销支出的付款和其他价值转移有关的信息,并要求其销售代表注册;州法律要求生物技术公司报告某些药品的定价信息;州和外国法律在某些情况下管理健康信息的隐私和安全,其中许多法律在很大程度上彼此不同,并且往往不会被HIPAA先发制人,因此 使合规工作复杂化。 |
定价和返点计划还必须符合美国1990年《综合预算调节法》的医疗补助返点要求,以及ACA(定义如下)的最新要求。如果向总务署联邦供应时间表的授权用户提供产品,则适用其他法律和 要求。制造、销售、促销和其他活动也可能受到联邦和州消费者保护和不正当竞争法律的约束。此外,药品和/或医疗器械 产品的分销还需遵守其他要求和法规,包括旨在防止未经授权销售药品和/或医疗器械产品的广泛记录保存、许可、存储和安全要求。产品 必须符合美国《毒物预防包装法》中适用的儿童安全包装要求以及其他适用的消费者安全要求。
如果不遵守这些法律或法规要求中的任何一项,公司将面临可能的法律或法规行动。根据 情况,未能满足适用的法规要求可能会导致重大的民事、刑事和行政处罚,包括损害赔偿,
234
罚款、交出、监禁、被排除在政府资助的医疗项目(如Medicare和Medicaid)之外、诚信监督和报告义务、合同 损害、声誉损害、利润减少和未来收益、禁令、召回请求、扣押产品、完全或部分暂停生产、拒绝或撤回产品批准或拒绝允许公司签订供应合同(包括政府合同)。
美国专利期恢复与市场排他性
根据FDA批准未来候选药物的时间、期限和细节,我们的一些美国专利可能有资格根据《哈奇-瓦克斯曼法案》(Hatch-Waxman Act)获得有限的 专利期延长。“哈奇-瓦克斯曼法案”(Hatch-Waxman Act)允许恢复最长五年的专利期,作为对在产品开发和FDA监管审查过程中失去的专利期的补偿。但是,专利期 恢复不能将专利的剩余期限从产品批准之日起总共延长14年。专利期恢复期一般为 IND的生效日期或专利的发布日期(以较晚的为准)与NDA的提交日期加上NDA的提交日期或专利的发布日期(以较晚的为准)之间的时间的一半,但审查期限会减少申请人未进行尽职调查的任何时间(以较晚的为准)。只有一项适用于批准的药物、使用方法或制造方法的专利有资格延期 延期申请必须在专利到期前提交。美国专利商标局与FDA协商,审查并批准任何延长或恢复专利期的申请。在未来, 如果我们的产品获得fda批准,我们可以申请恢复我们目前拥有或许可的专利的专利期,包括有资格延长专利期的产品,以延长其当前到期日之后的专利寿命。, 取决于临床试验的预期长度和提交相关保密协议所涉及的其他因素。欧洲和某些其他司法管辖区也有类似的规定,以延长涵盖经批准的 药物的专利期限。我们可以在任何司法管辖区为我们已颁发或许可的任何专利申请延长专利期;但是,不能保证包括美国FDA在内的适用当局会同意 我们对是否应批准延长以及延长的期限(如果批准)的评估。
FDCA中的市场排他性条款还可能延迟某些申请的提交或审批。FDCA向第一个获得NCE保密协议 批准的申请者提供为期五年的美国境内非专利营销专营权。如果FDA以前没有批准过任何其他含有相同活性部分的新药,那么一种药物就是NCE,活性部分是负责药物物质作用的分子或离子。在排他性 期间,FDA可能不接受另一家公司为该药物的仿制版本提交的简化新药申请(ANDA)或505(B)(2)保密协议(NDA)进行审查,但申请人不拥有或拥有合法的参考批准所需的所有 数据的权利。但是,如果申请包含专利无效或不侵权的证明,可以在四年后提交。如果FDA认为申请人进行或赞助的新的临床研究(生物利用度研究除外)对于批准 申请至关重要,则FDCA还为NDA、505(B)(2)NDA或现有NDA的补充提供三年的营销专营权,例如,现有药物的新适应症、剂量或强度。这项为期三年的专营权仅涵盖与新的临床研究相关的使用条件,并不禁止FDA批准含有原始活性物质的 药物的ANDA。五年和三年的专营权不会推迟提交或批准完整的保密协议。然而,提交完整的保密协议的申请人将被要求进行或获得参考所有 所有临床前研究和充分和良好控制的临床试验的权利,这些试验是证明安全性和有效性或自行生成此类数据所必需的。
235
欧盟药物开发
与美国类似,欧盟的临床前和临床研究的各个阶段都受到严格的监管 控制。尽管欧盟临床试验指令2001/20/EC试图协调欧盟临床试验监管框架,为欧盟临床试验的控制和授权制定了共同规则,但欧盟成员国以不同的方式调换和应用了该指令的规定。这导致了成员国制度的重大变化。在现行制度下,在启动临床试验之前,必须在欧盟 每个国家批准,在这些国家中,试验将由两个不同的机构进行:国家主管机构、NCA和一个或多个道德委员会(ECs)。根据现行制度,在临床试验期间发生的所有疑似被调查药物的意外严重不良反应都必须向发生这些反应的成员国的国家药品监督管理局和欧洲药品监督管理局报告。
欧盟临床试验立法目前正在进行过渡,主要目的是协调和简化临床试验授权,简化不良事件报告程序,改善临床试验的监督,并增加其 透明度。最近颁布的欧盟第536/2014号临床试验条例确保了在欧盟进行临床试验的规则将是相同的。同时,临床试验指令2001/20/EC继续管理在欧盟进行的所有临床试验 。
欧盟药品审查和批准
在由28个欧盟成员国和三个欧洲自由贸易联盟国家(挪威、冰岛和列支敦士登)组成的欧洲经济区(EEA),医药产品只有在获得营销授权(MA)后才能商业化。有两种类型的营销授权。
| • | 共同体MA由欧盟委员会根据欧洲药品管理局人用药品委员会(CHMP)的意见,通过集中程序颁发,并在整个欧洲经济区有效。对于某些类型的产品,如生物技术药品、孤儿药品、基因疗法、体细胞疗法或组织工程药物等高级治疗药物,以及含有用于治疗艾滋病毒、艾滋病、癌症、神经退行性疾病、糖尿病、自身免疫和其他免疫功能障碍以及病毒性疾病的新活性物质的医药产品,必须进行集中管理。对于含有EEA尚未授权的新活性物质的产品,或构成重大治疗、科学或技术创新的产品,或符合欧盟公共卫生利益的产品,集中化程序是可选的。 |
| • | 国家MA由欧洲经济区成员国的主管当局颁发,仅覆盖其各自的 领土,适用于不属于集中程序强制范围的产品。如果产品已被授权在欧洲经济区的一个成员国进行营销,则该国家MA可以通过相互认可程序在另一个成员国 获得认可。如果该产品在申请时没有在任何成员国获得国家MA,它可以通过分散的程序在不同的成员国同时获得批准。根据权力下放程序,向寻求MA的每个成员国的主管当局提交一份相同的档案,申请人选择其中一个作为参考成员国,或RMS。RMS的主管当局 准备评估报告草案、产品特性概要草案或SOPC以及标签和包装传单草案,并将其发送给其他成员国(指相关成员国)以供其 批准。如果有关成员国基于对公众健康的潜在严重危害没有对评估、SOPC、标签或包装提出异议 |
236
| 经RMS提议,该产品随后在所有成员国(即RMS和相关成员国)获得国家MA。 |
根据上述程序,在授予MA之前,EMA或欧洲经济区成员国主管当局根据有关产品质量、安全性和有效性的科学标准,对产品的风险-效益平衡进行评估。与美国专利期-恢复类似,补充保护证书(SPC)是欧洲专利权 最长五年的延伸。SPC适用于特定的制药产品,以弥补由于这些产品在获得监管市场批准之前需要进行漫长的测试和临床试验而失去的专利保护。
承保和报销
我们产品的销售将 在一定程度上取决于我们的产品将在多大程度上由第三方付款人承保,如政府医疗计划、商业保险和托管医疗机构。与第三方付款人 新批准产品的承保和报销相关的不确定性很大。例如,在美国,有关新产品报销的主要决定通常由CMS做出。CMS决定新产品是否以及在多大程度上将根据联邦医疗保险(Medicare)承保和报销,而私人第三方付款人通常在很大程度上遵循CMS关于承保和报销的决定。然而,对药品的覆盖和报销没有统一的政策。因此, 有关我们任何产品的承保范围和报销金额的决定将在逐个付款人基础。
越来越多的第三方付款人要求制药公司向他们提供标价的预定折扣,并挑战医疗产品的 价格。此外,这些付款人越来越多地挑战价格,检查医疗必要性,审查候选药物的成本效益。在获得新批准药品的承保和报销方面, 可能会出现特别严重的延误。第三方付款人可能会将覆盖范围限制到已批准清单(称为处方清单)上的特定候选药物,该清单可能不包括FDA批准的特定适应症的所有 药物。我们可能需要进行昂贵的药物经济学研究,以证明我们产品的医疗必要性和成本效益。因此,承保范围 确定过程通常是一个耗时且昂贵的过程,需要我们分别为每个付款人提供使用我们产品的科学和临床支持,但不能保证获得承保范围和足够的报销 。
此外,配套诊断测试需要单独承保和报销,并且除了 其配套药品或生物制品的承保和报销之外。适用于药品或生物制品的获得保险和报销的类似挑战也将适用于伴随诊断。
此外,在大多数外国,药品的拟议定价必须获得批准,才能合法上市。管理 药品定价和报销的要求因国家/地区而异。例如,欧盟为其成员国提供了各种选择,以限制其国家医疗保险系统提供报销的医疗产品的范围,并控制供人使用的医疗产品的价格。成员国可以批准医药产品的具体价格,也可以对将医药产品投放市场的公司的盈利能力采取直接或间接控制制度 。不能保证任何对药品实行价格控制或报销限制的国家/地区都会允许对我们的任何 产品进行优惠的报销和定价安排。从历史上看,在欧盟推出的产品并不遵循美国的价格结构,通常价格往往会低得多。
237
医疗改革
2003年的《联邦医疗保险处方药、改进和现代化法案》(MMA)设立了联邦医疗保险D部分计划,为联邦医疗保险受益人提供自愿的处方药福利。根据D部分,联邦医疗保险受益人可以参加由私人实体提供的处方药计划,这些实体提供门诊处方药的保险。与联邦医疗保险A部分和B部分不同,D部分 覆盖范围不是标准化的。虽然所有联邦医疗保险药物计划必须至少提供联邦医疗保险设定的标准承保水平,但D部分处方药计划发起人不需要为所有承保的D部分药物支付费用,每个药物计划可以 制定自己的药物处方,以确定它将覆盖哪些药物以及覆盖的级别或级别。但是,D部分处方药处方必须包括每个治疗类别和覆盖的D部分药物类别中的药物,但不一定 每个类别或类别中的所有药物。D部分处方药计划使用的任何处方都必须由药房和治疗委员会开发和审查。政府支付处方药的部分费用可能会增加对我们获得上市批准的产品的需求 。但是,D部分处方药计划涵盖的我们产品的任何协商价格都可能低于我们可能获得的价格。此外,虽然MMA只适用于医疗保险受益人的 药品福利,但私人第三方付款人在设置自己的付款率时通常会遵循医疗保险覆盖政策和支付限制。
美国政府、州立法机构和外国政府对实施成本控制计划表现出极大的兴趣,以 限制政府支付的医疗成本的增长,包括价格控制、报销限制和用仿制药替代品牌处方药的要求。例如,经2010年《医疗保健和教育和解法案》(或统称ACA)修订的2010年《患者保护和平价医疗法案》(Patient Protection And Affordable Care Act)获得通过,这极大地改变了政府和私营保险公司为医疗保健提供资金的方式,并对美国制药业产生了重大影响 。ACA包含的条款可能会通过以下方式降低药品的盈利能力:增加Medicaid计划报销药品的返点、将Medicaid返点扩大到Medicaid Managed Care 计划、对某些Medicare Part D受益人提供强制性折扣,以及根据制药公司在联邦医疗保健计划的销售份额计算的年费。医疗补助药品退税计划要求制药商 与美国卫生与公众服务部(HHS)部长签订并生效国家退税协议,作为各州获得制造商提供给医疗补助患者的门诊药物的联邦匹配资金的条件。ACA对医疗补助药品退税计划做出了几项改变,包括增加制药商的退税责任,将大多数品牌处方药的最低基本医疗补助退税从制造商平均价格的15.1%(br})提高到AMP的23.1%,并增加了品牌产品固体口服剂型的延长线(即新配方,如缓释剂)的新退税计算, 以及 修改AMP的法定定义可能会影响其返点责任。ACA还通过要求制药商为医疗补助 管理的医疗保健使用支付退款,以及通过扩大有资格享受医疗补助药物福利的潜在人口,扩大了受药品退税影响的医疗补助使用范围。此外,对于根据Medicaid或Medicare Part B计划获得联邦补偿或直接销售给美国 政府机构的药品,制造商必须向有资格参与340B药品定价计划的实体提供折扣。给定产品所需的340B折扣是根据制造商报告的AMP和医疗补助返点金额计算的。
ACA的一些条款尚未实施,ACA的某些方面受到了司法和国会的挑战,特朗普政府最近为废除或取代ACA的某些方面所做的努力也是如此。自2017年1月以来,特朗普总统签署了两项行政命令和其他指令,旨在推迟ACA某些条款的实施,或以其他方式规避医疗保险的一些要求
238
由ACA授权。与此同时,国会已经考虑了废除或废除并取代全部或部分ACA的立法。虽然国会还没有通过全面废除 立法,但已经通过了两项影响ACA下某些税收实施的法案。2017年12月22日,特朗普总统签署了新的联邦税收立法,通常被称为减税和就业法案,或税法, 其中包括一项条款,从2019年1月1日起废除ACA对某些个人实施的基于税收的分担责任付款,这些个人未能在一年的全部或部分时间内保持合格的医疗保险 。2018年1月22日,特朗普总统签署了一项关于2018财年拨款的持续决议,该决议推迟了某些条款的实施。包括对某些高成本雇主赞助的保险计划征收的所谓凯迪拉克税,根据市场份额向某些医疗保险提供商征收的年费,以及对非免税医疗器械征收的医疗器械消费税。2018年两党预算法案(BBA)等修订了ACA,自2019年1月1日起生效,以缩小大多数联邦医疗保险(Medicare)D部分药物计划的覆盖缺口。2018年12月,CMS发布了一项新的最终规则,允许根据ACA风险调整计划对某些符合ACA资格的健康计划 和医疗保险发行商进行进一步的收款和支付,以回应联邦地区法院关于CMS确定此风险调整的方法的诉讼结果。2018年12月14日,德克萨斯州一名地区法院法官裁定,ACA整体违宪,因为作为税法的一部分,国会废除了个人强制令。得克萨斯州地区法院法官, 以及特朗普政府和CMS, 表示,在对裁决提出上诉之前,裁决不会立即生效,目前尚不清楚这一裁决、随后的上诉以及其他废除和取代ACA的努力将如何影响ACA。
自ACA颁布以来,美国还提出并通过了其他立法修改。这些变化包括从2013年4月1日起将向提供者支付的医疗保险总金额削减 每财年最高2%,由于随后的立法修正案,这一削减将持续到2029年,除非国会采取额外行动。2013年1月,奥巴马总统签署了2012年《美国纳税人救济法》(American纳税人救济法),其中包括减少向几家医疗服务提供者支付的医疗保险,并将政府向提供者追回多付款项的诉讼时效从 三年延长至五年。这些新法律可能会导致医疗保险和其他医疗保健资金的进一步减少,如果获得批准,这可能会对我们药品的客户以及我们的财务运营产生实质性的不利影响。
此外,政府最近加强了对药品制造商为其销售的 产品定价方式的审查,这导致了几次国会调查,并提议并颁布了联邦和州立法,这些立法旨在提高产品定价的透明度,审查定价与 制造商患者计划之间的关系,以及改革药品的政府计划报销方法。例如,在联邦一级,特朗普政府2019年和2020财年的预算提案包含可能在预算过程或其他未来立法中颁布的进一步药品价格 控制措施,例如,允许联邦医疗保险D部分计划谈判联邦医疗保险B部分下某些药物的价格的措施,允许一些 州根据医疗补助谈判药品价格,以及取消低收入患者仿制药的成本分担。此外,特朗普政府2019年和 2020财年的预算提案包含进一步的药品价格控制措施,这些措施可能会在预算过程或其他未来立法中颁布,例如,包括允许联邦医疗保险D部分计划谈判联邦医疗保险B部分下某些药物的价格的措施,允许一些州根据医疗补助谈判药品价格,以及取消低收入患者仿制药的成本分担。此外,特朗普政府发布了一份降低药品价格和降低自付药品成本的蓝图,其中包含增加制造商竞争、提高某些联邦医疗保健计划的谈判力的额外建议, 激励 制造商降低其产品的标价,并降低消费者支付的药品自付成本。尽管其中一些
239
和其他措施可能需要额外授权才能生效,国会和特朗普政府都表示将继续寻求新的立法和/或 行政措施来控制药品成本。在州一级,立法机构越来越多地通过立法并实施旨在控制药品和生物制品定价的法规,包括价格或患者 报销限制、折扣、对某些产品准入的限制以及营销成本披露和透明度措施,在某些情况下,旨在鼓励从其他国家进口和批量购买。
战略协议
为了实现我们的使命,我们 与领先的生物技术公司、制药公司和学术研究机构合作,利用我们的发现技术确定新的疗法并解开生物学洞察力。我们的合作努力主要有两种形式: i)Discovery Platform Partnership和ii)基于资产的协作。
发现平台合作伙伴关系
我们已经并可能在未来与第三方合作,广泛探索不同的疾病领域(例如,纤维化、神经科学、肿瘤学、免疫学和炎症),以确定潜在的治疗方法。我们还可以探索公共资产类型战略,将地图中的搜索结果授权给合作伙伴。虽然到目前为止,我们的合作伙伴关系主要集中在小分子研究上,但未来的合作伙伴关系可能会扩展到新的治疗方式,包括大分子、基因疗法和细胞疗法。
每个合作伙伴的目标 都是创建治疗学,但方法可能有多种形式:
| • | 新疗法。在没有任何假定目标假设的情况下,我们可以通过快速评估大型(成百上千到数十万)化合物库以及由我们合作伙伴的主题专业知识提供信息的现有或从头开始的疾病模型来识别 差异化疗法。 |
| • | 新目标。通过在我们的平台上分析不同的生物扰动(例如,遗传的、可溶的 因素),我们可能能够识别新的可用药靶点,然后我们可以与合作伙伴一起利用这些靶点来产生候选治疗药物。 |
拜耳
2020年8月,我们与拜耳股份公司(Bayer AG)签订了为期五年的研究合作和选项协议-拜耳协议(Bayer Agreement),根据该协议,我们和拜耳可以启动十多个与肺、肝脏和心脏等多个器官系统纤维化相关的研究项目。根据协议,我们从我们的专有库贡献了大约190,000个化合物,拜耳从其专有库贡献了大约500,000个化合物,并将在整个合作过程中贡献科学专业知识。对于每个研究项目,我们和拜耳将共同拥有该项目过程中产生的项目成果的知识产权,但受使用方面的某些限制,双方 向对方授予全球范围内的、非独家的、免版税的许可,但无权根据其权利、所有权和利益对该项目产生的知识产权和专有技术以及某些背景知识产权和专有技术进行再许可。以及所贡献的库和其中的知识产权 ,以使另一方能够履行其在研究项目项目计划下的任务和义务所必需的范围内。作为协议的一部分,我们收到了3000万美元的预付技术访问费。
在拜耳协议期限内,禁止我们使用我们的专有方法进行研究和开发活动 化合物 管理,高通量
240
筛查实验室、数据分析算法、高维表型和其他分析、工程基础设施以及协作之外的数据库(单独或与纤维化领域的 第三方一起)。
在每个研究项目下,我们将与拜耳合作开发与纤维化疾病相关的筛查假设和适用于筛查化合物的生物学模型,以确定潜在的开发候选者。拜耳可能会通过确定符合特定标准的开发候选者来行使某些期权。 根据每个此类独家许可,我们将获得期权行使费,并有可能获得超过1亿美元的进一步开发和商业里程碑以及分级特许权使用费。
如果拜耳在 指定时间内未就开发候选项目行使选择权或以其他方式中止研究项目,我们可以行使选择权与拜耳真诚谈判,以获得拜耳根据研究项目开发的任何主导系列或开发候选项目的权益获得独家许可,以及获得拜耳背景知识产权项下的非独家许可,以便我们使用与该等化合物相关的项目成果。
该协议包含惯常的终止条款。截至本招股说明书发布之日,我们和拜耳尚未签订任何销售线索系列或 候选开发许可协议。
赛诺菲-Genzyme
2016年4月,我们与Genzyme Corporation或Sanofi-Genzyme达成了一项协议,该公司管理着一项 多年的研究合作,根据该合作,各方将合作,使用我们的内部遗传病模型,从赛诺菲-Genzyme提供的一个小型化合物库中确定罕见遗传病的候选药物。
根据协议,赛诺菲-Genzyme 有权开发针对任何新标识的产品。
基于资产的协作
除了NCE,递归地图还可能发现第三方拥有或控制的已知化学实体的新用途。在这种情况下,我们 可能会授予这些资产的权利,以便在内部推进这些计划。以下是我们的四个临床阶段计划的基础上的四个这样的授权许可协议。
REC-994:犹他大学研究基金会协议
2016年2月,我们与犹他大学研究基金会(UURF)签订了修订和重新签署的许可协议,根据该协议, 我们获得了某些专利下的独家许可和某些专有技术下的非独家许可,分别由UURF控制并与药物 tempol或REC-994相关,以在全球制造、制造、使用、提供销售、销售、进口和分销含有REC-994的产品,用于治疗脑腔狭窄 作为对许可权的部分对价,我们发行了我公司的UURF股权。此外,我们同意向UURF补偿与 许可专利权的申请、维护和起诉相关的特定部分费用。修订和重新签署的许可协议将于逐个国家/地区根据最后一个到期的适用国家专利权范围内的专利。如果我们停止在商业上努力开发或 商业化许可的产品或服务,或者我们的破产或资不抵债,UURF可能会终止我们未治愈的实质性违约的协议。
241
REC-2282:俄亥俄州立创新基金会 许可内
2018年12月,我们与俄亥俄州立创新基金会(Osif)签订了独家许可协议,根据该协议,我们获得了某些专利项下的独家、可再许可、不可转让、有版税的独家许可,以及某些专有技术项下的全额、免版税、非独家许可 ,这些许可均由Osif控制,并与泛组蛋白去乙酰化酶抑制剂OSU-HDAC42或REC-2282相关。Osif还向我们分配了某些资产,与名为AR-42的药物组合物有关。OSIF保留使用的权利,并允许其他学术、非营利和政府机构将许可的知识产权用于研究、非商业和教育目的。未经我们事先书面同意,OSIF不得出于任何临床目的而执业、已执业或转让此类保留权利,除非在许可协议签订时完成 项现有临床试验。我们正在开发用于治疗NF2的REC-2282,并正在使用我们的平台评估该化合物在其他 疾病状态中的效用。
根据协议,我们必须使用商业上合理的努力将授权产品商业化,并要求 在协议签署后两年内达到某些尽职调查里程碑,包括启动临床试验。许可协议还受 政府的某些权利和法规的限制和约束,包括《贝赫-多尔法案》(Bayh-Dole Act)。
作为许可证的对价,我们向Osif支付了200万美元的预付款, 有义务向Osif支付总计高达2000万美元的某些里程碑,以及授权产品净销售额的个位数中位数版税。此外,我们还欠二期临床试验前任何非特许权使用费再许可费用的25%或在二期临床试验开始后此类再许可费用的15%,前提是里程碑付款可抵免这些再许可费用 。截至本招股说明书发布之日,我们尚未向OSIF支付任何里程碑或特许权使用费。
协议 在许可专利内的最后一个有效权利要求到期时到期。我们可以提前90天书面通知OSIF终止本协议。任何一方均可提前60天书面通知终止协议,原因是另一方未治愈、重大违约或另一方破产或资不抵债。
REC-3599:Chromaderm 许可协议
2019年12月,我们与Chromaderm,Inc.或Chromaderm签订了一项许可协议,根据Chromaderm可能控制的某些专有技术和未来专利,我们获得了 独家的、可再许可的全球许可,用于开发、生产和商业化含有Ruboxistaurin的产品,Ruboxistaurin是一种蛋白激酶C的抑制剂,用于治疗、预防和/或诊断皮肤过度色素沉着状况或疾病以外的所有用途。Chromaderm从礼来公司获得了Ruboxistaurin开发、商业化和制造所需的某些知识产权的独家许可,并开发了某些额外的知识产权。Chromaderm保留使用 许可的知识产权来履行与我们签订的供应和制造协议项下的义务的权利,Chromaderm和礼来公司都保留使用许可的知识产权履行现有协议项下的义务的权利 ,对于Eli Lilly,保留将其用于内部研究的权利。我们正在开发Ruboxistaurin,或REC-3599,用于各种适应症,包括GM2。我们需要在商业上做出合理努力,根据指定的开发计划在该地区开发许可产品并 将其商业化,该计划可由我们自行决定随时修改。
根据协议,我们向Chromaderm支付了125万美元的预付款。我们有义务就许可产品向Chromaderm支付 某些开发里程碑,
242
第一个适应症的总金额高达3550万美元,如果追求多个适应症,则高达5250万美元,某些商业里程碑总计高达4900万美元。最后, 我们将按净销售额REC-3599向Chromaderm收取中位数个位数到低两位数的分级版税。截至本招股说明书发布之日,我们尚未向Chromaderm支付任何里程碑 或版税。
本协议将在获得许可的 上到期 按许可销售产品产品基础,逐个国家/地区以 (A)适用于在该国开发、制造或商业化许可产品的许可专利的最后到期日期,(B)自许可产品在该国首次商业销售之日起十年,或 (C)该许可产品在该国的监管排他性到期之日为准。我们可以提前90天书面通知Chromaderm终止协议。对于另一方未治愈的实质性违约,任何一方均可提前45天发出书面 通知(付款违约15天)即可终止本协议。
REC-4881:武田许可证 协议
2020年5月,我们与武田 制药有限公司或武田签订了许可协议或武田许可内协议,据此,我们获得了武田临床阶段化合物TAK-733的独家许可(即使是武田及其附属公司的许可),在全球范围内,在特定条件下可再许可、可转让、可承担版税的某些专利、技术诀窍和材料,以及与开发、制造和商业化武田的临床阶段化合物TAK-733有关的技术诀窍和材料。非ATP-竞争性MEK1和MEK2的变构抑制剂,受制于武田的非独家、免版税、不可撤销、全额支付的许可,可将 许可的化合物用于非临床研究目的。我们目前正在开发一种名为REC-4881的化合物,用于治疗FAP和自发性肺炎患者 装甲运兵车-突变肿瘤。我们还在使用我们的平台评估该化合物在其他疾病状态下的效用。
我们必须在(A)美国、 (B)至少以下三个欧洲国家/地区(英国、法国、德国、意大利和西班牙)以及(C)日本的每个国家/地区中至少使用一种商业上合理的努力来开发和商业化至少一种授权产品(A)美国、 (B)至少三个欧洲国家/地区:英国、法国、德国、意大利和西班牙,以及(C)日本。
协议签署后,我们向武田支付了150万美元的预付款。根据武田许可,我们有义务在完成指定开发和 监管里程碑事件后,向武田里程碑支付总计3950万美元。另外,我们有义务向武田付款。中低档个位数版税,基于我们、我们的附属公司或分被许可人对含有许可 化合物的产品的净销售额,但可按指定的减幅计算。我们支付特许权使用费的义务仍在继续逐个国家/地区直至武田授权的涵盖该产品的最后一项专利到期、该产品的任何监管专有期到期以及该产品在该国家/地区首次商业销售后十年为止。截至本招股说明书的 日期,我们尚未向武田支付任何里程碑或特许权使用费。
每一方均有权终止许可协议 对方未治愈的重大违约、资不抵债或破产。此外,我们可以在2023年5月之后的任何时间无故终止协议,如果我们没有开展任何实质性活动来支持许可化合物或含有许可化合物的任何产品的开发或商业化,并且没有证明我们连续12个月使用商业合理的努力来开发此类化合物或产品,武田可能会终止协议 ,此类失败不是由于我们无法合理控制的事件造成的。此外,如果我们对许可专利的有效性或可执行性提出质疑,武田可能会终止许可协议。在因 武田违反许可协议以外的任何原因终止时,应武田的请求,我们有义务在120天内真诚协商武田在协议期限内开发的特定技术下的许可条款和条件,目的是开发、商业化或以其他方式开发许可化合物和含有许可化合物的产品。
243
竞争
我们 是一家临床阶段的生物技术公司,利用跨越生物、化学、自动化和计算机科学的先进技术,以前所未有的规模和效率发现和设计疗法。到目前为止,我们的努力已经产生了35个早期发现和临床前开发方面的差异化计划和4个临床阶段计划,以及一个包括专利、商标、软件和商业秘密的知识产权组合。我们相信,我们的 技术支持的药物发现的差异化方法,结合了湿实验室和计算方法,并体现在递归图中,为我们提供了显著的竞争优势。
我们是一家混合型公司,由科技型药物研发公司、可扩展平台公司和传统 生物制药公司的最佳元素组成。因此,我们在制药和生物技术行业的多个类别内展开竞争,这些行业的公司同样致力于将快速发展的技术整合到他们的药物发现和开发活动中,和/或正在创建可扩展的科学平台,这些平台有可能产生大型治疗管道,其他公司正在开发针对我们正在或可能选择追求的适应症的疗法。虽然我们 相信我们拥有上述竞争优势,但我们面临着来自大型制药和生物技术公司、学术机构、政府机构、财团以及公共和私营研究机构等 其他机构的竞争,他们中的许多人拥有比我们大得多的资源。值得注意的竞争对手包括:
| • | 科技驱动的药物研发公司. 这类公司应用 复杂的计算工具来解锁新的洞察力,或加快价值链不同环节的药物发现和开发。代表性的例子包括Relay Treeutics、AbCellera、Schrodinger、Insitro、Valo Health、Cellicity和Atomwise。 |
| • | 可扩展的平台公司. 这些公司正在应用新的科学方法或设计新的治疗方式,有可能为大量的一流的治疗候选人。这些公司可能会 直接与我们的以小分子疗法为主的流水线竞争。具有代表性的公司包括现代公司、BioNTech公司、CureVac公司和BridgeBio公司。 |
| • | 传统生物制药公司. 这些公司在主要从事后期临床开发和产品商业化的同时,越来越多地在药物发现和开发价值链中对ML和先进计算工具的应用进行自己的投资。此类 投资可能包括与其他生物技术公司的合作(包括Recursion),我们可能从中受益。代表性公司包括诺华公司、扬森公司(强生公司的子公司)、罗氏公司、默克公司和辉瑞公司。 |
法律程序
我们可能会不时卷入法律诉讼或受到正常业务过程中产生的索赔的影响。我们目前不是任何重大法律程序的一方。无论结果如何,由于辩护和和解成本、资源转移和其他因素,此类诉讼或索赔可能会对我们产生不利的 影响,并且不能保证会获得有利的结果。
244
管理
高级管理人员、主要员工和董事
下表列出了截至2020年12月31日我们的高管、主要员工和董事的姓名和职位以及他们的年龄:
| 名字 |
年龄 | 职位 | ||||
| 行政人员: |
||||||
| 克里斯托弗·吉布森 |
37 | 首席执行官兼董事 | ||||
| 雷蒙娜·道尔 |
61 | 首席医疗官 | ||||
| 蒂娜·万豪·拉森 |
46 | 首席运营官兼总裁 | ||||
| 迈克尔·塞科拉 |
38 | 首席财务官 | ||||
| 沙菲克·维拉尼 |
49 | 首席企业发展官 | ||||
| 主要员工: |
||||||
| 路易莎·丹尼尔斯 |
63 | 首席法务官 | ||||
| 莎拉钱德拉·黑格德 |
57 | 首席科学官 | ||||
| 希瑟·柯克比 |
48 | 首席人事官 | ||||
| 本杰明·马贝(Benjamin Mabey) |
38 | 首席技术官 | ||||
| 梅森胜利者 |
33 | 首席产品官 | ||||
| 非雇员董事: |
||||||
| 扎卡里·博格。(2)(4) |
45 | 导演 | ||||
| 布莱克·博格森。(3)(4) |
39 | 导演 | ||||
| Terry-Ann Burrell(1)(4) |
43 | 导演 | ||||
| 马丁·查韦斯(R.Martin Chavez)(1) |
56 | 导演 | ||||
| 扎文·达尔(1)(3)(4) |
32 | 导演 | ||||
| 罗伯特·赫什伯格(2) |
57 | 导演 | ||||
| 李院长(2)(3) |
58 | 导演 | ||||
| (1) | 审计委员会委员 |
| (2) | 薪酬委员会委员 |
| (3) | 提名及企业管治委员会委员 |
| (4) | 社会责任委员会委员 |
行政主任
克里斯托弗·吉布森(Christopher Gibson)博士是我们自2013年11月公司成立以来的联合创始人兼首席执行官。吉布森博士从公司成立之初就一直担任我们的董事会主席,直到他在董事会其他成员的支持下,于2021年1月要求R.马丁·查韦斯博士接受董事长一职。在此之前,吉布森博士是犹他州大学的医学博士/博士研究生。完成博士学位后,他请假离开医学院,去 建立递归(Build Recursion)。他拥有生物工程学士学位(B.S.)和管理学(B.A.)莱斯大学颁发的荣誉证书。吉布森博士坚定地致力于为犹他州蓬勃发展的生命科学中心做出贡献。作为这项工作的一部分,自2020年11月以来,他一直担任生物蜂巢(犹他州生命科学集体和品牌努力,由治疗、诊断、医疗设备和健康IT公司以及支持它们的公司和公共部门组成)董事会的创始主席。自2019年1月以来,他还担任犹他州生物科学产业协会(犹他州生命科学行业协会)的董事会成员,递归基金会(OUR)的董事会成员非营利组织自2019年11月以来,他一直在海拔实验室(致力于在犹他州培养下一代多元化生物技术创始人的孵化器/加速器)工作,自2019年11月以来一直担任该委员会成员。应国家治疗中心主任的要求,吉布森博士自2020年9月以来一直在治疗加速网络审查委员会任职
245
加速翻译科学,这是美国国家卫生研究院的一个分部。吉布森博士与人合著了十几篇同行评议的 研究,发表在各种期刊上,包括自然,自然方案,循环,临床研究杂志,分子药剂学,公共科学图书馆综合,和糖尿病。我们的董事会相信吉布森博士有资格在我们的 董事会任职,因为他有科学和技术背景,以及他对公司的了解和远见。
雷蒙娜·多伊尔医学博士自2020年12月起担任 我们的首席医疗官。在加入我们之前,Doyle博士在2020年9月至今担任远程医疗非营利性组织MAVEN项目的首席执行官。Doyle博士从2011年10月至今一直担任加州大学旧金山医学中心 医学临床教授,并于2016年12月至今担任扎克伯格旧金山总医院和创伤中心的主治医生。Doyle博士之前 曾于2017年1月至2018年5月担任Blade Treeutics首席医疗官,并于2015年7月至2016年7月担任加州再生医学研究所(California Institute For Regenerative Medicine)副总裁。Doyle博士还在1995至2008年间担任斯坦福大学(Stanford University) 医学副教授。多伊尔博士拥有南方大学的英语语言文学学士学位和牛津大学的生理学学士学位和硕士学位。多伊尔博士还拥有埃默里大学医学院的医学博士学位,并获得了美国内科委员会颁发的内科、肺部医学和危重护理医学委员会认证。
蒂娜·万豪·拉森自2018年7月以来一直担任我们的首席运营官,自2019年10月以来担任我们的总裁。她之前是Achaogen的高级副总裁、执行委员会成员和合规委员会成员,Achaogen是一家上市的生物制药公司,在2016年5月至2018年6月期间发现、开发和商业化了传染病的治疗方法。她 建立了Achaogen的技术运营团队,负责流程开发、供应链和诊断开发,负责启动ZEMDRI®。在加入Achaogen之前,她在2014年10月至2016年4月期间担任罗氏技术开发业务运营全球主管 ,负责业务和技术基础设施。她在基因泰克/罗氏公司担任了总共20年的技术运营职务,包括自动化工程师、制造科学副总监、流程开发工程总监和技术开发运营与工程高级总监。她在生物制药生产的规模化以及管理技术和运营机构方面都拥有深厚的技术专长。拉森女士被医疗保健企业妇女协会认定为一颗冉冉升起的新星。犹他州 商务该杂志被评为年度首席执行官,并荣获女性科技委员会奖(Women Tech Council Awards)。自2015年以来,她一直在科罗拉多州立大学工程学院的顾问委员会任职,并于2019年被评为科罗拉多州立大学杰出校友。 拉森女士拥有科罗拉多州立大学化学工程学士学位。
迈克尔·塞科拉博士自2020年3月以来一直担任我们的首席财务官 。在加入我们之前,Secora博士于2010年7月至2020年2月在Laurion Capital Management担任资产经理,在那里他担任董事总经理兼资本市场和风险投资主管。 在Laurion任职期间,他制定、执行和管理了根本性的投资策略,并建立了业务合作伙伴关系和技术基础设施,用于在事件驱动型、基本面和宏观经济背景下进行投资。 Secora博士积极参与风险投资、跨界投资、资本市场投资、公共和特殊情况投资,尤其是新兴技术和生命科学领域的投资。作为一名技术和生物技术领域的科学家和投资者,他被技术驱动的药物发现所吸引,在那里他观察了该领域的出现和发展,并与该领域的知名公司进行了会面、评估、合作或投资。鉴于Secora博士 深入的投资分析方法、资本市场复合体中的活动以及资本化的整体理念,他一直是许多投资者以及私营和公共管理团队的思想合作伙伴。Secora 博士在普林斯顿大学获得应用和计算数学博士学位,在麻省理工学院获得数学和物理学学士学位。
246
沙菲克·维拉尼医学博士自2020年3月以来一直担任我们的首席企业发展官。在加入我们之前,他是Navire Pharma和CoA Treeutics(分别是BridgeBio Pharma,Inc.的子公司)的首席执行官。2017年9月至2019年12月和2018年6月至2019年12月。2017年6月至2019年12月,他还担任BioBridge LLC驻店首席执行官。在加入BridgeBio之前,他于2004年1月至2017年6月在基因泰克/罗氏担任神经科学、眼科和罕见疾病合作副总裁兼全球主管长达13年之久,在那里他帮助建立了一系列药物,包括用于脊髓性肌萎缩症的Risplam,用于治疗视神经脊髓炎光谱障碍的Enspyng,以及通过许可和收购处于中后期临床流水线的几种疗法。维拉尼博士在剑桥、英国和波士顿接受神经外科医生培训,并在诺丁汉大学(University Of Nottingham)获得医学博士学位。
关键员工
路易莎·丹尼尔斯,J.D.,M.B.A.自2021年1月以来, 一直担任我们的首席法务官和总法律顾问。在此之前,Daniels女士曾于2008年4月至2021年1月担任辉瑞副总裁兼助理总法律顾问,并于2016年5月至2021年1月担任全球 产品开发首席法律顾问,于2013年至2016年担任全球商业运营、战略与投资组合管理首席法律顾问,并于2008年至2013年担任医药治疗研发首席法律顾问。Daniels 女士在加州大学伯克利分校法学院获得法学博士学位,并在加州大学欧文分校Paul Merage商学院获得工商管理硕士学位。
Sharathchandra Hegde,博士自2019年8月以来一直担任我们的首席科学官。在此之前,Hegde博士从1999年9月到2019年7月在Theravance Biophma工作了19年,在那里他担任高级副总裁兼研究主管。在Theravance之前,Hegde博士在Syntex公司工作了9年,后来被罗氏控股有限公司收购。Hegde博士从休斯顿大学获得药理学博士学位,并从印度孟买大学获得药剂学/药理学学士/硕士学位。他参与了几种新药的发现,包括上市的药物Vibativ®(Telavancin),尤佩里®(Revefenancin),Aloxi® (帕隆司酮)和其他处于开发晚期的药物,包括TD-1473(IBD的2/3期)和氨普罗西汀(神经源性直立性低血压的3期)。Hegde博士在药物发现和早期临床开发的战略和战术方面拥有30多年的领导经验。Hegde博士受过经典药理学培训,在多种治疗领域(包括传染病、心血管、呼吸系统、泌尿生殖系统、胃肠、神经病学、纤维化、肿瘤学、自身免疫性和炎症性疾病)的药物发现方面拥有丰富的经验。
希瑟·柯克比,工商管理硕士自2019年5月以来一直担任我们的首席人事官。她于2004年1月至2019年3月在Intuit工作了15年后加入我们,拥有机械工程、产品管理和人才开发方面的背景。她以产品经理的心态和人民领袖的胸怀,为我们的团队创造了一个非凡的工作环境。柯克比女士拥有皇后大学机械工程专业的 学位和哈佛大学的工商管理硕士学位。柯克比的职业生涯始于在阿拉斯加的北极地区管理现场行动。从那以后,她找到了领导QuickBooks在线会计的全球产品组织的道路,后来成为Intuit负责人才开发的全球副总裁,开创了一个全球化的时代领袖兼教练。她的荣誉 包括Intuit著名的CEO领导力奖和女性技术委员会奖决赛选手。
本杰明·马贝(Benjamin Mabey),M.S.自2020年1月起担任我们的首席 技术官。他之前是我们的软件工程副总裁,于2017年3月加入我们。Mabey先生有一个
247
计算机科学、机器学习、软件工程和数据科学方面的多面手背景,拥有超过15年的行业经验。Mabey先生曾担任机器学习工程师, 在广告技术、客户服务和医疗保健行业构建自动化机器学习系统和解决方案。在加入我们之前,Mabey先生是Savvysherpa的高级数据科学家和团队负责人,从2014年1月到2017年3月,Savvysherpa收购了为财富500强公司提供数据科学咨询的Red Brain Labs,Mabey先生在2012年4月到2014年1月担任该公司的首席技术官,Savvysherpa现在是UnitedHealth Group研发部门的一部分。Mabey先生领导我们的技术组织,平衡对强大的可扩展系统和持续创新的需求。
梅森·维克尔斯(Mason Victors), M.S.自2019年1月以来一直担任我们的首席产品官。在此之前,他于2018年7月至2020年1月担任我们的首席技术官,从2015年9月开始担任高级数据科学家,并连续晋升。 维克托先生拥有应用数学、数据科学和机器学习的背景,将他的专业知识应用于从电信和电子商务到医疗保健和国家安全等领域的复杂数据科学和机器学习问题。在加入我们之前,Victors先生是Red Brain Labs的数据工程师,该公司是财富500强企业的数据科学咨询公司,被Savvysherpa收购, 现在是UnitedHealth Group研发部门的一部分,之前曾与技术专家合作,解决美国国家安全局(National Security Agency)的数据科学问题。维克托先生领导我们的产品组织,确定我们必须建立哪些新的科学和技术能力来进一步实现药物发现的工业化,从软件到生物、自动化到化学。
非雇员董事
扎卡里·博格,J.D.博格先生自2018年8月以来一直担任我们的董事会成员。 博格先生利用他在硅谷作为企业家、风险投资家、律师和天使投资者的20年经验。博格是DCVC的联合创始人,他将继续担任DCVC的联席管理合伙人。博格先生领导了DCVC对Freenome、Planet Labs、Tala、Oklo和Gro Intelligence的重大投资。在联合创立DCVC之前, 博格先生是一名企业家,在硅谷创立了三家公司和天使投资者,早期投资了Square,Inc.和Uber Technologies,Inc.等公司。2015年,世界经济论坛(World Economic Forum)任命博格先生为年轻的全球领导者,以表彰他在变革性技术和紧迫的全球问题交汇点上的领导能力,他活跃在达沃斯社区。博格先生以优异成绩毕业于哈佛大学环境科学和公共政策专业,并以优异成绩在乔治敦法学院获得法学博士学位。我们的董事会相信博格先生有资格在我们的董事会任职,因为他的技术背景以及他对公司的了解和看法。
布莱克·博格森(Blake Borgeson)博士自公司于2013年11月成立以来,他一直担任公司董事会成员,并于2013年11月至2018年7月担任公司首席技术官。博格森博士获得了莱斯大学电气工程学士学位。在此之后,他在瑞士伯尔尼的M.E.穆勒研究所(M.E.Mueller Institute)用了一年的时间研究并构建了外科手术的实时导航软件。2005年,他与人共同创立了电子商务公司BuildASign.com。 在担任该业务顾问后,博格森博士于2016年2月在马科特实验室的德克萨斯大学奥斯汀分校(UT Austin)完成了生物信息学博士学位,利用机器学习技术利用新的实验技术快速绘制蛋白质复合体。 博格森博士自2018年9月以来一直在伯克利的机器智能研究所(Machine Intelligence Research Institute)董事会任职,该研究所专注于进行基础数学研究,以确保比机器人更聪明。 博格森博士自2018年9月以来一直在伯克利的机器智能研究所(Machine Intelligence Research Institute)董事会任职,该研究所专注于基础数学研究,以确保比我们的董事会相信Borgeson博士有资格在我们的董事会任职,因为他的技术背景以及他对公司的了解和看法。
特里-安·伯雷尔,工商管理硕士自2020年4月以来一直担任我们的董事会成员。Burrell女士是金融业的资深人士,曾担任比姆治疗公司的首席财务官和财务主管
248
自2019年8月以来。在加入比姆之前,Burrell女士从2008年5月到2019年8月在摩根大通工作了11年,最近的一次是在2018年5月到2019年8月担任医疗保健投资银行集团的董事总经理 。在那里,她覆盖了生物技术和制药行业,帮助执行股权和股权挂钩融资和并购交易。她在为客户提供交易方面的建议方面发挥了重要作用,这些考虑因素包括战略基础、估值和结构。在加入摩根大通之前,伯雷尔曾在花旗集团(Citigroup)从事股票研究,负责专业药品和仿制药。Burrell女士拥有纽约大学伦纳德·N·斯特恩商学院的工商管理硕士学位和哈佛大学的社会学学士学位。我们的董事会相信Burrell女士有资格在我们的董事会任职,因为她的财务专长和她在生物技术行业的高级管理经验。
马丁·查韦斯博士。, 查韦斯博士自2020年4月以来一直担任我们的董事会成员。 查韦斯博士以将华尔街交易业务转变为软件业务,彻底改变了资本流动和运作的方式而闻名。2005年1月至2020年1月,他在高盛担任各种高级职务, 包括首席信息官、首席财务官和该公司证券部门的全球联席主管,并是高盛管理委员会的成员。在此之前,查韦斯博士是2004年被Sungard收购的Kiodex的首席执行官和联合创始人,以及Quorum Software Systems的首席技术官和联合创始人。查韦斯博士自2020年1月以来一直担任人工智能驱动的生物医学技术初创公司Paige的董事会成员;自2020年10月以来担任S.A.桑坦德银行(Banco Santander,S.A.)的董事会成员;自2020年4月以来担任精密基因组测试公司Sema4的董事会成员。查韦斯博士自2020年9月以来一直担任哈佛大学(校长)监事会成员,自2015年9月以来一直担任斯坦福大学医学院研究员委员会成员,自2019年5月以来一直担任高级研究院董事会成员。他拥有哈佛大学生物化学硕士学位和哈佛大学计算机科学硕士学位,以及斯坦福大学医学信息科学博士学位。我们的董事会 相信查韦斯博士有资格在我们的董事会任职,因为他的科学和技术背景以及他对公司的了解和看法。
扎文·达尔自2016年9月以来一直担任我们的董事会成员。达尔是Lux Capital的合伙人,该公司自2014年10月以来一直是一家科技风险投资公司 。在Lux,达尔投资的公司利用机器学习和人工智能来增强和取代现实世界的功能,包括生物、语言、制造和分析。除了领导Lux对Recursion的投资外, 达尔先生还领导了Lux对Primer、Thrive Detect(被Exact Sciences收购)、Creyon Bio、LabGenius、Tempo Automation、Braid Health和CryptoNumerics(被Snowflake收购)的投资。此外,他还是Anagenex治疗公司的创始投资者和Zymergen的早期天使。在此之前,达尔先生是一位创始人和计算机科学家。在Discovery Engine(被Twitter收购),他设计了跨越专有分布式计算 框架的机器学习和人工智能系统,以构建网络规模排名算法。达尔也是超本地化社交网络Fountainhop的联合创始人。达尔先生拥有斯坦福大学的符号系统学士学位和理论计算机科学硕士学位,他在斯坦福大学的人工智能实验室担任 研究员。达尔自2014年1月以来一直在斯坦福大学担任讲师,在那里他教授了为期四分之一的关于加密货币、人工智能和风险投资的研讨会。我们的董事会相信DAR先生有资格在我们的董事会任职,因为他的技术背景以及他对公司的了解和看法。
罗伯特·赫什伯格(Robert Hershberg),医学博士, 博士。, 自2020年3月以来一直担任我们的董事会成员。自2020年3月以来,他一直是Frazier Healthcare Partners的风险合伙人。之前,从2017年4月到2020年3月,赫什伯格博士是Celgene(2019年被百时美施贵宝(Bristol-Myers Squibb)收购)的执行副总裁兼业务发展和全球联盟负责人。自2014年加入Celgene以来,他一直在Celgene担任晋升责任职位,包括2016年1月至2020年3月担任首席科学官。在Celgene之前,他曾在VentiRx制药公司担任多个职务,VentiRx PharmPharmticals是一家临床阶段的生物制药公司,他于2006年与人共同创立,并从2012年9月起担任首席执行官 ,直到公司被Celgene收购
249
2017年2月。赫什伯格博士目前在NanoString Technologies,Inc.(纳斯达克市场代码:NSTG)、Adaptive Biotechnology公司(纳斯达克市场代码:ADPT)和Silverback Treeutics (纳斯达克市场代码:SBTX)的董事会任职。他是华盛顿大学医学院的临床教员,拥有加州大学圣地亚哥分校的生物学博士学位,以及索尔克研究所的附属博士项目,以及加州大学洛杉矶分校的医学博士和学士学位。我们的董事会认为赫什伯格博士有资格在我们的董事会任职,因为他有科学背景,他在制药行业的高级管理经验,以及他对公司的 知识和远见。
李彦宏院长,医学博士,博士。, 是 公司的联合创始人,自2013年11月公司成立以来一直担任董事会成员。李博士自2021年1月起担任默克研究实验室执行副总裁兼总裁。李博士曾于2018年11月至2020年12月担任默克研究实验室发现科学和转化医学高级副总裁。他于2017年2月加入默克,担任副总裁兼转化医学部负责人。在加入默克之前,李博士于1994年7月至2017年3月在犹他大学从事医学研究。在大学期间,他与人共同创立了多家生物技术公司,这些公司来源于他实验室的研究,包括Recursion、Hydra Biosciences和Navigen PharmPharmticals。李博士曾担任H.A.&Edna Benning医学和心脏病学教授、犹他大学健康科学中心研究部副院长以及犹他大学健康护理 首席科学官。李博士还在2015年6月至2016年8月期间担任美国第三大临床参考实验室联合地区大学病理学家的临时首席执行官。李博士曾在圣路易斯的华盛顿大学接受培训,之后转到犹他大学,在马克·基廷的实验室担任博士后科学家。我们的董事会相信李博士有资格在我们的董事会任职,因为他有科学 背景,他在制药行业的高级管理经验,以及他对公司的了解和远见。
家庭关系
我们的任何高管或董事之间都没有家族关系。
董事会组成
我们的董事会目前由 名成员组成。本次发售完成后,我们的董事会将根据我们修订和重述的公司注册证书以及修订和重述的章程的条款不时确定董事人数 。我们的每一位现任董事将继续担任董事,直到他或她的继任者当选并获得资格,或者直到他或她早先去世、辞职或被免职。
我们修订和重述的公司注册证书将规定,我们的董事会将分为三个级别,交错 三年任期。在每个年度股东大会上,只会选出一类董事,其他类别的董事将在各自三年任期的剩余时间内继续存在。我们的现任董事将分为三个 类,如下所示:
| • | 第一类董事为 ,其任期将于2022年召开的年度股东大会上届满; |
| • | 第二类董事为 名,其任期将于2023年召开的年度股东大会上届满; |
| • | 三类董事是 ,他们的任期将在二零二四年召开的年度股东大会上届满。 |
250
在每一届股东年会上,根据我们修订和重述的公司注册证书,将根据我们修订和重述的公司注册证书 选出该类董事的继任者 ,任期从当选和资格之日起至其当选后的第三次年度会议为止,直至其继任者正式当选并符合资格为止(br}将根据我们的修订和重述的公司注册证书)选出该类别董事的继任者 ,任期从当选之日起至其当选后的第三次年度股东大会为止。由于董事人数增加而增加的任何董事职位都将在这三个班级之间分配,以便每个班级将尽可能地 由我们的三分之一的董事组成。
我们董事会的这种分类可能会延迟或阻止 对我们公司的控制权变更。
董事独立性
此次发行 完成后,我们预计我们的普通股将在纳斯达克全球精选市场(Nasdaq Global Select Market)或纳斯达克(Nasdaq)上市。根据纳斯达克的规定,独立董事必须在本次发行完成后一年内在上市公司的 董事会中占多数。此外,纳斯达克的规则要求,除特定例外情况外,上市公司的审计、薪酬和公司治理以及提名 委员会的每个成员都是独立的。审计委员会成员和薪酬委员会成员还必须分别满足规则10A-3和规则10C-1(根据修订后的1934年证券交易法或交易法)中规定的独立性标准。根据纳斯达克的规则,只有在公司董事会认为董事在履行董事职责时没有干扰独立判断的关系的情况下,该董事才有资格成为独立董事 。
根据规则10A-3和纳斯达克规则,上市公司审计委员会成员除以审计委员会、董事会或任何其他董事会委员会成员的身份外,不得(1)直接或间接接受上市公司或其任何子公司的任何咨询、咨询或其他 补偿费,或(2)成为上市公司或其任何子公司的关联人。
根据规则10C-1和纳斯达克规则,要被视为独立, 董事会必须肯定地确定薪酬委员会的每名成员都是独立的,包括考虑与确定董事是否与公司有关系的所有具体因素,这对该董事在薪酬委员会成员的职责方面独立于管理层的能力是至关重要的,包括:(1)该董事的薪酬来源,包括任何咨询、咨询或其他 支付的补偿费。 董事董事会必须肯定地确定薪酬委员会的每位成员都是独立的,包括考虑与确定该董事是否与公司有关系有关的所有因素,这对该董事独立于管理层的能力至关重要,包括:(1)该董事的薪酬来源,包括所支付的任何咨询、咨询或其他 补偿费用。公司的子公司或公司的附属公司。
我们的董事会对董事会的组成、委员会的组成和董事的独立性进行了审查,并考虑了 是否有任何董事与我们有实质性的关系,可能会影响他或她在履行职责时独立判断的能力。根据每位董事 要求并提供的有关其背景、就业和从属关系(包括家庭关系)的信息,我们的董事会决定,扎卡里·博格、Terry-Ann Burrell、R.Martin Chavez、Zavain Dar、Robert Hershberg和Dean Li代表我们八名董事中的六名 ,他们之间的关系不会干扰在履行董事职责时行使独立判断,并且这些董事中的每一人都是独立的,正如该术语所定义的那样
在做出这些决定时,我们的董事会考虑了每位非雇员董事目前和以前与我们公司的关系,以及所有其他事实和
251
董事会认为与确定其独立性相关的情况,包括每位 非雇员董事对我们股本的实益所有权,以及标题为“某些关系和关联方交易”一节中描述的涉及他们的交易。
董事会领导结构
我们的董事会是 目前由R.马丁·查韦斯担任主席。作为一项总体政策,我们的董事会认为,董事会主席和首席执行官职位的分离加强了我们董事会与 管理层的独立性,创造了一个鼓励对管理层业绩进行客观监督的环境,并提高了我们董事会的整体效率。因此,吉布森博士担任我们的首席执行官,而查韦斯博士担任我们的董事会主席,但不是一名官员。我们目前预计并打算未来董事会主席和首席执行官的职位将继续由两人担任。
董事会在风险监督中的作用
我们的 董事会在监督我们的风险管理方面发挥着积极的作用,无论是作为一个整体,还是在委员会层面。我们的董事会负责对风险进行全面监督,并定期审查有关我们风险的信息,包括信用风险、流动性风险和操作风险。 薪酬委员会负责监督与我们的高管薪酬计划和安排有关的风险管理。审计委员会负责 监督与会计事项和财务报告相关的风险管理。公司治理和提名委员会负责监督与我们 董事会独立性和潜在利益冲突相关的风险管理。虽然每个委员会都负责评估某些风险并监督此类风险的管理,但我们的整个董事会会定期通过委员会 成员的讨论了解此类风险。
董事会委员会
在本次发行 完成之前,我们的董事会将有一个审计委员会、一个薪酬委员会、一个提名和公司治理委员会以及一个社会责任委员会,每个委员会的组成和职责 如下所述。
审计委员会
在注册说明书(招股说明书的一部分)生效后,我们审计委员会的成员将是Zavain Dar、R.马丁·查韦斯和特里-安·伯雷尔(Terry-Ann Burrell)。将担任我们的审计委员会主席,是审计委员会 财务专家,这一术语是根据美国证券交易委员会实施2002年萨班斯-奥克斯利法案第407条的规则定义的,并拥有纳斯达克规则定义的金融复杂性。我们的审计委员会将监督我们的 公司会计和财务报告流程,并协助我们的董事会监控我们的财务系统。我们的审计委员会还将:
| • | 选择、保留、补偿、评估、监督,并在适当的情况下终止独立注册会计师事务所 审计我们的财务报表; |
| • | 帮助确保独立注册会计师事务所的独立性和业绩; |
252
| • | 批准审计和非审计服务和收费; |
| • | 审查财务报表,并与管理层和独立注册会计师事务所讨论我们的年度经审计和季度财务报表、独立审计和季度审查的结果以及关于财务报告和披露控制的内部控制的报告和证明; |
| • | 准备SEC要求包含在我们年度委托书中的审计委员会报告; |
| • | 审查独立注册会计师事务所的报告和通信; |
| • | 审查我们内部控制、信息披露控制和程序的充分性和有效性; |
| • | 检讨我们的风险评估和风险管理政策; |
| • | 审查和监控利益冲突情况,批准或禁止任何可能涉及利益冲突或抓住公司机会的事务; |
| • | 审查我们的法律、法规和道德合规计划和报告在遵守适用法律、法规和内部合规计划方面的整体充分性和有效性 ; |
| • | 审查关联方交易;以及 |
| • | 建立并监督会计相关投诉的接收、保留和处理程序,以及员工对可疑会计或审计事项的机密提交。 |
我们的审计委员会 将根据书面章程运作,在本招股说明书所包含的注册声明生效后生效,该注册声明将满足美国证券交易委员会的适用规则和纳斯达克的上市标准。
赔偿委员会
在 注册说明书(招股说明书是其中一部分)生效后,我们薪酬委员会的成员将是Zachary Bogue、Li院长和Robert Hershberg。 将担任我们薪酬委员会的主席。我们的薪酬委员会将监督我们的薪酬政策、计划和福利计划。 薪酬委员会还将:
| • | 监督我们的整体薪酬理念和薪酬政策、计划和福利计划; |
| • | 审查并建议董事会批准我们高管和董事的薪酬; |
| • | 准备薪酬委员会报告,SEC将要求该报告包括在我们的年度委托书中;以及 |
| • | 管理我们的股权薪酬计划。 |
我们的薪酬委员会将根据书面章程运作,在注册说明书(招股说明书是其组成部分)生效时生效,该注册说明书将满足证券交易委员会的适用规则和纳斯达克的上市标准。
提名和公司治理委员会
在本招股说明书所包含的注册声明生效后,我们的提名和公司治理委员会的成员将是Zavain Dar、李院长和
253
布莱克·博格森。将担任我们提名和公司治理委员会的主席。我们的 提名和公司治理委员会将监督和协助我们的董事会审查和推荐提名的董事候选人。具体地说,提名和公司治理委员会将:
| • | 确定、评估并向董事会推荐董事会及其委员会的提名人选; |
| • | 审议董事会及其 委员会的组成,并向董事会提出建议; |
| • | 检讨企业管治实务的发展; |
| • | 评估我们的企业管治实务和报告是否足够;以及 |
| • | 评估我们董事会和个人董事的表现。 |
我们的提名和公司治理委员会将根据书面章程运作,并在本招股说明书所包含的注册声明 生效后生效,该声明将满足美国证券交易委员会的适用规则和纳斯达克的上市标准。
社会责任委员会
本招股说明书是注册声明的一部分,在注册声明生效后,我们的 社会责任委员会成员将是Zavain Dar、Terry-Ann Burrell、Christopher Gibson、Blake Borgeson和Zachary Bogue。克里斯托弗·吉布森(Christopher Gibson)将担任我们的社会责任委员会主席。 我们的社会责任委员会将监督和协助我们的董事会。具体地说,社会责任委员会 将:
| • | . |
我们的社会责任委员会将根据书面章程运作,并在 注册声明生效时生效,本招股说明书是该注册声明的一部分。
董事薪酬
在此次发行之前,我们尚未实施有关支付给非雇员董事 的薪酬的正式政策。我们不时颁发股权奖励,以吸引他们加入我们的董事会,并感谢他们继续在我们的董事会服务。2020年,除了股权奖励,我们没有向任何非员工董事支付任何 薪酬。我们向董事报销参加董事会及其委员会会议的相关费用。
关于此次发行,我们打算采纳并要求我们的股东批准我们 非雇员董事薪酬计划的初始条款。我们的董事会仍在考虑非雇员董事的薪酬政策。
254
吉布森博士是我们唯一一名在2020年担任董事的员工。有关吉布森博士薪酬的信息,请参阅 《高管薪酬》一节,其中包括吉布森博士在2020年担任我们首席执行官期间获得的薪酬。下表提供了截至2020年12月31日的年度非雇员董事薪酬的相关信息 :
| 名字 |
选择权 奖项($)(1) |
总计(美元) | ||||||
| 扎卡里·博格,J.D. |
$ | — | $ | — | ||||
| 布莱克·博格森(Blake Borgeson)博士 |
$ | — | $ | — | ||||
| 特里-安·伯雷尔 |
$ | 1,064,266 | $ | 1,064,266 | ||||
| 马丁·查韦斯博士。 |
$ | 1,063,800 | $ | 1,063,800 | ||||
| 扎文·达尔 |
$ | — | $ | — | ||||
| 罗伯特·赫什伯格,医学博士,博士。 |
$ | 1,064,584 | $ | 1,064,584 | ||||
| 李院长,医学博士。 |
$ | — | $ | — | ||||
| (1) | 根据美国证券交易委员会的规定,本栏中的金额反映的是根据会计准则编纂(ASC)第718主题计算的2020年期间授予的股票期权的总授予日期公允价值,而不是董事支付或变现的金额。我们在本招股说明书其他部分包括的经审计财务报表附注中提供了用于计算授予董事的所有股票 期权价值的假设信息。 |
薪酬委员会 连锁和内部参与
本招股说明书所包含的注册说明书生效后将在本公司薪酬委员会任职的董事会成员均不是或曾经是本公司的高级管理人员或雇员。如果我们的任何实体有一名或多名高管在我们的 董事会或薪酬委员会任职,我们的高管目前或在上一财年均未担任过该实体的董事会或薪酬委员会(或履行同等职能的其他董事会委员会,或在没有此类委员会的情况下,则为整个董事会)的成员。
商业行为和道德准则
在本招股说明书所包含的注册声明生效之前,我们打算采用适用于我们的董事、高级管理人员和员工(包括我们的首席执行官、首席财务官、首席会计官或财务总监)或执行类似职能的人员的书面业务行为准则和道德规范。在此次服务之后, 商业行为和道德准则将在我们的网站www.recursionpharma.com上提供。我们打算在我们的网站上或在当前的Form 8-K报告中披露适用于任何主要高管、主要财务官、主要会计官或控制人,或执行类似职能的人员或我们的董事的未来对该守则的修订或对其要求的任何豁免。网站上包含的 信息未通过引用并入本招股说明书,因此不应视为本招股说明书的一部分。本招股说明书所载本公司网址仅为非主动文本参考。
255
高管薪酬
我们提名的2020年高管(包括2020年担任我们首席执行官的每个人以及2020年薪酬最高的四位高管)是:
| • | 克里斯托弗·吉布森,我们的首席执行官兼董事 |
| • | 雷蒙娜·多伊尔,我们的首席医疗官 |
| • | 蒂娜·万豪·拉森,我们的首席运营官兼总裁 |
| • | 迈克尔·塞科拉,我们的首席财务官 |
| • | Shafique Virani,我们的首席企业发展官 |
薪酬汇总表
下表列出了 截至2020年12月31日的年度我们任命的高管的薪酬信息。
| 姓名和主要职位 |
年 | 薪金($) | 选择权 奖项($)(1) |
非股权 奖励 计划 补偿($)(2) |
所有其他 补偿($) |
总计($) | ||||||||||||||||||
| 克里斯托弗·吉布森 |
2020 | 266,864 | 2,268,661 | 25,700 | (3) | (4) | ||||||||||||||||||
| 首席执行官 |
||||||||||||||||||||||||
| 雷蒙娜·多伊尔 |
2020 | 2,192 | 1,134,331 | — | (4) | |||||||||||||||||||
| 首席医疗官(5) |
||||||||||||||||||||||||
| 蒂娜·万豪·拉森 |
2020 | 401,500 | 226,866 | 25,700 | (3) | (4) | ||||||||||||||||||
| 首席运营官兼总裁 |
||||||||||||||||||||||||
| 迈克尔·塞科拉 |
2020 | 170,833 | (6) | 100,500 | (7) | (4) | ||||||||||||||||||
| 首席财务官 |
||||||||||||||||||||||||
| 沙菲克·维拉尼 |
2020 | 416,667 | 991,749 | 33,526 | (8) | (4) | ||||||||||||||||||
| 首席企业发展官(5) |
||||||||||||||||||||||||
| (1) | 根据美国证券交易委员会的规定,本栏中的金额反映的是根据会计准则编纂(ASC)第718主题计算的2020年期间授予的股票期权的总授予日期公允价值,而不是董事支付或变现的金额。我们在本招股说明书其他部分包括的经审计财务报表附注中提供了用于计算授予董事的所有股票 期权价值的假设信息。对于绩效期权(如下所述),我们根据通过使用蒙特卡洛模拟开发的多条流动性事件值 路径计算授予日期公允价值。计算本栏报告的履约期权授予日期公允价值时使用的假设载于本招股说明书末尾的 综合财务报表附注中。请参阅?汇总薪酬表的叙述性披露??2020年CFO选项?了解更多信息。 |
| (2) | 2020年奖金计划下的赚取金额尚未确定。根据2020奖金计划确定支付给我们的 名高管的任何金额将在本文件的修正案中披露。我们的2020年奖金计划将在下面标题为的部分中进行更全面的描述--非股权激励计划薪酬.” |
| (3) | 金额包括为我们的401(K)计划缴纳的12,700美元的等额缴费和13,000美元的COVID生活援助奖金。 |
| (4) | 由于根据我们2020年的奖金计划赚取的现金奖金尚未确定,因此在本文件的修正案中确定此类奖金后,将 披露2020年的总薪酬。 |
| (5) | 被任命的高管的基本工资按比例计入该被任命的高管在2020年为我们工作的天数 。 |
| (6) | 由于Secora先生期权奖励的公允价值尚未确定,因此该金额将在本文件的 修正案中披露。请参阅汇总补偿表的叙述性披露2020年前CFO选项?了解更多信息。 |
256
| (7) | 金额包括50,000美元搬迁奖金、12,700美元对我们401(K)计划的配套缴费、24,800美元对补充退休计划的 缴费以及13,000美元的COVID生活援助奖金。 |
| (8) | 金额包括对我们的401(K)计划的12,900美元的匹配缴费,13,000美元的COVID生活援助奖金,以及7,623 美元的差旅费和住房报销。 |
对汇总薪酬表的叙述性披露
非股权激励计划薪酬
2020年初,我们采用了针对高管和非执行员工的奖金计划,为 年度的业绩提供现金奖励。我们高管2020年的奖金机会是基于我们的董事会对年初董事会制定的公司目标的实现情况进行的评估。公司2020年的目标 包括与扩展Recursion OS和Recursion Map的功能和广度、开发我们的候选药物以及加强员工敬业度和发展相关的里程碑。单个全公司绩效 乘数适用于每位员工的最高潜在奖金,即工资的10%。
我们的董事会还没有决定 公司2020年目标的实现情况。
在薪酬汇总表中 n列的非股权激励计划薪酬将根据被任命高管2020年工资的10%乘以我们董事会确定的绩效乘数(并根据该被任命高管在本年度受雇于我们的 时间段进一步按比例分摊)。
2020年CFO选项
2020年3月,我们的董事会授予塞科拉先生购买我们普通股的以下选择权:
| • | 购买75万股的选择权,或初始选择权; |
| • | 购买5万股的选择权,或签约选择权;以及 |
| • | 购买1,000,000股票的选择权,或业绩激励选择权。 |
这些拨款是在2020年2月聘用Secora先生时协商的,设定的水平旨在招募他 加入我们的公司,并为我们提供长期留在公司的激励。
初始购股权在Secora先生受雇于吾等的第一天之后每月授予受 初始期权约束的1/48股份,但须受Secora先生持续服务至相关归属日期的限制。
受制于 签署选择权的100%股份的签入选择权将于i)Secora先生受雇于我们的第一天或ii)Secora先生全职永久迁往犹他州盐湖城地区之日 以其继续服务至该较晚日期中较晚的日期为准。
257
每次发生某些流动性事件时,绩效激励期权将累计授予 受绩效激励期权约束的以下股票数量,但须受Secora先生持续服务至该流动性事件发生之日的限制:
| 流动性事件值 |
累计既得股份 | |||
| 超过10.67美元 |
100,000 | |||
| 超过13.87美元 |
200,000 | |||
| 超过18.04美元 |
300,000 | |||
| 超过23.45美元 |
400,000 | |||
| 超过30.48美元 |
500,000 | |||
| 超过44.20美元 |
600,000 | |||
| 超过64.09美元 |
700,000 | |||
| 大于92.93美元 |
800,000 | |||
| 超过134.75美元 |
900,000 | |||
| 超过195.39美元 |
1,000,000 | |||
258
一旦在 流动性事件发生时,受绩效激励期权约束的若干股票已归属,如果后续流动性事件中的流动性事件值低于先前流动性事件中的流动性事件值,则受绩效激励期权约束的既得股数量不会减少。
| 如果流动性事件是 |
然后 | |
| 我们签订条款说明书、意向书或类似的融资协议(将我们或我们任何子公司的股权证券(或可转换或可交换为股权证券的证券)出售并发行给独立的第三方,主要是为了融资目的),并经我们的董事会批准进行这项融资(根据该协议,我们或我们的任何子公司的股权证券(或可转换或可交换为股权证券的证券)将出售并发行给独立的第三方,主要用于融资目的)。 | 与融资有关的每股股本应支付的金额,如条款说明书所述。 | |
| 我们就控制权变更订立条款说明书、意向书或类似协议,并经我们董事会批准,(X)条款说明书中规定的或根据条款可确定的与控制权变更相关的普通股每股应付金额(br})或(Y)(如果控制权变更实际完成)金额中较大的一项,如条款说明书所述或根据条款可确定的(Y),如控制权变更实际完成,则以(X)与控制权变更相关的每股普通股应付金额(br})较大者为准;或(Y)如果控制权变更实际完成,则按条款说明书或条款确定 | 与控制权变更相关的普通股每股的实际应付金额(受第三方托管、赚取、扣留或其他类似安排约束的任何金额不包括在流动性事件价值中,除非实际支付此类金额) | |
| 我们普通股证券的承销公开发行,包括本招股说明书的一部分。 | 在提交给美国证券交易委员会(Securities And Exchange Commission)的表格S-1中的注册说明书中所列的最终招股说明书中所列的对公众的初始价格 这种包销的公开发行 | |
| 与直接上市相关的首次向公众出售或转售我们的普通股证券 | 由适用的证券交易所或国家市场体系设定的参考价 | |
| 衡量日期* | 在适用的证券交易所或国家市场系统所报的计量日期,我们普通股的收盘价 | |
| 重大财务事件** | 与适用的重大财务事件相关的每股股本应付金额 | |
| * | ?测量日期?是指我们的普通股在任何现有证券交易所或 全国市场系统上市的每个交易日。 |
| ** | 重大财务事件是指当我们的普通股在任何成熟的证券交易所或国家市场系统上市时发生以下任何事件:i)根据收购要约回购我们普通股的股票,ii)在公开股权交易中进行私人投资,我们将公开交易的普通股、优先股和/或可转换证券出售给私人投资者,或者iii)我们加速股票回购,以快速回购我们普通股的大笔流通股,以维持一定的估值, 我们的普通股的公开交易股票、优先股和/或可转换证券出售给私人投资者,或iii)我们加速股票回购,以快速回购我们普通股的大量流通股,以维持一定的估值, |
我们使用基于多条股票价格路径的 模型估计了绩效激励期权的授予日期公允价值,该模型是通过使用蒙特卡罗模拟建立的,该模型在估值中纳入了流动性事件价值目标可能无法实现的可能性。绩效激励期权的平均授予日期公允价值估计为1.06美元/
259
股票,我们将确认派生服务期内基于股票的薪酬支出总额约为1,060,000美元。如果流动性事件价值目标在 派生服务期之前实现,我们将调整基于股票的补偿费用,以反映与既得奖励相关的累计费用。如果Secora先生在 必需的服务期内提供服务,无论流动性事件价值目标是否实现,我们都将确认基于股票的补偿费用。
财政年度末的杰出股权奖
下表列出了截至2020年12月31日,我们 任命的每位高管持有的未偿还股权奖励的相关信息:
| 期权大奖 | ||||||||||||||||||||
| 名字 |
格兰特 日期(1) |
数量 有价证券 潜在的 未锻炼身体 选项 可操练的(#) |
数量 有价证券 潜在的 未锻炼身体 选项 不能行使(#) |
选择权 锻炼 价格($)(2) |
选择权 期满 日期 |
|||||||||||||||
| 克里斯托弗·吉布森 |
2020 | 1,000,000 | (3) | $ | 3.71 | 12/30/2030 | ||||||||||||||
| 雷蒙娜·道尔 |
2020 | 500,000 | (4) | $ | 3.71 | 12/30/2030 | ||||||||||||||
| 蒂娜·万豪·拉森 |
2018 | 308,125 | 201,875 | (5) | $ | 1.59 | 7/22/2028 | |||||||||||||
| 蒂娜·万豪·拉森 |
2020 | 100,000 | (6) | $ | 3.71 | 12/30/2030 | ||||||||||||||
| 迈克尔·塞科拉 |
2020 | 140,625 | 609,375 | (7) | $ | 3.33 | 3/03/2030 | |||||||||||||
| 迈克尔·塞科拉 |
2020 | 1,000,000 | (8) | $ | 3.33 | 3/03/2030 | ||||||||||||||
| 迈克尔·塞科拉 |
2020 | 50,000 | $ | 3.33 | 3/03/2030 | |||||||||||||||
| 沙菲克·维拉尼 |
2020 | 93,750 | 406,250 | (9) | $ | 3.33 | 3/03/2030 | |||||||||||||
| (1) | 每一项未完成的股权奖励都是根据我们的2016年计划授予的。 |
| (2) | 此栏代表授予日我们普通股的公允市场价值,由我们的 董事会决定。 |
| (3) | 四十八(1/48)股归属于2020年12月31日或吉布森归属生效日期后一个月,四十八(1/48)股归属于吉布森归属生效日期之后的每个月。 |
| (4) | 25%(25%)受奖励的股份将在2020年12月31日或Doyle 年度归属开始日期后一年归属,四十八分之一(1/48)受奖励的股票应在Doyle年度归属开始日期之后的每个月的同一天归属。 |
| (5) | 25%(25%)受奖励的股份将在2018年7月16日或Larson年度归属开始日期后一年归属,四十八分之一(148)受奖励的股份应在此后每月与Larson年度归属开始日期的同一天归属。 |
| (6) | 四十八分之一(1/48)受奖励的股份将在2020年12月31日或Larson 每月归属开始日期后一个月归属,四十八分之一(1/48)受奖励的股票应在此后每月与Larson每月归属开始日期的同一天归属。 |
| (7) | 四十八(1/48)股归属于2020年3月1日或Secora 归属生效日期后一个月,四十八(1/48)股归属于Secora归属生效日期之后的每个月。 |
| (8) | 有关奖励条款的说明,请参阅标题为2020 CFO选项的部分。 |
| (9) | 四十八分之一(1/48)受奖励的股份将在2020年3月4日或Virani 归属开始日期后一个月归属,四十八分之一(1/48)受奖励的股份将在其后每月与Virani归属开始日期的同一天归属。 |
与我们指定的行政人员的聘用安排
我们 已与我们任命的每位高管就其受雇于我们签订了雇佣协议。
260
克里斯托弗·吉布森
我们目前预计,在本次发售完成之前,我们将与我们的首席执行官吉布森博士签订一份确认性雇佣协议。验证性雇佣协议目前预计没有具体条款,将规定随意雇佣。吉布森博士目前的年度基本工资是45万美元,吉布森博士的年度目标奖金 是他年度基本工资的10%。
雷蒙娜·道尔
我们目前预计,在此服务完成之前,我们将与我们的首席医疗官Doyle博士签订一份确认性雇佣协议。验证性雇佣协议目前预计没有具体条款,将规定随意雇佣。Doyle博士目前的年度基本工资为44万美元,Doyle博士的年度目标奖金为其年度基本工资的10%。
蒂娜·万豪·拉森
我们目前预计,在本次发售完成之前,我们将与拉森女士、我们的总裁兼首席运营官 签订一份确认性雇佣协议。验证性雇佣协议目前预计没有具体条款,将规定随意雇佣。拉森目前的年度基本工资是401,500美元,拉森的年度目标奖金是她年度基本工资的10%。
迈克尔·塞科拉
我们目前预计,在本次发售完成之前,我们将与我们的 首席财务官塞科拉先生签订一份确认性雇佣协议。验证性雇佣协议目前预计没有具体条款,将规定随意雇佣。塞科拉目前的年度基本工资为20.5万美元,他的年度目标奖金是其年度基本工资的10%。
沙菲克·维拉尼
我们目前预计,在本次发售完成之前,我们将与我们的首席 企业发展官Virani先生签订一份确认性雇佣协议。验证性雇佣协议目前预计没有具体条款,将规定随意雇佣。维拉尼目前的年基本工资是50万美元,维拉尼的年度目标奖金是他年基本工资的10%。
终止或控制权变更时的潜在付款
我们目前预计,在本次发售完成之前,我们将为我们的高管作出安排,规定终止或控制权变更时的付款和 福利,这些安排可能包括在预期的确认性雇佣协议或单独的计划或协议中。
员工福利和股票计划
2021年股权激励计划
在此次发行生效之前,我们预计我们的董事会将通过,我们的股东将批准我们的2021年 股权激励计划,即2021年计划。2021年计划将是
261
本招股说明书包含的注册说明书生效日期的前一个工作日生效。我们的2021年计划将规定向我们的员工和任何母公司和子公司员工授予守则第422节所指的激励 股票期权,并向我们的员工、董事和顾问以及我们的子公司的员工和顾问授予非法定股票期权、限制性股票、限制性股票单位、股票 增值权、绩效单位和绩效股票。
授权股份。根据我们的2021年计划,我们总共保留了 股普通股以供发行。此外,根据我们的2021年计划为 发行保留的股份还将包括(1)截至股东批准2021年计划之日根据我们2016计划保留但未发行的股份,以及(2)根据我们2016计划授予的奖励 发行的普通股股票,在股东批准2021年计划之日之后,在没有全部行使的情况下到期或以其他方式终止,或由于未能归属而被我们没收或回购(前提是根据第(1)和(2)项可添加到2021计划的最大 股票数量为股票)。根据我们的2021计划,可供发行的股票数量 还将包括从我们的2022财年开始的每个财年的第一天每年增加的股票数量,相当于以下至少一个:
| • | 股份; |
| • | 截至上一会计年度最后一天我们普通股流通股的百分比 (%);或 |
| • | 其他金额由我们董事会决定。 |
如果奖励到期或在未完全行使的情况下不可行使,根据交换计划退还,或对于 限制性股票、限制性股票单位、绩效单位或绩效股票,由于未能授予而被没收或由我们回购,则未购买的股票(或用于股票期权或股票增值权以外的奖励, 被没收或回购的股票)将可用于2021计划下的未来授予或出售(除非2021计划已终止)。(br}如果奖励未全部行使,则根据交换计划交出,或因未能授予或回购而被我们没收或回购的未购买股票(或用于股票期权或股票增值权以外的奖励,被没收或回购的股票)将可用于2021计划下的未来授予或出售(除非2021计划已终止)。关于股票增值权,根据2021年计划,只有实际发行的净股票将不再可用 ,股票增值权下的所有剩余股票仍可用于2021年计划下的未来授予或出售(除非2021年计划已终止)。根据2021年计划实际发行的股票不会 返还给2021年计划,除非根据限制性股票、限制性股票单位、绩效股票或绩效单位奖励发行的股票因未能归属而被我们回购或没收,这些股票将 可用于未来根据2021年计划授予。根据2021年计划,用于支付奖励的行使价格或满足与奖励相关的预扣税款义务的股票将可用于未来的授予或出售。如果 奖励是以现金而不是股票的形式支付,这种现金支付不会导致根据2021年计划可供发行的股票数量减少。
计划管理。我们的董事会或董事会任命的一个或多个委员会将管理我们的2021计划。 我们董事会的薪酬委员会将首先管理我们的2021计划。此外,如果我们确定根据《交易法》规则 16b-3将我们的2021计划下的交易限定为豁免交易是可取的,则此类交易的结构将满足规则16b-3的豁免要求。根据我们的2021年计划的规定, 管理人有权管理我们的2021年计划,并做出所有被认为是管理2021年计划所必需或适宜的决定,包括但不限于确定我们普通股的公平市值、选择可能被授予奖励的服务提供商、确定每项奖励涵盖的股票数量、批准根据2021年计划使用的奖励协议表格、决定奖励的条款和条件(包括但不限于
262
加速或放弃或没收限制以及任何奖励或与之相关的股份的任何限制或限制),解释和解释我们的2021计划和根据该计划授予的奖励的条款,规定、修订和废除与我们的2021计划相关的规则,包括创建子计划,修改或修改每个奖励,包括但不限于延长奖励终止后可行使期的酌情权 (期权或股票增值权将不会超过其原来的最高期限)并允许参与者推迟收到现金付款或股票交付 ,否则根据奖励应向该参与者支付现金或股票。管理人还有权允许参与者有机会将未完成奖励转移到 管理人选择的金融机构或其他个人或实体,并启动一项交换计划,根据该计划,未完成奖励可以退还或取消,以换取相同类型的奖励,该相同类型的奖励可能具有更高或更低的行使价格和/或不同的条款、不同 类型的奖励和/或现金,或通过该计划增加或减少未完成奖励的行使价格。管理员的决定、解释和其他操作是最终的,对所有参与者都有约束力。
股票期权。根据我们的2021年计划,股票期权可能会被授予。根据我们的2021计划授予的期权的行权价格 必须至少等于授予日我们普通股的公平市值。期权期限不得超过十年。对于任何拥有我们(或我们的任何母公司或子公司)所有类别流通股投票权超过10%的参与者,授予该参与者的激励股票期权期限不得超过五年,且行使价格必须至少等于授予日公平市值的110%。管理人将 确定期权行权价格的支付方式,可能包括现金、股票或管理人接受的其他财产,以及适用法律允许的其他类型的对价。终止员工、董事或顾问的服务 后,该员工、董事或顾问可以在其期权协议中规定的时间内行使其期权。在奖励协议中没有指定时间的情况下,如果因死亡或 残疾而终止服务,则在服务终止后12个月内仍可行使选择权。在所有其他情况下,在授标协议中没有指定时间的情况下,在 服务终止后的三个月内,该选择权仍可行使。但是,期权的行使时间不得晚于其期满。根据我们的2021年计划的规定,管理员决定选项的其他条款。
股票增值权。根据我们的2021年计划,股票增值权可能会被授予。股票增值权允许 接受者在行权日和授予日之间以我们普通股的公平市场价值获得增值。股票增值权的期限不得超过十年。 员工、董事、顾问离职后,可以在股票增值权协议约定的期限内行使股票增值权。在奖励协议中没有规定时间的情况下,如果因死亡或残疾而终止 ,股票增值权在服务终止后的12个月内仍可行使。在所有其他情况下,在奖励协议中没有规定时间的情况下,股票增值权在服务终止后的三个月内仍可行使。但是,股票增值权的行使不得晚于期满。根据我们2021年计划的规定,管理人 决定股票增值权的其他条款,包括何时可以行使,以及是否以现金或我们普通股的股票或两者的组合支付任何增加的增值,但根据股票增值权的行使而发行的股票的每股行使价将不低于授予日每股公平市值的100%。
限制性股票。根据我们的2021年计划,可能会授予限制性股票。限制性股票奖励是根据管理人设定的条款和条件授予我们 普通股的股票。管理人将决定授予任何员工、董事或顾问的限制性股票数量,并在符合我们2021计划的 规定的情况下,
263
将确定此类奖励的条款和条件。管理员可以施加其认为合适的任何授予条件(例如,管理员可以根据特定绩效目标的实现情况或继续向我们提供服务来设置 限制),但管理员可以自行决定加快任何限制失效或取消的时间。限制性 股票奖励的接受者通常在授予时将对此类股票拥有投票权和股息权,而不考虑归属,除非管理人另有规定。未授予的限制性股票受我们 回购或没收的权利约束。
限制性股票单位。根据我们的2021年计划,可能会授予限制性股票单位。 限制性股票单位是代表相当于一股普通股的公平市值的簿记分录。根据我们2021计划的规定,管理人决定RSU的条款和条件, 包括归属标准以及付款形式和时间。管理人可以根据公司范围、部门、业务单位或个人目标(包括但不限于继续聘用或服务)、适用的联邦或州证券法或管理人自行决定的任何其他基础来设定授予标准。管理人可自行决定以现金、股票 或两者的某种组合的形式支付赚取的限制性股票单位。此外,管理人可自行决定加速任何限制失效或取消的时间。
绩效单位和绩效份额。绩效单位和绩效份额可根据我们的2021计划授予。 绩效单位和绩效份额是只有在实现管理员设定的绩效目标或授予其他奖励的情况下才会向参与者付款的奖励。管理员将自行确定 绩效目标或其他归属标准,这些标准将根据绩效目标的实现程度确定要支付给参与者的绩效单位和绩效份额的数量或价值。 管理人可以根据公司范围、部门、业务单位或个人目标(包括但不限于继续雇佣或服务)的实现情况、适用的联邦或州证券法或 管理人自行决定的任何其他基础来设定绩效目标。授予绩效单位或绩效份额后,管理人可自行决定减少或免除 此类绩效单位或绩效份额的任何绩效目标或其他归属条款。绩效单位将具有由管理员在授予日期或之前建立的初始值。绩效股票的初始价值将等于授予日我们普通股的公平市值 。管理人可自行决定以现金、股票或两者的某种组合方式支付赚取的业绩单位或业绩份额。
外部董事。根据我们的2021计划,所有外部(非员工)董事都有资格 获得所有类型的奖励(激励性股票期权除外)。为了对我们的外部董事的现金薪酬和股权奖励提供最大限制,我们的2021计划规定,在任何给定的财政 年度,外部董事不得获得总价值超过$ 的现金薪酬和股权奖励。 ,每个股权奖励的价值基于其授予日期的公允价值, 根据公认会计准则(GAAP)为此限制而确定。对个人作为雇员或顾问(外部董事除外)的服务而支付的任何现金补偿或奖励将不计入这一限额。
裁决不得转让。除非管理人另有规定,否则我们的 2021计划一般不允许转移奖励,只有获奖者才可以在其有生之年行使奖励。如果管理员使奖励可转让,则该奖励将包含管理员认为合适的附加条款和 条件。
某些调整。如果我们的 资本发生某些变化,为防止我们的2021计划提供的好处或潜在好处减少或扩大,管理员将
264
调整根据我们的2021计划可以交付的股票数量和类别,和/或每个未完成奖励所涵盖的股票数量、类别和价格,以及我们的2021计划中设定的数字股票限制 。
解散或清盘。如果我们提议的清算或解散, 管理人将在可行的情况下尽快通知参与者,如果没有行使,所有奖励将在该提议的交易完成之前立即终止。
合并或控制权变更。我们的2021计划规定,如果发生合并或控制权变更(如 我们的2021计划所定义),则在未征得参与者同意的情况下,每个未完成的奖励将按照管理员的决定处理。管理员无需以类似方式处理所有奖项、参与者持有的所有奖项或同一类型的所有奖项 。
如果继任公司不承担或替代任何未完成的奖励,则参与者将完全授予并拥有 行使其所有未偿还期权和股票增值权的权利,对限制性股票和限制性股票单位的所有限制将失效,对于基于业绩授予的奖励,除非适用的奖励协议或适用于参与者的其他协议或政策另有明确规定,否则所有绩效目标或其他归属标准将被视为100%达到目标水平以及满足所有其他条款和条件。如果控制权变更时未采用或替代期权或股票增值权,管理人将以书面或电子方式通知参与者,该期权或股票增值权将在管理人自行决定的 期限内行使,该期权或股票增值权将在该期限届满时终止。
对于授予外部董事的奖励,如果控制权发生变化,外部董事将完全授予并有权行使 所有未行使的期权和股票增值权,对限制性股票和限制性股票单位的所有限制将失效,对于基于业绩归属的奖励,除非适用的奖励协议或适用于参与者的其他协议或政策另有规定,否则所有业绩目标或其他归属标准将被视为100%达到目标水平和满足所有其他条款和条件。
退款。奖励将受我们的任何退还政策的约束,管理员还可以在奖励 协议中指定,参与者与奖励有关的权利、付款和/或福利在发生某些特定事件时将受到减少、取消、没收和/或补偿的限制。我们的董事会可以 要求参与者没收、退还或偿还我们的全部或部分奖励和/或根据奖励发行的股票、根据奖励支付的任何金额以及在出售根据奖励发行的股票时支付或提供的任何付款或收益,以遵守此类退还政策或适用法律。
修改;终止。管理员 有权修改、更改、暂停或终止我们的2021计划,前提是此类操作不会对任何参与者的权利造成实质性损害。我们的2021年计划将在2031年自动终止,除非我们更早地终止它。
2021年员工购股计划
在此次发售 生效之前,我们预计我们的董事会将通过,我们的股东将批准我们的2021年员工股票购买计划,或2021年ESPP。我们预计,我们的2021年ESPP将在本招股说明书包含的注册声明生效日期之前的下一个工作日 生效。然而,除非我们的董事会另有决定,否则2021年ESPP下的任何报价期或购买期都不会开始。
265
授权股份。共计 根据我们2021年的ESPP,我们的普通股将可供出售。根据我们的2021年ESPP,我们的普通股可供出售的股票数量 还包括在2021年ESPP规定的第一个发售期间开始的财年之后的每个财年的第一天每年增加的股票数量 ,相当于以下至少一个:
| • | 股份; |
| • | 截至上一会计年度最后一天我们普通股流通股的百分比 (%);或 |
| • | 其他金额由管理员决定。 |
2021年ESPP管理。我们期望我们董事会的薪酬委员会将管理我们的2021年ESPP,并将拥有全面和专有的自由裁量权来解释、解释和应用2021年ESPP的条款,将部长职责委托给我们的任何员工,根据2021年ESPP指定单独的产品,指定我们的子公司和附属公司参与2021年ESPP,确定资格,裁决根据2021年ESPP提交的所有有争议的索赔,并建立它认为必要的程序。采用必要或适当的程序和子计划,以允许外籍员工或在美国境外受雇的员工参与2021年ESPP。管理员的调查结果、决定和决定是最终的,并在法律允许的最大范围内对所有参与者具有约束力。
资格。一般来说,如果我们或 任何参与的子公司或附属公司通常雇用我们的所有员工每周至少工作20个小时,并且在任何日历年度中超过5个月,则他们都有资格参加。在登记日期之前,管理员可自行决定以下员工:(1)自上次聘用日期以来未完成至少两年的服务(或管理员确定的较短时间段);(2)通常每周工作不超过20小时 (或管理员确定的较短时间段);(3)每历年工作时间通常不超过五个月(或管理员确定的较短时间段),在登记日期之前,可确定以下员工:(1)自上次聘用日期以来未完成至少两年的服务(或管理员确定的较短时间段);(3)每历年通常工作不超过五个月(或管理员确定的较短时间段),(2)每周工作不超过20小时(或管理员确定的较短时间段),(3)每历年通常工作不超过五个月(4)为守则第414(Q)节所指的高薪雇员,或(5)为守则第414(Q)节所指的高薪雇员且薪酬水平高于某一水平,或根据交易所法案第(br})节第16(A)节的披露要求,是否有资格参与该要约期。
但是,根据我们的2021年ESPP,员工可能不会被授予 购买我们普通股的权利,但满足以下条件的员工:
| • | 紧接授予后,将拥有股本和/或持有未偿还期权,以购买我们或我们的任何母公司或子公司的所有类别股本的总投票权或总价值的5%或 以上的该等股票;或 |
| • | 根据我们的所有员工股票购买计划或我们的任何母公司或 子公司的所有员工股票购买计划,持有购买我们普通股的权利,而该等股票的累计比率超过我们普通股的价值25,000美元,在每个日历年度内,该等权利在任何时候都有流通性。 |
供货期。我们的2021年ESPP将包括一个组件,该组件允许我们提供符合本规范第423节的条件的产品,以及一个允许我们向指定公司提供不符合本规范第423节的产品的组件,如我们的2021年ESPP中所述。预计在本次发售完成之前,我们的 董事会将不会根据2021年ESPP授权任何发售。如果我们的董事会根据2021年ESPP批准了一个要约期,我们的董事会有权确定要约期和 购买期的持续时间,包括要约期和购买期的开始和结束日期,前提是任何要约期的持续时间不得超过27个月。
266
捐款。我们的2021年ESPP将允许参与者通过缴费(以工资扣除的形式或其他方式,在管理员允许的范围内)购买 我们普通股的股票,金额最高可达 他们合格补偿的%。参与者最多可以购买 购买期间我们普通股的股份。
购买权的行使。如果我们的董事会根据2021年ESPP批准了发售和购买期, 参与者在任何发行期内贡献和积累的金额将在每个购买期结束时用于购买我们的普通股。股票收购价为 在发行期的第一个交易日或行使日,我们普通股公允市值的较低者的百分比。参与者可以在发售期间的任何时间终止其参与 ,并将获得尚未用于购买我们普通股股票的应计供款。一旦终止与我们的雇佣关系,参与即自动终止。
不可转让。参与者不得转让根据我们的2021年ESPP ESPP授予的权利(除遗嘱、世袭和分配法或我们的2021年ESPP另有规定外)。
合并或变更 控制权。我们的2021年ESPP将规定,在我们2021年ESPP定义的合并或控制权变更的情况下,继任者公司可以接管或替代每一项未完成的购买权。如果继承人 公司拒绝承担或替代未完成的购买权,则正在进行的要约期限将缩短,并将设定一个新的行使日期,该日期将在拟议的合并或控制权变更日期之前。 管理员将通知每位参与者锻炼日期已更改,参与者的选择权将在新的锻炼日期自动行使,除非在此日期之前参与者已退出 服务期。
修订;终止董事会将有权暂停或终止我们的2021年ESPP, 管理人将有权修改2021年ESPP,但除非我们的2021年ESPP中描述了某些例外情况,否则此类行动不得对我们根据2021年ESPP购买普通股的任何未偿还权利产生不利影响 ESPP。我们的2021年ESPP将在2040年自动终止,除非我们更早地终止它。
修订后的2016年度股权激励计划
我们的2016股权激励计划或2016计划允许我们向符合条件的员工、董事和顾问(包括我们任何母公司或子公司的 员工和顾问)提供代码第422节所指的激励性股票期权、股票增值权、限制性股票奖励和限制性股票单位(每个奖励和此类奖励的获得者、参与者)。预计自本招股说明书生效前一个工作日起,我们的2016计划将终止,此后我们 将不再根据我们的2016计划授予任何额外奖励。然而,我们的2016年计划将继续管理我们2016年计划之前授予的未完成奖项的条款和条件。
截至2020年12月31日,根据我们的2016计划,涵盖我们普通股的股票期权 已发行,2016计划中没有股票增值权、限制性股票奖励或 未偿还的限制性股票单位。
计划管理。我们的薪酬委员会拥有 权力,与我们的董事会同时管理我们的2016年计划。不同的委员会可能会针对不同的服务提供商管理我们的2016年计划。管理员拥有所有必要或适当的权限和自由裁量权 来管理我们2016年的计划并控制其运行,包括解释的权限
267
并解释我们2016年计划的条款和2016年计划下授予的奖励。管理员的决定是最终决定,对所有参与者和持有 奖项的任何其他人员具有约束力。
管理人的权力包括制定交换计划(无需股东批准)的权力,根据该计划, (1)放弃或取消未完成的奖励,以换取相同类型的奖励(可能具有更高或更低的行使价格和不同的条款)、不同类型的奖励和/或现金,(2)参与者将有 机会将任何未完成的奖励转移到由管理员选择的金融机构或其他个人或实体,和/或(3)提高或降低未完成奖励的行使价格。管理人 的权力还包括规定、修订和废除与我们2016计划相关的规则和法规,修改或修改每个裁决,以及做出执行我们2016计划所需或建议的所有其他决定的权力。
资格。员工、董事和顾问,包括我们任何母公司或 子公司的员工和顾问,都有资格获得奖励,前提是这些顾问提供与融资交易中的证券发售或销售无关的真诚服务,并且不直接促进或维持我们证券的市场 。只有我们的员工或我们母公司或子公司的员工才有资格获得激励性股票期权。股票期权。根据我们2016年的计划,已经授予了股票期权。根据我们2016 计划的规定,管理人决定期权的期限、受期权约束的股票数量以及可以行使期权的时间段。
期权的期限在适用的授予协议中规定,但期权的期限自授予之日起不得超过10年。 管理人决定期权的行权价格,除非2016计划另有规定,否则行权价格一般不得低于授予日我们普通股公平市值的100%。但是,授予 直接或通过归属拥有我们所有股票类别或任何母公司或子公司总投票权的10%以上的个人的奖励股票期权的有效期不超过授予日期起五年, 将拥有至少相当于授予日普通股公平市值的110%的行权价。(=此外,如果员工在任何日历年(根据我们的所有计划以及我们的任何母公司或子公司)首次可行使激励性股票期权的股票的公平市值合计超过100,000美元,此类期权将被视为非法定股票期权。
管理员决定参与者如何支付期权的行权价格,允许的方法通常在 适用的奖励协议中规定。如果参与者作为服务提供商的身份(如我们2016年计划中所定义)终止,该参与者可以在 适用奖励协议中规定的时间段内行使其期权的既得部分。如果参与者的服务提供商身份因 死亡或残疾以外的其他原因终止,则在30天或适用奖励协议中规定的更长时间内,既得期权通常仍可行使。如果参与者的服务提供商身份因死亡或残疾而终止,则在终止之日起六个月内(或适用奖励协议中规定的其他较长期限),既得期权通常仍可行使。在任何情况下,期权在超过原定期限后都不能继续行使。如果参与者未在奖励协议规定的时间内行使其期权,期权将终止。 除上述情况外,管理员有权决定期权终止后的可行使期。
不可转让获奖名单。除非管理人另有决定,否则不得以遗嘱或继承法和分配法以外的任何方式出售、转让、质押、转让或以其他方式转让或质押奖励。此外,在适用参与者的有生之年,只有该参与者可以行使其奖励。如果管理员创建了
268
奖励可转让,此类奖励只能(1)通过遗嘱转让,(2)通过世袭和分配法转让,或(3)经修订的1933年证券法第701条(证券法)允许转让。
某些调整。如果有股息或其他分配(无论是以现金、股票、其他证券或其他财产的形式)、资本重组、股票拆分、反向股票拆分、重组、合并, 合并,拆分,剥离,合并,回购、交换股票或我们的其他证券或影响股票的公司结构的其他变更 ,管理人将对我们2016年计划下可能交付的股票数量和类别,或每个未偿还奖励所涵盖的股票数量、类别和价格进行相应的调整。 管理员关于此类调整的决定将是最终的、具有约束力的和决定性的。
解散或 清算。在我们建议解散或清算的情况下,管理人将在该建议交易的生效日期之前尽快通知每个参与者。如果裁决之前没有 行使过,裁决将在该提议的行动完成之前立即终止。
控制权方面的合并和变更 。如果我们与另一家公司或实体合并或合并到另一家公司或实体,或者控制权发生变化(根据我们2016年计划的定义),每一项未完成的奖励都将按照管理人的决定处理, 包括但不限于:(1)收购或继承公司(或其附属公司)将承担奖励,或由实质上相等的奖励取代,并对股票和价格的数量和种类进行适当调整 ;(2)在书面通知参与者后,参与者的奖励将在以下日期或之前终止(3)在合并或控制权变更完成之前或之后,未完成的裁决将被授予并成为可行使、可变现或应支付的裁决,或适用于裁决的限制将全部或部分失效,并在管理人确定的范围内,在紧接该合并或控制权变更生效之前终止或 终止;(4)(A)终止奖励,以换取一笔现金或财产(如有的话),该数额等于在交易发生之日行使该 奖励或实现参与者权利时本应获得的金额(并且,为免生疑问,如果管理人真诚地确定在行使该奖励或实现参与者权利时不会获得 金额,则为免生疑问,);(B)(A)终止奖励,以换取一笔现金或财产(如有的话),该数额等于在交易发生之日行使该奖励或实现参与者权利时本应获得的金额(并且,为免生疑问,如果管理人真诚地确定在行使该奖励或实现参与者权利时不会获得任何 金额),则该裁决可由我们终止而不支付任何费用)或(B)以管理人自行决定选择的其他权利或财产 替换该裁决;(五)上述各项的任意组合。管理员没有义务以同样的方式对待所有奖项、参与者持有的所有奖项或相同类型的所有奖项。
如果继任公司不承担或替代奖励(或部分奖励),参与者将完全授予并有 行使其所有未偿还期权和股票增值权的权利,包括这些奖励本来不会被授予或行使的股票,对限制性股票和限制性股票单位的所有限制将 失效,对于基于业绩的奖励,所有业绩目标或其他归属标准将被视为达到100%的目标水平和所有其他条款此外,如果在合并或控制权变更时期权或股票 增值权未被承担或替代,管理人将以书面或电子方式通知参与者,该期权或股票增值权将在管理人自行决定的 期限内可行使,该期权或股票增值权将在该期限届满时终止。
修订及终止。我们的董事会可以随时在 任何方面修订、更改、暂停或终止我们的2016年计划,包括但不限于修订根据我们2016年计划签署的任何形式的授标协议或文书。在必要和必要的范围内
269
为遵守适用法律,我们对2016计划的任何修订都将获得股东批准。我们2016计划的任何修改、更改、暂停或终止都不会损害参与者的权利 ,除非参与者和管理员以书面形式达成一致。如上所述,预计自注册说明书( 招股说明书的一部分)生效前一个工作日起,我们的2016计划将终止,此后我们将不再根据2016计划授予任何额外奖励。
高管激励 薪酬计划
在本次发售生效之前,我们预计我们的董事会将采用高管激励 薪酬计划,或激励薪酬计划。我们预计我们的奖励薪酬计划将在注册说明书生效日期的前一个工作日生效,本招股说明书是注册说明书的一部分。我们的 激励薪酬计划将允许我们的薪酬委员会根据薪酬委员会设定的绩效目标 向薪酬委员会挑选的员工(包括我们指定的高管)授予激励奖励(通常以现金支付)。
根据我们的激励薪酬计划,我们的薪酬委员会将确定适用于任何奖励的绩效目标 ,这些目标可能包括但不限于与研发相关的目标、法规里程碑或法规相关目标、毛利率、财务里程碑、新产品或业务开发、 营业利润率、产品发布时间表或其他产品发布里程碑、出版物、现金流、采购、储蓄、内部结构、领导力发展、项目、功能或投资组合特定的里程碑、许可或研究 合作协议、融资、绩效目标可能因参与者而异 且因奖项而异。
我们预计,我们董事会的薪酬委员会将管理我们的激励薪酬计划, 将在任何时候自行决定增加、减少或取消参与者的实际奖励,和/或增加、减少或取消分配给特定绩效期间奖金池的金额。实际奖励可以是 以下,等于或高于参与者的目标奖励,由管理员自行决定。管理员可以根据其认为相关的因素确定任何增加、减少或取消的金额,并且不需要 针对其考虑的因素确定任何分配或权重。
实际奖励通常仅在获得后才会以现金(或等值的 )支付,除非管理员另有决定,否则参与者必须在实际奖励支付之日之前由我们雇用,才能获得实际奖励。薪酬委员会可能保留权利 根据我们当时的股权薪酬计划授予股权奖励来解决实际奖励,该股权奖励可能具有薪酬委员会确定的条款和条件(包括归属)。奖励的支付将在获得奖励后尽快支付 ,但不迟于我们的激励薪酬计划中规定的日期。
我们的 董事会和薪酬委员会将有权修改、暂停或终止我们的激励薪酬计划,前提是此类行动不会损害任何参与者在任何已获奖励方面的现有权利。
401(K)计划
我们维持401(K)退休储蓄 计划,以使我们的员工受益,包括我们指定的高级管理人员,他们仍然受雇于我们,并满足某些资格
270
要求。根据401(K)计划,符合条件的员工可以选择在守则规定的限额内,通过向401(K)计划缴费,在 税前或税后(Roth)的基础上推迟支付部分薪酬。401(K)计划授权雇主提供安全港捐款。401(K)计划旨在 符合本规范第401(A)和501(A)节的规定。作为一种符合税收条件的退休计划,401(K)计划的税前缴费和这些税前缴费的收入在从401(K)计划分配之前不应向员工纳税,Roth缴费的收入从401(K)计划分配时也不应纳税。
责任限制及弥偿
我们修订和 重述的公司注册证书以及修订和重述的章程都将在本次发售完成后生效,规定我们将在特拉华州法律允许的最大程度上赔偿我们的董事和高级管理人员,并可能赔偿我们的员工和其他代理人。 我们将在特拉华州法律允许的最大程度上赔偿我们的董事和高级管理人员,并可能赔偿我们的员工和其他代理。特拉华州法律禁止我们修改和重述的公司证书限制我们董事对以下事项的责任:
| • | 任何违反董事对我们或我们的股东的忠诚义务的行为; |
| • | 不诚实信用的行为或者不作为,或者涉及故意不当行为或者明知违法的; |
| • | 非法支付股息或非法回购或赎回股票;以及 |
| • | 董事从中获得不正当个人利益的任何交易。 |
如果修改特拉华州法律以授权公司采取行动,进一步取消或限制董事的个人责任,则我们的 董事的责任将在修订后的特拉华州法律允许的最大范围内取消或限制。我们修订和重述的公司注册证书并不取消董事的注意义务,在适当的情况下, 根据特拉华州的法律,仍然可以获得衡平法救济,例如禁令或其他形式的非金钱救济。此条款也不影响董事根据任何其他法律(如联邦证券法或其他州或联邦法律)承担的责任。 根据我们修订和重述的附例,我们也将有权代表我们被要求或允许赔偿的任何人购买保险。
除了我们修订和重述的公司证书以及修订和重述的章程中所要求的赔偿外,我们打算在完成发售之前与我们的每一位董事会成员和我们的每一位高级管理人员签订一份赔偿协议 。这些协议规定,我们的董事和高级管理人员因他们在担任高级管理人员期间的任何行动、诉讼、法律程序或替代纠纷解决机制或听证、查询或调查可能导致上述情况,或由于他们在担任高级管理人员期间的任何行动或不作为而被 作为或曾是我公司或我们任何子公司的董事、高级管理人员、雇员、代理人或受托人,而 因他们是或曾是我们公司或我们的任何子公司的董事、高级管理人员、雇员、代理人或受托人,而导致上述行为、调查或调查而产生的某些费用和责任,可由 予以赔偿。或者 因为他们是应我们的要求作为另一个实体的董事、高级管理人员、员工、代理或受托人提供服务的。在由我公司或我公司任何子公司提起的诉讼或诉讼中,如果法院认定被赔方被禁止接受赔偿,则不会为任何索赔提供赔偿 。我们认为,这些章程和章程条款以及赔偿协议对于吸引和留住 名合格的董事和高级管理人员是必要的。
我们修订和重述的公司注册证书和修订和重述的章程中的责任限制和赔偿条款可能会阻止股东提起诉讼。
271
指控董事违反受托责任。它们还可能降低针对董事和高级管理人员的衍生品诉讼的可能性,即使一项诉讼如果成功,可能会 使我们和我们的股东受益。此外,如果我们根据这些赔偿条款向董事和高级管理人员支付和解费用和损害赔偿金,股东的投资可能会受到损害。鉴于根据证券法产生的责任可根据前述条款或其他规定对我们的董事、高级管理人员和控制人进行赔偿,我们已被告知,SEC认为,此类 赔偿违反证券法中所表达的公共政策,因此不能强制执行。没有任何未决的诉讼或程序点名我们的任何董事或高级管理人员寻求赔偿, 我们也不知道任何可能导致任何董事或高级管理人员要求赔偿的未决或威胁诉讼。
272
某些关系和关联方交易
除了与我们的董事和高管之间的薪酬安排,包括雇佣、终止雇佣和控制安排的变更,包括标题为管理薪酬和高管薪酬的章节中讨论的安排,以及股本登记权利说明章节中描述的登记权利,以下是自2017年1月1日以来的每笔交易以及目前提议的每笔交易的说明:
| • | 我们已经或将要成为参与者; |
| • | 涉案金额超过12万元;及 |
| • | 我们的任何董事、高管或持有超过5%的已发行股本的任何人,或这些个人或实体的任何直系 家庭成员或与这些个人或实体共享家庭的人,曾经或将拥有直接或间接的重大利益。 |
可转换优先股发行
从2017年9月 到2018年2月,我们以每股4.19152美元的收购价发行和出售了总计14,314,610股B系列可转换优先股,总收购价为6,000万美元。
从2019年2月到2019年8月,我们以每股9.75091美元的购买价格发行和出售了总计12,517,569股C系列可转换优先股,总购买价格为1.221亿美元。
从2020年9月到2020年10月,我们以每股10.06181美元的收购价发行和出售了总计24,599,042股D系列可转换优先股,总收购价为2.459亿美元。
我们可转换优先股的购买者包括实益拥有我们5%以上已发行股本和/或 在我们董事会的代表的风险投资基金。下表列出了这些实体支付的股份数量和总收购价。
在B系列可转换优先股融资中发行的可转换优先股
| 股东超过5% (1) |
的股份敞篷车 B系列 优先股 |
集料 购货价格(单位:千) |
||||||
| 莱克斯风险投资公司(Lux Ventures IV,L.P.)(2) |
2,385,769 | $ | 10,000 | |||||
| MDC Capital Partners(风险投资),LP(3) |
2,385,769 | $ | 10,000 | |||||
| DCVC机会基金II,L.P.(4) |
2,147,192 | $ | 9,000 | |||||
| 显而易见的风险投资II,L.P.(5) |
1,192,884 | $ | 5,000 | |||||
| Advantage Capital犹他州合伙人I,LLC(6) |
1,002,023 | $ | 4,200 | |||||
| 数据收集IV,L.P.(4) |
715,730 | $ | 3,000 | |||||
| 中西部社区发展基金VIII, L.L.C.(6) |
429,438 | $ | 1,800 | |||||
| (1) | 有关这些股东及其所持股权的更多详细信息,请参阅本招股说明书中题为主要股东的 部分。 |
| (2) | 见Lux Ventures,标题为主要股东。 |
| (3) | 见MDC Capital Partners,标题为?主要股东。 |
| (4) | 请参阅标题为主要股东的部分下的数据收集。 |
| (5) | 见“主要股东”部分下的“显而易见的风险投资”。 |
| (6) | 请参阅Advantage Capital在标题为主要股东的一节下。 |
273
在C系列可转换优先股融资中发行的可转换优先股
| 股东超过5% (1) |
的股份敞篷车 C系列 优先股 |
集料 购货价格(单位:千) |
||||||
| 苏格兰抵押投资信托公司。 |
5,127,726 | $ | 50,000 | |||||
| MDC Capital Partners(风险投资),LP(2) |
1,538,317 | $ | 15,000 | |||||
| 莱克斯联合投资机会公司(Lux Co-Investment Opportunities,L.P.)(3). |
1,025,545 | $ | 10,000 | |||||
| 数据收集IV,L.P.(4) |
615,327 | $ | 6,000 | |||||
| 显而易见的风险投资II,L.P.(5) |
512,772 | $ | 5,000 | |||||
| DCVC机会基金II,L.P.(4) |
410,218 | $ | 4,000 | |||||
| (1) | 有关这些股东及其所持股权的更多详细信息,请参阅本招股说明书中题为主要股东的 部分。 |
| (2) | 见MDC Capital Partners,标题为?主要股东。 |
| (3) | 见Lux Ventures,标题为主要股东。 |
| (4) | 请参阅标题为主要股东的部分下的数据收集。 |
| (5) | 见“主要股东”部分下的“显而易见的风险投资”。 |
在D系列可转换优先股融资中发行的可转换优先股
| 股东超过5% (1) |
的股份敞篷车 D系列 优先股 |
集料 购货价格(单位:千) |
||||||
| 拜耳阿克蒂恩格塞尔斯哈夫特 |
4,969,284 | $ | 50,000 | |||||
| 第三十五投资公司有限责任公司(2) |
3,975,427 | $ | 40,000 | |||||
| DCVC V.L.P.(3) |
2,484,642 | $ | 25,000 | |||||
| 苏格兰抵押投资信托公司。 |
2,484,642 | $ | 25,000 | |||||
| 莱克斯联合投资机会公司(Lux Co-Investment Opportunities,L.P.)(4) |
795,085 | $ | 8,000 | |||||
| 很明显是SPV I,L.L.C.(5) |
695,699 | $ | 7,000 | |||||
| MDC Capital Partners(风险投资),LP(2) |
496,928 | $ | 5,000 | |||||
| 中西部社区发展基金VIII, L.L.C.(6) |
372,696 | $ | 3,750 | |||||
| 莱克斯风险投资公司(Lux Ventures IV,L.P.)(4) |
198,771 | $ | 2,000 | |||||
| (1) | 有关这些股东及其所持股权的更多详细信息,请参阅本招股说明书中题为主要股东的 部分。 |
| (2) | 见MDC Capital Partners,标题为?主要股东。 |
| (3) | 请参阅标题为主要股东的部分下的数据收集。 |
| (4) | 见Lux Ventures,标题为主要股东。 |
| (5) | 见“主要股东”部分下的“显而易见的风险投资”。 |
| (6) | 请参阅Advantage Capital在标题为主要股东的一节下。 |
投资者权利协议
我们与我们股本的某些持有者签订了经修订的 投资者权利协议,其中包括Bayer Aktiengesellschaft、Data Collective IV、L.P.、DCVC Opportunity Fund II,L.P.、DCVC V,L.P.、Lux Co-Invest Opportunities,L.P.、Lux Ventures IV,L.P.、Object SPV I、L.L.C、Object Ventures II,L.P.、苏格兰抵押贷款投资信托基金Advantage Capital Utah Partner I,L.L.C.,Midwest Community Development Fund VIII,L.L.C.,Christopher Gibson,Blake Borgeson和Dean Li。根据我们的投资者权利协议,我们股本的某些持有者有 权利要求我们提交注册声明,或要求我们以其他方式提交的注册声明涵盖他们在我们股本中的股份。有关这些注册权的其他信息,请参阅标题为?股本注册说明 权利?的小节。
274
投票协议
我们与我们股本的某些持有者签订了经修订的投票协议,其中包括拜耳Aktiengesellschaft、Data Collective IV,L.P.、DCVC Opportunity Fund II,L.P.、DCVC V,L.P.、Lux Co Investment Opportunities,L.P.、Lux Ventures IV,L.P.、Object SPV I,L.L.C、Object Ventures II,L.P.、苏格兰抵押贷款投资信托基金(Scottish Mortgage Investment Trust Plc)、MDC Capital{L.P.、Thirty Five Investment Company L.L.C.、Advantage Capital Utah Partner I、L.L.C.、中西部社区发展基金VIII、L.L.C.、克里斯托弗·吉布森(Christopher Gibson)、布莱克·博格森(Blake Borgeson)和李院长。投票协议各方已 同意在一定条件下投票表决他们持有的我们的股本股份,以选举以下个人为董事:(1)Data Collective IV,L.P.指定的一名个人,现任Zachary Bogue,(2)Lux Ventures IV,L.P.指定的一名个人,现任Zavain Dar,(3)我们的首席执行官,现任Christopher Gibson,(4)一名由股东指定的占普通股已发行股票多数的个人 i)(A)当时正在为本公司提供服务或(B)截至2017年9月25日是本公司的全职员工,且未被本公司以(其中定义的)原因解雇(投票普通股持有人)和ii)犹他州大学研究基金会,UURF,现任Blake Borgeson,(5)由投票普通股持有者和UURF和UURF提名的一名个人,(2)UURF犹他大学研究基金会(UURF),现任布莱克·博格森(Blake Borgeson),(5)由投票普通股持有者和UURF提名的一名个人,以及作为一个单独的类别投票,以及可转换优先股的大多数流通股的持有人,作为一个单独的类别在转换为普通股的基础上投票,目前R.马丁·查韦斯(6)一名由投票普通股持有人和UURF提名并由普通股的多数流通股持有人选举产生的个人,作为一个单独的类别投票, 和可转换优先股多数流通股的持有人 ,按转换为普通股的基准作为单独类别投票,现任李院长,(7)由可转换优先股的多数流通股持有人 提名的一名个人,作为单独的类别和转换为普通股的基础投票,并由可转换优先股的多数流通股的持有人选举, 以转换为普通股的基础作为单独类别的投票, 投票为独立类别的可转换优先股, 由可转换优先股的大多数流通股的持有人选举, 在转换为普通股的基础上作为单独的类别投票, 由可转换优先股的多数流通股的持有人提名的个人,和大多数普通股流通股的持有人,作为一个单独的类别投票,目前是Robert Hershberg和 (8)一名个人,通过普通股的大多数流通股持有人的赞成票选出,作为一个单独的类别投票,以及作为一个单独的类别投票的可转换优先股的多数流通股的持有人, 在转换为普通股的基础上作为一个单独的类别投票,目前是Terry-Ann Burrell。本次发行完成后,投票协议各方 投票选出这些被提名者的义务以及本协议项下的其他权利和义务将终止,我们的股东将不再拥有任何有关提名、选举或指定我们董事会成员的特殊权利。我们现有的公司注册证书包含与投票协议相对应的有关选举董事会成员的条款;但是,在本次发行结束时生效的修订和重述的公司注册证书中,这些条款将被 删除。
赔偿协议
除了我们修订和重述的公司注册证书和章程中规定的赔偿外,我们还与我们的每位董事和高管签订了单独的赔偿协议。赔偿协议以及我们将在本次发售结束后生效的经修订的重述公司证书和章程要求我们在特拉华州法律允许的最大程度上赔偿 我们的董事、高管和某些控制人。有关更多信息,请参阅标题为《高管薪酬与责任限制和赔偿》的小节。
275
关联方交易政策
我们的审计委员会将主要负责审查和批准或不批准关联方交易,这些交易是我们与关联人之间的 交易,涉及的总金额超过或可能超过120,000美元,并且关联人在其中拥有或将拥有直接或间接的重大利益。我们审计委员会的章程将规定,我们的审计委员会应事先审查和批准任何关联方交易。
在 招股说明书(招股说明书是其组成部分)生效之前,我们打算采用正式的书面政策,规定未经我们的审计委员会同意,我们不得进行任何超过12万美元的交易,并且任何相关人士在其中都有直接或 间接的重大利益。在批准或拒绝任何此类交易时,我们的审计委员会将考虑现有和被认为与我们的审计委员会相关的相关事实和情况, 包括交易条款是否不低于在相同或相似情况下非关联第三方通常可获得的条款,以及相关人士在交易中的权益程度。
276
主要股东
下表列出了截至2020年12月31日,我们普通股的受益所有权:
| • | 我们所知的实益拥有我们普通股5%以上的每一个人或一组附属公司; |
| • | 每一位被提名的行政官员; |
| • | 我们的每一位董事;以及 |
| • | 我们所有现任高管和董事作为一个团队。 |
我们已根据证券交易委员会的规则确定实益所有权,因此它代表对我们的证券拥有 的单独或共享投票权或投资权。除非下面另有说明,据我们所知,表中列出的个人和实体对其实益拥有的所有股份拥有独家投票权和独家投资权,但须遵守适用的社区财产法 。该信息不一定表明受益所有权用于任何其他目的,包括交易法第13(D)和13(G)条的目的。
我们根据截至2020年12月31日的89,601,858股已发行普通股计算本次发售前的实益所有权百分比,在此之前,我们的可转换优先股的所有流通股已自动转换为我们的普通股。我们的 本次发行后受益所有权百分比的计算基于紧随本次发行完成后发行的普通股的股份 ,假设承销商没有行使购买额外股份的选择权。我们已将受股票期权约束的普通股股票视为未偿还股票,并由持有该股票期权的人实益拥有,以计算该人的所有权百分比。这些股票目前可在2020年12月31日后60天内行使或行使。但是,为了计算任何其他人的所有权百分比,我们没有将这些股票视为已发行股票。
277
除非另有说明,否则下表中列出的每个受益者的地址是c/o Recursion 制药公司,地址是德克萨斯州盐湖城格兰德街41 S号,邮编:84101。
| 实益拥有的股份 在此之前 |
实益拥有的股份 在这次献祭之后 |
|||||||||||||||
| 实益拥有人姓名或名称 |
股票 | 百分比 | 股票 | 百分比 | ||||||||||||
| 5%及更大股东: |
||||||||||||||||
| 莱克斯风险投资公司(Lux Ventures)(1) |
11,266,354 | 12.6 | % | |||||||||||||
| 数据集合(2) |
8,887,773 | 9.9 | % | |||||||||||||
| MDC Capital Partners(3) |
8,396,441 | 9.4 | % | |||||||||||||
| 苏格兰抵押贷款投资信托公司(4) |
7,612,368 | 8.5 | % | |||||||||||||
| 克里斯托弗·吉布森(5) |
6,353,588 | 7.1 | % | |||||||||||||
| 显而易见的风险投资(6) |
5,217,595 | 5.8 | % | |||||||||||||
| 布莱克·博格森(7) |
5,121,406 | 5.7 | % | |||||||||||||
| 优势资本(8) |
4,948,239 | 5.5 | % | |||||||||||||
| 拜耳阿克蒂恩格塞尔斯哈夫特(9) |
4,969,284 | 5.5 | % | |||||||||||||
| 被任命的高管和董事: |
||||||||||||||||
| 克里斯托弗·吉布森(5) |
6,353,588 | 7.1 | % | |||||||||||||
| 雷蒙娜·道尔(10) |
20,833 | * | ||||||||||||||
| 蒂娜·万豪·拉森(11) |
333,541 | * | ||||||||||||||
| 迈克尔·塞科拉(12) |
130,635 | * | ||||||||||||||
| 沙菲克·维拉尼(13) |
125,000 | * | ||||||||||||||
| 扎卡里·博格(14) |
8,887,773 | 9.9 | % | |||||||||||||
| 布莱克·博格森(7) |
5,121,406 | 5.7 | % | |||||||||||||
| Terry-Ann Burrell(15) |
14,583 | * | ||||||||||||||
| 马丁·查韦斯(R.Martin Chavez)(16) |
72,916 | * | ||||||||||||||
| 扎文·达尔(17) |
11,266,354 | 12.6 | % | |||||||||||||
| 罗伯特·赫什伯格(18) |
80,208 | * | ||||||||||||||
| 李院长(19) |
2,536,366 | 2.8 | % | |||||||||||||
| 所有现任执行干事和董事作为一个整体(12人)(20) |
34,922,368 | 38.8 | % | |||||||||||||
| * | 代表实益持有我们普通股流通股不到1%的股份。 |
| (1) | 由(A)9,445,724股由Lux Ventures IV,L.P.和(B)1,820,630股由Lux Co-Invest Opportunities,L.P.Lux Venture Partners IV,LLC登记持有,LLC是Lux Ventures IV,L.P.的普通合伙人,并对Lux Ventures IV,L.P.Lux Co-Invest Partners,LLC是Lux Co-Investment Opportunities,L.P.和L.P.彼得·赫伯特(L.P.Peter Hebert)和乔什·沃尔夫(Josh Wolfe)是Lux Venture Partners IV,LLC和Lux Co-Invest Partners,LLC的个人管理成员,或 个人经理。作为Lux Venture Partners IV,LLC和Lux Co-Invest Partners,LLC的唯一管理人,个人经理人可被视为分享本文提及的由Lux Ventures IV,L.P.和Lux Co-Invest Opportunities,L.P.持有的股份的投票权和处分权。Lux Venture Partners IV,LLC,Lux Co-Invest Partners,LLC和个人经理人分别否认对本文提及的股票的实益所有权 ,但他们的金钱除外这些实体和个人的地址是C/o Lux Capital Management,地址:纽约百老汇920号,11楼,NY 10010。 |
| (2) | 由(A)3,845,721股由Data Collective IV,L.P.或DCVC IV登记持有,(B)2,557,410股由DCVC Opportunity Fund II,L.P.或DCVC Opportunity Fund II记录持有,以及(C)2,484,642股由DCVC V L.P.或DCVC IV GP登记持有,是DCVC IV的普通合伙人。DCVC V GP是DCVC V的普通合伙人,Zachary Bogue和Matthew Ocko分别是DCVC IV GP、DCVC Opportunity Fund II GP和DCVC V GP的管理成员。Zachary Bogue和Matthew Ocko对DCVC IV、DCVC Opportunity Fund II和DCVC V持有的股份行使投票权和处置权。 |
| (3) | 包括(A)MDC Capital Partners(Ventures)LP登记在册的4,421,014股,以及(B)第三十五投资公司(Thirty Five Investment Company LLC)登记在册的3,975,427股。MDC Capital Partners(Ventures)LP和Thirty Five Investment Company LLC是穆巴达拉投资公司PJSC的全资子公司。列出的实体地址 |
278
| 这里是C/o Mubadala Capital,Al Sila Tower,Al Maryah Island,Abu Dhabi Global Market,4500,阿拉伯联合酋长国阿布扎比。 |
| (4) | 这些证券由苏格兰抵押贷款投资信托公司(SMIT)持有。作为SMIT的代理人,Baillie Gifford&Co可能被视为有权指导SMIT持有的证券的处置和投票。贝利·吉福德公司(Baillie Gifford&Co)否认对SMIT持有的所有股份拥有实益所有权。SMIT是一家上市公司。SMIT的 地址是C/o Baillie Gifford&Co,Calton Square,1 Greenside Row,EH1 3AN,UK。 |
| (5) | 包括(A)Gibson博士登记持有的6,211,922股股本(B)Gibson家族信托持有的100,000股股本 以及(C)1,000,000股受限于Gibson博士持有的期权的股份,其中41,666股可在2020年12月31日起60天内行使和归属。 |
| (6) | 包括(A)由显性SPV I、L.L.C.或显性SPV登记持有的695,699股,以及(B)由显性风险投资II、L.P.或Ov2持有的 登记在册的4,521,896股。明显SPV的管理者是明显生长GPⅠ、L.L.C.或OG1 GP。OG1 GP的管理成员James Joaquin、Vishal Vasishth、Andrew Beebe、Nan Li和Evan Williams可能被认为对明显SPV持有的股份拥有投票权和处置权。Ov2的普通合伙人是Ventures GP II、L.L.C.或Ov2 GP。Ov2 GP的管理成员James Joaquin、Vishal Vasishth、Andrew Beebe和Evan Williams可能被视为 对Ov2 GP持有的股份拥有共同投票权和处置权。APPLICE SPV、OV2、OG1GP和OV2GP的地址是220Halleck Street,Suite120,San Francisco,CA 94129。 |
| (7) | 包括博格森博士记录在案的股本。 |
| (8) | 包括(A)Advantage Capital Utah Partners I,L.P.或Advantage持有的1,022,023股,以及(B)中西部社区发展基金VIII,L.L.C.或中西部社区发展基金持有的3,946,216股 。Advantage的唯一成员是Advantage Capital Utah-MM-I,LLC或Advantage GP,中西部的管理成员是Advantage Capital Community Development Fund或ACCDF, Advantage GP和ACCDF分别以Advantage和Midwest的成员和经理身份行使投资酌处权,并控制Advantage和Midwest实益拥有的股票。Steven T.Stull可能被认为对Advantage和Midwest持有的记录在案的股票拥有投票权和投资权。与Advantage和Midwest关联的实体的地址是洛杉矶新奥尔良2230Poydras Street 909Suit2230,邮编:70112。 |
| (9) | 这些证券由拜耳Aktiengesellschaft或拜耳股份公司(Bayer AG)持有,拜耳股份公司是一家上市公司,根据德国法律成立并 作为股份公司存在。拜耳股份公司的任何个人股东或由三名或更少的个人股东组成的集团均无权作出拜耳股份公司的投资或投票决定,因此,拜耳股份公司的任何个人股东都不是股票的实益所有者。拜耳股份公司的地址是德国勒沃库森凯撒-威廉-阿利1,51373。 |
| (10) | 包括500,000股受Doyle博士持有的期权限制的股票,其中20,833股在2020年12月31日起60 天内归属并可行使。 |
| (11) | 包括(A)35,000股由Larson女士登记持有的股本及(B)575,000股由Larson女士持有的受期权 规限的股份,其中298,541股可于2020年12月31日起60天内行使及既有行使。 |
| (12) | 包括(A)由Secora先生登记持有的99,385股股本及(B)1,593,750股由Secora博士持有的受 期权约束的股份,其中31,250股可于2020年12月31日起60天内行使及归属。 |
| (13) | 包括(A)Virani博士登记持有的12,000股和(B)488,000股受Virani先生持有的期权约束,其中113,000股在2020年12月31日起60天内归属并可行使。 |
| (14) | 由上文脚注(2)所述股份组成。 |
| (15) | 包括291,667股,受制于Burrell女士持有的期权,其中14,853股在2020年12月31日起 60天内归属并可行使。 |
| (16) | 由350,000股受查韦斯博士持有的期权约束的股票组成,其中72,916股在2020年12月31日起60天内归属并可行使。 |
| (17) | 由上文脚注(1)所述股份组成。 |
| (18) | 由350,00股股票组成,受Hershberg博士持有的期权的限制,其中80,208股在2020年12月31日起60天内归属并可行使。 |
| (19) | 由(A)李博士登记持有的388,334股股份及(B)李院长及李嘉诚可撤销信托基金登记持有的2,148,032股股份组成。 |
| (20) | 包括(A)于2020年12月31日由我们现任行政人员及董事实益拥有的34,270,204股股份及(B)484,457股可于2020年12月31日起60天内行使的购股权,所有股份均于该日期归属。 |
279
股本说明
以下对我们股本的描述以及我们修订和重述的公司注册证书以及修订和重述的公司章程的某些规定 为摘要,仅限于参考将于本次发售完成后生效的修订和重述的公司注册证书和修订和重述的公司章程。这些文件的副本将作为我们注册说明书的证物提交给证券交易委员会,本招股说明书是其中的一部分。对普通股和优先股的描述反映了本次发行完成后我们的资本结构将发生的变化。
在本次发售完成并提交我们修订和重述的公司证书(将于 本次发售完成时生效)之前,我们的法定股本将包括普通股,每股票面价值0.00001美元,以及 优先股,每股票面价值0.00001美元。
在本次发行完成之前,我们的可转换优先股的所有流通股将自动转换为我们普通股的 股合计。
根据截至2020年12月31日的已发行普通股 ,并在紧接本次发售完成前将我们所有已发行的可转换优先股自动转换为普通股的总和以及本次发售中普通股的发行后,本次发售完成后将有 股已发行普通股。截至2020年12月31日,我们有11名登记在册的股东。
普通股
投票权
普通股的每位持有者在提交股东表决的所有事项上,包括选举 名董事,每股有权投一票。我们将于本次发售完成后生效的经修订及重述的公司注册证书及经修订及重述的章程并不规定累积投票权。正因为如此,有权在任何董事选举中投票的 股普通股的持有者可以选举所有参选董事,如果他们愿意这样做的话。关于董事选举以外的事项,除法律另有规定外,在任何出席或派代表出席 的股东大会上,亲自出席或委派代表出席该会议并有权就该事项投票的股份的多数表决权的赞成票应为股东的行为, 。在 股东的所有会议上,持有已发行和已发行股票的多数并有权投票、亲自出席或由其代表出席的股东应构成处理事务的法定人数。
分红
根据可能适用于任何当时尚未发行的优先股的优惠 ,我们普通股的持有者有权从我们的董事会不时宣布的合法可用资金中获得股息(如果有的话)。
清算
如果我们进行清算、 解散或清盘,我们普通股的持有者将有权在支付我们所有债务和其他债务并满足授予任何当时已发行的优先股持有人的任何 清算优先权后,按比例分享合法可分配给股东的净资产。
280
权利和优惠
我们普通股的持有者没有优先购买权、转换权、认购权或其他权利,也没有适用于我们普通股的赎回或偿债基金条款 。我们普通股持有人的权利、优先权和特权受到我们未来可能指定的任何系列优先股股票持有人的权利的制约,并可能受到这些权利的不利影响 。
全额支付和免税
我们所有的普通股流通股 将在本次发行中发行的普通股将在根据承销协议支付和交付时全额支付和免税。
优先股
本次发行完成后,我们的 董事会将有权在不需要股东采取进一步行动的情况下,发行一个或多个系列的最多优先股 ,并确定其权利、优惠、特权和限制。这些权利、优先权和特权可能包括股息权、转换权、投票权、赎回权、清算优先权、偿债基金条款和 组成任何系列的股份数量或该系列的名称,任何或所有这些都可能大于普通股的权利。优先股的发行可能会对普通股持有人的投票权以及这些持有人在清算时获得股息和支付的可能性产生不利影响。此外,优先股的发行可能会延迟、推迟或阻止我们的控制权变更或其他公司行动。 此次发行完成后,将不会有任何优先股流通股,我们目前也没有发行任何优先股的计划。
选项
截至2020年12月31日,根据我们的2020计划,我们拥有未偿还的 期权,可以购买我们普通股的总股票,加权平均行权价为每股$。
注册权
本次发售完成后,根据经修订的我们的投资者权利协议,普通股持有人或其 受让人将有权要求我们登记其股票的发售和出售,或将其股票包括在我们提交的任何登记声明中,每种情况如下所述。
要求登记权利
本次发行完成后,持有最多普通股的股东将有权获得特定的需求登记权。在2025年9月1日和本招股说明书组成的登记说明书生效后180 天之前,持有当时已发行的至少50%具有登记权的股份的持有者可以请求我们提交登记说明书,以 登记其股票的要约和出售。我们只有义务完成最多两个这样的注册。每个此类注册申请必须涵盖预期毛收入总额在扣除承销折扣和费用之前至少为500万美元的证券。这些需求注册权受特定条件和限制的约束,包括承销商有权限制任何此类 中包含的股票数量。
281
在某些情况下注册。如果我们确定实施这样的要求注册将对我们和我们的股东造成重大损害,我们有权推迟此类 注册,在任何12个月内不得超过两次,最长为180天。
表单S-3注册 权限
本次发行完成后,持有本公司普通股最多 股的持有者将有权获得某些表格S-3注册权。在 本次发售完成后的任何时间,当我们有资格以表格S-3提交登记声明时,当时拥有这些权利的股票持有人可以请求我们在表格S-3的登记声明中登记 其普通股的发售和出售,只要该请求涵盖预期公开发行总价至少为100万美元的证券。这些 股东可以在表格S-3的注册声明中提出不限次数的注册请求。但是,如果我们在申请日期之前的12个月内完成了三次此类注册,我们将不需要在表格 S-3上进行注册。这些表格S-3注册权受 特定条件和限制的约束,包括承销商在某些情况下限制任何此类注册中包含的股票数量的权利。此外,如果我们确定实施此类要求注册将对我们和 我们的股东造成严重损害,我们有权推迟此类注册,在任何12个月内不得超过两次,最长可达180天。
搭载登记权
本次发行完成后,持有最多普通股的持有者将有权享有某些搭便式注册权。如果我们提议根据证券法 登记我们普通股的发售和出售,这些股份的持有人可以请求我们将其股票纳入此类登记,但须受某些营销和其他限制,包括 承销商在某些情况下有权限制任何此类登记声明中包含的股份数量。因此,当我们建议根据《证券法》提交登记声明时,除非涉及(1)仅针对员工福利计划的登记,(2)与债务证券的发售和销售有关的登记,(3)与根据《证券法》颁布的第145条规定的公司重组或其他交易有关的登记,(4)任何不允许二级销售的登记表格上的登记,或(5)根据前两项 所述的要求或表格S-3登记权进行登记。这些股份的持有者有权获得登记通知,并有权在一定限制的情况下将其股份纳入登记。
注册的开支
除指定的例外情况外,我们将支付与任何需求注册、表格S-3注册和搭载注册相关的所有费用 。
终端
注册权终止于 (1)本次发售结束后两年的日期(2)紧接某些清算事件结束之前,以及(3)对于特定的登记权持有人而言,即本次发售结束后 该登记权持有人可根据证券法颁布的第144条在任何90天期间出售所有此类持有人的可登记证券的日期中最早的一个。
282
特拉华州法律的某些条款、我们修订和恢复的公司注册证书以及我们修订和重新修订的附例的反收购效果
特拉华州法律的某些条款以及将包括在我们修订和重述的公司证书以及以下概述的修订和重述的章程中的某些条款可能被视为具有反收购效力,并可能延迟、阻止或阻止股东可能认为符合其最佳 利益的要约或收购尝试,包括可能导致为股东持有的股票支付高于市场价格的溢价的尝试。
优先股
我们修订和重述的公司注册证书将包含一些条款,允许我们的董事会发行一个或多个系列的优先股,而无需股东的进一步投票或行动,并就每个此类系列确定组成该系列的股票数量和该系列的名称、该系列股票的投票权(如果有)以及该系列股票的权力、优先权或亲属、参与权、选择权和其他特别权利(如果有),以及任何资格、限制或限制。
分类董事会
我们修改并重述的公司注册证书 将规定,我们的董事会分为三个级别,指定为I类、II类和III类。每一类的董事人数将尽可能相等,占整个董事会总人数的三分之一 。首届一级董事任期至2022年年会之日止,首届二级董事任期至2023年年会之日 止,首届三类董事任期至2024年年会之日止。从2021年开始的每届年度股东大会上,在该年度会议上任期届满的董事级别将获得连任,任期三年。
罢免董事
我们修订和重述的公司注册证书将规定,股东只有在亲自或委派代表出席会议并有权投票的情况下,才能以不低于 多数的股份投票罢免董事。
董事空缺
我们修订和重述的公司注册证书将只授权我们的董事会填补空缺的董事职位。
无累计投票
我们修订并重述的公司注册证书将规定,股东无权在董事选举中累积投票权。
股东特别会议
我们修订和重述的公司注册证书以及修订和重述的章程将规定,除非法律另有要求 ,股东特别会议只能在我们的董事会多数成员、我们的董事会主席或我们的首席执行官的要求下由高级管理人员召开。
283
提名董事的预告程序
我们修订和重述的章程将规定,寻求在股东年度会议或特别会议 上提名董事候选人的股东必须及时提供书面通知。为了及时,股东的通知通常必须在公司秘书 发布会议通知之前送达我们的主要执行办公室并在那里收到,该通知在会议前不少于90天也不超过120天送达。尽管修订和重述的章程不会赋予董事会批准或不批准将在年会上当选的 候选人的股东提名的权力,但如果没有遵循适当的程序,修订和重述的章程可能会阻止某些业务在会议上进行,或者可能会阻止或阻止潜在的收购者 进行委托书征集以选举自己的董事名单或以其他方式试图获得公司的控制权。
经书面同意采取行动
我们修订和重述的公司注册证书以及修订和重述的章程将规定, 股东采取的任何行动必须在正式召开的股东年会或特别会议上进行,不得通过书面同意进行。
修改我们的 公司注册证书和章程
我们修改和重述的公司证书可以按照特拉华州公司法(DGCL)规定的任何方式进行修改或更改 。我们修订和重述的章程只有在获得当时普通股所有已发行股票 的至少多数投票权的批准后,才可由股东采纳、修订、更改或废除,但对上述条款的任何修订除外,这将需要我们当时已发行普通股的三分之二多数批准。此外,我们修订和重述的公司注册证书 将规定董事会可以修订、更改或废除我们的章程。
授权但未发行的股票
除纳斯达克上市标准要求外,我们授权但未发行的普通股和优先股将可供未来发行,无需股东批准。 可用于各种公司目的,包括未来发行以筹集额外资本、收购和员工福利计划。授权但 未发行和未保留的普通股和优先股的存在可能会使通过代理竞争、要约收购、合并或其他方式获得公司控制权的企图变得更加困难或受到阻碍。
专属管辖权
我们修订和重述的附例将规定,除非我们同意选择替代法院,否则特拉华州衡平法院将是代表我们提起的任何派生诉讼或诉讼、任何声称违反受托责任的诉讼 、任何主张根据DGCL提出的索赔的诉讼、任何关于我们修订和重述的公司注册证书或修订和重述的法律的诉讼、或者任何针对我们的索赔的诉讼 的唯一和排他性的诉讼场所。本条款不适用于为执行《交易法》规定的义务或责任而提起的诉讼,也不适用于美国联邦法院对其拥有专属管辖权的任何其他索赔。我们修订和重述的附例进一步规定,美利坚合众国联邦地区法院将是解决根据证券法提出的任何诉因的独家论坛。任何 个人或实体购买或以其他方式获得我们证券的任何权益,应被视为已通知
284
并同意这些规定。尽管我们认为这些条款为特定类型的诉讼和诉讼提供了更一致的法律适用,从而使我们受益,但 这些条款可能会起到阻止针对我们或我们的董事和高级管理人员提起诉讼的效果。法院是否会强制执行此类条款存在不确定性,其他 公司章程文件中类似选择的法院条款的可执行性在法律程序中受到了质疑。我们还注意到,股东不能放弃遵守(或同意不遵守)联邦证券法及其下的规则和条例。请参阅 标题为《风险因素与我们的修订和重述》的章节,这些修订和重述的章程将在本次发售结束后生效,规定特拉华州衡平法院和美国联邦地区法院将是我们与股东之间几乎所有争议的独家法庭,这可能会限制我们的股东就与我们或我们的董事、高级管理人员或 员工之间的纠纷获得有利的司法论坛的能力,这可能会限制我们的股东就与我们或我们的董事、高级管理人员或 员工之间的纠纷获得有利的司法论坛的能力。
与有利害关系的股东的业务合并
我们受DGCL第203条的管辖。除某些例外情况外,《DGCL》第203条禁止特拉华州上市公司 在该股东成为有利害关系的股东后的三年内, 与有利害关系的股东(一般定义为实益拥有该公司15%或以上已发行有表决权股票的任何人或与该人有关联的任何人)进行业务合并(如该条款所定义),除非(1)在此之前,该公司的董事会批准了该业务 合并或(br}与该人有关联的任何人),除非(1)在此之前,该公司的董事会批准了该业务 合并或与该股东有关联的任何人,除非(1)在此之前,该公司的董事会批准了该业务 合并或(2)在导致股东成为有利害关系的股东的交易完成后,有利害关系的股东在交易开始时拥有该公司至少85%的有表决权股票(不包括为确定该公司已发行的有表决权股票(但不包括由有利害关系的股东拥有的已发行有表决权股票),这些股份(A)由身为该公司董事和高级管理人员的人和(B)由员工股票计划拥有,在该员工股票计划中,员工参与者无权秘密确定是否持有{或(3)在该时间或之后,该企业合并由该公司的董事会批准,并在股东大会上(而不是经 书面同意)以至少662/3%的该公司的已发行有表决权股票的赞成票批准(而不是由该股东持有),而不是由感兴趣的股东拥有的至少662/3%的已发行有表决权股票的赞成票批准。
我们修订和重述的公司注册证书以及我们修订和重述的章程将规定,我们必须在DGCL授权的最大程度上对我们的董事和高级管理人员进行赔偿 。我们被明确授权购买董事和高级管理人员保险,为我们的董事、高级管理人员和某些员工提供部分责任保险。我们相信,这些 赔偿条款和保险有助于吸引和留住合格的董事和高管。
我们的公司证书和章程中对责任的限制 和赔偿条款可能会阻止股东对董事违反受托责任提起诉讼。这些规定还可能降低针对董事和高级管理人员提起衍生品诉讼的 可能性,即使此类诉讼如果成功,可能会使我们和我们的股东受益。此外,如果我们根据这些赔偿条款向董事和高级管理人员支付 和解和损害赔偿的费用,您的投资可能会受到不利影响。
上市
我们打算申请将我们的普通股在纳斯达克全球精选市场上市,代码为RXRX。
285
转会代理和注册处
本次发行完成后,我们普通股的转让代理和注册商将为 。转移代理和注册商的地址是。
286
有资格在未来出售的股份
在此次发行之前,我们的普通股还没有公开市场,虽然我们预计我们的普通股将被批准在纳斯达克全球精选市场上市 ,但我们不能向投资者保证,此次发行后我们的普通股将有一个活跃的公开市场。我们无法预测在公开市场上出售我们的股票或可供出售的股票 会对我们普通股的市场价格产生什么影响(如果有的话)。然而,未来在公开市场上出售大量普通股,包括行使已发行期权时发行的股票,或认为可能发生此类 出售的看法,可能会对我们普通股的市场价格产生不利影响,也可能对我们未来通过出售我们的普通股或其他与股权相关的证券筹集资金的能力以及我们认为合适的 价格产生不利影响。
本次发行完成后,根据我们截至2020年12月31日的已发行股票,并在使我们所有可转换优先股的流通股转换 生效后,我们的普通股将是流通股,或者 如果承销商行使了购买额外股份的选择权,我们的普通股将是流通股。预计在此次发行中出售的所有普通股股票将可以自由交易,不受限制,也可以根据证券法进一步注册,除非由我们的关联公司持有,这一术语在证券法第144条中有定义。我们普通股的剩余 流通股将被视为受限证券,这一术语在规则144中定义。仅当受限证券的发售和销售已根据《证券法》进行登记,或者这些证券的发售和销售符合豁免注册的条件(包括《证券法》第144条和第701条规定的豁免)时,才能在公开市场出售受限证券,具体内容如下。
根据下文描述的锁定协议和市场对峙条款 以及规则144或701的规定,我们普通股中将被视为受限证券的股票将可在本次发售完成后在公开市场上出售,如下所示:
| • | 于本招股说明书日期,任何股份均无出售资格;及 |
| • | 股票将有资格在 以下描述的锁定协议和市场对峙条款到期时出售,即本招股说明书日期后180天。 |
锁定协议和市场对峙协议
我们的高级管理人员、董事以及我们几乎所有股本和期权的持有者已经与我们签订了 市场对峙协议,并已经或将与承销商签订锁定协议,但在某些例外情况下, 在本招股说明书发布之日起至本招股说明书发布后180天期间,除非事先获得高盛公司的同意,否则不会处置或对冲其任何普通股或可转换为普通股或可转换为普通股的证券。 有关更多信息,请参阅标题为?承保?的小节。
规则第144条
目前有效的第144条规则 一般规定,一旦我们遵守交易法第13节或第15(D)节的上市公司报告要求至少90天,在之前90天内的任何时间都不被视为我们的附属公司的股东,并且实益拥有我们拟出售的股本股票的股东
287
在不遵守第144条的数量限制、销售方式或通知条件的情况下,有权依据第144条出售该等股票至少6个月。如果该 股东实益拥有我们拟出售的股本股份至少一年,则该股东有权依据规则144出售此类股票,而无需遵守规则144的任何其他条件。
规则144还规定,股东如果在之前90 天内的任何时间被视为我们的附属公司之一,并且实益拥有我们拟出售的普通股股票至少六个月,则有权根据规则144在本 招股说明书日期后90天后的任何三个月内出售不超过以下数额较大的股票:
| • | 我们当时已发行股本的1%,假设承销商没有行使购买额外股份的选择权,那么在本次发行完成后,这将 立即相当于股份; 或 |
| • | 在向 表格144提交有关此类出售的通知之前的4个日历周内,我们普通股的每周平均交易量。 |
如果股东在之前90天内的任何时间被视为我们的关联公司之一,则根据第144条的规定出售我们的股本也受第144条的当前公开信息、出售方式和通知条件的约束。
规则第701条
规则701一般规定,一旦 我们受到交易法第13条或第15(D)条的上市公司报告要求至少90天的约束,根据书面补偿利益计划或合同购买我们普通股股票的股东,如果在之前90天内的任何时候都不被视为我们的附属公司,则可以依据规则144出售此类股票,而不遵守规则144的当前公开信息或持有期条件 。规则701还规定,根据书面补偿福利计划或合同购买我们普通股股票的股东,如果在之前90天内被视为我们的关联公司之一 ,则可以根据规则144出售此类股票,而无需遵守规则144的持有期条件。然而,所有根据书面补偿福利计划或合同购买我们普通股股票的股东, 必须等到本招股说明书日期后90天,才能根据第701条出售该等股票。
注册权
本次发行完成后,持有最多 股我们普通股的持有者将有权根据证券法获得与此类股票登记相关的某些权利。根据证券法注册我们普通股的这些股票将导致这些股票在此类注册生效后立即不受证券法的限制而有资格在公开市场出售。 注册生效后,我们的普通股即有资格在公开市场出售,不受限制。 注册生效后,我们的普通股即可在公开市场出售。有关这些注册权的说明,请参阅标题为?股本注册权说明?的小节。
288
注册声明
本次发行完成后,我们打算根据证券法 提交一份S-8表格注册声明,以注册我们普通股的所有股票,但须遵守我们的股权奖励计划,或根据我们的股权补偿计划为发行而保留的股权奖励。受归属限制、规则144适用于关联公司的条件以及任何适用的市场对峙协议和锁定协议的 限制,此类注册声明涵盖的我们普通股股票将 在证券法生效后立即不受限制地在公开市场上出售。有关我们股权薪酬计划的 说明,请参阅标题为高管薪酬、员工福利和股票计划的章节。
289
美国联邦所得税对非美国普通股持有者的重要对价
以下是非美国持有者(定义如下)在本次发行中收购的普通股的所有权和处置权的重大美国联邦所得税 考虑事项的摘要,但并不是对所有与此相关的 潜在税务考虑事项的完整分析。本摘要基于1986年修订的《国内税收法典》或该法典的规定、根据该法典颁布的财政条例、行政裁决和司法裁决,所有这些都截至本摘要日期 。这些权限可能会发生变化(可能具有追溯力),从而导致美国联邦所得税后果不同于下文所述的后果。我们没有也不打算寻求 美国国税局(IRS)对以下摘要中的声明和结论做出任何裁决,也不能保证IRS或法院会同意此类声明和结论。
本摘要也不涉及替代最低税、对净投资收入征收的联邦医疗保险缴费税、根据任何非美国、州或地方司法管辖区的法律或根据美国联邦赠与和遗产、税收规则产生的税收考虑因素,也不涉及适用于投资者特殊情况的税收考虑因素 或可能受特殊税收规则约束的投资者,包括但不限于:
| • | 银行、保险公司、受监管的投资公司、房地产投资信托基金或其他金融机构; |
| • | 免税组织; |
| • | 养老金计划和符合税务条件的退休计划; |
| • | 受控外国公司、被动外国投资公司和积累收益以逃避美国联邦所得税的公司; |
| • | 证券、货币经纪、交易商; |
| • | 选择使用 按市值计价所持证券的核算方法; |
| • | 拥有或被视为拥有我们5%以上股本的人员(以下具体规定的除外); |
| • | 某些前美国公民或长期居民; |
| • | 合伙企业(或为美国联邦所得税目的归类的实体或安排)、其他直通实体及其投资者; |
| • | 在套期保值交易、跨境交易、转换交易或其他降低风险交易中持有我们普通股头寸的人; |
| • | 根据任何期权的行使或以其他方式作为补偿持有或接受我们的普通股的人; |
| • | 由于与我们普通股有关的任何毛收入项目被计入守则第451(B)节定义的适用财务报表中而受到特别税务会计规则约束的人员 ; |
| • | 不持有本公司普通股作为守则第1221条所指的资本资产的个人(一般为投资而持有的财产);或 |
| • | 根据守则的推定销售条款被视为出售我们普通股的人。 |
290
此外,如果根据 美国联邦所得税的目的被归类为合伙企业或直通实体的合伙企业、实体或安排持有我们的普通股,则合伙人的纳税待遇通常取决于合伙人的身份以及合伙企业或其他实体的活动。将持有我们普通股的合伙企业或其他此类实体 的合伙人应就通过合伙企业或其他此类实体(如果适用)拥有和处置我们普通股的税收后果咨询其自己的税务顾问。
我们敦促您就美国联邦所得税法在您的特定情况下的适用情况以及根据美国联邦赠与税或遗产税规则或根据任何州、地方、非美国或其他征税管辖区的法律或任何适用的税收条约购买、拥有和处置我们的普通股产生的任何税收后果咨询您的税务顾问 。
非美国持有者定义
在本讨论中,如果您是我们 普通股的实益所有者,且就美国联邦所得税而言,该普通股不是合伙企业(包括任何被视为合伙企业的实体或安排),则您是非美国持有者,或者:
| • | 是美国公民或居民的个人; |
| • | 在美国或根据美国或其任何行政区的法律成立或组织的公司或其他实体应纳税的公司或其他实体,或为美国联邦所得税目的而被视为公司的公司或其他实体; |
| • | 其收入应缴纳美国联邦所得税的遗产,无论其来源如何;或 |
| • | 信托(1)其管理受美国法院的主要监督,并且有一个或多个美国 人员有权控制该信托的所有重大决策,或(2)已根据适用的财政部法规作出有效选择,被视为美国人。 |
分配
正如题为股息政策的章节中所述,我们从未宣布或支付过股本的现金股息,我们预计在本次发行完成后不会支付任何现金股息。但是,如果我们对普通股进行分配, 这些支付将构成美国联邦所得税用途的股息,根据美国联邦所得税原则从我们当前或累计的收益和利润中支付。如果这些分配超过 我们当前和累积的收益和利润,超出的部分将构成资本回报,并将首先减少您在我们普通股中的基数,但不会低于零,然后将被视为出售股票的收益。
根据下面关于有效关联收入的讨论,以及在报告和报告外国账户税收合规法案(FATCA)和报告备份预扣和信息 一节中,通常向您支付的任何股息都将缴纳美国联邦预扣税,税率为股息总额的30%,或者 可能由美国和您居住的国家之间适用的所得税条约指定的较低税率。为了获得降低的协议率,您必须向我们提供正确签署的IRS表 W-8BEN或W-8BEN-E或其他适当版本的IRS Form W-8证明降低费率的资格 。如果根据所得税条约,您有资格享受美国联邦预扣税的降低税率,您可以通过向美国国税局提出适当的退款申请,获得任何超额预扣金额的退款。如果您通过金融机构或其他代理机构持有我们的普通股,
291
如果您代表持有者,您将被要求向代理商提供适当的文档,然后代理商将被要求直接或 通过其他中介向我们或我们的付款代理商提供认证。
您收到的被视为与您进行美国贸易或业务有效相关的股息 (如果适用的所得税条约要求,可归因于您在美国设立的常设机构或固定基地)通常免征美国联邦预扣税,这取决于下面标题为?备份预扣和信息报告?和??外国帐户税务合规法案,或FATCA的 部分中的讨论。要获得此项豁免,您必须向我们提供一份适当执行的美国国税局(IRS)。此类有效关联的股息虽然不需要缴纳美国联邦预扣税,但其税率与适用于美国 个人的税率相同,扣除某些扣除和抵免后,受适用的所得税条约另有规定的限制。此外,如果您是非美国公司持有者,您收到的与您在美国进行贸易或业务有关的股息 也可能需要缴纳30%的分支机构利得税,税率可能会低于美国和您居住的国家之间适用的所得税条约规定的税率, 根据某些项目进行调整。您应该咨询您的税务顾问,了解我们普通股所有权和处置的税收后果,包括任何可能规定不同规则的适用税收条约。
普通股处置收益
根据题为备份预扣和信息报告部分中的 讨论,您一般不会因出售或以其他方式处置我们的普通股而获得的任何收益缴纳美国联邦所得税,除非:
| • | 收益实际上与您在美国进行贸易或业务有关(如果适用的所得税条约 规定,收益可归因于您在美国设立的永久机构或固定基地); |
| • | 您是在发生出售或处置且满足某些其他条件的 日历年内在美国居住一段或多段时间(总计183天或更长时间)的个人;或 |
| • | 由于我们作为美国不动产控股公司或USRPHC的身份,我们的普通股构成美国不动产权益,在您处置我们的普通股或您持有我们的普通股之前的较短五年期间内的任何时间,出于美国联邦所得税的目的,除非我们的普通股 定期在成熟的证券市场交易,并且您始终直接、间接和建设性地持有不超过我们已发行普通股的5%,在截至应税 处置之日或您持有我们普通股之日的五年期间中较短的一个期间内。 |
我们认为,对于美国联邦所得税而言,我们目前不是也不会成为USRPHC,本讨论的其余部分也是这样假设的。然而,由于我们是否为USRPHC的决定取决于我们在美国的房地产相对于我们美国和全球房地产以及我们的其他业务资产的公平市场价值的公平市场价值,因此不能保证我们未来不会成为USRPHC。如果我们是USRPHC,并且我们的普通股没有定期在成熟的证券市场交易,或者您 在适用的测试期内直接或间接持有或被视为持有我们已发行普通股的5%以上,您通常将按与美国贸易或业务的 进行有效相关的收益相同的方式对任何收益征税,但分支机构利润税一般不适用。如果我们是USRPHC,并且我们的普通股不定期在成熟的证券市场交易,您从出售 股票获得的收益通常也将受到
292
按15%的费率扣缴。我们鼓励您咨询您自己的税务顾问,了解如果我们是或将要成为市建局的税务顾问可能会给您带来的后果。
如果您是上述第一个项目符号中描述的非美国持有人,您将被要求为根据常规美国联邦所得税税率出售所获得的收益 缴税(扣除某些扣除和抵免),并且上述第一个项目符号中描述的非美国公司持有人还可能按30%的税率或适用所得税条约指定的较低税率缴纳分行 利润税。如果您是上述第二个项目符号中所述的非美国个人持有人,您将按30%(或适用所得税条约指定的较低税率)的销售收益缴纳 税,如果您已及时提交有关此类损失的美国联邦所得税 报税表,则该收益可能会被当年的美国来源资本损失抵消。你应该向你的税务顾问咨询任何适用的所得税或其他可能规定不同规则的条约。
备份扣缴和信息报告
一般来说,我们 必须每年向美国国税局报告支付给您的股息金额、您的姓名和地址以及扣缴的税款(如果有)。我们将向您发送一份类似的报告。根据适用的所得税条约或其他协议,美国国税局可以 将这些报告提供给您居住的国家的税务机关。
出售给您的普通股的股息或收益的支付也可能按目前24%的税率进行备用预扣,除非您建立了豁免,例如,通过在正确填写的IRS表格 W-8BEN上正确证明您的非美国身份,或 W-8BEN或 W-8BEN或 W-8BEN W-8BEN W-8BEN或W-8BEN-E或另一个适当版本的美国国税局W-8表格。尽管 如上所述,如果我们或我们的付款代理实际知道或有理由知道您是美国人,则可能适用后备预扣。
备用预扣不是附加税;相反,接受备用预扣的人员的美国联邦所得税义务将减少 预扣税额。如果扣缴税款导致多缴税款,只要及时向美国国税局提供必要的信息,一般可以从国税局获得退税或抵免。
外国账户税收遵从法,简称FATCA
《外国账户税收合规法》(Foreign Account Tax Compliance Act)、据此发布的财政部条例和美国国税局(IRS)官方指南,或统称为FATCA,一般对股息征收30%的美国联邦预扣税,并在下文讨论某些拟议的财政部法规的前提下,对支付给外国金融机构的普通股出售或其他处置的毛收入征收30%的预扣税,除非该机构与美国政府达成协议,除其他事项外,扣缴某些款项,并收集并向美国税务机关提供有关该机构的美国账户持有人(包括 该机构的某些股权和债务持有人,以及某些具有美国所有者的外国实体的账户持有人)的实质性信息,或以其他方式建立豁免。FATCA通常还对向非金融外国实体(如这些 规则中特别定义)出售或以其他方式处置我们的普通股所得的股息征收30%的美国联邦预扣税,并根据下面对某些拟议的财政部法规的讨论 ,除非该实体向扣缴义务人提供识别该实体的主要直接和间接美国所有者的证明,证明它没有任何主要的美国所有者,或以其他方式建立 豁免。无论付款是否免征美国非居民预扣税和备用预扣税,都将适用预扣税,包括根据
293
上述其他豁免。在某些情况下,非美国持有者可能有资格获得此类税款的退款或抵免。 美国与适用的外国之间的政府间协定可以修改本节所述的要求。潜在投资者应就FATCA 预扣适用于他们在我们普通股的投资、所有权和处置问题咨询他们自己的税务顾问。
财政部长已经发布了拟议的财政部 法规,如果以目前的形式最终敲定,将取消FATCA关于支付出售或以其他方式处置我们普通股的毛收入的扣缴。美国财政部在其拟议的财政部条例的序言中表示,在最终法规发布之前,纳税人一般可以依赖拟议的财政部条例。
前面有关美国联邦税收考虑事项的讨论仅供参考。在投资者的特殊情况下,这不是给他们的税务建议。每个潜在投资者应就购买、持有和处置我们的普通股的特定美国联邦、州、地方和非美国税收后果咨询其自己的税务顾问,包括任何拟议的适用法律变更的后果。
294
承保
本公司与下列承销商已就本次发行的股票达成承销协议。在符合某些条件的情况下, 各承销商已各自同意购买下表所示数量的股票。高盛公司(Goldman Sachs&Co.LLC)和摩根大通证券公司(J.P.Morgan Securities LLC)是承销商的代表。
| 承销商 |
数量 股票 |
|||
| 高盛有限责任公司 |
||||
|
|
|
|||
| 摩根大通证券有限责任公司 |
||||
|
|
|
|||
| 美国银行证券公司 |
||||
|
|
|
|||
| SVB Leerink LLC |
||||
|
|
|
|||
| Allen&Company LLC |
||||
|
|
|
|||
| KeyBanc资本市场公司 |
||||
|
|
|
|||
| 总计 |
||||
|
|
|
|||
承销商承诺认购并支付以下期权涵盖的 股以外的所有要约股票(如果有),除非行使该期权。某些承销商可能会通过他们的一个或多个附属公司或销售代理提供和出售我们普通股的股票。
承销商有权向我们额外购买最多 股,以弥补承销商出售的股票数量超过上表所列总数。他们可以在30天内执行 该选项。如果根据此选择权购买任何股票,承销商将按上表所列的大致相同比例分别购买股票。
下表显示了我们支付给承销商的每股和总承保折扣和佣金。这些金额显示 假设没有行使和完全行使承销商从我们手中购买额外股份的选择权。
| 不是 锻炼 |
饱满 锻炼 |
|||||||
| 每股 |
$ | $ | ||||||
| 总计 |
$ | $ | ||||||
承销商向公众出售的股票最初将按本招股说明书封面上的首次公开募股(IPO)价格 发行。承销商出售给证券交易商的任何股票都可以在首次公开发行价格(br})的基础上以每股最高$的折让出售。股票首次发行后,代表人可以变更发行价和其他出售条件。承销商的股票发售以收到和接受为准,并受 承销商有权全部或部分拒绝任何订单的约束。
我们,我们的高级管理人员、董事和几乎所有普通股的持有者 已与承销商达成协议,除某些例外情况外,不得i)提供、质押、出售、合同出售、购买任何期权或合同、购买任何期权或合同、授予任何期权、权利或认购权证, 直接或间接出借或以其他方式转让或处置,或根据证券法向美国证券交易委员会提交或向美国证券交易委员会提交与以下事项有关的登记声明:我们普通股的任何股份或证券 可转换为或可行使或可交换为我们普通股的任何股份,或公开披露提出任何要约的意图,
295
出售、质押、贷款、处置或存档,或ii)达成任何互换或其他安排,转移与任何 普通股或任何此类其他证券的所有权相关的全部或部分经济后果(无论这些交易是否以现金或其他方式通过交付普通股或此类其他证券的股份来结算),在每种情况下,均未事先获得本招股说明书日期后180天内我们普通股股份以外的 书面同意如上所述,对我们行动的限制 将受到惯例例外的约束,不适用于某些交易。
高盛公司(Goldman Sachs&Co.LLC)和摩根大通证券公司(J.P.Morgan Securities LLC)可根据与上述承销商达成的任何锁定协议,在任何时候全部或部分释放证券。 本协议不适用于任何 现有员工福利计划。有关某些转让限制的讨论,请参阅本招股说明书标题为有资格未来出售的股份一节。
我们已同意赔偿承保人的某些责任,包括1933年证券法规定的责任。
在此次发行之前,这些股票还没有公开市场。首次公开募股价格已经在我们和 代表之间进行了协商。在确定股票首次公开募股价格时,除了当前的市场状况外,还将考虑我们的历史业绩、对我们的业务潜力和盈利前景的估计、对我们管理层的评估,以及与相关业务公司的市场估值相关的上述因素的考虑。
我们打算申请将我们的普通股在纳斯达克全球精选市场上市,代码为RXRX。
承销商可以在公开市场买卖普通股。这些交易可能包括卖空 、稳定交易和买入,以回补卖空建立的头寸。卖空涉及承销商出售的股票数量超过其在发行中所需购买的数量,空头头寸 代表未被后续购买覆盖的此类出售的金额。备兑空头头寸是指不超过上述承销商期权 可以行使的额外股票金额的空头头寸。承销商可以通过行使购买额外股票的选择权或在公开市场购买股票来回补任何被覆盖的空头头寸。在确定回补 空头头寸的股票来源时,承销商将特别考虑公开市场上可供购买的股票价格与他们根据上述期权购买额外股票的价格的比较。 n裸卖空是指任何产生的空头头寸大于可行使上述期权的额外股票金额的卖空行为。承销商必须通过在公开市场购买股票来回补任何此类赤裸裸的空头头寸。如果承销商担心定价后普通股在公开市场的价格可能存在下行压力,从而可能对购买此次发行的投资者产生不利影响,则更有可能建立裸空头头寸。稳定交易包括承销商在发行完成前在公开市场上对普通股进行的各种出价或购买。
承销商也可以实施惩罚性投标。当特定承销商向承销商偿还其收到的部分承销折扣 ,因为代表在稳定或空头回补交易中回购了该承销商出售或代其出售的股票时,就会发生这种情况。
回补空头和稳定交易的买入,以及承销商为自己的账户进行的其他买入,可能具有防止或延缓公司股票市场价格下跌的 效果,与实施惩罚性出价一起,可能会稳定下来。
296
维持或以其他方式影响普通股的市场价格。因此,普通股的价格可能会高于公开市场上可能存在的价格。 承销商不需要参与这些活动,并且可以随时结束任何这些活动。这些交易可能在纳斯达克进行,在 非处方药不管是不是市场。
某些承销商 及其关联公司过去曾向我们及其关联公司提供过某些商业银行、财务咨询、投资银行和其他服务,未来可能会在正常的业务过程中为我们及其关联公司提供某些商业银行、财务咨询、投资银行和其他服务,他们已经收取并可能继续收取常规费用和佣金。此外,某些承销商及其关联公司可能会不时为他们自己的账户或客户的 账户进行交易,并代表他们自己或他们的客户持有我们债务或股权证券或贷款的多头或空头头寸,并可能在未来这样做。
承销商及其关联公司是从事各种活动的全方位服务金融机构,这些活动可能包括销售和 交易、商业和投资银行、咨询、投资管理、投资研究、本金投资、对冲、做市、经纪和其他金融和非金融活动以及 服务。某些承销商及其各自的关联公司已经并可能在未来向发行人以及与发行人有关系的个人和实体提供各种此类服务,他们已收到或 将收到常规费用和开支。
在各项业务活动的正常过程中,承销商及其关联公司、高级管理人员、董事和员工可以购买、出售或持有广泛的投资,并为自己的账户和客户的账户积极交易证券、衍生品、贷款、商品、货币、信用违约互换和其他金融工具,此类投资和交易活动可能涉及或涉及发行人的资产、证券和/或工具(直接作为担保其他义务或其他担保的抵押品)和/或个人和实体。承销商及其各自的关联公司还可以就该等资产、证券或工具传达独立的投资建议、市场色彩或交易理念和/或发表或表达关于该等资产、证券或工具的独立研究观点,并可随时持有或向客户推荐他们应收购该等资产、证券和工具的多头和/或空头头寸。
限售
欧洲经济区潜在投资者注意事项
对于欧洲经济区的每个成员国,或在每一种情况下,对于一个相关国家,在发布有关证券的招股说明书之前,没有或将根据该相关国家向公众发行的证券 发行任何证券,该招股说明书已由该相关国家的主管当局批准,或在适当的情况下,在另一个相关国家批准并通知该相关国家的主管当局,所有这些都符合招股说明书条例的规定,但在该招股说明书发布之前,该等证券的要约可在该招股说明书发布前在该相关国家向公众发行,但在该招股说明书的规定下,可在该招股说明书中向公众发行该证券。
(A)招股章程规例所界定的合资格投资者的任何法人实体;
(B)少于150名自然人或法人(招股章程规例所界定的合资格 投资者除外),但须事先征得该代表的同意;或
(C)在招股章程规例第1(4)条所指的任何其他情况下,
297
但该等证券要约不得要求吾等或任何代表根据招股章程规例第3条 刊登招股章程或根据招股章程规例第23条补充招股章程。
就本 条款而言,就任何相关国家的证券向公众提供要约一词是指以任何形式和方式就要约条款和将要约的任何证券进行充分信息的沟通,以使投资者能够决定购买或认购任何证券,而招股说明书法规一词指的是(EU)2017/1129号条例(EU)2017/1129的意思是指以任何形式和方式就要约条款和将要约的任何证券进行沟通,以使投资者能够决定购买或认购任何证券,而招股说明书法规指的是(EU)2017/1129号条例。
英国潜在投资者须知
就英国而言,在刊登招股说明书之前,英国并无根据本次发售向公众发售普通股,招股说明书涉及i)已获得金融市场行为监管局 批准,或ii)将被视为已根据招股章程(修订等)第74条中的过渡性条款获得金融市场行为监管局批准的普通股。(欧盟退出) 2019年法规,但根据英国招股说明书法规的以下豁免,可以随时在英国向公众发出股票要约:
| • | 属于英国招股说明书条例第2条所界定的合格投资者的任何法人实体; |
| • | 向150名以下的自然人或法人(英国招股说明书 法规第2条所界定的合格投资者除外)出售;或 |
| • | 2000年《金融服务和市场法》第86条规定范围内的任何其他情形 |
但任何此类股份要约均不得要求发行人或任何代表根据FSMA 第85条刊登招股说明书,或根据英国招股说明书规例第23条补充招股说明书。
就本条款而言,就任何相关国家的任何股票向公众提供要约,是指以任何形式和方式就要约条款和将予要约的任何股份进行充分信息的沟通,以使投资者能够 决定购买或认购任何股份,而该词句是指根据2018年欧盟(退出)法案构成国内法律一部分的英国招股说明书法规(EU)2017/1129。
吾等并无授权亦不会授权代表其透过任何金融中介提出任何股份要约,但承销商就本招股说明书所预期的最终配售股份而提出的要约 除外。因此,除承销商外,任何股份购买者均无权代表吾等或 承销商提出任何进一步股份要约。
此外,在英国,本文档仅分发给且仅面向合格投资者(如英国招股说明书条例第2条所定义),且随后提出的任何要约仅面向在与修订后的《金融服务和市场法》2005年(金融促进)令第19(5)条 范围内的投资相关事项方面拥有专业经验的人,或该命令。和/或ii)属于命令第49(2)(A)至 (D)条范围内的高净值公司(或以其他方式可以合法传达给他们的人)(所有这些人统称为相关人士),或在没有也不会导致在 FSMA含义内向英国公众提供证券的情况下的高净值公司(或以其他方式可以合法传达给他们的人),或在其他情况下属于该命令第49(2)(A)至 (D)条的高净值公司(或以其他方式可能被合法传达的人)(所有该等人士合称为相关人士)。
298
在英国,任何非相关人员都不应采取行动或依赖本文档中包含的信息 ,或将其用作采取任何行动的基础。在英国,与本文件有关的任何投资或投资活动均可由相关人士独家进行或进行。
加拿大
根据National Instrument 45-106招股说明书豁免或证券法 (安大略省)第73.3(1)款的定义,证券只能在加拿大出售给作为本金购买或被视为购买的 购买者,并且是被允许的客户,如National Instrument 31-103注册要求、豁免和持续注册义务所定义。证券的任何转售必须根据 进行,豁免适用证券法的招股说明书要求,或在不受适用证券法招股说明书要求的交易中进行。
如果本要约备忘录(包括对其进行的任何修订)包含失实陈述,加拿大某些省或地区的证券法可以向购买者提供撤销或损害赔偿,前提是购买者在购买者所在省或地区的证券法规定的期限内行使撤销或损害赔偿。买方应参考 买方所在省或地区有关这些权利的证券法规的任何适用条款,或咨询法律顾问。
根据National Instrument 33-105承销冲突(NI 33-105)第3A.3节的规定,承销商无需遵守NI 33-105 关于与本次发行相关的承销商利益冲突的披露要求。
香港
在不构成“公司(清盘及杂项规定)条例”(第I章)所指的向公众提出要约的情况下,股份不得在香港以除本人以外的任何文件发售或出售 。香港法例第32条),或《公司(清盘及杂项规定)条例》,或不构成《证券及期货条例》(第32章)所指的向公众发出邀请 。香港法例第571条或《证券及期货条例》,或(Ii)《证券及期货条例》及根据该条例订立的任何规则所界定的专业投资者,或(Iii)在其他情况下不会导致该文件成为《公司(清盘及杂项条文)条例》所界定的招股章程,且不得为发行目的而发出或由任何人管有与股份有关的广告、邀请或文件(不论是否在香港香港公众(香港证券法允许的除外),但仅出售给或打算出售给香港以外的人士或仅出售给香港的专业投资者(如证券及期货条例及根据该条例制定的任何规则所界定的 )的股份则不在此限。(B)在香港的公众(根据香港证券法允许出售的除外),但只出售给或拟出售给香港以外的人士或只出售给香港的专业投资者(如证券及期货条例及根据该条例订立的任何规则所界定)。
新加坡
本招股说明书尚未在新加坡金融管理局注册为招股说明书。因此,本招股说明书以及与股票的要约或出售、认购或购买邀请有关的任何其他文件或材料不得分发或分发,也不得直接或间接向机构投资者(根据新加坡第289章证券和期货法案第4A节或国家证券监督管理局)向新加坡境内的其他人士发出认购或 购买邀请,也不得将其作为认购或 购买的邀请的标的。
299
SFA第275(2)条)根据SFA第275(1)条,或根据SFA第275(1A)条规定的任何人,或根据SFA第275条规定的条件,或iii)以其他方式依据并符合SFA的任何其他适用条款,在每种情况下均受SFA中规定的条件的约束。(br}SFA第275(2)条)或根据SFA第275(1)条,或根据SFA第275(1A)条规定的条件,或根据SFA第275(1A)条规定的条件,或iii)以其他方式依据和符合SFA的任何其他适用条款。
如果股份是由相关人士根据SFA第275条认购或购买的,而该人是一家公司(其唯一业务是持有投资,且其全部股本由一个或多个个人拥有,每个人都是认可投资者)(该公司不是经认可的 投资者(见SFA第4A条的定义)),该法团的证券(如本条例第239(1)条所界定)在该法团根据本条例第275条取得股份后6个月内不得转让,但以下情况除外:(1)根据本条例第274条向机构投资者或向有关人士(如本条例第275(2)条所界定)转让;(2)如转让是由根据本条例第275(1A)条对该法团的证券作出要约而产生的,(3)(4)如属法律的实施,(5)如“证券及期货条例”第276(7)条所指明,或(6)如“2005年新加坡证券及期货(投资要约)(股份及债券)规例”第32条所指明。
如果股票是由 相关人士根据国家外汇管理局第275条认购或购买的,而该相关人士是一个信托(受托人不是认可投资者(根据国家外汇管理局第4A条的定义)),而该信托的唯一目的是持有投资,并且该信托的每个受益人都是认可投资者,该信托中的受益人权利和利益(无论如何描述)在该信托根据SFA第275条获得股份后6个月内不得转让,但以下情况除外:(1)根据SFA第274条向机构投资者或向相关人士(如SFA第275(2)条所定义)转让;(2)如果转让的要约是以每笔交易不低于20万新加坡元(或其等值的外币)的代价获得的(无论该金额是以现金、证券交换或其他资产支付),(3)没有或将不会就转让给予对价,(4)如果转让是通过法律的实施,(5)按照国家外汇管理局第276(7)条的规定,或(5)按照国家外汇管理局第276(7)条的规定,(4)转让的权利或利益是以不低于 新加坡元(或等值的外币)的代价获得的,(3)没有或将会对转让给予任何代价,(4)如果转让是通过法律实施的,(5)按照国家外汇管理局第276(7)条的规定,或(
日本
这些证券没有也不会根据日本《金融工具和交易法》(1948年第25号法案,经修订)、 或FIEA注册。不得直接或间接在日本或为任何日本居民(包括任何在日本居住的个人或根据日本法律成立的任何公司或其他实体)或为其利益而直接或间接向任何日本居民或任何日本居民提供或出售证券 或向任何日本居民或为其利益而直接或间接再发售或转售证券,除非豁免了FIEA的注册要求,并以其他方式遵守日本任何相关的 法律和法规。
300
法律事务
本招股说明书中提供的普通股发行的有效性将由华盛顿州西雅图专业公司的Wilson Sonsini Goodrich&Rosati为我们传递。加利福尼亚州门洛帕克的Davis Polk&Wardwell LLP担任承销商的法律顾问。
专家
独立注册会计师事务所安永会计师事务所(Ernst&Young LLP)已审计了我们截至2019年12月31日的合并财务报表 以及报告中所述的该年度的合并财务报表。我们根据安永会计师事务所作为会计和审计专家的权威报告,将我们的财务报表包括在招股说明书和注册说明书的其他部分。
在那里您可以找到更多信息
我们已根据证券法以表格S-1的形式向证券交易委员会提交了一份关于本招股说明书提供的普通股 股票的注册声明。本招股说明书是注册说明书的一部分,并不包含SEC规则和 规定允许的注册说明书中列出的所有信息。关于我们和我们的普通股的更多信息,我们建议您参考注册声明,包括作为注册声明的一部分提交的展品。本招股说明书中包含的有关任何合同或任何其他文件内容的陈述不一定完整。如果已将合同或文件作为登记声明的证物存档,请查看已存档的合同或文件的副本。 本招股说明书中与作为证物存档的合同或文件相关的每一项陈述在所有方面都符合提交的证物的要求。SEC还维护一个互联网网站,其中包含招股说明书 包含的注册声明及其展品。这些文件以及未来的报告、委托书和其他有关我们的信息可在证券交易委员会的网站www.sec.gov上查阅。
作为此次发行的结果,我们将遵守《交易所法案》的信息和报告要求,根据该法, 将向证券交易委员会提交定期报告、委托书和其他信息。这些定期报告、委托书和其他信息将在证券交易委员会的公共参考机构和上述证券交易委员会的 网站上供查阅和复制。我们还在www.Recursion.com上维护了一个网站,在那里可以获得这些材料。完成本次发售后,您可以在 以电子方式向SEC提交或向SEC提供这些材料后,在合理可行的情况下尽快免费访问这些材料。本招股说明书中包含或可通过本招股说明书访问的信息不属于本招股说明书的一部分,本招股说明书中包含的本网站地址仅作为非活动的 文本参考。
301
递归制药公司
合并财务报表索引
| 独立注册会计师事务所报告 |
F-2 | |||
| 合并资产负债表 |
F-3 | |||
| 合并经营表和全面损失表 |
F-4 | |||
| 可转换优先股和股东亏损合并报表 |
F-5 | |||
| 合并现金流量表 |
F-6 | |||
| 合并财务报表附注 |
F-7 |
F-1
独立注册会计师事务所报告
致Recursion PharmPharmticals,Inc.的股东和董事会。
对财务报表的意见
我们审计了所附的Recursion PharmPharmticals,Inc.(本公司)截至2019年12月31日的综合资产负债表、截至该年度的相关综合经营表和全面亏损、可转换优先股和股东赤字及现金流 以及相关附注(统称为合并财务报表)。我们认为,合并财务报表在所有重要方面都公平地反映了本公司于2019年12月31日的财务状况,以及截至该年度的运营结果和现金流,符合美国公认会计原则。
意见基础
这些财务报表由 公司管理层负责。我们的责任是根据我们的审计对公司的财务报表发表意见。我们是一家在美国上市公司会计监督委员会(PCAOB) (PCAOB)注册的公共会计师事务所,根据美国联邦证券法以及美国证券交易委员会(SEC)和PCAOB的适用规则和法规,我们必须与公司保持独立。
我们是根据PCAOB的标准和美国公认的审计标准进行审计的。这些 标准要求我们计划和执行审计,以获得财务报表是否没有重大错报的合理保证,无论是由于错误还是欺诈。
我们的审计包括执行评估财务报表重大错报风险的程序(无论是由于错误还是欺诈),以及执行应对这些风险的 程序。这些程序包括在测试的基础上审查关于财务报表中的金额和披露的证据。我们的审计还包括评估使用的会计原则和管理层做出的重大估计,以及评估财务报表的整体列报。我们相信,我们的审计为我们的观点提供了合理的基础。
/s/安永律师事务所
自2017年来,我们一直担任本公司的审计师。
犹他州盐湖城
2021年1月26日
F-2
递归制药公司
合并资产负债表
(以千为单位, 不包括每股和每股金额)
| 十二月三十一日, 2019 |
||||
| 资产 |
||||
| 流动资产: |
||||
| 现金和现金等价物 |
$ | 69,883 | ||
| 受限现金 |
5,288 | |||
| 应收账款 |
151 | |||
| 其他流动资产 |
1,076 | |||
|
|
|
|||
| 流动资产总额 |
76,398 | |||
| 财产和设备,净值 |
24,370 | |||
| 其他非流动资产 |
663 | |||
|
|
|
|||
| 总资产 |
$ | 101,431 | ||
|
|
|
|||
| 负债、可转换优先股和股东亏损 |
||||
| 流动负债: |
||||
| 应付帐款 |
$ | 1,261 | ||
| 应计费用和其他负债 |
4,879 | |||
| 应付票据的当期部分 |
77 | |||
| 租赁激励义务的当期部分 |
467 | |||
|
|
|
|||
| 流动负债总额 |
6,684 | |||
| 递延租金 |
2,278 | |||
| 应付票据,扣除当期部分 |
12,418 | |||
| 租赁激励义务,扣除当期部分 |
3,207 | |||
|
|
|
|||
| 总负债 |
24,587 | |||
| 承担和或有事项(附注9) |
||||
| 可转换优先股(A、A-1、B和C系列),面值0.00001美元 ;61,712,989股授权股票;50,126,356股已发行和已发行股票;203,339美元的清算优先权 |
201,109 | |||
| 股东赤字: |
||||
| 普通股面值0.00001美元;授权发行100,000,000股;已发行14,425,074股,已发行 股 |
— | |||
| 额外实收资本 |
2,330 | |||
| 累计赤字 |
(126,595 | ) | ||
|
|
|
|||
| 股东赤字总额 |
(124,265 | ) | ||
|
|
|
|||
| 总负债、可转换优先股和股东赤字 |
$ | 101,431 | ||
|
|
|
|||
请参阅合并财务报表附注。
F-3
递归制药公司
合并经营报表和全面亏损
(单位为千,每股除外)
| 年终 2019年12月31日 |
||||
| 收入: |
||||
| 赠款收入 |
$ | 608 | ||
| 营业收入 |
1,711 | |||
|
|
|
|||
| 总收入 |
2,319 | |||
| 运营费用: |
||||
| 研发 |
45,809 | |||
| 一般事务和行政事务 |
18,951 | |||
|
|
|
|||
| 总运营费用 |
64,760 | |||
|
|
|
|||
| 运营亏损 |
(62,441 | ) | ||
| 其他收入,净额 |
562 | |||
|
|
|
|||
| 净亏损和综合亏损 |
$ | (61,879 | ) | |
|
|
|
|||
| 每股基本和稀释后净亏损 |
$ | (4.30 | ) | |
|
|
|
|||
| 基本普通股和稀释普通股的加权平均份额 |
14,380,177 | |||
|
|
|
|||
请参阅合并财务报表附注。
F-4
递归制药公司
可转换优先股和股东亏损合并报表
(单位为千,份额除外)
| 敞篷车 优先股 |
普通股 | 其他内容 已付清的-资本 |
累计 赤字 |
股东回报 赤字 |
||||||||||||||||||||||||||||||||
| 股票 | 金额 | 股票 | 金额 | |||||||||||||||||||||||||||||||||
| 2019年1月1日 |
37,608,787 | $ | 81,194 | 14,305,314 | $ | — | $ | 869 | $ | (64,716 | ) | $ | (63,847 | ) | ||||||||||||||||||||||
| 净损失 |
— | — | — | — | — | (61,879 | ) | (61,879 | ) | |||||||||||||||||||||||||||
| 提前行使股票期权的归属 |
— | — | — | — | 11 | — | 11 | |||||||||||||||||||||||||||||
| 股票期权的行使 |
— | — | 119,760 | — | 65 | — | 65 | |||||||||||||||||||||||||||||
| 发行C系列可转换优先股,扣除发行成本2,143美元 |
12,517,569 | 119,915 | — | — | — | — | — | |||||||||||||||||||||||||||||
| 基于股票的薪酬 |
— | — | — | — | 1,385 | — | 1,385 | |||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
| 2019年12月31日的余额 |
50,126,356 | $ | 201,109 | 14,425,074 | $ | — | $ | 2,330 | $ | (126,595 | ) | $ | (124,265 | ) | ||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
请参阅合并财务报表附注。
F-5
递归制药公司
合并现金流量表
(单位: 千)
| 年终 十二月三十一日, 2019 |
||||
| 经营活动的现金流 |
||||
| 净损失 |
$ | (61,879 | ) | |
| 对净亏损与经营活动中使用的现金净额进行调整: |
||||
| 折旧 |
3,543 | |||
| 基于股票的薪酬 |
1,385 | |||
| 租赁激励义务摊销 |
(499 | ) | ||
| 营业资产和负债变动情况: |
||||
| 应收账款 |
(27 | ) | ||
| 其他资产 |
632 | |||
| 应付帐款 |
(340 | ) | ||
| 应计费用、递延收入和其他流动负债 |
143 | |||
|
|
|
|||
| 用于经营活动的现金净额 |
(57,042 | ) | ||
| 投资活动的现金流 |
||||
| 购置物业和设备 |
(3,910 | ) | ||
|
|
|
|||
| 用于投资活动的净现金 |
(3,910 | ) | ||
| 融资活动的现金流 |
||||
| 出售优先股所得收益(扣除发行成本) |
119,915 | |||
| 行使股票期权所得收益 |
65 | |||
| 偿还长期债务 |
(11,183 | ) | ||
| 长期债务收益 |
11,888 | |||
| 债券发行成本的支付 |
(275 |
) | ||
|
|
|
|||
| 融资活动提供的现金净额 |
120,410 | |||
|
|
|
|||
| 现金、现金等价物和限制性现金净变化 |
59,458 | |||
| 期初现金等价物和限制性现金 |
15,713 | |||
|
|
|
|||
| 现金等价物和限制性现金,期末 |
$ | 75,171 | ||
|
|
|
|||
| 补充披露非现金投融资信息: |
||||
| 提前行使股票期权的归属 |
$ | 11 | ||
|
|
|
|||
| 补充披露现金流信息: |
||||
| 支付利息的现金 |
$ | 485 | ||
|
|
|
|||
请参阅合并财务报表附注。
F-6
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
1.业务和组织
业务概述
递归制药公司(Recursion PharmPharmticals,Inc.)或递归制药公司(Recursion)最初成立于2013年11月4日,并在特拉华州注册成立。
Recursion是一家生物技术公司,它结合了自动化、人工智能、机器学习、活体验证能力和高度 跨职能团队来发现新药,扩大了我们对生物学的集体理解。递归公司的机器人平台上生成的丰富、相关的生物图像数据库使先进的机器学习方法能够揭示候选药物、作用机制、新的化学物质和潜在的毒性,最终目标是解码生物学并推进新的疗法,从根本上改善人们的生活。 机器人平台 机器人平台使先进的机器学习方法能够揭示候选药物、作用机制、新的化学物质和潜在的毒性,最终目标是解码生物学并推动新疗法的发展,从而从根本上改善 人们的生活。
流动性、风险和财务状况
截至2019年12月31日,公司累计亏损126595美元。该公司预计在未来 期间将出现巨额运营亏损,并将需要额外资金来推进其候选药物。在公司与其子公司或与第三方合作成功完成重要的药物开发里程碑之前,公司预计不会从外部许可交易、开发里程碑或特许权使用费中获得大量收入 ,公司预计这将需要数年时间。为了将其候选药物 商业化,该公司或其合作伙伴需要完成临床开发并遵守全面的法规要求。该公司面临许多与生物技术行业内其他同等规模的公司类似的风险和不确定因素,例如临床试验结果的不确定性、额外资金的不确定性以及运营亏损的历史。
该公司还面临许多与早期企业相关的其他风险,包括竞争加剧、经营历史有限、 需要开发和完善其发现平台和开发运营、获得足够的资金来完成其开发活动、聘用管理层和其他关键人员、扩展其实验室流程以最大限度地提高生产能力 避免污染和其他导致平台停机的原因,以及整合整个公司团队的跨职能运营。成功完成公司的开发计划,并最终实现 盈利运营取决于未来事件,其中包括获得融资、吸引、留住和激励合格人员、高效管理供应链、经济高效地扩大和维护实验室运营以适应增长、保护知识产权和执行战略合作伙伴关系的能力。尽管管理层相信本公司将能够成功缓解这些风险,但不能保证 本公司能够做到这一点,也不能保证本公司将永远盈利。
截至2019年12月31日,公司没有任何 无条件的额外资金承诺。2020年8月27日,公司董事会批准出售和发行至多30,617,846股公司D系列优先股 ,面值为0.00001美元,并于2020年8月27日获得公司股东的批准。作为构成公司系列的综合交易系列的一部分
F-7
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
D优先股融资,所有未偿还可转换票据的持有人注销并交换其未偿还票据及其项下的所有义务,以换取本公司802,155系列D优先股 。包括交换可转换票据股票在内,该公司于2020年9月和10月发行和出售了23,367,659股、198,771股和1,032,612股D系列优先股,总收购价分别为233,507美元、2,000美元和10,390 美元(每股10.06美元)。
我们可能会被要求筹集额外的资本。如果公司无法 在需要时获得额外资金,则可能无法继续开发其产品,或者公司可能被要求推迟、缩减或放弃部分或全部开发计划和其他业务。任何额外的股权融资(如果向公司提供)可能不会以优惠条款提供,很可能会稀释现有股东的权益,而债务融资(如果有)可能涉及限制性契约和稀释融资工具。 如果公司通过合伙或许可安排获得资金,则可能需要放弃其某些技术或候选产品的权利,否则将寻求自行开发或商业化这些技术或产品,而获得此类资金的条款可能对公司不利。 如果公司通过合伙或许可安排获得资金,则可能需要放弃某些技术或候选产品的权利,否则这些技术或候选产品将自行开发或商业化。 获得此类资金的条款可能不利于公司在需要时获得资本的能力不能得到保证,如果不能及时实现,可能会对其业务、财务状况和 运营结果造成重大损害。
附注2.主要会计政策摘要
陈述的基础
随附的财务 报表是根据美国公认会计原则(GAAP)编制的。
段信息
我们已经确定,我们作为一个单一的运营部门运营,并有一个可报告的部门。公司的首席运营决策者是其首席执行官,他在综合层面上分配资源并评估业绩。
合并原则
合并财务报表包括该公司及其全资子公司的账目:在德国注册成立的递归制药有限公司和在美国注册成立的CereXis。所有重要的公司间余额和交易都已在合并中冲销。
预算的使用
按照公认会计原则编制财务报表要求管理层作出估计、判断和假设,这些估计、判断和假设会影响合并财务报表和附注中报告的金额。实际结果可能与这些估计值大不相同 。管理层做出的重要估计和假设包括长期资产(财产和设备)的估计寿命、基于股票发放的奖励的公允价值、临床试验应计费用以及用于确定我们的估值津贴的估计。
F-8
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
金融工具的公允价值
会计指引界定了公允价值,为计量公允价值建立了一致的框架,并扩大了按公允价值经常性或非经常性基础上计量的每项主要资产和负债类别的披露范围。公允价值是一种基于市场的计量,应该根据市场参与者在为资产或负债定价时使用的假设来确定。作为考虑此类假设的基础,会计准则建立了一个三级公允价值层次结构,对计量公允价值时使用的投入进行了优先排序,如下所示:
| 级别1: | 相同资产或负债在活跃市场上的报价。 |
| 级别2: | 除活跃市场报价外,直接或间接可观察到的可观察投入。 |
| 级别3: | 无法观察到的输入,其中市场数据很少或根本没有,这要求报告实体制定自己的 假设。 |
我们的金融工具包括现金等价物、应收账款、其他资产、应付账款和应计费用。这些工具的公允价值估计是根据相关市场信息在特定时间点进行的。这些估计可能是主观的,涉及不确定性和重大判断事项,因此无法精确确定 。现金等价物、应收账款、其他资产、应付账款和应计费用的账面金额通常被认为代表其各自的价值,因为这些工具具有短期性质 。本公司优先股权证负债的公允价值采用期权定价模型(第3级)进行估值。
信用风险集中
可能使公司面临集中信用风险的金融工具 包括现金和现金等价物。本公司的所有现金和现金等价物主要存放在管理层认为具有高信用质量的两家美国金融机构。这样的存款有时可能会超过联邦保险的限额。
现金和现金等价物及限制性现金
现金由存入支票账户和储蓄账户的银行存款组成。公司将购买期限为90天 或以下的所有高流动性投资视为现金等价物。
2019年,本公司开始与摩根大通建立新的商业银行关系。 公司需要在抵押账户中保持1,000美元的余额,以确保公司信用卡的安全。截至2019年12月31日,仅限于信用证抵押的现金为4288美元。这些金额 作为限制性现金计入综合资产负债表。
F-9
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
下表对合并资产负债表中报告的现金和现金等价物及限制性现金进行了对账,这些现金和现金等价物的总和与合并现金流量表中显示的相同金额的总和相同。现金和现金等价物以及限制性现金包括以下内容(以千计):
| 十二月三十一日, 2019 |
||||
| 现金和现金等价物 |
$ | 69,883 | ||
| 受限现金 |
5,288 | |||
|
|
|
|||
| 总计 |
$ | 75,171 | ||
|
|
|
|||
财产和设备
财产和设备按购置成本减去累计折旧入账。与财产和设备相关的正常、经常性或定期维修和维护 活动的成本在发生时计入费用。
折旧采用基于相关资产的 预计使用寿命的直线法计算。按资产分类估计的使用寿命一般如下:
| 软件/许可证 |
3年 | |
| 办公设备 |
5年 | |
| 计算机设备 |
5年 | |
| 实验室设备 |
7年 | |
| 租赁权的改进 |
较短的15年或租约的剩余时间 |
对财产和设备的减值进行审查,如下文长期资产减值会计部分所述 。
长期资产减值的会计处理
只要发生事件或环境变化 表明一项资产的账面价值可能无法收回,就会审查长期资产(如物业和设备以及需要摊销的无形资产)的减值情况。如果情况需要对长期资产或资产组进行潜在减值测试,本公司首先将该资产或资产组预计产生的未贴现现金流与其账面价值进行比较。如果长期资产或资产组的账面价值无法按未贴现现金流量法收回,则在账面价值超过 公允价值时确认减值。公允价值是使用各种估值技术来确定的,包括贴现现金流模型、报价市值和第三方独立评估,具体取决于资产的性质。截至2019年12月31日的 年度未发现任何减值。
租契
公司根据经营租赁协议租赁其设施,并根据租赁条款以直线方式确认相关租金费用。租赁协议包括租户改善津贴、租金假期、预定租金 上涨和续订选项。租房度假
F-10
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
在租赁期内记录的租金费用的确定中包括预定的租金上涨。本公司已就已发生但未支付的租金费用进行应计。在确定租赁期限时不会 假定续订,除非在租赁开始时认为它们得到了合理的保证。本公司自取得使用及控制租赁空间的法定权利之日起确认租金开支。 本公司的租约包括业主提供的租户改善津贴,用于对新空间进行结构性及美观的改动。租户改善津贴作为物业和设备入账,并承担相应的租赁 奖励义务,在各自的租赁期限内作为租金支出的减少额摊销。
收入确认
该公司采用了会计准则更新(ASU,2014-09)或ASC 606,自2019年1月1日起生效 使用完全追溯过渡方法。这些脚注中规定的所有披露都已更新,以符合新标准。采用ASC 606并未导致任何收入流、 应收账款或其他账户的会计处理发生变化;因此,没有记录累积影响调整。
赠款收入
本公司在根据赠款协议赚取收入的期间内确认赠款收入,该期间是 根据赠款协议产生相应的可报销费用的期间。在截至2019年12月31日的年度内,公司确认了608美元的赠款收入。
在截至2017年12月31日的年度内,本公司获得比尔和梅林达·盖茨基金会的私人赠款。2017年11月17日,比尔和梅林达·盖茨基金会根据这笔赠款向本公司发放了546美元。收入确认为执行了符合条件的活动。截至2019年12月31日,没有与此赠款相关的未赚取收入余额。截至2019年12月31日的一年中,与这笔赠款相关的确认收入为223美元。截至2019年12月31日,隔离账户中没有剩余金额可供资金使用。
在截至2018年12月31日的年度内,该公司获得了美国国立卫生研究院(National Institutes Of Health)的拨款,其中包括1,391美元的潜在资金。截至2019年12月31日的一年中,与这笔赠款相关的确认收入为385美元。截至2019年12月31日,潜在资金中仍有448美元。
营业收入
营业收入主要 是通过与武田药品工业株式会社签订的一项出资研发协议产生的(见附注13.合作和其他研发合同)。在截至2019年12月31日的年度内,公司 从与本协议相关的里程碑中确认了1,334美元的营业收入。
应收帐款
来自赠款的应收款项被记录为应付给公司的金额,该金额与美国国立卫生研究院的可报销研发费用有关。这些应收账款是
F-11
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
评估以确定是否应在每个报告日期建立任何准备金或津贴。截至2019年12月31日,该公司在美国国家卫生研究院有142美元的未付应收账款,所有这些应收账款都被视为应收账款。
发票提交给美国国家卫生研究院,与 可报销的研发成本相关。该公司还有权根据基本赠款协议中规定的费率获得间接费用的报销。该公司对其间接成本率的计算受到美国政府的审计 。
研发费用
研发费用包括进行研发活动所产生的成本,包括药物发现研究和药物开发研究、外部研究以及购买实验室用品的成本。公司根据适用合同中规定的活动完成情况确认与第三方合同服务相关的费用。在 终止与第三方的合同时,公司的财务义务仅限于迄今发生或承诺的成本。根据合同安排在未来的研究和产品开发活动中使用或提供的任何商品或服务的任何预付款都被归类为预付费用,直到提供此类商品或服务为止。
研究和开发费用和临床试验应计费用
作为编制财务报表过程的一部分,该公司需要估计 其根据与供应商、临床研究组织和顾问签订的合同以及临床现场协议承担的与进行临床试验相关的费用。这些合同的财务条款 有待协商,这些条款因合同而异,可能导致付款条款与此类合同提供材料或服务的期限不匹配。公司的目标是通过将这些费用与提供服务和付出努力的时间相匹配,在其财务报表中反映 适当的费用。公司根据费用的各个方面的时间对这些费用进行会计处理。 公司通过与相关人员和外部服务提供商就临床试验的进展或完成的服务进行讨论来确定应计估计。在临床试验过程中,如果实际结果与其估计的结果不同,公司 会调整其临床费用确认。该公司根据当时所知的事实和情况对截至每个资产负债表日的应计费用进行估计。实际 费用可能与应计金额不同。
利息支出和递延融资成本
截至2019年12月31日的年度的利息支出为635美元,主要与太平洋西部贷款协议和Midcap Financial Loan 协议(定义见附注5,ρ应付票据)有关。与贷款协议谈判和执行直接相关的成本已资本化,并从资产负债表上的应付票据中扣除。在前几年, 公司根据与太平洋西部公司的贷款协议授予购买A系列和B系列可转换优先股的认股权证。认股权证的初始公允价值已资本化,并与资产负债表 上的应付票据进行净额结算,并计入贷款有效期内的利息支出。相关认股权证负债的公允价值随后的变动记为
F-12
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
发生公允价值变动当年的其他收入或费用。资本化递延融资成本采用 实际利率法在贷款协议期限内摊销为利息支出。截至2019年12月31日的年度,计入利息支出的递延融资成本和原始发行折扣的摊销为36美元。截至2019年12月31日的年度,与随后重新计量认股权证相关的收入为11美元(br})。利息支出,以及与现金账户相关的1,741美元的利息收入,以及与权证重新计量相关的收入,都包括在 经营和全面亏损合并报表上的净其他收益中。
我们利用与正在进行的股权融资直接相关的某些法律、专业、会计和其他第三方费用作为递延发行成本,直到此类融资完成。完成此类融资后,这些成本将计入发行所产生的收益的减少额 。如果放弃计划的股权融资,递延发行成本将立即在综合经营和全面亏损报表中支出。
可转换优先股的分类与增值
本公司的可转换优先股在综合资产负债表上被归类为股东亏损以外的类别,因为该等股份的持有人 在被视为清算的情况下拥有清算权,而在某些情况下,该清算并不完全在本公司的控制范围内,并且需要赎回当时已发行的可转换优先股。 可转换优先股不可赎回,除非发生被视为清算的情况(见附注6.可转换优先股)。由于目前不太可能发生被视为清算事件, 可转换优先股的账面价值不会计入其赎回价值。只有当可能发生被视为清算事件时,才会对可转换优先股的账面价值进行后续调整。
基于股票的薪酬
公司在营业报表中确认 以股票为基础的薪酬支出,以及向员工和董事支付的所有以股票为基础的所有薪酬的全面亏损。本公司根据奖励授予之日的公允价值,记录奖励必需服务期或归属 期间的补偿费用。奖励通常授予员工四年以上的时间。该公司使用Black-Scholes期权定价模型来确定截至授予日每个期权授予的公允价值。 Black-Scholes期权定价模型需要输入无风险利率、股息收益率、预期股价波动性和期权的预期期限。期权的公允价值在必要的服务期内按直线确认为费用 (有关更多详细信息,请参阅附注8,基于股份的薪酬)。我们认识到当没收发生时,没收对基于股票的补偿费用的影响。我们将 费用确认的直线方法应用于所有仅具有基于服务的授予条件的奖励。
所得税
所得税财务报告采用资产负债法。递延收入余额反映公司资产和负债的财务报告和所得税基础之间的暂时性差异 的影响,并使用制定的税率来衡量。
F-13
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
预计在实际缴税或退税时适用。此外,递延税项资产计入利用净营业亏损(NOL)和研发抵免结转的未来收益,并使用颁布的税率和法律计量,这些税率和法律将在该等项目预期逆转时生效。
如果部分或全部递延税项资产很可能无法变现 ,则针对递延税项资产提供估值津贴。在作出该等厘定时,吾等会考虑所有可得的正面及负面证据,包括可用结转期间的应税收入、现有应课税暂时性差异的未来冲销、税务筹划策略及 不包括冲销暂时性差异及结转的未来应课税收入。
每股净亏损
每股基本净亏损的计算方法是,普通股股东应占净亏损除以当期已发行普通股的加权平均股数 。
由于本公司已发行符合参与证券定义的股份,因此本公司采用两级法计算其基本及 摊薄每股净亏损。两级法是一种收益分配公式,它将参与证券视为 拥有普通股股东本来可以获得的收益的权利。本公司的参与证券根据合约赋予该等股份持有人参与股息的权利,但不按合约要求持有该等股份的 名持有人分担本公司的亏损。因此,在公司报告净亏损的期间,此类亏损不会分配给此类参与证券。
由于本公司报告截至2019年12月31日的年度净亏损,稀释后每股净亏损与每股基本净亏损相同,因为 如果稀释普通股的效果是反稀释的,则不会假设其已发行。
新兴成长型公司
2012年的Jumpstart Our Business Startups Act或JOBS Act的第102(B)(1)节豁免新兴成长型公司遵守新的或修订后的财务会计准则,直到 要求非上市公司(即尚未宣布生效的证券法注册声明或没有根据交易法注册的证券类别) 遵守新的或修订后的财务会计准则。就业法案规定,新兴成长型公司可以选择退出延长的过渡期,并遵守适用于非新兴成长型公司的要求,但任何这样的选择退出都是不可撤销的。本公司已选择不退出延长的过渡期,这意味着当标准发布或修订时,如果标准对上市公司或私人公司有不同的应用日期,公司作为新兴成长型公司,可以在私人公司采用新的或修订的标准时采用新的或修订的标准。
这可能会使本公司的财务报表与另一家既不是新兴成长型公司也不是 新兴成长型公司的上市公司进行比较,后者因所用会计准则的潜在差异而选择不使用延长的过渡期。
F-14
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
近期会计公告
2016年2月,FASB发布了ASU 2016-02、租赁(主题842)或ASU 2016-02。根据主题842,公司将被要求确认租赁责任和使用权在每个租赁开始日期,所有租赁的资产 (短期租赁除外)。ASU 2016-02在2021年12月15日或之后开始的年度和过渡期内有效,允许提前采用 。本公司正在评估ASU 2016-02年度对其综合财务报表和相关披露的影响。公司将于2022年1月1日采用新标准。
注3.财产和设备
财产和 设备包括以下内容:
| 2019年12月31日 | ||||
| 实验室设备 |
$ | 16,113 | ||
| 租赁权的改进 |
12,897 | |||
| 办公设备 |
1,075 | |||
|
|
|
|||
| 30,085 | ||||
| 减去:累计折旧 |
(5,715 | ) | ||
|
|
|
|||
| 财产和设备,净值 |
$ | 24,370 | ||
|
|
|
|||
截至2019年12月31日的一年,物业和设备的折旧费用为3543美元。
附注4.应计费用和其他负债
应计 费用和其他负债包括:
| 2019年12月31日 | ||||
| 应计补偿 |
$ | 1,704 | ||
| 应计发展费用 |
941 | |||
| 应计物业税和租金费用 |
292 | |||
| 应计其他费用 |
1,942 | |||
|
|
|
|||
| 应计费用和其他负债 |
$ | 4,879 | ||
|
|
|
|||
附注5.应付票据
中型股 财务
2019年9月,本公司与Midcap Financial Trust或MidCap及其 其他贷款方签订了一项新的信用和安全协议,或Midcap贷款协议。Midcap贷款协议规定了一项定期贷款安排,其中包括:i)首批本金总额为11,888美元;以及ii)第二批本金总额最高为15,000美元,如果提取,将产生总计26,888美元的未偿还最高本金金额。第二批资金将在3月31日之前供公司借款。
F-15
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
2021年,在某些药物开发里程碑实现后。该公司使用首期定期贷款的一部分,以11,199美元全额偿还其根据下文所述的太平洋西部银行贷款协议 未偿还的定期贷款。根据Midcap贷款协议,定期贷款的收益可用于一般企业用途。截至2019年12月31日,中型股贷款协议下的未偿还本金余额为11,888美元。
中型股定期贷款的利息按未偿还本金计提,年利率等于伦敦银行同业拆借利率(LIBOR)加5.75%,每月支付欠款。本公司须在2019年9月至2021年9月期间只支付利息,此后每月支付36笔本金330美元外加利息,从2021年10月开始,一直持续到2024年9月到期日。如果公司实现了某些筹资相关的里程碑,仅限利息的期限将再延长12个月。
本公司可随时自愿预付中型股定期贷款,但须遵守若干最低还款要求及预付费用。MidCap 定期贷款必须用某些伤亡事件和资产出售的收益强制提前还款。
债务以本公司几乎所有资产为抵押 。Midcap贷款协议包括标准的肯定和限制性契约,包括限制本公司及其子公司处置 资产、授予某些许可证、进行投资、合并或完成收购、招致债务、授予留置权以及进行股息或分派的能力(除某些例外情况外)的契约。贷款协议还包括 违约的标准事件,包括(在某些情况下受宽限期限制)付款违约、违反契诺、违反陈述和担保、与某些其他债务的交叉违约、资不抵债和破产违约、 公司或任何子公司的控制权变更,以及公司业务、运营或条件的重大不利变化。一旦发生违约事件,MidCap可宣布所有立即到期和应付的未偿债务, 将适用利率提高2%,并采取信用与担保协议中规定的其他行动。截至2019年12月31日,本公司遵守所有债务契约。
2019年,本公司支付了与发起信贷和担保协议相关的费用约298美元。该等费用已递延 ,并记作直接从应付贷款账面价值中扣除,并于信贷协议余下期限内摊销为利息开支。
太平洋西部
2016年12月,本公司与太平洋西部银行(简称太平洋银行)签订贷款和担保协议,提供本金总额高达4,000美元的定期贷款,或太平洋贷款协议。2018年2月,本公司与太平洋修订了贷款协议 ,将定期贷款承诺总额提高至本金总额16,199美元,其中本公司借款11,199美元。太平洋贷款协议项下的定期贷款以本公司除知识产权以外的几乎所有资产作为抵押。根据最初的太平洋贷款协议和修订,该公司发行了太平洋完全既有认股权证,以购买A系列优先股和B系列优先股。认股权证的初始公允价值被记录为直接从应支付票据的账面价值中扣除。
F-16
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
合并资产负债表,在贷款协议期限内作为利息支出摊销。认股权证按公允价值作为负债计入综合资产负债表 。认股权证负债的公允价值变动在综合经营和全面亏损报表中记为其他收入或费用。有关认股权证的更多信息,请参阅备注8?基于股份的薪酬。
2019年9月,公司全额偿还了与太平洋西部协议相关的所有未偿还定期贷款。在2019年财政年度确认了与注销未摊销债务发行成本、未摊销认股权证和最终付款费用有关的 债务清偿亏损555美元。这一损失包括在 综合经营报表和全面亏损中的其他净收益中。
2018年5月8日,太平洋为公司房东的利益签发了面值为3,800美元的不可撤销备用信用证,以确保与租户改善相关的某些公司义务。截至2019年12月31日,未偿还信用证为3800美元,公司持有4288美元的限制性现金作为抵押品。
可转换票据
2020年3月13日和2020年4月9日,公司发行了本金总额为6400美元的可转换本票。如果 公司通过发行总收益至少为50,000美元的优先股筹集资金,可转换票据将自动转换为公司的优先股,价格为优先股股东支付的每股价格的80%。 如前所述,这些股票在2020年9月转换为D系列优先股802,155股。
中型股贷款协议应付票据 和租户改善津贴
2018年,该公司还选择从我们的 房东处额外借款992美元,用于改善租户状况。有关更多信息,请参见附注9?承付款和或有事项。根据租赁条款,票据将在10年内按8% 利率偿还。
中型股贷款协议和租户改善津贴的应付票据包括 以下内容:
| 2019年12月31日 | ||||
| 应付票据的当期部分 |
$ | 77 | ||
| 应付票据的长期部分 |
12,693 | |||
| 减少未摊销发行成本 |
(275 | ) | ||
|
|
|
|||
| 应付票据净额 |
$ | 12,495 | ||
|
|
|
|||
F-17
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
下表显示了截至2019年12月31日公司债务本金偿还义务的相关信息 :
| 截至十二月三十一日止的年度, |
||||
| 2020 |
$ | 77 | ||
| 2021 |
1,074 | |||
| 2022 |
4,052 | |||
| 2023 |
4,060 | |||
| 2024 |
3,077 | |||
| 此后 |
430 | |||
|
|
|
|||
| 债务本金支付总额 |
$ | 12,770 | ||
|
|
|
注6.可转换优先股
2013年11月,本公司根据特拉华州法律成立,名称为Recursion PharmPharmticals,LLC,一家有限责任公司。在2014年3月至2015年11月期间,公司发行和出售了3872美元的可转换本票本金。
2016年9月,作为构成本公司A系列优先股融资的综合系列交易的一部分,所有未偿还可转换本票持有人注销并交换了其未偿还本票及其项下的所有义务 ,以换取本公司3,817,836股A系列优先股和3,317,014股A-1优先股。在这种交换之后,Recursion PharmPharmticals LLC立即从特拉华州的一家有限责任公司转换为特拉华州的Recursion PharmPharmticals,Inc.,每个未完成的普通单位、A系列优先单位和A-1系列优先单位在一对一分别为普通股、A系列优先股和A-1系列优先股的股票基准。2016年9月和11月,本公司分别发行和出售了12,119,208股和1,994,834股A系列优先股,总收购价分别为12,910美元和2,125美元(每股1.06525美元)。
2017年7月,作为构成公司B系列优先股融资的综合系列交易的一部分,公司发行了 并出售了2,045,292股A系列优先股,总收购价为2,179美元(每股1.06525美元)。2017年9月和2018年2月,公司分别发行和出售了13,312,580股和1,002,023股B系列优先股,总收购价分别为55,800美元和4,200美元(每股4.19152美元),减去发行成本87美元。
2019年2月,公司 发行并出售了11,511,733股C系列优先股,总购买价为112,250美元(每股9.75091美元)。在截至2019年6月和8月的一系列额外交易中,该公司额外发行和出售了951,190股C系列优先股 ,总收购价为9,275美元(每股9.75091美元),减去2,143美元的发行成本,其中包括54,646股C系列优先股,作为向第三方的支付,公允价值为533美元(每股9.75091美元)。
F-18
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
可转换优先股包括以下内容:
| 2019年12月31日 | ||||||||||||||||||||
| 择优 股票 授权 |
择优 已发行股份 和 杰出的 |
携带 价值 |
清算 偏好 |
的股份 普普通通 可发行股票 vt.在.的基础上 转换 |
||||||||||||||||
| A系列优先股 |
20,052,268 | 19,977,170 | $ | 19,390 | $ | 21,281 | 19,977,170 | |||||||||||||
| A系列-1优先股 |
3,317,014 | 3,317,014 | 1,891 | — | 3,317,014 | |||||||||||||||
| B系列优先股 |
14,343,707 | 14,314,603 | 59,913 | 60,000 | 14,314,603 | |||||||||||||||
| C系列优先股 |
24,000,000 | 12,517,569 | 119,915 | 122,058 | 14,857,528 | |||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
| 可转换优先股总额 |
61,712,989 | 50,126,356 | $ | 201,109 | $ | 203,339 | 52,466,315 | |||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
清算优先权
如果公司发生任何清算、解散或清盘,无论是自愿的还是非自愿的,C系列优先股、B系列优先股和A系列优先股的持有人有权在同等基础上优先于将公司的任何资产分配给 A-1系列优先股或普通股的持有人,金额相当于:1)A-1系列优先股或普通股的原始发行价为每股9.75091美元B系列优先股每股4.19152美元 和A系列优先股每股1.06525美元,以及II)均以未支付股息(如果有)宣布。如果在公司清算、解散或清盘时,公司合法可供分配给C系列优先股、B系列优先股和A系列优先股持有人的资产不足以支付上述规定的全部金额,则 本公司合法可供分配的全部资产应按同等优先级和比例在C系列优先股、B系列优先股和A系列优先股持有人之间按其本来应支付的全额分配。 如果公司被清算、解散或清盘,公司合法可供分配给C系列优先股、B系列优先股和A系列优先股的资产不足以支付上述规定的全部金额,则公司合法可供分配的全部资产应在C系列优先股、B系列优先股和A系列优先股持有人之间按同等优先级和比例分配。
股息拨备
当董事会宣布时,C系列优先股、B系列优先股、A系列优先股和A-1系列优先股的流通股持有人有权在董事会宣布时从合法可用的任何资产中获得股息,优先于该日历年度普通股的任何 声明或支付。获得优先股股息的权利不是累积性的,优先股持有者没有因未宣布或支付优先股股息而获得股息的权利 。截至2019年12月31日,无累计拖欠或拖欠股息。
转换 权限
如上文所述,C系列优先股、B系列优先股、A系列优先股和A-1系列优先股的每股流通股可转换为C系列、B系列、A系列和A-1系列原始发行价除以分别为8.2152美元、4.19152美元、1.06525美元和1.06525美元 的C系列、B系列、A系列和A-1系列转换价格所确定的缴足股款和不可评估普通股数量。
F-19
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
每股可转换优先股应在紧接确定承诺包销公开发售结束前自动转换为缴足股款和不可评估普通股,每股价格至少为9.75091美元,且总收益不低于 $90,000美元,或在本公司收到当时已发行优先股的多数持有人提出的书面转换请求后自动转换为普通股(作为单一类别投票,并按转换为 普通股的基准进行投票)。由于股票分红、拆分和其他股权结构交易,以及随后以较低的实际价格出售普通股,可转换优先股的转换价格可能会进行调整。
投票权
每股可转换优先股 的持有者有权获得与该股可转换为普通股的股数相等的表决权。
资产负债表分类
本公司的可转换优先股在综合资产负债表上被归类为股东赤字以外的类别,因为该等股份的持有人在被视为清盘的情况下拥有清算权,而在某些情况下,该等股份并非完全在本公司的控制范围内,因此需要赎回当时尚未发行的可转换优先股。可转换优先股不可赎回,除非发生被视为清算的事件。
注7.普通股
每股普通股使 股东有权对提交公司股东表决的所有事项投一票。普通股股东有权获得公司董事会可能宣布的股息。截至2019年12月31日,未宣布分红 。
截至2019年12月31日,授权发行普通股1亿股,其中流通股分别为14,425,074股 股。
此外,公司还预留了以下普通股供发行:
| 2019年12月31日 | ||||
| A系列优先股的转换 |
19,977,170 | |||
| A-1系列优先股的转换 |
3,317,014 | |||
| B系列优先股的转换 |
14,326,532 | |||
| C系列优先股的转换 |
24,000,000 | |||
| A系列权证的转换 |
75,098 | |||
| B系列认股权证的转换 |
17,175 | |||
| 2016股权激励计划 |
9,818,483 | |||
| 关键人员激励计划 |
898,711 | |||
|
|
|
|||
| 预留供发行的普通股总股份 |
72,430,183 | |||
|
|
|
|||
F-20
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
注8.基于股份的薪酬
股票期权
关键人员激励计划
2013年11月,公司通过了关键人员激励计划或KPI计划,并预留了300万个公司普通股用于出售和 根据KPI计划发行。KPI计划规定向公司的员工、非员工董事和顾问授予受限单位和非法定期权奖励 。截至2019年12月31日,根据KPI计划,购买总计898,711股普通股的期权仍未偿还。截至2019年12月31日,根据KPI 计划,没有普通股可供授予。
关键绩效指标计划规定及早行使期权。在行使时,该期权持有人将获得本公司普通股,但受 回购权失效的限制。该人士终止后,本公司可行使权利,以购股权持有人支付的行使价回购任何未归属股份。
2016股权激励计划
2016年8月, 公司董事会和股东通过了2016年度股权激励计划。2016年计划保留了购买总计9999,077股普通股的期权。根据2016年计划,公司可以授予购买普通股、股票增值权、限制性股票奖励和其他形式的基于股票的薪酬的选择权。股票期权一般在四年内授予,不晚于授予之日起10年内到期。董事会 有权选择被授予期权的员工并决定每个期权的条款,包括i)受期权约束的普通股数量;ii)期权何时可行使;iii)期权行使价,必须至少为授予之日普通股公平市值的100%;iv)期权的期限,不得超过10年。(3)董事会有权选择被授予期权的员工,并决定每个期权的条款,包括:i)受期权约束的普通股股票数量;ii)期权何时可行使;iii)期权行权价格,必须至少为授予日普通股公平市值的100%;iv)期权期限,不得超过10年。
截至2019年12月31日,购买总计5785,079股普通股的期权仍未偿还,根据2016年计划和KPI计划,仍有4,932,115股可供 授予。
F-21
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
截至2019年12月31日的年度股票期权活动如下:
| 股份标的 至选项 杰出的 |
加权的- 平均资助金 日期 公允价值 |
加权的- 平均运动量 价格 |
加权平均 剩余合同 寿命(以年为单位) |
集料 固有的 价值 |
||||||||||||||||
| 未偿还金额2019年1月1日 |
4,632,804 | $ | 0.57 | $ | 0.94 | 8.39 | $ | 11,064 | ||||||||||||
| 授与 |
1,775,000 | 2.01 | 3.33 | 9.52 | ||||||||||||||||
| 取消 |
(502,965 | ) | 1.00 | 1.73 | 8.37 | |||||||||||||||
| 练习 |
(119,760 | ) | 0.30 | 0.55 | 6.81 | 333 | ||||||||||||||
|
|
|
|||||||||||||||||||
| 未偿债务,2019年12月31日 |
5,785,079 | $ | 0.97 | $ | 1.62 | 7.92 | $ | 9,910 | ||||||||||||
|
|
|
|||||||||||||||||||
| 于2019年12月31日归属并可行使 |
2,890,585 | $ | 0.51 | $ | 0.82 | 6.98 | $ | 7,243 | ||||||||||||
| 2019年1月1日的非既得期权 |
2,790,941 | $ | 0.71 | $ | 1.19 | 8.94 | $ | 1,027 | ||||||||||||
| 2019年12月31日的非既得期权 |
2,894,494 | $ | 1.44 | $ | 2.41 | 8.86 | $ | 2,667 | ||||||||||||
授予员工的期权的公允价值在授予日使用Black-Scholes期权估值 模型进行估算。这种基于股票的薪酬费用估值模型要求公司对计算中使用的变量做出假设和判断,包括预期期限(授予的期权 预计未偿还的加权平均时间段)、公司普通股的波动性、假设的无风险利率和预期股息。本公司采用简化的预期寿命和波动率计算方法,基于与本公司特征相似的几家上市实体普通股历史波动率的平均值 。无风险利率以授予时有效的美国国债收益率曲线为基础,期限为 ,与期权的预期寿命相对应。本公司采用直线法进行费用归属。
以下 加权平均假设用于计算员工股票期权授予日期的公允价值:
| 年终十二月三十一日, 2019 |
||||
| 预期期限(以年为单位) |
6.17 | |||
| 预期波动率 |
63.88 - 65.01 | % | ||
| 预期股息收益率 |
— | |||
| 无风险利率 |
1.68 - 2.44 | % | ||
在截至2017年12月31日的年度内,公司向非雇员顾问授予购买220,000股普通股的选择权。授予这些期权是为了换取在服务期限内提供和授予的咨询服务,服务期限与期权授予期限大致相同。每个期权在授予日的公允价值 是使用Black-Scholes期权模型估算的。这些期权的公允价值在每个计量日重新计量,直到完全归属为止。在截至2019年12月31日的年度内,没有向非员工 顾问发放补助金。
F-22
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
下表列出了合并运营和全面亏损报表中员工和 非员工的股票薪酬费用分类:
| 年终十二月三十一日, 2019 |
||||
| 研发 |
$ | 915 | ||
| 一般事务和行政事务 |
470 | |||
|
|
|
|||
| 总计 |
$ | 1,385 | ||
|
|
|
|||
截至2019年12月31日,与未归属股票 期权相关的未摊销股票薪酬成本为3704美元,预计将在2.83年的加权平均期限内确认。
认股权证
在执行2016年12月太平洋贷款协议(见附注5,应付票据)方面,本公司发行了太平洋 全既得权证,以购买A系列优先股的56,324股或2016年认股权证,收购价为每股1.06525美元,可行使至2026年12月。2017年5月,本公司动用了太平洋贷款协议项下剩余的1,000美元额外 借款能力,根据该协议,本公司有义务发行太平洋完全既有认股权证,以每股1.06525美元的收购价购买18,774股A系列股票,或2017年认股权证,可在2026年12月之前行使。于2019年12月31日仍未发行的太平洋认股权证可即时行使,认股权证交收后将发行的股份数目为75,098股。
2018年7月,该公司选择提取修订协议下剩余的7200美元。与此次抽签相关,公司发行了 太平洋完全既得权证,以每股4.1952美元的收购价购买17,175股B系列优先股。截至2019年12月31日,这些权证仍未结清,均可立即行使。认股权证结算后将发行的 股数量为17,175股。
下表汇总了截至2019年12月31日的未偿还认股权证:
| 系列A |
授予日期 | 数量 认股权证 |
行权价格 | 截至的公允价值 2019年12月31日 |
||||||||||||
| 2016认股权证 |
12/19/2016 | 56,324 | $ | 1.06525 | $ | 60 | ||||||||||
| 2017年认股权证 |
5/27/2017 | 18,774 | $ | 1.06525 | $ | 20 | ||||||||||
| B系列 |
授予日期 | 数量 认股权证 |
行权价格 | 截至的公允价值 2019年12月31日 |
||||||||||||
| 2018年认股权证 |
7/9/2018 | 17,175 | $ | 4.1915 | $ | 48 | ||||||||||
F-23
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
已发行认股权证的公允价值是根据Black-Scholes-Merton期权定价模型 在以下假设下计算得出的:
| 十二月三十一日, 2019 |
||||
| 预期期限(以年为单位) |
6.97 - 8.14 | |||
| 预期波动率 |
64.65 | % | ||
| 预期股息收益率 |
— | |||
| 无风险利率 |
1.92 | % | ||
财务会计准则委员会就可赎回(可认购或强制赎回)的 股票的独立权证和其他类似工具的分类发布了会计指导意见。该指导意见要求对某些可行使为可转换优先股的权证进行责任分类。认股权证的初始公允价值 记录为直接扣除应付票据的账面价值,并在贷款期限内摊销。公司在每个资产负债表日重新计量认股权证。估值变动记为 综合经营及全面亏损表认股权证公允价值重新计量收益。截至2019年12月31日,未偿还权证的公允价值为128美元。
以下为截至2019年12月31日止年度本公司认股权证负债余额变动摘要:
| 2019年1月1日 |
$ | 139 | ||
| 所有认股权证的公允价值净减少 |
(11 | ) | ||
|
|
|
|||
| 2019年12月31日 |
$ | 128 | ||
|
|
|
附注9.承付款和或有事项
租赁义务
科玛斯租赁公司
2016年8月,本公司签订了新的设施租赁,使用权和支付权从2017年1月开始。租期为7年 年。这份租约包括递增租金的条款。租金费用在租赁期内以直线方式确认。这份租约包括租户改善的津贴。租户装修记录为 财产和设备,并在租赁期内折旧。连同租户改善津贴一起,公司记录了847美元的租赁奖励义务,这笔债务将在租赁期内摊销,作为租金费用的减少 。截至2019年12月31日,相关未摊销租赁激励义务为494美元。
41号站租赁
2017年8月,公司签订了新的设施租赁,使用权从2017年12月开始,付款从2018年6月开始。租期 为10年,本公司可行使一项五年续期选择权。这份租约包括递增租金的条款。租金费用在租赁期内是直线确认的。此租约包括
F-24
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
租户改善津贴3967美元,全部余额在年底提取。租户的改善工程将记录为财产和设备,并将在租约剩余期限内完成时进行折旧。连同租户改善津贴一起,公司记录了3967美元的租赁债务,这笔债务将在租赁期内摊销,以减少租金 费用。截至2019年12月31日,相关未摊销租赁激励义务为3180美元。
在截至2018年12月31日的年度内,公司选择提取第41站租约中提供的额外992美元的租户改善贷款。这笔贷款并入了租约剩余期限的基本租金中,并起到了增加的作用。租金上涨包括 利息,本金按8%的利率计息。本公司将这笔额外的租户改善贷款作为综合资产负债表上的应付票据入账,当前部分包括在应付票据的当前部分 。本公司向出租人发出书面通知,表示有意于2018年提取额外免税额。该公司于2019年5月完成了与津贴相关的现金收取。
于截至2019年12月31日止年度内,本公司修订第41号车站租约,加入毗连单位的额外空间,并有权 自2020年6月起再使用新空间7年。这项有关额外地方的修订,包括逐步增加租金的条文。租金费用在租赁期内是直线确认的。
2021年1月22日,该公司修订了第41站租约,将租赁面积增加了91,478平方英尺。这项修订 包括租金上涨的条款,期限为10年,额外支付的最低金额为33,920美元。
米尔皮塔斯租赁公司
2019年8月,公司签订了新的设施租赁,使用权和支付权从2019年8月开始。租期为9年 年。这份租约包括递增租金的条款。租金费用在租赁期内以直线方式确认。
未来 最低租赁付款
在截至2019年12月31日的一年中,总租金支出为3739美元。科马斯租约、米尔皮塔斯租约和41号站租约被 归类为运营租约。截至2019年12月31日,本公司租赁协议下的未来最低承诺如下:
| 截至十二月三十一日止的年度, |
金额 | |||
| 2020 |
$ | 3,688 | ||
| 2021 |
3,865 | |||
| 2022 |
3,980 | |||
| 2023 |
4,316 | |||
| 2024 |
4,252 | |||
| 此后 |
15,187 | |||
|
|
|
|||
| 最低付款总额 |
$ | 35,288 | ||
|
|
|
|||
F-25
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
合同义务
在正常业务过程中,本公司与临床研究机构、药品制造商和其他供应商签订合同,提供 临床前和临床研究研究、研发用品以及用于运营目的的其他服务和产品。这些合同一般规定在通知后终止,因此是可撤销的合同。
此外,在截至2020年12月31日的年度内,公司已与Dell EMC达成协议,将额外购买一台超级计算机、附件 和零部件,预计价格约为18,637美元。
赔偿
公司已同意在高级管理人员或董事正在或曾经应 公司的要求以此类身份服务期间,对其高级管理人员和董事的某些事件或事件进行赔偿。本公司购买董事和高级管理人员责任保险,规定公司偿还承保义务,限制本公司的风险敞口,并使其能够收回潜在未来支付金额的 部分。截至2019年12月31日,本公司没有记录这些协议的负债,因为没有超过保险覆盖范围的金额可能或可评估。
员工协议
本公司已与若干关键员工签订雇佣 协议,根据该协议,若员工在本公司控制权变更后被本公司终止聘用,则该等员工有权获得若干福利,包括加速授予股权 奖励。
法律事项
本公司目前不是任何重大诉讼或其他重大法律程序的当事人 。本公司可能会不时卷入因正常业务活动而引起的各种法律诉讼, 任何这些问题的不利解决方案都可能对本公司未来的运营业绩、现金流或财务状况产生重大影响。
注10.所得税
截至2019年12月31日止年度,本公司并无记录任何所得税支出。本公司历来出现营业亏损, 对其递延税项净资产维持全额估值津贴。
所得税准备金由以下部分组成(全部 递延):
| 年终十二月三十一日, 2019 |
||||
| 联邦制 |
$ | 15,555 | ||
| 状态 |
1,517 | |||
| 更改估值免税额 |
(17,072 | ) | ||
|
|
|
|||
| 总计 |
$ | — | ||
|
|
|
|||
F-26
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
本公司截至2019年12月31日的年度实际税率为0%,与 美国法定联邦税率不同,如下所示;
| 年终十二月三十一日, 2019 |
||||
| 法定税率 |
$ | (12,995 | ) | |
| 研发信用产生 |
(2,233 | ) | ||
| 孤儿药品信贷产生 |
(932 | ) | ||
| 不确定的税收状况 |
316 | |||
| 其他不可扣除的费用 |
288 | |||
| 更改估值免税额 |
15,556 | |||
|
|
|
|||
| 实际税率 |
$ | — | ||
|
|
|
|||
导致递延税项资产重要组成部分的暂时性差异的税收影响如下 :
| 十二月三十一日, 2019 |
||||
| 递延税项资产: |
||||
| 准备金和应计项目 |
$ | 1,846 | ||
| 净营业亏损结转 |
27,665 | |||
| 基于股票的薪酬 |
178 | |||
| 研发信贷结转 |
5,343 | |||
| 明确的活着的无形资产 |
423 | |||
| 其他 |
31 | |||
|
|
|
|||
| 递延税项总资产 |
35,486 | |||
| 估值免税额 |
(33,786 | ) | ||
|
|
|
|||
| 递延税金净资产 |
1,700 | |||
| 递延税项负债 |
||||
| 可折旧资产 |
(1,700 | ) | ||
|
|
|
|||
| 递延税金净资产 |
$ | — | ||
|
|
|
|||
截至2019年12月31日,该公司记录了其递延税项资产中被确定为更有可能达到 门槛的部分。对剩余的递延税项资产计入估值津贴。在确定本公司的所得税拨备、记录针对 递延税项资产的估值津贴以及评估本公司不确定的税务状况时,需要作出重大判断。由于自成立以来的净亏损和实现递延税项资产的不确定性,公司对其递延税项净额资产有全额估值津贴 。在本公司产生正收益并预期(有合理确定性)继续产生正收益的范围内,本公司可在未来期间发放全部或部分估值津贴。此次释放 将导致确认公司的全部或部分递延税项资产,从而减少该释放期间的所得税支出。截至2019年12月31日,公司记录的估值 津贴为33,786美元,截至2019年12月31日的年度增加了约17,072美元。
F-27
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
NOL和税收抵免结转要接受美国国税局(IRS)的审查和可能的调整,并且可能会因为之前发生或将来可能发生的所有权变更而受到年度限制,根据修订后的《国税法》第382条和类似的州规定 。这些所有权变化可能会限制每年可用于抵消未来应税收入的结转金额。一般而言,根据第382条的定义,所有权变更是指在三年内将某些股东或公众团体在公司股票中的所有权 增加50%以上的交易的结果。本公司尚未进行研究,以评估是否发生了控制权变更,或自成立以来是否由于此类研究的重大复杂性和成本而发生了多次 控制权变更。如果本公司自成立以来的任何时间经历了第382条所定义的控制权变更,则根据第382条的规定,对净营业亏损结转或研发税收抵免结转的使用将受到第382条规定的年度限制,该限制首先由 所有权变更时公司股票价值乘以适用的长期免税税率确定,然后可根据需要进行额外调整。任何限制都可能导致净营业亏损的一部分到期 结转或使用前的研发税收抵免。此外,在一项研究完成并知道任何限制之前,不会将任何金额作为不确定的税收状况列报。
截至2019年12月31日,本公司有116,575美元的联邦NOL结转可用于减少应纳税所得额,其中18,614美元从2036年开始到期 ,97,961美元未到期。截至2019年12月31日,该公司有117,771美元的州NOL结转可用于减少未来的州应税收入,其中19,810美元从2031年开始到期,97,961美元未到期。
截至2019年12月31日,本公司还拥有联邦和州研发信贷结转,分别为3846美元和1242美元。 联邦研发信贷结转将于2036年到期,州研发信贷结转将于2030年到期。截至2019年12月31日,该公司还拥有932美元的联邦孤儿药物抵免,该抵免将于2036年开始 到期。截至2019年12月31日,该公司为这些抵免结转的不确定税收头寸预留了677美元。
公司确认不确定税务头寸的好处,前提是这些头寸很有可能仅根据其技术价值进行审查而得以维持,这是最终结算时更有可能实现的最大金额的好处。 本公司的政策是将与所得税相关的罚款和利息支出作为其他收入的一部分,必要时按净额计入。
该公司在美国、犹他州和加利福尼亚州提交所得税申报单。本公司目前未在这两个 司法管辖区接受审查。本公司自2016年纳税申报单以来的所有报税表均须接受所得税审查。
F-28
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
注11.每股净亏损
下表列出了每股基本净亏损和摊薄净亏损的计算方法:
| 年终十二月三十一日, 2019 |
||||
| 分子: |
||||
| 净损失 |
$ | (61,879 | ) | |
| 分母: |
||||
| 加权平均已发行普通股 |
14,380,177 | |||
|
|
|
|||
| 每股基本和稀释后净亏损 |
$ | (4.30 | ) | |
|
|
|
|||
本公司的潜在摊薄证券,包括可转换优先股及购买普通股的期权及认股权证 ,已从每股摊薄净亏损的计算中剔除,因为此举将减少每股净亏损。因此,用于计算基本 和稀释后每股净亏损的已发行普通股加权平均数是相同的。该公司将以下潜在普通股排除在所指时期的每股稀释净亏损计算之外,因为如果计入这些股票,将会产生反稀释效果:
| 年终十二月三十一日, 2019 |
||||
| 可转换优先股 |
52,466,330 | |||
| 购买普通股的期权 |
5,785,079 | |||
| 认股权证 |
92,273 | |||
|
|
|
|||
| 总计 |
58,362,848 | |||
|
|
|
|||
附注12.关联方应收票据
2017年12月5日,该公司与其首席执行官(CEO)签订了一项贷款协议,向CEO提供595美元的贷款。 这笔贷款的期限为7年。截至2019年12月31日,595美元的未偿还余额记录在合并资产负债表中的其他非流动 资产中。在截至2020年12月31日的年度内,该贷款的未偿还余额已全部偿还。
注13.协作及其他研究和开发合同
2017年10月10日,该公司宣布与武田药业 株式会社建立研究合作关系。根据这次合作的条款,Recursion将利用其发现平台为武田的TAK-celerator提供临床前候选产品™开发管道。协议的财务条款包括90,000美元以上的预付款和以成功为基础的里程碑,如果合作导致多个新药审批,则按净销售额支付个位数版税。 2018年,武田行使了选择权,使其能够根据合作确定的两种适应症继续开发药物化合物。2019年,该公司确认了1,334美元的合作收入 。
F-29
递归制药公司
合并财务报表附注
(以千为单位,不包括每股和每股数据)
注14.员工福利计划
公司根据《国税法》第401(K)条制定了员工福利计划。该计划允许员工做出最高为其薪酬的 指定百分比的贡献。该公司目前的贡献最高为员工基本工资的4%,方法是将每位员工贡献的前4%的年度基本工资的100%等同于员工基本工资的100%。截至2019年12月31日的一年中,雇主支出约为931美元。
注15.后续事件
该公司评估了从资产负债表日期到2021年1月26日(合并财务报表 发布之日)的后续事件。公司的结论是,除了上述注释中披露的事件或交易外,没有发生任何需要在随附的综合财务报表中披露的事件或交易,但以下情况除外:
(一)新冠肺炎的影响
2020年3月,世界卫生组织宣布新型冠状病毒病或新冠肺炎的爆发为大流行。新冠肺炎在全球各个行业引发了市场波动和不确定性。虽然新冠肺炎疫情的严重程度、持续时间和影响程度仍存在不确定性,但本公司目前预计新冠肺炎疫情不会对本公司的运营和财务状况造成影响。公司将继续 主动监控和评估这场快速发展的危机可能对我们业务造成的潜在影响,并避免对我们的计划造成任何不必要的潜在延误。目前,我们的主要计划和研究活动仍在 轨道上。员工、患者和合作伙伴的安全和福祉是我们的首要任务。
(B)Vium公司的资产购买协议。
2020年7月,本公司签订了一项资产购买协议,以总现金代价2600美元收购Vium,Inc.的100%资产。
(C)拜耳合作协议
2020年8月,公司与拜耳股份公司(Bayer AG,简称拜耳)签订了战略合作伙伴协议。根据协议条款,该公司收到了3万美元的预付款。此外,公司和拜耳可能会启动十多个计划 ,每个计划可能向公司支付100,000美元的开发和商业里程碑费用,外加未来销售的特许权使用费。拜耳将获得独家授权来自研究活动的新疗法的选择权。
(D)发行期权
在截至2020年12月31日的年度内,公司授予了8,884,057份额外期权。
F-30
股票
递归制药公司
普通股

联合簿记管理人
| 高盛有限责任公司 | 摩根大通 |
| 美国银行证券 | SVB Leerink | Allen&Company LLC |
被动簿记管理人
KeyBanc资本市场
招股说明书日期:2021年
|
将 生物学解码为 从根本上改善生活
自豪的创始会员
|
第二部分
招股章程不需要的资料
第十三项. 其他发行发行费用
下表列出了除承保折扣和佣金外,与本注册声明中描述的 发行相关的费用,所有费用将由我们支付。除美国证券交易委员会(SEC)注册费、金融业监管局(FINRA)申请费和纳斯达克上市费外,所有金额均为估计数。
| 已支付的金额或 待付款 |
||||
| 证券交易委员会注册费 |
$ | * | ||
| FINRA备案费用 |
* | |||
| 纳斯达克上市费 |
* | |||
| 印刷费和雕刻费 |
* | |||
| 律师费及开支 |
* | |||
| 会计费用和费用 |
* | |||
| 转会代理费和登记费 |
* | |||
| 杂费 |
* | |||
|
|
|
|||
| 总计 |
$ | * | ||
|
|
|
|||
| * | 将由修正案提供。 |
项目14.对董事和高级职员的赔偿
特拉华州公司法第145条授权公司赔偿其董事和高级管理人员,并 就其董事和高级管理人员的身份或地位所产生的责任购买保险,前提是该人本着善意行事,并以合理地相信符合我们最大利益的方式行事,并且对于任何刑事行为, 没有合理的理由相信该人的行为是非法的。特拉华州公司法进一步规定,根据该法律允许的赔偿不应被视为排除 董事和高级管理人员根据公司章程、任何协议、股东投票或其他方式可能享有的任何其他权利。注册人的公司注册证书将在本次发行完成后生效,规定在特拉华州公司法允许的最大范围内对注册人的董事和高级管理人员进行 赔偿。此外,注册人的章程将在本次发售完成后生效,该章程要求注册人对任何曾是或曾经是注册人的董事或高级职员,或现在或曾经是注册人的董事或高级职员,或因该人是或曾经是注册人的董事或高级职员而被威胁成为任何受威胁、待决或已完成的诉讼、诉讼或法律程序(无论是民事、刑事、行政或调查)的一方的任何人,给予充分的赔偿。 注册人是或曾经是注册人的董事或高级职员,或者是或曾经是注册人的董事或高级人员。合资企业、信托或其他企业在适用法律允许的最大范围内,就该人在与该等诉讼、诉讼或诉讼相关的实际和合理发生的费用(包括律师费)、判决、罚款和为达成和解而支付的金额进行赔偿。 在适用法律允许的最大限度内,赔偿该人实际和合理地发生的与该等诉讼、诉讼或诉讼相关的费用、判决、罚款和金额。
特拉华州公司法第102(B)(7)条允许公司在其 公司注册证书中规定,公司董事不应因违反董事的受托责任而对公司或其股东承担个人赔偿责任,但以下情况除外:(1)违反董事对公司或其股东的忠诚义务;(2)不真诚的行为或不作为,或涉及故意不当行为或知晓法律的行为或不作为;(3)
II-1
支付非法股息或非法股票回购或赎回,或(4)董事从中获得不正当个人利益的任何交易。本次发行完成后生效的注册人公司注册证书 规定,注册人的董事不应因违反董事的受托责任而对其或其股东承担个人责任 ,如果修改特拉华州一般公司法以授权公司采取行动,进一步取消或限制董事的个人责任,则注册人的董事的责任应在特拉华州一般公司法允许的最大限度内取消或限制为 。
特拉华州公司法第174条规定,除其他事项外,故意或疏忽批准非法支付股息或非法购买或赎回股票的董事可能被追究此类行为的责任。在违法行为获得批准时缺席或当时持不同意见的董事,可以通过在违法行为发生时或在该缺席董事收到违法行为通知后立即将其对该违法行为的异议记入载有董事会会议记录的账簿中来逃避责任。 该董事在该违法行为获得批准时或在该董事收到该违法行为的通知后,可立即将其对该违法行为的异议记入董事会会议纪要的账簿中,以避免承担责任。
在特拉华州公司法允许的情况下,注册人 已与注册人的每一名董事和高管签订单独的赔偿协议,要求注册人(除其他事项外)就其董事或高管身份 可能产生的某些责任进行赔偿。
注册人期望获得并维护保险单,根据该保险单,其董事和 高级管理人员在该等保单的限制范围内,就其作为或曾经是董事或高级管理人员的诉讼、诉讼或诉讼的当事人所承担的与辩护相关的某些费用和可能施加的某些责任投保。无论注册人是否有权根据特拉华州一般公司法的规定 向其赔偿此类责任,这些保单提供的保险范围都可能适用。
注册人 与注册人的高级职员和董事之间签订的这些赔偿条款和赔偿协议可能足够广泛,以允许对注册人的高级职员和董事根据修订后的 1933年证券法产生的责任(包括报销所发生的费用)进行赔偿。
注册人与承销商之间作为本注册声明附件1.1提交的承销协议 规定,注册人董事和高级管理人员以及某些控制人的承销商应承担特定责任,包括《证券法》规定的与承销商提供的信息相关的责任 ,这些信息专门包含在注册声明中。与我们股本的某些持有人签订的投资者权利协议还规定了与代表该等持有人注册注册人的普通股相关的交叉赔偿。
II-2
第15项近期出售未登记证券
以下列表列出了我们自2017年1月1日以来出售的所有未注册证券的相关信息。 没有承销商参与销售,代表出售和发行的证券的证书包含限制未根据《证券法》注册或获得适用豁免注册的证券转让的图例。
| (1) | 从2017年9月到2018年2月,我们以每股4.19152美元的收购价发行和出售了总计14,314,610股B系列可转换优先股,总收购价为6,000万美元。 |
| (2) | 从2019年2月到2019年8月,我们以每股9.75091美元的收购价发行和出售了总计12,517,569股C系列可转换优先股 ,总收购价为1.221亿美元。 |
| (3) | 从2020年9月到2020年10月,我们以每股10.06181美元的收购价发行和出售了总计24,599,042股D系列可转换优先股,总收购价为2.475亿美元。 |
| (4) | 从2017年1月到2020年12月31日,我们授予了股票期权,根据我们2016年的计划,在行使期权时,我们授予了股票期权,以购买总计 股普通股,行权价从每股 $到$不等,总行权价约为 $。 |
| (5) | 从2017年1月至2020年12月31日,我们在2016年计划下行使期权时,向我们的某些服务提供商发行和出售了总计 股普通股,每股行权价从 $到$不等,总行权价约为 $。 |
第15(1)项、第15(2)项和第15(3)项所述证券的要约、销售和 发行,根据证券法第4(A)(2)节或根据证券法颁布的法规D,作为不涉及公开发行的 发行人的交易,豁免根据证券法注册。在每笔交易中,证券的接受者仅为投资而购买证券,而不是为了与其任何分销相关的目的或为出售而购买,在这些交易中发行的证券上贴上了适当的说明 。这些交易中的每一位证券接受者都是经认可的人,并通过雇佣、业务或其他关系充分接触到有关注册人的信息。
第15(4)和15(5)项所述证券的要约、销售和发行根据(1)规则701豁免根据证券法 注册,因为交易是根据证券法第701条规定的补偿性福利计划和与补偿有关的合同或(2)证券法第4(A)(2)条规定的 发行人不涉及任何公开发行的交易。该等证券的接受者为注册人的雇员、顾问或董事,并根据我们的2016年计划收取该等证券。每笔 这些交易中的证券接受者表示,他们仅出于投资的目的收购证券,而不是为了或与其任何分销相关的销售而购买证券,在这些 交易中发行的证券上贴上了适当的图例。
II-3
项目16.证物和财务报表明细表
(A)展品。
有关作为S-1表格注册声明的一部分提交的展品列表,请参阅紧靠本签名页前面的展品索引,该展品索引在此引用作为参考。
(B)财务报表附表。
附表 已被省略,因为其中要求列出的信息不适用或显示在财务报表或附注中。
项目17. 承诺
以下签署的注册人特此承诺在承销协议规定的截止日期向承销商提供按承销商要求的面额和名称登记的证书,以便迅速交付给每位买方。
鉴于根据证券法产生的责任的赔偿可根据前述条款允许注册人的董事、高级管理人员和控制人承担,注册人已被告知,美国证券交易委员会认为此类赔偿违反证券法规定的公共政策,因此 不可执行。如果注册人的董事、高级职员或控制人就正在登记的证券提出赔偿要求(注册人支付注册人的董事、高级职员或控制人为成功抗辩任何诉讼、诉讼或法律程序而招致或支付的费用除外),除非注册人的律师认为此事已通过控制先例解决,否则注册人将向具有适当管辖权的法院提交是否该等补偿的问题。
以下签署人特此承诺:
| (1) | 为了确定证券法项下的任何责任,根据规则430A作为本注册说明书的一部分提交的招股说明书 表格中遗漏的信息,以及注册人根据1933年证券法第424(B)(1)或(4)或497(H)条提交的招股说明书中包含的信息,应视为本注册说明书在宣布生效时的一部分。 |
| (2) | 为确定证券法项下的任何责任,每一项包含招股说明书表格 的生效后修订应被视为与招股说明书中提供的证券有关的新的登记声明,届时该等证券的发售应被视为其首次善意发售。 |
II-4
展品索引
| 展品 |
描述 | |
| 1.1* | 承销协议书格式。 | |
| 3.1* | 修改并重新签署了现行有效的注册人注册证书。 | |
| 3.2* | 注册人注册证书的修订和重新注册证书格式,在本次发售完成后生效。 | |
| 3.3* | 注册人的现行章程。 | |
| 3.4* | 经修订及重新修订的注册人章程格式,于本次发售完成后生效。 | |
| 4.1* | 由注册人及其某些股东于2020年9月1日修订和重新签署的投资者权利协议。 | |
| 4.2* | 注册人普通股证书式样。 | |
| 5.1* | 威尔逊·桑西尼·古德里奇和罗萨蒂的观点,专业公司。 | |
| 10.1+* | 注册人与其每一位董事和高级管理人员之间的赔偿协议格式。 | |
| 10.2+* | 经修订的2016年度股权激励计划及其协议格式。 | |
| 10.3+* | 2021年股权激励计划及其协议形式,将在本次发售完成后生效。 | |
| 10.4+* | 2021年员工股票购买计划及其协议形式,将在本次发售完成后生效。 | |
| 10.5+* | 注册人与每位行政人员之间的行政人员聘用协议表格。 | |
| 10.9+* | 高管激励薪酬计划。 | |
| 10.10+* | 控制和服务政策的变化。 | |
| 10.11+* | 外部董事薪酬政策。 | |
| 10.12* | Vestar Gateway,LLC和注册人之间的办公室租赁,日期为2017年11月13日,经修订。 | |
| 10.13* | 由Berrueta Family L.P.和Mousera,Inc.于2015年7月27日修订并重新签订的租约,于2019年8月16日修订并分配给注册人。 | |
| 10.14* | 拜耳股份公司和注册人之间的研究合作和期权协议,日期为2020年8月28日。 | |
| 10.15* | 修改并重新签署了注册人与犹他州大学研究基金会之间的许可协议,日期为2016年2月9日。 | |
| 10.16* | 独家许可协议编号俄亥俄州创新基金会和注册人之间的A2019-1229,日期为2018年12月21日。 | |
| 10.17* | 武田制药有限公司和注册人之间的许可协议,日期为2020年5月1日。 | |
| 23.1* | 独立注册会计师事务所同意。 | |
| 23.2* | 经Wilson Sonsini Goodrich&Rosati专业公司同意(见附件5.1)。 | |
| 24.1* | 授权书(见本表格S-1第II-6页)。 | |
| * | 须以修订方式提交。 |
| + | 注明管理合同或补偿计划。 |
II-5
签名
根据修订后的1933年证券法的要求,注册人已于2021年(2021年)在犹他州盐湖城,由其正式授权的以下签名人代表其签署了本注册声明。
| 递归制药公司 | ||
| 由以下人员提供: | ||
| 克里斯托弗·吉布森 | ||
| 首席执行官 | ||
授权书
通过这些礼物知道 所有人,签名出现在下面的每个人都构成并指定克里斯托弗·吉布森和迈克尔·塞科拉为他或她真实和合法的 事实律师和代理人,以任何和所有身份签署本注册书的任何或所有修正案(包括生效后的修正案),并根据经修订的1933年证券法第462(B)条将本注册书和任何和所有附加注册书连同其所有证物以及与此相关的所有其他文件提交给证券交易委员会(SEC),并向美国证券交易委员会(Securities And Exchange Commission)提交所有 证物和与之相关的所有其他文件,并具有完全替代和替代的权力,并授予上述公司和代理人以任何和所有身份签署本注册书和附加注册书的任何或所有修正案(包括生效后的修正案),并将其连同所有 证物和所有其他相关文件提交给上述事实律师和代理人,以及他们中的每一位 有充分的权力和权限,按照他们本人可能或可以亲自做的一切意图和目的,作出和执行在该处所内和周围所必需和必要的每一项行为和事情,特此批准并 确认所有上述内容事实律师代理人或他们中的任何一人,或他们的一名或多名替代者,可以合法地根据本协议作出或导致作出 。
根据修订后的1933年证券法的要求,本注册声明已由以下 人员以指定的身份和日期签署。
| 签名 |
标题 |
日期 | ||
|
克里斯托弗·吉布森 |
总裁、首席执行官兼董事(首席行政主任) | , 2021 | ||
|
迈克尔·塞科拉 |
首席财务官(首席财务会计官) | , 2021 | ||
|
扎卡里·博格 |
导演 | , 2021 | ||
|
布莱克·博格森 |
导演 | , 2021 | ||
|
特里-安·伯雷尔 |
导演 | , 2021 | ||
II-6
| 签名 |
标题 |
日期 | ||
|
马丁·查韦斯(R.Martin Chavez) |
导演 | , 2021 | ||
|
扎文·达尔 |
导演 | , 2021 | ||
|
罗伯特·赫什伯格 |
导演 | , 2021 | ||
|
李院长 |
导演 | , 2021 | ||
II-7